Red Biotechnology市場規模・シェア
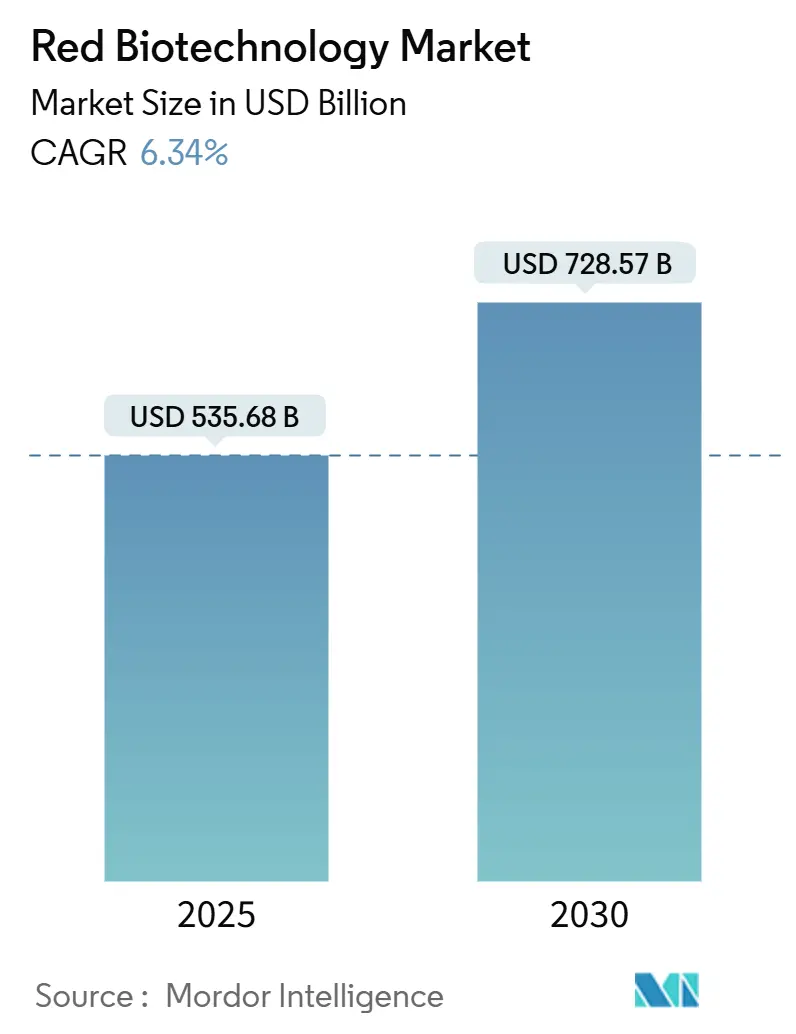
Mordor IntelligenceによるRed Biotechnology市場分析
Red Biotechnology市場規模は2025年に5,356.8億USDとなり、2030年には7,285.7億USDに達すると予測され、年平均成長率6.34%で成長する見込みです。成長の要因は、パンデミック対応ワクチン生産から、細胞・遺伝子治療、次世代モノクローナル抗体、精密診断を含む多様化パイプラインへの移行にあります。迅速な規制審査が勢いを支えており、2024年にFDAが承認した24の生物学的製剤承認がその例です。政府支出の並行、特に2027年までのPHEMCE(公衆衛生緊急医学対策企業)への795億USD配分が、開発・製造両面での国内能力を強化しています。産業側では、Merckによるノースカロライナ州10億USDワクチン施設などの大規模資本プロジェクトが、パンデミック対応と通常の商業生産の間で柔軟に対応できる強固な能力を追加しています。これらの要因が相まって、高複雑性バイオ医薬品のスケールアップのための予測可能な環境を創出し、革新的資産の臨床入りまでの時間を短縮するベンチャー投資や官民パートナーシップを促進しています。
主要レポートポイント
- 製品カテゴリー別では、治療薬セグメントが2024年のRed Biotechnology市場シェアの54.67%を獲得しており、同セグメントは2030年まで年平均成長率6.87%で拡大すると予測されています。
- エンドユーザー別では、バイオ医薬品企業が2024年のRed Biotechnology市場規模の44.89%を占める一方、学術・研究機関は2030年まで最高の年平均成長率7.35%を記録する見込みです。
- 地域別では、北米が2024年のRed Biotechnology市場規模の39.13%を占めており、アジア太平洋地域は同期間に年平均成長率7.26%で成長しています。
世界Red Biotechnology市場動向・洞察
促進要因インパクト分析
| 促進要因 | CAGR予測への影響(概算%) | 地域的関連性 | 影響時期 |
|---|---|---|---|
| 慢性・希少疾患の発症率・有病率の増加 | +1.2% | 世界、北米・欧州の高齢化人口に集中 | 長期(4年以上) |
| 医療資金拡大・官民パートナーシップ | +0.9% | 世界、特にAPAC・新興市場で強い | 中期(2-4年) |
| 個別化医療導入・コンパニオン診断の普及 | +0.8% | 北米・EU主導、APACに拡大 | 中期(2-4年) |
| mRNAプラットフォーム波及による新規バイオ医薬品開発加速 | +0.7% | 世界、北米・欧州の製造ハブ中心 | 短期(2年以下) |
| AI主導による初期段階バイオ医薬品設計リスク軽減 | +0.6% | 世界、イノベーションセンターに集中 | 中期(2-4年) |
| 政府主導パンデミック準備プログラムによる世界ワクチン製造能力拡大 | +0.5% | 世界、国内能力への戦略的焦点 | 長期(4年以上) |
| 情報源: Mordor Intelligence | |||
慢性・希少疾患の発症率・有病率の増加
2024年にFDA審査を通過した8つの新規細胞・遺伝子治療は、未充足ニーズ領域がいかに科学的ブレイクスルーを商業資産に転換するかを示しています。腫瘍学は承認を独占し続けており、2024年の全新規生物学的製品の34%[1]Zinnet Sevval Aksoyalp, "A Year in Pharmacology: New Drugs Approved by the US Food and Drug Administration in 2024," Naunyn-Schmiedeberg's Archives of Pharmacology, link.springer.comを占めました。人口動態の変化が需要を強化しており、日本の次世代モノクローナル抗体・遺伝子治療に関する政策優先順位は、急速に高齢化する人口の管理という課題を反映しています。希少疾病パイプラインはOrphan Drug優遇措置の恩恵を受けており、2024年の遺伝子治療承認の88%がその指定を受けています。FDAのRare Disease Innovation HubとSTARTパイロットプログラムが開発タイムラインを短縮し、かつて商業的に魅力的でないとされたニッチ疾患を企業が標的とすることを促進しています。
医療資金拡大・官民パートナーシップ
2023-2027年PHEMCE配分は対策R&D・国内製造に795億USD[2]U.S. Department of Health & Human Services, "Public Health Emergency Medical Countermeasures Enterprise Multi-Year Budget FY 2023-2027," U.S. Department of Health & Human Services, aspr.hhs.govを確保し、これは前回計画サイクルから155億USDの増額です。BARDAの20億USDのBioMaP-Consortiumは、数ヶ月で抗体からmRNAワクチンに転換可能な柔軟施設への共同投資によりこの支援を拡張しています。カナダのモントリオール生物学的製造センターは、ウイルスベクター・タンパク質サブユニットワクチン用に年間2.5億回分の製造能力を追加しています。欧州委員会のGenAI4EUプログラムは、バイオ医薬品発見を含むAIプロジェクトに10億ユーロを確保し、国境を越えた知識移転を強化しています。新興経済国も同様のモデルを採用しており、インドのBIO-E3フレームワークは新しいバイオ生産キャンパス向けの優遇融資と簡素化された土地取得を提供しています。
個別化医療導入・コンパニオン診断の普及
2025年に発表されたFDAガイダンスは、バイオ医薬品の規制判断に人工知能がいかに増強効果をもたらすかを明確化し、ML駆動コンパニオン診断の正式受け入れを示しています。遺伝子検査は現在商業精密診断キットの45%を占めており、腫瘍学が全体需要の4分の1を占めています。病院はクラウド連携POCT(ポイントオブケア検査)プラットフォームを展開しており、この市場は2030年までに902.5億USDを超えると予想され、治療開始前に臨床医がリアルタイムで変異状況を把握できます。次世代シーケンシングへのアクセス拡大により、ゲノム当たりのコストが下がり、中規模バイオファーマが禁止的な予算なしに試験を階層化できます。規制の明確化、アッセイコストの低下、容易にアクセス可能なバイオインフォマティクスが相まって、個別化治療レジメンの基盤となるコンパニオン診断の普及を促進しています。
新規バイオ医薬品開発を加速するmRNAプラットフォーム波及効果
2024年6月時点で、COVID-19を超えたmRNAベースワクチンを評価する70の臨床試験が進行中で、腫瘍学、RSV、嚢胞性線維症を標的としています。Trans-amplifying構造体はRNA投入量を40分の1に削減し、免疫原性を維持しながら製造原価を低減しています。名古屋大学で合成された環状mRNAベクターは200倍高いタンパク質産生を実現し、代謝・希少遺伝性疾患での治療ウィンドウを開いています。Modernaは英国、オーストラリア、カナダの3つの地域工場を建設中で、各々1億回分相当の充填能力を有し、生産が連続・使い捨て形式に移行するにつれて、技術移転タイムラインが短縮され、小規模開発者が12ヶ月未満でINDからフェーズ1へ進むことを可能にしています。
阻害要因インパクト分析
| 阻害要因 | CAGR予測への影響(概算%) | 地域的関連性 | 影響時期 |
|---|---|---|---|
| 高バイオ製造・コールドチェーンコスト | -0.8% | 世界、特に新興市場で困難 | 中期(2-4年) |
| 複雑で変化する世界バイオ医薬品規制 | -0.6% | 世界、地域による規制要件の違い | 長期(4年以上) |
| 重要原材料のサプライチェーン脆弱性 | -0.5% | 世界、アジア太平洋サプライヤーの集中リスク | 短期(2年以下) |
| 次世代遺伝子治療における免疫原性リスク | -0.4% | 世界、北米・欧州で厳格な監視 | 中期(2-4年) |
| 情報源: Mordor Intelligence | |||
高バイオ製造・コールドチェーンコスト
コールドチェーン障害による業界損失は年間350億USDに達し、温度感受性バイオ医薬品の手頃性を損なっています。CAR-T自家治療は労働集約的製造・極低温流通により患者当たり50万USD以上のコストがかかります。Annex 1改訂により無菌処理規則が厳格化され、アイソレータ技術・環境モニタリングのアップグレードが必要となり、グリーンフィールド工場の設備投資を増大させています。サプライチェーンの集中が問題を複雑化しており、米国API輸入の75%以上が国外を起源とし、地政学的ショックに生産をさらしています。AI対応ルート計画ソフトウェアとデジタルツインが15-25%の物流削減を約束するものの、広範な展開はパイロット段階にとどまり、短期的救済が遅延しています。
複雑で変化する世界バイオ医薬品規制
2025年1月発効のEU臨床試験規則により、スポンサーは既存研究データを新しいCTISポータルにアップロードすることが義務付けられ、行政的なバックログが発生しています。同時に、EMA手数料見直しにより科学的助言コストが最高98,400ユーロまで上昇し、小規模開発者に負担をかけています。FDAのCoGenT Globalイニシアチブは統一遺伝子治療ガイドラインを目指していますが、現在は希少疾患のみをカバーしており、より広範囲のカテゴリーが規制の不透明さに残されています。米国では、2025年6月のACIP(予防接種実施に関する諮問委員会)メンバー全員の交代により、今後のワクチン政策スケジュールに不確実性がもたらされました。総合的に、基準の不整合により承認までの時間が延び、多地域上市に必要なブリッジング研究の量が増加しています。
セグメント分析
製品別:治療薬がイノベーション波を主導
治療薬は2024年に2,930億USDを創出し、Red Biotechnology市場規模の54.67%に相当し、2030年まで年平均成長率6.87%で成長すると予測されています。モノクローナル抗体がカテゴリーの中核となり、200を超える承認薬剤と世界で約1,400の活発な臨床候補[3]Silvia Crescioli, "Antibodies to Watch in 2025," mAbs, tandfonline.comを誇っています。二重特異性フォーマットが最高の臨床承認転換率を達成し、BioNTechやBristol Myers Squibbなどの企業が数十億ドルの共同開発契約を追求しています。2024年にFDAが8製品を承認したことで遺伝子治療が加速し、CRISPR改変CAR-Tプラットフォームが血液腫瘍学初期段階試験を支配しています。mRNA治療薬は感染症を超えて心血管代謝適応症に進出し、体内タンパク質産生を倍増する環状RNA技術に支えられています。
ワクチンはアウトブレイク時の最低コールオフ量を保証するBARDAオプション条項に支えられ、戦略的関連性を維持しています。診断・研究ツールは、シーケンシング試薬・液体生検アッセイが分散環境で普及するにつれて拡大しています。並行して、治療用タンパク質は特定疾患微小環境に特化した抗体薬物複合体・融合サイトカインへと進化し、精密標的化へのRed Biotechnology市場の重点を反映しています。
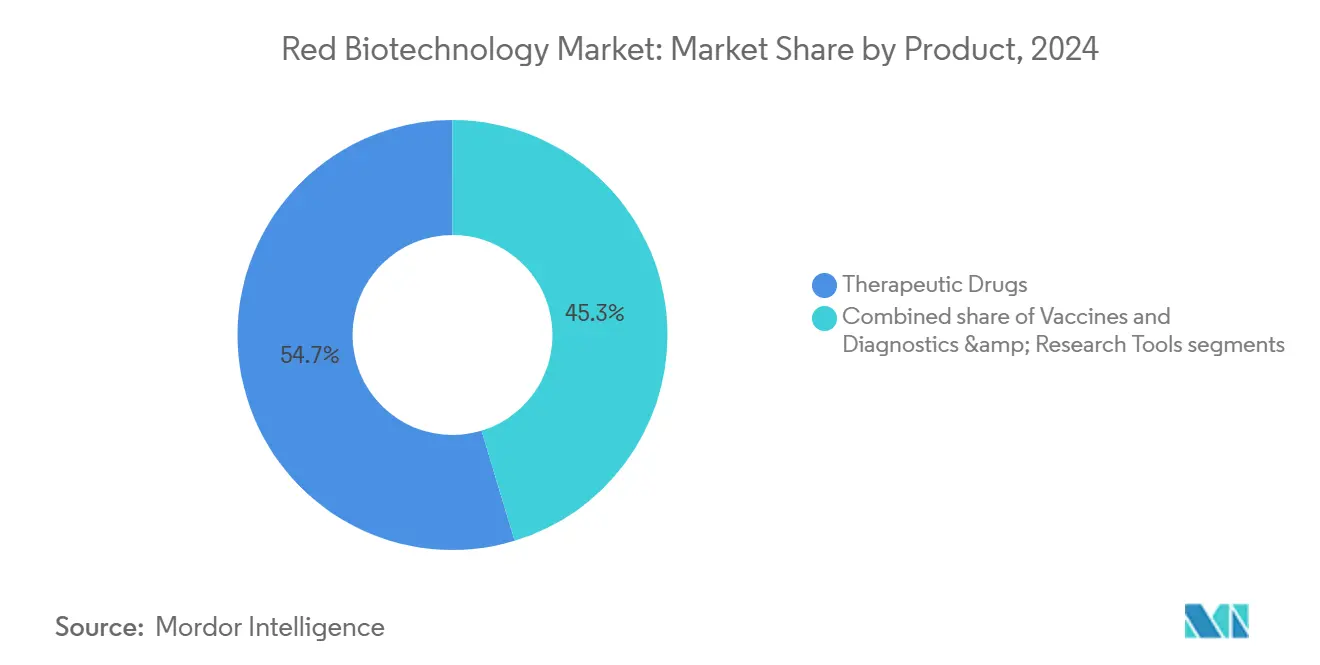
注記: すべての個別セグメントのシェアはレポート購入時に利用可能
エンドユーザー別:学術パートナーシップが成長を牽引
バイオ医薬品企業は2024年のRed Biotechnology市場シェアの44.89%を、発見から商業供給に至る垂直統合により保持しました。しかし、学術・研究機関は、助成金流入と企業による主任研究者の共同採用に支えられ、年平均成長率7.35%で最も成長が速い構成要素となっています。大学の中核施設は現在GMP準拠のベクタースイートを提供し、スピンアウトが専用インフラを構築することなく初期試験を実施できます。NVIDIAとNovo Nordiskの提携により、100を超える学術研究室にクラウドGPUクレジットと構造予測アルゴリズムが提供され、AI設計ツールへのアクセスが民主化されています。
アウトソーシングが資本負担を軽減するため、受託製造機関(CMO)と受託研究機関は並行して勢いを見せており、CMOは2028年までに世界バイオ医薬品能力の54%を支配する軌道にあり、小規模革新企業の製造対購入の計算を再構築しています。病院・専門クリニックは、特に閉鎖系製造ポッドを備えた腫瘍学センターでのポイントオブケア細胞治療のニッチエンドユーザーとして台頭しています。この能力の拡散は、分散されているが相互接続された開発ネットワークへの業界移行を反映しています。
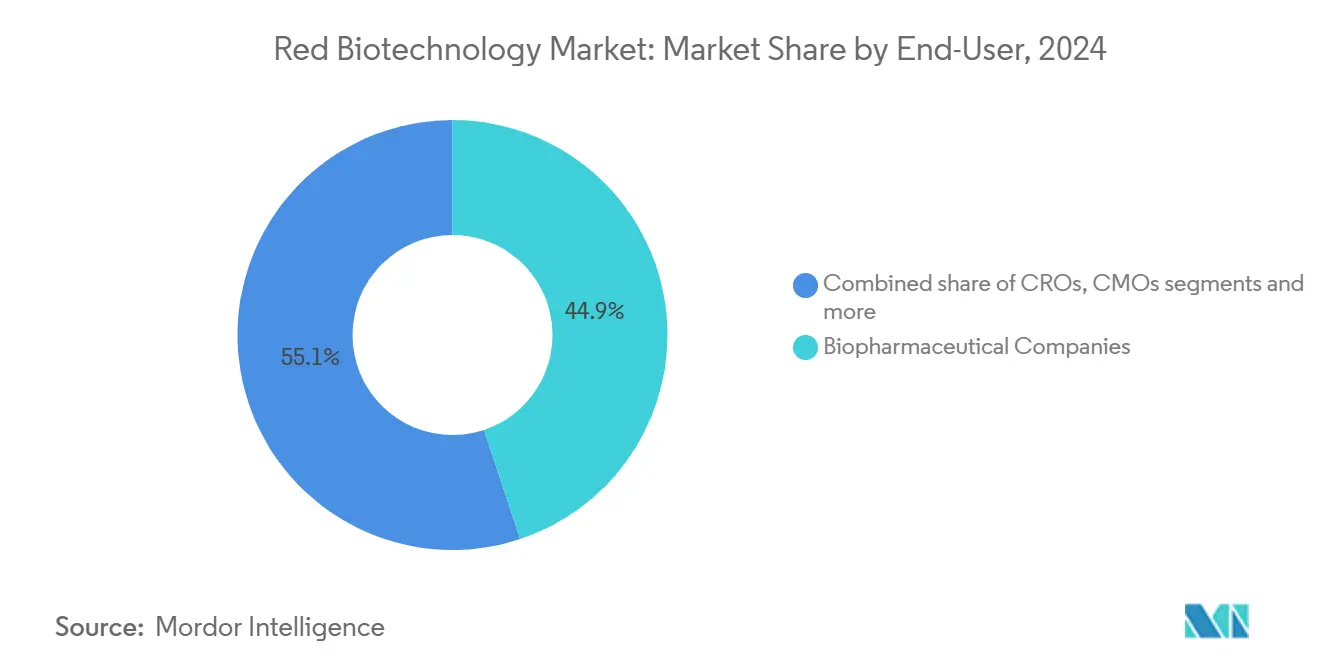
注記: すべての個別セグメントのシェアはレポート購入時に利用可能
地域分析
北米は2024年のRed Biotechnology市場規模の39.13%を占め、2030年まで年平均成長率6.01%を記録すると予測されています。この地域は発見、規制、産業規模製造を束ねたフルスペクトラムエコシステムの恩恵を受けています。BARDAのBioMaP-ConsortiumとPHEMCE資本プールは、通常および緊急バイオ医薬品の両方の国内生産を保護し、FDAの迅速指定が革新的治療の開発期間を短縮しています。ACIP構成員見直しなどの進行中の規制再編は、ワクチン上市タイミングに短期的不確実性をもたらしています。しかし、バイオテクノロジー競争力に150億USDを求める大規模な議会提案は、持続的な政治的コミットメントを示しています。
欧州は2030年まで年平均成長率6.24%で成長すると予測されています。臨床試験規則やHorizon Europe資金を含む政策改革が、多国間試験と国境を越えた知識共有を促進しています。HERAのEUFabインフラストラクチャは、100日以内にmRNA、ウイルスベクター、タンパク質ワクチンを切り替え可能な機敏なサージ能力を提供し、ブロックの自律性を高めています。新しいEMA規則下での手数料増加はコスト圧力を加えますが、バイオシミラー申請書の簡素化に関する同時協議により、国家支払者の低価格バイオ医薬品へのアクセスが拡大する可能性があります。
アジア太平洋地域は年平均成長率7.26%で最も速い勢いを示し、2030年までにセグメント価値が2倍以上になると予想されています。日本の国家戦略は税額控除と加速審査レーンにより、2030年までにセクター産出を15兆円に3倍化することを目指しています。インドのバイオテクノロジー価値は2014年の100億USDから2024年の1,300億USD[4]Press Information Bureau, "2025 Will Witness India Assuming Critical Role in Global Biotechnology Revolution; India's 1st Biotechnology Policy BIO-E3 Brought by Modi Govt 3.0 Has Already Paved the Way for It, Says Science Minister Dr. Jitendra Singh," Press Information Bureau, pib.gov.inへ急上昇し、コスト優位性と世界ワクチン量の60%シェアを活用しています。中国はAI主導発見を深化させており、AstraZenecaとCSPC Pharmaceuticalの53億USDパートナーシップが自己免疫疾患を標的とすることに象徴されています。地域政府は国境を越えた臨床試験を容易にするため規制を同期させており、ヒト初回投与研究とその後の近隣受託工場でのスケールアップを加速しています。
競合環境
市場リーダーシップは、純粋な規模よりも差別化プラットフォームとネットワーク提携を組み合わせる企業に傾いています。BioNTechとBristol Myers Squibbの76億USD二重特異性抗体協定は、モジュラー免疫腫瘍学プラットフォームに投資家が置くプレミアムを示しています。AstraZenecaのCSPCとのAI中心の取引は、リード最適化サイクルを最大50%短縮するマルチオミクスモデルを進展させました。これらのパートナーシップは、大手製薬の資本と専門ノウハウが融合してリスクを共有し、検証を加速するパターンを例示しています。
一方、Red Biotechnology市場はRNAモダリティに白地を開いており、セグメントは6倍拡大すると予測され、脂質ナノ粒子やタンパク質ナノケージなどの送達ビークルに焦点を当てたスタートアップの余地を創出しています。CMOはプラグアンドプレイ能力を提供することで不釣り合いな価値を獲得し、2030年までに世界バイオ医薬品産出のより高いシェアを所有するという予測があります。新興破壊者-例えば、Arcturus Therapeuticsの自己増幅RNAワクチンや、8.7億USDのLilly提携を支えるCamurusの脂質ベースデポゲル-は、製剤革新が患者の利便性と経済的利益の両方を解き放つ方法を実証しています。
高い資本障壁が単一製品企業の参入を制限するため、競争強度は穏やかです。しかし、AIの役割が発見コストを下げ、新規参入者が資産重視のフットプリントを構築するよりも製造をライセンスすることで迅速に牽引力を得ることを可能にしています。結果として、既存企業はIP地位を強化し、Agenusがそのチェックポイント抗体をZydusに許可しながら米国BioCDMO事業を共同立ち上げすることで例示されるように、パイプラインの深さを確保するためより早期段階のライセンスを追求しています。
Red Biotechnology業界リーダー
-
AstraZeneca PLC
-
F. Hoffmann-La Roche Ltd
-
Bristol Myers Squibb
-
Novartis AG
-
Pfizer Inc.
- *免責事項:主要選手の並び順不同

最近の業界動向
- 2025年6月:BioNTechとBristol Myers Squibbは、複数の腫瘍に対するPD-L1とVEGF-Aを標的とする二重特異性抗体BNT327の共同開発・商業化を目的とした76億USDの協力を発表し、50/50ベースで利益を分配
- 2025年6月:AstraZenecaは、1.1億USDの先行支払いを含む慢性疾患の低分子治療薬発見を目的とした53億USDのAI主導研究協定をCSPC Pharmaceutical Groupと締結
- 2025年6月:Eli LillyはCamurusの脂質ベースゲルデポ技術を使用した長時間作用型GLP-1・インクレチンベース肥満薬の共同開発を目的とした8.7億USDの提携をCamurusと締結
- 2025年6月:AgenusとZydus Lifesciencesは、botensilimab・balstilimabを中心とした1.41億USDのパートナーシップを最終化し、ZydusがAgenusの既存施設を活用した米国BioCDMOユニットを立ち上げ
世界Red Biotechnology市場レポート範囲
レポートの範囲によれば、Red Biotechnologyは治療法・診断技術の開発・製造に生物を利用するプロセスです。Red Biotechnology市場は製品別(ワクチン、薬物、その他)、エンドユーザー別(バイオ医薬品企業、CMO・CRO、その他)、地域別(北米、欧州、アジア太平洋、中東・アフリカ、南米)にセグメント化されています。市場レポートは世界の主要地域17カ国の推定市場規模と動向もカバーしています。レポートは上記セグメントの価値(USD)を提供します。
| ワクチン | mRNAワクチン |
| ウイルスベクターワクチン | |
| 組換えタンパク質ワクチン | |
| 結合・サブユニットワクチン | |
| 弱毒生・不活化ワクチン | |
| 治療薬 | モノクローナル抗体 |
| 組換えタンパク質 | |
| 遺伝子治療 | |
| 細胞治療 | |
| RNA治療薬 | |
| 診断・研究ツール | シーケンシング試薬・キット |
| コンパニオン診断アッセイ | |
| ポイントオブケア分子検査 |
| バイオ医薬品企業 |
| 受託製造機関(CMO) |
| 受託研究機関(CRO) |
| 学術・研究機関 |
| 病院・専門クリニック |
| 北米 | 米国 |
| カナダ | |
| メキシコ | |
| 欧州 | ドイツ |
| 英国 | |
| フランス | |
| イタリア | |
| スペイン | |
| その他欧州 | |
| アジア太平洋 | 中国 |
| インド | |
| 日本 | |
| オーストラリア | |
| 韓国 | |
| その他アジア太平洋 | |
| 中東・アフリカ | GCC |
| 南アフリカ | |
| その他中東・アフリカ | |
| 南米 | ブラジル |
| アルゼンチン | |
| その他南米 |
| 製品別 | ワクチン | mRNAワクチン |
| ウイルスベクターワクチン | ||
| 組換えタンパク質ワクチン | ||
| 結合・サブユニットワクチン | ||
| 弱毒生・不活化ワクチン | ||
| 治療薬 | モノクローナル抗体 | |
| 組換えタンパク質 | ||
| 遺伝子治療 | ||
| 細胞治療 | ||
| RNA治療薬 | ||
| 診断・研究ツール | シーケンシング試薬・キット | |
| コンパニオン診断アッセイ | ||
| ポイントオブケア分子検査 | ||
| エンドユーザー別 | バイオ医薬品企業 | |
| 受託製造機関(CMO) | ||
| 受託研究機関(CRO) | ||
| 学術・研究機関 | ||
| 病院・専門クリニック | ||
| 地域別 | 北米 | 米国 |
| カナダ | ||
| メキシコ | ||
| 欧州 | ドイツ | |
| 英国 | ||
| フランス | ||
| イタリア | ||
| スペイン | ||
| その他欧州 | ||
| アジア太平洋 | 中国 | |
| インド | ||
| 日本 | ||
| オーストラリア | ||
| 韓国 | ||
| その他アジア太平洋 | ||
| 中東・アフリカ | GCC | |
| 南アフリカ | ||
| その他中東・アフリカ | ||
| 南米 | ブラジル | |
| アルゼンチン | ||
| その他南米 | ||
レポートで回答される主要質問
Red Biotechnologyでどの治療モダリティが最も迅速な規制承認を得ていますか?
細胞・遺伝子治療は、FDAのRare Disease Innovation Hubなどのプログラム下で迅速審査を受けており、ニッチで高インパクトな治療の承認が早まっています。
人工知能はバイオ医薬品の発見・開発をどのように再構築していますか?
深層学習モデルは現在、タンパク質フォールディングと免疫原性ホットスポットを数時間で予測し、研究者が迅速に設計を反復し、初期段階の失敗リスクを削減できます。
バイオ医薬品企業は受託製造機関(CMO)とのパートナーシップによりどのような戦略的優位性を得ますか?
CMOは、スポンサーが重い設備投資なしに生産をスケールできるモジュラー・使い捨て施設を提供し、より迅速な商業上市と柔軟なパンデミックサージ能力を可能にします。
進化する世界規制は市場参入戦略にどのような影響を与えていますか?
2025年以降のEU・米国での異なる規則により、企業は申請の順序付け、地域特化ブリッジング研究の実施、より高い科学的助言手数料の予算化を行っています。
個別化医療の台頭は診断ワークフローをどのように変えていますか?
コンパニオン診断はポイントオブケアに近づいており、初回患者訪問時に臨床医が標的治療を選択するのに役立つ迅速ゲノムアッセイを統合しています。
どの技術進歩がバイオ医薬品のコールドチェーン物流コスト低減に貢献していますか?
Trans-amplifying mRNAワクチンと次世代安定化添加剤が標準冷蔵での製品保存期間を延長し、超低温保存ネットワークへの依存を軽減しています。
最終更新日:



