Tamanho e Participação do Mercado de Fabricação de Vetores Virais
Análise do Mercado de Fabricação de Vetores Virais pela Mordor Intelligence
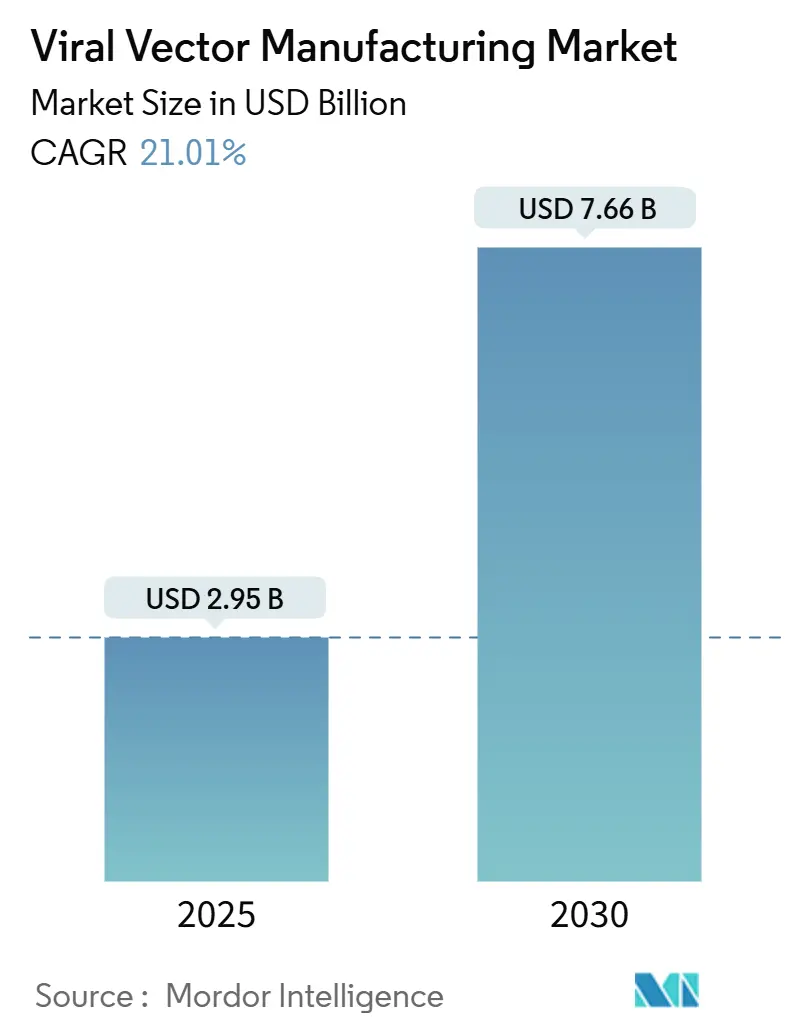
O tamanho do mercado de fabricação de vetores virais foi de USD 2,95 bilhões em 2025 e está previsto para alcançar USD 7,66 bilhões até 2030, implicando uma TCAC de 21,01%. Esta trajetória espelha a transformação da terapia gênica de um nicho experimental em uma classe de tratamento regulamentada, conforme o número de produtos aprovados pela FDA subiu para 14 em 2024. Autorizações inovadoras como Casgevy para doença falciforme e novas indicações para Elevidys na distrofia muscular de Duchenne validaram a demanda comercial e aceleraram o financiamento para infraestrutura de produção. Mais de USD 8 bilhões em projetos greenfield e brownfield foram anunciados pelas principais CDMOs durante 2024-2025, liderados pela Fujifilm Diosynth e Lonza, porém muitas suítes ainda operam abaixo de 50% de utilização porque foram projetadas para trabalhos de fase inicial em vez de produção comercial sustentada. A consolidação está se intensificando conforme os adquirentes buscam capacidades de ponta a ponta, análises avançadas e conhecimento regulatório que reduzam o tempo de chegada ao mercado.
Principais Conclusões do Relatório
- Por tipo de vetor, plataformas virais adeno-associadas representaram 72,45% da receita de 2024, enquanto vetores adenovirais devem crescer a uma TCAC de 23,56% até 2030.
- Por doença, distúrbios genéticos representaram 48,45% da participação do mercado de fabricação de vetores virais em 2024; distúrbios neurológicos devem se expandir a 24,67% de TCAC até 2030.
- Por aplicação, terapias in-vivo detiveram 64,35% do tamanho do mercado de fabricação de vetores virais em 2024 e terapias celulares ex-vivo estão avançando a uma TCAC de 23,55% até 2030.
- Por modo de fabricação, produção interna capturou 62,45% da receita de 2024, enquanto fabricação por contrato deve registrar uma TCAC de 24,56% até 2030.
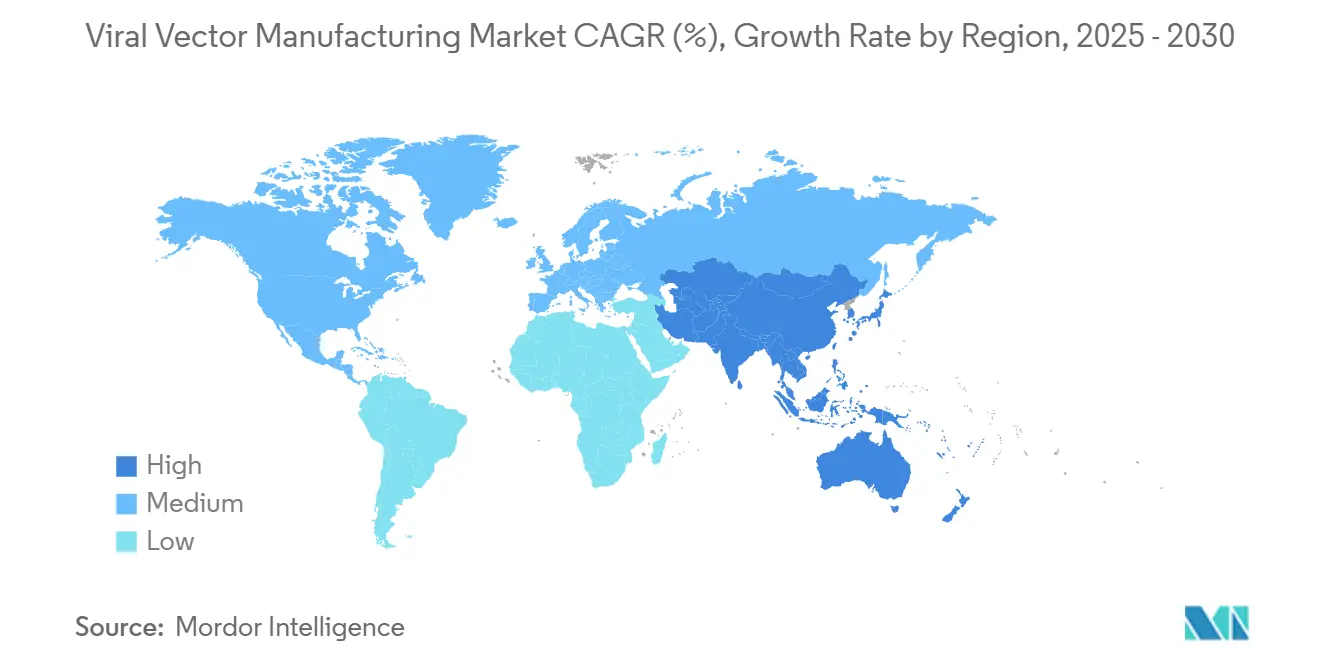
- Por geografia, América do Norte comandou 47,34% da receita de 2024 e Ásia-Pacífico deve crescer a 22,56% de TCAC entre 2025 e 2030.
Tendências e Insights do Mercado Global de Fabricação de Vetores Virais
Análise de Impacto dos Direcionadores
| Direcionador | % de Impacto na Previsão de TCAC | Relevância Geográfica | Cronograma de Impacto |
|---|---|---|---|
| Pipeline crescente de terapia gênica e sucessos clínicos | +4.2% | América do Norte, UE, Ásia-Pacífico | Médio prazo (2-4 anos) |
| Crescente terceirização para CDMOs e expansões de capacidade | +3.8% | América do Norte, Ásia-Pacífico | Curto prazo (≤ 2 anos) |
| Forte financiamento de capital de risco e governamental | +3.1% | América do Norte, UE, China, Singapura | Médio prazo (2-4 anos) |
| Transição para plataformas de cultura celular em suspensão | +2.9% | Hubs globais | Longo prazo (≥ 4 anos) |
| Adoção de biorreatores de uso único | +2.7% | Global | Curto prazo (≤ 2 anos) |
| Engenharia de capsídeo guiada por IA emergente | +2.4% | América do Norte, UE, APAC selecionados | Longo prazo (≥ 4 anos) |
| Fonte: Mordor Intelligence | |||
Pipeline Crescente de Terapia Gênica e Sucessos Clínicos
Mais de 2.000 terapias gênicas estavam em desenvolvimento até 2024, destacando a amplitude de indicações progredindo em direção à comercialização[1]Food and Drug Administration, "Novel Gene Therapy Approvals and Guidance Documents," fda.gov. A aprovação do Kebilidi para deficiência de descarboxilase de aminoácidos aromáticos L marcou a primeira opção terapêutica para este distúrbio neurológico raro e estabeleceu um precedente regulatório para administração de AAV intraparenquimal. O ensaio BENEGENE-2 reportou uma queda de 71% em episódios de sangramento para hemofilia B, confirmando expressão durável do fator IX. Tais marcos clínicos fortalecem a confiança dos pagadores e estimulam estudos de coortes maiores de pacientes, que por sua vez expandem os requisitos de volume de lotes dentro do mercado de fabricação de vetores virais. Conforme o conhecimento do processo melhora, os custos médios de dose de AAV caíram para dezenas de milhares de dólares, permitindo exploração de doenças comuns sem sacrificar a viabilidade econômica.
Crescente Terceirização para CDMOs e Expansões de Capacidade
CDMOs e fabricantes híbridos devem possuir 54% da capacidade global de produtos biológicos até 2028-subindo de 43% em 2024-refletindo um movimento decisivo em direção a modelos com poucos ativos entre desenvolvedores de terapias. A parceria da Charles River com o Gates Institute para serviços lentivirais e a implantação de reatores de uso único de 5.000 L pela Takara Bio ilustram a escala especializada que patrocinadores agora alugam em vez de construir. A UniQure vendeu sua planta em Lexington e terceirizou a fabricação do Hemgenix para a Genezen, demonstrando o cálculo econômico que favorece produção externa para vetores de alta complexidade. A Resilience investiu USD 225 milhões para impulsionar a produção além de 200 milhões de unidades até 2025, mostrando quão rapidamente a demanda está crescendo no mercado de fabricação de vetores virais.
Forte Financiamento de Capital de Risco e Governamental em Terapias Celulares e Gênicas
Apesar de um arrefecimento mais amplo no financiamento de biotecnologia, investidores despejaram capital em plataformas fabricáveis. A VectorBuilder garantiu USD 76 milhões para uma instalação de 30 suítes em Guangzhou, enquanto a China destinou USD 4,17 bilhões para projetos de biofabricação começando em 2025. A estratégia nacional da Alemanha apoiou o centro de terapia gênica de EUR 90 milhões da Roche em Penzberg. O financiamento de risco para empresas de edição gênica caiu para USD 280 milhões em 2024, mas rodadas do início de 2025 apontam para confiança renovada conforme programas alcançam ensaios pivotais. A alocação de capital agora favorece empreendimentos que demonstram caminhos de produção escaláveis e com qualidade assegurada dentro do mercado de fabricação de vetores virais.
Estratégias Emergentes de Engenharia de Capsídeo Guiada por IA
Estruturas de aprendizado de máquina como CAP-PLM predizem a aptidão de capsídeo AAV com alta precisão, permitindo que desenvolvedores estreitem bibliotecas experimentais e reduzam ciclos de descoberta[2]Phys.org Editors, "Machine Learning Elevates AAV Capsid Design," phys.org. Capsídeos melhor projetados podem reduzir pela metade os requisitos de dose de vetor, aliviando pressões de custo e liberando espaço do fermentador. Adotantes precoces nos Estados Unidos e Europa integraram plataformas de IA no desenvolvimento de processos, sinalizando ganhos de eficiência de longo prazo para o mercado de fabricação de vetores virais.
Análise de Impacto das Restrições
| Análise de Impacto das Restrições | (~) % de Impacto na Previsão de TCAC | Relevância Geográfica | Cronograma de Impacto |
|---|---|---|---|
| Alto custo de mercadorias e preocupações com preços de terapia | -2,8% | Global, com ênfase em mercados sensíveis ao preço | Médio prazo (2-4 anos) |
| Complexidade regulatória e atrasos na liberação de lotes | -2,1% | Global, variando por jurisdição regulatória | Curto prazo (≤ 2 anos) |
| Restrições na cadeia de suprimentos para plasmídeos de grau GMP | -1,9% | Hubs de fabricação da América do Norte, Europa, Ásia-Pacífico | Curto prazo (≤ 2 anos) |
| Competição de tecnologias de entrega não-virais | -1,7% | Global, notavelmente em clusters de inovação de terapia avançada | Longo prazo (≥ 4 anos) |
| Fonte: Mordor Intelligence | |||
Alto Custo de Mercadorias e Preocupações com Preços de Terapia
A produção de AAV ainda abrange cerca de três semanas e custa aproximadamente USD 50.000 por construto, com capsídeos vazios inflando volumes e complicando cálculos de título[3]Form Bio Product Team, "AI-Enabled Vector Design Platform," formbio.com. Preços comerciais permanecem altos-Casgevy está listado a USD 2,2 milhões e Hemgenix a USD 3,5 milhões por paciente-levantando preocupações dos pagadores sobre acessibilidade. Debates éticos sobre acesso equitativo limitam a penetração de mercado em regiões de baixa renda. Fabricação de plataforma, densidades celulares mais altas e análises in-line estão reduzindo desperdício, porém grandes economias aparecerão apenas conforme portfólios de estágio tardio amadurecem e volumes aumentam dentro do mercado de fabricação de vetores virais.
Complexidade Regulatória e Atrasos na Liberação de Lotes
A revisão Q5A(R2) da FDA aprofundou requisitos de segurança viral e prolongou pacotes de validação. Distinguir capsídeos cheios de vazios demanda ultracentrifugação analítica ou fotometria de massa que muitas plantas não possuem. Escassez de força de trabalho para essas habilidades especializadas adiciona mais atrasos. A EMA está harmonizando diretrizes, porém cronogramas nacionais escalonados forçam fabricantes a navegar caminhos paralelos. Esses obstáculos retardam lançamentos de produtos e reduzem perspectivas de crescimento para o mercado de fabricação de vetores virais.
Análise de Segmentos
Por Tipo de Vetor: Dominância de AAV Impulsiona Expansão do Mercado
Vetores AAV entregaram 72,45% da receita de 2024 conforme segurança favorável, tropismo tecidual e seis terapias aprovadas pela FDA ancoraram a demanda. O tamanho do mercado de fabricação de vetores virais para produtos AAV deve aumentar drasticamente conforme tratamentos para hemofilia e distrofia muscular escalam volumes comerciais. Mais de 225 ensaios ativos dependem de backbones de AAV, cimentando necessidades de capacidade de múltiplos anos. CDMOs estão comissionando suítes dedicadas a AAV que alavancam biorreatores de suspensão para elevar produtividade.
Vetores adenovirais mantêm a perspectiva de crescimento mais rápida a 23,56% de TCAC até 2030. Engenharia de serotipos novos mitiga imunidade preexistente, abrindo aplicações de vacinas de dose repetida e oncolíticas. Vetores lentivirais permanecem essenciais para fluxos de trabalho autólogos CAR-T; controle de pH melhorado e inibição competitiva agora reduzem 62,1% de perda de partículas funcionais antes comum na fabricação. Plataformas retrovirais e oncolíticas atendem usos oncológicos de nicho, frequentemente em combinação com inibidores de checkpoint, e se beneficiam de parcerias proprietárias de linhagens celulares que melhoram o rendimento.
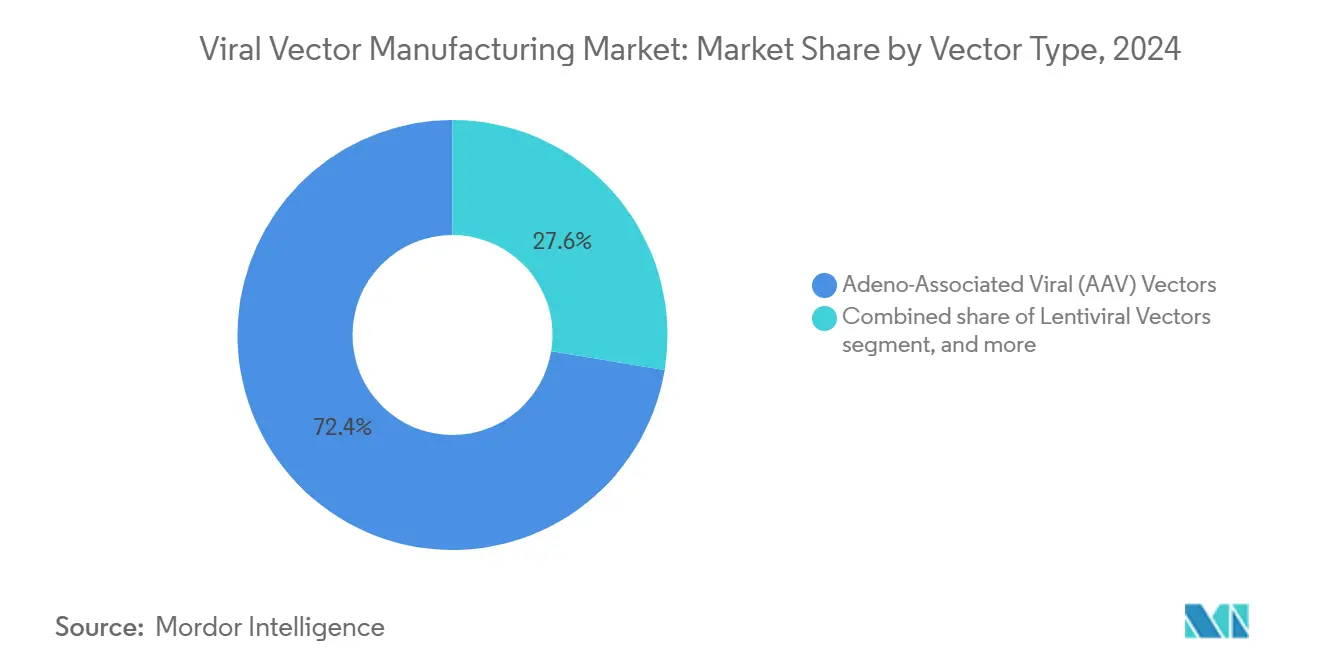
Nota: Participações de segmentos de todos os segmentos individuais disponíveis na compra do relatório
Por Doença: Distúrbios Genéticos Lideram Aplicações Terapêuticas
Distúrbios genéticos responderam por 48,45% da receita de 2024 entre todas as indicações conforme resultados curativos justificaram estruturas de preços premium. Dados de longo prazo em hemofilia A, hemofilia B e doença falciforme incentivaram pagadores a adotar esquemas de pagamento baseados em resultados. O tamanho do mercado de fabricação de vetores virais para essas condições raras permanece considerável devido à demanda reprimida, programas de triagem neonatal e uso expandido do rótulo.
Distúrbios neurológicos devem registrar uma TCAC de 24,67% até 2030. Métodos de administração intratecal e intraparenquimal superaram barreiras anteriores impostas pela barreira hematoencefálica. Resultados positivos de segurança e eficácia em atrofia muscular espinhal e doenças retinianas hereditárias estão impulsionando novos candidatos para Parkinson e ELA. Oncologia mantém uma participação estável via terapias CAR-T que dependem de backbones lentivirais, enquanto projetos de doenças infecciosas pivotam em direção a vetores adenovirais durante cenários de surto.
Por Aplicação: Terapias In-Vivo Impulsionam Crescimento do Mercado
Terapias in-vivo capturaram 64,35% da receita de 2024 porque requerem apenas fabricação de vetores em vez de manipulação celular individualizada. Inovações recentes de capsídeo elevaram eficiência de transdução, permitindo doses menores e encurtando tempos de infusão. Dois candidatos AAV intramusculares protocolados em 2025 destacam o substrato em expansão para administração direta.
Programas de terapia celular ex-vivo mantêm a taxa de crescimento mais alta a 23,55% de TCAC, impulsionados por edições para doença falciforme e beta-talassemia que validaram a economia de fabricação. Linhagens produtoras modificadas como NuPro-2S reduzem impurezas de DNA em 89%, melhorando consistência. Vacinologia preventiva aproveita vetores adenovirais para preparação pandêmica, mas enfrenta pressão competitiva de plataformas de mRNA rapidamente adaptáveis.
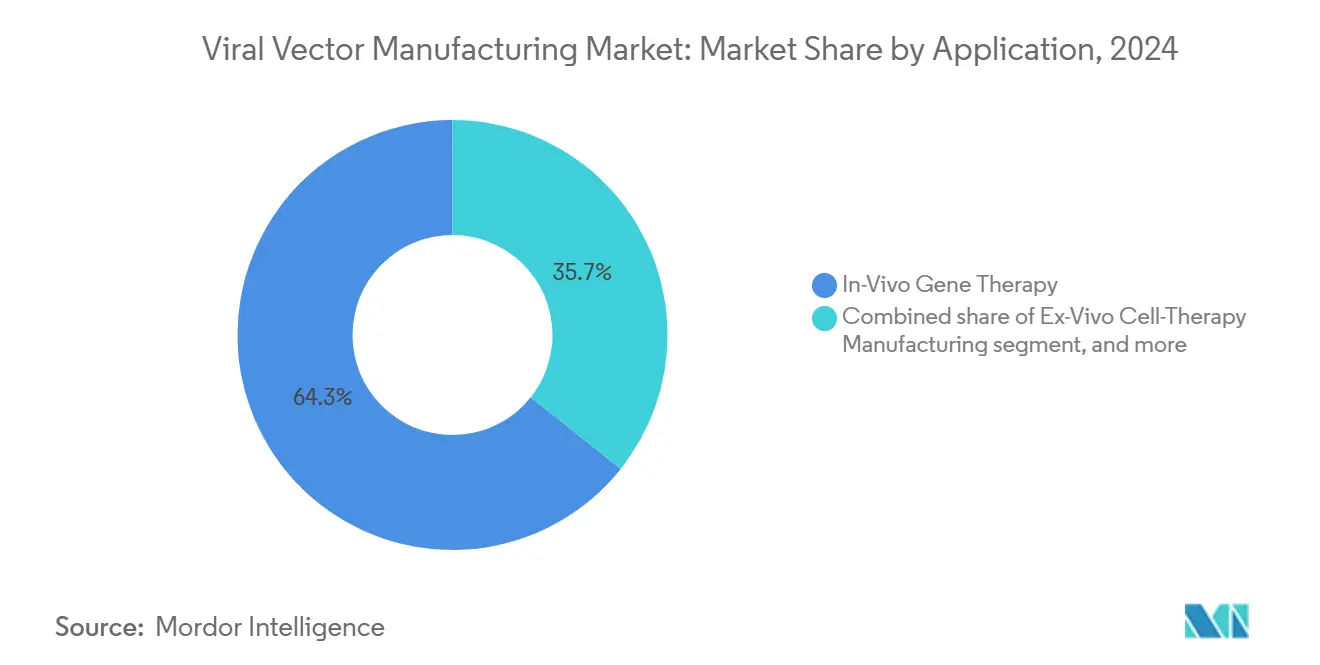
Nota: Participações de segmentos de todos os segmentos individuais disponíveis na compra do relatório
Por Modo de Fabricação: Fabricação por Contrato Acelera
Suítes internas ainda geraram 62,45% da receita de 2024 conforme empresas salvaguardaram conhecimento de processo. Contudo, limites de capacidade e CapEx crescente levaram numerosos patrocinadores a migrar em direção a parceiros externos. O mercado de fabricação de vetores virais está, portanto, inclinando-se em direção a CDMOs que fornecem análises turn-key, validação de processo e suporte regulatório.
Serviços por contrato devem crescer a 24,56% de TCAC até 2030. A aquisição de USD 1,2 bilhão da Vacaville pela Lonza e a expansão de USD 1,2 bilhão da Carolina do Norte pela Fujifilm Diosynth cada uma adicionaram mais de 300.000 L de volume de biorreator. Estratégias híbridas estão ganhando favor conforme desenvolvedores mantêm P&D de pequena escala interno enquanto terceirizam lotes comerciais, dando flexibilidade sem abrir mão do controle central de propriedade intelectual.
Análise Geográfica
América do Norte deteve 47,34% da receita de 2024, impulsionada pelo roteiro regulatório claro da FDA e clusters densos de biotecnologia em Boston, Research Triangle Park e área da Baía de São Francisco. A construção de capacidade de USD 225 milhões da Resilience em Ohio e o site de 128.000 pés² da GenScript ProBio em Nova Jersey sublinham a fé do investidor na infraestrutura doméstica. A região também se beneficia do pool de trabalho mais profundo de especialistas qualificados em vetores.
Europa ficou em segundo lugar e recebeu um impulso do centro de EUR 90 milhões de Penzberg da Alemanha e da instalação completamente robotizada de USD 43 milhões da Novartis na Eslovênia. Diretrizes harmonizadas da EMA simplificam protocolos, embora o Brexit ainda imponha revisões de qualidade de site duplo para produtos que cruzam o Canal. Regulamentações ambientais na UE encorajam sistemas de uso único que reduzem uso de água e pegadas de carbono, influenciando políticas de aquisição em todo o mercado de fabricação de vetores virais.
Ásia-Pacífico deve registrar uma TCAC de 22,56% até 2030. A China reservou USD 4,17 bilhões para linhas de biofabricação começando em 2025, enquanto Japão, Índia e Coreia do Sul atualizam estruturas regulatórias para atrair ensaios multinacionais. A WuXi Biologics reportou crescimento de receita em 2024 que financia linhas adicionais de vetores em Wuxi e Suzhou. Grandes pools de pacientes inexperientes em tratamento e custos operacionais competitivos fazem da região uma plataforma de lançamento preferida para terceirização de fase tardia.
Cenário Competitivo
O mercado de fabricação de vetores virais mostra concentração moderada conforme CDMOs líderes adquirem empresas especializadas para integrar desenvolvimento de linhagens celulares, ensaios analíticos e fill-finish sob um teto. A compra de USD 292,5 milhões da Vigene Biosciences pela Charles River, a aquisição de USD 600 milhões da Mirus Bio pela Merck KGaA e a compra de USD 1,2 bilhão da planta Vacaville da Genentech pela Lonza ilustram os prêmios pagos por escalabilidade comprovada.
Diferenciação tecnológica é agora essencial. O motor de IA da Form Bio prevê capsídeos AAV ótimos, reduzindo loops de tentativa e erro e cortando meses dos cronogramas de desenvolvimento. Linhagens celulares modificadas que reduzem DNA residual abaixo dos limites regulatórios e gêmeos digitais orientados por IA que preveem rendimentos de lotes fornecem ganhos de desempenho mensuráveis. Operadores sem tais conjuntos de ferramentas arriscam competir em preço em vez de ciência de valor agregado.
Perspectivas de espaço branco estão em mercados emergentes e vetores de nicho. A VIVEbiotech levantou capital fresco para expandir serviços lentivirais para programas de neuro-oncologia. A ViroCell Biologics completou financiamento sobre-subscrito para acelerar produção de estágio clínico no Reino Unido. Novos entrantes ainda podem ganhar tração especializando-se em serotipos raros, fill-finish regional ou análises de próxima geração.
Líderes da Indústria de Fabricação de Vetores Virais
-
Lonza
-
Thermo Fisher Scientific, Inc.
-
Charles River Laboratories
-
Fujifilm Diosynth Biotechnologies
-
Catalent
- *Isenção de responsabilidade: Principais participantes classificados em nenhuma ordem específica
Desenvolvimentos Recentes da Indústria
- Março de 2025: WuXi Biologics reportou resultados sólidos de 2024 e previu crescimento acelerado para 2025, citando nova capacidade de vetores na Ásia-Pacífico.
- Fevereiro de 2025: Takara Bio lançou biorreatores de uso único de 50 L-5.000 L para produção de vetores em larga escala.
- Fevereiro de 2025: Novartis abriu uma planta automatizada de vetores virais de EUR 40 milhões na Eslovênia.
- Janeiro de 2025: Fujifilm Diosynth disse que 2025 será seu maior ano de expansão, triplicando o volume de biorreatores de Holly Springs.
- Dezembro de 2024: VIVEbiotech garantiu investimento de crescimento da Ampersand Capital Partners.
Escopo do Relatório Global do Mercado de Fabricação de Vetores Virais
Conforme o escopo deste relatório, vetores virais representam uma das ferramentas primárias para entregar material genético em células. O mercado de fabricação de vetores virais é segmentado por tipo, doença e aplicação. Por tipo, o mercado é segmentado em vetores adenovirais, vetores virais adeno-associados, vetores lentivirais, vetores retrovirais e outros tipos. Por doença, o mercado é segmentado em câncer, distúrbios genéticos, doenças infecciosas e outras doenças. Por aplicação, o mercado é segmentado em terapia gênica e vacinologia. Por geografia, o mercado global é segmentado em América do Norte (Estados Unidos, Canadá, México), Europa (Alemanha, Reino Unido, França, Itália, Espanha, Resto da Europa), Ásia-Pacífico (China, Japão, Índia, Austrália, Coreia do Sul, Resto da Ásia-Pacífico), Oriente Médio e África (CCG, África do Sul, Resto do Oriente Médio e África), e América do Sul (Brasil, Argentina, Resto da América do Sul).
O relatório de mercado também cobre o tamanho estimado do mercado de fabricação de vetores virais e tendências para 17 países em principais regiões globalmente. O relatório oferece o valor (em USD bilhões) para os segmentos acima.
| Vetores Virais Adeno-Associados (AAV) |
| Vetores Lentivirais |
| Vetores Adenovirais |
| Vetores Retrovirais e γ-Retrovirais |
| Vírus Oncolíticos e Outros Vírus Modificados |
| Câncer |
| Distúrbios Genéticos |
| Doenças Infecciosas |
| Distúrbios Neurológicos |
| Outras Áreas Terapêuticas |
| Terapia Gênica In-Vivo |
| Fabricação de Terapia Celular Ex-Vivo (CAR-T, TCR-T, Etc.) |
| Vacinologia Preventiva e Terapêutica |
| Fabricação Interna |
| Fabricação por Contrato (CDMOs) |
| América do Norte | Estados Unidos |
| Canadá | |
| México | |
| Europa | Alemanha |
| Reino Unido | |
| França | |
| Itália | |
| Espanha | |
| Resto da Europa | |
| Ásia-Pacífico | China |
| Japão | |
| Índia | |
| Austrália | |
| Coreia do Sul | |
| Resto da Ásia-Pacífico | |
| Oriente Médio e África | CCG |
| África do Sul | |
| Resto do Oriente Médio e África | |
| América do Sul | Brasil |
| Argentina | |
| Resto da América do Sul |
| Por Tipo de Vetor | Vetores Virais Adeno-Associados (AAV) | |
| Vetores Lentivirais | ||
| Vetores Adenovirais | ||
| Vetores Retrovirais e γ-Retrovirais | ||
| Vírus Oncolíticos e Outros Vírus Modificados | ||
| Por Doença | Câncer | |
| Distúrbios Genéticos | ||
| Doenças Infecciosas | ||
| Distúrbios Neurológicos | ||
| Outras Áreas Terapêuticas | ||
| Por Aplicação | Terapia Gênica In-Vivo | |
| Fabricação de Terapia Celular Ex-Vivo (CAR-T, TCR-T, Etc.) | ||
| Vacinologia Preventiva e Terapêutica | ||
| Por Modo de Fabricação | Fabricação Interna | |
| Fabricação por Contrato (CDMOs) | ||
| Geografia | América do Norte | Estados Unidos |
| Canadá | ||
| México | ||
| Europa | Alemanha | |
| Reino Unido | ||
| França | ||
| Itália | ||
| Espanha | ||
| Resto da Europa | ||
| Ásia-Pacífico | China | |
| Japão | ||
| Índia | ||
| Austrália | ||
| Coreia do Sul | ||
| Resto da Ásia-Pacífico | ||
| Oriente Médio e África | CCG | |
| África do Sul | ||
| Resto do Oriente Médio e África | ||
| América do Sul | Brasil | |
| Argentina | ||
| Resto da América do Sul | ||
Questões Principais Respondidas no Relatório
Qual é o tamanho atual do mercado de fabricação de vetores virais?
O mercado está avaliado em USD 2,95 bilhões em 2025 e deve alcançar USD 7,66 bilhões até 2030 com uma TCAC de 21,01%.
Qual tipo de vetor domina o mercado de fabricação de vetores virais?
Plataformas virais adeno-associadas lideram com 72,45% de participação de receita graças a perfis de segurança favoráveis e múltiplas terapias aprovadas pela FDA.
Por que CDMOs estão ganhando importância na indústria de fabricação de vetores virais?
Desenvolvedores preferem CDMOs especializadas por seus processos validados, análises avançadas e capacidade pronta, evitando o alto CapEx de construir plantas proprietárias.
Qual região está crescendo mais rapidamente no mercado de fabricação de vetores virais?
Ásia-Pacífico deve crescer a 22,56% de TCAC até 2030, apoiada pelas iniciativas de biofabricação multibilionárias da China e capacidades regionais em expansão.
Qual é a principal barreira de custo para adoção mais ampla de terapias gênicas?
Altas despesas de produção mantêm preços de terapia na faixa de USD 2 milhões-USD 3,5 milhões, mas otimização de processos está lentamente reduzindo custo por dose.
Quão concentrada é a competição no mercado de fabricação de vetores virais?
Os cinco principais fornecedores controlam cerca de 60% da capacidade comercial global, indicando concentração moderada que ainda permite que novos entrantes ganhem participação.
Página atualizada pela última vez em:



