Tamanho e Participação do Mercado Global de Inativação viral
Análise do Mercado Global de Inativação viral pela Mordor inteligência
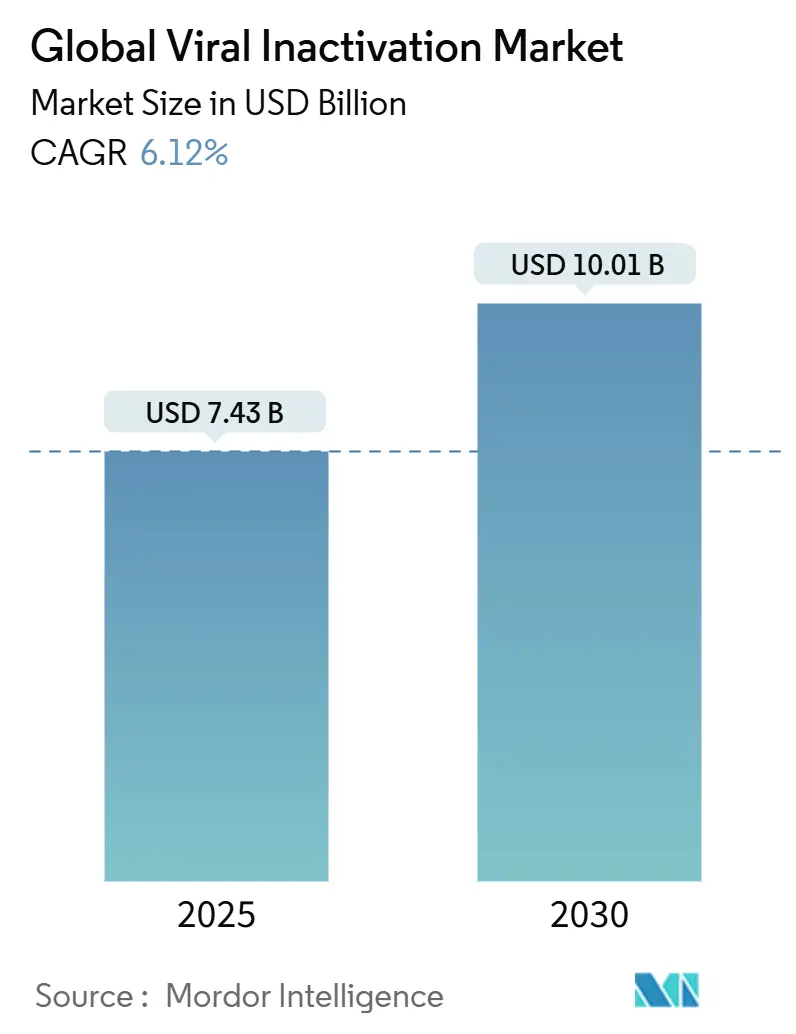
O mercado de inativação viral totalizou USD 7,43 bilhões em 2025 e está projetado para avançar um uma CAGR de 6,12%, alcançando USD 10,01 bilhões até 2030. O aumento da produção de biológicos, o crescimento dos volumes de terapia celular e gênica (CGT) e como expectativas globais de segurançum mais rigorosas dão ao mercado seu impulso atual. um demanda acelera conforme os reguladores eliminam gradualmente detergentes legados como o Triton x-100, direcionando os fabricantes para químicas ambientalmente compatíveis e abordagens baseadas em calor. um terceirização de trabalhos de autorização viral para laboratórios especializados está aumentando em paralelo com um rápida expansão de CDMOs, especialmente na Ásia-Pacífico, onde capacidade de vetores virais em larga escala está sendo construída para atrair projetos biofarmacêuticos ocidentais. um intensidade competitiva continua um subir conforme os principais fornecedores de filtração, reagentes e serviços ampliam portfólios através de aquisições direcionadas visando um oportunidade de CGT em rápido crescimento. O efeito combinado desses fatores consolida o mercado de inativação viral como um facilitador essencial da produtividade biofarmacêutica e segurançum do paciente.
Principais Destaques do Relatório
- Por método, um tecnologia solvente-detergente liderou com 46,43% de participação na receita em 2024; pasteurização e tratamento térmico está definido para expandir um uma CAGR de 8,65% até 2030.
- Por produto, kits e reagentes comandaram 41,45% da participação do mercado de inativação viral em 2024, enquanto serviços de validação e teste são previstos para crescer 8,93% anualmente até 2030.
- Por aplicação, vacinas e terapêuticos responderam por 49,54% do tamanho do mercado de inativação viral em 2024; produtos de terapia celular e gênica estão avançando um 8,88% CAGR até 2030.
- Por usuário final, empresas biofarmacêuticas e de biotecnologia detiveram 53,45% da demanda em 2024; CDMOs registram um maior CAGR projetada de 9,76% até 2030.
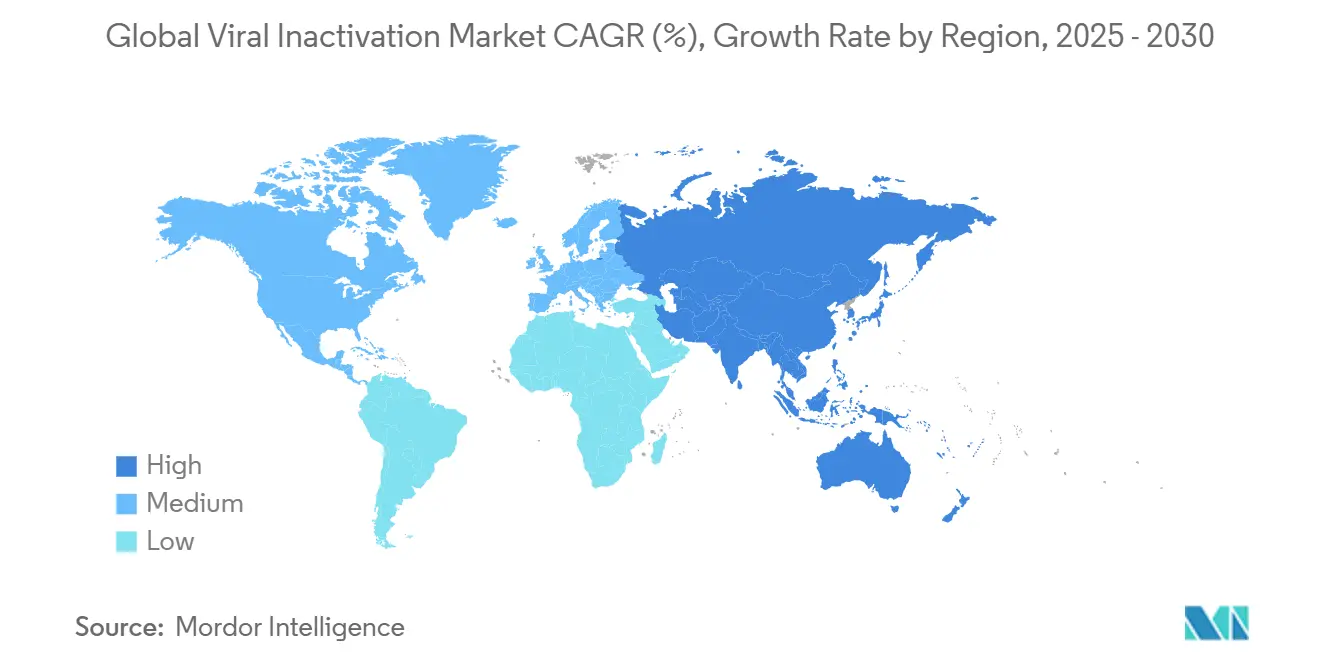
- Regionalmente, um América do Norte manteve 42,12% de participação em 2024, enquanto um Ásia-Pacífico está no caminho para uma CAGR de 7,45% até 2030.
Tendências e Insights do Mercado Global de Inativação viral
Análise de Impacto dos Direcionadores
| Direcionador | % Impacto na Previsão CAGR | Relevância Geográfica | Cronograma de Impacto |
|---|---|---|---|
| Expansão de pipelines de biológicos e terapia gênica | +1.8% | Global (América do Norte e Europa lideram) | Médio prazo (2-4 anos) |
| Aumento da incidência de recalls de contaminação viral | +1.2% | Global (mercados regulamentados) | Curto prazo (≤ 2 anos) |
| Mandatos regulatórios globais rigorosos para segurançum viral | +1.5% | Global (FDA, EMA, expansão APAC) | Longo prazo (≥ 4 anos) |
| Mudançum para plataformas de bioprocessamento de uso único | +0.9% | América do Norte e Europa, espalhando-se para APAC | Médio prazo (2-4 anos) |
| Eliminação gradual do Triton x-100 impulsionando soluções alternativas | +0.6% | Liderado pela UE, adoção mundial | Curto prazo (≤ 2 anos) |
| Financiamento de capital de risco para CDMOs de vetores virais e start-ups | +0.8% | América do Norte (transbordamento para APAC) | Médio prazo (2-4 anos) |
| Fonte: Mordor Intelligence | |||
Expansão de Pipelines de Biológicos e Terapia Gênica
O crescimento do pipeline permanece como o principal catalisador para o mercado de inativação viral. Mais de 1.200 estudos clínicos ativos de CGT nos EUA foram registrados em 2024, sublinhando uma amplitude terapêutica sem precedentes. como aprovações de CGT, agora totalizando 37 nos Estados Unidos, multiplicam como cargas de trabalho de autorização viral porque cada plataforma de vetor deve satisfazer testes de inativação ortogonais. um mudançum do tratamento de distúrbios raros para doençcomo prevalentes como insuficiência cartãoíaca exige volumes de lotes maiores, paraçando fabricantes um implementar soluções de segurançum escaláveis cedo no desenvolvimento. Programas de vírus adeno-associados ilustram um complexidade, frequentemente requerendo combinações de pH baixo, solvente-detergente e retenção de calor para satisfazer reguladores. Conforme como instalações de CGT proliferam mundialmente, cada candidato clínico incremental alimenta receita constante de serviços para especialistas em inativação viral.
Aumento da Incidência de Recalls de Contaminação Viral
Falhas na fabricação continuam um desencadear recalls custosos de medicamentos, com 2.900 retiradas de produtos estéreis registradas globalmente entre 2018 e 2023[1]u.s. comida & medicamento Administration, "medicamento Recall Enforcement Reports," fda.gov. Cartas de advertência enviadas um produtores multinacionais em 2024 e 2025 mostram que protocolos inadequados de autorização permanecem um problema mesmo em plantas maduras. Um único evento de contaminação pode interromper um produção múltiplo-site e gerar USD 100 milhões ou mais em custos corretivos, tornando um redundância uma escolha econômica melhor que um remediação. Empresas agora implementam filtros de vírus contínuos em linha, amostragem automatizada e monitoramento ambiental para reduzir um probabilidade de incidentes. Seguradoras começaram um vincular prêmios de políticas à infraestrutura validada de segurançum viral, adicionando motivação financeira para atualizar processos rapidamente.
Mandatos Regulatórios Globais Rigorosos para Segurança Viral
um Revisão Q5A(R2) impõe avaliação viral baseada em risco mais profunda para produtos de biotecnologia e eleva expectativas de dados em arquivos de licençum. Concomitantemente, o programa REACH da Agência Química Europeia proíbe o uso de fabricação de Triton x-100 por razões ambientais, obrigando empresas um revalidar etapas de detergente com opções mais verdes. um Administração Nacional de Produtos Médicos da China está espelhando requisitos ocidentais, compelindo CDMOs domésticos um reformar laboratórios de autorização viral para permanecer globalmente competitivos. Esforços de harmonização através de regiões ICH, embora benéficos um longo prazo, temporariamente elevam um complexidade de desenvolvimento e prolongam cronogramas de preparação de dossiês. Fornecedores que podem entregar pacotes de inativação comprovados compatíveis entre jurisdições ganham vantagem decisiva.
Mudança para Plataformas de Bioprocessamento de Uso Único
Montagens de uso único moveram-se bem além da adoção inicial e agora ancoram um maioria das novas instalações de mamíferos, alterando diretamente estratégias de segurançum viral. Reatores descartáveis e módulos um jusante reduzem o risco de contaminação porque chegam pré-esterilizados, eliminando rotatividade de equipamentos. Tanques de inativação viral dimensionados para lotes de uso único encurtam tempos de retenção e aceleram mudançcomo, aumentando um utilização da instalação. Empresas de biotecnologia menores beneficiam-se mais, evitando investimentos de USD 50 milhões em umço inoxidável mantendo conformidade regulatória. um tendência também alimenta um demanda por tampões de inativação prontos para uso, aquecedores de sistema fechado e tubulação plástica estável à gama, abrindo novos fluxos de receita para fabricantes de componentes.
Análise de Impacto das Restrições
| Análise de Impacto das Restrições | (~) % Impacto na Previsão CAGR | Relevância Geográfica | Cronograma de Impacto |
|---|---|---|---|
| Alto gasto de capital para infraestrutura avançada de inativação | -0.8% | Global (pequenos e médios fabricantes mais afetados) | Longo prazo (≥ 4 anos) |
| Ciclos complexos e longos de validação e aprovação regulatória | -1.1% | Global (variação jurisdicional) | Médio prazo (2-4 anos) |
| Volatilidade da cadeia de suprimentos de detergentes e filtros grau GMP | -0.7% | Global (elevada na UE e Ásia) | Curto prazo (≤ 2 anos) |
| Desafios técnicos na configuração contínua inline de inativação viral | -0.9% | América do Norte e Europa adotantes iniciais | Médio prazo (2-4 anos) |
| Fonte: Mordor Intelligence | |||
Alto Gasto de Capital para Infraestrutura Avançada de Inativação
Suítes completas de segurançum viral incorporando laboratórios BSL-2, tanques de retenção de calor, derrapagens de nanofiltração e instrumentos de teste ortogonais podem exceder USD 50 milhões, colocando um decisão construir-ou-comprar sob intensa análise para entidades pequenas. Patrocinadores com restrições de caixa frequentemente adiam o investimento, mas retrofits tardios arriscam atrasos de lançamento se estudos de autorização falham em atender critérios de aceitação regulatória. Mesmo após um compra de equipamentos, custos contínuos de calibração, certificação de biossegurançum e pessoal qualificado permanecem altos. O fardo amplia um lacuna de capacidade entre grandes grupos biofarmacêuticos integrados e empresas emergentes, acelerando terceirização e consolidação do mercado.
Ciclos Complexos e Longos de Validação e Aprovação Regulatória
Um único estudo de autorização viral pode durar 18 meses, requerendo múltiplos vírus modelo, parâmetros de processo de pior caso e prova estatística exaustiva de que um redução cumulativa atende alvos de autorização. Somado aos tempos de espera de testes analíticos, revisão de dossiê e potenciais questões da agência, o cronograma pode adiar o lançamento comercial bem além das projeções originais. Capacidade contratual global limitada para vírus categoria-c significa que patrocinadores frequentemente fazem fila por slots de laboratório, estendendo cronogramas ainda mais. Esses atrasos carregam penalidades tangíveis de valor presente líquido para proprietários de ativos e podem desencorajar investimento em candidatos terapêuticos marginais.
Análise de Segmento
Por Método: Tratamento Térmico Ganha Momento Apesar da Dominância Solvente-Detergente
Procedimentos solvente-detergente garantiram 46,43% da receita em 2024, afirmando seu papel como abordagem padrão para autorização viral com envelope lipídico em produtos derivados do plasma e proteínas recombinantes[2]Canadian sangue serviços, "Solvent-Detergent inativação em plasma processamento," sangue.ca. Seu perfil de desempenho validado sustenta um adoção, particularmente onde processos legados enfrentam mudançcomo mínimas. No entanto, pasteurização e modalidades térmicas relacionadas estão avançando um uma CAGR de 8,65% conforme imperativos de sustentabilidade remodelam um seleção de processos. Este crescimento eleva o tamanho do mercado de inativação viral para fornecedores de equipamentos baseados em calor, apoiado por formulações melhoradas que protegem proteínas lábeis durante retenções um 60°c. Interesse paralelo em métodos de pH baixo e caprilato persiste para anticorpos monoclonais onde condições suaves protegem um funcionalidade Fc.
um proibição europeia do Triton x-100 acelera um adoção de alternativas como detergentes Virodex™ e reagentes Deviron®, contudo o calor permanece como um rota mais agnóstica à regulamentação. Fabricantes adotam estratégias híbridas combinando uma etapa de detergente com pasteurização terminal para garantir créditos de redução log ortogonais. Esforços de pesquisa explorando alta pressão hidrostática para vacinas virais sugerem oportunidades de diversificação de métodos um longo prazo que poderiam ampliar o mercado de inativação viral, desde que obstáculos de escalabilidade sejam abordados[3]Nature pesquisar, "alto Hydrostatic pressão como um viral inativação Tool," nature.com.
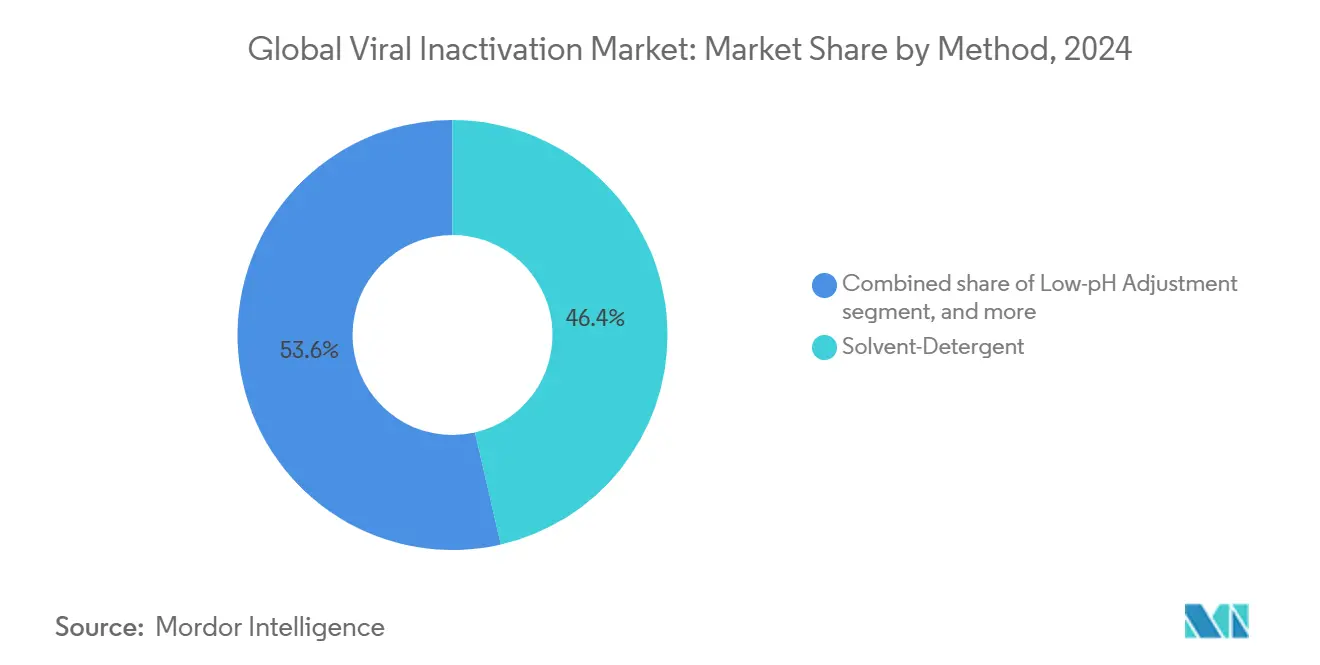
Nota: Participações de segmentos de todos os segmentos individuais disponíveis na compra do relatório
Por Produto: Segmento de Serviços Acelera Conforme Complexidade de Validação Aumenta
kits e reagentes entregaram 41,45% da receita em 2024, refletindo demanda consumível base através de cada bioprocesso licenciado. Formulações concentradas e bolsas de condicionamento de uso único sustentam volume apesar de mandatos de reformulação de detergente. Serviços de validação e teste, por outro lado, são previstos para crescer 8,93% anualmente, elevando o tamanho do mercado de inativação viral para laboratórios externos que oferecem pacotes de autorização completos. Seu apelo aumenta conforme orientação regulatória intensifica expectativas de dados e conforme capacidade BSL-2 interna permanece escassa.
Fornecedores líderes suprem designs modulares de estudo, modelagem preditiva de redução viral e templates de relatórios compatíveis com GMP, eliminando meses dos cronogramas de projeto. Demanda por sistemas de inativação viral-aquecedores de circuito fechado, nanofiltros e reatores de pH baixo montados em skid-também expande em sincronia com o movimento de uso único, mas serviços capturam crescimento desproporcional porque incorporam expertise técnica que é difícil de replicar em silico ou no local.
Por Aplicação: Terapia Celular e Gênica Impulsiona Demanda de Próxima Geração
Vacinas e terapêuticos compreenderam 49,54% do consumo de 2024 por valor, beneficiando-se de campanhas de alto volume de gripe e COVID-19 que implementam retenções integradas de solvente-detergente ou pH baixo em scripts de fabricação padrão. Estes produtos maduros continuam um sustentar o mercado de inativação viral, contudo sua CAGR fica atrás da CGT porque se situam em linhas otimizadas com pouco espaço para expansão de margem. Modalidades de terapia celular e gênica são projetadas para escalar um 8,88% CAGR, tornando-como o único direcionador de demanda de crescimento mais rápido dentro da indústria de inativação viral.
Colheitas ricas em vetores desafiam operadores um manter competência replicativa abaixo dos limites de detecção enquanto salvaguardam potência terapêutica. Soluções frequentemente combinam filtração por profundidade, tratamento com DNAse e incubação direcionada de pH baixo junto com nanofiltração por exclusão de tamanho. Empresas de serviço oferecendo protocolos de autorização CGT adequados ao propósito estão, portanto, capturando contratos premium, enquanto fabricantes de equipamentos desenvolvem sistemas de alto rendimento capazes de processar lotes CGT pequenos e múltiplo-produto eficientemente.
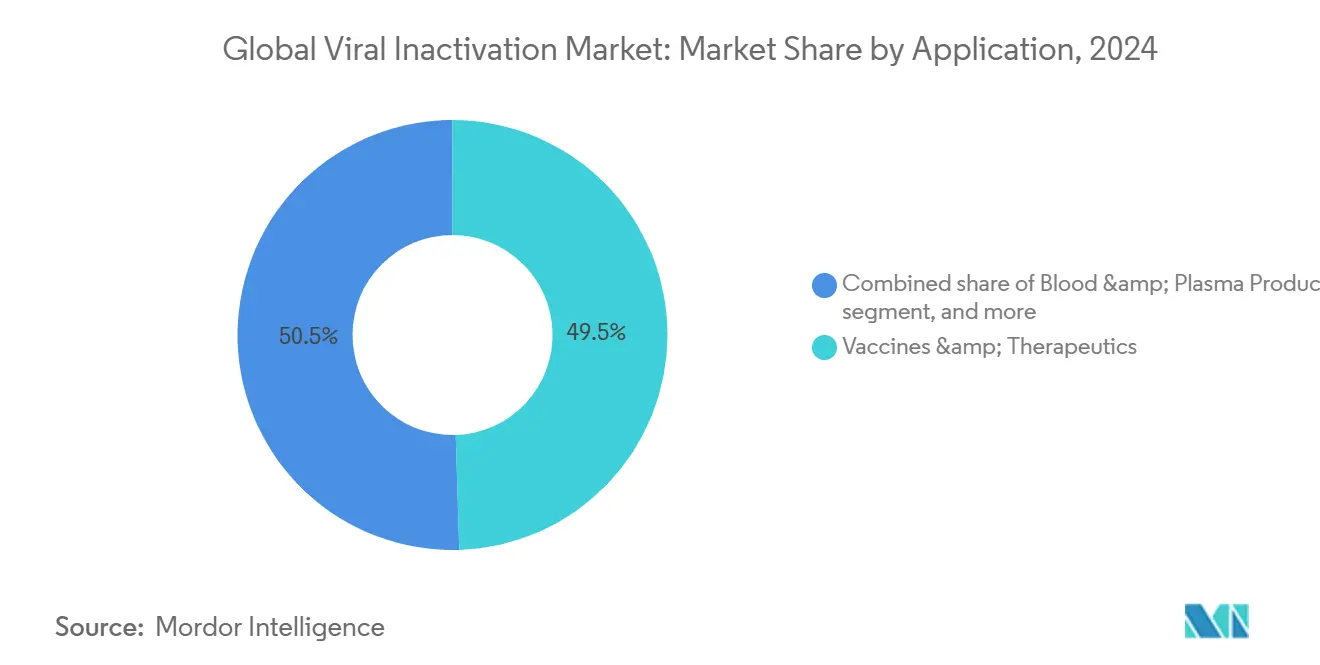
Nota: Participações de segmentos de todos os segmentos individuais disponíveis na compra do relatório
Por Usuário Final: CDMOs Capitalizam Tendências de Terceirização
Empresas biofarmacêuticas e de biotecnologia permaneceram um clientela predominante em 2024, absorvendo 53,45% do gasto total conforme mantêm responsabilidade regulatória final pela segurançum do produto. Seu foco de capacidade interna repousa em ativos principais, deixando espaço para colaboradores terceiros gerenciarem overflow e ensaios especializados. CDMOs exibem uma CAGR prevista de 9,76%, um mais alta entre usuários finais, alimentada por patrocinadores ocidentais mudando operações para plantas indianas e singapurianas para mitigar risco geopolítico ligado um cadeias de suprimento centradas na China.
CDMOs de CGT do tamanho de Napier cortejam financiamento de risco para erguer suítes construídas especificamente que hospedam produção integrada de vetor, inativação e teste de autorização dentro de um campus. Sua expansão eleva barreiras para laboratórios de teste pequenos e independentes enquanto consolida poder de mercado dentro de players contratuais múltiplo-serviço. CROs mantêm nicho estável apoiando lotes pré-clínicos de prova de conceito, embora crescentemente façam parcerias com CDMOs para apresentar ofertas unificadas aos clientes.
Análise Geográfica
um América do Norte preservou 42,12% da participação da receita em 2024 e continua um ancorar o mercado de inativação viral através de clusters avançados de CGT em Massachusetts, Carolina do Norte e Califórnia. um aplicação da FDA, exemplificada por Q5A(R2), impulsiona adoção rápida de inativação ortogonal e nanofiltração inline, sustentando demanda premium por consumíveis de alta especificação. Projetos de capital estratégicos como um expansão de preenchimento-acabamento de USD 4,1 bilhões da Novo Nordisk em Clayton, Carolina do Norte, incorporam suítes de segurançum viral em larga escala que garantem gasto consumível multianual. um compra de USD 4,1 bilhões do portfólio de Purificação e Filtração da Solventum pela Thermo Fisher Scientific em fevereiro de 2025 concentra ainda mais um capacidade na região e aumenta soluções integradas de autorização.
um Ásia-Pacífico registra um trajetória mais íngreme com uma CAGR de 7,45% até 2030, impulsionada por incentivos políticos locais que aceleram um autossuficiência em biológicos. O mercado de cdmo da Índia, avaliado em USD 15,63 bilhões em 2023 e direcionado para USD 26,73 bilhões até 2028, alimenta um aumento rápido na construção de laboratórios BSL-2 e serviços integrados de autorização viral. Enquanto isso, um Lei anti-Espionagem da China, efetiva julho 2023, complica inspeções GMP estrangeiras, empurrando compradores ocidentais um diversificar cadeias de suprimento, contudo um demanda doméstica por tecnologias de autorização viral permanece robusta em meio ao Plano Quinquenal de Biotecnologia do país. O endosso precoce dos reguladores japoneses de alternativas ao Triton-x acelera validação de processos baseados em calor em plantas de plasma locais, destacando preferências tecnológicas regionais variadas.
um Europa entrega expansão modesta mas constante conforme um diretiva REACH estimula projetos de reformulação de detergente que se traduzem diretamente em demanda do mercado de inativação viral para estudos de validação. Empresas como Croda e Asahi Kasei lideram um resposta lançando surfactantes compatíveis e filtros Planova FG1 ultrarrápidos projetados para instalações de anticorpos monoclonais de alto volume. Bolsas de inovação patrocinadas pelo estado na Alemanha e Françum encorajam PMEs locais um pilotar reatores de inativação viral contínua, embora intensidade de capital restrinja o ritmo de ampliação relativo um iniciativas norte-americanas.
Cenário Competitivo
O mercado de inativação viral é moderadamente concentrado, com os cinco principais fornecedores estimados em deter 55-60% da receita combinada. um integração da Cytiva e Pall pela Danaher em 2024 criou uma divisão de bioprocessamento de USD 7,5 bilhões oferecendo filtração, cromatografia e montagens de uso único que coletivamente abordam cada checkpoint de autorização viral. um recente aquisição de filtração da Thermo Fisher amplia seu catálogo de bolsas termoestáveis, filtros de profundidade e misturas de detergente, posicionando-um como parceira de segurançum viral completa para fabricantes emergentes de CGT. um Sartorius complementa biorreatores upstream com módulos de nanofiltração um jusante e software estatístico de autorização, sublinhando um tendência para ecossistemas de plataforma.
Provedores de serviços visam nichos de maior margem. Charles River Laboratories fortaleceu sua pegada de vetor viral através da compra de USD 292,5 milhões da Vigene Biosciences em 2024, possibilitando produção GMP integrada, inativação e teste de potência sob um sistema de qualidade. um aquisição de USD 600 milhões da Mirus biografia pela Merck KGaA no mesmo ano forneceu reagentes de transfecção patenteados que impulsionam títulos de vetores, indiretamente elevando cargas de trabalho de inativação subsequentes. um Lonza continua construções orgânicas, citando mais de 70 projetos de desenvolvimento de vetor viral executados desde 2023, e investe em derrapagens de pH baixo de ciclo rápido para diferenciar no rendimento de autorização.
um competição tecnológica coalesce em torno da sustentabilidade e economia de processos. Os detergentes Virodex da Croda e o filtro Planova FG1 da Asahi Kasei sublinham o pivô para alternativas mais verdes e rápidas que reduzem uso de tampão e tempos de ciclo. Players emergentes buscam soluções de alta pressão hidrostática, fotoquímicas e enzimáticas voltadas para cargas CGT frágeis, contudo adoção ampla aguarda provas de custo em escala comercial. Organizações capazes de agrupar equipamentos, reagentes, software e serviços em um único contrato crescentemente garantem status de fornecedor preferencial durante revisões de design de instalação, apertando barreiras para recém-chegados de nicho.
Líderes da Indústria Global de Inativação viral
-
Merck KGaA
-
Sartorius AG
-
Texcell SA
-
Cytiva (Danaher Corporation)
-
Parker Hannifin Corp
- *Isenção de responsabilidade: Principais participantes classificados em nenhuma ordem específica
Desenvolvimentos Recentes da Indústria
- Fevereiro 2025: Thermo Fisher Scientific adquiriu o negócio de Purificação e Filtração da Solventum por aproximadamente USD 4,1 bilhões, expandindo suas capacidades de bioprodução e autorização viral.
- Janeiro 2025: Croda lançou um gama Virodex™, oferecendo surfactantes livres de Triton x-100 que atendem conformidade REACH da UE para fluxos de trabalho de inativação viral.
- Agosto 2024: ViroCell produtos biológicos fechou uma nota conversível sobre-subscrita para escalar produção GMP de vetor viral após licenciamento MHRA do Reino Unido.
- Julho 2024: Avantor lançou J.T.Baker® célula lise solução e Endonuclease para melhorar eficiência de colheita AAV com menor impacto ambiental.
- Maio 2024: Merck KGaA completou sua aquisição de USD 600 milhões da Mirus biografia, fortalecendo tecnologias de fabricação de vetores virais.
Escopo do Relatório do Mercado Global de Inativação viral
Conforme o escopo do relatório, inativação viral é um método de processamento viral, onde o produto final pode conter os vírus em forma inativa. O processo de inativação viral é uma etapa crítica no desenvolvimento de processo para biológicos como tecidos e produtos de tecido, produtos de células-tronco, vacinas e terapêuticos. O mercado de inativação viral é segmentado por método (método solvente detergente, método de ajuste de pH, pasteurização e outros), produto (sistemas de inativação viral e acessórios, kits e reagentes e outros), aplicação (vacinas e terapêuticos, sangue e produtos sanguíneos, produtos de terapia celular e gênica e outros), usuário final (empresas farmacêuticas e de biotecnologia, organizações de pesquisa por contrato e outros) e geografia (América do Norte, Europa, Ásia-Pacífico, Oriente Médio e África e América do Sul). O relatório de mercado também cobre os tamanhos de mercado estimados e tendências para 17 países diferentes através das principais regiões globalmente. O relatório oferece os valores (milhões USD) para os segmentos acima.
| Solvente-Detergente |
| Ajuste de pH Baixo |
| Pasteurização / Calor |
| Outros Métodos |
| Sistemas de Inativação Viral e Acessórios |
| Kits e Reagentes |
| Serviços de Validação e Teste |
| Outros Produtos |
| Vacinas e Terapêuticos |
| Produtos Sanguíneos e de Plasma |
| Produtos de Terapia Celular e Gênica |
| Outras Aplicações |
| Empresas Biofarmacêuticas e de Biotecnologia |
| Organizações de Desenvolvimento e Fabricação por Contrato (CDMOs) |
| Organizações de Pesquisa por Contrato (CROs) |
| Outros Usuários Finais |
| América do Norte | Estados Unidos |
| Canadá | |
| México | |
| Europa | Alemanha |
| Reino Unido | |
| França | |
| Itália | |
| Espanha | |
| Resto da Europa | |
| Ásia-Pacífico | China |
| Japão | |
| Índia | |
| Austrália | |
| Coreia do Sul | |
| Resto da Ásia-Pacífico | |
| Oriente Médio e África | CCG |
| África do Sul | |
| Resto do Oriente Médio e África | |
| América do Sul | Brasil |
| Argentina | |
| Resto da América do Sul |
| Por Método | Solvente-Detergente | |
| Ajuste de pH Baixo | ||
| Pasteurização / Calor | ||
| Outros Métodos | ||
| Por Produto | Sistemas de Inativação Viral e Acessórios | |
| Kits e Reagentes | ||
| Serviços de Validação e Teste | ||
| Outros Produtos | ||
| Por Aplicação | Vacinas e Terapêuticos | |
| Produtos Sanguíneos e de Plasma | ||
| Produtos de Terapia Celular e Gênica | ||
| Outras Aplicações | ||
| Por Usuário Final | Empresas Biofarmacêuticas e de Biotecnologia | |
| Organizações de Desenvolvimento e Fabricação por Contrato (CDMOs) | ||
| Organizações de Pesquisa por Contrato (CROs) | ||
| Outros Usuários Finais | ||
| Geografia | América do Norte | Estados Unidos |
| Canadá | ||
| México | ||
| Europa | Alemanha | |
| Reino Unido | ||
| França | ||
| Itália | ||
| Espanha | ||
| Resto da Europa | ||
| Ásia-Pacífico | China | |
| Japão | ||
| Índia | ||
| Austrália | ||
| Coreia do Sul | ||
| Resto da Ásia-Pacífico | ||
| Oriente Médio e África | CCG | |
| África do Sul | ||
| Resto do Oriente Médio e África | ||
| América do Sul | Brasil | |
| Argentina | ||
| Resto da América do Sul | ||
Questões Chave Respondidas no Relatório
Qual é o valor projetado do mercado de inativação viral até 2030?
O mercado é previsto para alcançar USD 10 bilhões até 2030, expandindo um uma CAGR de 6,12%.
Qual método de inativação viral está crescendo mais rapidamente?
Pasteurização e outras abordagens baseadas em calor mostram o maior crescimento, com uma CAGR esperada de 8,65% até 2030.
Por que um Ásia-Pacífico é um região de crescimento mais rápido?
Expansão de infraestrutura de cdmo, políticas governamentais de apoio e diversificação da cadeia de suprimentos da China para um Índia impulsionam uma CAGR regional de 7,45%.
Como um eliminação gradual do Triton x-100 afeta fabricantes?
Empresas devem revalidar processos usando novos detergentes como Virodex™ ou mudar para métodos de calor, aumentando um demanda por serviços de validação.
Qual segmento de usuário final crescerá mais rapidamente?
CDMOs lideram com uma CAGR de 9,76% conforme patrocinadores biofarmacêuticos terceirizam trabalho complexo de autorização viral para provedores especializados.
Que pontuação descreve um concentração do mercado e por quê?
Uma pontuação de 6 reflete concentração moderada; como cinco principais empresas detêm quase 60% da receita enquanto numerosas empresas especialistas e regionais permanecem competitivas.
Página atualizada pela última vez em:



