がん悪液質市場規模とシェア
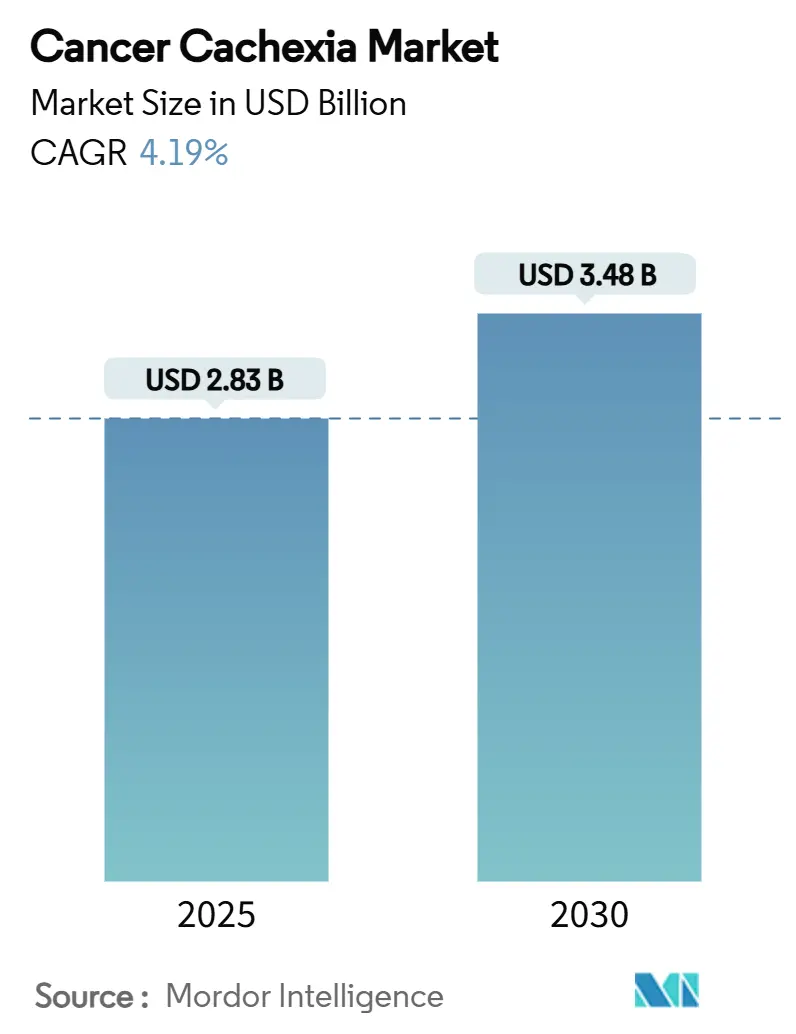
Mordor Intelligenceによるがん悪液質市場分析
がん悪液質市場規模は2025年に28億3,000万米ドルを創出し、年平均成長率4.19%で推移し、画期的な治療薬がコンセプト実証から承認申請試験に移行し、早期診断プログラムが適格患者プールを拡大することにより、2030年には34億8,000万米ドルに達すると予測されています。進行中のがん生存率向上、バイオマーカー対応患者特定、明確な規制ガイダンスの融合により、がん悪液質市場は持続的な拡大が期待されます。成長は既に臨床的実績を持つグレリン受容体アゴニストによって支えられていますが、GDF-15、ミオスタチン、または双方向同化・異化経路をブロックする次世代薬剤が競争分野を多様化させる見込みです。複雑な導入プロトコルのため病院薬局が主要な調剤拠点として残りますが、デジタル在庫ソリューションによりオンラインチャネルがシェア獲得を加速させています。地域的な勢いは米国、日本、中国に依存しており、政府支援の償還パイロット事業により、悪液質が緩和的エンドポイントではなく治療可能な独立疾患として分類され始めています。
主要レポート要点
- 治療薬分類別では、グレリン受容体アゴニストが2024年のがん悪液質市場シェアの34.56%を占めて首位;β遮断薬/ACTAは2030年まで6.56%の年平均成長率で成長すると予測されています。
- 作用機序別では、食欲刺激薬が2024年のがん悪液質市場規模の46.54%のシェアを占める一方、異化経路阻害薬は2030年まで6.83%の年平均成長率で進展しています。
- がん種別では、肺がんが2024年のがん悪液質市場規模の29.54%を占める;血液悪性腫瘍が2030年まで7.99%の年平均成長率で最も速い成長を示しています。
- 段階別では、確立悪液質が2024年のボリュームの48.43%を占める一方、前悪液質介入は7.82%の年平均成長率で拡大しています。
- 流通チャネル別では、病院薬局が2024年に52.34%の売上シェアを維持する一方、オンライン薬局は2030年まで7.65%の年平均成長率を記録しています。
- 地域別では、北米が2024年に43.45%の売上を貢献;アジア太平洋が2030年まで5.43%の年平均成長率で最も急成長している地域です。
世界がん悪液質市場の動向と洞察
推進要因インパクト分析
| 推進要因 | 年平均成長率予測への%インパクト | 地理的関連性 | インパクトタイムライン |
|---|---|---|---|
| がん罹患率の上昇と患者生存率向上 | +1.2% | 世界、北米と欧州に集中 | 長期(4年以上) |
| 体重・筋肉保持に対する高いアンメットニーズ | +0.9% | 世界、アジア太平洋新興市場で深刻 | 中期(2~4年) |
| 悪液質病態生理学理解の進歩 | +0.8% | 北米とEUの研究拠点、アジア太平洋への波及 | 中期(2~4年) |
| がん治療薬パイプライン拡大と併用療法機会 | +0.7% | 世界、米国FDA経路確立が主導 | 長期(4年以上) |
| 主要市場における償還・規制支援の好転 | +0.5% | 北米とEU、日本で新興 | 短期(2年以内) |
| 多角的ケアアプローチの採用拡大 | +0.4% | 世界、統合ヘルスシステムでの最速導入 | 中期(2~4年) |
| 情報源: Mordor Intelligence | |||
がん罹患率の上昇と患者生存率向上
世界的な発症率は2024年に2,000万件を超える新規診断に上昇し、5年生存率は現在平均68%となり、リスク集団を効果的に拡大し代謝低下の窓を延長しています[1]National Cancer Institute, "Cancer Statistics Snapshot," cancer.gov。生存期間の延長により、悪液質は終末的兆候ではなく慢性併存症となり、持続的な薬理学的管理が不可欠となります。免疫がん治療薬はさらに体重減少軌道を変化させ、反復介入を必要とする間欠的筋量減少期を作り出します。高齢人口ががん発症率上昇と重なるため、累積有病率は年々蓄積されます。これらの構造的要因により、がん悪液質市場はより広範ながん治療成長曲線と結びついています。
体重・筋肉保持に対する高いアンメットニーズ
米国および欧州市場でのFDA承認薬剤の不存在により、医師は適応外のコルチコステロイドとメゲストロールに頼らざるを得ませんが、いずれも除脂肪体重や機能的能力を維持しません。がん専門医は悪液質を化学療法用量強度と免疫療法反応の制限因子として捉える傾向が強まり、筋萎縮を予防する薬剤への需要を押し上げています。健康関連生活の質調査では、体重安定性が患者の最優先事項として一貫してランク付けされていますが、現在の治療レジメンでは限定的な利益しか提供されません。異なる基準が多施設試験と償還監査を妨げるため、診断の不透明性が治療ギャップを複雑化しています。
悪液質病態生理学理解の進歩
GDF-15の主要シグナル伝達サイトカインとしての発見により精密介入が可能となり、第2相がんコホートでプラセボに対する平均体重増加5.6%を示したポンセグロマブによって例示されています[2]New England Journal of Medicine Editorial Board, "Targeting GDF-15 in Cancer Cachexia," nejm.org。分子層別化により、炎症負荷、ミトコンドリア機能不全、タンパク質代謝回転率によって患者をセグメント化し、規制証拠基準を満たすカスタマイズされた試験デザインを可能にしています。早期発見のバイオマーカーパネルは病理がまだ可逆的である前悪液質段階での登録を促進しています。産学コンソーシアムは代謝的・遺伝的予測因子の検証を加速させ、ベンチからベッドサイドまでの翻訳タイムラインを短縮しています。
がん治療薬パイプライン拡大と併用療法機会
製薬スポンサーが無増悪生存における除脂肪体重保持の付加価値を評価するにつれ、悪液質エンドポイントの主流がん治療プロトコルへの統合が拡大しています。併用試験では悪液質候補薬をチェックポイント阻害薬、チロシンキナーゼ阻害薬、または細胞毒性薬と組み合わせて、双方向の腫瘍および宿主代謝制御をテストしています。二重目的戦略は全体的な治療アドヒアランスを改善し、原発がん治療においてより高い耐容用量を可能にし、悪液質開発企業に強いパートナーシップレバレッジを提供します。規制当局は合理化された治験薬修正を通じてこのような提携を奨励しています。
制約要因インパクト分析
| 制約要因インパクト分析 | 年平均成長率予測への(~)%インパクト | 地理的関連性 | インパクトタイムライン |
|---|---|---|---|
| 承認薬理療法の限定 | −0.8% | 世界、北米と欧州で最も深刻 | 短期(2年以内) |
| 新規薬剤の安全性・有効性懸念 | −0.6% | 世界、米国とEUでの規制精査強化 | 中期(2~4年) |
| 標準化診断基準と試験エンドポイントの欠如 | −0.5% | 世界 | 中期(2~4年) |
| 高い開発コストと償還不確実性 | −0.4% | 世界、費用対効果要求市場で顕著 | 長期(4年以上) |
| 情報源: Mordor Intelligence | |||
承認薬理療法の限定
欧州医薬品庁のアナモレリン承認拒否は、機能的利益不足を理由としており、変動するエンドポイント期待が開発企業の信頼を冷やすことを実証しています[3]European Medicines Agency, "Assessment Report for Anamorelin," ema.europa.eu。体重と食欲指標だけでは、入院率や生存率との検証された相関を求める支払者を満足させることは稀です。明確な前例がないため、パイプライン企業はより重い財務リスクを負い、しばしばより大きなパートナーとの共同開発を選択し、全体的なイノベーション速度を遅らせます。ラベル承認選択肢の不存在も臨床実践の異質性を永続化させ、真の需要を覆い隠します。
新規薬剤の安全性・有効性懸念
悪液質患者は複雑な併存症と多剤併用負荷を抱えているため、規制当局は特に中枢神経系や心血管系経路を調節する薬剤について、有害事象プロファイルを綿密に精査します。限定的な長期データは持続的な同化刺激と潜在的な腫瘍成長シグナル伝達に関する疑問を提起します。市販後薬事監視コミットメントは総開発コストを押し上げ、小規模バイオテック企業を早期ライセンス・エグジットに向かわせる可能性があります。単一経路阻害薬が分子的に定義されたサブグループでは強固な反応を示すにもかかわらず、疾患の異質性により控えめな総合改善を示す可能性があるため、有効性検証はさらに複雑化します。
セグメント分析
治療薬分類別:ACTA革新の中でグレリンアゴニストがリード
グレリン受容体アゴニストは2024年のがん悪液質市場シェアの34.56%を占め、アナモレリンに対する日本の臨床的親しみやすさと6,000人を超える治療患者から収集された支持的リアルワールドデータを反映しています。この分類のがん悪液質市場規模は、新規承認を待つ市場での段階的導入により、着実な勢いを維持すると予測されています。しかし、β遮断薬ベースの同化・異化変換薬剤(ACTA)は6.56%の年平均成長率の軌道にあり、大腸がんコホートでの蛋白質分解の同時減衰と筋蛋白質合成刺激を示すS-ピンドロールの第2相成功により推進されています。
薬剤開発企業は効果を高めるために、グレリンアゴニストを抗炎症薬またはアンドロゲン受容体調節薬とますます組み合わせています。プロゲストーゲンとコルチコステロイドは進行期疾患でのニッチな有用性を維持していますが、代謝毒性が長期投薬スケジュールを制限するため、限定的な増分収益しか貢献しません。エノボサルムなどの選択的アンドロゲン受容体調節薬は機序的新規性を提供しますが、規制当局は慢性投与の安全性を継続的に精査しています。したがって、ポートフォリオ戦略は機序的多様化に向かい、企業は検証された食欲経路と新興ACTA併用療法のバランスを取っています。
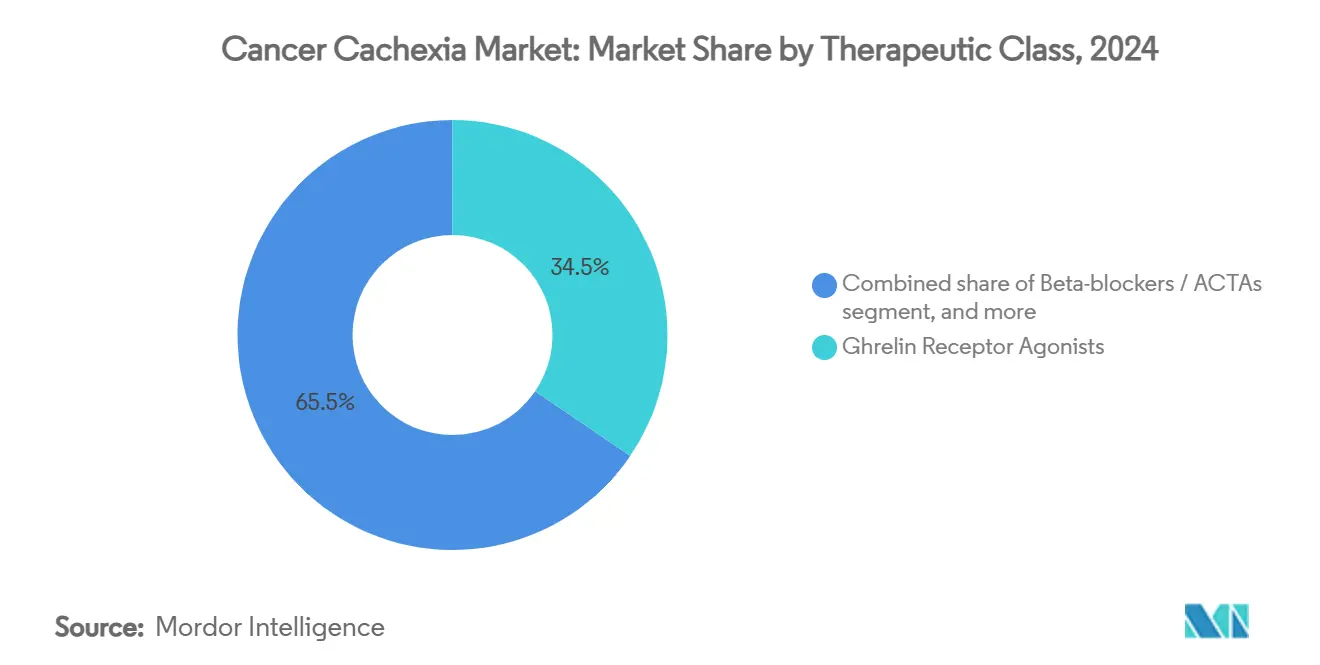
注記: すべての個別セグメントのシェアはレポート購入時に利用可能
作用機序別:食欲刺激の優位性が経路阻害薬に挑戦される
食欲刺激薬は2024年の収益プールの46.54%を確保しましたが、異化経路阻害薬は最速の6.83%年平均成長率が予測され、カロリー摂取だけではサルコペニアを止められないという臨床医の信念の高まりを反映しています。食欲ベース薬剤は規制クリアランスが十分研究された分子を支持する地域での第一選択療法の基盤となりますが、第二世代治療薬は現在、摂食行動を完全にバイパスして筋肉プロテアソーム活性化をブロックしています。したがって、がん悪液質業界はユビキチンリガーゼ活性や下流炎症カスケードを中断する薬剤への転換を目撃しています。
選択的アンドロゲン受容体結合とミオスタチン阻害による同化支援は、しばしば多角的レジメンでパイプライン枠を埋め続けています。IL-1やTNF-αをターゲットとする免疫調節薬は、グレリンアゴニストと組み合わせた場合に相加効果を示し、組み合わせエコシステムが単剤療法の優位性に取って代わる将来を示唆しています。双方向作用ACTAは、欧州で規制認知された機能エンドポイントである握力向上と併せて体重増加を提供することで、この転換を体現しています。業界アナリストは、企業がフランチャイズ価値を守るために統合メカニズムを特許化するにつれ、分類境界が曖昧になると予想しています。
がん種別:血液学的急増による肺がんリーダーシップ
肺がんは最大の単一貢献適応症として残り、全身炎症、慢性低酸素症、積極的な治療レジメンが交差して体重減少を加速するため、2024年のがん悪液質市場規模の29.54%を占めました。しかし、血液悪性腫瘍はCAR-Tおよびバイスペシフィック抗体により生存期間が延長され、異化シグナル伝達への暴露が延長されることを反映して、魅力的な7.99%年平均成長率見通しを示しています。
消化器がんは外科切除と吸収不良が代謝欠損を複合化するため、早期治療介入につながり、相当なセグメントを形成しています。乳がんや前立腺がんなどのホルモン感受性腫瘍では中程度の悪液質発症率を示しますが、臨床的警戒の向上から恩恵を受けています。データが薬剤反応に影響を与える異なるサイトカイン署名を明らかにするにつれ、試験プロトコルは腫瘍生物学による層別化を開始し、精密投薬アルゴリズムを進歩させています。
悪液質段階別:前悪液質予防が勢いを増す
標準化スクリーニングが臨床的消耗が現れる数か月前に微妙な不随意体重減少と炎症マーカーにフラグを立てるため、前悪液質治療は7.82%の年平均成長率で拡大しています。早期開始はより強い除脂肪量保持と改善された治療耐容性と相関するため、がん専門医は筋肉健康チェックをベースライン検査に統合するよう促されています。対照的に、確立悪液質は後期体重減少を中心とした従来の診断習慣のため、2024年のボリュームの48.43%を依然として制御していました。
治療抵抗性悪液質は最も難治性のカテゴリーとして残り、しばしば緩和措置に限定され、高い罹患率のため試験での代表性が不足しています。業界の焦点は、多施設検証研究での77-85%の精度範囲を持つAIモデルを活用して、患者を予防的プロトコルにルーティングできるリスク予測アルゴリズムへとシフトしています。これらのツールは、臨床ガイドラインが進化するにつれて最終的に後期治療を上回る可能性のある予防市場を支援しています。
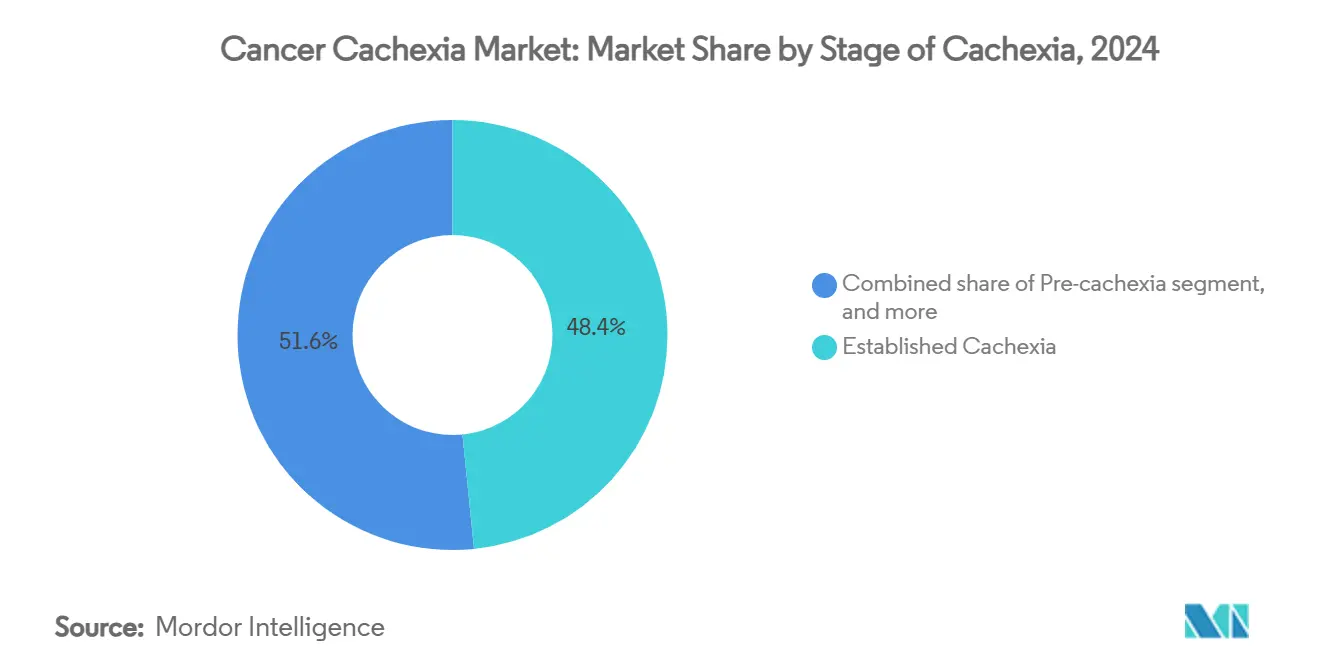
注記: すべての個別セグメントのシェアはレポート購入時に利用可能
流通チャネル別:デジタル変革の中での病院優位
病院薬局は2024年に52.34%の収益を獲得し、導入および早期滴定中のがん専門医監督の必要性を強調しています。ポンセグロマブなどの薬剤は心血管および代謝パラメータのモニタリングを必要とするため、病院販売のがん悪液質市場規模は相当なものとして残るでしょう。それにもかかわらず、遠隔がん治療が償還の正当性を獲得し、コールドチェーン物流が成熟するにつれ、オンライン薬局は7.65%の年平均成長率を示しています。
専門小売店は化学療法スイートと地域診療を橋渡しする医学的統合調剤モデルを採用していますが、償還の遅れが浸透を抑制しています。デジタル・アドヒアランス・プログラム、体重追跡アプリケーション、バーチャル・カウンセリングは経口レジメンを強化し、ハイブリッド・サービス・アーキテクチャを作り出しています。ヘルスシステムは、患者が事前定義された筋肉ベンチマークの維持に失敗した場合に製薬会社がコストを払い戻すアウトカムベース契約を評価し、拡張されたデジタルフォローアップを奨励しています。
地域分析
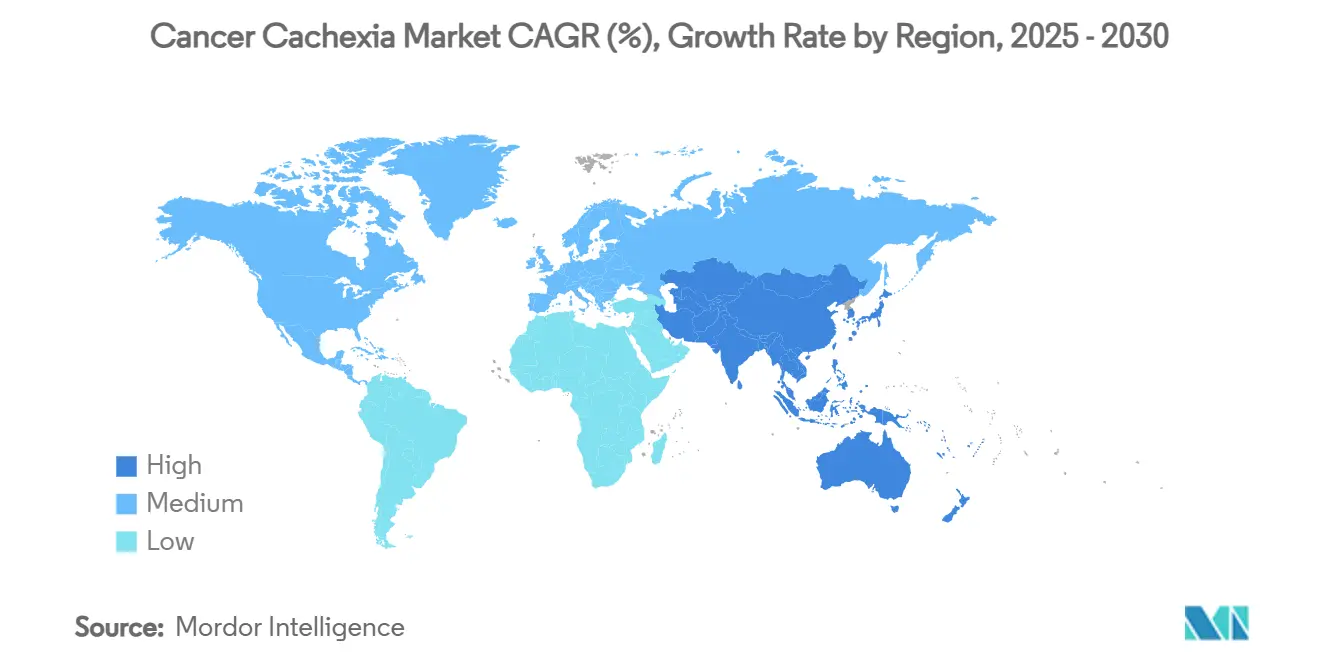
北米は2024年に世界収益の43.45%を創出し、堅調な研究開発資金調達、広範な臨床試験ネットワーク、主要な承認申請試験内での悪液質エンドポイントの早期包含により支えられています。学術センターは日常的にがん治療経路内に代謝モニタリングを組み込み、支持療法クリニックへのタイムリーな診断と紹介を推進しています。この優位性にもかかわらず、民間支払者が短期薬剤コストと未定量の入院節約を比較検討するため、償還向かい風が残存しています。
アジア太平洋は2030年まで5.43%の年平均成長率で進歩しており、日本の画期的アナモレリン収載と中国の急速に拡大するがん治療インフラにより推進されています。韓国、オーストラリア、シンガポール全体の調和されたガイドラインは、外国申請書類の審査タイムラインを短縮しています。地元のバイオテック・パイプラインはミオスタチンとGDF-15経路をターゲットとし、ファーストインクラス発売に対する強力な政府インセンティブを反映しています。官民パートナーシップは、栄養カウンセリングと薬物療法を組み合わせた筋肉健康プログラムに投資し、包括的ソリューションへの需要を加速させています。
欧州は細分化された償還ランドスケープが展開を遅らせるため、中程度の成長を示しています。EMAの機能エンドポイントへの固執は複数の候補薬の市場参入を遅らせていますが、各国のがん計画が現在悪液質スクリーニング指標を追加しており、これが診断率を押し上げるはずです。ドイツとイタリアの主要機関は、理学療法士を薬理学的レジメンと組み合わせる多角的クリニックをパイロット実施し、採用を支持する費用対効果評価を傾ける可能性のあるリアルワールドデータを生成しています。
競争環境
19の注目すべき企業が世界的舞台を共有し、低い2桁の売上を超える企業はなく、市場集中度スコア4を与えています。ファイザーはポンセグロマブと提携の深さを活用して規制先例を設定する一方、Actimed TherapeuticsはACTAノウハウを活用して専門家マインドシェアを切り開いています。Helsinnは市販後調査と地域ライセンシングを通じてアナモレリン・ライフサイクルを延長し、グレリン・フランチャイズの関連性を保っています。
デジタル・ヘルス新規参入企業は製薬会社と協力して、従来の試験募集に対してアルゴリズム患者選択を重ね、登録窓を縮小し統計力を向上させています。特許書類はGDF-15抗体、ミオスタチン阻害薬、選択的アンドロゲン受容体調節薬周辺のクラスタリングを明らかにし、多くの出願が送達ベクターと併用方法をカバーして参入障壁を拡大しています。
メルクKGaAのSpringWorks Therapeutics 39億米ドル買収により支持療法多様化への戦略的欲求が例示され、悪液質に適応可能な希少腫瘍ノウハウを追加する合併買収が例証されています。ライセンス取引は機能エンドポイントに結び付けられたマイルストーン重視の支払いを構造化し、後期価値実現への信頼の高まりを示しています。小規模バイオテックは大型株ポートフォリオを補完する表現型特異的データパッケージを通じて交渉レバレッジを維持しています。
がん悪液質業界リーダー
-
Helsinn Group
-
小野薬品工業
-
Actimed Therapeutics
-
ファイザー
-
ブリストル・マイヤーズ スクイブ
- *免責事項:主要選手の並び順不同
最近の業界動向
- 2025年4月:メルクKGaAがSpringWorks Therapeuticsを39億米ドルで買収し、がん支持療法での存在感を拡大すると発表。
- 2025年3月:Henlius BiotechがHLX22抗HER2モノクローナル抗体の胃がんにおけるFDA希少疾病用医薬品指定を取得。
- 2025年1月:Biomed IndustriesがICOCD-2025でNA-931四重受容体アゴニストとTirzepatideの併用療法プロトコルを発表し、第1相結果で筋肉量減少なしの体重管理ポテンシャルを実証。
- 2024年12月:ファイザーがNew England Journal of Medicineでポンセグロマブ第2相結果を発表し、プラセボに対して5.6%の体重増加を示した。
- 2024年12月:Endevica BioがTCMCB07ペプチドの転移性大腸がんにおける体重減少予防の第2相試験を開始。
世界がん悪液質市場レポート範囲
レポートの範囲によると、がん悪液質は体重減少、食欲不振、無力症、貧血を特徴とする消耗症候群です。この症候群の病原性は、腫瘍と宿主因子の複雑な相互作用により多因子性です。悪液質の徴候と症状は、がん患者の予後パラメータとして考えられています。がん悪液質薬は状態の治療または軽減に使用されます。がん悪液質市場は、治療薬(プロゲストーゲン、コルチコステロイド、併用療法、その他の治療薬)、作用機序(食欲刺激薬と体重減少安定剤)、地域(北米、欧州、アジア太平洋、中東・アフリカ、南米)によってセグメント化されています。市場レポートは世界の主要地域17か国の推定市場規模と動向もカバーしています。レポートは上記セグメントの価値(百万米ドル)を提供しています。
| グレリン受容体アゴニスト |
| 選択的アンドロゲン受容体調節薬(SARM) |
| β遮断薬/ACTA |
| プロゲストーゲン |
| コルチコステロイド |
| 併用療法 |
| その他の治療薬分類 |
| 食欲刺激薬 |
| 同化薬 |
| 異化経路阻害薬 |
| 抗炎症/免疫調節薬 |
| マルチターゲットACTA |
| 肺がん |
| 消化器がん |
| 乳がん |
| 前立腺がん |
| 血液悪性腫瘍 |
| その他のがん種 |
| 前悪液質 |
| 確立悪液質 |
| 治療抵抗性悪液質 |
| 病院薬局 |
| 小売薬局 |
| オンライン薬局 |
| 北米 | 米国 |
| カナダ | |
| メキシコ | |
| 欧州 | ドイツ |
| 英国 | |
| フランス | |
| イタリア | |
| スペイン | |
| その他の欧州 | |
| アジア太平洋 | 中国 |
| 日本 | |
| インド | |
| オーストラリア | |
| 韓国 | |
| その他のアジア太平洋 | |
| 中東・アフリカ | GCC |
| 南アフリカ | |
| その他の中東・アフリカ | |
| 南米 | ブラジル |
| アルゼンチン | |
| その他の南米 |
| 治療薬分類別 | グレリン受容体アゴニスト | |
| 選択的アンドロゲン受容体調節薬(SARM) | ||
| β遮断薬/ACTA | ||
| プロゲストーゲン | ||
| コルチコステロイド | ||
| 併用療法 | ||
| その他の治療薬分類 | ||
| 作用機序別 | 食欲刺激薬 | |
| 同化薬 | ||
| 異化経路阻害薬 | ||
| 抗炎症/免疫調節薬 | ||
| マルチターゲットACTA | ||
| がん種別 | 肺がん | |
| 消化器がん | ||
| 乳がん | ||
| 前立腺がん | ||
| 血液悪性腫瘍 | ||
| その他のがん種 | ||
| 悪液質段階別 | 前悪液質 | |
| 確立悪液質 | ||
| 治療抵抗性悪液質 | ||
| 流通チャネル別 | 病院薬局 | |
| 小売薬局 | ||
| オンライン薬局 | ||
| 地域 | 北米 | 米国 |
| カナダ | ||
| メキシコ | ||
| 欧州 | ドイツ | |
| 英国 | ||
| フランス | ||
| イタリア | ||
| スペイン | ||
| その他の欧州 | ||
| アジア太平洋 | 中国 | |
| 日本 | ||
| インド | ||
| オーストラリア | ||
| 韓国 | ||
| その他のアジア太平洋 | ||
| 中東・アフリカ | GCC | |
| 南アフリカ | ||
| その他の中東・アフリカ | ||
| 南米 | ブラジル | |
| アルゼンチン | ||
| その他の南米 | ||
レポートで回答される主要質問
がん悪液質市場の現在価値は何ですか?
市場は2025年に28億3,000万米ドルと評価され、2030年までに34億8,000万米ドルに達すると予測されています。
がん悪液質市場を牽引する治療薬分類は何ですか?
日本でのアナモレリンの広範な使用により、グレリン受容体アゴニストが34.56%の市場シェアで首位です。
最も急成長している作用機序は何ですか?
異化経路阻害薬は、臨床医が食欲刺激よりも筋肉保持を優先するため、2030年まで6.83%の最高年平均成長率予測を示しています。
最も強い成長機会を提供するがん種は何ですか?
新規治療薬からの生存期間延長が悪液質リスクを増加させるため、血液悪性腫瘍は7.99%年平均成長率で拡大すると予測されています。
最も急速に拡大している地域はどこですか?
増加するがん治療能力と支持的規制経路により、アジア太平洋が5.43%年平均成長率で最速成長を示しています。
なぜ悪液質管理において早期介入が強調されるのですか?
前悪液質治療は不可逆的消耗が起こる前に除脂肪体重を保持し、より良い治療耐容性と下流医療費削減につながります。
最終更新日:



