Taille et part du marché de la médecine régénérative
Analyse du marché de la médecine régénérative par Mordor Intelligence
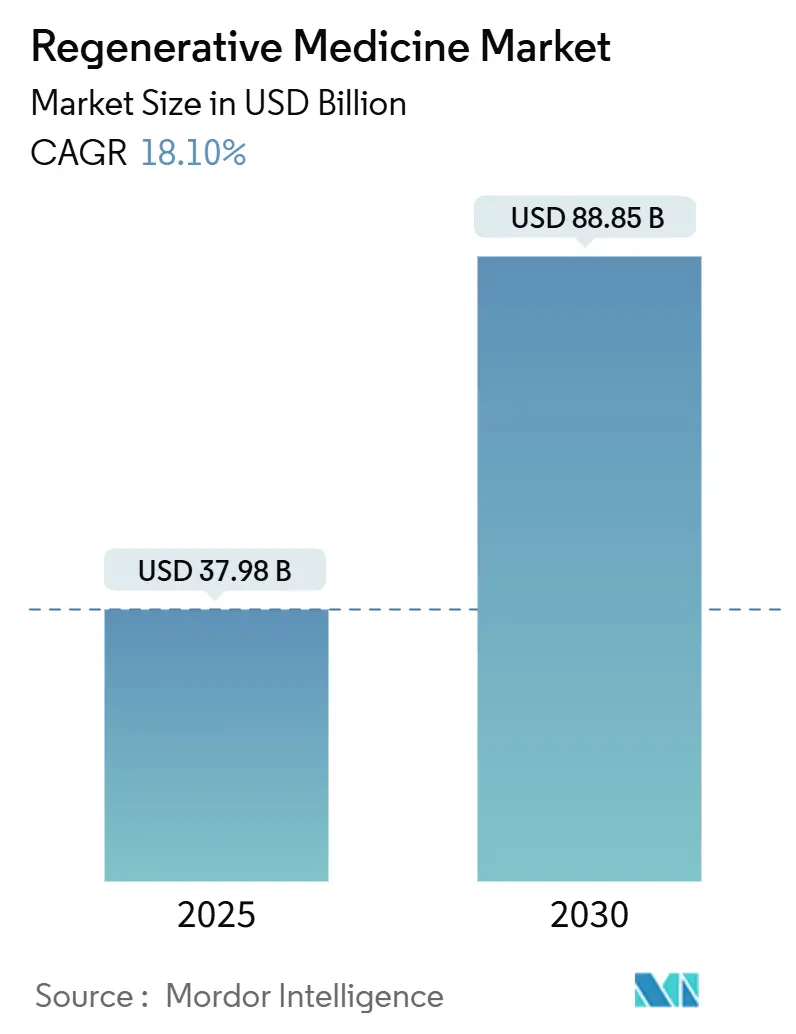
La taille du marché de la médecine régénérative est estimée à 37,98 milliards USD en 2025, et devrait atteindre 88,85 milliards USD d'ici 2030, à un TCAC de 18,10 % pendant la période de prévision (2025-2030).
Le financement soutenu des thérapies cellulaires et géniques avancées, le succès des voies d'approbation accélérées et les investissements importants dans l'infrastructure de fabrication stimulent la demande dans presque tous les domaines thérapeutiques. Les percées en édition génique telles que Casgevy de CRISPR Therapeutics accélèrent l'adoption commerciale, tandis que le modèle allogénique facilite les obstacles historiques de montée en échelle qui limitaient les approches autologues. Les réglementations rationalisées de l'Asie-Pacifique et l'activité croissante des essais cliniques positionnent la région comme un pôle d'innovation pivot. Parallèlement, les obstacles de remboursement pour les produits autologues à coût élevé provoquent une courbe d'adoption inégale qui favorise les payeurs disposant de ressources plus importantes, incitant les développeurs à explorer des accords basés sur les résultats et d'autres modèles de paiement flexibles.
Points clés du rapport
- Par type de produit, les thérapies cellulaires ont dominé avec 42,12 % de part de revenus en 2024 ; les thérapies géniques devraient croître à un TCAC de 25,39 % jusqu'en 2030.
- Par origine des cellules, les thérapies allogéniques ont détenu 55,14 % de la part de marché de la médecine régénérative en 2024, tandis que les thérapies autologues devraient croître à un TCAC de 21,47 % jusqu'en 2030.
- Par source de cellules souches, les cellules souches adultes ont représenté 64,68 % de part du marché de la médecine régénérative en 2024 ; les cellules souches pluripotentes induites (iPSC) progressent à un TCAC de 26,73 % jusqu'en 2030.
- Par application, l'orthopédie et les troubles musculo-squelettiques ont dominé avec 34,64 % de la part de marché de la médecine régénérative en 2024, tandis que l'oncologie devrait croître à un TCAC de 24,59 % jusqu'en 2030.
- Par utilisateur final, les hôpitaux et centres chirurgicaux ont dominé avec 49,13 % de part de revenus en 2024 ; les biobanques et banques cellulaires devraient croître à un TCAC de 20,12 % sur la période de prévision.
- Par géographie, l'Amérique du Nord a détenu 39,95 % de la taille du marché de la médecine régénérative en 2024, tandis que l'Asie-Pacifique devrait croître à un TCAC de 16,22 % jusqu'en 2030.
Tendances et perspectives du marché mondial de la médecine régénérative
Analyse d'impact des moteurs
| Moteur | (~) % Impact sur les prévisions TCAC | Pertinence géographique | Chronologie d'impact |
|---|---|---|---|
| Thérapies allogéniques prêtes à l'emploi rapides | +2.5% | Mondial, mené par l'Amérique du Nord | Moyen terme (2-4 ans) |
| Charge des troubles musculo-squelettiques liés au vieillissement | +2.0% | Asie-Pacifique, Europe | Long terme (≥ 4 ans) |
| Désignations RMAT raccourcissant les approbations | +2.2% | États-Unis | Court terme (≤ 2 ans) |
| Adoption croissante de la technologie iPSC | +1.8% | Amérique du Nord, Japon | Long terme (≥ 4 ans) |
| Centres nationaux de fabrication cellulaire financés par le gouvernement augmentant la capacité GMP | +1.7% | États-Unis, Asie-Pacifique | Long terme (≥4 ans) |
| Intégration de la bio-impression 3D avec des échafaudages de biomatériaux stimulant les substituts cutanés personnalisés | +1.6% | Amérique du Nord, Europe | Moyen terme (2-4 ans) |
| Source: Mordor Intelligence | |||
Translation clinique rapide des thérapies cellulaires allogéniques prêtes à l'emploi
Les plateformes allogéniques redéfinissent l'évolutivité en remplaçant la fabrication spécifique au patient par des lots standardisés qui peuvent être cryoconservés et expédiés selon les besoins. Ces constructions prêtes à l'emploi gagnent en popularité alors que les développeurs obtiennent le statut RMAT qui raccourcit les cycles d'examen réglementaire. En décembre 2024, la FDA a accordé la désignation RMAT au régime acimtamig plus AlloNK d'Affimed après un taux de réponse globale précoce de 83,3 %, validant le modèle pour l'oncologie hématologique.[1]U.S. Food and Drug Administration, "Regenerative Medicine Advanced Therapy (RMAT) Designations," fda.gov Des coûts de production plus bas, couplés à l'expansion de la capacité GMP, permettent aux petites entreprises d'adresser des indications de niche qui manquaient auparavant de faisabilité économique. À mesure que les plateformes iPSC multi-donneurs mûrissent, les avantages de coût de la production allogénique devraient comprimer davantage les prix des thérapies et élargir l'accès des patients.
Augmentation de la charge des troubles musculo-squelettiques dans les populations vieillissantes alimentant les implants d'ingénierie tissulaire
L'espérance de vie croissante fait gonfler la prévalence de l'arthrose, de la maladie discale dégénérative et des conditions connexes, stimulant une part de revenus de 34,64 % pour l'orthopédie au sein du marché de la médecine régénérative. Les implants d'ingénierie tissulaire offrent une durabilité et une intégration biologique supérieures aux prothèses traditionnelles, mais les obstacles à la commercialisation tels que le contrôle de la charge microbienne et la logistique de la chaîne du froid persistent. Les entreprises, notamment Evonik, atténuent ces obstacles grâce aux polymères de qualité médicale (RESOMER) et au collagène recombinant (VECOLLAN) qui améliorent la fidélité de la bio-impression et la stabilité de stockage. La convergence des biomatériaux avancés et de l'impression 3D permet la personnalisation anatomique pour les reconstructions articulaires complexes. Les pilotes des systèmes de santé nationaux au Japon et en Allemagne démontrent déjà des gains de qualité de vie postopératoires qui pourraient soutenir un remboursement plus large des implants d'ingénierie tissulaire, façonnant davantage les tendances du marché de la médecine régénérative.
Désignations de thérapie avancée de médecine régénérative (RMAT) accélérant les approbations
Établi sous le 21st Century Cures Act, le statut RMAT offre des conseils intensifs de la FDA et la perspective d'une approbation accélérée basée sur des critères de substitution. Plus de 35 % de candidats allogéniques supplémentaires ont obtenu RMAT en 2024 par rapport à 2023, soulignant son influence croissante. REGENECYTE basé sur le sang de cordon, ciblant le syndrome Long COVID, a récemment rejoint la liste, obtenant des interactions prioritaires qui raccourcissent les temps de démarrage des essais pivots. Les développeurs adaptent maintenant les conceptions cliniques pour répondre aux critères RMAT tôt, ce qui attire à son tour le capital-risque dans les programmes de phase intermédiaire qui avaient du mal à obtenir un financement de suivi. Les boucles de rétroaction réglementaire plus rapides réduisent l'attrition des programmes et aident les modalités nouvelles, comme les cellules NK éditées génétiquement, à atteindre les patients plus tôt.
Adoption croissante de la technologie des cellules souches dans le marché de la médecine régénérative
Les cellules souches pluripotentes induites (iPSC) sont sur une trajectoire de TCAC de 26,73 %, alimentée par une capacité de différenciation polyvalente et la liberté de l'éthique des tissus embryonnaires. L'algorithme hiPSCore, publié en 2024, identifie 172 gènes prédictifs, donnant aux fabricants une porte de qualité robuste qui réduit le risque d'échec de lot dans la montée en échelle. Simultanément, les équipes de recherche ont démontré que la densité initiale d'ensemencement d'iPSC corrèle de manière quadratique avec le rendement de différenciation, une découverte qui devrait réduire les coûts de milieu dans les grands bioréacteurs. Les pipelines CAR-T dérivés d'iPSC promettent une source inépuisable de cellules T qui contourne les longs cycles de récolte autologue et atténue la menace d'épuisement des cellules T. Les feux verts réglementaires pour les premiers essais iPSC chez l'homme dans la maladie de Parkinson élargissent le manuel clinique au-delà de l'oncologie.
Analyse d'impact des contraintes
| Contrainte | (~) % Impact sur les prévisions TCAC | Pertinence géographique | Chronologie d'impact |
|---|---|---|---|
| Remboursement limité pour les thérapies autologues | -3.0% | Mondial, prononcé dans les marchés émergents | Court terme (≤ 2 ans) |
| Surveillance de sécurité PMDA du Japon pour les constructions éditées génétiquement | -1.5% | Japon | Moyen terme (2-4 ans) |
| Variabilité lot à lot dans les produits dérivés de cellules souches entravant la montée en échelle commerciale | -2.1% | Mondial | Moyen terme (2-4 ans) |
| Faible adoption par les médecins due à la complexité de manipulation des thérapies cellulaires cryoconservées dans les économies émergentes | -1.8% | Marchés émergents | Court-moyen terme (≤3 ans) |
| Source: Mordor Intelligence | |||
Voies de remboursement limitées pour les thérapies autologues à coût élevé
Les étiquettes de prix qui peuvent dépasser 1 million USD par patient entrent en collision avec les systèmes de payeurs à budget plafonné, freinant la vitesse à laquelle les traitements autologues pénètrent les soins de routine. Les réseaux de santé plus riches aux États-Unis et en Europe occidentale ont piloté des contrats basés sur les résultats, mais l'adoption large reste sporadique. Les flux de capital-risque vers les produits médicaux d'ingénierie tissulaire ont modéré alors que les investisseurs évaluent le risque de remboursement par rapport aux longs délais de développement. Bien que les modèles de paiement échelonné et de rente gagnent en traction politique, la complexité administrative du suivi des résultats du monde réel continue de limiter l'évolutivité. Cette incertitude de financement amplifie l'intérêt pour les solutions allogéniques et d'édition génique à coût plus bas, remodelant potentiellement la trajectoire du marché de la médecine régénérative.
Surveillance de sécurité stricte de la PMDA du Japon augmentant le temps de mise sur le marché pour les constructions éditées génétiquement
La PMDA du Japon, bien que louée pour sa législation progressive en médecine régénérative, a introduit des exigences renforcées de surveillance post-commercialisation et de criblage hors cible pour les technologies d'édition génique. Des entreprises telles que Rege Nephro ont échelonné le séquençage clinique pour générer des jeux de données de sécurité spécifiques au Japon avant de migrer les essais vers des sites américains, prolongeant les délais et élevant les coûts. L'examen renforcé intensifie la demande d'essais plus sensibles qui détectent les éditions de faible fréquence, stimulant la collaboration entre la biotechnologie et les laboratoires d'imagerie académiques. Bien que les mesures puissent retarder les lancements, elles devraient renforcer la confiance du public dans les thérapeutiques d'édition génique, facilitant finalement une acceptation plus large en Asie, stimulant ainsi le marché de la médecine régénérative.
Analyse des segments
Par type de produit : Les thérapies géniques redéfinissent les paradigmes de traitement
Les thérapies géniques se rassemblent sur un TCAC de 25,39 % qui pousse le segment vers la parité avec les thérapies cellulaires, qui détenaient 42,12 % de la part de marché de la médecine régénérative en 2024. L'approbation de Casgevy et la première intervention prénatale d'amyotrophie spinale soulignent la portée clinique croissante de l'édition génique. Les développeurs raffinent les nanoparticules lipidiques et la délivrance de vecteurs viraux pour améliorer le ciblage tissulaire et la précision de dose, tandis que les payeurs évaluent les compensations de coût à long terme des guérisons potentielles. Les conseils réglementaires qui clarifient les essais de puissance et les études d'excrétion vectorielle facilitent le progrès clinique à travers l'hématologie, la neurologie et les conditions métaboliques rares. Les investissements de chaîne d'approvisionnement, tels que les suites modulaires de vecteurs viraux, sont prêts à réduire les goulots d'étranglement alors que les pipelines de phase tardive gonflent.
L'élan dans l'édition génique stimule la demande en aval de services auxiliaires, notamment la bio-informatique, la caractérisation génomique et le séquençage de lecture longue. Les organisations de développement contractuel augmentent la fabrication de plasmides pour répondre aux besoins croissants des sponsors. À mesure que les données de résultats s'accumulent, les cadres de tarification basés sur la valeur devraient évoluer, ancrant les calendriers de paiement sur les benchmarks de durabilité sur des horizons de plusieurs années. Ces changements renforcent collectivement le marché de la médecine régénérative contre les vents contraires de remboursement et élargissent les critères d'éligibilité des patients.
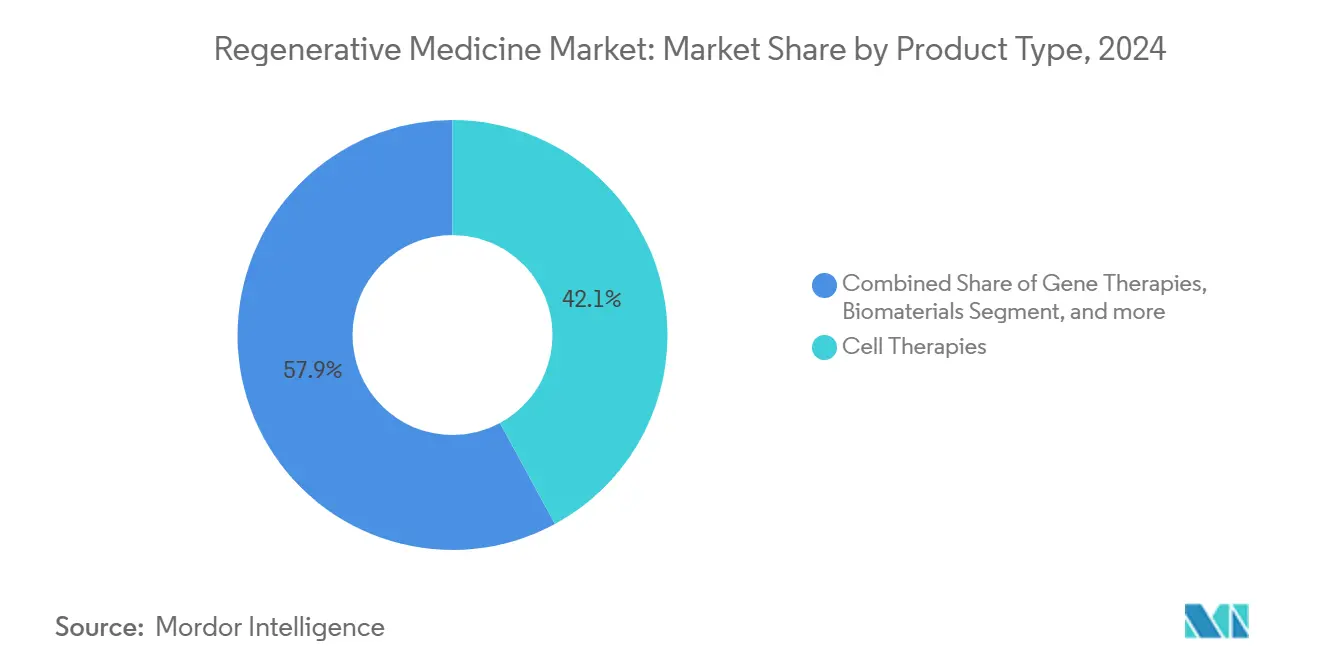
Note: Parts de segment de tous les segments individuels disponibles à l'achat du rapport
Par origine des cellules : Les solutions allogéniques stimulent l'évolutivité
Les produits allogéniques ont mené avec 55,14 % de part de revenus du marché de la médecine régénérative en 2024, capitalisant sur la production par lots qui homogénéise la qualité et réduit le coût par dose. La différence d'échelle se traduit directement par des délais plus courts pour les indications aiguës comme le lymphome en rechute, où les retards dans la fabrication autologue peuvent être fatals. Les cellules T dérivées d'iPSC multifonctionnelles, montrant déjà une activité anti-myélome robuste, sont positionnées pour amplifier cette trajectoire une fois que les données biologiques de phase 1 mûrissent.
Les approches autologues, cependant, maintiennent un avantage dans la reconnaissance d'antigènes tumoraux personnalisés et affichent actuellement un TCAC solide de 21,47 %. Les modèles hybrides - où les patients reçoivent une dose de démarrage autologue suivie d'une consolidation allogénique - sont sous investigation précoce et pourraient brouiller les frontières existantes. La résilience de la chaîne d'approvisionnement, notamment les pools de donneurs redondants et les unités automatisées de décongélation cellulaire, reste cruciale pour assurer la cohérence des produits lors d'un déploiement mondial rapide.
Par source : Les iPSC révolutionnent les paradigmes de développement
Les cellules souches adultes ont détenu 64,68 % de la taille du marché de la médecine régénérative en 2024, soutenues par des décennies de familiarité clinique. Pourtant, les iPSC évoluent à un TCAC de 26,73 % grâce à des paysages de brevets permissifs et à la capacité de dériver des lignées spécifiques au patient ou entièrement universelles. L'outil hiPSCore donne aux régulateurs des métriques standardisées pour l'évaluation de la pluripotence, réduisant le besoin d'essais de tératome exhaustifs en aval.
En production, le lien quadratique documenté entre la densité iPSC initiale et le rendement de différenciation permet une planification prédictive des lots, lissant le transfert de technologie vers les réacteurs commerciaux. Le succès dans les premières greffes de maladie de Parkinson élargit l'intérêt des investisseurs au-delà de l'oncologie, avec des essais cardiovasculaires et ophtalmologiques en file d'attente. La convergence de l'' édition de base ' CRISPR avec les plateformes iPSC pourrait bientôt permettre la correction simultanée de multiples défauts monogéniques.
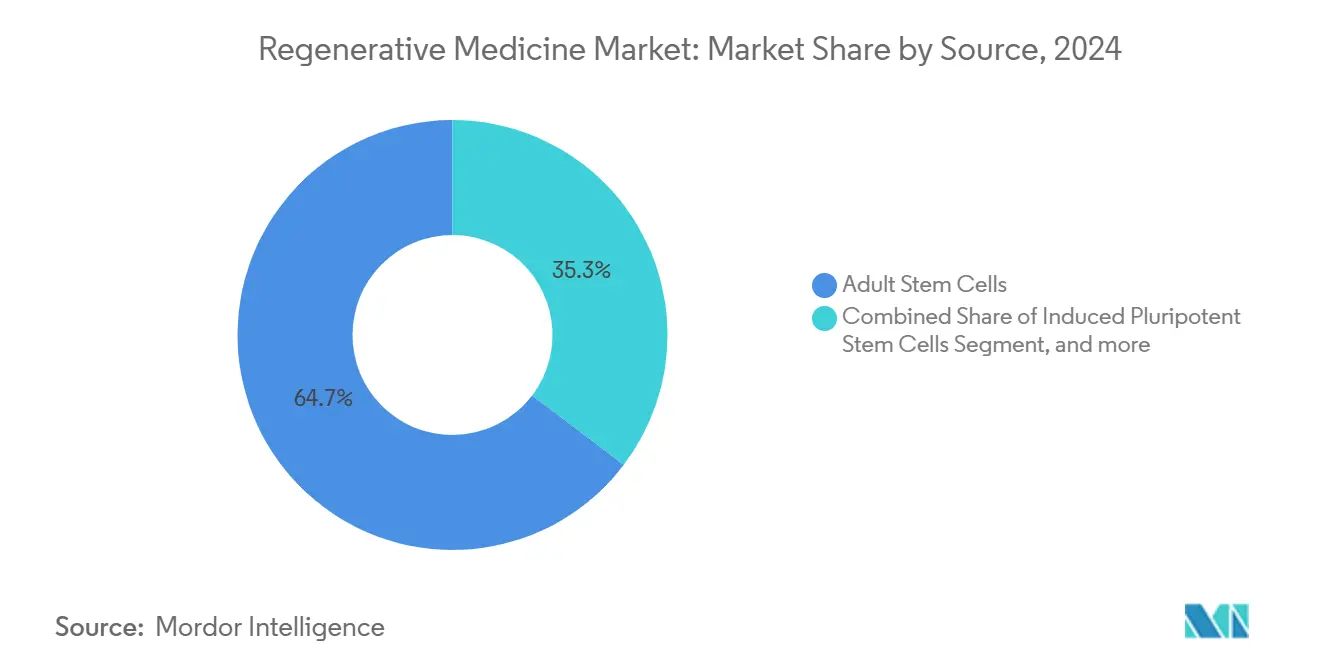
Note: Parts de segment de tous les segments individuels disponibles à l'achat du rapport
Par application : L'oncologie stimule l'innovation et la croissance
L'orthopédie continue d'ancrer 34,64 % de la part de marché de la médecine régénérative, mais l'oncologie trace un TCAC de 24,59 % qui pourrait la propulser à la première position de revenus avant 2030. Les actifs soutenus par RMAT tels que les extensions Kymriah de Novartis dans le lymphome folliculaire soulignent la volonté du payeur de financer les thérapies à intention curative. Les données précliniques suggèrent que les constructions CAR-T dérivées d'iPSC peuvent être cryoconservées sans perdre de puissance cytotoxique, réduisant les coûts logistiques et améliorant la faisabilité des essais.
Au-delà des malignités hématologiques, les applications de tumeurs solides bénéficient de techniques d'édition génique en tandem qui intègrent des modules de blocage de point de contrôle dans les charges utiles cellulaires, augmentant la persistance dans les microenvironnements hostiles. Ces percées filtrent dans la neuro-oncologie et les cancers pédiatriques rares, élargissant la portée thérapeutique du marché de la médecine régénérative.
Par utilisateur final : Les biobanques émergent comme infrastructure critique
Les hôpitaux et centres chirurgicaux ont représenté 49,13 % des revenus d'utilisateurs finaux du marché de la médecine régénérative en 2024, reflétant leur rôle de gardien dans l'administration aiguë. Les biobanques, bien que plus petites aujourd'hui, dépassent tous les autres canaux à un TCAC de 20,12 % alors que la demande de sang de cordon standardisé et de lignées iPSC s'intensifie. Les avancées dans l'expansion des cellules souches hématopoïétiques permettent maintenant à une seule unité de cordon de traiter plusieurs receveurs, renforçant la justification économique du stockage à long terme.
Les régulateurs rédigent des cadres qui clarifient les règles de consentement, propriété et partage de données, ce qui à son tour débloque les partenariats entre biobanques et fabricants de thérapies. L'intégration de la chaîne de valeur de la collecte à l'infusion au chevet est attendue pour comprimer les délais d'exécution et améliorer la traçabilité. Ces tendances positionnent les biobanques comme des nœuds stratégiques qui permettent des modèles de fabrication distribués et juste-à-temps.
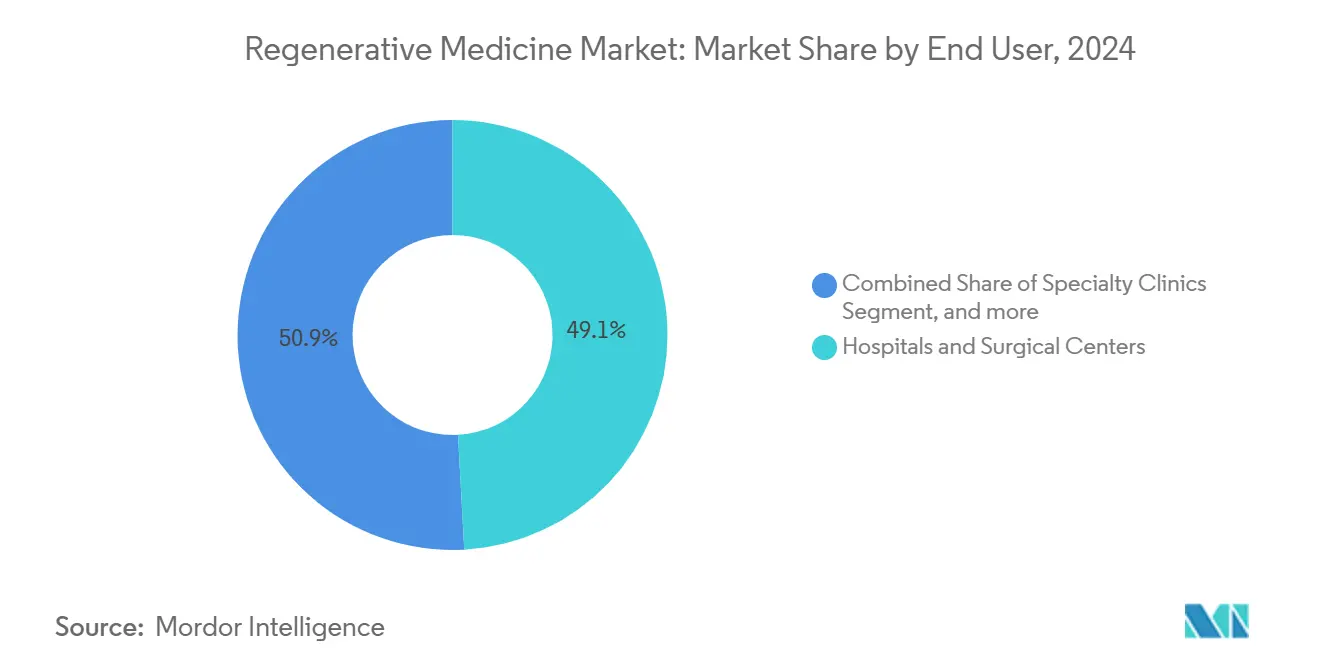
Note: Parts de segment de tous les segments individuels disponibles à l'achat du rapport
Analyse géographique
L'Amérique du Nord a contrôlé 39,95 % du marché de la médecine régénérative en 2024, tirant parti d'une structure FDA qui récompense l'innovation révolutionnaire. La voie RMAT a déjà donné le feu vert à plusieurs candidats first-in-class, réduisant le risque de développement perçu et déclenchant des afflux de capitaux substantiels. L'engagement de 23 milliards USD de Novartis pour étendre la fabrication aux États-Unis, avec sept nouvelles usines en ligne, illustre comment les grandes pharma cimentent la souveraineté de la chaîne d'approvisionnement.[2]Novartis, "USD 23 Billion U.S. Manufacturing Expansion Plan," novartis.com Les collaborations académiques précoces, telles que le programme de cellules souches cardiaques pédiatriques de la Mayo Clinic, continuent d'alimenter le pipeline clinique avec des indications à fort impact. Les disparités persistantes de remboursement, cependant, créent des poches d'accès limité même dans un environnement généralement favorable.
L'Asie-Pacifique avance à un TCAC de 16,22 %, propulsée par les règles de licence adaptative du Japon et la part de 42 % de la Chine des essais mondiaux sponsorisés par l'industrie en 2023. Les initiatives d'harmonisation à la NMPA de Chine réduisent les dépôts redondants, permettant l'exploitation de données transfrontalières. Les centres GMP soutenus par le gouvernement, typifiés par le programme multi-organes du Wake Forest Institute for Regenerative Medicine, mettent à l'échelle le savoir-faire de fabrication qui bénéficie aux petites entreprises.[3]Wake Forest Institute for Regenerative Medicine, "Translational Regenerative Medicine Programs," wfirm.org Pourtant, les lacunes infrastructurelles dans la logistique de la chaîne du froid et l'analyse de contrôle qualité restreignent encore le rythme auquel les thérapies s'étendent au-delà des villes de niveau un.
L'Europe maintient un pied concurrentiel malgré la fragmentation réglementaire. L'Allemagne héberge la plus forte concentration d'entreprises de médecine régénérative, aidée par une culture de recherche collaborative et des schémas de financement public-privé. La Commission européenne a commencé à rédiger des directives unifiées de thérapie avancée, visant à réduire les évaluations au cas par cas qui ralentissent actuellement les lancements de produits ec.europa.eu. Les pilotes de paiement innovants, notamment le remboursement basé sur les jalons en Italie pour les perfusions de thérapie génique, aident à réconcilier la valeur clinique avec la prudence fiscale. Les alliances transatlantiques sont en hausse, avec des entreprises de l'UE licenciant des biomatériaux propriétaires aux développeurs américains qui fournissent une expertise d'essai de phase tardive.
Paysage concurrentiel
Le paysage concurrentiel du marché de la médecine régénérative inclut des biotechs spécialisées dirigeant la découverte précoce et de grandes entreprises pharmaceutiques mettant à l'échelle les actifs de phase tardive. Novartis a approfondi son portefeuille en procédant à l'acquisition de 91,04 % des actions de MorphoSys AG en 2024, une étape qui intègre l'expertise en anticorps axée sur l'oncologie dans la plateforme cellulaire et génique de l'entreprise. Les entreprises de niveau intermédiaire s'associent avec des organisations de développement contractuel pour surmonter les goulots d'étranglement des vecteurs viraux, tandis que les spin-offs académiques fournissent des pipelines de découverte à haute valeur.
Les opportunités d'espace blanc persistent dans la fabrication évolutive et les indications non-oncologiques telles que la maladie rénale chronique et les troubles auto-immuns. Le lancement par Evonik de collagène recombinant de qualité médicale montre comment les entreprises de science des matériaux capturent des parts en résolvant les obstacles structurels dans l'ingénierie tissulaire. Les incitations réglementaires, particulièrement RMAT, inclinent la sélection de partenaires vers les candidats avec viabilité d'approbation accélérée, provoquant une hausse des accords de licence basés sur les jalons.
La consolidation devrait s'accélérer alors que les thérapies géniques commercialisées valident les modèles commerciaux. Les acteurs établis recherchent l'ampleur de plateforme englobant les modalités allogéniques, d'édition génique et iPSC pour diversifier le risque et séduire les payeurs mondiaux. Les centres d'excellence de fabrication émergent comme cibles d'acquisition stratégiques car ils livrent une capacité immédiate et une bonne volonté réglementaire. Cette agglomération graduelle devrait élever les standards de service globaux tout en continuant à laisser de la place aux innovateurs de niche.
Leaders de l'industrie de la médecine régénérative
-
Smith+Nephew plc
-
Organogenesis Holdings Inc.
-
Baxter International Inc.
-
Medtronic
-
Integra LifeSciences Holdings Corporation
- *Avis de non-responsabilité : les principaux acteurs sont triés sans ordre particulier
Développements récents de l'industrie
- Mai 2025 : L'Autorité des dispositifs médicaux de Malaisie a ouvert une consultation sur les règles des dispositifs d'exportation uniquement, s'alignant avec un ordre d'exemption plus large. Le projet, s'il est mis en œuvre, devrait simplifier les expéditions transfrontalières et pourrait indirectement raccourcir les délais de livraison pour les dispositifs auxiliaires de thérapie cellulaire.
- Avril 2025 : Rege Nephro a acquis les actifs Tamibarotène de Syros Pharmaceuticals pour renforcer son programme de maladie polykystique rénale autosomique dominante, selon les communiqués de presse de l'entreprise. La transaction a également transféré les contrats de fabrication, suggérant que la propriété de la chaîne d'approvisionnement devient rapidement un actif stratégique dans les discussions d'évaluation.
- Décembre 2024 : Affimed a reçu la désignation FDA RMAT pour sa thérapie combinée d'acimtamig et AlloNK d'Artiva Biotherapeutics pour traiter le lymphome de Hodgkin en rechute/réfractaire, basée sur des données d'efficacité précoces montrant un taux de réponse globale de 83,3 %.
- Septembre 2024 : Poseida Therapeutics, Inc. a obtenu la désignation de thérapie avancée de médecine régénérative (RMAT) de la Food and Drug Administration (FDA) des États-Unis pour P-BCMA-ALLO1. Cette thérapie expérimentale, basée sur les cellules T mémoire de cellules souches (TSCM), est un traitement CAR-T allogénique en essais cliniques de Phase 1/1b, ciblant les patients atteints de myélome multiple en rechute ou réfractaire.
Portée du rapport mondial sur le marché de la médecine régénérative
Selon la portée du rapport industriel, les médicaments de médecine régénérative sont utilisés pour réparer, remplacer et régénérer les tissus et organes affectés par les blessures, les maladies ou le processus de vieillissement naturel. Ces médicaments restaurent la fonctionnalité des cellules et tissus et sont utilisés dans plusieurs troubles dégénératifs, tels que la dermatologie, les maladies neurodégénératives, cardiovasculaires et l'orthopédie.
Le marché de la médecine régénérative est segmenté par type de produit, origine des cellules, source (type de cellules souches), application, utilisateur final et géographie. Par type de produit, le marché est segmenté en thérapies cellulaires, thérapies géniques, produits d'ingénierie tissulaire, biomatériaux et produits régénératifs acellulaires (PRP, ECM). Par origine des cellules, le marché est segmenté en autologue, allogénique et xénogénique. Par source (type de cellules souches), le marché est segmenté en cellules souches adultes, cellules souches pluripotentes induites, cellules souches embryonnaires et cellules souches hématopoïétiques. Par application, le marché est segmenté en orthopédie et troubles musculo-squelettiques, dermatologie et soins des plaies, cardiovasculaire, neurologie, oncologie, ophtalmologie et autres. Les autres applications incluent l'endocrinologie, le rénal, etc. Par utilisateur final, le marché est segmenté en hôpitaux et centres chirurgicaux, cliniques spécialisées, instituts académiques et de recherche, et biobanques et banques cellulaires. Par géographie, le marché est segmenté en Amérique du Nord, Europe, Asie-Pacifique, Moyen-Orient et Afrique, et Amérique du Sud. Le rapport de marché couvre également les tailles de marché estimées et les tendances pour 17 pays différents à travers les principales régions, globalement. Le rapport de marché offre la valeur (en milliards USD) pour les segments ci-dessus.
| Thérapies cellulaires |
| Thérapies géniques |
| Produits d'ingénierie tissulaire |
| Biomatériaux |
| Produits régénératifs acellulaires |
| Autologue |
| Allogénique |
| Xénogénique |
| Cellules souches adultes |
| Cellules souches pluripotentes induites |
| Cellules souches embryonnaires |
| Cellules souches hématopoïétiques |
| Orthopédie et troubles musculo-squelettiques |
| Dermatologie et soins des plaies |
| Cardiovasculaire |
| Neurologie |
| Oncologie |
| Ophtalmologie |
| Autres |
| Hôpitaux et centres chirurgicaux |
| Cliniques spécialisées |
| Instituts académiques et de recherche |
| Biobanques et banques cellulaires |
| Amérique du Nord | États-Unis |
| Canada | |
| Mexique | |
| Europe | Allemagne |
| Royaume-Uni | |
| France | |
| Italie | |
| Espagne | |
| Reste de l'Europe | |
| Asie-Pacifique | Chine |
| Japon | |
| Inde | |
| Australie | |
| Corée du Sud | |
| Reste de l'Asie-Pacifique | |
| Moyen-Orient et Afrique | CCG |
| Afrique du Sud | |
| Reste du Moyen-Orient et de l'Afrique | |
| Amérique du Sud | Brésil |
| Argentine | |
| Reste de l'Amérique du Sud |
| Par type de produit | Thérapies cellulaires | |
| Thérapies géniques | ||
| Produits d'ingénierie tissulaire | ||
| Biomatériaux | ||
| Produits régénératifs acellulaires | ||
| Par origine des cellules | Autologue | |
| Allogénique | ||
| Xénogénique | ||
| Par source | Cellules souches adultes | |
| Cellules souches pluripotentes induites | ||
| Cellules souches embryonnaires | ||
| Cellules souches hématopoïétiques | ||
| Par application | Orthopédie et troubles musculo-squelettiques | |
| Dermatologie et soins des plaies | ||
| Cardiovasculaire | ||
| Neurologie | ||
| Oncologie | ||
| Ophtalmologie | ||
| Autres | ||
| Par utilisateur final | Hôpitaux et centres chirurgicaux | |
| Cliniques spécialisées | ||
| Instituts académiques et de recherche | ||
| Biobanques et banques cellulaires | ||
| Par géographie | Amérique du Nord | États-Unis |
| Canada | ||
| Mexique | ||
| Europe | Allemagne | |
| Royaume-Uni | ||
| France | ||
| Italie | ||
| Espagne | ||
| Reste de l'Europe | ||
| Asie-Pacifique | Chine | |
| Japon | ||
| Inde | ||
| Australie | ||
| Corée du Sud | ||
| Reste de l'Asie-Pacifique | ||
| Moyen-Orient et Afrique | CCG | |
| Afrique du Sud | ||
| Reste du Moyen-Orient et de l'Afrique | ||
| Amérique du Sud | Brésil | |
| Argentine | ||
| Reste de l'Amérique du Sud | ||
Questions clés répondues dans le rapport
Quelle est la taille projetée du marché de la médecine régénérative d'ici 2030 ?
Le secteur devrait atteindre environ 88,85 milliards USD d'ici 2030, reflétant une croissance soutenue à deux chiffres stimulée par les thérapies géniques et cellulaires.
Quel segment affiche le TCAC le plus rapide entre 2025 et 2030 ?
Les thérapies géniques devraient afficher environ 25,39 % de TCAC, dépassant les segments de thérapie cellulaire et d'ingénierie tissulaire.
Quelle est la taille de la part de marché des thérapies cellulaires allogéniques en 2024 ?
Les produits allogéniques détiennent environ 55,14 % de part de marché, bénéficiant des efficacités de fabrication standardisée et prête à l'emploi.
Quelle région connaît la croissance la plus rapide ?
L'Asie-Pacifique mène avec un TCAC estimé de 16,22 %, propulsée par les réglementations progressives du Japon et l'activité d'essais cliniques de la Chine.
Dernière mise à jour de la page le:



