Taille et part du marché des solutions d'évidence du monde réel
Analyse du marché des solutions d'évidence du monde réel par Mordor Intelligence
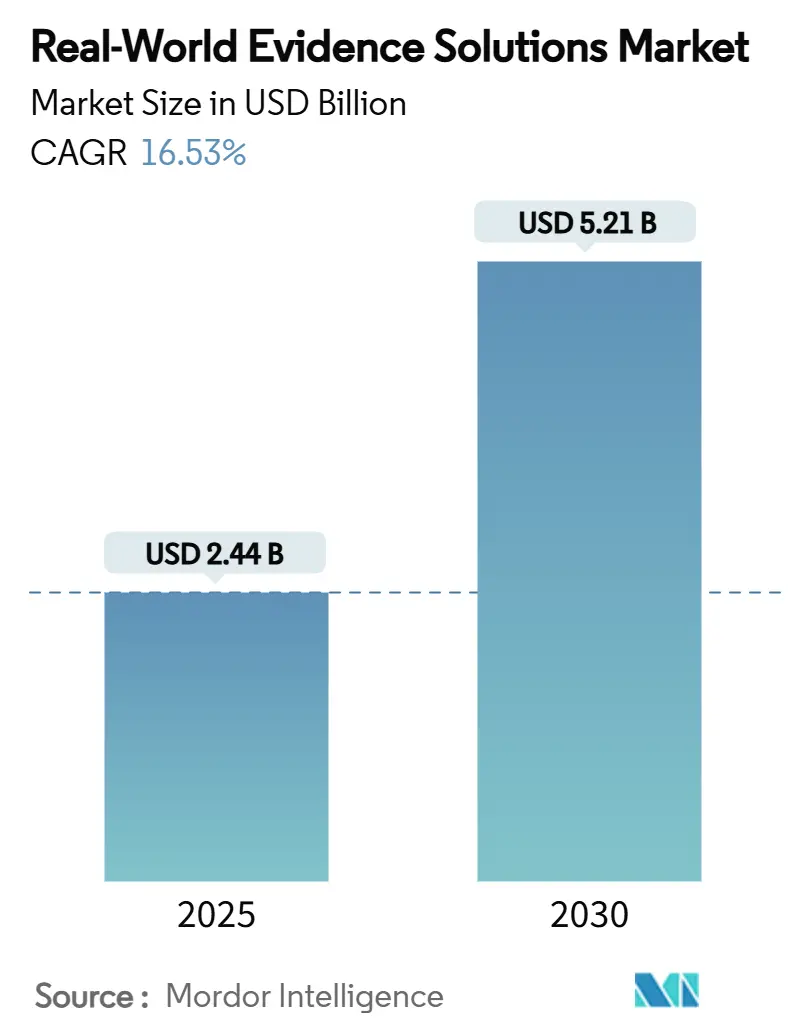
La taille du marché des solutions d'évidence du monde réel s'élève à 2,44 milliards USD en 2025 et devrait atteindre 5,21 milliards USD d'ici 2030, progressant à un TCAC vigoureux de 16,53 %. Les ensembles de données cliniques, génomiques et administratives numérisées s'étendent à des taux à deux chiffres dans les principaux systèmes de santé, tandis que les régulateurs aux États-Unis, dans l'Union européenne et au Japon continuent de publier des orientations sur la façon dont les promoteurs peuvent incorporer des données non traditionnelles dans les soumissions, réduisant les délais de développement sans sacrifier la rigueur scientifique[1]Food and Drug Administration, "Framework for Real-World Evidence Program," fda.gov. Les budgets biopharma s'orientent vers de grandes cohortes de patients organisées qui réduisent les risques de recrutement, et les payeurs lient les prix premium aux résultats, forçant les fabricants à adopter des analyses qui valident l'efficacité du monde réel au lancement. Les afflux de capital-risque favorisent les entreprises de plateforme avec des architectures cloud évolutives, leur donnant le capital pour acquérir des ensembles de données de niche et consolider leurs parts. En même temps, les techniques de préservation de la confidentialité telles que la tokenisation et l'apprentissage fédéré deviennent des prérequis d'approvisionnement, orientant les contrats vers les fournisseurs ayant une sécurité et une gouvernance prouvées.
Points clés du rapport
- Par composant, les services ont dominé avec 55,0 % de la part du marché des solutions d'évidence du monde réel en 2024, tandis que les plateformes logicielles et d'analyse progressent à un TCAC de 18,0 % jusqu'en 2030.
- Par mode de déploiement, le cloud un capturé 65 % de la taille du marché des solutions d'évidence du monde réel en 2024, tandis que l'hybride progresse à un TCAC de 21,0 % jusqu'en 2030.
- Par domaine thérapeutique, l'oncologie un commandé 35 % de la part du marché des solutions d'évidence du monde réel en 2024 ; la neurologie progresse à un TCAC de 19 % jusqu'en 2030.
- Par application, le développement et les approbations de médicaments ont représenté 40 % de la taille du marché des solutions d'évidence du monde réel en 2024, tandis que la prise de décision réglementaire et le remboursement croissent à un TCAC de 18 %.
- Par utilisateur final, les entreprises pharmaceutiques et de dispositifs médicaux ont détenu 50,0 % du marché des solutions d'évidence du monde réel en 2024. Alors que le segment des prestataires de soins de santé et réseaux payeur-prestataire devrait croître au TCAC le plus rapide de 17,0 %
- Par région, l'Amérique du Nord un dominé avec 41,3 % de la part du marché des solutions d'évidence du monde réel en 2024. Alors que l'Asie-Pacifique devrait croître au TCAC le plus rapide de 17,8 %.
Tendances et insights du marché mondial des solutions d'évidence du monde réel
Analyse d'impact des moteurs
| Moteur | (~) % Impact sur les prévisions TCAC | Pertinence géographique | Calendrier d'impact |
|---|---|---|---|
| Acceptation réglementaire dans les principales agences | +3% | Amérique du Nord, Europe, Japon | Moyen terme (2-4 ans) |
| Expansion des données de santé numérisées | +4% | Mondial | Long terme (≥ 4 ans) |
| Utilisation pharmaceutique des bras de contrôle externes | +2% | Amérique du Nord, Asie-Pacifique | Moyen terme (2-4 ans) |
| Modèles de remboursement basés sur la valeur | +3% | Amérique du Nord, Europe | Long terme (≥ 4 ans) |
| Intelligence artificielle et plateformes d'analyse avancées qui arrivent à maturité | +2% | Mondial | Moyen terme (2-4 ans) |
| Collaborations stratégiques entre CRO, fournisseurs technologiques et systèmes de santé | +2% | Amérique du Nord, Europe | Court terme (≤ 2 ans) |
| Source: Mordor Intelligence | |||
Acceptation réglementaire croissante dans les principales agences
Le cadre d'évidence du monde réel de la FDA américaine et les programmes pilotes correspondants ont formalisé les voies pour soumettre des cohortes contrôlées extérieurement construites à partir de réclamations et d'enregistrements de DSE. L'Agence européenne des médicaments reflète cette tendance sous son réseau d'analyse de données et d'interrogation du monde réel, publiant des avis de qualification positifs pour plusieurs propositions de bras synthétiques. La PMDA du Japon un suivi avec ses orientations 2024 sur les tests de fiabilité des données du monde réel[2]Pharmaceuticals and Medical Devices Agency, "Guidance on Reliability of RWD," pmda.go.jp. Les promoteurs intègrent maintenant des critères d'évaluation observationnels dès la phase II, réduisant l'incertitude dans les essais pivots. La traçabilité transparente des données est ainsi passée d'une réflexion après coup de conformité à un différenciateur de première ligne, récompensant les fournisseurs qui livrent des pipelines prêts pour l'audit et accélérant les signatures de contrats parmi les équipes d'approvisionnement biopharma averses au risque.
Expansion rapide des données de santé numérisées
Les niveaux d'adoption des dossiers de santé électroniques ont dépassé 89,0 % parmi les hôpitaux américains de soins aigus non fédéraux en 2024, ajoutant des pétaoctets de données structurées au marché des solutions d'évidence du monde réel. Les objets connectés génèrent des flux physiologiques continus, tandis que les sorties de séquençage de nouvelle génération enrichissent les registres de maladies avec des signatures moléculaires. Les liaisons multi-modales permettent aux chercheurs de combiner l'imagerie, les réclamations de pharmacie et les indicateurs de déterminants sociaux, découvrant des phénotypes invisibles aux essais traditionnels. Pourtant, des statuts de confidentialité plus stricts tels que le RGPD de l'UE et le CPRA de Californie renforcent la surveillance. Les fournisseurs de tokenisation qui convertissent les identifiants en hachages non réversibles sont devenus des partenaires centraux, et les réseaux d'apprentissage fédéré qui déplacent le code vers les données plutôt que d'agréger des fichiers bruts permettent une collaboration transfrontalière sans violer les règles de résidence. Les fournisseurs capables d'harmoniser des taxonomies disparates sous des modèles de données communes raccourcissent le démarrage d'étude de mois, gagnant un avantage mesurable.
Les entreprises pharmaceutiques exploitent l'évidence du monde réel pour réduire les délais et coûts de R&D
Les bras de contrôle externes construits à partir de registres d'oncologie existants ont réduit les délais de recrutement jusqu'à 25 semaines dans plusieurs dépôts 2024, selon les mémos de révision publics de la FDA. Les cohortes synthétiques réduisent les coûts de surveillance par patient, libérant du capital pour financer des expansions d'indication supplémentaires. Les outils de recherche de cohorte alimentés par l'IA-commercialisés par des entreprises telles que ConcertAI-mappent les critères d'inclusion contre des dizaines de millions d'enregistrements longitudinaux, réduisant drastiquement les taux d'échec de criblage. Les suivis observationnels étendent la valeur du cycle de vie des actifs, soutenant les extensions d'étiquette et renforçant les positions de formulaire. Les rapports financiers des 20 premières pharmas indiquent un coût des marchandises vendues stable mais une augmentation à deux chiffres des budgets de génération d'évidence, validant la trajectoire de croissance du marché.
Les modèles de remboursement basés sur la valeur stimulent l'évidence orientée résultats
Les assureurs commerciaux américains ont exécuté plus de 90 accords basés sur les résultats en 2024, liant souvent les remises sur médicaments de spécialité aux métriques de réponse du monde réel divulguées via des tableaux de bord partagés. Les systèmes multi-payeurs européens ont répliqué ce modèle alors que les agences en Allemagne et en France ont ajouté des clauses de remboursement conditionnel dépendant de l'efficacité du monde réel. Les fournisseurs qui intègrent des métriques économiques et cliniques dans des portails unifiés permettent aux payeurs de visualiser les ratios coût-efficacité incrémentaux (ICER) par sous-population, soutenant des cycles de négociation plus rapides. Les clients de plan de santé demandent maintenant des clauses contractuelles mandatant des actualisations continues de données, transformant les engagements de service épisodiques en abonnements récurrents qui stabilisent les revenus des fournisseurs.
Analyse d'impact des contraintes
| Contrainte | (~) % Impact sur les prévisions TCAC | Pertinence géographique | Calendrier d'impact |
|---|---|---|---|
| Obstacles de confidentialité des données et d'interopérabilité | -2% | Mondial | Moyen terme (2-4 ans) |
| Fragmentation réglementaire dans les études transfrontalières | -1% | Europe, Asie-Pacifique | Court terme (≤ 2 ans) |
| Coûts élevés d'acquisition et de licence pour les ensembles de données longitudinales organisées | -1% | Mondial | Court terme (≤ 2 ans) |
| Scepticisme des parties prenantes concernant la rigueur méthodologique et les biais dans les études d'évidence du monde réel | -1% | Mondial | Moyen terme (2-4 ans) |
| Source: Mordor Intelligence | |||
L'IA et les plateformes d'analyse avancées arrivent à maturité pour extraire des insights actionnables
Les modèles de traitement du langage naturel basés sur des transformateurs ont atteint des scores F1 supérieurs à 0,90 sur l'extraction de critères d'évaluation d'oncologie à partir de rapports de pathologie non structurés dans les études de validation 2024, réduisant les coûts d'abstraction manuelle de plus de 60 %. Les clusters DGX H100 de NVIDIA, déployés via le portefeuille Applied AI d'IQVIA, réduisent les temps d'entraînement de modèles de jours à heures, permettant une itération rapide sur les modèles prédictifs[3]IQVIA, "IQVIA and NVIDIA Announce Strategic Collaboration," iqvia.com. Les techniques de génération de données synthétiques adressent le déséquilibre de classe et les contraintes de confidentialité, élargissant les ensembles d'entraînement sans exposer des enregistrements identifiables. De tels gains de productivité justifient des frais de licence premium, poussant la croissance des plateformes IA plus vite que l'ensemble du marché des solutions d'évidence du monde réel. L'inférence accélérée par GPU réduit également la latence de requête, un critère d'achat clé pour les équipes d'affaires médicales effectuant des recherches d'évidence à la demande pendant les négociations de payeurs.
Les défis de confidentialité des données et d'interopérabilité entravent l'intégration transparente
Les mises à jour HIPAA, les lois de confidentialité des consommateurs au niveau de l'État et les décisions d'adéquation internationales divergentes compliquent la mise en commun d'ensembles de données transfrontalières. Par exemple, les hôtes de données de santé français doivent détenir une certification HDS locale, créant des frictions pour les fournisseurs américains cherchant à analyser les réclamations européennes à grande échelle. Les fournisseurs de tokenisation résolvent une partie du puzzle mais introduisent de nouveaux compromis : l'erreur de liaison ou les champs démographiques limités peuvent éroder le pouvoir analytique. Les cadres d'apprentissage fédéré promettent la conformité mais nécessitent un investissement DevOps lourd ; en conséquence, les petites entreprises d'analyse s'associent de plus en plus avec des spécialistes d'infrastructure plutôt que de construire des piles propriétaires. Ces dynamiques consolident les parts parmi les opérateurs historiques qui associent les certifications de sécurité avec des architectures haute disponibilité.
Analyse de segment
Par composant : les services maintiennent l'échelle, les logiciels accélèrent
Les services ont généré 55,0 % du marché des solutions d'évidence du monde réel en 2024, reflétant la dépendance des promoteurs envers les épidémiologistes externes, les consultants HEOR et les biostatisticiens pour la conception d'étude, la curation de données et la stratégie réglementaire. Les grands fournisseurs de services tels qu'IQVIA, ICON et Syneos Health regroupent des pipelines de tokenisation qui connectent les réclamations de pharmacie avec les flux DSE, étendant le suivi longitudinal et augmentant les coûts de changement de client. Les cadres d'externalisation pluriannuels assurent une visibilité de revenus prévisible, amortissant les oscillations macro-économiques. Les équipes de services conseillent également sur les évaluations d'impact de confidentialité requises sous le RGPD, expédiant les approbations d'études européennes.
Les logiciels, bien qu'actuellement plus petits, évoluent à un TCAC de 18,0 % alors que les fournisseurs de plateformes commercialisent des architectures cloud natives. Les modèles d'abonnement remplacent les frais de projet volatils, améliorant le flux de trésorerie des fournisseurs. Les modules IA intégrés dans les plateformes principales extraient automatiquement les critères d'évaluation des rapports de radiologie et génomiques, éliminant les goulots d'étranglement de codage manuel. La suite SaaS de ConcertAI, par exemple, ingère des notes de pathologie non structurées, classifie la stadification tumorale avec des modèles de transformateur et retourne des formats de données structurées prêts pour l'analyse. L'adoption de plateforme déclenche souvent des demandes de services de suivi pour des analyses sur mesure, créant une boucle de croissance symbiotique entre les unités logicielles et de conseil.
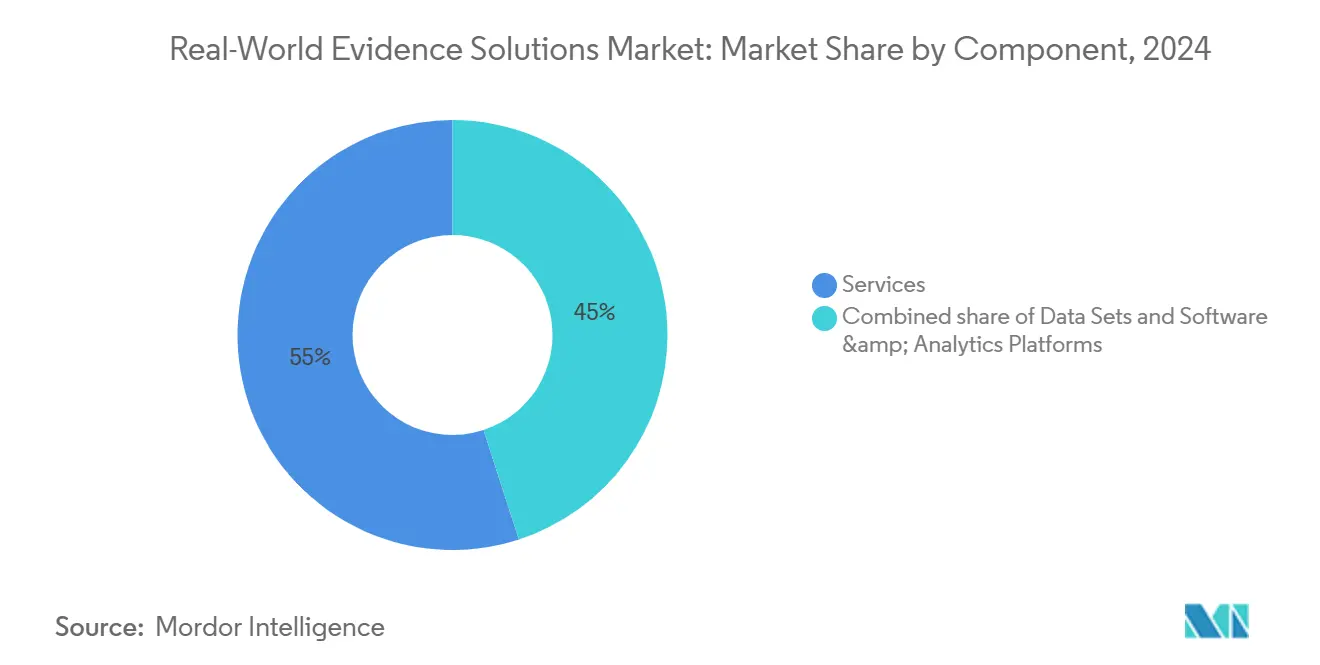
Note: Parts de segment de tous les segments individuels disponibles à l'achat du rapport
Par mode de déploiement : le cloud domine, l'hybride gagne en élan
Le cloud un capturé 65,0 % de la taille du marché des solutions d'évidence du monde réel en 2024, bénéficiant du calcul élastique et des prix à l'utilisation. Les listes AWS Marketplace pour l'analyse d'évidence du monde réel ont augmenté de plus de 40 % d'une année à l'autre, indiquant une forte préférence d'acheteur pour les fournisseurs pré-approuvés qui satisfont les modèles de sécurité de responsabilité partagée. Les migrations précoces impliquent des cohortes désidentifiées, avec des informations de santé protégées ne se déplaçant qu'après que les cadres de cryptage et les politiques de gestion de clés arrivent à maturité. Les systèmes de santé américains exploitent les rafales GPU de cloud public pour entraîner des modèles NLP pendant la demande de pointe, évitant les achats de serveurs à forte intensité de capital.
Le déploiement hybride progresse à un TCAC de 21,0 % alors que les centres médicaux académiques et les réseaux de recherche financés publiquement équilibrent la souveraineté des données sur site avec l'analyse évolutive. Les nœuds Cloud@Customer d'Oracle, par exemple, se situent derrière les pare-feu hospitaliers mais se fédèrent avec des régions publiques pour des tâches de calcul haute intensité, satisfaisant les orientations de résidence du Comité européen de protection des données. Les fournisseurs qui livrent l'orchestration de charge de travail basée sur les politiques-routant automatiquement les requêtes sensibles PHI vers des clusters privés-adressent un obstacle d'adoption critique et déplacent les installations on-prem héritées. Les sites à forte intensité de capital étendent la durée de vie des racks de serveurs existants tout en accédant aux GPU cloud pour les charges de travail en rafale, améliorant le coût total de possession.
Par domaine thérapeutique : l'oncologie conserve l'échelle, la neurologie accélère
L'oncologie un commandé 35,0 % de la part du marché des solutions d'évidence du monde réel en 2024. Les ensembles de données de biomarqueurs riches, le profilage génomique de routine et la haute vélocité de lancement de médicaments rendent les voies du cancer idéales pour la génération d'évidence. Les métriques de réponse tumorale du monde réel dérivées de l'imagerie et des fichiers de pathologie soutiennent les soumissions d'approbation accélérée et les extensions d'étiquette. Le registre d'hématologie conjoint de NeoGenomics et ConcertAI, couvrant 370 000 patients, illustre comment les essais de pathologie liés et les données DSE longitudinales raccourcissent le criblage d'éligibilité[4]NeoGenomics, "NeoGenomics and ConcertAI Launch Hematology Données Suite," neogenomics.com. La prolifération des produits d'oncologie de précision assure une demande soutenue pour des cohortes mises à jour, cimentant l'avantage d'échelle de l'oncologie.
La neurologie est le segment à croissance la plus rapide, projeté à 19 % de TCAC. Les biomarqueurs numériques capturés par des objets connectés d'analyse de démarche et des applications de modèles de parole permettent une surveillance continue dans les troubles neurodégénératifs, élargissant les entrées de données du monde réel. L'Association Alzheimer note une augmentation des études observationnelles activées par des dispositifs qui réduisent le fardeau des soignants et améliorent la détection de signal. Les analyses multi-conditions qui combinent des données cognitives, de santé mentale et cardiovasculaires améliorent les insights des payeurs sur les moteurs de coût liés à la comorbidité, encourageant un remboursement plus large des ensembles de données de neurologie. Les fournisseurs élargissant les modules de neurologie se positionnent pour la prochaine vague de lancements de thérapie de précision.
Par application : le développement de médicaments mène, l'évidence de remboursement s'élève
Le développement et les approbations de médicaments ont détenu 40,0 % de la taille du marché des solutions d'évidence du monde réel en 2024. Les bras de contrôle externes dérivés de registres établis rationalisent les essais pivots et réduisent le risque d'attrition. La boîte à outils de démarrage améliorée par IA d'ICON projette la disponibilité des patients à travers les sites mondiaux, réduisant les taux d'échec de criblage et accélérant les jalons de premier patient. L'intégration d'évidence du monde réel dans les phases de découverte précoce aide les équipes biopharma à stratifier les populations de patients, optimisant l'allocation de capital.
La prise de décision réglementaire et le remboursement, croissant à un TCAC de 18,0 %, sont alimentés par les mandats de payeur pour la preuve de résultats au lancement. Le Comité fédéral conjoint (G-BA) de l'Allemagne demande maintenant des données observationnelles pour les évaluations de bénéfice de médicaments orphelins, forçant les promoteurs à collecter des mesures d'efficacité post-lancement. Les fournisseurs capables de fusionner des résultats cliniques, économiques et rapportés par les patients en soumissions uniques réduisent le fardeau des promoteurs et sécurisent des contrats premium. La rigueur méthodologique-telle que l'ajustement pour le biais de temps immortel-est devenue une exigence de base, poussant les entreprises d'analyse à certifier leurs processus sous ISO/IEC 27001 et des cadres similaires.
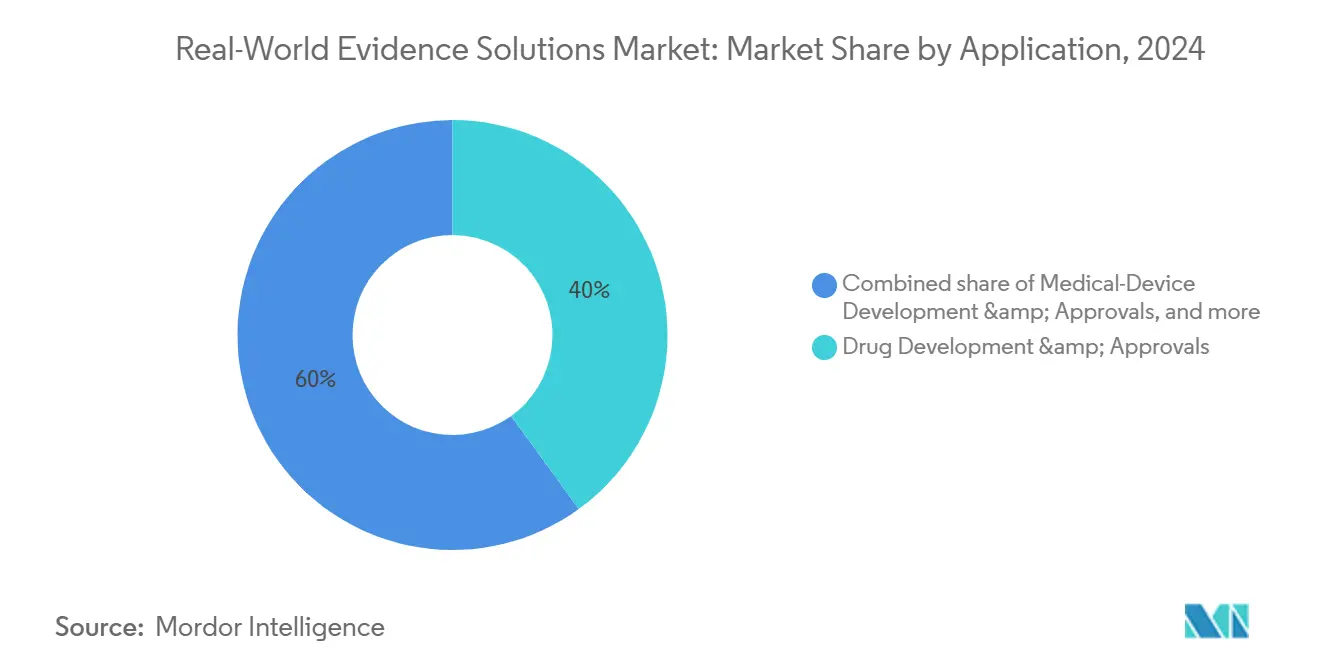
Note: Parts de segment de tous les segments individuels disponibles à l'achat du rapport
Par utilisateur final : les entreprises de sciences de la vie dominent, les réseaux de prestataires dépassent
Les entreprises pharmaceutiques et de dispositifs médicaux représentent 50,0 % du marché des solutions d'évidence du monde réel, alors que la pression pour démontrer la valeur post-lancement augmente. L'adoption par Pfizer de tableaux de bord d'évidence du monde réel à travers les équipes de marques d'oncologie permet une surveillance de sécurité quasi temps réel et une prise de décision d'expansion d'étiquette. Les chaînes d'outils intégrées qui connectent les fonctions de pharmacovigilance et d'accès au marché réduisent les retards liés aux silos, renforçant les positions concurrentielles.
Les prestataires de soins de santé et les réseaux payeur-prestataire sont la cohorte d'utilisateurs finaux à croissance la plus rapide à 17,0 % de TCAC. Les réseaux de livraison intégrés américains intègrent les sorties d'évidence du monde réel dans les projets de refonte de voies de soins, ciblant la variation clinique injustifiée. Le DSE IntelliCare d'InterSystems, lancé en 2025, vient pré-intégré avec des API d'analyse qui font ressortir des insights de santé de population aux cliniciens de première ligne, minimisant la dépendance aux analystes de back-office. Les fournisseurs mettant l'accent sur des UI intuitives et des budgets de formation minimaux gagnent de la traction, alors que les contraintes de temps des cliniciens élèvent l'utilisabilité à un facteur d'achat critique.
Analyse géographique
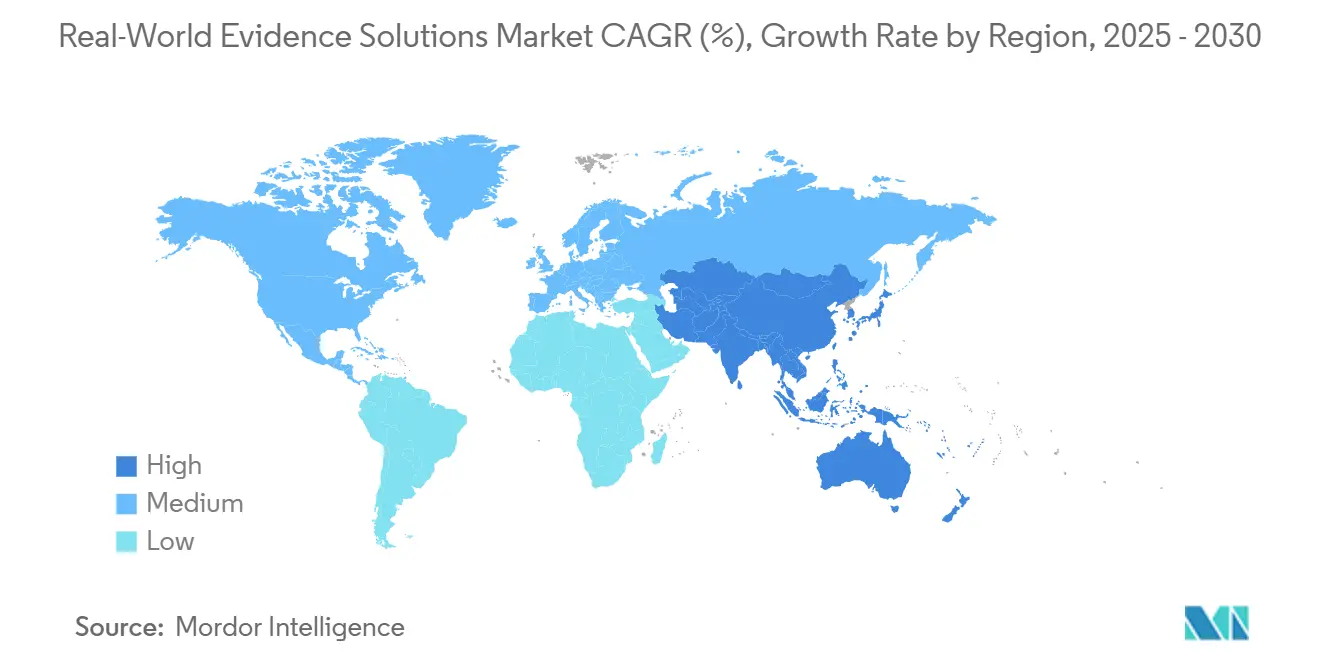
L'Amérique du Nord un mené le marché des solutions d'évidence du monde réel en 2024 avec une part de 41,3 %. Les programmes pilotes d'évidence du monde réel de la FDA fournissent des orientations procédurales claires, réduisant le risque d'évidence pour les promoteurs, tandis que les assureurs américains intègrent des métriques de résultats dans les contrats de médicaments à coût élevé, stimulant indirectement la demande pour des analyses conformes. Les marchés de capitaux récompensent les modèles commerciaux centrés sur les données ; les évaluations pour les fournisseurs d'évidence du monde réel cotés sur Nasdaq se négocient à des multiples de revenus au-dessus des pairs CRO cliniques, permettant un réinvestissement agressif dans les feuilles de route produits.
L'Europe s'est classée deuxième, soutenue par le prochain règlement sur l'espace européen des données de santé, qui mandate des cadres techniques et légaux pour la réutilisation de données transfrontalières. Les architectures conformes au RGPD et l'accréditation HDS facilitent l'intégration des fournisseurs avec les services de santé nationaux. Les environnements multi-payeurs favorisent les opportunités de niche : le système ATU de la France et la voie AMNOG de l'Allemagne acceptent de plus en plus l'évidence du monde réel pour confirmer le bénéfice ajouté, ouvrant des affaires pour des ensembles de données spécialisés en oncologie et maladies rares.
L'Asie-Pacifique est la région à croissance la plus rapide, projetée à un TCAC de 17,8 %. L'Administration nationale des produits médicaux de Chine un émis des orientations 2024 sur l'acceptation de données du monde réel étrangères pour les demandes de nouveaux médicaments supplémentaires, abaissant les barrières de soumission pour les promoteurs multinationaux. Le MHLW du Japon finance des pilotes de biomarqueurs numériques, élargissant les sources pour les études de neurologie. Le système My Health Record d'Australie dépasse 95 % de couverture de population, créant des ensembles de données longitudinales robustes qui attirent les promoteurs d'outre-mer. Les partenariats public-privé transfrontaliers standardisent les dictionnaires de données, permettant la mise en commun de cohortes multi-pays et améliorant la généralisabilité d'algorithmes pour les modèles IA mondiaux.
Paysage concurrentiel
L'industrie des solutions d'évidence du monde réel reste modérément concentrée. Les cinq premiers fournisseurs commandent collectivement un peu plus de 60 % des revenus mondiaux, exploitant des ensembles de données longitudinales propriétaires qui couvrent les prescriptions, diagnostics et réclamations de procédures. IQVIA associe ces actifs avec des modules Applied AI et une modélisation accélérée par GPU, livrant des analyses clés en main qui s'intègrent directement dans les pipelines de promoteurs. Des offres intégrées similaires d'Optum Life Sciences et Veradigm ancrent la dépendance client en couvrant l'ingestion de données, la tokenisation, l'analyse et le support de soumission réglementaire.
Les alliances stratégiques s'intensifient en réponse aux charges de travail pilotées par l'IA. Le partenariat 2025 d'IQVIA avec NVIDIA aligne les ensembles de données de santé organisées avec l'infrastructure GPU, réduisant les temps d'entraînement de modèles et débloquant de nouveaux cas d'usage dans l'analyse multi-modale. Les pipelines d'acquisition priorisent les ensembles de données de niche difficiles à répliquer-référentiels d'imagerie, bibliothèques génomiques et portails de communautés de patients-permettant aux opérateurs historiques de se différencier sans de longs cycles de collecte de données. Les primes d'évaluation s'attachent aux cibles détenant des cohortes de maladies rares avec des cadres de consentement patient solides.
La gouvernance transparente et l'auditabilité sont maintenant des différenciateurs centraux. Les fournisseurs offrant une traçabilité de données documentée de l'ingestion à travers la transformation algorithmique jusqu'à la sortie commandent des prix premium, alors que les promoteurs cherchent à dérisquer les audits réglementaires. Les entreprises centrées sur la technologie élargissent donc leurs équipes de conseil : Oracle Health, par exemple, un créé une unité de science réglementaire qui guide les clients sur la méthodologie, brouillant la ligne entre fournisseur de logiciel et partenaire de conseil. Cette convergence élève la barre concurrentielle et peut accélérer la consolidation future.
Leaders de l'industrie des solutions d'évidence du monde réel
-
IQVIA Inc.
-
Optum Inc.
-
Oracle Health
-
ICON plc
-
IBM
- *Avis de non-responsabilité : les principaux acteurs sont triés sans ordre particulier


Développements récents de l'industrie
- Février 2025 : IQVIA et NVIDIA ont conclu une collaboration stratégique pour automatiser les flux de travail de santé complexes avec l'IA de niveau santé, alignant l'infrastructure DGX avec des ensembles de données organisées.
- Janvier 2025 : Helix un élargi son réseau de recherche en ajoutant trois systèmes de santé et un lié sa plateforme à la carte de santé de Komodo Health, enrichissant les liaisons génomiques-réclamations.
- Janvier 2025 : Picnic Health s'est associé à Orsini pour construire des registres améliorés par l'IA pour les maladies rares, fusionnant les enregistrements EMR avec les résultats rapportés par les patients PicnicHealth.
- Décembre 2024 : ConcertAI et NeoGenomics ont lancé une solution SaaS IA pour la recherche en hématologie couvrant 370 000 vies de patients.
- Décembre 2024 : La FDA un émis un projet d'orientation sur les bonnes pratiques cliniques pour les essais incorporant des éléments décentralisés et des données du monde réel
- Mars 2025 : InterSystems un dévoilé IntelliCare, un DSE alimenté par l'IA visant à stimuler l'efficacité clinique et administrative
- Janvier 2025 : ICON plc un amélioré sa boîte à outils IA pour accélérer le démarrage d'étude et les prévisions de ressources
- Janvier 2025 : Charles River Laboratories un étendu son écosystème Apollo, fournissant des plateformes cloud qui capturent des données précliniques alimentant les pipelines d'évidence du monde réel en aval
Portée du rapport sur le marché mondial des solutions d'évidence du monde réel
Selon la portée du rapport, l'évidence du monde réel (RWE) est l'évidence clinique sur l'utilisation et les bénéfices potentiels ou les risques d'un produit médical dérivée de l'analyse de données du monde réel (RWD).
Le marché des solutions d'évidence du monde réel est segmenté en composants, domaines thérapeutiques, applications, utilisateurs finaux et géographie. Par composant, le marché est segmenté en services et ensembles de données (données de cadre clinique, données de réclamations, données de pharmacie, données alimentées par les patients, et autres composants (registres de maladies et dossiers de santé électroniques). Par domaine thérapeutique, le marché est segmenté en oncologie, cardiologie, diabète, neurologie, psychiatrie, et autres domaines thérapeutiques (orthopédie et respiratoire). Par application, le marché est segmenté en développement et approbations de médicaments, développement et approbations de dispositifs médicaux, études de pharmacovigilance, et prise de décision réglementaire et remboursement/couverture. Par utilisateur final, le marché est segmenté en entreprises pharmaceutiques et de dispositifs médicaux, organisations de recherche clinique, et prestataires de soins de santé. Par géographie, le marché est segmenté en Amérique du Nord, Europe, Asie-Pacifique, Moyen-Orient et Afrique, et Amérique du Sud.
Le rapport de marché couvre également les tailles de marché estimées et les tendances pour 17 pays à travers les principales régions mondiales. Le rapport offre la valeur (USD) pour les segments ci-dessus.
| Services | |
| Ensembles de données | Données de cadre clinique |
| Données de réclamations et de facturation | |
| Données de distribution de pharmacie | |
| Données alimentées par les patients et PRO | |
| Autres composants | |
| Plateformes logicielles et d'analyse |
| Basé sur le cloud |
| Sur site |
| Hybride |
| Oncologie |
| Cardiologie |
| Diabète |
| Neurologie |
| Psychiatrie |
| Immunologie |
| Autres domaines thérapeutiques |
| Développement et approbations de médicaments |
| Développement et approbations de dispositifs médicaux |
| Pharmacovigilance et études de sécurité |
| Prise de décision réglementaire et remboursement |
| Entreprises pharmaceutiques et de dispositifs médicaux |
| Organisations de recherche contractuelle (CRO) |
| Prestataires de soins de santé et réseaux payeur-prestataire |
| Autres utilisateurs finaux |
| Amérique du Nord | États-Unis |
| Canada | |
| Mexique | |
| Europe | Allemagne |
| Royaume-Uni | |
| France | |
| Italie | |
| Espagne | |
| Reste de l'Europe | |
| Asie-Pacifique | Chine |
| Japon | |
| Inde | |
| Corée du Sud | |
| Australie | |
| Reste de l'Asie-Pacifique | |
| Moyen-Orient et Afrique | CCG |
| Afrique du Sud | |
| Reste du Moyen-Orient et de l'Afrique | |
| Amérique du Sud | Brésil |
| Argentine | |
| Reste de l'Amérique du Sud |
| Par composant | Services | |
| Ensembles de données | Données de cadre clinique | |
| Données de réclamations et de facturation | ||
| Données de distribution de pharmacie | ||
| Données alimentées par les patients et PRO | ||
| Autres composants | ||
| Plateformes logicielles et d'analyse | ||
| Par mode de déploiement | Basé sur le cloud | |
| Sur site | ||
| Hybride | ||
| Par domaine thérapeutique | Oncologie | |
| Cardiologie | ||
| Diabète | ||
| Neurologie | ||
| Psychiatrie | ||
| Immunologie | ||
| Autres domaines thérapeutiques | ||
| Par application | Développement et approbations de médicaments | |
| Développement et approbations de dispositifs médicaux | ||
| Pharmacovigilance et études de sécurité | ||
| Prise de décision réglementaire et remboursement | ||
| Par utilisateur final | Entreprises pharmaceutiques et de dispositifs médicaux | |
| Organisations de recherche contractuelle (CRO) | ||
| Prestataires de soins de santé et réseaux payeur-prestataire | ||
| Autres utilisateurs finaux | ||
| Géographie | Amérique du Nord | États-Unis |
| Canada | ||
| Mexique | ||
| Europe | Allemagne | |
| Royaume-Uni | ||
| France | ||
| Italie | ||
| Espagne | ||
| Reste de l'Europe | ||
| Asie-Pacifique | Chine | |
| Japon | ||
| Inde | ||
| Corée du Sud | ||
| Australie | ||
| Reste de l'Asie-Pacifique | ||
| Moyen-Orient et Afrique | CCG | |
| Afrique du Sud | ||
| Reste du Moyen-Orient et de l'Afrique | ||
| Amérique du Sud | Brésil | |
| Argentine | ||
| Reste de l'Amérique du Sud | ||


Questions clés auxquelles répond le rapport
Quelle est la taille actuelle du marché des solutions d'évidence du monde réel ?
Le marché est évalué à 2,44 milliards USD en 2025 et devrait atteindre 5,21 milliards USD d'ici 2030, reflétant un TCAC de 16,53 %.
Quel composant domine le marché des solutions d'évidence du monde réel ?
Les services représentent 55 % du marché, car les promoteurs dépendent encore d'experts externes pour la conception d'étude, la curation de données et la stratégie réglementaire
Pourquoi les ensembles de données d'oncologie commandent-ils la plus grande part ?
L'oncologie détient 35 % du marché des solutions d'évidence du monde réel car les registres riches en biomarqueurs et la haute vélocité de lancement nécessitent une génération d'évidence continue pour soutenir les approbations de thérapie de précision
À quelle vitesse le marché Asie-Pacifique s'étend-il ?
L'Asie-Pacifique est la région à croissance la plus rapide avec un TCAC de 17,8 % jusqu'en 2030, stimulée par la numérisation rapide des dossiers de santé en Chine, au Japon et en Australie et l'acceptation croissante par les régulateurs de données du monde réel étrangères
Quel rôle l'IA joue-t-elle dans la génération d'évidence du monde réel ?
L'IA automatise l'extraction à partir de données non structurées, réduit le temps de révision manuelle et fournit des insights prédictifs, permettant aux fournisseurs de commander des frais de licence premium et de croître plus vite que l'ensemble du marché
Quelles sont les principales barrières à une adoption plus large de l'évidence du monde réel ?
Les réglementations de confidentialité fragmentées et les défis d'interopérabilité ralentissent les études transfrontalières, bien que la tokenisation et l'apprentissage fédéré atténuent les obstacles pour les fournisseurs avec de solides capacités d'ingénierie
Dernière mise à jour de la page le:









