一次性医疗器械再处理市场规模与份额
魔多智能一次性医疗器械再处理市场分析
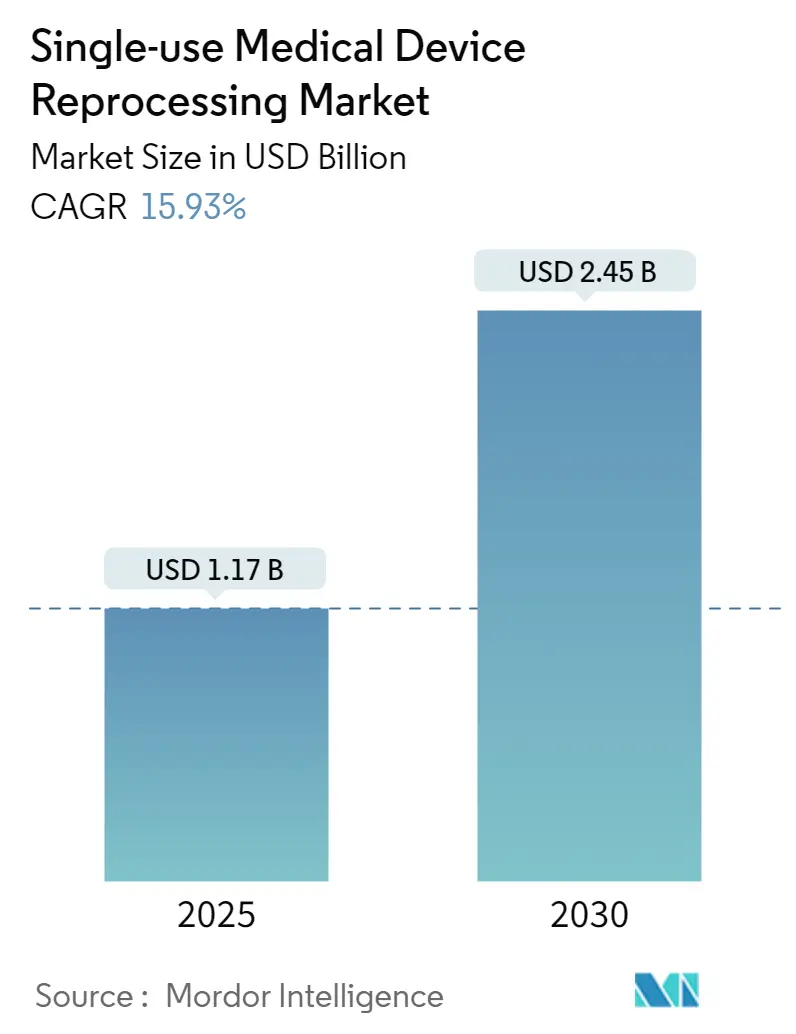
一次性医疗器械再处理市场在2025年价值11.7亿美元,预测到2030年将扩张至24.5亿美元,复合年增长率为15.93%,凸显了全球医疗保健系统对经过验证的成本控制和可持续发展解决方案的强劲需求。美国FDA在2024年5月发布的再制造指导文件带来的监管清晰度,以及对过氧化氢汽化灭菌接受度的提高,减少了合规不确定性,扩大了被认为安全可再处理的器械范围[1]来源:美国食品药品监督管理局,"FDA发布最终指导明确设备'再制造'",fda.gov。在通胀和报销逆风中,医院采购团队将再处理视为保持利润的条目杠杆,特别是在17个国家2024年节省了4.51亿美元的记录之后[2]来源:Dan Vukelich,"地球日新闻:医院和手术中心节省4.51亿美元",amdr.org。可持续发展要求、范围3碳核算以及针对限制性原始设备制造商合同的反垄断执法正在加速设备级采用,而AI驱动的可追溯性平台和自动化灭菌器增强了患者安全信心。
关键报告要点
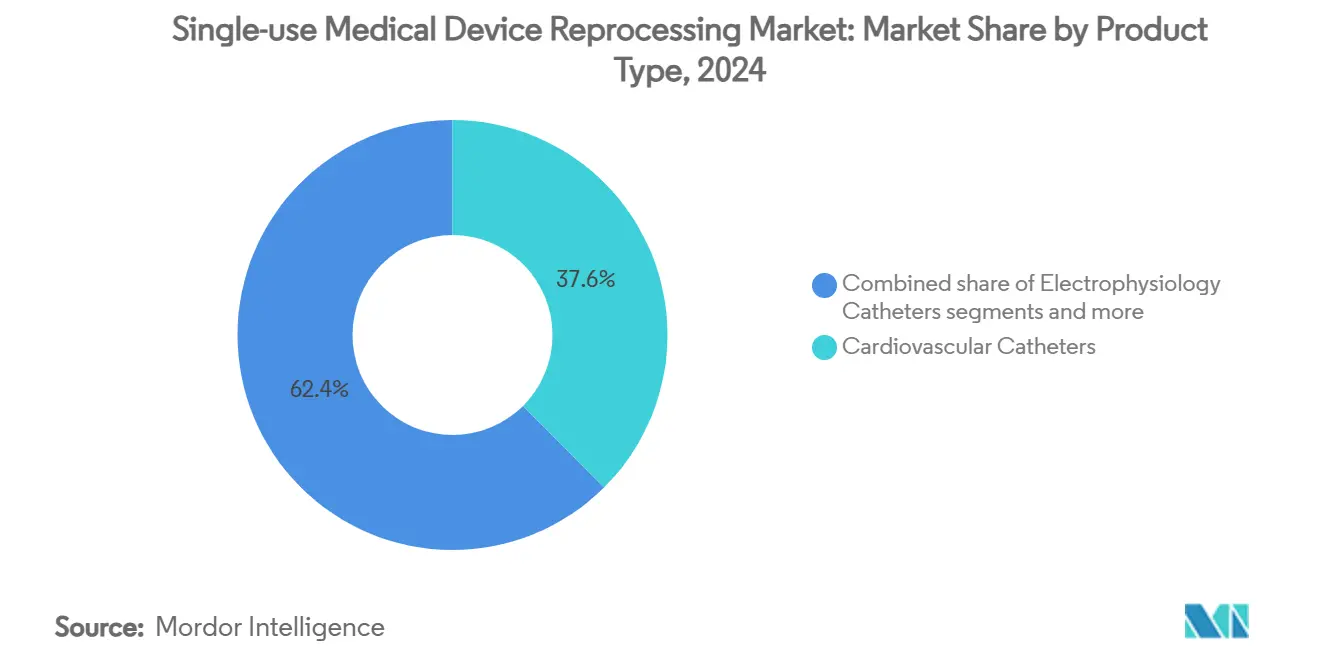
按产品类型,心血管导管在2024年以37.56%的一次性医疗器械再处理市场份额领先;电生理导管预计到2030年将实现最快的16.09%复合年增长率。
按服务提供商,第三方商业再处理商在2024年占据了一次性医疗器械再处理市场规模的84.45%,而该细分市场预计在2025年至2030年间将以16.37%的复合年增长率扩张。
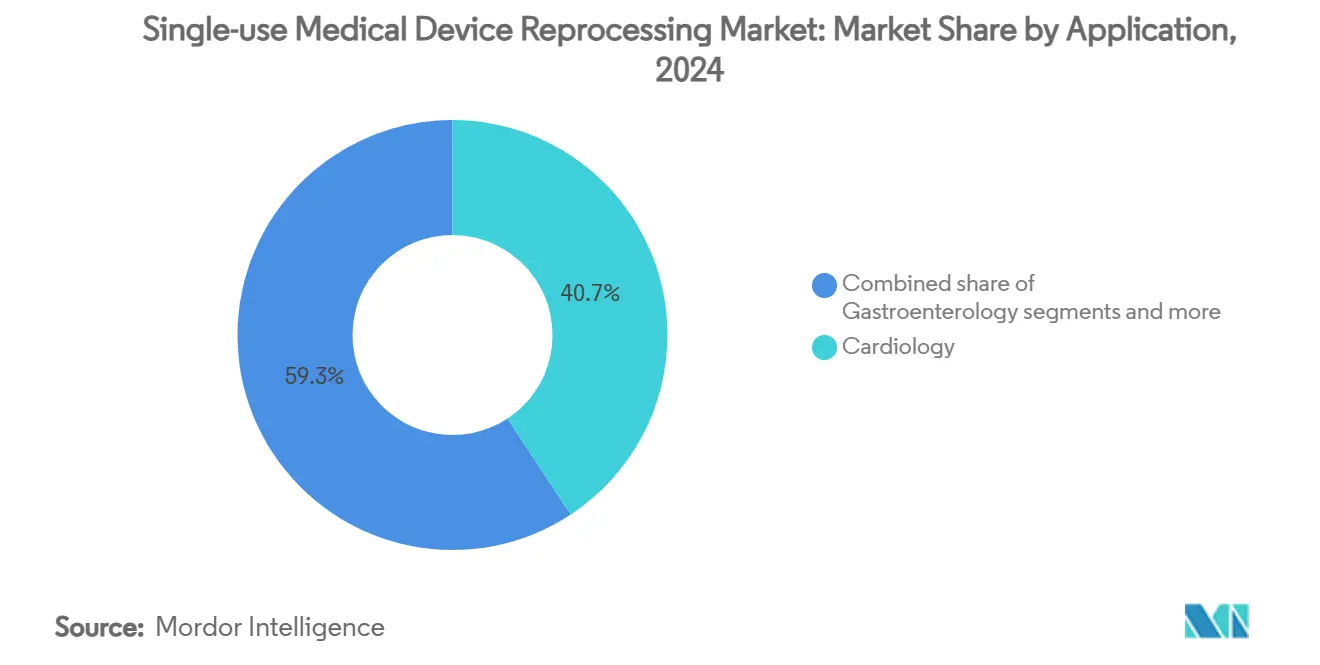
按应用,心脏病学在2024年占一次性医疗器械再处理市场规模的40.73%份额;胃肠病学应用显示出到2030年最高的16.66%复合年增长率前景。
按最终用户,医院和手术中心在2024年代表64.32%的需求,而门诊手术中心正以16.95%的复合年增长率推进到2030年。
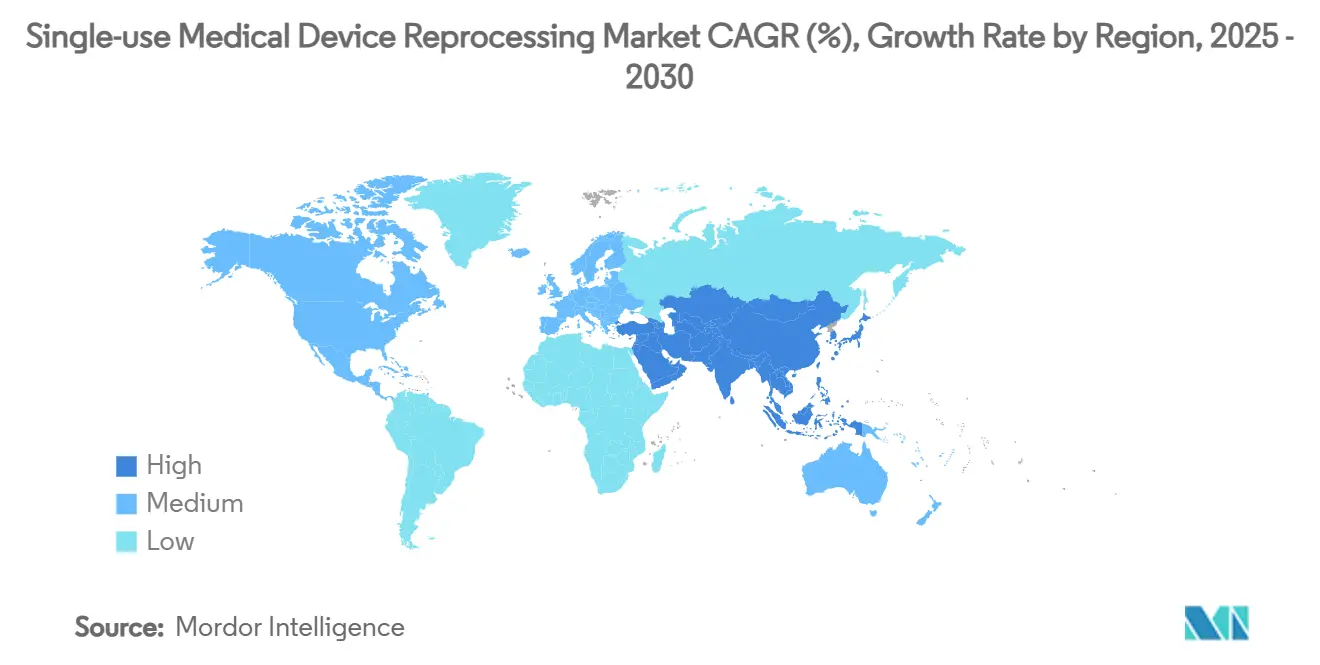
按地理区域,北美在2024年占43.53%的收入,而亚太地区预计将以17.25%的复合年增长率扩张一次性医疗器械再处理市场到2030年。
全球一次性医疗器械再处理市场趋势与见解
驱动因素影响分析
| 驱动因素 | (~) 对复合年增长率预测的影响百分比 | 地理相关性 | 影响时间线 |
|---|---|---|---|
| 医院成本控制压力 | +4.2% | 全球,在北美和欧洲影响急剧 | 中期(2-4年) |
| 一次性医疗器械再处理的监管批准与许可 | +3.8% | 北美和欧盟为主,扩展至亚太地区 | 长期(≥ 4年) |
| 可持续发展和减废要求 | +2.9% | 欧盟领先,北美跟随,亚太地区新兴 | 长期(≥ 4年) |
| ESG报告将范围3排放与采购联系 | +2.1% | 全球企业市场,集中在发达经济体 | 中期(2-4年) |
| 反垄断裁决限制原始设备制造商限制性合同 | +1.8% | 北美为主,欧盟潜在溢出效应 | 短期(≤ 2年) |
| 疫情后个人防护装备短缺的供应链韧性 | +1.5% | 全球,重点在战略储备地区 | 中期(2-4年) |
| 来源: Mordor Intelligence | |||
医院成本控制压力
经营利润率收缩使再处理从医院供应链战略手册中的可选项变为必需项,通常相对于原始设备制造商目录价格提供40-60%的设备级节省。医疗保险付费改革和私人支付方合约提高了一次性器械支出的可见性,促使退伍军人健康管理局在2025年重新审视自己的再处理限制。首席财务官越来越多地将再处理投资回报率纳入年度资本配置模型,转化为多医院网络的系统性采用。节省规模现在对评估非营利健康系统流动性的债券评级机构来说是重要的,加强了管理层的承诺。随着通胀持续,财务管理预计将支撑到2027年至少三分之一的新客户转换。
一次性医疗器械再处理的监管批准与许可
FDA的2024年再制造指导明确了维修和再处理之间的界限,减少了第三方运营商的法律模糊性。过氧化氢汽化获得了作为既定灭菌模式的认可,使验证方法多样化,超越了环氧乙烷。日本将一次性器械再制造纳入其QMS条例,设定了到2024年的分阶段合规截止日期,为其他亚太地区监管机构设定了模板。FDA在2025年批准的VARIPULSE和Sphere-9导管系统,每个都包含可重复使用的组件,标志着对混合使用平台日益增长的信心。这些里程碑共同扩大了一次性医疗器械再处理市场的可寻址基础,超越心脏病学进入复杂的电生理学细分领域。
可持续发展和减废要求
欧盟和英国的国家健康系统现在将再处理视为填埋场转移和碳减排目标的合规杠杆,而不是可自由选择的绿色倡议。超过70%的美国医院在2024年报告了正式的手术室废物项目,再处理被确定为避免填埋场吨位的最大贡献者。英国到2045年消除可避免一次性医疗产品的计划明确将器械再处理列为认可的策略之一。几个欧盟司法管辖区正在评估以公斤产出为指数的废物税,可能到2026年提升再处理的经济理由。随着医疗保健估计贡献全球温室气体排放的4.4%,每个再处理单位40%的排放减少切实改善了提供商的范围3档案。
ESG报告将范围3排放与采购联系
评级机构和投资者越来越多地审查医院范围3披露,将供应链排放与大型系统的资本成本联系起来。领先再处理商的专有碳计算器现在量化每个器械的CO₂避免量,使采购团队能够在供应商记分卡中货币化可持续性溢价。大型综合交付网络在授予多年供应合同时将碳指标与价格捆绑,将再处理从战术节约工具提升为战略ESG差异化因素。健康系统首席财务官在债券发行文件中突出范围3表现,以挖掘绿色债券投资者池,为积极的设备级再处理采用创造财务上行空间。总体而言,这些压力预计将推动到2028年通过2028年18-20%的新再处理客户获胜。
约束因素影响分析
| 约束因素 | (~) 对复合年增长率预测的影响百分比 | 地理相关性 | 影响时间线 |
|---|---|---|---|
| 原始设备制造商游说和限制性标签做法 | -2.8% | 全球,集中在原始设备制造商影响力强的市场 | 中期(2-4年) |
| 设备设计限制多次重复使用周期 | -1.9% | 全球,依赖技术而非地理特定 | 长期(≥ 4年) |
| 欧盟MDR第17条跨境碎片化 | -1.4% | 欧盟为主,潜在监管溢出效应 | 长期(≥ 4年) |
| AI驱动的可追溯性暴露再处理失败 | -0.8% | 拥有先进医疗保健IT基础设施的发达市场 | 短期(≤ 2年) |
| 来源: Mordor Intelligence | |||
原始设备制造商游说和限制性标签做法
强生公司2025年的反垄断败诉,伴随着4.42亿美元的罚款,凸显了原始设备制造商对再处理采用的系统性阻力。制造商继续利用"一次性使用"标签播种法律不确定性,特别是在监管监督新兴的新兴市场中。由原始设备制造商资助的行业协会游说反对扩大器械资格清单,延迟腹腔镜器械等大容量类别的临床采用。即使在反垄断审查限制明显合同限制的地方,诸如员工培训撤回等软性障碍仍能阻碍提供商信心。由此产生的法律环境预计将在短期内从预测的复合年增长率中削减近三个百分点。
欧盟MDR第17条跨境碎片化
欧盟医疗器械法规第17条创建了国家实施的复杂拼凑,碎片化了欧洲再处理市场并增加了合规成本。各成员国保留限制或禁止再处理的权力,导致监管套利,这使泛欧再处理策略复杂化。德国联邦参议院考虑在超过10年的实践后禁止CE再处理,表明了创造投资不确定性的监管不稳定性。用于再处理的跨境器械移动面临制造商义务的不同国家解释,创造了有利于具有多司法管辖区合规能力的较大再处理商的物流复杂性。欧盟委员会2022年12月关于第17条实施的研究揭示了国家方法的显著差异,表明持续碎片化而非协调。
细分分析
按产品类型:心血管主导地位推动市场成熟
心血管导管类别在2024年提供了一次性医疗器械再处理市场规模的37.56%,由充分记录的临床等效性研究和标准化灭菌工作流程支撑。电生理导管以16.09%的复合年增长率领跑,得益于FDA批准的包含可重复使用组件的VARIPULSE和Sphere-9系统的催化。腹腔镜器械受益于机器人手术规模,但复杂几何形状需要主要在大型商业再处理商处可用的自动化清洁隧道。胃肠病学器械增长依赖于诸如ULTRA GI过氧化氢气体等离子体循环等灭菌突破,这些突破减轻了过去的感染风险。骨科外固定硬件由于患者定制配置和延长佩戴时间仍然是利基市场,而通用外科工具提供稳定的数量但面临定价商品化压力。
技术进步,特别是基于AI的器械跟踪标签和云分析,现在允许跨重复使用周期的产品级性能基准测试,培养外科医生对再处理替代品的信任。增强的检查光学器件和非破坏性完整性测试继续提升质量保证,帮助心血管和腹腔镜器械在故障率方面与新的原始设备制造商单位保持近乎对等。随着类别生命周期排放进入正式ESG记分卡,提供商优先考虑诸如导管等高容量一次性类别进行最早转换,加强心血管亚细分领域在一次性医疗器械再处理市场中的领导地位。
备注: 购买报告后可获得所有单独细分的细分份额
按服务提供商:第三方整合加速
第三方运营商在2024年占一次性医疗器械再处理市场份额的84.45%,反映了在灭菌、验证和物流方面的规模优势。该行业到2030年16.37%的复合年增长率受到支付方和监管机构对ISO认证专业设施相对于资源紧张的内部单位的偏好推动。整合继续,以美德兰2024年收购艺康的外科解决方案业务为例,将再处理整合到简化提供商采购的全线分销模式中。
评估内部项目的医院面临灭菌器、可追溯性软件和质量测试的资本支出,每个站点超过500万美元,使成本效益计算倾向于外包。2026年FDA QSR与ISO 13485协调的监管修订预计将加重文档负担,不利于缺乏专门监管团队的较小内部单位。随着商业合作伙伴采用AI视觉检查和机器人包装生产线,吞吐量效率产生5-8点利润优势,扩大与医院运营的差距。因此,大多数美国前100名IDN现在运营混合模式,其中只有非常低容量的器械留在现场,而大容量导管实验室和EP器械每周运送到第三方工厂。
按应用:心脏病学领导地位与胃肠病学加速
心脏病学程序在2024年占一次性医疗器械再处理市场规模的40.73%,建立在数十年证明再处理导管安全性的临床研究基础上。消融量增长和拆除原始设备制造商服务扣留政策的反垄断裁决应该维持到2030年的势头。胃肠病学显示出最高的16.66%复合年增长率预测,得益于新验证的用于十二指肠镜的过氧化氢汽化灭菌周期,消除了感染控制障碍。
骨科因程序标准化程度低和患者特定器械而仍然受限,但创伤中心仍然在具有可预测几何形状的外固定构件上实现节省。泌尿科应用受益于一次性输尿管镜采用增加,一旦管腔清洁机器人技术在2027年达到商业成熟度,就会创造对验证二次重复使用周期的需求。普通外科的增长与手术室可持续发展要求平行,但由于商品化器械套装而面临价格上限约束。
备注: 购买报告后可获得所有单独细分的细分份额
按最终用户:门诊手术中心增长超过医院采用
医院和综合交付网络在2024年需求中占64.32%,但增长率落后于整体市场,因为决策层级延长了评估周期。相比之下,门诊手术中心将在2030年之前实现16.95%的复合年增长率,受到按服务收费迁移和投资者拥有的门诊手术中心链优先考虑器械费用线快速回报的推动。门诊手术中心利用再处理来避开库存持有成本并减轻供应商缺货风险,通常与单个商业合作伙伴签署独家协议以简化物流。
学术医疗中心虽然是可持续发展项目的早期采用者,但面临独特的研究协议约束,这些约束放慢了向再处理器械的完全转换。专业导管实验室利用高器械重复使用潜力,谈判基于数量的回扣,这可能在顶级美国心脏研究所每年超过200万美元。门诊手术中心-诊所合并细分市场预计将在未来五年内获得一次性医疗器械再处理市场增量收入的38%,反映了由支付方激励加速的程序护理地点转移。
地理分析
北美在2024年产生了43.53%的收入,受到FDA指导确定性、反垄断执法和发达的第三方网络的支撑。美国市场还受益于将再处理与ESG关键绩效指标对齐的医院可持续发展章程。加拿大的公共资助健康系统采用再处理来抵消预算上限,而墨西哥在下加利福尼亚的医疗器械集群为跨境提供商提供近岸灭菌产能扩张。
亚太地区预计到2030年将录得17.25%的复合年增长率,由日本的QMS规则协调和中国的医院现代化项目领导,这些项目针对到2028年在一线城市实现70%器械重复使用认证。印度的Ayushman Bharat计划扩大保险覆盖范围,迫使公立医院拉伸固定预算,从而从2026年开始在采购招标中提升再处理地位。韩国和澳大利亚,两个早期电子束灭菌采用者,试点AI跟踪导管重复使用以满足到2035年的国家零废物目标。
欧洲的前景受到第17条碎片化的影响,该碎片化在成员国之间引入了不同的再处理规则,为跨境运营商将合规成本提高了多达25%。德国潜在的CE再处理禁令如果在2026年颁布,可能会移除每年9000万美元的收入,尽管丹麦和荷兰已发布指导,在严格的质量管理监督下启用再处理。英国在欧盟框架之外,正式针对到2045年消除可避免的一次性医疗用品,将再处理定位为中心合规机制。法国卫生部在2024年启动了有限试点以评估十二指肠镜再处理经济学,可能在2027年为国家政策提供信息。
竞争格局
一次性医疗器械再处理市场仍然适度分散,但随着ISO质量合规和先进灭菌投资提高准入门槛,规模驱动的整合正在加速。史赛克的可持续发展解决方案部门在2023年服务了超过3000家美国医院,为客户节省了2.38亿美元,利用AI驱动的跟踪追溯仪表板来区分服务水平。美德兰2024年收购艺康外科解决方案组合将端到端物流控制从原始制造延伸到再处理,增强了与寻求捆绑采购的医院的谈判力量。
独立专业参与者利用电生理和胃肠病学利基市场,其中器械复杂性历史上限制了重复使用;创新健康对强生公司的成功反垄断判决验证了当原始设备制造商扣留支持时市场准入挑战的路径。具有云原生质量管理系统和模块化灭菌舱的新进入者旨在服务缺乏传统轮辐模式数量的农村医院。
展望未来,2026年FDA QSR-ISO 13485对齐应该简化双重合规负担,有利于敏捷的中层公司,同时保持严格的患者安全阈值。灭菌器性能指标和预测性维护算法的系统数字化可能会支撑下一波差异化,实现将器械重复使用周期与碳节约分析联系起来的实时客户仪表板。原始设备制造商内部再处理单位的预期剥离可能会注入额外的整合目标,可能到2028年将前五大市场份额提升到当前55%阈值以上。
一次性医疗器械再处理行业领导者
-
史赛克公司
-
美德兰工业公司
-
创新健康公司
-
强生公司(Sterilmed公司)
-
雅乐公司
- *免责声明:主要玩家排序不分先后
近期行业发展
- 2025年6月:强生医疗科技因与对使用再处理导管的医院扣留临床支持相关的反垄断违规被命令支付4.42亿美元
- 2022年6月:医疗器械再处理商协会启动了《"一次性"医疗器械再处理和再制造的全球监管标准》,这是帮助公告机构、卫生部和医疗器械监管当局为全世界医院和健康系统解锁这些益处的首个路线图。
全球一次性医疗器械再处理市场报告范围
根据报告范围,一次性器械(SUD)再处理包括清洁、消毒、灭菌、测试以及恢复使用过器械的技术和功能安全性。一次性医疗器械再处理使医院能够在节省大量资金的同时保持患者护理质量。
一次性医疗器械再处理市场按器械类型(I类器械(腹腔镜抓钳、手术刀、止血带袖套和其他I类器械)和II类器械(脉搏血氧仪传感器、序贯加压套筒、导管和导丝,以及其他II类器械))和地理区域进行细分(北美、欧洲、亚太地区、中东非洲和南美)。市场报告还涵盖全球主要地区17个国家的估计市场规模和趋势。
报告为上述细分提供价值(美元)。
| 心血管导管 |
| 电生理导管 |
| 腹腔镜器械 |
| 胃肠病学器械 |
| 骨科外固定器械 |
| 普通外科器械 |
| 第三方/商业再处理商 |
| 内部/医院再处理单位 |
| 心脏病学 |
| 胃肠病学 |
| 骨科 |
| 泌尿科 |
| 普通外科 |
| 医院和手术中心 |
| 门诊手术中心 |
| 专科诊所和导管实验室 |
| 学术和研究机构 |
| 北美 | 美国 |
| 加拿大 | |
| 墨西哥 | |
| 南美 | 巴西 |
| 阿根廷 | |
| 南美其他地区 | |
| 欧洲 | 德国 |
| 法国 | |
| 英国 | |
| 意大利 | |
| 西班牙 | |
| 欧洲其他地区 | |
| 亚太地区 | 中国 |
| 日本 | |
| 印度 | |
| 韩国 | |
| 澳大利亚 | |
| 亚太其他地区 | |
| 中东和非洲 | 海湾合作委员会 |
| 沙特阿拉伯 | |
| 中东和非洲其他地区 |
| 按产品类型(价值,美元) | 心血管导管 | |
| 电生理导管 | ||
| 腹腔镜器械 | ||
| 胃肠病学器械 | ||
| 骨科外固定器械 | ||
| 普通外科器械 | ||
| 按服务提供商(价值,美元) | 第三方/商业再处理商 | |
| 内部/医院再处理单位 | ||
| 按应用(价值,美元) | 心脏病学 | |
| 胃肠病学 | ||
| 骨科 | ||
| 泌尿科 | ||
| 普通外科 | ||
| 按最终用户(价值,美元) | 医院和手术中心 | |
| 门诊手术中心 | ||
| 专科诊所和导管实验室 | ||
| 学术和研究机构 | ||
| 按地理区域(价值,美元) | 北美 | 美国 |
| 加拿大 | ||
| 墨西哥 | ||
| 南美 | 巴西 | |
| 阿根廷 | ||
| 南美其他地区 | ||
| 欧洲 | 德国 | |
| 法国 | ||
| 英国 | ||
| 意大利 | ||
| 西班牙 | ||
| 欧洲其他地区 | ||
| 亚太地区 | 中国 | |
| 日本 | ||
| 印度 | ||
| 韩国 | ||
| 澳大利亚 | ||
| 亚太其他地区 | ||
| 中东和非洲 | 海湾合作委员会 | |
| 沙特阿拉伯 | ||
| 中东和非洲其他地区 | ||
报告中回答的关键问题
一次性医疗器械再处理市场在2030年的预测价值是多少?
预测到2030年将达到24.5亿美元,从2025年的11.7亿美元以15.93%的复合年增长率增长。
目前哪种产品类型在器械再处理中占主导地位?
心血管导管占37.56%的收入份额,得到长期临床验证的支持。
为什么门诊手术中心采用再处理的速度比医院快?
门诊手术中心优先考虑利润管理并具有简化的治理,到2030年实现16.95%的复合年增长率。
环境法规如何影响采用?
范围3碳报告和填埋场减少要求将再处理定位为也产生器械级节省的合规途径。
2025年强生反垄断裁决产生了什么影响?
4.42亿美元的罚款限制了原始设备制造商合同限制,为独立提供商开放了导管再处理机会。
页面最后更新于:



