Taille et part du marché de la thérapie du cancer gastrique
Analyse du marché de la thérapie du cancer gastrique par Mordor Intelligence
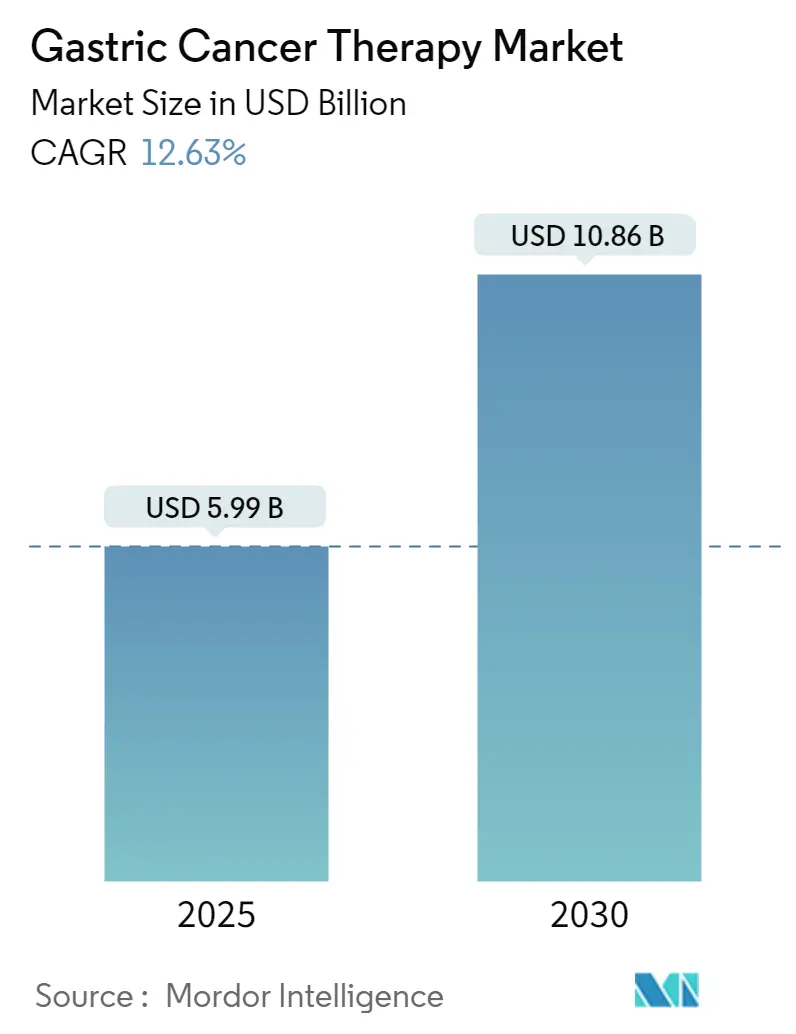
La taille du marché du traitement du cancer gastrique un atteint 5,99 milliards USD en 2025 et devrait atteindre 10,86 milliards USD d'ici 2030 grâce à un TCAC solide de 12,63 % tout au long de la période de prévision, soulignant une expansion vigoureuse de la demande dans tous les contextes de soins. L'incidence accélérée parmi les cohortes vieillissantes, l'adoption rapide de l'immunothérapie, les tests de biomarqueurs plus précoces, et les réformes d'approvisionnement à haut volume de la Chine soutiennent ensemble l'élan de croissance dans toutes les grandes régions. Le dépistage endoscopique assisté par intelligence artificielle fait évoluer la détection vers des stades curables, tandis que les diagnostics compagnons informent désormais un ensemble élargi de régimes de précision qui améliorent les résultats et prolongent la durée du traitement. Cinq approbations révolutionnaires ont obtenu l'autorisation aux États-Unis entre octobre 2024 et mars 2025, et les systèmes de voie rapide parallèles au Japon et dans l'Union européenne réduisent les délais de lancement pour les candidats en phase avancée, renforçant la visibilité des revenus pour les innovateurs. Inversement, les coûts élevés des complications post-chirurgicales et le remboursement inégal des biomarqueurs dans les économies émergentes créent encore des frictions sur les soins optimaux, tempérant les courbes d'adoption à court terme pour les médicaments premium sur certains marchés.
Points clés du rapport
- Par type de thérapie, la chimiothérapie un dominé avec 42,19 % de part de revenus en 2024, tandis que l'immunothérapie devrait progresser à un TCAC de 13,45 % jusqu'en 2030.
- Par classe de médicaments, les inhibiteurs PD-1/PD-L1 ont capturé 20,23 % de la part du marché du traitement du cancer gastrique en 2024, tandis que les inhibiteurs FGFR2 sont positionnés pour croître à un TCAC de 12,55 % jusqu'en 2030.
- Par stade de la maladie, les cas récurrents ont représenté 22,91 % de la taille du marché du traitement du cancer gastrique en 2024, et la maladie au stade précoce (0-IA) devrait s'étendre à un TCAC de 13,71 % jusqu'en 2030.
- Par voie d'administration, l'administration intraveineuse un dominé avec 68,82 % de part en 2024 ; les formulations orales devraient augmenter à un TCAC de 12,93 % sur le même horizon.
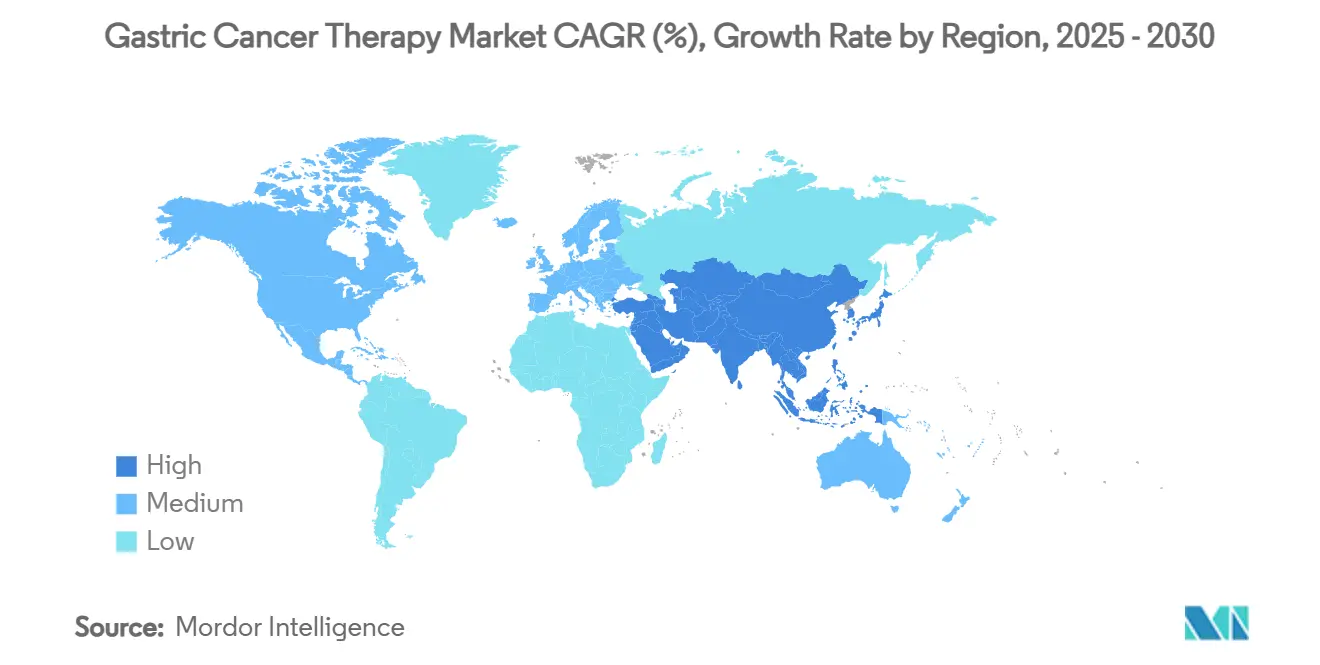
- Par géographie, l'Amérique du Nord un généré 42,23 % de part de revenus en 2024, tandis que l'Asie-Pacifique devrait afficher le TCAC le plus rapide de 15,56 % vers 2030.
Tendances et insights du marché mondial de la thérapie du cancer gastrique
Analyse d'impact des moteurs
| Moteur | (~) % Impact sur les prévisions TCAC | Pertinence géographique | Calendrier d'impact |
|---|---|---|---|
| Vieillissement de la population et augmentation de la prévalence d'H. pylori | +2.8% | Mondial, concentré en Asie-Pacifique et en Europe | Long terme (≥ 4 ans) |
| Adoption des inhibiteurs de points de contrôle PD-1/PD-L1 | +1.9% | Amérique du Nord et UE en tête, APAC qui suit | Moyen terme (2-4 ans) |
| Protocoles de tests HER2-positifs plus précoces | +1.2% | Mondial, avec adoption plus rapide sur les marchés développés | Moyen terme (2-4 ans) |
| Baisses de prix d'approvisionnement basé sur le volume en Chine | +0.8% | Chine principalement, répercussion sur d'autres marchés APAC | Court terme (≤ 2 ans) |
| Pilotes de dépistage endoscopique assisté par IA | +1.1% | Japon, Corée du Sud, Allemagne en tête d'adoption | Moyen terme (2-4 ans) |
| Pipelines de vaccins néo-antigène ARNm | +0.7% | Centres cliniques d'Amérique du Nord et UE | Long terme (≥ 4 ans) |
| Source: Mordor Intelligence | |||
Vieillissement de la population et augmentation de la prévalence d'H. pylori
Le vieillissement démographique se combine avec l'infection persistante à H. pylori pour maintenir l'incidence de base sur une pente ascendante, particulièrement au Japon, en Corée du Sud, en Chine et dans le sud de l'Europe où l'exposition historique persiste malgré les programmes d'éradication. Les bases de données de sorties hospitalières de Tokyo montrent que les personnes ≥65 ans représentent plus de 70 % des nouveaux diagnostics de cancer gastrique, confirmant la vague de demande entrant dans les cliniques d'oncologie. Parce que la rémission nécessite souvent une thérapie multimodale longue et un suivi fréquent, les patients âgés consomment généralement des volumes de médicaments cumulés plus élevés, une dynamique qui gonfle les dépenses à vie par cas dans le marché du traitement du cancer gastrique. De plus, les analyses du monde réel indiquent que les protocoles de gestion de la toxicité gériatrique se sont remarquablement améliorés au cours des deux dernières années, permettant aux cliniciens de maintenir les régimes systémiques plus longtemps sans réductions de dose, augmentant ainsi les volumes de vente moyens pour les inhibiteurs de points de contrôle et les agents ciblés. Les payeurs luttent néanmoins avec l'impact budgétaire du traitement de cohortes âgées plus importantes, provoquant un passage vers des schémas de remboursement basés sur la valeur qui lient le paiement aux résultats sur des horizons pluriannuels. Bien que les mesures préventives continuent de s'étendre, leur bénéfice épidémiologique ne se matérialisera que graduellement, sécurisant une longue piste de demande thérapeutique soutenue dans le marché du traitement du cancer gastrique.
Adoption des inhibiteurs de points de contrôle PD-1/PD-L1
L'adoption en première ligne du pembrolizumab plus trastuzumab et chimiothérapie, approuvée en mars 2025, un augmenté la survie médiane sans progression de 7,3 à 10,9 mois, modifiant les algorithmes de traitement de première carte en Amérique du Nord et en Europe. Les dossiers d'évaluation des technologies de santé soumis en France et en Italie indiquent un coût incrémental par année de vie ajustée sur la qualité qui tombe en dessous des seuils nationaux de volonté de payer lorsque le médicament est utilisé chez les patients biomarqueurs-positifs, propulsant l'inclusion au formulaire et ancrant la croissance des revenus dans le marché du traitement du cancer gastrique. De même, l'utilisation périopératoire des combinaisons durvalumab un réduit le risque de récurrence de 29 % dans les essais randomisés présentés à l'ASCO 2025, incitant les comités de directives à recommander la modulation immunitaire plus tôt dans le cours de la maladie. Notamment, la durabilité de la réponse pour les patients avec des scores PD-L1 faibles s'est améliorée lorsque le blocage des points de contrôle est associé au trastuzumab ou aux agents cytotoxiques, élargissant la cohorte traitable d'autant qu'un tiers selon les données de Phase 3 groupées.
Protocoles de tests HER2-positifs plus précoces
L'approbation par l'Union européenne du test VENTANA CLDN18 RxDx en juillet 2024 un initié un passage vers le profilage tumoral basé sur des Panneaux qui évalue HER2, CLDN18.2, FGFR2, et PD-L1 à partir d'une seule lame de biopsie, réduisant le temps jusqu'au résultat à moins de cinq jours dans les centres de cancer de pointe. Les études d'adoption en Allemagne ont trouvé que les Panneaux larges doublaient la proportion de patients signalés pour la thérapie ciblée versus les tests séquentiels de marqueur unique, élargissant le volume adressable pour le trastuzumab deruxtecan, le zolbetuximab, et les inhibiteurs FGFR2 à venir. Les hôpitaux de Séoul métropolitain rapportent que les tests réflexes le jour même intègrent la pathologie moléculaire dans les flux de travail diagnostiques initiaux, permettant aux oncologues de commencer les régimes guidés par biomarqueurs un cycle de traitement plus tôt, ce qui peut améliorer la survie globale de deux à trois mois dans les cas à intention curative. L'identification précoce réduit également l'exposition futile à la chimiothérapie inefficace, tronquant les dépenses liées à la toxicité et renforçant le soutien des payeurs pour l'expansion systématique des tests. Alors que les marchés émergents modernisent les laboratoires de pathologie avec des plateformes d'immunohistochimie automatisées, le marché du traitement du cancer gastrique gagne un nouveau levier pour l'expansion du volume de cas entraînée par la pénétration diagnostique plutôt que par l'incidence brute seule.
Baisses de prix d'approvisionnement basé sur le volume en Chine
Sous les négociations de la Liste nationale des médicaments remboursables conclues en décembre 2024, les prix sortie usine moyens pour les marques clés d'oncologie gastrique ont chuté de 60-80 %, élargissant l'accès pour environ 150 000 patients annuellement. Les fabricants ont répondu en adoptant une stratégie de prix échelonnés : des marges plus faibles en Chine sont contrebalancées par des volumes élevés garantis, tandis que les prix ailleurs référencent maintenant l'approvisionnement chinois dans les contrats basés sur la valeur. Les audits de prescription du monde réel confirment que l'usage hospitalier du nivolumab et du trastuzumab deruxtecan un augmenté de plus de trois fois dans les centres provinciaux durant les deux premiers trimestres de 2025, compensant l'érosion du prix unitaire et générant des gains de revenus absolus régionalement. Les pays voisins comme le Vietnam et la Malaisie ont commencé à explorer des modèles d'approvisionnement comparables, signalant une propagation potentielle du paradigme volume-à-échelle qui pourrait remodeler les marges mais aussi élargir la portée des patients dans le marché du traitement du cancer gastrique.
Analyse d'impact des contraintes
| Contrainte | (~) % Impact sur les prévisions TCAC | Pertinence géographique | Calendrier d'impact |
|---|---|---|---|
| Coûts élevés des complications post-chirurgicales | -1.4% | Mondial, plus prononcé sur les marchés émergents | Moyen terme (2-4 ans) |
| Remboursement limité des biomarqueurs hors des villes de niveau 1 | -0.9% | Chine, Inde, autres marchés APAC émergents | Court terme (≤ 2 ans) |
| Pénurie de spécialistes en oncologie GI en LATAM | -0.7% | Amérique latine, répercussion sur d'autres régions émergentes | Long terme (≥ 4 ans) |
| Fragilité de la chaîne d'approvisionnement pour les formulations liposomales | -0.6% | Mondial, aigu dans les régions avec infrastructure de chaîne du froid limitée | Moyen terme (2-4 ans) |
| Source: Mordor Intelligence | |||
Coûts élevés des complications post-chirurgicales
Les complications majeures de gastrectomie surviennent dans 15-25 % des cas et coûtent 15 000-25 000 USD par réadmission, grevant les payeurs et retardant la thérapie adjuvante, ce qui peut aggraver les résultats de survie de 10-15 % pour les patients affectés. Les données des hôpitaux publics au Brésil, en Afrique du Sud et en Indonésie montrent que les soins des complications absorbent jusqu'à 30 % des budgets d'oncologie hospitalière totaux, évincant les fonds pour les agents systémiques modernes. La récupération améliorée après chirurgie et les approches laparoscopiques réduisent les taux de complications à près de 10 % dans les centres à haut volume, pourtant les dépenses d'investissement pour la robotique restent prohibitives pour de nombreux pays à revenu intermédiaire. Jusqu'à ce qu'une standardisation chirurgicale plus large soit atteinte, les payeurs peuvent plafonner les dépenses sur les médicaments adjuvants premium pour les candidats à haut risque, amortissant le potentiel d'adoption dans des parties du marché du traitement du cancer gastrique. Les consortiums impliquant les fabricants d'appareils, les organismes de formation chirurgicale et les prêteurs multilatéraux explorent le financement basé sur les résultats pour abaisser les barrières d'entrée pour les plateformes mini-invasives, mais l'impact tangible prendra plusieurs cycles budgétaires pour se manifester.
Remboursement limité des biomarqueurs hors des villes de niveau 1
En Chine et en Inde, les Panneaux complets de séquençage de nouvelle génération dépassent souvent 400 USD-un montant dépassant le revenu mensuel de larges populations rurales-forçant les médecins à s'appuyer sur la chimiothérapie seule pour de nombreuses tumeurs biomarqueurs-positives. Les assureurs provinciaux en Chine remboursent généralement seulement l'immunohistochimie pour HER2 dans les hôpitaux tertiaires, laissant les tests pour CLDN18.2 ou FGFR2 non couverts, ce qui restreint la vérification d'éligibilité pour le zolbetuximab ou les inhibiteurs FGFR2. Une disparité similaire survient dans les anciennes installations de la Mission nationale de santé de l'Inde, où les coûts diagnostiques payés en espèces dissuadent les tests. La conséquence est l'inéquité thérapeutique : les registres publiés montrent que la pénétration de la thérapie guidée par biomarqueurs tombe en dessous de 15 % hors des hubs urbains de niveau 1, limitant l'empreinte du monde réel des médicaments de précision. La télépathologie et les tests PCR basés sur cartouches promettent de réduire les coûts jusqu'à 60 %, pourtant leur mise à l'échelle nécessite une harmonisation réglementaire et des cadres de sécurité cloud qui restent en développement. Jusqu'à ce que ces écarts d'accès se ferment, une certaine marge de croissance pour le marché du traitement du cancer gastrique restera non réalisée.
Analyse des segments
Par type de thérapie : L'immunothérapie pilote l'innovation
L'immunothérapie un généré environ 1,2 milliard USD de revenus dans le marché du traitement du cancer gastrique en 2025, représentant le segment avec le TCAC le plus rapide de 13,45 % et confirmant son rôle fondamental dans les algorithmes de soins modernes. La chimiothérapie un néanmoins conservé une part formidable de 42,19 % en 2024 car elle reste l'épine dorsale des régimes de première ligne, particulièrement dans les contextes métastatiques, et conserve des avantages de prix qui en font le défaut dans les hôpitaux à budget contraint. Les volumes de résection chirurgicale augmentent grâce aux protocoles périopératoires améliorés, mais les cycles de thérapie systémique par patient continuent d'augmenter alors que les agents immunologiques prolongent la survie, soutenant ainsi le dosage répété. La radiothérapie occupe une niche modeste, largement confinée aux tumeurs localement avancées où les stratégies de préservation d'organes augmentent les marges de résection.
Le pivot rapide vers les protocoles multimédicaments brouille les catégorisations historiques : les inhibiteurs de points de contrôle se lancent maintenant simultanément avec les bases cytotoxiques, et les combinaisons trastuzumab deruxtecan plus nivolumab ont progressé dans les tests de Phase 3 pour les contextes adjuvants, indiquant que la "thérapie combinée" éclipsera bientôt les catégories d'agent unique. L'adoption de thérapie ciblée s'accélère chaque fois que les tests HER2 ou FGFR2 sont remboursés, tandis que les régimes palliatifs et de soins de soutien commencent plus tôt car l'amélioration de la survie prolonge les besoins de gestion des symptômes. En raison de ces lignes de thérapie entrelacées, les oncologues spécialisés voient de plus en plus la sélection de médicaments à travers une lentille de plateforme intégrée plutôt que des classes discrètes, une perspective qui favorise les entreprises capables de regrouper immunothérapie, ADC, et agents de soutien en offres coordonnées dans le marché du traitement du cancer gastrique.
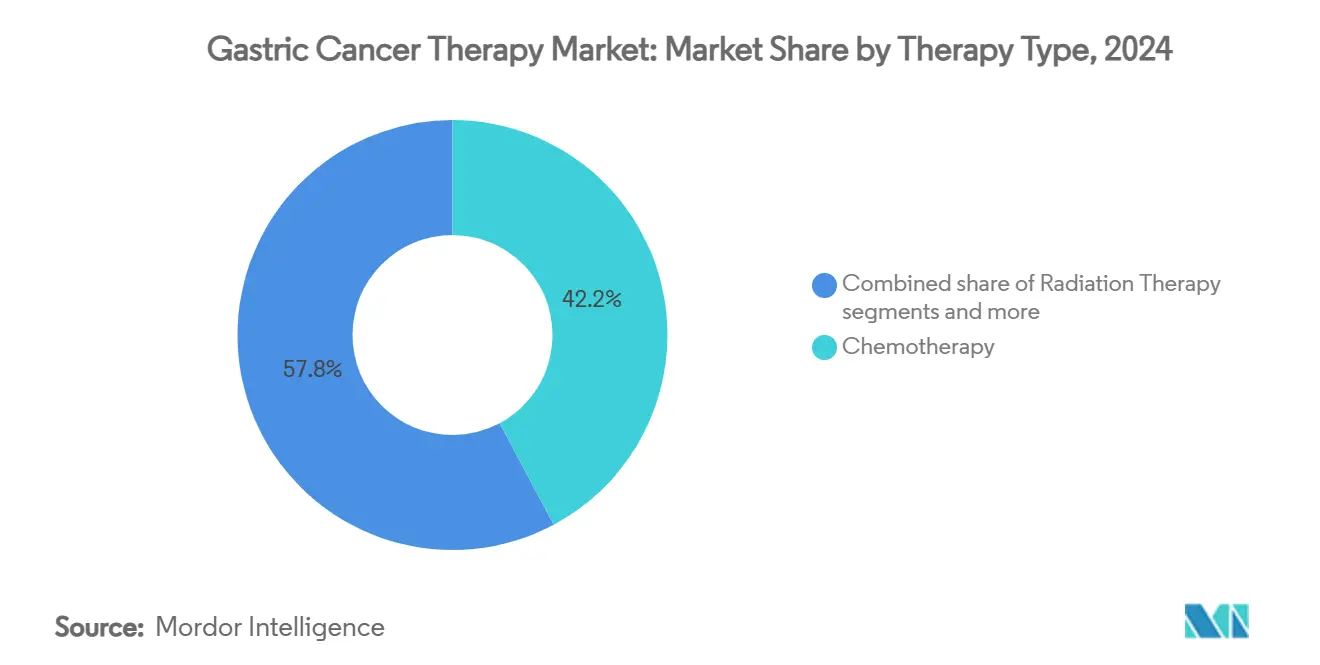
Note: Parts de segments de tous les segments individuels disponibles à l'achat du rapport
Par classe de médicaments : Les inhibiteurs FGFR2 mènent la croissance
Les inhibiteurs PD-1/PD-L1 ont enregistré la plus grande part de 20,23 % des revenus de classe de médicaments de 2024, reflétant leur ancrage comme standard de soins à travers plusieurs lignes. Pourtant leur croissance annuelle se modère alors que la pénétration sur les marchés à hauts revenus approche la saturation. En revanche, les inhibiteurs FGFR2 devraient enregistrer le TCAC le plus rapide de 12,55 %, portés par des taux de réponse frappants près de 42 % dans les tumeurs amplifiées FGFR2 et les approbations attendues au Japon et en Corée du Sud d'ici 2026. À l'horizon, les anticorps bispécifiques qui fusionnent le blocage PD-1 avec le ciblage FGFR2 entrent dans les évaluations cliniques précoces, préparant le terrain pour une efficacité de changement d'étape qui pourrait stimuler davantage la part de classe.
Les agents cytotoxiques conservent la pertinence en ancrant les régimes nouveaux et maintenant les avantages de remboursement, spécialement dans les marchés où la doxorubicine biosimilaire ou l'oxaliplatine coûtent des centimes sur le dollar comparé aux biologiques de marque. Les antagonistes HER2 ont renforcé les bases après l'approbation agnostique tumorale de la FDA pour le trastuzumab deruxtecan en avril 2024, qui un incité le dépistage HER2 universel pour toutes les présentations métastatiques. Les inhibiteurs VEGF/VEGFR et les ADC fournissent une activité adjuvante importante : la normalisation vasculaire améliore l'infiltration immune, tandis que les ADC délivrent des charges utiles létales aux cellules riches en marqueurs, amplifiant la synergie avec le blocage des points de contrôle immuns. Collectivement, la mosaïque des classes de médicaments souligne que la différenciation soutenue naît du ciblage précis des patients et du potentiel de combinaison modulaire, renforçant les stratégies multiplateformes dans le marché du traitement du cancer gastrique.
Par stade de la maladie : Le stade précoce gagne de l'élan
La maladie au stade précoce 0-IA un généré environ 580 millions USD de revenus en 2025 et mène tous les stades à un TCAC de 13,71 % alors que le dépistage assisté par IA déplace le diagnostic vers des formes moins avancées. Les cas récurrents se classent encore premiers en valeur, capturant 22,91 % des dollars de segment de 2024 en raison de l'incidence élevée de rechute et de la thérapie systémique prolongée. Les cas résécables IB-III bénéficient de la chimiothérapie néoadjuvante couplée à l'immunothérapie, qui un augmenté les taux de résection R0 de 14 % dans les essais multicentriques récents et amélioré la survie médiane sans maladie de six mois par rapport à la chirurgie seule.
La gestion des tumeurs localement avancées non résécables reste complexe ; cependant, les régimes nivolumab plus paclitaxel ont atteint 38,5 % de réponse dans les métastases péritonéales sévères, suggérant une amélioration pour un sous-groupe historiquement réfractaire. L'adoption soutenue de l'immunothérapie périopératoire compresse l'écart de temps entre la chirurgie et l'initiation de la thérapie systémique, potentiellement limitant la progression micro-métastatique. La maladie avancée/métastatique continue de générer le volume de médicaments le plus élevé par patient en raison des lignes de traitement successives, pourtant un meilleur contrôle de première ligne pourrait graduellement réduire la dépendance aux cytotoxiques de ligne tardive. Alors que la migration de stade favorise la détection précoce, l'expansion de valeur future dans le marché du traitement du cancer gastrique dépendra plus de l'innovation adjuvante que des thérapies de sauvetage.
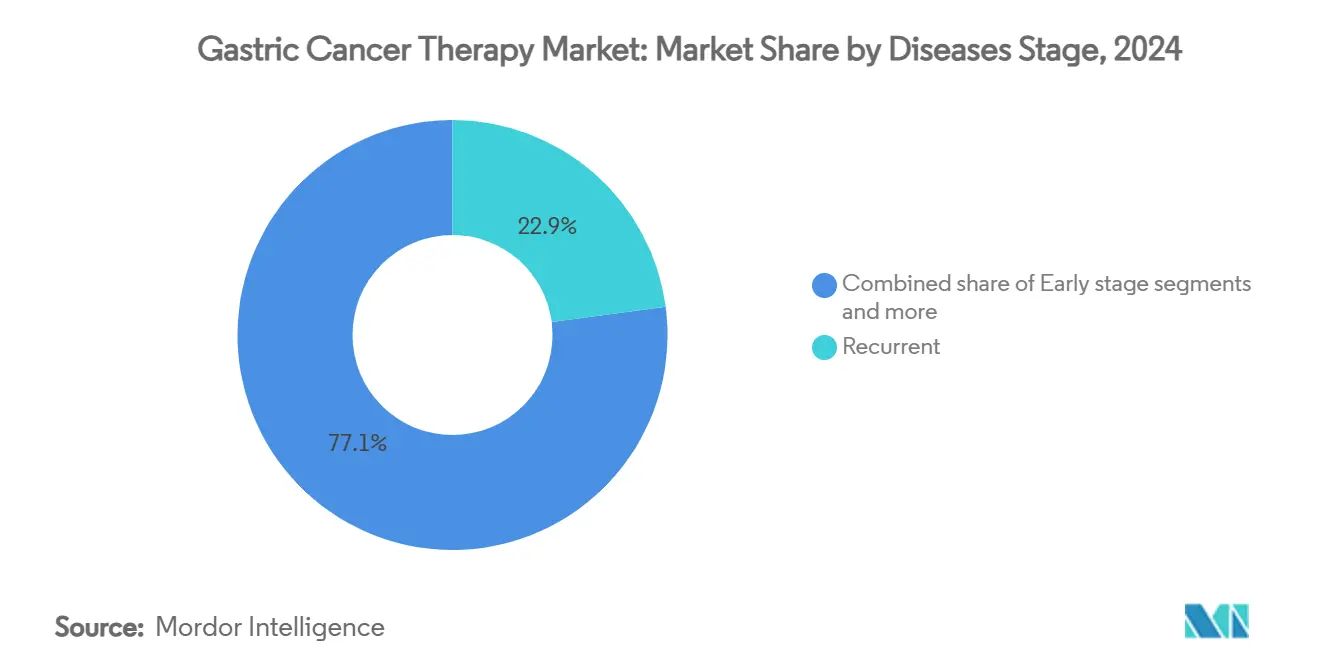
Note: Parts de segments de tous les segments individuels disponibles à l'achat du rapport
Par voie d'administration : Les formulations orales s'étendent
Les perfusions intraveineuses ont réalisé environ 4,1 milliards USD en 2025, égal à 68,82 % des dépenses totales grâce aux protocoles hospitaliers ancrés et à la prédominance des biologiques. Les médicaments oraux, menés par la capécitabine et l'apatinib, ont augmenté à un TCAC de 12,93 %, soulignant une forte préférence des patients pour le dosage à domicile et l'intérêt des payeurs pour la réduction des frais généraux des centres de perfusion.
Le focus de recherche se dirige maintenant vers les inhibiteurs de points de contrôle oraux et les ADC oraux construits sur des liants clivables par protéase qui survivent au pH gastrique et libèrent la charge utile une fois absorbés systémiquement, technologie initialement commercialisée en hématologie mais ciblant maintenant les tumeurs solides gastriques. Les systèmes de santé en Australie ont documenté 15 % d'économies de coûts après avoir basculé les patients de maintien appropriés vers la thérapie orale, renforçant les incitations économiques. La surveillance d'adhérence activée par télésanté un davantage augmenté la confiance dans les régimes à domicile, réduisant les préoccupations sur les doses manquées. Pourvu que la parité pharmacocinétique soit maintenue, de nombreux agents intraveineux pourraient se convertir à l'oral, érodant la part de perfusion et insufflant une croissance fraîche dans le marché du traitement du cancer gastrique.
Analyse géographique
L'Amérique du Nord un généré 42,23 % des revenus mondiaux en 2024 grâce à la large couverture d'assurance, au pouvoir de prix élevé des médicaments, et aux voies d'examen FDA accélérées telles que la thérapie révolutionnaire et l'examen d'oncologie en temps réel qui accélèrent l'accès de six à huit mois versus les voies standard. Pourtant la décélération de croissance est visible alors que les payeurs superposent des formulaires basés sur la valeur : le remboursement limité dans le temps du Canada de mai 2025 pour le trastuzumab deruxtecan lie la continuation du paiement aux résultats intérimaires du monde réel, préfigurant des contrats basés sur les résultats plus larges.
L'Asie-Pacifique mène la croissance avec un TCAC de 15,56 %, alimentée par l'approvisionnement basé sur le volume de la Chine, l'infrastructure d'oncologie en expansion de l'Inde, et le remboursement quasi-automatique du Japon pour les agents approuvés dans les 90 jours. Les réclamations hospitalières chinoises montrent que l'usage du nivolumab un triplé dans les villes de niveau inférieur après l'inclusion dans le tour d'approvisionnement 2024, soulignant l'élasticité du volume. Le réseau hospitalier gouvernemental du cancer de l'Inde un ajouté huit nouveaux centres tertiaires en 2025, chacun équipé de laboratoires de diagnostics moléculaires qui accélèrent le dépistage de biomarqueurs. Les régulateurs japonais ont approuvé un nouveau système d'endoscopie guidé par IA en avril 2025, positionnant le pays pour maintenir le leadership en détection précoce qui alimente les volumes de cas dans les pipelines de thérapie systémique.
L'Europe reste un adopteur mature mais prudent, avec la rigueur d'évaluation des technologies de santé poussant les entreprises à accumuler rapidement des preuves du monde réel pour sécuriser les remboursements nationaux. Les assureurs statutaires allemands remboursent largement l'immunothérapie périopératoire après l'évaluation positive IQWiG, tandis que l'Italie requiert des accords prix-volume qui plafonnent les dépenses publiques. L'Amérique du Sud et le Moyen-Orient/Afrique représentent ensemble juste sous 7 % du marché du traitement du cancer gastrique mais détiennent un potentiel latent alors que les multinationales pilotent des schémas d'assistance aux patients qui subventionnent les tests de biomarqueurs et le soutien de co-paiement. Largement, la diversification géographique réduit la surexposition à tout environnement de remboursement unique et ajoute de la résilience au marché mondial du traitement du cancer gastrique.
Paysage concurrentiel
Le marché du traitement du cancer gastrique montre une consolidation modérée : les cinq premières entreprises-Roche, Merck, Bristol Myers Squibb, AstraZeneca, et Pfizer-capturent collectivement légèrement au-dessus de la moitié des ventes annuelles, soulignant les hautes barrières de développement liées à la fabrication biologique complexe et aux standards de preuve réglementaires stricts.
Les entreprises leaders pivotent des lancements d'actifs uniques vers des stratégies d'écosystème qui enveloppent médicament, diagnostic, et services numériques en offres cohésives. Roche emballe ses biologiques anti-HER2 avec le test CLDN18 approuvé, tandis qu'AstraZeneca déploie des applications d'adhérence et des dispositifs portables de surveillance à distance aux côtés de son pipeline oral, visant à verrouiller la part de marché via une expérience patient supérieure. Les entrants biosimilaires grignotent les anticorps de première génération, pourtant les ADC de nouvelle génération et les constructions bispécifiques restent isolées par la profondeur de propriété intellectuelle et la complexité de fabrication.
Les accords de licence et co-développement s'intensifient alors que les majors occidentales s'associent avec les biotechs chinoises-BeiGene licence les droits de commercialisation américaine du tislelizumab à Novartis, tandis qu'Innovent collabore avec Eli Lilly sur des fusions globales de blocage de points de contrôle et d'inhibition VEGF. Les partenariats d'intelligence artificielle ciblent l'accélération de la découverte ; l'alliance de Merck avec une start-up de Silicon Valley un réduit de moitié le temps d'identification de cible préclinique, compressant potentiellement les cycles de développement. À l'avenir, les entreprises maniant des plateformes intégrées thérapie-diagnostic-analytique semblent les mieux positionnées pour maintenir le leadership dans le marché du traitement du cancer gastrique.
Leaders de l'industrie de la thérapie du cancer gastrique
Eli Lilly and Company
Pfizer Inc.
F. Hoffmann-La Roche Ltd
Celltrion Inc.
Merck & Co
- *Avis de non-responsabilité : les principaux acteurs sont triés sans ordre particulier
Développements récents de l'industrie
- Juin 2025 : ENHERTU un réduit le risque de décès de 30 % versus ramucirumab plus paclitaxel dans l'essai Phase 3 DESTINY-Gastric04 pour la maladie métastatique HER2-positive, établissant un nouveau benchmark de deuxième ligne
- Avril 2025 : L'Agence des médicaments du Canada un émis un remboursement limité dans le temps pour ENHERTU, permettant l'accès des patients près de deux ans plus tôt que les délais d'examen standard
Portée du rapport mondial du marché de la thérapie du cancer gastrique
Le cancer de l'estomac est caractérisé par la croissance de cellules cancéreuses dans la muqueuse de l'estomac. Le cancer de l'estomac est un type de cancer relativement rare. Certains des facteurs de risque associés au cancer de l'estomac sont le lymphome, les infections bactériennes H. pylori, les tumeurs dans d'autres parties du système digestif, et les polypes d'estomac.
Le marché de la thérapie du cancer gastrique est segmenté par type de thérapie (chimiothérapie, thérapie ciblée, immunothérapie, radiothérapie, et chirurgie), utilisateur final (centres de chirurgie ambulatoire, hôpitaux et cliniques spécialisées, et autres utilisateurs finaux), et géographie, et Géographie (Amérique du Nord, Europe, Asie-Pacifique, Moyen-Orient et Afrique, et Amérique du Sud). Le rapport de marché couvre également les tailles de marché estimées et les tendances pour 17 pays différents à travers les principales régions mondialement.
Le rapport offre la valeur (en USD) pour les segments ci-dessus.
| Chirurgie |
| Chimiothérapie |
| Radiothérapie |
| Thérapie ciblée |
| Immunothérapie |
| Thérapie combinée |
| Soins palliatifs et de soutien |
| Agents cytotoxiques |
| Antagonistes HER2 |
| Inhibiteurs PD-1/PD-L1 |
| Inhibiteurs VEGF / VEGFR |
| Inhibiteurs FGFR2 |
| ADC (Conjugués anticorps-médicament) |
| Autres |
| Intraveineuse |
| Orale |
| Stade précoce (0-IA) |
| Résécable (IB-III) |
| Localement avancé non résécable |
| Avancé / Métastatique |
| Amérique du Nord | États-Unis |
| Canada | |
| Mexique | |
| Europe | Allemagne |
| Royaume-Uni | |
| France | |
| Italie | |
| Espagne | |
| Reste de l'Europe | |
| Asie-Pacifique | Chine |
| Inde | |
| Japon | |
| Corée du Sud | |
| Australie | |
| Reste de l'Asie-Pacifique | |
| Amérique du Sud | Brésil |
| Argentine | |
| Reste de l'Amérique du Sud | |
| Moyen-Orient et Afrique | CCG |
| Afrique du Sud | |
| Reste du Moyen-Orient et de l'Afrique |
| Par type de thérapie | Chirurgie | |
| Chimiothérapie | ||
| Radiothérapie | ||
| Thérapie ciblée | ||
| Immunothérapie | ||
| Thérapie combinée | ||
| Soins palliatifs et de soutien | ||
| Par classe de médicaments | Agents cytotoxiques | |
| Antagonistes HER2 | ||
| Inhibiteurs PD-1/PD-L1 | ||
| Inhibiteurs VEGF / VEGFR | ||
| Inhibiteurs FGFR2 | ||
| ADC (Conjugués anticorps-médicament) | ||
| Autres | ||
| Par voie d'administration | Intraveineuse | |
| Orale | ||
| Par stade de la maladie | Stade précoce (0-IA) | |
| Résécable (IB-III) | ||
| Localement avancé non résécable | ||
| Avancé / Métastatique | ||
| Par géographie | Amérique du Nord | États-Unis |
| Canada | ||
| Mexique | ||
| Europe | Allemagne | |
| Royaume-Uni | ||
| France | ||
| Italie | ||
| Espagne | ||
| Reste de l'Europe | ||
| Asie-Pacifique | Chine | |
| Inde | ||
| Japon | ||
| Corée du Sud | ||
| Australie | ||
| Reste de l'Asie-Pacifique | ||
| Amérique du Sud | Brésil | |
| Argentine | ||
| Reste de l'Amérique du Sud | ||
| Moyen-Orient et Afrique | CCG | |
| Afrique du Sud | ||
| Reste du Moyen-Orient et de l'Afrique | ||
Questions clés répondues dans le rapport
Quelle sera la taille du marché du traitement du cancer gastrique d'ici 2030 ?
La taille du marché du traitement du cancer gastrique devrait atteindre 10,86 milliards USD d'ici 2030.
Quelle modalité thérapeutique croît le plus rapidement ?
L'immunothérapie mène avec un TCAC de 13,45 % jusqu'en 2030.
Où la demande régionale s'étend-elle le plus rapidement ?
L'Asie-Pacifique affiche le TCAC le plus élevé de 15,56 %, portée par la Chine, l'Inde et le Japon.
Quelle classe de médicaments commande actuellement la plus grande part ?
Les inhibiteurs PD-1/PD-L1 détenaient 20,23 % de part de marché en 2024.
À quel point les traitements oraux deviendront-ils significatifs ?
Les formulations orales devraient croître à un TCAC de 12,93 % alors que les soins à domicile gagnent en faveur.
Dernière mise à jour de la page le:



