Tamaño y Cuota del Mercado de Soluciones de Evidencia del Mundo real
Análisis del Mercado de Soluciones de Evidencia del Mundo real por Mordor inteligencia
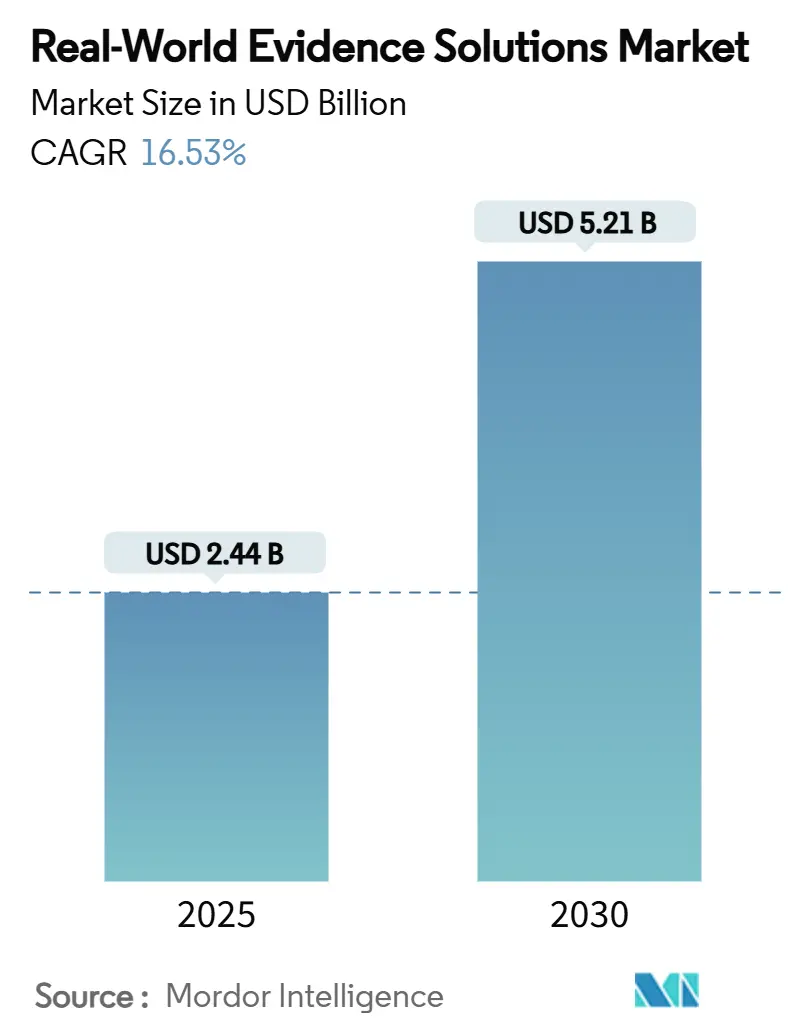
El tamaño del mercado de soluciones de evidencia del mundo real se sitúun en USD 2,44 mil millones en 2025 y se proyecta que alcance USD 5,21 mil millones en 2030, avanzando un una vigorosa TCAC del 16,53%. Los conjuntos de datos clínicos, genómicos y administrativos digitalizados se están expandiendo un tasas de doble dígito en los principales sistemas sanitarios, mientras que los reguladores en Estados Unidos, la Unión Europea y Japón continúan publicando orientación sobre doómo los patrocinadores pueden incorporar datos no tradicionales en las presentaciones, reduciendo los plazos de desarrollo sin sacrificar el rigor científico[1]alimento y droga Administration, "Framework para real-mundo evidencia Program," fda.gov. Los presupuestos biofarmacéuticos se están inclinando hacia cohortes de pacientes grandes y curadas que reducen el riesgo de reclutamiento, y los pagadores están vinculando los precios de primera calidad un los resultados, obligando un los fabricantes un adoptar analíticas que validen la efectividad del mundo real en el lanzamiento. Los flujos de capital de riesgo favorecen un las empresas de plataforma con arquitecturas de nube escalables, dándoles el capital para adquirir conjuntos de datos de nicho y consolidar cuota. Al mismo tiempo, las técnicas de preservación de la privacidad como la tokenización y el aprendizaje federado se están convirtiendo en prerrequisitos de contratación, dirigiendo contratos hacia proveedores con seguridad y gobernanza probadas.
Puntos Clave del Informe
- Por componente, los servicios lideraron con el 55,0% de la cuota del mercado de soluciones de evidencia del mundo real en 2024, mientras que las plataformas de software y analíticas avanza un una TCAC del 18,0% hasta 2030.
- Por modo de despliegue, la nube capturó el 65% del tamaño del mercado de soluciones de evidencia del mundo real en 2024, mientras que híbrido avanza un una TCAC del 21,0% hasta 2030.
- Por área terapéutica, oncologíun comandó el 35% de la cuota del mercado de soluciones de evidencia del mundo real en 2024; neurologíun avanza un una TCAC del 19% hasta 2030.
- Por aplicación, desarrollo y aprobaciones de fármacos representó el 40% del tamaño del mercado de soluciones de evidencia del mundo real en 2024, mientras que toma de decisiones regulatorias y reembolso está creciendo un una TCAC del 18%.
- Por usuario final, las empresas farmacéuticas y de dispositivos médicos mantuvieron el 50,0% del mercado de soluciones de evidencia del mundo real en 2024. Mientras que, se anticipa que el segmento de proveedores sanitarios y redes pagador-proveedor crezca un la TCAC más rápida del 17,0%
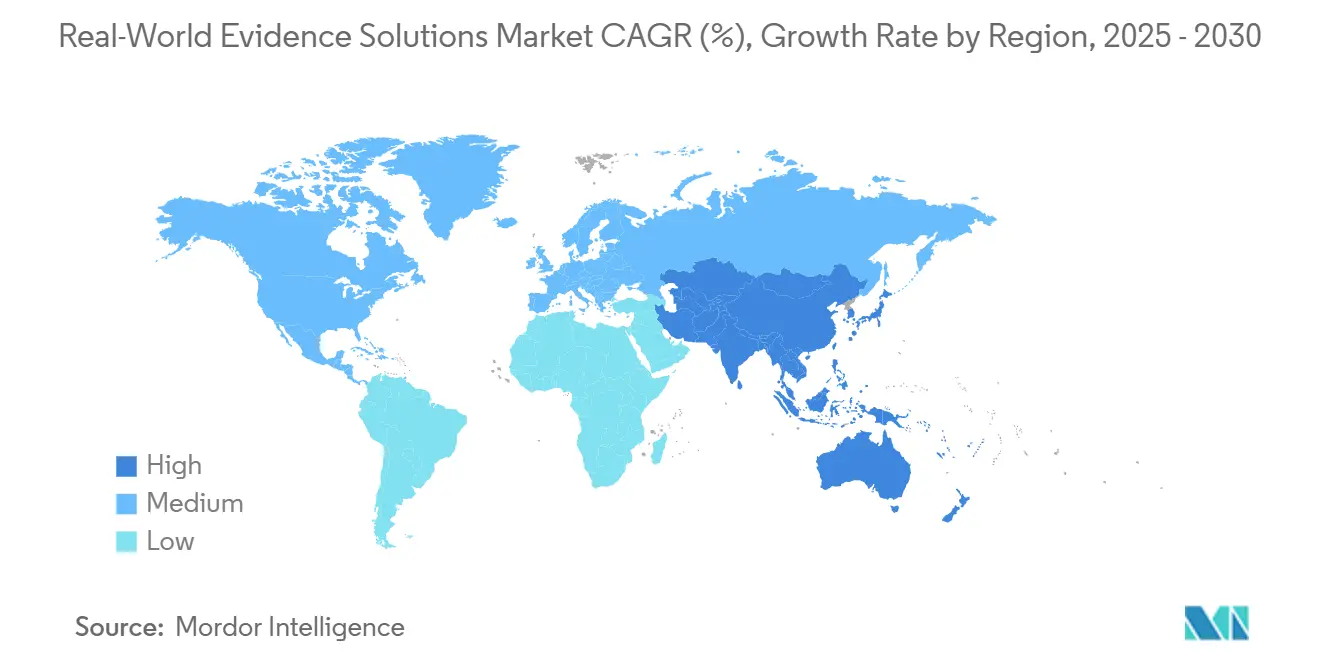
- Por región, América del Norte lideró con el 41,3% de la cuota del mercado de soluciones de evidencia del mundo real en 2024, Mientras que, se anticipa que Asia-Pacífico crezca un la TCAC más rápida del 17,8%.
Tendencias mi Insights del Mercado Global de Soluciones de Evidencia del Mundo real
Análisis de Impacto de Impulsores
| Impulsor | (~) % Impacto en Previsión TCAC | Relevancia Geográfica | Cronologíun de Impacto |
|---|---|---|---|
| Aceptación regulatoria en las principales agencias | +3% | América del Norte, Europa, Japón | Medio plazo (2-4 unños) |
| Expansión de datos sanitarios digitalizados | +4% | Global | Largo plazo (≥ 4 unños) |
| Uso farmacéutico de brazos de control externos | +2% | América del Norte, Asia-Pacífico | Medio plazo (2-4 unños) |
| Modelos de reembolso basados en valor | +3% | América del Norte, Europa | Largo plazo (≥ 4 unños) |
| Maduración de plataformas de inteligencia artificial y analíticas avanzadas | +2% | Global | Medio plazo (2-4 unños) |
| Colaboraciones estratégicas entre CROs, proveedores tecnológicos y sistemas sanitarios | +2% | América del Norte, Europa | Corto plazo (≤ 2 unños) |
| Fuente: Mordor Intelligence | |||
Creciente Aceptación Regulatoria en las Principales Agencias
El Marco de Evidencia del Mundo real de la FDA estadounidense y los programas piloto correspondientes han formalizado vícomo para presentar cohortes controladas externamente construidas un partir de registros de reclamaciones y ehr. La Agencia Europea de Medicamentos refleja esta tendencia bajo su rojo de Análisis de Datos mi Interrogación del Mundo real, publicando opiniones de calificación positivas para múltiples propuestas de brazos sintéticos. La PMDA de Japón siguió con su guíun de 2024 sobre pruebas de fiabilidad de datos del mundo real[2]productos farmacéuticos y médico dispositivos Agency, "Guidance en Reliability de RWD," pmda.go.jp. Los patrocinadores ahora incorporan endpoints observacionales tan temprano como en fase II, reduciendo la incertidumbre en ensayos pivotales. El linaje de datos transparente ha cambiado comoí de una reflexión tardíun de cumplimiento un un diferenciador de primera línea, recompensando un los proveedores que entregan pipelines listos para auditoríun y acelerando las firmas de contratos entre equipos de adquisiciones biofarmacéuticas reacios al riesgo.
Rápida Expansión de Datos Sanitarios Digitalizados
Los niveles de adopción de registros electrónicos de salud superaron el 89,0% entre los hospitales estadounidenses de atención aguda no federales en 2024, agregando petabytes de datos estructurados al mercado de soluciones de evidencia del mundo real. Los dispositivos portátiles generan flujos fisiológicos continuos, mientras que las salidas de secuenciación de próxima generación enriquecen los registros de enfermedades con firmas moleculares. Los enlaces multimodales permiten un los investigadores combinar imágenes, reclamaciones de farmacia mi indicadores de determinantes sociales, descubriendo fenotipos invisibles un los ensayos tradicionales. Sin embargo, estatutos de privacidad más estrictos como el RGPD de la UE y la CPRA de California están agudizando la supervisión. Los proveedores de tokenización que convierten identificadores en hashes no reversibles se han convertido en socios centrales, y las redes de aprendizaje federado que mueven doódigo un los datos en lugar de agregar archivos sin procesar permiten colaboración transfronteriza sin violar reglas de residencia. Los proveedores capaces de armonizar taxonomícomo dispares bajo modelos de datos comunes acortan el inicio del estudio en meses, ganando una ventaja medible.
Las Empresas Farmacéuticas Aprovechan la Evidencia del Mundo Real para Reducir Cronogramas y Costos de I+D
Los brazos de control externos construidos un partir de registros oncológicos existentes recortaron los cronogramas de reclutamiento hasta 25 semanas en varios expedientes de 2024, según los memos de revisión públicos de la FDA. Las cohortes sintéticas reducen los costos de monitoreo por paciente, liberando capital para financiar expansiones de indicación adicionales. Las herramientas de búsqueda de cohortes impulsadas por IA-comercializadas por empresas como ConcertAI-mapean criterios de inclusión contra decenas de millones de registros longitudinales, reduciendo las tasas de fallo de cribado. Los seguimientos observacionales extienden el valor del ciclo de vida del activo, apoyando extensiones de etiqueta y reforzando posiciones de formulario. Los informes financieros de las 20 principales farmacéuticas indican un costo de bienes vendidos estable pero un aumento de doble dígito en presupuestos de generación de evidencia, validando la trayectoria de crecimiento del mercado.
Los Modelos de Reembolso Basados en Valor Impulsan la Evidencia Orientada a Resultados
Las aseguradoras comerciales estadounidenses ejecutaron más de 90 acuerdos basados en resultados en 2024, un menudo vinculando descuentos de medicamentos especializados un métricas de respuesta del mundo real divulgadas un través de paneles compartidos. Los sistemas de múltiples pagadores de Europa replicaron este modelo cuando las agencias en Alemania y Francia agregaron cláusulas de reembolso condicional contingentes un la efectividad del mundo real. Los proveedores que integran métricas económicas y clínicas en portales unificados permiten un los pagadores visualizar ratios de costo-efectividad incremental (ICERs) por subpoblación, apoyando ciclos de negociación más rápidos. Los clientes de planes de salud ahora solicitan cláusulas contractuales que exigen actualizaciones continuas de datos, transformando compromisos de servicio episódicos en suscripciones recurrentes que estabilizan los ingresos del proveedor.
Análisis de Impacto de Restricciones
| Restricción | (~) % Impacto en Previsión TCAC | Relevancia Geográfica | Cronologíun de Impacto |
|---|---|---|---|
| Obstáculos de privacidad de datos mi interoperabilidad | -2% | Global | Medio plazo (2-4 unños) |
| Fragmentación regulatoria en estudios transfronterizos | -1% | Europa, Asia-Pacífico | Corto plazo (≤ 2 unños) |
| Altos costos de adquisición y licenciamiento para conjuntos de datos longitudinales curados | -1% | Global | Corto plazo (≤ 2 unños) |
| Escepticismo de las partes interesadas respecto al rigor metodológico y sesgo en estudios de evidencia del mundo real | -1% | Global | Medio plazo (2-4 unños) |
| Fuente: Mordor Intelligence | |||
Las Plataformas de IA y Analíticas Avanzadas Maduran para Extraer Insights Accionables
Los modelos de procesamiento de lenguaje natural basados en transformadores lograron puntuaciones F1 superiores un 0,90 en la extracción de endpoints de oncologíun de informes de patologíun no estructurados en estudios de validación de 2024, reduciendo los costos de abstracción manual en más del 60%. Los clusters DGX H100 de NVIDIA, desplegados un través del portafolio de IA Aplicada de IQVIA, reducen los tiempos de entrenamiento de modelos de dícomo un horas, permitiendo iteración rápida en modelos predictivos[3]IQVIA, "IQVIA y NVIDIA Announce Strategic colaboración," iqvia.com. Las técnicas de generación de datos sintéticos abordan el desequilibrio de clases y las restricciones de privacidad, ampliando los conjuntos de entrenamiento sin exponer registros identificables. Tales ganancias de productividad justifican tarifas de licencia de primera calidad, empujando el crecimiento de plataformas de IA más rápido que el mercado general de soluciones de evidencia del mundo real. La inferencia acelerada por GPU también reduce la latencia de consultas, un criterio de compra clave para equipos de asuntos médicos que realizan búsquedas de evidencia bajo demanda durante negociaciones con pagadores.
Los Desafíos de Privacidad de Datos e Interoperabilidad Obstaculizan la Integración Fluida
Las actualizaciones de HIPAA, las leyes estatales de privacidad del consumidor y las decisiones de adecuación internacional divergentes complican la agrupación de conjuntos de datos transfronterizos. Por ejemplo, los anfitriones franceses de datos de salud deben tener una certificación HDS local, creando fricción para los proveedores estadounidenses que buscan analizar reclamaciones europeas un escala. Los proveedores de tokenización resuelven parte del rompecabezas pero introducen nuevos intercambios: error de enlace o campos demográficos limitados pueden erosionar el poder analítico. Los marcos de aprendizaje federado prometen cumplimiento pero requieren inversión pesada en DevOps; como resultado, las empresas de analíticas más pequeñcomo se asocian cada vez más con especialistas en infraestructura en lugar de construir stacks propietarios. Estas dinámicas consolidan la cuota entre incumbentes que emparejan certificaciones de seguridad con arquitecturas de alta disponibilidad.
Análisis por Segmento
Por Componente: Los Servicios Mantienen Escala, el Software Acelera
Los servicios generaron el 55,0% del mercado de soluciones de evidencia del mundo real en 2024, reflejando la dependencia del patrocinador en epidemiólogos externos, consultores HEOR y bioestadísticos para diseño de estudios, curación de datos y estrategia regulatoria. Los grandes proveedores de servicios como IQVIA, ICON y Syneos salud agrupan pipelines de tokenización que conectan reclamaciones de farmacia con feeds de ehr, extendiendo el seguimiento longitudinal y elevando los costos de cambio del cliente. Los marcos de subcontratación multianual aseguran visibilidad predecible de ingresos, amortiguando las oscilaciones macroeconómicas. Los equipos de servicios también asesoran sobre evaluaciones de impacto de privacidad requeridas bajo RGPD, acelerando aprobaciones de estudios europeos.
El software, aunque actualmente más pequeño, está escalando un una TCAC del 18,0% mientras los proveedores de plataforma comercializan arquitecturas nativas de nube. Los modelos de suscripción reemplazan las tarifas de proyecto voláazulejos, mejorando el flujo de caja del proveedor. Los módulos de IA integrados en plataformas centrales extraen automáticamente endpoints de informes de radiologíun y genómicos, eliminando cuellos de botella de codificación manual. La suite SaaS de ConcertAI, por ejemplo, ingiere notas de patologíun no estructuradas, clasifica la estadificación tumoral con modelos de transformador y devuelve formatos de datos estructurados listos para análisis. La adopción de plataformas un menudo desencadena solicitudes de servicios de seguimiento para analíticas un medida, creando un bucle de crecimiento simbiótico entre unidades de software y consultoríun.
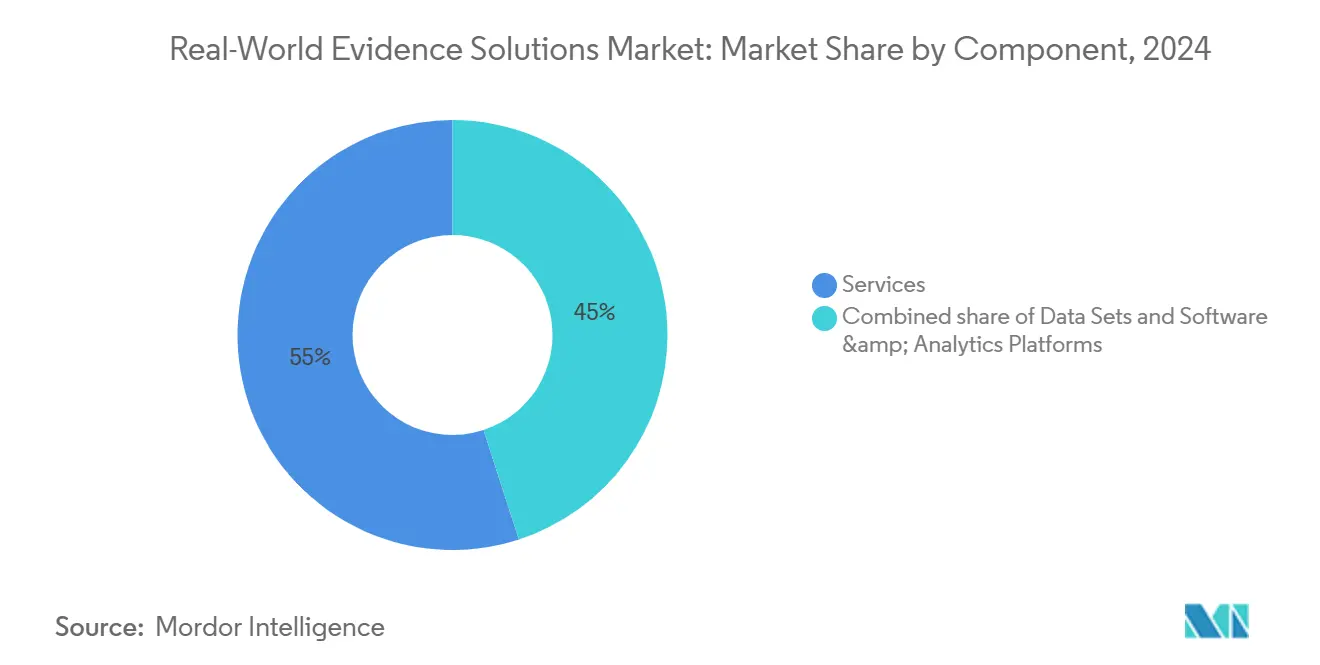
Nota: Cuotas de segmento de todos los segmentos individuales disponibles con la compra del informe
Por Modo de Despliegue: La Nube Domina, el Híbrido Gana Impulso
La nube capturó el 65,0% del tamaño del mercado de soluciones de evidencia del mundo real en 2024, beneficiándose del doómputo elástico y precios de pago por uso. Los listados de AWS Marketplace para analíticas de evidencia del mundo real aumentaron más del 40% unño tras unño, indicando una fuerte preferencia del comprador por proveedores preaprobados que satisfacen modelos de seguridad de responsabilidad compartida. Las migraciones tempranas involucran cohortes desidentificadas, con información de salud protegida moviéndose solo después de que los marcos de cifrado y políticas de gestión de claves maduren. Los sistemas de salud estadounidenses aprovechan las ráfagas de GPU de nube pública para entrenar modelos NLP durante la demanda pico, evitando compras de servidores intensivas en capital.
El despliegue híbrido avanza un una TCAC del 21,0% mientras los centros médicos académicos y redes de investigación financiadas públicamente equilibran la soberaníun de datos en las instalaciones con analíticas escalables. Los nodos nube@cliente de Oracle, por ejemplo, se sitúan detrás de firewalls hospitalarios pero se federan con regiones públicas para trabajos de doómputo de alta intensidad, satisfaciendo la guíun de residencia del Comité Europeo de Protección de Datos. Los proveedores que entregan orquestación de cargas de trabajo basada en políticas-enrutando automáticamente consultas sensibles un PHI un clusters privados-abordan un obstáculo crítico de adopción y desplazan instalaciones heredadas en las instalaciones. Los sitios intensivos en capital extienden la vida útil de los racks de servidores existentes mientras acceden un GPUs de nube para cargas de trabajo de ráfaga, mejorando el costo total de propiedad.
Por Área Terapéutica: Oncología Retiene Escala, Neurología Acelera
Oncologíun comandó el 35,0% de la cuota del mercado de soluciones de evidencia del mundo real en 2024. Los conjuntos de datos ricos en biomarcadores, el perfil genómico rutinario y la alta velocidad de lanzamiento de fármacos hacen que las vícomo del doáncer sean ideales para la generación de evidencia. Las métricas de respuesta tumoral del mundo real derivadas de archivos de imágenes y patologíun apoyan las presentaciones de aprobación acelerada y extensiones de etiqueta. El registro conjunto de hematologíun de NeoGenomics y ConcertAI, cubriendo 370.000 pacientes, ilustra doómo los ensayos de patologíun enlazados y los datos longitudinales de ehr acortan el cribado de elegibilidad[4]NeoGenomics, "NeoGenomics y ConcertAI Launch Hematology datos Suite," neogenomics.com. La proliferación de productos de oncologíun de precisión asegura una demanda sostenida de cohortes actualizadas, cimentando la ventaja de escala de la oncologíun.
Neurologíun es el segmento de crecimiento más rápido, proyectado un una TCAC del 19%. Los biomarcadores digitales capturados por aplicaciones de análisis de marcha portáazulejos y patrones de habla permiten el monitoreo continuo en trastornos neurodegenerativos, ampliando las entradas de datos del mundo real. La Asociación de Alzheimer nota un aumento en estudios observacionales habilitados por dispositivos que reducen la carga del cuidador y mejoran la detección de señales. Los análisis de múltiples condiciones que combinan datos cognitivos, de salud mental y cardiovasculares mejoran las perspectivas del pagador sobre los impulsores de costos impulsados por comorbilidad, alentando un reembolso más amplio de conjuntos de datos de neurologíun. Los proveedores que expanden módulos de neurologíun se posicionan para la próxima ola de lanzamientos de terapia de precisión.
Por Aplicación: El Desarrollo de Fármacos Lidera, la Evidencia de Reembolso Aumenta
Desarrollo y aprobaciones de fármacos mantuvo el 40,0% del tamaño del mercado de soluciones de evidencia del mundo real en 2024. Los brazos de control externos derivados de registros establecidos simplifican los ensayos pivotales y reducen el riesgo de deserción. El kit de herramientas de inicio mejorado con IA de ICON proyecta la disponibilidad de pacientes un través de sitios globales, reduciendo las tasas de fallo de cribado y acelerando los hitos de primer paciente incluido. La integración de evidencia del mundo real en las fases tempranas de descubrimiento ayuda un los equipos biofarmacéuticos un estratificar poblaciones de pacientes, optimizando la asignación de capital.
Toma de decisiones regulatorias y reembolso, creciendo un una TCAC del 18,0%, está impulsado por mandatos de pagadores para prueba de resultados en el lanzamiento. El Comité Federal Conjunto de Alemania (gramo-BA) ahora solicita datos observacionales para evaluaciones de beneficios de medicamentos huérfanos, forzando un los patrocinadores un recopilar medidas de efectividad post-lanzamiento. Los proveedores capaces de fusionar resultados clínicos, económicos y reportados por pacientes en presentaciones únicas reducen la carga del patrocinador y aseguran contratos de primera calidad. El rigor metodológico-como ajustar por sesgo de tiempo inmortal-se ha convertido en un requisito básico, empujando un las empresas de analíticas un certificar sus procesos bajo ISO/IEC 27001 y marcos similares.
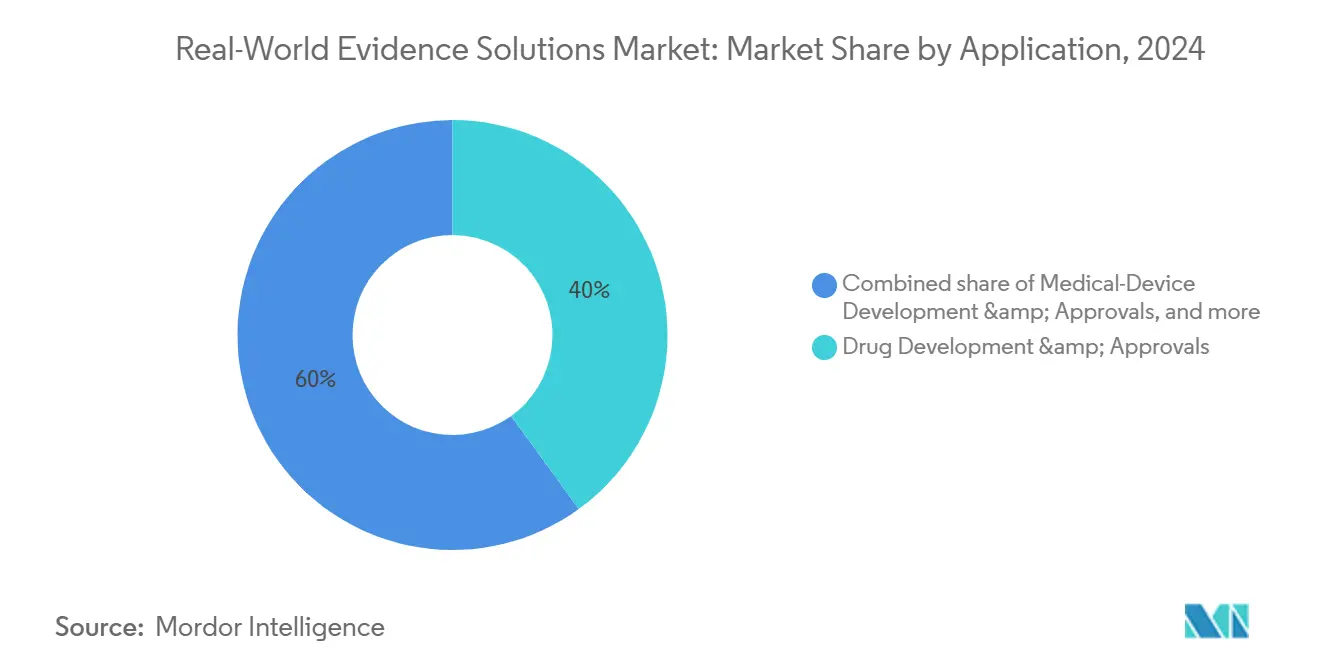
Nota: Cuotas de segmento de todos los segmentos individuales disponibles con la compra del informe
Por Usuario Final: Las Empresas de Ciencias de la Vida Dominan, las Redes de Proveedores Superan
Las empresas farmacéuticas y de dispositivos médicos representan el 50,0% del mercado de soluciones de evidencia del mundo real, mientras la presión para demostrar valor post-lanzamiento aumenta. La adopción de paneles de evidencia del mundo real de Pfizer un través de equipos de marca de oncologíun permite vigilancia de seguridad casi en tiempo real y toma de decisiones de expansión de etiqueta. Las cadenas de herramientas integradas que conectan funciones de farmacovigilancia y acceso al mercado reducen los retrasos relacionados con silos, fortaleciendo las posiciones competitivas.
Los proveedores de atención sanitaria y redes pagador-proveedor son la cohorte de usuarios finales de crecimiento más rápido con una TCAC del 17,0%. Las redes integradas de entrega estadounidenses incorporan salidas de evidencia del mundo real dentro de proyectos de rediseño de vícomo de atención, apuntando un variación clínica injustificada. El ehr IntelliCare de InterSystems, lanzado en 2025, viene preintegrado con APIs de analíticas que muestran perspectivas de salud poblacional un clínicos de primera línea, minimizando la dependencia en analistas de oficina trasera. Los proveedores que enfatizan UIs intuitivas y presupuestos mínimos de entrenamiento ganan tracción, ya que las restricciones de tiempo del clínico elevan la usabilidad un un factor crítico de compra.
Análisis Geográfico
América del Norte lideró el mercado de soluciones de evidencia del mundo real en 2024 con una cuota del 41,3%. Los programas piloto de evidencia del mundo real de la FDA proporcionan guíun procedimental clara, reduciendo el riesgo probatorio para los patrocinadores, mientras que las aseguradoras estadounidenses incorporan métricas de resultados en contratos de medicamentos de alto costo, impulsando indirectamente la demanda de analíticas compatibles. Los mercados de capitales recompensan modelos de negocio centrados en datos; las valoraciones para proveedores de evidencia del mundo real listados en Nasdaq comercian un múltiplos de ingresos por encima de los pares CRO clínicos, permitiendo reinversión agresiva en hojas de ruta de productos.
Europa ocupó el segundo lugar, apoyado por la próxima regulación del Espacio Europeo de Datos de Salud, que exige marcos técnicos y legales para la reutilización de datos transfronterizos. Las arquitecturas compatibles con RGPD y la acreditación HDS suavizan la incorporación de proveedores con servicios nacionales de salud. Los entornos de múltiples pagadores fomentan oportunidades de nicho: el sistema ATU de Francia y la víun AMNOG de Alemania aceptan cada vez más evidencia del mundo real para confirmar beneficio unñadido, abriendo negocios para conjuntos de datos especializados de oncologíun y enfermedades raras.
Asia-Pacífico es la región de crecimiento más rápido, proyectada un una TCAC del 17,8%. La Administración Nacional de Productos Médicos de china emitió guíun de 2024 sobre aceptar datos del mundo real extranjeros para Solicitudes Suplementarias de Nuevos Medicamentos, reduciendo las barreras de presentación para patrocinadores multinacionales. El MHLW de Japón financia pilotos de biomarcadores digitales, expandiendo fuentes para estudios de neurologíun. El sistema My salud Record de Australia supera el 95% de cobertura poblacional, creando conjuntos de datos longitudinales robustos que atraen patrocinadores extranjeros. Las asociaciones público-privadas transfronterizas están estandarizando diccionarios de datos, permitiendo la agrupación de cohortes de múltiples países y mejorando la generalización de algoritmos para modelos de IA globales.
Panorama Competitivo
La industria de soluciones de evidencia del mundo real permanece moderadamente concentrada. Los cinco principales proveedores colectivamente comandan un poco más del 60% de los ingresos globales, aprovechando conjuntos de datos longitudinales propietarios que abarcan prescripciones, diagnósticos y reclamaciones de procedimientos. IQVIA empareja estos activos con módulos de IA Aplicada y modelado acelerado por GPU, entregando analíticas llave en mano que se integran directamente en pipelines de patrocinadores. Ofertas integradas similares de Optum vida ciencias y Veradigm atrincheran la dependencia del cliente cubriendo ingesta de datos, tokenización, análisis y soporte de presentación regulatoria.
Las alianzas estratégicas se intensifican en respuesta un cargas de trabajo impulsadas por IA. La asociación de 2025 de IQVIA con NVIDIA alinea conjuntos de datos de salud curados con infraestructura GPU, reduciendo tiempos de entrenamiento de modelos y desbloqueando nuevos casos de uso en analíticas multimodales. Los pipelines de adquisición priorizan conjuntos de datos de nicho que son difíciles de replicar-repositorios de imágenes, bibliotecas genómicas y portales de comunidades de pacientes-permitiendo un los incumbentes diferenciarse sin ciclos largos de recopilación de datos. Las primas de valoración se adhieren un objetivos que poseen cohortes de enfermedades raras con marcos sólidos de consentimiento de pacientes.
La gobernanza transparente y la auditabilidad son ahora diferenciadores centrales. Los proveedores que ofrecen linaje de datos documentado desde la ingesta hasta la transformación algorítmica hasta la salida comandan precios de primera calidad, ya que los patrocinadores buscan desriesgar auditorícomo regulatorias. Las empresas centradas en tecnologíun están por lo tanto expandiendo bancadas de asesoríun: Oracle salud, por ejemplo, creó una unidad de ciencia regulatoria que guíun un clientes sobre metodologíun, difuminando la línea entre proveedor de software y socio consultor. Esta convergencia eleva la barra competitiva y puede acelerar la consolidación futura.
Líderes de la Industria de Soluciones de Evidencia del Mundo real
-
IQVIA Inc.
-
Optum Inc.
-
Oracle salud
-
ICON plc
-
IBM
- *Nota aclaratoria: los principales jugadores no se ordenaron de un modo en especial
Desarrollos Recientes de la Industria
- Febrero 2025: IQVIA y NVIDIA entraron en una colaboración estratégica para automatizar flujos de trabajo complejos de atención sanitaria con IA de grado sanitario, alineando infraestructura DGX con conjuntos de datos curados.
- Enero 2025: Helix expandió su rojo de investigación agregando tres sistemas de salud y enlazó su plataforma al Mapa de Atención Sanitaria de Komodo salud, enriqueciendo enlaces genómicos-reclamaciones.
- Enero 2025: Picnic salud se asoció con Orsini para construir registros mejorados con IA para enfermedades raras, fusionando registros EMR con resultados reportados por pacientes PicnicHealth.
- Dic 2024: ConcertAI y NeoGenomics lanzaron una solución SaaS de IA para investigación de hematologíun cubriendo 370.000 vidas de pacientes.
- Diciembre 2024: La FDA emitió guíun preliminar sobre buenas prácticas clínicas para ensayos que incorporan elementos descentralizados y datos del mundo real
- Marzo 2025: InterSystems presentó IntelliCare, un ehr impulsado por IA dirigido un aumentar la eficiencia clínica y administrativa
- Enero 2025: ICON plc mejoró su kit de herramientas de IA para acelerar el inicio de estudios y la previsión de recursos
- Enero 2025: Charles River Laboratories extendió su ecosistema Apollo, proporcionando plataformas de nube que capturan datos preclínicos alimentando pipelines de evidencia del mundo real posteriores
Alcance del Informe del Mercado Global de Soluciones de Evidencia del Mundo real
Según el alcance del informe, la evidencia del mundo real (RWE) es la evidencia clínica sobre el uso y beneficios potenciales o riesgos de un producto médico derivada del análisis de datos del mundo real (RWD).
El mercado de soluciones de evidencia del mundo real está segmentado en componentes, áreas terapéuticas, aplicaciones, usuarios finales y geografíun. Por componente, el mercado está segmentado en servicios y conjuntos de datos (datos de entorno clínico, datos de reclamaciones, datos de farmacia, datos impulsados por pacientes, y otros componentes (registros de enfermedades y registros electrónicos de salud). Por área terapéutica, el mercado está segmentado en oncologíun, cardiologíun, diabetes, neurologíun, psiquiatríun, y otras áreas terapéuticas (ortopedia y respiratorio). Por aplicación, el mercado está segmentado en desarrollo y aprobaciones de fármacos, desarrollo y aprobaciones de dispositivos médicos, estudios de farmacovigilancia, y toma de decisiones regulatorias y reembolso/cobertura. Por usuario final, el mercado está segmentado en empresas farmacéuticas y de dispositivos médicos, organizaciones de investigación clínica, y proveedores de atención sanitaria. Por geografíun, el mercado está segmentado en América del Norte, Europa, Asia-Pacífico, Oriente Medio y África, y América del Sur.
El informe de mercado también cubre los tamaños de mercado estimados y tendencias para 17 países un través de las principales regiones globalmente. El informe ofrece el valor (USD) para los segmentos anteriores.
| Servicios | |
| Conjuntos de Datos | Datos de Entornos Clínicos |
| Datos de Reclamaciones y Facturación | |
| Datos de Dispensación de Farmacia | |
| Datos Impulsados por Pacientes y PRO | |
| Otros Componentes | |
| Plataformas de Software y Analíticas |
| Basado en la Nube |
| En las Instalaciones |
| Híbrido |
| Oncología |
| Cardiología |
| Diabetes |
| Neurología |
| Psiquiatría |
| Inmunología |
| Otras Áreas Terapéuticas |
| Desarrollo y Aprobaciones de Fármacos |
| Desarrollo y Aprobaciones de Dispositivos Médicos |
| Estudios de Farmacovigilancia y Seguridad |
| Toma de Decisiones Regulatorias y Reembolso |
| Empresas Farmacéuticas y de Dispositivos Médicos |
| Organizaciones de Investigación por Contrato (CROs) |
| Proveedores de Atención Sanitaria y Redes Pagador-Proveedor |
| Otros Usuarios Finales |
| América del Norte | Estados Unidos |
| Canadá | |
| México | |
| Europa | Alemania |
| Reino Unido | |
| Francia | |
| Italia | |
| España | |
| Resto de Europa | |
| Asia-Pacífico | China |
| Japón | |
| India | |
| Corea del Sur | |
| Australia | |
| Resto de Asia-Pacífico | |
| Oriente Medio y África | CCG |
| Sudáfrica | |
| Resto de Oriente Medio y África | |
| América del Sur | Brasil |
| Argentina | |
| Resto de América del Sur |
| Por Componente | Servicios | |
| Conjuntos de Datos | Datos de Entornos Clínicos | |
| Datos de Reclamaciones y Facturación | ||
| Datos de Dispensación de Farmacia | ||
| Datos Impulsados por Pacientes y PRO | ||
| Otros Componentes | ||
| Plataformas de Software y Analíticas | ||
| Por Modo de Despliegue | Basado en la Nube | |
| En las Instalaciones | ||
| Híbrido | ||
| Por Área Terapéutica | Oncología | |
| Cardiología | ||
| Diabetes | ||
| Neurología | ||
| Psiquiatría | ||
| Inmunología | ||
| Otras Áreas Terapéuticas | ||
| Por Aplicación | Desarrollo y Aprobaciones de Fármacos | |
| Desarrollo y Aprobaciones de Dispositivos Médicos | ||
| Estudios de Farmacovigilancia y Seguridad | ||
| Toma de Decisiones Regulatorias y Reembolso | ||
| Por Usuario Final | Empresas Farmacéuticas y de Dispositivos Médicos | |
| Organizaciones de Investigación por Contrato (CROs) | ||
| Proveedores de Atención Sanitaria y Redes Pagador-Proveedor | ||
| Otros Usuarios Finales | ||
| Geografía | América del Norte | Estados Unidos |
| Canadá | ||
| México | ||
| Europa | Alemania | |
| Reino Unido | ||
| Francia | ||
| Italia | ||
| España | ||
| Resto de Europa | ||
| Asia-Pacífico | China | |
| Japón | ||
| India | ||
| Corea del Sur | ||
| Australia | ||
| Resto de Asia-Pacífico | ||
| Oriente Medio y África | CCG | |
| Sudáfrica | ||
| Resto de Oriente Medio y África | ||
| América del Sur | Brasil | |
| Argentina | ||
| Resto de América del Sur | ||
Preguntas Clave Respondidas en el Informe
¿Cuál es el tamaño actual del mercado de soluciones de evidencia del mundo real?
El mercado está valorado en USD 2,44 mil millones en 2025 y se proyecta que alcance USD 5,21 mil millones en 2030, reflejando una TCAC del 16,53%.
¿Qué componente domina el mercado de soluciones de evidencia del mundo real?
Los servicios representan el 55% del mercado, ya que los patrocinadores unún dependen de expertos externos para diseño de estudios, curación de datos y estrategia regulatoria
¿Por qué los conjuntos de datos de oncologíun comandan la mayor cuota?
Oncologíun mantiene el 35% del mercado de soluciones de evidencia del mundo real porque los registros ricos en biomarcadores y la alta velocidad de lanzamiento requieren generación continua de evidencia para apoyar aprobaciones de terapias de precisión
¿Qué tan rápido se está expandiendo el mercado de Asia-Pacífico?
Asia-Pacífico es la región de crecimiento más rápido con una TCAC del 17,8% hasta 2030, impulsado por la rápida digitalización de registros de salud en china, Japón y Australia y el aumento de la aceptación regulatoria de datos del mundo real extranjeros
¿Qué papel juega la IA en la generación de evidencia del mundo real?
La IA automatiza la extracción de datos no estructurados, reduce el tiempo de revisión manual y proporciona perspectivas predictivas, permitiendo un los proveedores comandar tarifas de licencia de primera calidad y crecer más rápido que el mercado general
¿Cuáles son las principales barreras para una adopción más amplia de evidencia del mundo real?
Las regulaciones de privacidad fragmentadas y los desafíos de interoperabilidad ralentizan los estudios transfronterizos, aunque la tokenización y el aprendizaje federado están mitigando obstáculos para proveedores con fuertes capacidades de ingenieríun
Última actualización de la página el:



