Marktgröße und Marktanteil für elektronische klinische Outcome-Assessment-Lösungen (ECOA)
Marktanalyse für elektronische klinische Outcome-Assessment-Lösungen (ECOA) von Mordor Intelligence
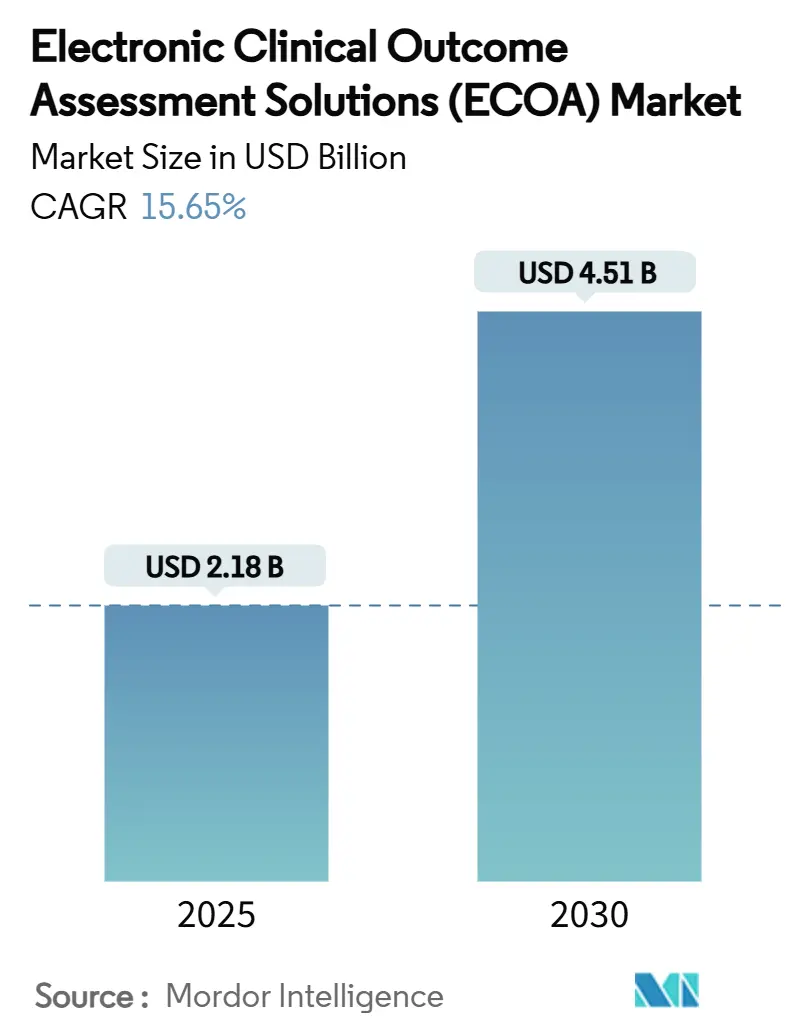
Die Marktgröße für elektronische klinische Outcome-Assessment-Lösungen beläuft sich 2025 auf 2,18 Milliarden USD und soll bis 2030 4,51 Milliarden USD erreichen, bei einer Wachstumsrate von 15,65% CAGR. Der verstärkte regulatorische Fokus auf patientenzentrierte Evidenz, die schnelle Migration zu cloud-nativen eClinical-Stacks und die weitverbreitete Einführung dezentraler Studienmodelle beschleunigen die Plattformnachfrage [1]Center for Drug Evaluation and Research, "Electronic Systems in Clinical Investigations," FDA.gov . Pharma-Sponsoren betrachten diese Systeme als primären Mechanismus zur Erfassung hochwertiger Daten zu patientenberichteten, klinikberichteten, beobachterberichteten und Leistungsendpunkten, die Kennzeichnung und Erstattung beeinflussen. Etablierte Anbieter erweitern kontinuierlich ihre Suiten durch Akquisitionen, während Nischenplayer sich durch KI-gestützte Entscheidungsunterstützung und integrierte Zahlungsfunktionen differenzieren. Schwellenmärkte bieten zusätzlichen Rückenwind durch Kostenvorteile, die multiregionale Studienausführung fördern.
Wichtige Erkenntnisse des Berichts
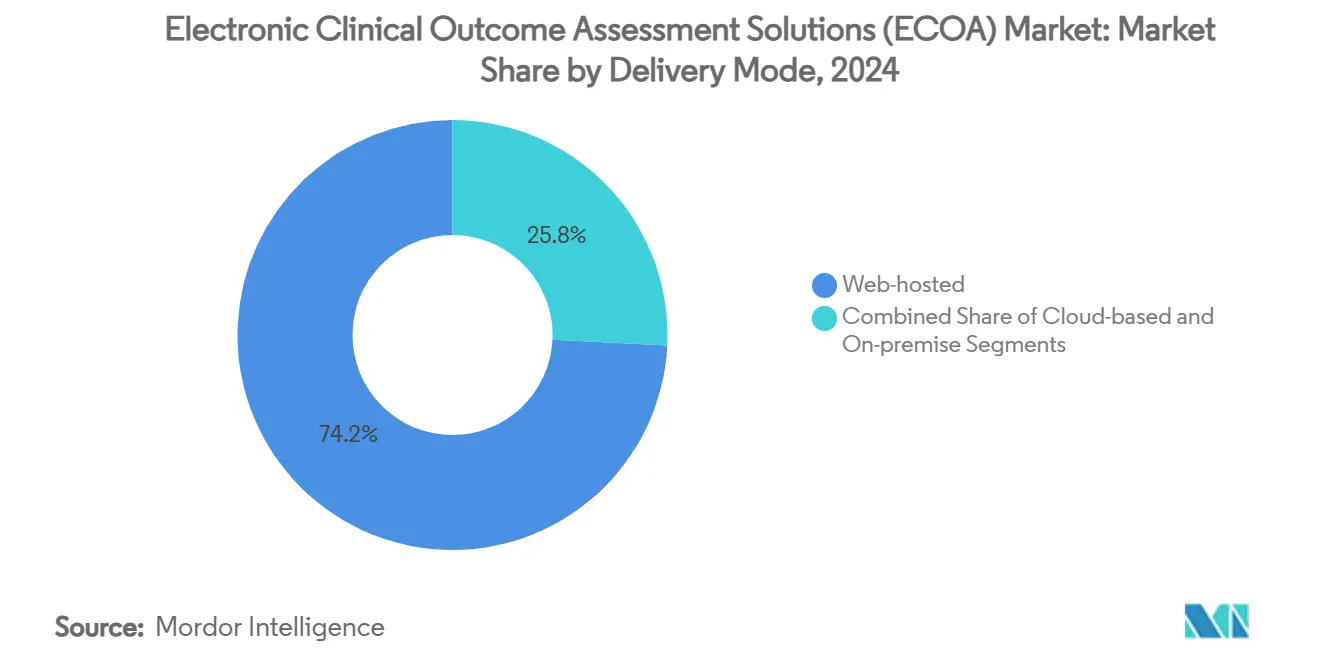
- Nach Bereitstellungsart führten webbasierte Lösungen 2024 mit 74,23% Umsatzanteil; cloudbasierte Plattformen werden voraussichtlich bis 2030 mit einer CAGR von 16,23% expandieren.
- Nach Ansatz erreichten patientenberichtete Endpunkte 48,98% des Marktanteils für elektronische klinische Outcome-Assessment-Lösungen im Jahr 2024; klinikberichtete Endpunkte wachsen mit einer CAGR von 16,34% bis 2030.
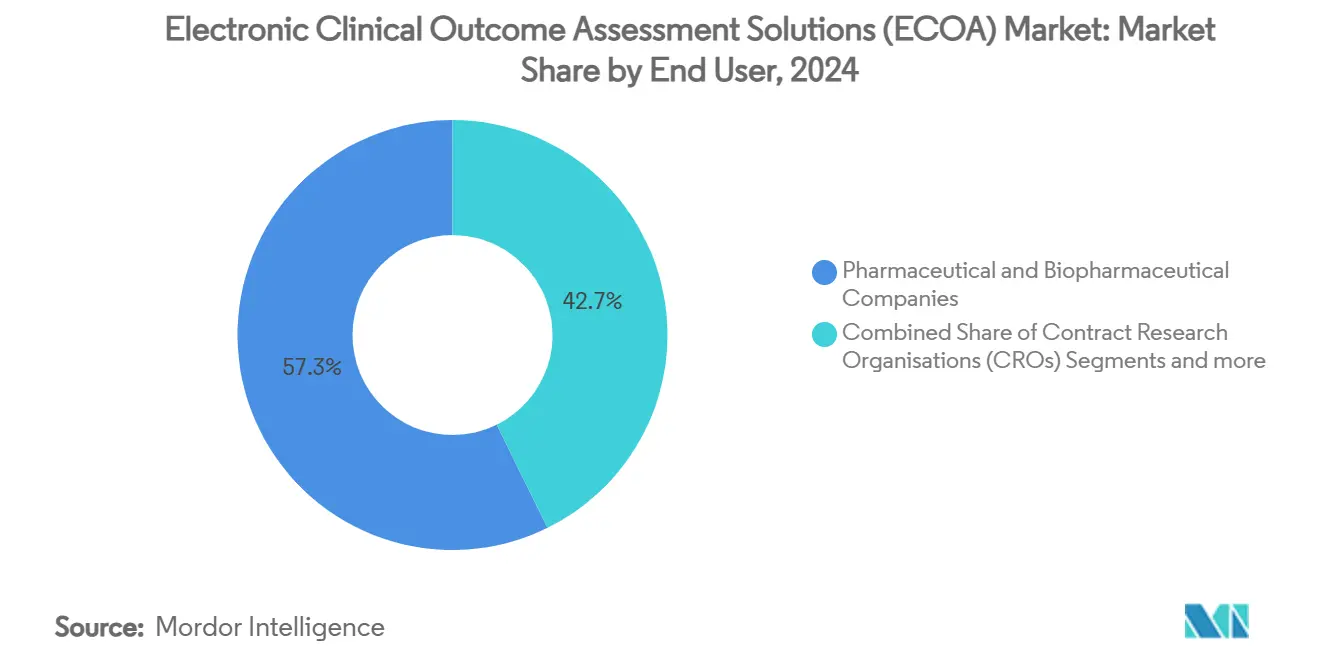
- Nach Endnutzer machten Pharmaunternehmen 57,29% der Marktgröße für elektronische klinische Outcome-Assessment-Lösungen im Jahr 2024 aus, während Auftragsforschungsorganisationen für ein CAGR-Wachstum von 16,31% bis 2030 positioniert sind.
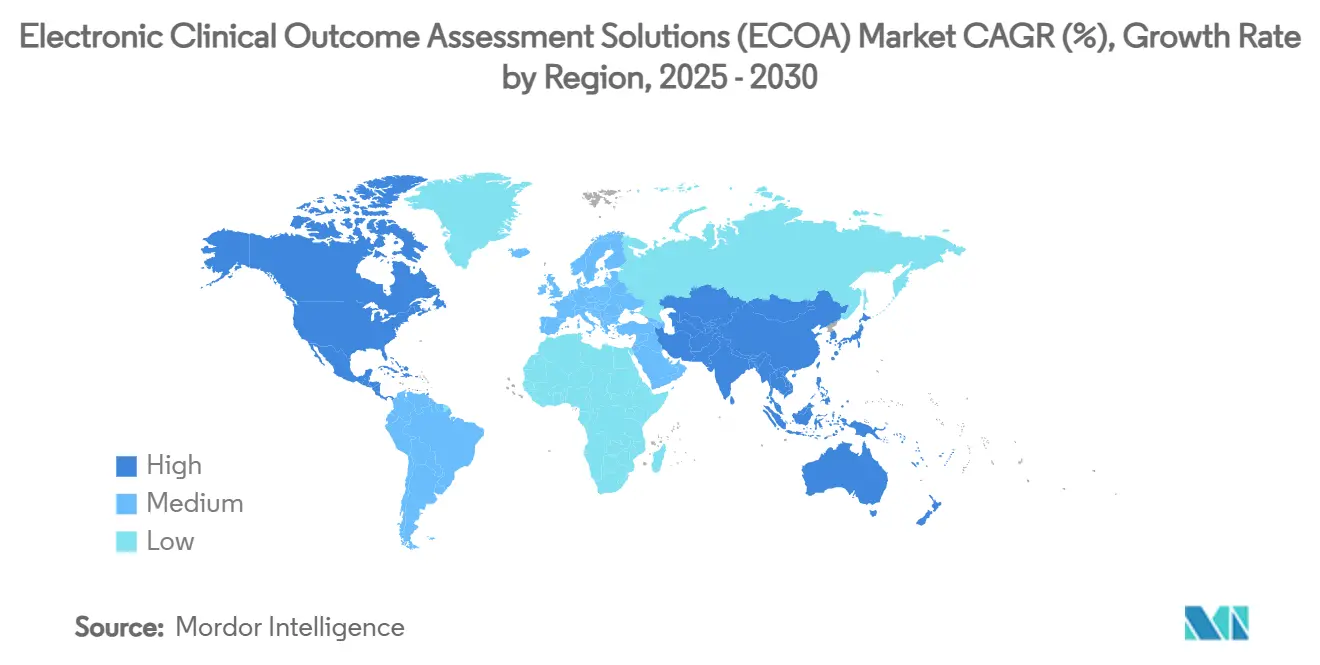
- Nach Geografie kommandierte Nordamerika 2024 einen Anteil von 42,21% der Marktgröße für elektronische klinische Outcome-Assessment-Lösungen, während Asien-Pazifik voraussichtlich die höchste regionale CAGR von 16,57% bis 2030 verzeichnen wird.
Globale Trends und Einblicke zum Markt für elektronische klinische Outcome-Assessment-Lösungen (ECOA)
Analyse der Treiber-Auswirkungen
| Treiber | (~) % Auswirkung auf CAGR-Prognose | Geografische Relevanz | Auswirkungszeitraum |
|---|---|---|---|
| Wachsende Auslagerung klinischer Studien durch Pharma- & Biotech-Sponsoren | +2.8% | Global, mit Konzentration in Nordamerika & Europa | Mittelfristig (2-4 Jahre) |
| Expansion cloudbasierter/SaaS-basierter eClinical-Stacks | +3.1% | Global, angeführt von Nordamerika, Expansion nach Asien-Pazifik | Kurzfristig (≤ 2 Jahre) |
| Regulatorischer Schub für patientenfokussierte Arzneimittelentwicklung | +2.5% | Global, mit FDA- und EMA-Führung | Langfristig (≥ 4 Jahre) |
| Beschleunigter Wechsel zu dezentralen & BYOD-Studienmodellen | +3.4% | Nordamerika & Europa als Kern, Übergriff nach Asien-Pazifik | Mittelfristig (2-4 Jahre) |
| BYOD-fähige Wearables senken Gerätekosten & steigern Compliance | +1.9% | Global, mit früher Einführung in entwickelten Märkten | Mittelfristig (2-4 Jahre) |
| KI-gestütztes Adherence-Coaching verbessert PRO-Datenqualität | +1.8% | Nordamerika & Europa, Expansion nach Asien-Pazifik | Langfristig (≥ 4 Jahre) |
| Quelle: Mordor Intelligence | |||
Wachsende Auslagerung klinischer Studien durch Pharma- & Biotech-Sponsoren
Auftragsforschungsorganisationen übernehmen einen wachsenden Anteil der Studienausführung, weil Sponsoren sich auf Kernentdeckungsaktivitäten konzentrieren. In den Vereinigten Staaten wird der biopharmazeutische CRO-Markt voraussichtlich bis 2033 19,75 Milliarden USD erreichen, ein Signal für anhaltenden Outsourcing-Appetit. CROs übernehmen nun schlüsselfertige Plattformen für elektronische klinische Outcome-Assessment-Lösungen und bieten Sponsoren vereinheitlichte Datenerfassung, Randomisierung und Patientenbetreuungsservices im großen Maßstab. Konsolidierung, exemplarisch durch die Fusion Suvoda-Greenphire, schafft integrierte Ökosysteme, die eCOA, Zahlungen und Supply-Chain-Funktionen umfassen [2]Suvoda LLC, Suvoda and Greenphire to merge creating a technology platform optimizing clinical trial processes and streamlining the patient journey,
suvoda.com. Post-pandemische Personalknappheit-die Fluktuationsraten von Clinical Research Associates übersteigen 25%-verstärken die Präferenz für externe Partner, die geschultes Personal für digitale Studien bereitstellen können [3]Grace Parrish, CRA Turnover Within Contract Research Organizations Post-COVID-19: A Cross-Sectional Study,
Clinical Researcher, acrpnet.org.
Expansion cloudbasierter/SaaS-basierter eClinical-Stacks
Cloud-Deployments übertreffen Legacy-webbasierte Modelle, da Sponsoren Elastizität, automatisierte Validierung und niedrigere Gesamtbetriebskosten anstreben. Die FDA-Leitlinie zur Computer Software Assurance unterstützt risikobasierte Verifikation und reduziert Hürden für Cloud-Adoption bei gleichzeitiger Wahrung der 21 CFR Part 11-Anforderungen. Große Anbieter wie Microsoft Azure erfüllen SOC 1-, SOC 2- und ISO/IEC 27001-Standards und geben Life-Science-Teams sofort einsatzbereite Sicherheitsframeworks. Spezialisierte Unternehmen wie USDM automatisieren Patch-Management und erhalten kontinuierliche Audit-Bereitschaft, was multiregionale Compliance für Sponsoren ermöglicht, die gleichzeitige Studien durchführen.
Regulatorischer Schub für patientenfokussierte Arzneimittelentwicklung
Das FDA-Programm zur patientenfokussierten Arzneimittelentwicklung schreibt die systematische Erfassung von Patientenerfahrungsmaßen während zentraler Studien vor und macht zweckgerechte eCOA-Plattformen unverzichtbar. Die Oktober 2024-Leitlinie zu patientenberichteten Kernergebnissen in der Onkologie liefert standardisierte Instrumentenvorlagen und reduziert Methodenqualifikationsunsicherheiten. Parallele EMA-Empfehlungen zu computerisierten Systemen schaffen transatlantische Ausrichtung, die Implementierungskomplexität für globale Studien senkt. Digitale Endpunktqualifikation-wie Schrittgeschwindigkeit bei Duchenne-Muskeldystrophie-illustriert die Offenheit der Regulatoren für neuartige Outcome-Maße, die von Echtzeit-Sensordaten abhängen.
Wandel hin zu dezentralen & BYOD-Studienmodellen
Dezentrale Designs erreichen 10% schnellere Rekrutierung und verbesserte demografische Vielfalt im Vergleich zu standortzentrierten Modellen. Die September 2024 FDA-Leitlinie klärt operative Erwartungen für Studien mit Hausbesuchen, Telemedizin und direktem Patienten-IMP-Versand und zementiert DCT-Legitimität. Bring-your-own-device-Strategien senken Bereitstellungskosten und erhöhen Adherence, weil Teilnehmer vertraute Smartphones nutzen, erfordern aber rigorose Äquivalenztests über Betriebssysteme hinweg. Regierungsunterstützung, belegt durch BARDAs fünfjährige Vereinbarung mit Allucent zum Skalieren dezentraler Infrastruktur, legitimiert das Modell weiter.
Analyse der Beschränkungen-Auswirkungen
| Beschränkung | (~) % Auswirkung auf CAGR-Prognose | Geografische Relevanz | Auswirkungszeitraum |
|---|---|---|---|
| Datensicherheits- & Datenschutzverletzungsbedenken | -1.7% | Global, mit verstärktem EU-Fokus unter DSGVO | Kurzfristig (≤ 2 Jahre) |
| Hohe Vorlaufimplementierungs- & Validierungskosten | -2.1% | Global, größere Auswirkung auf kleinere Biotech | Mittelfristig (2-4 Jahre) |
| Mangel an eCOA-qualifiziertem Personal im klinischen Betrieb | -1.4% | Primär Nordamerika & Europa | Mittelfristig (2-4 Jahre) |
| Geräteheterogenität gefährdet Messäquivalenz | -1.2% | Global, mit regulatorischem Fokus in entwickelten Märkten | Langfristig (≥ 4 Jahre) |
| Quelle: Mordor Intelligence | |||
Datensicherheits- und Datenschutzverletzungsbedenken
Die FDA verlangt nun eine Software-Stückliste für vernetzte Medizintechnologien und zwingt eCOA-Anbieter, robuste Schwachstellenüberwachungsprogramme zu unterhalten. Europas DSGVO fügt strikte Datenübertragungsbeschränkungen hinzu und zwingt Sponsoren, regionale Datenresidenz-Kontrollen und geschichtete Verschlüsselung einzusetzen. Durchsetzungsmaßnahmen-wie die FDA-Warnschreiben 2024 an Exer Labs-unterstreichen die finanziellen und reputativen Gefahren unzureichender Cybersicherheit. Steigende Kontrolle algorithmischer Transparenz führt dazu, dass 72% der Gesundheitsorganisationen staatliche Aufsicht über KI-gestützte prädiktive Modelle bevorzugen und Anbieter unter Druck setzen, Machine-Learning-Logik in verständlicher Sprache zu erklären.
Hohe Vorlaufimplementierungs- und Validierungskosten
Phase-III-Studien absorbieren bereits den Großteil der Entwicklungsbudgets, und die Validierung von eCOA-Software über Geräte, Sprachen und demografische Untergruppen hinweg fügt weitere Kosten hinzu. Das eCOA-Konsortium betont, dass sensorbasierte Datenströme zweckgerechte Bewertung durchlaufen müssen, was Projektzeitleisten verlängert. Wearable-Validierungsstudien offenbaren Inter-Site-Variabilität und verpflichten Sponsoren, umfangreiche Standardisierungs- und Überwachungsinfrastruktur zu finanzieren. Obwohl das Computer Software Assurance-Framework einige Papierlast reduziert, benötigen Sponsoren weiterhin spezialisierte Qualitätsingenieure und Statistiker-Ressourcen, die bei Frühphasen-Biotech-Unternehmen knapp sind.
Segmentanalyse
Nach Bereitstellungsart: Cloud-Migration gewinnt Dynamik
Webbasierte Deployments hielten 2024 74,23% des Marktanteils für elektronische klinische Outcome-Assessment-Lösungen, weil viele Sponsoren auf etablierte Rechenzentrumsverträge setzen. Die Vertrautheit des Modells und bewährte Audit-Bereitschaft erhalten kurzfristige Präferenz, besonders für Spätphasen-Portfolios, wo Kontinuität Innovation übertrifft. Jedoch expandieren cloud-native Plattformen mit 16,23% CAGR bis 2030, was das Streben der Sponsoren nach elastischer Kapazität, Echtzeit-Analytik und automatisierten regulatorischen Updates widerspiegelt. Microsoft Azures Sicherheitszertifikate und FDA-unterstützte risikobasierte Validierung schaffen Vertrauen, dass Cloud-Infrastruktur Datenintegritätsmandate erfüllen kann.
Sponsoren verlagern Arbeitslasten schrittweise, oft beginnend mit Früh- oder Beobachtungsstudien, bevor sie zentrale Studien migrieren, sobald interne Richtlinien reifen. Hybridarchitekturen, die Legacy-webbasierte Datenbanken an Cloud-Analytikservices anbinden, helfen Unternehmen, Übergangsrisiken zu managen. Infolgedessen werden Cloud-Lösungen voraussichtlich einen wachsenden Anteil der Marktgröße für elektronische klinische Outcome-Assessment-Lösungen erfassen, während On-Premise-Instanzen sich auf Nischenszenarios zurückziehen, die maximale Datenkontrolle erfordern, wie verteidigungsfinanzierte Infektionskrankheitsprojekte.
Notiz: Segmentanteile aller einzelnen Segmente verfügbar beim Berichtskauf
Nach Ansatz: PRO-Dominanz trifft auf ClinRO-Beschleunigung
Patientenberichtete Endpunkte machten 2024 48,98% der Marktgröße für elektronische klinische Outcome-Assessment-Lösungen aus, verankert durch langjährige FDA-Kennzeichnungspräzedenzfälle und patientenfokussierte Arzneimittelentwicklungspolitik. Klinikberichtete Endpunkte sind auf Kurs für 16,34% CAGR, angetrieben durch eingebettete eSource-Module, die Prüfärzte Scores direkt in elektronischen Patientenakten-Umgebungen eingeben lassen. Beobachterberichtete Maße behalten spezialisierten Einsatz in Pädiatrie und Demenz, während Leistungsendpunkte neben validierten digitalen Biomarkern steigen.
Natural Language Processing transformiert nun unstrukturierte narrative Felder in strukturierte ClinRO-Variablen und reduziert Zeitbelastung und Fehlerquoten für beschäftigte Ärzte. Signant Healths elektronische Kliniker-Rating-Module exemplifizieren, wie Entscheidungsunterstützungsaufforderungen Bewertung standardisieren bei gleichzeitiger Wahrung klinischer Nuancen. Da Wearable-Unternehmen zusätzliche digitale Biomarker qualifizieren-Ganggeschwindigkeit, Herzratenvariabilität-werden Leistungsendpunkte von explorativen Endpunkten zu co-primärem Status übergehen und die Nachfrage nach multimodalen eCOA-Suiten erweitern, die nahtlos Sensordaten aufnehmen.
Nach Endnutzer: CRO-Nachfrage übertrifft Sponsor-Investment
Pharma- und biopharmazeutische Unternehmen repräsentierten 2024 57,29% des Marktanteils für elektronische klinische Outcome-Assessment-Lösungen, was direkte Verantwortlichkeit für Zulassungsdatenintegrität widerspiegelt. Dennoch wachsen Auftragsforschungsorganisationen mit 16,31% CAGR und spiegeln die breitere Outsourcing-Welle wider, die Sponsoren operative Komplexität externalisieren sieht. Führende CROs bündeln eCOA-Fähigkeit mit Standortzahlungen, eConsent und Randomisierung, um vereinheitlichte digitale Studienblaupausen zu bieten. Die Suvoda-Greenphire-Fusion typisiert, wie Serviceanbieter komplementäre Assets kombinieren, um Studienstart-up und Prüfarztremuneration zu straffen.
Akademische medizinische Zentren und Regierungsbehörden, obwohl kleinere Verbraucher, fördern Innovation durch Pilotierung neuartiger digitaler Endpunkte in seltenen Krankheitskohorten, wo kommerzielle Anreize begrenzt sind. Das expandierende öffentlich-private Partnerschaftsmodell, unterstützt durch das NIH Decentralized Trial Innovation Network, führt Open-Source-Toolkits ein, die Adoptionshürden für ressourcenbeschränkte Institutionen senken und indirekt Expertise nähren, die später zu CRO- und Sponsor-Teams migriert.
Notiz: Segmentanteile aller einzelnen Segmente verfügbar beim Berichtskauf
Geografieanalyse
Nordamerika dominiert den Markt für elektronische klinische Outcome-Assessment-Lösungen mit 42,21% Anteil, angetrieben durch strenge aber klar definierte FDA-Regulierungen, anspruchsvolle klinische Forschungsinfrastruktur und frühe Einführung patientenzentrierter Metriken. Kontinuierliche FDA-Leitlinien, einschließlich des Computer Software Assurance-Frameworks, untermauern Sponsor-Vertrauen durch Klärung von Validierungserwartungen. Die Vereinigten Staaten machen den Großteil des regionalen Umsatzes aus, mit Kanadas Beitrag zu spezialisierten Tag-1-Zugriffsprogrammen für seltene Krankheiten und Mexikos kosteneffizienten Phase-I-Einheiten.
Asien-Pazifik verzeichnet die schnellste regionale Expansion mit 16,57% CAGR, was harmonisierte Studienpolitik, steigende inländische F&E-Investitionen und das Versprechen niedrigerer Pro-Patient-Kosten widerspiegelt. Chinas Straffung der klinischen Studien-Genehmigungszeitleisten, Indiens Digital-Health-Mission und Südkoreas Telemedizin-Pilotprojekte fördern kollektiv eine empfängliche Umgebung für dezentrale Studiendesigns, die robuste eCOA-Backbones erfordern. Dennoch erfordern divergierende Datenlokalisation-Politiken und Sprachkomplexität, dass Anbieter Multi-Tenant-Architekturen mit konfigurierbaren Souveränitätskontrollen liefern.
Europa, unterstützt durch EMA-Ausrichtung und nationale eHealth-Agenden, bleibt ein stabiler Adopter. Deutschlands Krankenhaus-Digitalisierungsbudget und die UK Medicines and Healthcare products Regulatory Agency Sandbox stimulieren die Aufnahme sensorgestützter Outcomes in Onkologie und Neurologie. Unterdessen drängen DSGVO-Compliance-Kosten kleinere Biotech zur Partnerschaft mit etablierten Anbietern, die vorab zertifizierte Hosting-Zonen halten und unterbrechungsfreien Fluss von Transaktionen im Markt für elektronische klinische Outcome-Assessment-Lösungen über den Kontinent gewährleisten.
Wettbewerbslandschaft
Der Markt zeigt moderate Konzentration. Medidata, Signant Health und Clario halten zusammen einen beträchtlichen Anteil, doch zahlreiche Mittelschicht- und aufkommende Anbieter nutzen Spezialnischen aus. Medidata erweitert ihre Führung durch Integration von eCOA in ihre einheitliche klinische Plattform und durch Start des Site Insights Program, das Site-Feedback in Studiendesign einfließen lässt. Signant Health kollaboriert mit IQVIA am One Home for Sites Framework und konsolidiert Prüfarztportale und elektronische Quelle zur Workflow-Effizienzverbesserung. Clario stärkte ihr Portfolio durch Akquisition von WCGs eCOA-Unit, erweiterte geografische Reichweite und vertiefte Expertise in komplexen Therapiebereichen.
Neue Marktteilnehmer differenzieren sich durch KI-Module. Kayentis analysiert Adherence-Muster für personalisierte Anstöße, während Medable Studio Drag-and-Drop-Konfiguration mehrsprachiger Instrumente zur Reduzierung der Build-Zeit ermöglicht. Oracle und Veeva Systems positionieren Unternehmens-Datenplätze, die operative und klinische Signale zusammenführen und Echtzeit-risikobasiertes Monitoring versprechen. Mittelgroße Player spezialisieren sich weiter: einige fokussieren auf pädiatrische Endpunkte, andere auf Integration hochfrequenter Wearable-Feeds.
Inmitten der Konsolidierung bleibt White-Space in ressourcenarmen Umgebungen, wo lokale Sprachunterstützung, Offline-Funktionalität und robuste Hardware essentiell sind. Anbieter, die diese Anforderungen erfüllen können, sind positioniert, zusätzliche Marktanteile für elektronische klinische Outcome-Assessment-Lösungen zu erfassen, da Sponsoren Studien nach Afrika und Lateinamerika ausdehnen.
Branchenführer für elektronische klinische Outcome-Assessment-Lösungen (ECOA)
-
Kayentis
-
IQVIA Inc.
-
Parexel International Corporation
-
Signant Health
-
WIRB-Copernicus Group
- *Haftungsausschluss: Hauptakteure in keiner bestimmten Reihenfolge sortiert
Aktuelle Branchenentwicklungen
- Mai 2025: Clario erwarb das elektronische klinische Outcome-Assessment-Geschäft von WCG und verstärkte seine Fähigkeit, umfassende Lösungen für globale Studien zu liefern.
- März 2025: Medidata Solutions startete das Site Insights Program zur Erhöhung des Site-Engagements und direkten Einbettung von Studiendesign-Feedback in seine einheitliche Plattform.
- Januar 2025: Suvoda und Greenphire kündigten eine Fusion an, um eine kombinierte klinische Studien-Technologie-Suite zu bilden, die Randomisierung, Supply-Management, eConsent, eCOA und Patientenzahlungen umfasst.
- August 2024: Medable führte Medable Studio ein, eine All-in-One-Umgebung zur Konfiguration und Validierung multikomponenter eCOA-Deployments.
Globaler Berichtsumfang für elektronische klinische Outcome-Assessment-Lösungen (ECOA)
Gemäß dem Umfang dieses Berichts nutzt elektronische klinische Outcome-Assessment (eCOA) Technologie wie Smartphones, Tablets und Computer, um Patienten, Pflegekräften und Ärzten zu ermöglichen, die Ergebnisse klinischer Studien direkt zu berichten. eCOA produziert hochpräzise Daten, die ein besseres Verständnis der Patientenerfahrung in klinischen Studien ermöglichen und letztendlich dabei helfen, den Weg zur Zulassung zu vereinfachen.
Der Markt für elektronische klinische Outcome-Assessment-Lösungen (eCOA) ist nach Bereitstellungsart, Ansatz, Endnutzer und Geografie segmentiert. Nach Bereitstellungsart ist der Markt in webbasiert und cloudbasiert segmentiert. Nach Ansatz ist der Markt nach patientenberichteten Endpunkten (PRO), klinikberichteten Endpunkten (ClinRO), beobachterberichteten Endpunkten (ObsRO) und Leistungsendpunkten (PerfO) segmentiert. Nach Endnutzer ist der Markt in Pharma- und biopharmazeutische Unternehmen, Auftragsforschungsorganisationen und andere Endnutzer segmentiert. Nach Geografie ist der Markt in Nordamerika, Europa, Asien-Pazifik, Naher Osten und Afrika sowie Südamerika segmentiert. Der Marktbericht deckt auch die geschätzten Marktgrößen und Trends für 17 verschiedene Länder in wichtigen Regionen weltweit ab. Der Bericht bietet den Wert (in USD) für die oben genannten Segmente.
| Webbasiert |
| Cloudbasiert |
| On-Premise |
| Patientenberichtete Endpunkte (PRO) |
| Klinikberichtete Endpunkte (ClinRO) |
| Beobachterberichtete Endpunkte (ObsRO) |
| Leistungsendpunkte (PerfO) |
| Pharma- und biopharmazeutische Unternehmen |
| Auftragsforschungsorganisationen (CROs) |
| Sonstige |
| Nordamerika | Vereinigte Staaten |
| Kanada | |
| Mexiko | |
| Europa | Deutschland |
| Vereinigtes Königreich | |
| Frankreich | |
| Italien | |
| Spanien | |
| Übriges Europa | |
| Asien-Pazifik | China |
| Japan | |
| Indien | |
| Australien | |
| Südkorea | |
| Übriger Asien-Pazifik | |
| Naher Osten und Afrika | GCC |
| Südafrika | |
| Übriger Naher Osten und Afrika | |
| Südamerika | Brasilien |
| Argentinien | |
| Übriges Südamerika |
| Nach Bereitstellungsart | Webbasiert | |
| Cloudbasiert | ||
| On-Premise | ||
| Nach Ansatz | Patientenberichtete Endpunkte (PRO) | |
| Klinikberichtete Endpunkte (ClinRO) | ||
| Beobachterberichtete Endpunkte (ObsRO) | ||
| Leistungsendpunkte (PerfO) | ||
| Nach Endnutzer | Pharma- und biopharmazeutische Unternehmen | |
| Auftragsforschungsorganisationen (CROs) | ||
| Sonstige | ||
| Nach Geografie | Nordamerika | Vereinigte Staaten |
| Kanada | ||
| Mexiko | ||
| Europa | Deutschland | |
| Vereinigtes Königreich | ||
| Frankreich | ||
| Italien | ||
| Spanien | ||
| Übriges Europa | ||
| Asien-Pazifik | China | |
| Japan | ||
| Indien | ||
| Australien | ||
| Südkorea | ||
| Übriger Asien-Pazifik | ||
| Naher Osten und Afrika | GCC | |
| Südafrika | ||
| Übriger Naher Osten und Afrika | ||
| Südamerika | Brasilien | |
| Argentinien | ||
| Übriges Südamerika | ||
Im Bericht beantwortete Schlüsselfragen
Was treibt die starke CAGR im Markt für elektronische klinische Outcome-Assessment-Lösungen?
Expansion dezentraler Studien, regulatorische Mandate für patientenfokussierte Evidenz und beschleunigte Cloud-Adoption untermauern kollektiv eine 15,65% CAGR bis 2030.
Welche Bereitstellungsart wächst am schnellsten?
Cloudbasierte Plattformen wachsen mit 16,23% CAGR und übertreffen webbasierte und On-Premise-Modelle, da Sponsoren skalierbare, compliance-bereite Infrastruktur suchen.
Warum gewinnen CROs Marktanteile für elektronische klinische Outcome-Assessment-Lösungen?
Sponsoren lagern Studienausführung an CROs aus, um Personalknappheit zu kompensieren und spezialisierte digitale Expertise zu nutzen, was 16,31% CAGR für CRO-Adoption befeuert.
Welche Region bietet die größte Wachstumschance?
Asien-Pazifik wird voraussichtlich 16,57% CAGR verzeichnen, geholfen durch regulatorische Harmonisierung und kosteneffiziente Patientenrekrutierung.
Was sind die Hauptbarrieren für breitere Plattform-Adoption?
Datensicherheitsbedenken unter strengen Datenschutzregimen und hohe Validierungskosten bleiben Schlüsselhindernisse, besonders für kleinere Biotechnologie-Unternehmen.
Wie beeinflusst künstliche Intelligenz die Plattform-Differenzierung?
Anbieter integrieren Machine-Learning-Module für Adherence-Coaching, Outcome-Vorhersage und automatisierte Datenqualitätsprüfungen und erhöhen den Wert für Sponsoren und Sites.
Seite zuletzt aktualisiert am:



