脂質レギュレーター市場規模とシェア
Mordor Intelligenceによる脂質レギュレーター市場分析
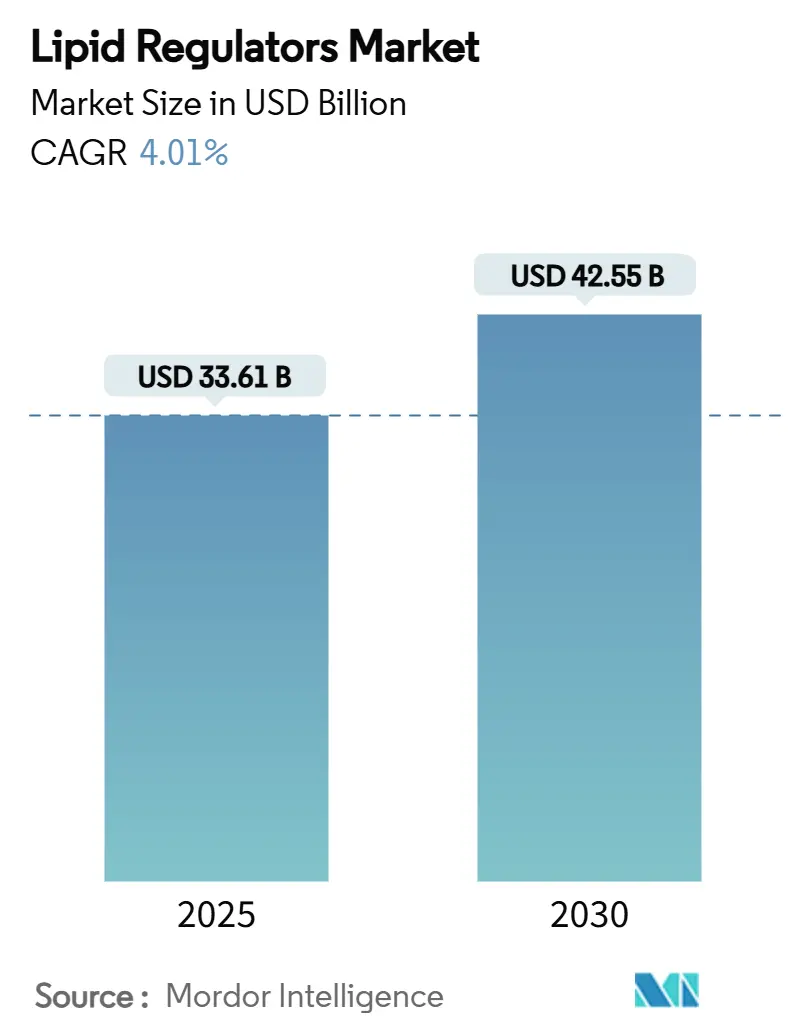
脂質レギュレーター市場規模は2025年に336億1,000万米ドルに達し、2030年には425億5,000万米ドルまで成長すると予測され、年平均成長率は4.01%となる。この統制された拡大は、スタチン系薬剤の特許切れ後の安定化を反映し、RNA干渉や経口PCSK9阻害薬などの精密治療薬への移行を示している。需要は世界的な心血管疾患負担の拡大に支えられており、高LDLコレステロールは2021年に381万人の死亡に寄与した。併用療法の受け入れ拡大、新興経済国での検診イニシアチブの拡張、高リスク患者への先進薬剤に対する支払者の償還意欲がさらなる推進力を強化している。同時に、デジタル服薬支援プラットフォームと遠隔モニタリングプログラムが継続性を向上させ、実世界での転帰を改善し、製造業者の安定した収益成長を支援している。
主要レポートハイライト
- 薬剤クラス別では、スタチン系が2024年の脂質レギュレーター市場シェアの46.54%を維持する一方、PCSK9阻害薬は2030年まで最速の年平均成長率6.78%を記録した。
- 患者タイプ別では、原発性高コレステロール血症が2024年の脂質レギュレーター市場規模の38.54%を占め、高トリグリセリド血症は最も急速な年平均成長率6.65%を記録した。
- 投与経路別では、経口剤形が2024年の脂質レギュレーター市場規模の55.32%のシェアを獲得し、生体内遺伝子治療は2030年まで年平均成長率7.54%で加速すると予測される。
- 流通チャネル別では、病院薬局が2024年に57.89%の収益シェアを保持し、オンライン薬局は年平均成長率7.89%で最も速く拡大した。
- 地域別では、北米が2024年に43.12%の収益シェアを保持し、アジア太平洋地域は予測期間中に年平均成長率5.43%で成長すると予測される。
世界の脂質レギュレーター市場トレンドと洞察
ドライバー影響分析
| ドライバー | 年平均成長率予測への影響(%) | 地理的関連性 | 影響時期 |
|---|---|---|---|
| 心血管疾患負担の拡大 | +1.2% | 北米・欧州が主導 | 長期(4年以上) |
| 併用脂質低下療法の採用拡大 | +0.8% | 北米・EU、APAC地域に拡張 | 中期(2~4年) |
| 長時間作用型RNAiと経口PCSK9阻害薬の革新 | +1.1% | 世界、北米主導 | 中期(2~4年) |
| 高リスク集団への償還適用拡大 | +0.7% | 北米・EUの中核市場 | 短期(2年以内) |
| 予防検診プログラムの拡大 | +0.5% | APAC中核、MEAへの波及 | 長期(4年以上) |
| デジタル服薬支援ツールの統合拡大 | +0.4% | 世界、北米での早期採用 | 中期(2~4年) |
| 情報源: Mordor Intelligence | |||
心血管疾患負担の拡大
心血管疾患は2025年に1億2,790万人のアメリカ人に影響し、動脈硬化性イベントが年間4,223億米ドルの経済コストを引き起こしている[1]American Heart Association, "Heart Disease and Stroke Statistics 2025 Update," heart.org。高LDLコレステロールは最も修正可能なリスクファクターであり続け、15億人以上の成人の対処可能な世界人口を生み出している。高所得国の人口高齢化とアジアの急速な都市化が組み合わさって発症率を押し上げている。その結果、医療制度は予防的脂質管理への注力を強化し、脂質レギュレーター市場の持続的な数量成長を確保している。地域診療所での検診を助成する多部門連携がさらに治療対象者を拡大し、長期的な処方需要を支えている。
併用脂質低下療法の採用拡大
TANDEMなどの臨床試験では、オビセトラピブとエゼチミブの併用でプラセボと比較してLDLコレステロールが48.6%低下することが実証された。配合剤は服薬負担を軽減し、服薬遵守率を向上させ、特に家族性高コレステロール血症に対して医師がより早期に二剤併用療法を開始することを促進している。2024年のガイドライン改訂では、超高リスク患者のLDLコレステロール目標値を55mg/dL未満として導入し、採用を加速した。これに対応して、企業はNexlizetなどの製品を発売し、リスク軽減のためのFDA承認拡大を獲得した。段階的エスカレーションから精密併用への移行は、治療患者あたりの収益を拡大し、脂質レギュレーター市場でのブランドロイヤルティを強化している。
長時間作用型RNAiと経口PCSK9阻害薬の革新
インクリシランは年2回の注射で約50%のLDLコレステロール低下を達成する[2]U.S. Food and Drug Administration, "Inclisiran Prescribing Information," fda.gov。ゼルラシランなどの新興siRNA薬剤は中期試験でリポタンパク質(a)を80%以上削減した[3]American College of Cardiology, "Zerlasiran First-in-Human Results," acc.org。一方、AstraZenecaの経口PCSK9阻害薬AZD0780は第IIb相結果で50.7%のLDLコレステロール低下を示した。これらのモダリティは注射疲労を克服し、専門医と一般診療医の両方の処方を拡大する。安全性データが蓄積されるにつれ、長時間作用型RNAiと便利な経口薬剤は、ニッチな高リスクコホートから主流の脂質異常症管理へと移行し、脂質レギュレーター市場を拡大すると予想される。
高リスク集団への償還適用拡大
2024年のMedicareによるWegovy心血管リスク軽減への償還決定は、予防的脂質療法のより広範な支払者受入への道を開いた。CLEAR Outcomes試験はベンペド酸の主要イベント13%減少を確認し、米国の適格人口を約7,000万人の成人に拡大するFDAラベル拡張を促した。欧州の医療技術機関も費用対効果に基づいてインクリシランを承認した。適用範囲の改善は患者の自己負担費用を圧縮し、処方を刺激し、先進療法の高い表示価格を相殺し、脂質レギュレーター市場規模を直接押し上げる。
制約要因影響分析
| 制約要因影響分析 | 年平均成長率予測への影響(%) | 地理的関連性 | 影響時期 |
|---|---|---|---|
| スタチン系分野でのジェネリック競争激化 | −0.9% | 世界、新興市場で最も深刻 | 短期(2年以内) |
| 新規生物製剤の高い治療費 | −0.6% | 世界、特にLMIC(低中所得国)のアクセスに影響 | 長期(4年以上) |
| 低・中所得国での限定的アクセス | −0.7% | MEA、南米、APAC地域の一部のLMIC | 長期(4年以上) |
| 核酸治療薬の製造複雑性 | −0.5% | 世界、分散生産地域への影響が深刻 | 中期(2~4年) |
| 情報源: Mordor Intelligence | |||
スタチン系分野でのジェネリック競争激化
特許期限切れにより、低コスト生産者にかなりのシェアを譲り、価格を圧迫し、ブランド収益を侵食している。多くの国家処方集は、先進薬承認前にジェネリックスタチン試用を義務付ける段階療法プロトコルを実施している。新興市場では、積極的な入札がさらに利幅を狭めている。製造業者はスタチンをエゼチミブやベンペド酸と組み合わせることで対抗しているが、競争の激しさは予測期間中の脂質レギュレーター市場全体の成長を依然として抑制している。
新規生物製剤の高い治療費
PCSK9モノクローナル抗体での年間療法は約14,000米ドル近くに留まり、100米ドル未満のジェネリックスタチン療法を大幅に上回っている。RNA系製品は専門製造とコールドチェーン物流を必要とし、コスト削減レバーを制限している。高所得地域では支払者適用は改善されているが、低・中所得国での手頃な価格は遅れており、かなりの人口が治療不足のままで、脂質レギュレーター市場の普遍的浸透を制約している。
セグメント分析
薬剤クラス別:治療革新がプレミアム採用を牽引
スタチン系は2024年収益のほぼ半分に寄与したが、ジェネリック商品化の下でその成長は停滞している。ベンペド酸とエゼチミブなどの配合剤は、相加的有効性と利便性により差別化を図り、浸食を緩和している。PCSK9阻害薬は、心血管転帰エビデンスの蓄積と自己投与・経口製剤の登場により、年平均成長率6.78%で他を上回ると予測される。コレステロール吸収阻害薬は基盤アドオン薬剤としての関連性を維持している。一方、ATP-クエン酸リアーゼ阻害薬は2024年のFDAラベル拡張後、スタチン不耐性集団で牽引力を獲得している。リポタンパク質(a)を標的とするパイプライン参入者は、後期試験が終了すれば高リスク遺伝的サブセットの脂質レギュレーター市場規模を再構築する可能性がある。
継続的なR&D投資は、服薬遵守のボトルネックに対処する経口低分子化合物とより長時間作用型注射剤に焦点を当てている。開発者は、プレミアムコストを正当化するための転帰検証に対する支払者の主張を考慮し、堅固なエンドポイント試験を重視している。競合他社のポートフォリオが多様化するにつれ、耐容性を損なうことなく平均販売価格をさらに押し上げ、クラス横断的併用戦略が拡大している。
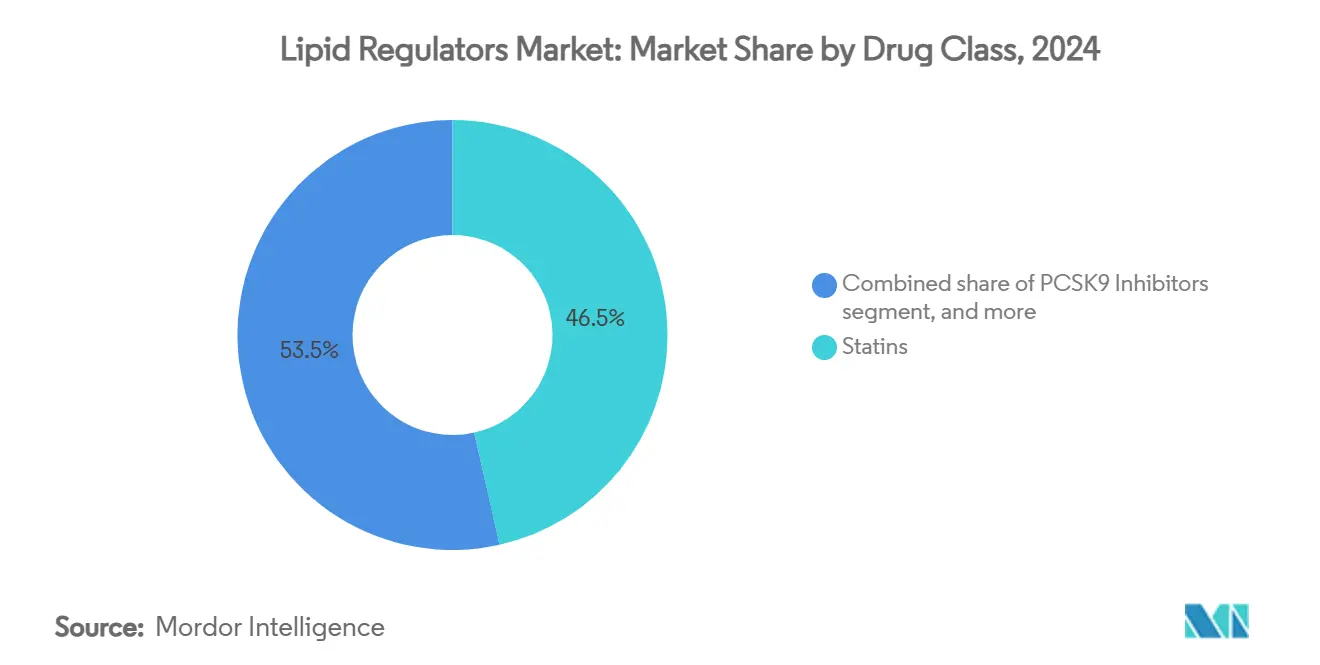
注記: すべての個別セグメントのシェアはレポート購入時に利用可能
患者タイプ別:リスク層別化が治療配分を推進
原発性高コレステロール血症は主要コホートであり続けたが、高トリグリセリド血症は臨床医が残存心血管リスクにおけるトリグリセリドの役割を認識するにつれ、最も急峻な年平均成長率6.65%を記録した。家族性高コレステロール血症集団、特にヘテロ接合体変異は、スタチンが効果不十分な場合にRNAiとPCSK9薬剤に引き寄せられる。ASCVD(動脈硬化性心血管疾患)イベント後の二次予防は、厳格なガイドライン目標により一貫した生物製剤需要を固める。糖尿病と肥満予防セグメントは、GLP-1心血管データに続いて拡大し、脂質低下ブランドのクロスセリング機会を開く。
多遺伝子リスクスコアリングを含む精密医療ツールは、患者をより細かく区分し、疾患連続体のより早期での治療エスカレーションを情報提供する。支払者が薬理遺伝学的検査を償還するにつれ、製造業者は医師への教育アウトリーチを調整し、ガイドライン準拠の処方を強化し、高リスククラスター内での脂質レギュレーター市場シェアを向上させる。
投与経路別:利便性が選好階層を形成
従来の経口錠剤は55.32%のシェアで優勢を維持し、患者の親しみやすさと広範な一般診療統合を反映している。注射用生物製剤は、強力なLDLコレステロール低下により心臓病学・内分泌学クリニックで強い採用を維持しているが、頻回投与は一部のコホートでの服薬遵守を制限している。年2回投与を必要とする長時間作用型RNAi療法はこの摩擦を部分的に解決し、一方で新興経口PCSK9分子は、効力と利便性を統合することで競争状況の再構築を約束している。
静脈内または脂質ナノ粒子を介して送達される遺伝子編集治療薬は、単回治療での生涯LDL低下を標的とする初期試験を通じて進歩している。安全性のハードルがクリアされれば、そのような一回限りのモダリティは慢性投与モデルを侵食し、支払者への治癒的魅力を提供することで脂質レギュレーター市場規模全体を拡大する可能性がある。
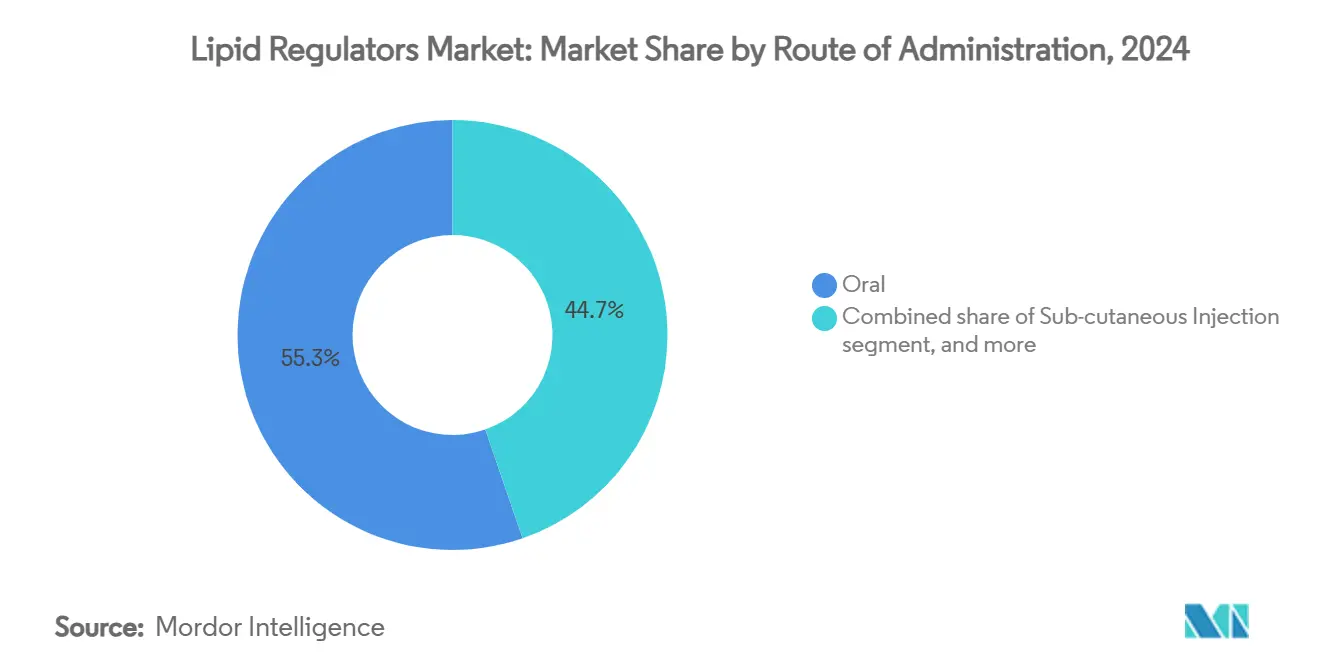
注記: すべての個別セグメントのシェアはレポート購入時に利用可能
流通チャネル別:デジタルプラットフォームが患者リーチを強化
病院薬局は、特にコールドチェーン依存型生物製剤について、売上の大部分を確保し続けた。小売チェーンは、薬剤師主導の脂質パネルとアルゴリズム処方を組み込んだ市販スタチンサービス提供を拡大している。オンライン薬局は、直接消費者向け遠隔診療と自動詰め替えに後押しされ、年平均成長率7.89%で急増した。専門クリニックは、遺伝カウンセリングと治療開始を統合し、家族性高コレステロール血症と複雑な脂質異常症の調整ハブとして登場した。
COVID時代の宅配への移行は、慢性薬物療法の郵送調剤を正常化した。リアルタイム服薬遵守分析と相まって、Eコマースプラットフォームは継続性を向上させ、従来の実店舗チャネルから脂質レギュレーター市場シェアのより大きな部分をシフトする可能性を保持している。
地域分析
北米は2024年収益の43.12%を占め、広範な保険適用、成熟した臨床試験エコシステム、デジタル服薬支援ツールの迅速な採用から恩恵を受けている。転帰ベース償還に対する強い支払者の重視は、長期コストオフセットモデルが信頼性を得るにつれ、生物製剤採用を加速している。事前承認の複雑性は依然として即座の成長を抑制しているが、合理化された電子給付確認システムが遅延を削減し、安定した需要を支えている。
欧州は、統一EMA承認と実証可能な心血管イベント削減を報いる厳格な医療技術評価に支えられた価値主導軌道を辿っている。強力なジェネリック浸透は基準治療費を下げ、高リスクコホート向けプレミアム薬剤への再投資を可能にしている。継続中のBrexit後規制再調整は一時的な発売ずれを生み出すが、国境を越えた参考価格設定は相対的手頃さを維持し、患者を表示価格変動から守っている。
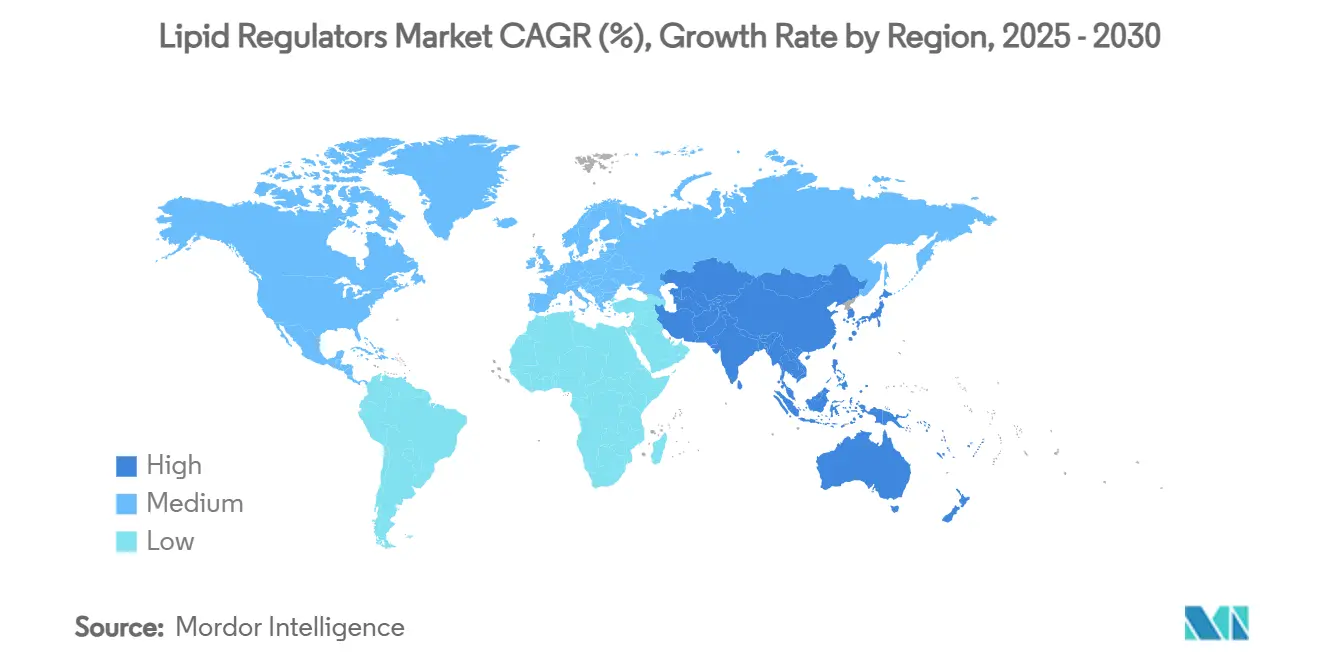
アジア太平洋地域は最も迅速な年平均成長率5.43%を記録し、都市心血管リスクの上昇、政策支援検診プログラム、拡大する中間層保険適用に刺激されている。現地ジェネリックスタチン生産は基準アクセスを確保するが、新規薬剤の手頃さギャップは持続している。進歩する規制調和は新規製品審査を迅速化し、国内企業との多国籍アライアンスは市場参入を促進している。中国の健康中国2030アジェンダとインドのアユシュマン・バーラト制度は、予防的カーディオメタボリックケアの公的資金封筒を拡大し、プレミアム脂質低下療法の対処可能ベースを広げると予想される。
南米、中東、アフリカは、ドナー支援必須医薬品イニシアチブを通じて段階的改善を目撃している。しかしながら、生物製剤採用は制約された予算と流通物流により制限されている。段階的価格設定モデルと地域製造パートナーシップの進歩は、これらの地域での意味ある浸透への前提条件となる可能性が高い。
競争環境
脂質レギュレーター市場は中程度の集中プロファイルを呈している。Novartisはインクリシランの年2回投与を活用してリーディングポジションを守り、Amgenはエボロクマブの堅固な転帰データと拡大する小児適応で推進している。AstraZenecaは経口PCSK9候補AZD0780を通じて差別化を図り、注射嫌悪患者の獲得を目指している。これら3社を合わせて2024年世界収益の35%弱を統制した。
戦略的コラボレーションがパイプライン多様化を加速している。Novartisは第二世代リポタンパク質(a)siRNA療法の共同開発のためIonisに6,000万米ドルを投資し、そのRNAポートフォリオを補完している。AstraZenecaの新規Lp(a)破壊薬でのCSPC Pharmaceuticalとの1億米ドル取引は、その脂質異常症フランチャイズを強化している。一方、Eli LillyのVerve Therapeutics買収は、一回限りLDL低下のための生体内塩基編集の最前線に同社を位置づけている。
NewAmsterdam PharmaとEsperion Therapeuticsを含む挑戦者バイオテック企業は、経口低分子プラットフォームを活用して利便性で注射競合を下回る価格設定を行っている。漸進参入者は、迅速な市場到達のために加速規制経路を使用し、同型接合体家族性高コレステロール血症などのニッチ適応を培養している。ポートフォリオが拡大するにつれ、クラス横断併用療法は中心的競争レバーとなり、治療患者あたりの総対処可能収益を押し上げている。
脂質レギュレーター業界リーダー
-
AstraZeneca
-
AbbVie Inc
-
Teva Pharmaceuticals
-
Pfizer, Inc.
-
AbbVie, Inc.
- *免責事項:主要選手の並び順不同
最近の業界動向
- 2025年6月:Eli Lillyは家族性高コレステロール血症を標的とする一回限りPCSK9遺伝子編集治療の推進のためVerve Therapeuticsを買収した。
- 2025年5月:HLS TherapeuticsはカナダでのNEXLETOLとNEXLIZETの商業化のため、100万米ドルの前払い合意でEsperionと提携した。
- 2025年4月:Novartisは適格患者ベースを拡大するV-MONO第III相インクリシラン単剤療法の陽性データを発表した。
- 2025年3月:AstraZenecaの経口PCSK9阻害薬AZD0780はPURSUIT第IIb相で50.7%のLDLコレステロール低下を達成した。
- 2024年3月:FDAは一次予防での心血管リスク軽減を含むベンペド酸ラベルを拡張した。
- 2024年10月:AstraZenecaはCSPCの低分子Lp(a)破壊薬YS2302018を1億米ドル前払いでライセンス取得した。
世界脂質レギュレーター市場レポート範囲
レポートの範囲に従い、脂質レギュレーターまたは脂質レギュレーターは脂質異常症、心血管疾患、骨粗鬆症、閉経後合併症の治療に使用される。このため、これらの脂質レギュレーターは最も処方される薬剤クラスに含まれる。脂質レギュレーター市場は種類別(スタチン系(ブランドスタチン、スタチン配合剤、ジェネリックスタチン)、非スタチン系(フィブリン酸誘導体、胆汁酸隔離剤、ニコチン酸誘導体、その他新製品))、地域別(北米、欧州、アジア太平洋、中東・アフリカ、南米)に区分される。レポートは世界の主要地域17カ国の推定市場規模とトレンドもカバーしている。レポートは上記セグメントの価値(百万米ドル)を提供している。
| スタチン系 | ブランドスタチン |
| ジェネリックスタチン | |
| 配合剤 | |
| PCSK9阻害薬 | mAbs(アリロクマブ、エボロクマブ) |
| siRNA(インクリシラン) | |
| 経口低分子PCSK9阻害薬 | |
| コレステロール吸収阻害薬(エゼチミブ) | |
| ベンペド酸・ACLY阻害薬 | |
| フィブリン酸誘導体 | |
| 胆汁酸隔離剤 | |
| オメガ3脂肪酸誘導体 | |
| ニコチン酸誘導体 | |
| リポタンパク質(a)標的薬剤 |
| 原発性高コレステロール血症 | ヘテロ接合体FH |
| 同型接合体FH | |
| 混合型脂質異常症 | |
| 高トリグリセリド血症(500mg/dL以上) | |
| ASCVD二次予防 | |
| 糖尿病・肥満予防ケア |
| 経口 |
| 皮下注射 |
| 静脈内 |
| 生体内遺伝子治療 |
| 病院薬局 |
| 小売薬局 |
| オンライン薬局 |
| 専門クリニック |
| 北米 | 米国 |
| カナダ | |
| メキシコ | |
| 欧州 | ドイツ |
| 英国 | |
| フランス | |
| イタリア | |
| スペイン | |
| その他欧州 | |
| アジア太平洋 | 中国 |
| 日本 | |
| インド | |
| オーストラリア | |
| 韓国 | |
| その他アジア太平洋 | |
| 中東・アフリカ | GCC |
| 南アフリカ | |
| その他中東・アフリカ | |
| 南米 | ブラジル |
| アルゼンチン | |
| その他南米 |
| 薬剤クラス別 | スタチン系 | ブランドスタチン |
| ジェネリックスタチン | ||
| 配合剤 | ||
| PCSK9阻害薬 | mAbs(アリロクマブ、エボロクマブ) | |
| siRNA(インクリシラン) | ||
| 経口低分子PCSK9阻害薬 | ||
| コレステロール吸収阻害薬(エゼチミブ) | ||
| ベンペド酸・ACLY阻害薬 | ||
| フィブリン酸誘導体 | ||
| 胆汁酸隔離剤 | ||
| オメガ3脂肪酸誘導体 | ||
| ニコチン酸誘導体 | ||
| リポタンパク質(a)標的薬剤 | ||
| 患者タイプ別 | 原発性高コレステロール血症 | ヘテロ接合体FH |
| 同型接合体FH | ||
| 混合型脂質異常症 | ||
| 高トリグリセリド血症(500mg/dL以上) | ||
| ASCVD二次予防 | ||
| 糖尿病・肥満予防ケア | ||
| 投与経路別 | 経口 | |
| 皮下注射 | ||
| 静脈内 | ||
| 生体内遺伝子治療 | ||
| 流通チャネル別 | 病院薬局 | |
| 小売薬局 | ||
| オンライン薬局 | ||
| 専門クリニック | ||
| 地域 | 北米 | 米国 |
| カナダ | ||
| メキシコ | ||
| 欧州 | ドイツ | |
| 英国 | ||
| フランス | ||
| イタリア | ||
| スペイン | ||
| その他欧州 | ||
| アジア太平洋 | 中国 | |
| 日本 | ||
| インド | ||
| オーストラリア | ||
| 韓国 | ||
| その他アジア太平洋 | ||
| 中東・アフリカ | GCC | |
| 南アフリカ | ||
| その他中東・アフリカ | ||
| 南米 | ブラジル | |
| アルゼンチン | ||
| その他南米 | ||
レポートで回答される主要質問
2025年から2030年の脂質レギュレーター市場の予測成長率は?
脂質レギュレーター市場は年平均成長率4.01%で拡大し、2025年の336億1,000万米ドルから2030年には425億5,000万米ドルに上昇すると予想される。
最も急成長している薬剤クラスは?
PCSK9阻害薬は、より強力な臨床エビデンスと新興経口製剤を反映し、2030年まで予測年平均成長率6.78%で最も急成長するクラスを代表している。
なぜ併用脂質低下療法が牽引力を得ているのか?
TANDEMなどの試験はより大きなLDLコレステロール低下と良好な服薬遵守を示し、高リスク患者での早期併用使用を好む更新ガイドラインを促している。
脂質管理においてデジタルツールはどのような役割を果たすか?
モバイル服薬支援アプリと遠隔モニタリングプログラムは平均24mg/dLのLDLコレステロール削減を実現し、継続性を支援し実世界転帰を改善している。
最も高い成長率を記録すると予想される地域は?
アジア太平洋地域は、特に中国とインドで検診プログラムが拡大し保険適用が拡大するにつれ、年平均成長率5.43%を記録すると予測される。
競争環境はどの程度集中しているか?
上位5社が世界収益の約50%を占め、革新的バイオテック参入者の機会を伴う中程度の集中を示している。
最終更新日:



