胃がん治療市場規模・シェア
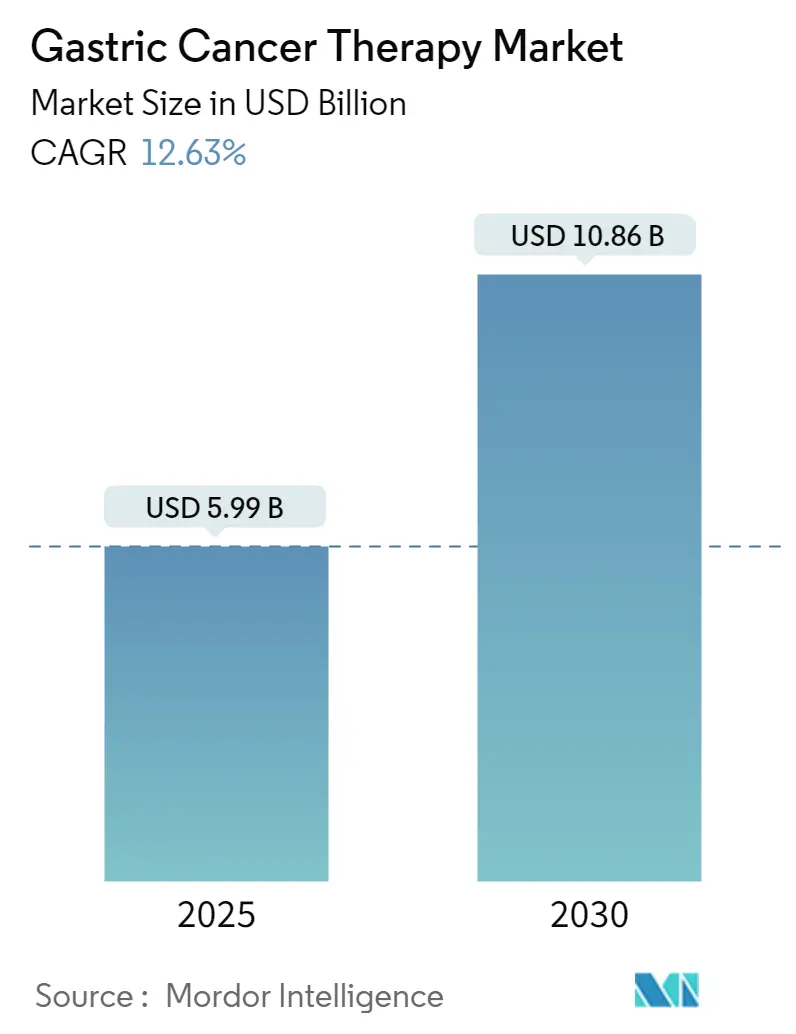
Mordor Intelligence による胃がん治療市場分析
胃がん治療市場規模は2025年に59億9000万米ドルに達し、予測期間を通じて堅調な年平均成長率12.63%により2030年までに108億6000万米ドルに達すると予測されており、全ての医療現場における旺盛な需要拡大を示しています。高齢化コホートにおける発症率の加速、免疫療法の急速な普及、より早期のバイオマーカー検査、中国の大量調達改革が合わさって、すべての主要地域で成長の勢いを支えています。人工知能支援内視鏡スクリーニングは検出を治癒可能なステージへと移行させており、コンパニオン診断は現在、転帰を改善し治療期間を延長する精密治療レジメンの拡大セットに情報を提供しています。2024年10月から2025年3月の間に5つの画期的承認が米国の認可を取得し、日本と欧州連合の並行ファストトラックシステムは後期段階候補のローンチタイムラインを短縮しており、イノベーターの収益可視性を強化しています。逆に、術後合併症の高コストと新興経済国でのバイオマーカー償還の不均一は依然として最適な治療に摩擦をもたらし、一部市場での高級薬の短期採用曲線を抑制しています。
主要レポートポイント
- 治療タイプ別では、化学療法が2024年に収益シェア42.19%でリードしており、免疫療法は2030年まで年平均成長率13.45%で進展する見込みです。
- 薬物クラス別では、PD-1/PD-L1阻害薬が2024年に胃がん治療市場シェアの20.23%を獲得し、FGFR2阻害薬は2030年まで年平均成長率12.55%で成長する見込みです。
- 疾患ステージ別では、再発例が2024年に胃がん治療市場規模の22.91%を占めており、早期ステージ(0-IA)疾患は2030年まで年平均成長率13.71%で拡大すると予測されています。
- 投与経路別では、静脈内投与が2024年に68.82%のシェアで支配的であり、経口製剤は同じ期間で年平均成長率12.93%で上昇すると予測されています。
- 地域別では、北米が2024年に収益シェア42.23%を生成し、アジア太平洋地域は2030年に向けて最速の年平均成長率15.56%を記録すると予想されています。
世界の胃がん治療市場トレンド・インサイト
推進要因インパクト分析
| 推進要因 | 年平均成長率予測への(〜)%インパクト | 地理的関連性 | インパクト期間 |
|---|---|---|---|
| 高齢化人口・ヘリコバクター・ピロリ菌有病率上昇 | +2.8% | 全世界、アジア太平洋・欧州に集中 | 長期(4年以上) |
| PD-1/PD-L1チェックポイント阻害薬の普及 | +1.9% | 北米・EU主導、APAC追随 | 中期(2-4年) |
| より早期のHER2陽性検査プロトコル | +1.2% | 全世界、先進国市場でより速い採用 | 中期(2-4年) |
| 中国の数量ベース調達価格下落 | +0.8% | 主に中国、他APAC市場への波及 | 短期(2年以下) |
| AI駆動内視鏡スクリーニングパイロット | +1.1% | 日本、韓国、ドイツが採用をリード | 中期(2-4年) |
| mRNA新抗原ワクチンパイプライン | +0.7% | 北米・EU臨床センター | 長期(4年以上) |
| 情報源: Mordor Intelligence | |||
高齢化人口・ヘリコバクター・ピロリ菌有病率上昇
人口の高齢化は残存するヘリコバクター・ピロリ菌感染と結びつき、ベースライン発症率を上昇傾向に保っており、特に除菌プログラムにもかかわらず歴史的暴露が持続する日本、韓国、中国、南欧では顕著です。東京の病院退院データベースでは、65歳以上の人々が新規胃がん診断の70%以上を占めており、腫瘍学クリニックに入ってくる需要の波を確認しています。寛解には長期間の集学的治療と頻繁な経過観察が必要であるため、高齢患者は通常、より高い累積薬物量を消費し、胃がん治療市場内で1症例当たりの生涯支出を膨張させる動態です。加えて、実世界分析では、老年医学毒性管理プロトコルが過去2年間で著しく改善され、臨床医が用量減少なしに全身レジメンをより長く維持できるようになり、チェックポイント阻害薬や分子標的薬の平均販売量を押し上げています。それでも支払者は、より大きな高齢コホートを治療する予算への影響に苦慮しており、支払いを複数年にわたる転帰に連結する成果ベース償還スキームへの移行を促しています。予防措置は拡大を続けていますが、その疫学的利益は徐々にしか実現されず、胃がん治療市場内で持続的な治療需要の長期滑走路を確保しています。
PD-1/PD-L1チェックポイント阻害薬の普及
2025年3月に承認されたペムブロリズマブ+トラスツズマブ+化学療法の一次治療採用は、無増悪生存期間中央値を7.3カ月から10.9カ月に向上させ、北米と欧州における一次治療アルゴリズムを変化させました。フランスとイタリアで提出された医療技術評価書類は、バイオマーカー陽性患者に使用される場合、薬剤が国の支払意思額閾値を下回る質調整生存年当たりの増分費用を示しており、処方集収載を推進し胃がん治療市場全体で収益成長を定着させています。同様に、デュルバルマブ併用の術前術後使用は、ASCO 2025で発表された無作為化試験で再発リスクを29%削減し、ガイドライン委員会に疾患経過のより早期での免疫調節を推奨させました。重要なことに、PD-L1スコアが低い患者における反応持続性は、チェックポイント阻害がトラスツズマブや細胞毒性薬剤と組み合わせられた場合に改善されており、統合第3相データによると治療可能コホートを最大3分の1拡大しています。
より早期のHER2陽性検査プロトコル
2024年7月の欧州連合によるVENTANA CLDN18 RxDxアッセイ承認は、単一の生検スライドからHER2、CLDN18.2、FGFR2、PD-L1を評価するパネルベース腫瘍プロファイリングへの移行を開始し、主要がんセンターで結果までの時間を5日未満に短縮しました。ドイツでの採用研究では、広範囲パネルが連続的な単一マーカー検査と比べて分子標的治療に対してフラグが立てられた患者の割合を倍増させ、トラスツズマブ デルクステカン、ゾルベツキシマブ、および今後のFGFR2阻害薬の対象可能量を拡大しました。首都圏ソウルの病院では、当日反射検査が分子病理学を初回診断ワークフローに組み込み、腫瘍医がバイオマーカーガイド治療レジメンを1治療サイクル早く開始できるようになり、根治意図症例で全生存期間を2-3カ月改善する可能性があります。早期同定は無効な化学療法への無駄な暴露も減らし、毒性関連支出を短縮し系統的検査拡大への支払者支援を強化します。新興市場が自動免疫組織化学プラットフォームで病理学ラボを改修するにつれ、胃がん治療市場は生の発症率だけでなく診断浸透によって駆動される症例数拡大の新しいレバーを獲得しています。
中国の数量ベース調達価格下落
2024年12月に締結された国家償還薬物リスト交渉の下で、主要胃がん腫瘍学ブランドの平均工場出荷価格は60-80%下落し、年間推定15万人の患者へのアクセスを拡大しました。メーカーは段階的価格戦略で対応しました:中国でのより低いマージンは保証された高ボリュームで相殺され、他の地域での価格設定は現在、成果ベース契約で中国調達を参照しています。実世界処方監査では、2025年前半2四半期の間に地方センターでのニボルマブとトラスツズマブ デルクステカンの病院使用が3倍以上成長し、単価浸食を補償し地域的に絶対収益利得を推進したことを確認しています。ベトナムやマレーシアなどの近隣諸国は同様の調達モデルの探索を開始しており、マージンを再形成する可能性があるがまた胃がん治療市場での患者リーチを拡大する大量規模パラダイムの潜在的拡散を示しています。
制約要因インパクト分析
| 制約要因 | 年平均成長率予測への(〜)%インパクト | 地理的関連性 | インパクト期間 |
|---|---|---|---|
| 術後合併症の高コスト | -1.4% | 全世界、新興市場でより顕著 | 中期(2-4年) |
| 第1級都市外での限定的バイオマーカー償還 | -0.9% | 中国、インド、他の新興APAC市場 | 短期(2年以下) |
| 中南米でのGI腫瘍専門医不足 | -0.7% | 中南米、他の新興地域への波及 | 長期(4年以上) |
| リポソーム製剤のサプライチェーン脆弱性 | -0.6% | 全世界、限定的コールドチェーンインフラを持つ地域で深刻 | 中期(2-4年) |
| 情報源: Mordor Intelligence | |||
術後合併症の高コスト
主要胃切除術合併症は症例の15-25%で発生し、再入院当たり15,000-25,000米ドルのコストがかかり、支払者に負担をかけ補助療法を遅らせ、影響を受けた患者の生存転帰を10-15%悪化させる可能性があります。ブラジル、南アフリカ、インドネシアの公立病院からのデータでは、合併症治療が入院腫瘍学予算の最大30%を吸収し、現代的全身薬剤のための資金を圧迫していることを示しています。術後回復強化と腹腔鏡アプローチは合併症率を高ボリュームセンターで10%近くまで削減していますが、ロボティクスへの資本支出は多くの中所得国にとって禁止的なままです。より広範な外科標準化が達成されるまで、支払者は高リスク候補者への高級補助薬剤への支出を制限する可能性があり、胃がん治療市場の一部で普及ポテンシャルを抑制します。機器メーカー、外科訓練機関、多国間貸手を含むコンソーシアムは、低侵襲プラットフォームへの参入障壁を下げるための成果ベース資金調達を探索していますが、具体的インパクトは数予算サイクルを要して現れます。
第1級都市外での限定的バイオマーカー償還
中国とインドでは、包括的次世代シーケンシングパネルはしばしば400米ドルを超え、大規模農村人口の月収を上回る金額であり、医師は多くのバイオマーカー陽性腫瘍に対して化学療法のみに頼ることを強いられています。中国の省保険者は通常、三次病院でのHER2免疫組織化学のみを償還し、CLDN18.2やFGFR2の検査は対象外のままで、ゾルベツキシマブやFGFR2阻害薬の適格性確認を制限します。インドの古い国家保健使命施設でも同様の格差が生じており、現金支払い診断コストが検査を阻害しています。結果として治療不平等が生じます:公表された登録データでは、バイオマーカーガイド治療浸透は第1級都市ハブ外では15%未満に留まり、精密薬剤の実世界フットプリントを制限しています。遠隔病理学とカートリッジベースPCRアッセイは最大60%のコスト削減を約束していますが、それらの拡大には開発中の規制調和とクラウドセキュリティフレームワークが必要です。このようなアクセス格差が閉じるまで、胃がん治療市場の一部の成長余地は実現されないままとなります。
セグメント分析
治療タイプ別:免疫療法がイノベーションを推進
免疫療法は2025年に胃がん治療市場内で約12億米ドルの収益を生み出し、最速の年平均成長率13.45%を持つセグメントを代表し、現代治療アルゴリズムでの基礎的役割を確認しています。それでも化学療法は、特に転移設定における一次治療レジメンの中核であり続け、予算制約のある病院でデフォルトとなる価格優位性を維持しているため、2024年に手強い42.19%のシェアを保持しました。外科切除量は術前術後プロトコルの強化により上昇していますが、免疫学的薬剤が生存を延長するにつれ患者当たりの全身療法サイクルは上昇を続け、それによって反復投与を維持しています。放射線療法は控えめなニッチを保持し、主に臓器温存戦略が切除マージンを拡大する局所進行腫瘍に限定されています。
多剤プロトコルへの急速な転換は歴史的分類を曖昧にします:チェックポイント阻害薬は現在細胞毒性バックボーンと同時に開始され、トラスツズマブ デルクステカン+ニボルマブ併用は補助設定での第3相試験に進展しており、「併用療法」が間もなく単剤カテゴリーを凌駕することを示しています。分子標的治療の普及はHER2またはFGFR2検査が償還される場合は常に加速し、改善された生存が症状管理ニーズを延長するにつれて緩和・支持療法レジメンはより早期に開始されます。これらの相互関連する治療ラインにより、専門腫瘍医はますます個別クラスではなく統合プラットフォーム視点を通じて薬剤選択を見るようになっており、胃がん治療市場全体で免疫療法、ADCs、支持薬剤を協調的オファリングにバンドルできる企業を有利にする見解です。
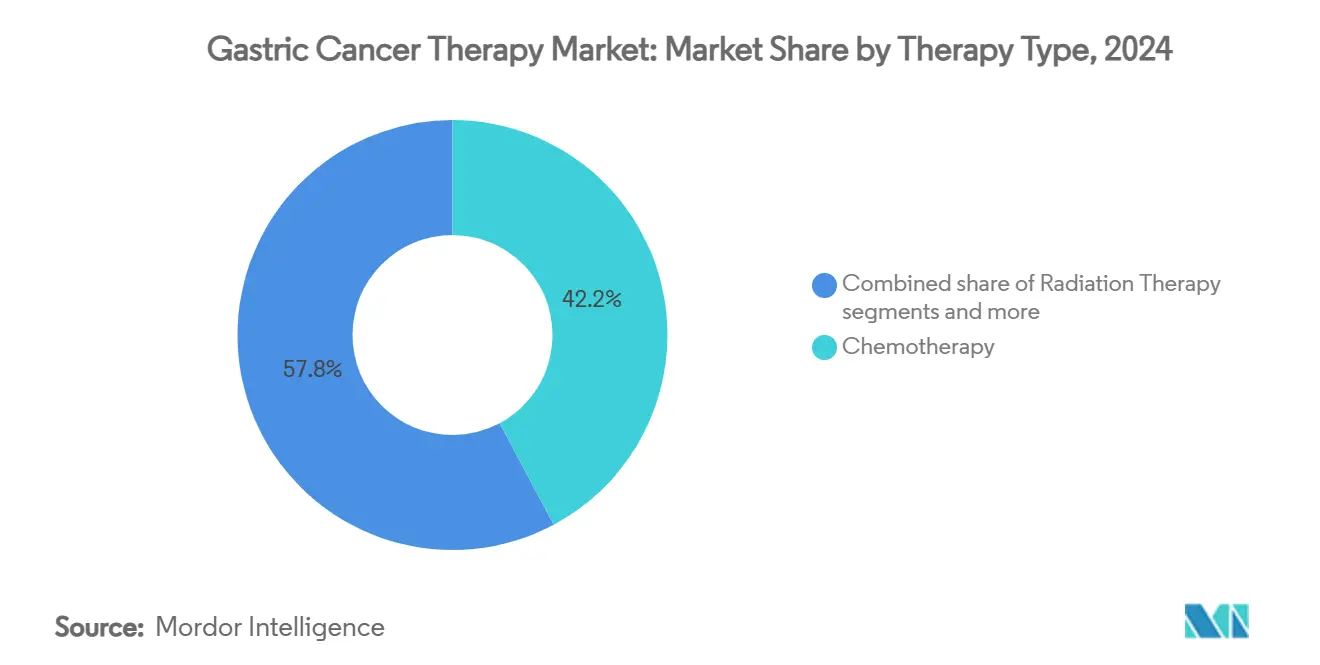
注記: すべての個別セグメントのセグメントシェアはレポート購入時に利用可能
薬物クラス別:FGFR2阻害薬が成長をリード
PD-1/PD-L1阻害薬は2024年薬物クラス収益の単独最大20.23%シェアを記録し、複数ライン間での標準治療としての定着を反映しています。しかし、高所得市場での浸透が飽和に近づくにつれ、その年間成長は緩和しています。対照的に、FGFR2阻害薬はFGFR2増幅腫瘍で42%近い著しい奏効率と2026年までの日本・韓国での承認予想により、最速の年平均成長率12.55%を記録すると予測されています。将来的には、PD-1阻害とFGFR2標的化を融合する二重特異性抗体が初期臨床評価に入っており、クラスシェアをさらに押し上げる可能性のある段階的効力変化のステージを設定しています。
細胞毒性薬剤は新規レジメンを固定し償還優位性を維持することで関連性を保持し、特にブランド生物学的製剤と比べてバイオシミラーのドキソルビシンやオキサリプラチンが1ドルに対してペニーのコストがかかる市場では顕著です。HER2阻害薬は2024年4月のトラスツズマブ デルクステカンの腫瘍非依存的FDA承認後に足場を強化し、すべての転移性症例での汎用HER2スクリーニングを促しました。VEGF/VEGFR阻害薬とADCsは重要な補助活性を供給します:血管正常化は免疫浸潤を改善し、ADCsはマーカー豊富細胞に致死的ペイロードを届け、免疫チェックポイント阻害との相乗効果を増幅します。総合的に、薬物クラスのモザイクは、持続的差別化が精密患者標的化とモジュラー併用ポテンシャルから生じることを強調し、胃がん治療市場全体でマルチプラットフォーム戦略を強化しています。
疾患ステージ別:早期ステージが勢いを増す
早期ステージ0-IA疾患は2025年に約5億8000万米ドルの収益を生み出し、AI支援スクリーニングが診断をより軽度な形態に移行させるにつれて年平均成長率13.71%ですべてのステージをリードしています。再発例は高い再発発症率と長期全身療法により2024年セグメント価値の22.91%を獲得し、依然として価値で第1位にランクしています。切除可能IB-III症例は免疫療法と組み合わせた術前化学療法から恩恵を受け、最近の多施設試験でR0切除率を14%向上させ、手術単独と比べて無病生存期間中央値を6カ月改善しました。
切除不能局所進行腫瘍の管理は依然複雑ですが、ニボルマブ+パクリタキセルレジメンは重篤な腹膜転移で38.5%の奏効を達成し、歴史的に難治性のサブグループでの改善を示唆しています。術前術後免疫療法の持続的採用は外科と全身療法開始間の時間ギャップを圧縮し、微小転移進展を潜在的に抑制します。進行/転移性疾患は連続治療ラインのため患者当たり最高の薬物量を生み出し続けていますが、より良い一次治療制御は後期ライン細胞毒性薬剤への依存を徐々に減らす可能性があります。ステージ移行がより早期検出を有利にするにつれ、胃がん治療市場での将来の価値拡大はサルベージ療法よりも補助イノベーションにより依存するでしょう。
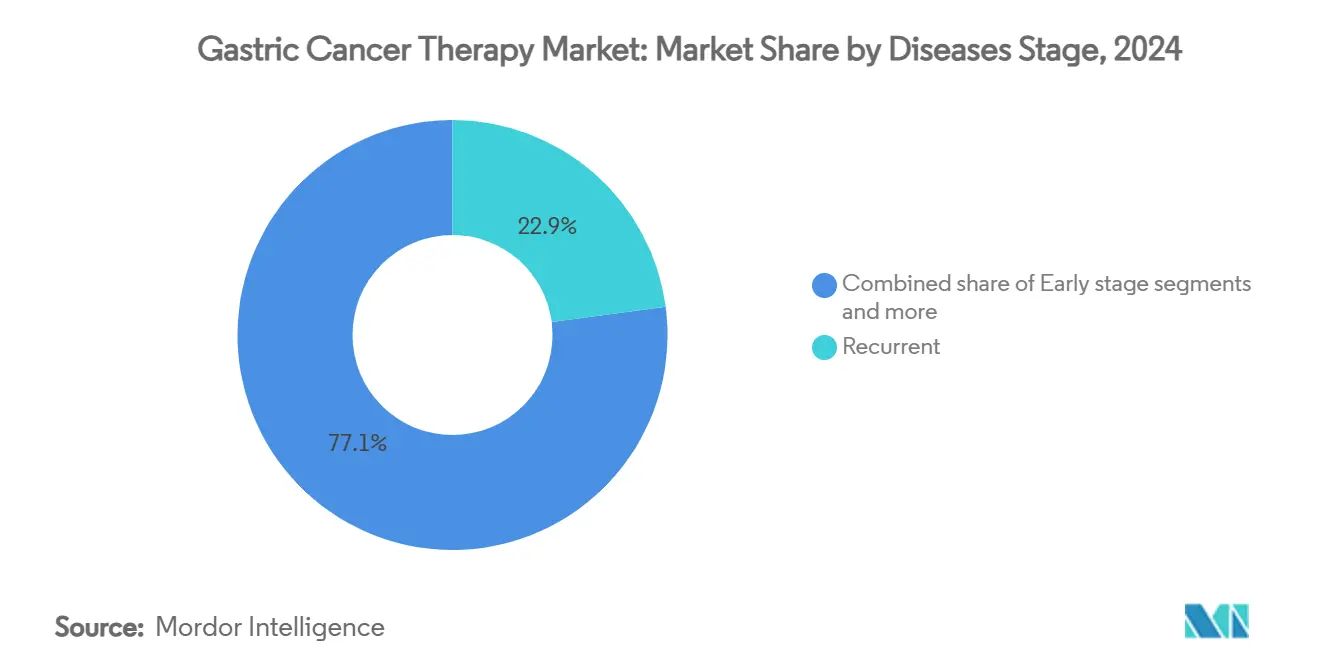
注記: すべての個別セグメントのセグメントシェアはレポート購入時に利用可能
投与経路別:経口製剤が拡大
静脈内注入は定着した病院プロトコルと生物学的製剤の優位性により2025年に約41億米ドル、総支出の68.82%に相当することを実現しました。カペシタビンとアパチニブに主導される経口薬剤は年平均成長率12.93%で増加し、在宅投与への強い患者選好と注入センター経費削減への支払者関心を強調しています。
研究焦点は現在、胃pH環境を生き残り全身吸収後にペイロードを放出するプロテアーゼ切断可能リンカー上に構築された経口チェックポイント阻害薬と経口ADCsに向けられており、この技術は当初血液学で商業化されたが現在胃固形腫瘍を標的としています。オーストラリアの医療システムは、適切な維持患者を経口療法に切り替えた後15%のコスト削減を記録し、経済的インセンティブを強化しました。遠隔医療対応アドヒアランス監視は在宅レジメンへの信頼をさらに向上させ、服用忘れへの懸念を縮小しました。薬物動態学的同等性が維持される限り、多くの静脈内薬剤は経口に変換でき、注入シェアを浸食し胃がん治療市場に新鮮な成長を注入する可能性があります。
地域分析
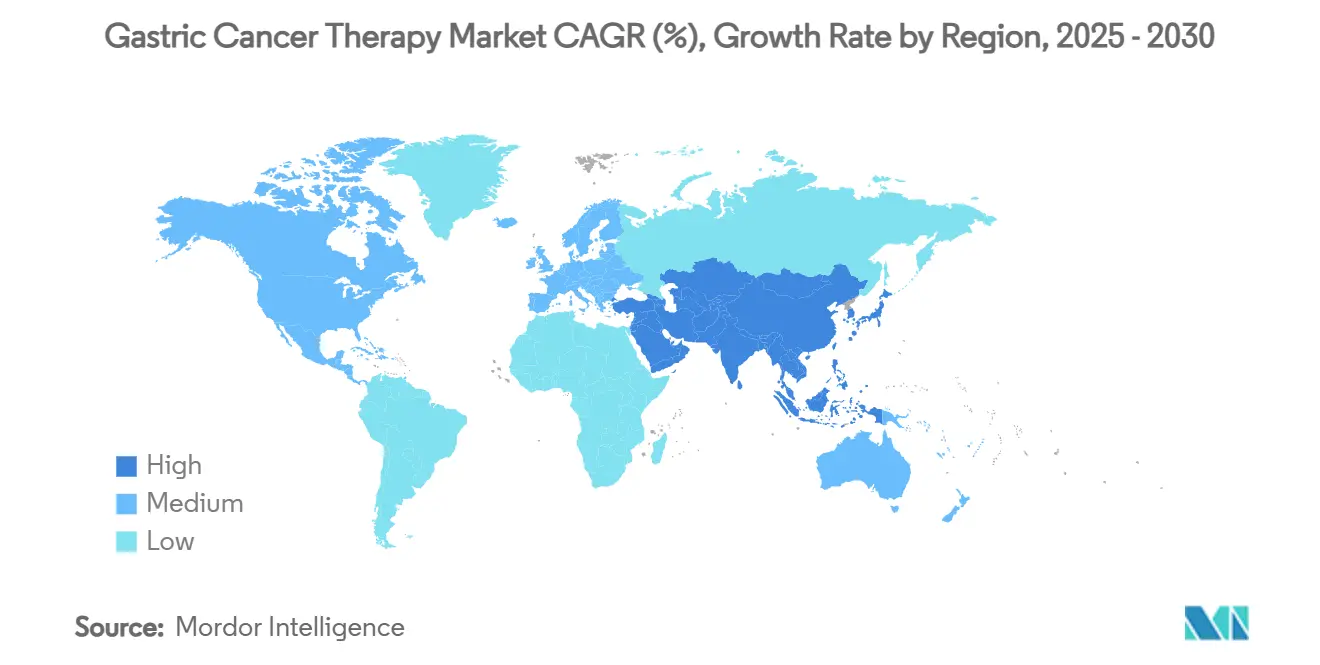
北米は、広範囲な保険適用範囲、高い薬価設定力、標準経路より6-8カ月アクセスを加速するブレークスルー療法やリアルタイム腫瘍学審査などの迅速FDA審査ルートの強さにより2024年に世界収益の42.23%を生み出しました。しかし支払者が成果ベース処方集を重ねるにつれ成長減速が見られます:カナダの2025年5月のトラスツズマブ デルクステカンに対する期限付き償還は、支払継続を中間実世界転帰にリンクし、より広範囲な成果ベース契約を予兆しています。
アジア太平洋地域は、中国の数量ベース調達、インドの拡大する腫瘍学インフラ、承認薬剤の90日以内のほぼ自動償還により年平均成長率15.56%で成長をリードしています。中国の病院請求データでは、2024年調達ラウンド組み入れ後に下位都市でのニボルマブ使用が3倍になり、ボリューム弾力性を強調しています。インドの政府がんセンターネットワークは2025年に8つの新しい三次センターを追加し、それぞれバイオマーカースクリーニングをファストトラックする分子診断ラボを装備しました。日本の規制当局は2025年4月に新しいAIガイド内視鏡システムを承認し、全身療法パイプラインに症例ボリュームを供給する早期検出でのリーダーシップ維持の立場に国を位置づけました。
欧州は成熟した慎重な採用者であり続け、医療技術評価の厳格さが企業に国家償還を確保するための実世界エビデンスの高速蓄積を押し進めています。ドイツの法定保険者は肯定的IQWiG評価後に術前術後免疫療法を広く償還していますが、イタリアは公的支出を制限する価格ボリューム合意を要求しています。南米と中東・アフリカは合わせて胃がん治療市場の7%弱を占めていますが、多国籍企業がバイオマーカー検査と自己負担支援を助成する患者支援スキームをパイロットするにつれ潜在的上昇を保持しています。広範囲に、地理的多様化は単一償還環境への過度の暴露を減らし、世界の胃がん治療市場にレジリエンスを追加しています。
競争環境
胃がん治療市場は中程度の集約を示しています:上位5社-ロシュ、メルク、ブリストル マイヤーズ スクイブ、アストラゼネカ、ファイザー-は年間売上の半分をわずかに上回る集合的獲得であり、複雑な生物学的製造と厳格な規制証明基準に結びついた高い開発障壁を強調しています。
主要企業は単一資産ローンチから薬剤、診断、デジタルサービスを結束的オファリングにラップするエコシステム戦略へ転換しています。ロシュはその抗HER2生物学的製剤を承認されたCLDN18アッセイとパッケージ化し、アストラゼネカは優れた患者体験を通じて市場シェアをロックインすることを狙い、経口パイプラインと併せてアドヒアランスアプリと遠隔監視ウェアラブルを展開しています。バイオシミラー参入者は第一世代抗体を侵食していますが、次世代ADCsと二重特異性構築物は知的財産の深度と製造複雑性により絶縁されたままです。
西欧メジャーが中国バイオテクノロジーとチームを組むにつれライセンス・共同開発取引は激化しています-BeiGeneはtislelizumabの米国商業化権をノバルティスにライセンスし、Innoventはチェックポイント阻害とVEGF阻害の世界融合でイーライリリーと協力しています。人工知能パートナーシップは発見加速を標的とします;メルクのシリコンバレースタートアップとの提携は前臨床標的同定時間を半分に削減し、潜在的に開発サイクルを圧縮しました。将来を見据えて、統合された治療-診断-分析プラットフォームを持つ企業が胃がん治療市場でリーダーシップを維持する最良のポジションにあるようです。
胃がん治療業界リーダー
イーライリリー・アンド・カンパニー
ファイザー社
エフ・ホフマン・ラ・ロシュ社
セルトリオン社
メルク・アンド・カンパニー
- *免責事項:主要選手の並び順不同
最近の業界動向
- 2025年6月:ENHERTUがHER2陽性転移性疾患のDESTINY-Gastric04第3相試験でramucirumab+パクリタキセルと比べて死亡リスクを30%削減し、新しい二次治療ベンチマークを設定
- 2025年4月:カナダ薬事庁がENHERTUに期限付き償還を発行し、標準審査タイムラインより約2年早い患者アクセスを可能に
世界の胃がん治療市場レポート範囲
胃がんは胃の内膜内でがん細胞が成長することによって特徴づけられます。胃がんは比較的稀ながんの一種です。胃がんに関連するリスクファクターには、リンパ腫、ヘリコバクター・ピロリ菌感染、消化器系の他の部分の腫瘍、胃ポリープなどがあります。
胃がん治療市場は治療タイプ別(化学療法、分子標的治療、免疫療法、放射線療法、外科手術)、エンドユーザー別(外来手術センター、病院・専門クリニック、その他のエンドユーザー)、地域別にセグメント化され、地域(北米、欧州、アジア太平洋、中東・アフリカ、南米)でセグメント化されています。市場レポートは世界の主要地域17カ国での推定市場規模とトレンドもカバーしています。
レポートは上記セグメントについて価値(米ドル)を提供しています。
| 外科手術 |
| 化学療法 |
| 放射線療法 |
| 分子標的治療 |
| 免疫療法 |
| 併用療法 |
| 緩和・支持療法 |
| 細胞毒性薬剤 |
| HER2阻害薬 |
| PD-1/PD-L1阻害薬 |
| VEGF/VEGFR阻害薬 |
| FGFR2阻害薬 |
| ADCs(抗体薬物複合体) |
| その他 |
| 静脈内 |
| 経口 |
| 早期ステージ(0-IA) |
| 切除可能(IB-III) |
| 切除不能局所進行 |
| 進行/転移性 |
| 北米 | 米国 |
| カナダ | |
| メキシコ | |
| 欧州 | ドイツ |
| 英国 | |
| フランス | |
| イタリア | |
| スペイン | |
| その他の欧州 | |
| アジア太平洋 | 中国 |
| インド | |
| 日本 | |
| 韓国 | |
| オーストラリア | |
| その他のアジア太平洋 | |
| 南米 | ブラジル |
| アルゼンチン | |
| その他の南米 | |
| 中東・アフリカ | 湾岸協力会議 |
| 南アフリカ | |
| その他の中東・アフリカ |
| 治療タイプ別 | 外科手術 | |
| 化学療法 | ||
| 放射線療法 | ||
| 分子標的治療 | ||
| 免疫療法 | ||
| 併用療法 | ||
| 緩和・支持療法 | ||
| 薬物クラス別 | 細胞毒性薬剤 | |
| HER2阻害薬 | ||
| PD-1/PD-L1阻害薬 | ||
| VEGF/VEGFR阻害薬 | ||
| FGFR2阻害薬 | ||
| ADCs(抗体薬物複合体) | ||
| その他 | ||
| 投与経路別 | 静脈内 | |
| 経口 | ||
| 疾患ステージ別 | 早期ステージ(0-IA) | |
| 切除可能(IB-III) | ||
| 切除不能局所進行 | ||
| 進行/転移性 | ||
| 地域別 | 北米 | 米国 |
| カナダ | ||
| メキシコ | ||
| 欧州 | ドイツ | |
| 英国 | ||
| フランス | ||
| イタリア | ||
| スペイン | ||
| その他の欧州 | ||
| アジア太平洋 | 中国 | |
| インド | ||
| 日本 | ||
| 韓国 | ||
| オーストラリア | ||
| その他のアジア太平洋 | ||
| 南米 | ブラジル | |
| アルゼンチン | ||
| その他の南米 | ||
| 中東・アフリカ | 湾岸協力会議 | |
| 南アフリカ | ||
| その他の中東・アフリカ | ||
レポートで回答される主要質問
2030年までに胃がん治療市場はどの程度の規模になりますか?
胃がん治療市場規模は2030年までに108億6000万米ドルに達すると予測されています。
どの治療形式が最も急速に成長していますか?
免疫療法が2030年まで年平均成長率13.45%でリードしています。
地域需要はどこで最も急速に拡大していますか?
アジア太平洋地域が中国、インド、日本により推進され最高の年平均成長率15.56%を記録しています。
どの薬物クラスが現在最大のシェアを占めていますか?
PD-1/PD-L1阻害薬が2024年に市場シェア20.23%を保持しました。
経口治療はどの程度重要になりますか?
経口製剤は在宅医療が好まれるようになるにつれ年平均成長率12.93%で成長すると予想されています。
最終更新日:



