Tamaño y Participación del Mercado de Biotecnología Roja
Análisis del Mercado de Biotecnología Roja por Mordor Intelligence
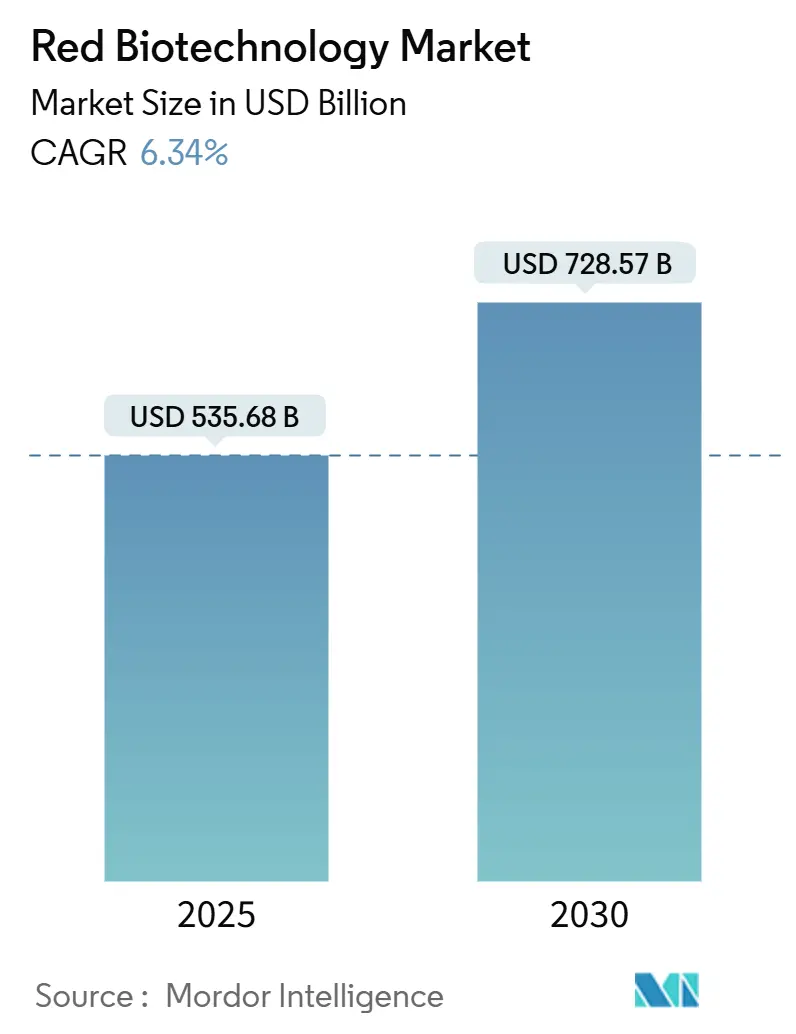
El tamaño del mercado de biotecnología roja se situó en USD 535.68 mil millones en 2025 y se prevé que alcance USD 728.57 mil millones en 2030, avanzando a una TCAC del 6.34%. El crecimiento se basa en una transición desde la producción de vacunas centradas en la pandemia hacia carteras diversificadas que ahora incluyen terapias celulares y génicas, anticuerpos monoclonales de próxima generación y diagnósticos de precisión. Las revisiones regulatorias más rápidas sustentan el impulso, ilustrado por las 24 aprobaciones de licencias biológicas emitidas por la FDA en 2024. El gasto gubernamental paralelo-más notablemente la asignación de USD 79.5 mil millones de la Public Health Emergency Medical Countermeasures Enterprise (PHEMCE) hasta 2027-refuerza la capacidad doméstica tanto para desarrollo como para fabricación. En el lado de la industria, proyectos de capital a gran escala como la instalación de vacunas de USD 1 mil millones de Merck en Carolina del Norte agregan capacidad resiliente que puede flexibilizarse entre respuesta pandémica y producción comercial rutinaria. Juntos, estos factores crean un entorno predecible para escalar productos biológicos de alta complejidad, fomentando la inversión de capital de riesgo y las asociaciones público-privadas que acortan el tiempo hasta la clínica para activos innovadores.
Puntos Clave del Informe
- Por categoría de producto, el segmento de medicamentos terapéuticos capturó el 54.67% de la participación del mercado de biotecnología roja en 2024; se proyecta que el mismo segmento se expanda a una TCAC del 6.87% hasta 2030.
- Por usuario final, las empresas biofarmacéuticas mantuvieron el 44.89% del tamaño del mercado de biotecnología roja en 2024, mientras que los institutos académicos y de investigación registraron la TCAC proyectada más alta del 7.35% hasta 2030.
- Por geografía, América del Norte representó el 39.13% del tamaño del mercado de biotecnología roja en 2024; Asia-Pacífico está avanzando a una TCAC del 7.26% durante el mismo período.
Tendencias e Insights del Mercado Global de Biotecnología Roja
Análisis del Impacto de Impulsores
| Impulsor | (~) % Impacto en Pronóstico TCAC | Relevancia Geográfica | Cronología de Impacto |
|---|---|---|---|
| Incidencia y prevalencia creciente de enfermedades crónicas y raras | +1.2% | Global, con concentración en poblaciones envejecidas de América del Norte y Europa | Largo plazo (≥ 4 años) |
| Expansión de financiamiento sanitario y asociaciones público-privadas | +0.9% | Global, particularmente fuerte en APAC y mercados emergentes | Mediano plazo (2-4 años) |
| Adopción de medicina personalizada y aceptación de diagnósticos complementarios | +0.8% | América del Norte y UE lideran, expandiéndose a APAC | Mediano plazo (2-4 años) |
| Derrame de plataforma de ARNm acelerando nuevos productos biológicos | +0.7% | Global, con centros de fabricación en América del Norte y Europa | Corto plazo (≤ 2 años) |
| Reducción de riesgo impulsada por IA del diseño de productos biológicos en etapa temprana | +0.6% | Global, concentrado en centros de innovación | Mediano plazo (2-4 años) |
| Programas gubernamentales de preparación pandémica que escalan la capacidad global de fabricación de vacunas | +0.5% | Global, con enfoque estratégico en capacidades domésticas | Largo plazo (≥ 4 años) |
| Fuente: Mordor Intelligence | |||
Incidencia y prevalencia creciente de enfermedades crónicas y raras
Ocho terapias celulares y génicas novedosas pasaron la revisión de la FDA en 2024, subrayando cómo las áreas de necesidad no satisfecha convierten avances científicos en activos comerciales. La oncología continuó dominando las aprobaciones, representando el 34% de todos los nuevos productos biológicos[1]Zinnet Sevval Aksoyalp, "A Year in Pharmacology: New Drugs Approved by the US Food and Drug Administration in 2024," Naunyn-Schmiedeberg's Archives of Pharmacology, link.springer.com en 2024. Los cambios demográficos intensifican la demanda; la prioridad política de Japón sobre anticuerpos monoclonales de próxima generación y terapias génicas refleja el desafío de manejar una población que envejece rápidamente. Las carteras de enfermedades raras se benefician de los incentivos de Medicamentos Huérfanos, ya que el 88% de las aprobaciones de terapia génica de 2024 llevaron esa designación. El Rare Disease Innovation Hub de la FDA y su piloto START comprimen los cronogramas de desarrollo, alentando a las empresas a dirigirse a enfermedades de nicho una vez consideradas comercialmente poco atractivas.
Expansión de financiamiento sanitario y asociaciones público-privadas
La asignación PHEMCE 2023-2027 reservó USD 79.5 mil millones[2]U.S. Department of Health & Human Services, "Public Health Emergency Medical Countermeasures Enterprise Multi-Year Budget FY 2023-2027," U.S. Department of Health & Human Services, aspr.hhs.gov para I+D de contramedidas y fabricación doméstica, un aumento de USD 15.5 mil millones sobre el ciclo de planificación anterior. El BioMaP-Consortium de BARDA de USD 2 mil millones extiende este apoyo co-invirtiendo en instalaciones flexibles que pueden pivotar de anticuerpos a vacunas de ARNm en meses. El Centro de Fabricación de Productos Biológicos de Canadá en Montreal añade 250 millones de dosis de capacidad anual para vacunas de vectores virales y subunidades proteicas. El programa GenAI4EU de la Comisión Europea destina EUR 1 mil millones para proyectos de IA incluyendo descubrimiento de productos biológicos, reforzando la transferencia de conocimiento transfronterizo. Las economías emergentes reflejan el modelo; el marco BIO-E3 de India suministra financiación concesional y adquisición de tierras simplificada para nuevos campus de bioproducción.
Adopción de medicina personalizada y aceptación de diagnósticos complementarios
Las directrices de la FDA publicadas en 2025 clarifican cómo la inteligencia artificial puede aumentar la toma de decisiones regulatorias para productos biológicos, señalando la aceptación formal de diagnósticos complementarios potenciados por ML. Las pruebas genéticas ahora representan el 45% de los kits de diagnóstico de precisión comerciales, con la oncología representando una cuarta parte de la demanda general. Los hospitales despliegan cada vez más plataformas POCT vinculadas a la nube, un mercado que se espera supere los USD 90.25 mil millones en 2030, dando a los clínicos el estado de mutación en tiempo real antes del inicio de la terapia. El acceso más amplio a la secuenciación de próxima generación reduce los costos por genoma, permitiendo a las empresas biofarmacéuticas de tamaño medio estratificar ensayos sin presupuestos prohibitivos. La claridad regulatoria, menores costos de ensayos y bioinformática fácilmente accesible impulsan colectivamente la adopción de diagnósticos complementarios que anclan los regímenes terapéuticos personalizados.
Derrame de plataforma de ARNm acelerando nuevos productos biológicos
Setenta ensayos clínicos activos evaluaron vacunas basadas en ARNm más allá de COVID-19 a junio de 2024, dirigiéndose a oncología, VRS y fibrosis quística. Los constructos trans-amplificantes reducen la entrada de ARN cuarenta veces, disminuyendo el costo de bienes mientras mantienen la inmunogenicidad. Los vectores de ARNm circular sintetizados en la Universidad de Nagoya entregan 200 veces mayor producción de proteínas, abriendo ventanas terapéuticas en trastornos metabólicos y genéticos raros. Moderna está comisionando tres plantas regionales-Reino Unido, Australia y Canadá-cada una capaz de llenar 100 millones de equivalentes de dosis, demostrando escalabilidad global para carteras de ARNm de rotación rápida ya que la producción se mueve a formatos continuos de un solo uso, los cronogramas de transferencia tecnológica se reducen, permitiendo a pequeños desarrolladores navegar desde IND hasta Fase 1 en menos de 12 meses.
Análisis del Impacto de Restricciones
| Restricción | (~) % Impacto en Pronóstico TCAC | Relevancia Geográfica | Cronología de Impacto |
|---|---|---|---|
| Altos costos de biofabricación y cadena de frío | -0.8% | Global, particularmente desafiante en mercados emergentes | Mediano plazo (2-4 años) |
| Regulaciones biológicas globales complejas y cambiantes | -0.6% | Global, con variaciones regionales en requisitos de cumplimiento | Largo plazo (≥ 4 años) |
| Fragilidad de la cadena de suministro para materias primas críticas | -0.5% | Global, con riesgos de concentración en proveedores de Asia-Pacífico | Corto plazo (≤ 2 años) |
| Riesgos de inmunogenicidad en terapias génicas de próxima generación | -0.4% | Global, con mayor escrutinio en América del Norte y Europa | Mediano plazo (2-4 años) |
| Fuente: Mordor Intelligence | |||
Altos costos de biofabricación y cadena de frío
Las pérdidas de la industria por fallas de cadena de frío alcanzan USD 35 mil millones anuales, socavando la asequibilidad de productos biológicos sensibles a la temperatura. Las terapias CAR-T autólogas aún cuestan más de USD 500,000 por paciente debido a la fabricación intensiva en mano de obra y distribución criogénica. Las revisiones del Anexo 1 endurecieron las reglas de procesamiento aséptico, obligando actualizaciones a tecnología de aisladores y monitoreo ambiental que inflan capex para plantas nuevas. La concentración de la cadena de suministro agrava el problema; más del 75% de las importaciones de API de EE.UU. se originan fuera de sus fronteras, exponiendo la producción a choques geopolíticos. Aunque el software de planificación de rutas habilitado por IA y los gemelos digitales prometen ahorros logísticos del 15-25%, el despliegue generalizado permanece en etapas piloto, retrasando el alivio a corto plazo.
Regulaciones biológicas globales complejas y cambiantes
La Regulación de Ensayos Clínicos de la UE, efectiva enero 2025, obliga a los patrocinadores a cargar datos de estudios heredados en el nuevo portal CTIS, causando atrasos administrativos. Concurrentemente, una revisión de tarifas de EMA elevó los costos de asesoramiento científico hasta EUR 98,400, tensando a pequeños desarrolladores. La iniciativa CoGenT Global de la FDA busca directrices armonizadas de terapia génica pero actualmente cubre solo enfermedades raras, dejando categorías más amplias en limbo regulatorio. En Estados Unidos, el reemplazo de todos los miembros del Advisory Committee on Immunization Practices (ACIP) en junio 2025 inyectó incertidumbre en los próximos cronogramas de política de vacunas. Colectivamente, los estándares desalineados extienden el tiempo hasta aprobación y aumentan el volumen de estudios puente necesarios para lanzamientos multi-regionales.
Análisis por Segmento
Por Producto: Medicamentos Terapéuticos Lideran la Ola de Innovación
Los medicamentos terapéuticos generaron USD 293 mil millones en 2024, correspondiente a una participación del 54.67% del tamaño del mercado de biotecnología roja, y se prevé que crezcan a una TCAC del 6.87% hasta 2030. Los anticuerpos monoclonales anclan la categoría, presumiendo más de 200 agentes aprobados y cerca de 1,400 candidatos clínicos activos[3]Silvia Crescioli, "Antibodies to Watch in 2025," mAbs, tandfonline.com mundialmente. Los formatos biespecíficos logran la conversión clínica-a-aprobación más alta, motivando a empresas como BioNTech y Bristol Myers Squibb a buscar acuerdos de codesarrollo de múltiples mil millones de dólares. Las terapias génicas se aceleraron tras el respaldo de la FDA de ocho productos en 2024, mientras que las plataformas CAR-T modificadas con CRISPR ahora dominan los ensayos de hemo-oncología en fase temprana. Los terapéuticos de ARNm se mueven más allá de enfermedades infecciosas hacia indicaciones cardiometabólicas, apoyados por tecnología de ARN circular que multiplica el rendimiento proteico in vivo.
Las vacunas mantienen relevancia estratégica, apoyadas por cláusulas de opción de BARDA que garantizan volúmenes mínimos de llamada durante brotes. Los diagnósticos y herramientas de investigación se expanden ya que los reactivos de secuenciación y ensayos de biopsia líquida ganan adopción en entornos descentralizados. En paralelo, las proteínas terapéuticas evolucionan hacia conjugados anticuerpo-medicamento y citoquinas de fusión adaptadas a microambientes de enfermedad específicos, reflejando el énfasis del mercado de biotecnología roja en la focalización de precisión.
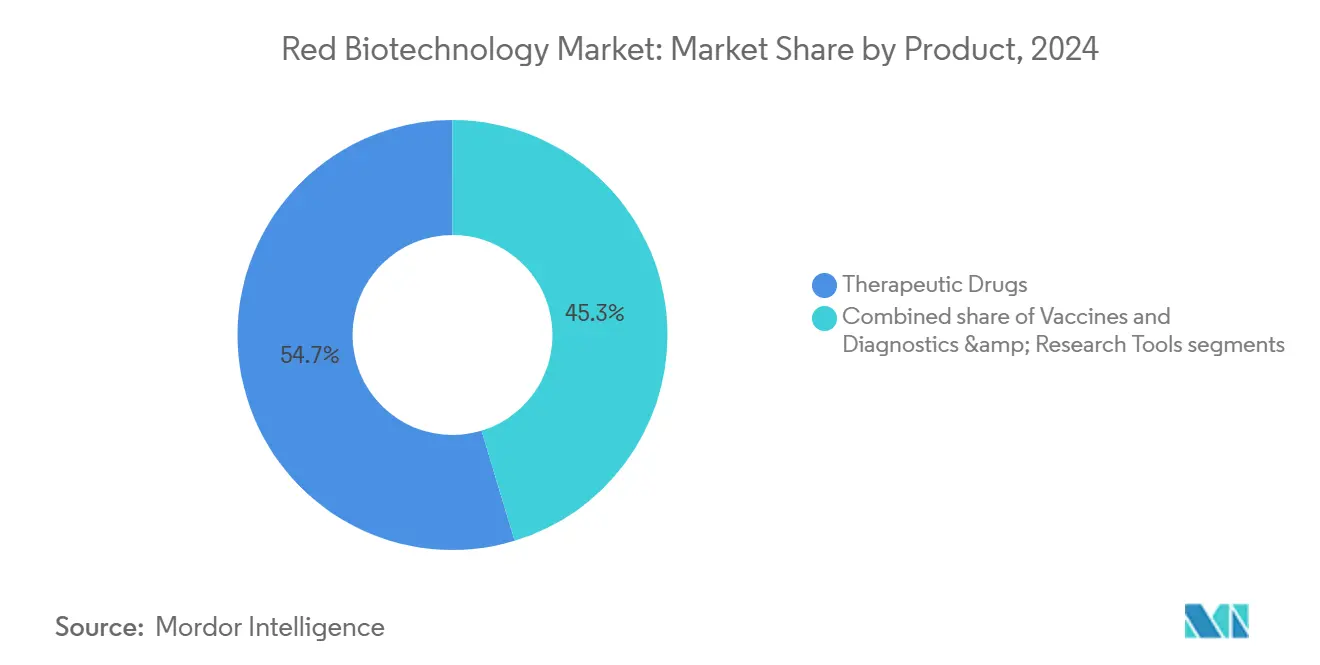
Nota: Participaciones de segmento de todos los segmentos individuales disponibles con la compra del informe
Por Usuario Final: Asociaciones Académicas Impulsan el Crecimiento
Las empresas biofarmacéuticas retuvieron el 44.89% de la participación del mercado de biotecnología roja en 2024 a través de integración vertical que abarca desde descubrimiento hasta suministro comercial. Los institutos académicos y de investigación, sin embargo, representan el electorado de crecimiento más rápido al 7.35% TCAC, impulsado por afluencias de subvenciones y co-reclutamiento corporativo de investigadores principales. Las instalaciones centrales universitarias ahora proporcionan suites de vectores compatibles con GMP, permitiendo a spin-outs ejecutar ensayos tempranos sin construir infraestructura dedicada. La alianza de NVIDIA con Novo Nordisk suministra créditos de GPU en la nube y algoritmos de predicción estructural a más de 100 laboratorios académicos, democratizando el acceso a herramientas de diseño de IA.
Las organizaciones de fabricación por contrato (CMO) y organizaciones de investigación por contrato ven impulso paralelo ya que la externalización mitiga la carga de capital; las CMO están en camino de controlar el 54% de la capacidad global de productos biológicos en 2028, remodelando el cálculo de hacer-versus-comprar para pequeños innovadores. Los hospitales y clínicas especializadas emergen como usuarios finales de nicho para terapias celulares en el punto de atención, especialmente en centros oncológicos equipados con cápsulas de fabricación de sistema cerrado. Esta difusión de capacidad refleja una migración de la industria hacia redes de desarrollo distribuidas pero interconectadas.
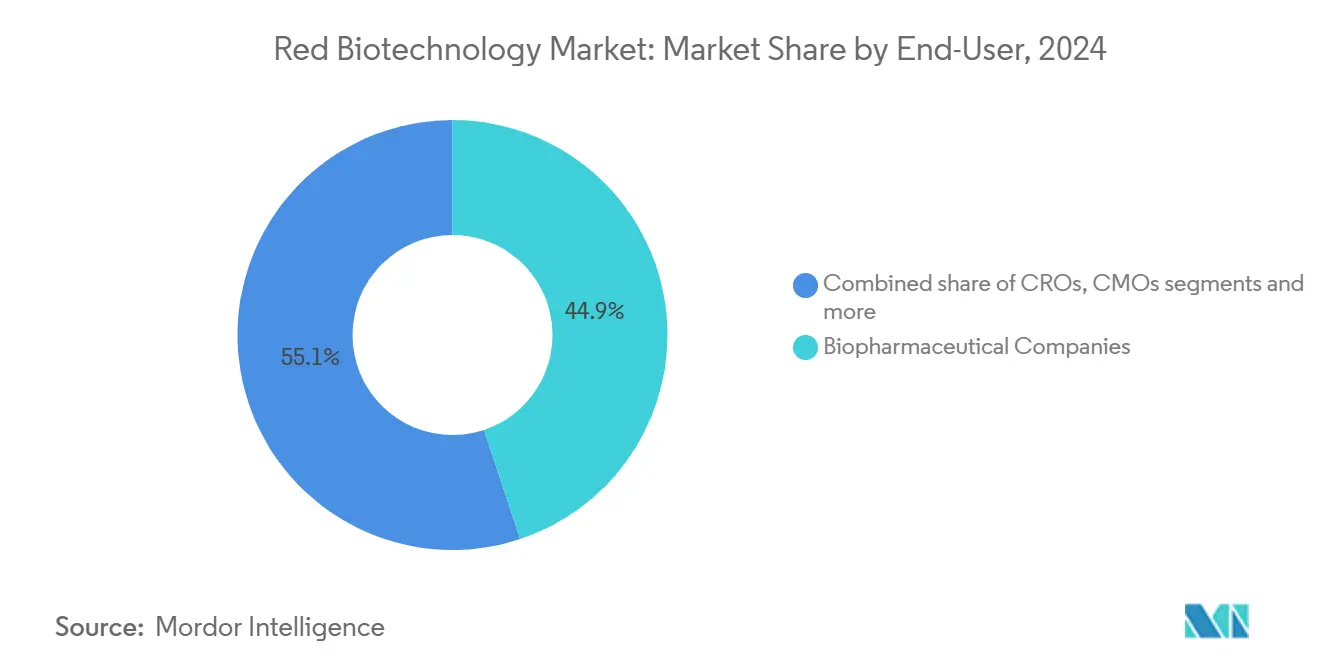
Nota: Participaciones de segmento de todos los segmentos individuales disponibles con la compra del informe
Análisis Geográfico
América del Norte capturó el 39.13% del tamaño del mercado de biotecnología roja en 2024, y se proyecta que registre una TCAC del 6.01% hasta 2030. La región se beneficia de un ecosistema de espectro completo que agrupa descubrimiento, regulación y fabricación a escala industrial. El BioMaP-Consortium de BARDA y el pool de capital PHEMCE salvaguardan la producción doméstica tanto para productos biológicos rutinarios como de emergencia, mientras que las designaciones expeditas de la FDA acortan los tiempos de entrega para terapias innovadoras. La reestructuración regulatoria en curso, como la renovación de membresía del ACIP, introduce incertidumbre a corto plazo para el momento de lanzamiento de vacunas. Sin embargo, propuestas del Congreso de gran tamaño que buscan USD 15 mil millones para competitividad biotecnológica subrayan el compromiso político sostenido.
Se proyecta que Europa crezca a una TCAC del 6.24% hasta 2030. Las reformas políticas, incluyendo la Regulación de Ensayos Clínicos y fondos de Horizon Europe, facilitan ensayos multinacionales y el intercambio de conocimiento transfronterizo. La infraestructura EUFab de HERA ofrece capacidad de aumento ágil, capaz de cambiar entre vacunas de ARNm, vectores virales y proteínas en 100 días, mejorando la autonomía del bloque. Los aumentos de tarifas bajo las nuevas regulaciones de EMA añaden presión de costos, pero la consulta simultánea sobre expedientes de biosimilares simplificados podría ampliar el acceso a productos biológicos de menor precio para pagadores estatales.
Asia-Pacífico muestra el impulso más rápido, expandiéndose a una TCAC del 7.26% y se espera que más que duplique su valor de segmento en 2030. La estrategia nacional de Japón busca triplicar la producción sectorial a 15 billones de yenes en 2030 a través de créditos fiscales y carriles de revisión acelerada. El valor biotecnológico de India se disparó de USD 10 mil millones en 2014 a USD 130 mil millones[4]Press Information Bureau, "2025 Will Witness India Assuming Critical Role in Global Biotechnology Revolution; India's 1st Biotechnology Policy BIO-E3 Brought by Modi Govt 3.0 Has Already Paved the Way for It, Says Science Minister Dr. Jitendra Singh," Press Information Bureau, pib.gov.in en 2024, aprovechando ventajas de costos y una participación del 60% del volumen global de vacunas. China profundiza el descubrimiento habilitado por IA, personificado por la asociación de USD 5.3 mil millones de AstraZeneca con CSPC Pharmaceutical que se dirige a trastornos autoinmunes. Los gobiernos regionales están sincronizando regulaciones para facilitar ensayos clínicos transfronterizos, acelerando estudios de primera-en-humanos y posterior escalamiento en plantas de contrato cercanas.
Panorama Competitivo
El liderazgo del mercado se inclina hacia empresas que combinan plataformas diferenciadas con alianzas en red más que pura escala. El pacto de anticuerpos biespecíficos de USD 7.6 mil millones de BioNTech y Bristol Myers Squibb señala la prima que los inversores colocan en plataformas modulares de inmunooncología. El acuerdo centrado en IA de AstraZeneca con CSPC avanzó modelos multi-ómicos que acortan los ciclos de optimización de leads hasta en 50%. Estas asociaciones ejemplifican un patrón donde el capital de big-pharma se fusiona con know-how especializado para compartir riesgo y acelerar validación.
El mercado de biotecnología roja, mientras tanto, abre espacio en blanco en modalidades de ARN; se prevé que el segmento se expanda seis veces, creando espacio para startups enfocadas en vehículos de entrega como nanopartículas lipídicas y nanocages proteicas. Las CMO capturan valor desproporcionado ofreciendo capacidad plug-and-play, con proyecciones de que poseerán una participación mayor de la producción global de productos biológicos en 2030. Los disruptores emergentes-p.ej., la vacuna de ARN auto-amplificante de Arcturus Therapeutics, o los geles depot basados en lípidos de Camurus que sustentan una alianza de USD 870 millones con Lilly-demuestran cómo la innovación de formulación puede desbloquear tanto conveniencia del paciente como ventaja económica.
La intensidad competitiva permanece moderada porque las altas barreras de capital limitan la entrada de entidades de producto único. Sin embargo, el papel de la IA está bajando los costos de descubrimiento, permitiendo a nuevos participantes ganar tracción rápidamente licenciando fabricación en lugar de construir huellas intensivas en activos. Consecuentemente, los incumbentes fortalecen posiciones de PI y buscan licencias de etapa más temprana para asegurar profundidad de cartera, ilustrado por Agenus otorgando a Zydus derechos sobre sus anticuerpos de checkpoint mientras co-lanza un negocio BioCDMO de EE.UU.
Líderes de la Industria de Biotecnología Roja
-
AstraZeneca PLC
-
F. Hoffmann-La Roche Ltd
-
Bristol Myers Squibb
-
Novartis AG
-
Pfizer Inc.
- *Nota aclaratoria: los principales jugadores no se ordenaron de un modo en especial

Desarrollos Recientes de la Industria
- Junio 2025: BioNTech y Bristol Myers Squibb anunciaron una colaboración de USD 7.6 mil millones para co-desarrollar y co-comercializar BNT327, un anticuerpo biespecífico dirigido a PD-L1 y VEGF-A para múltiples tumores, compartiendo beneficios en base 50/50
- Junio 2025: AstraZeneca firmó un acuerdo de investigación liderado por IA de USD 5.3 mil millones con CSPC Pharmaceutical Group para descubrir terapias de moléculas pequeñas para enfermedades crónicas, incluyendo un pago inicial de USD 110 millones.
- Junio 2025: Eli Lilly formó una alianza de USD 870 millones con Camurus para co-desarrollar medicamentos para obesidad basados en GLP-1 y incretinas de acción prolongada usando la tecnología de gel depot basada en lípidos de Camurus.
- Junio 2025: Agenus y Zydus Lifesciences finalizaron una asociación de USD 141 millones centrada en botensilimab y balstilimab, junto con Zydus lanzando una unidad BioCDMO de EE.UU. utilizando las instalaciones existentes de Agenus.
Alcance del Informe Global del Mercado de Biotecnología Roja
Según el alcance del informe, la biotecnología roja es un proceso que utiliza organismos para el desarrollo y fabricación de terapias y técnicas diagnósticas. El mercado de biotecnología roja está segmentado por producto (vacunas, medicamentos y otros), usuario final (empresas biofarmacéuticas, CMO y CRO, y otros), y geografía (América del Norte, Europa, Asia-Pacífico, Medio Oriente y África, y América del Sur). El informe del mercado también cubre los tamaños de mercado estimados y tendencias para 17 países diferentes en las principales regiones globalmente. El informe ofrece el valor (en USD) para los segmentos mencionados.
| Vacunas | Vacunas de ARNm |
| Vacunas de Vectores Virales | |
| Vacunas de Proteínas Recombinantes | |
| Vacunas Conjugadas y de Subunidades | |
| Vacunas Vivas Atenuadas e Inactivadas | |
| Medicamentos Terapéuticos | Anticuerpos Monoclonales |
| Proteínas Recombinantes | |
| Terapias Génicas | |
| Terapias Celulares | |
| Terapéuticos de ARN | |
| Herramientas de Diagnóstico e Investigación | Reactivos y Kits de Secuenciación |
| Ensayos de Diagnóstico Complementario | |
| Pruebas Moleculares en el Punto de Atención |
| Empresas Biofarmacéuticas |
| Organizaciones de Fabricación por Contrato (CMO) |
| Organizaciones de Investigación por Contrato (CRO) |
| Institutos Académicos y de Investigación |
| Hospitales y Clínicas Especializadas |
| América del Norte | Estados Unidos |
| Canadá | |
| México | |
| Europa | Alemania |
| Reino Unido | |
| Francia | |
| Italia | |
| España | |
| Resto de Europa | |
| Asia-Pacífico | China |
| India | |
| Japón | |
| Australia | |
| Corea del Sur | |
| Resto de Asia-Pacífico | |
| Medio Oriente y África | CCG |
| Sudáfrica | |
| Resto de Medio Oriente y África | |
| América del Sur | Brasil |
| Argentina | |
| Resto de América del Sur |
| Por Producto | Vacunas | Vacunas de ARNm |
| Vacunas de Vectores Virales | ||
| Vacunas de Proteínas Recombinantes | ||
| Vacunas Conjugadas y de Subunidades | ||
| Vacunas Vivas Atenuadas e Inactivadas | ||
| Medicamentos Terapéuticos | Anticuerpos Monoclonales | |
| Proteínas Recombinantes | ||
| Terapias Génicas | ||
| Terapias Celulares | ||
| Terapéuticos de ARN | ||
| Herramientas de Diagnóstico e Investigación | Reactivos y Kits de Secuenciación | |
| Ensayos de Diagnóstico Complementario | ||
| Pruebas Moleculares en el Punto de Atención | ||
| Por Usuario Final | Empresas Biofarmacéuticas | |
| Organizaciones de Fabricación por Contrato (CMO) | ||
| Organizaciones de Investigación por Contrato (CRO) | ||
| Institutos Académicos y de Investigación | ||
| Hospitales y Clínicas Especializadas | ||
| Por Geografía | América del Norte | Estados Unidos |
| Canadá | ||
| México | ||
| Europa | Alemania | |
| Reino Unido | ||
| Francia | ||
| Italia | ||
| España | ||
| Resto de Europa | ||
| Asia-Pacífico | China | |
| India | ||
| Japón | ||
| Australia | ||
| Corea del Sur | ||
| Resto de Asia-Pacífico | ||
| Medio Oriente y África | CCG | |
| Sudáfrica | ||
| Resto de Medio Oriente y África | ||
| América del Sur | Brasil | |
| Argentina | ||
| Resto de América del Sur | ||
Preguntas Clave Respondidas en el Informe
¿Qué modalidades terapéuticas están ganando mayor tracción regulatoria en biotecnología roja?
Las terapias celulares y génicas están recibiendo revisiones aceleradas bajo programas como el Rare Disease Innovation Hub de la FDA, llevando a aprobaciones más rápidas para tratamientos de nicho de alto impacto.
¿Cómo está remodelando la inteligencia artificial el descubrimiento y desarrollo de productos biológicos?
Los modelos de aprendizaje profundo ahora predicen el plegamiento de proteínas y puntos calientes inmunogénicos en horas, permitiendo a los investigadores iterar diseños rápidamente y reducir el riesgo de falla en etapa temprana.
¿Qué ventajas estratégicas obtienen las empresas biofarmacéuticas asociándose con organizaciones de fabricación por contrato (CMO)?
Las CMO ofrecen instalaciones modulares de un solo uso que permiten a los patrocinadores escalar producción sin gran desembolso de capital, permitiendo lanzamiento comercial más rápido y capacidad de aumento pandémico flexible.
¿De qué maneras las regulaciones globales en evolución influyen en las estrategias de entrada al mercado?
Las reglas divergentes post-2025 en la UE y Estados Unidos están motivando a las empresas a secuenciar presentaciones, ejecutar estudios puente específicos por región y presupuestar para tarifas de asesoramiento científico más altas.
¿Cómo está alterando el auge de la medicina personalizada los flujos de trabajo de diagnóstico?
Los diagnósticos complementarios se están moviendo más cerca del punto de atención, integrando ensayos genómicos rápidos que ayudan a los clínicos a seleccionar terapias dirigidas durante la visita inicial del paciente.
¿Qué avances tecnológicos están ayudando a reducir los costos de logística de cadena de frío para productos biológicos?
Las vacunas de ARNm trans-amplificantes y excipientes estabilizadores de próxima generación extienden la vida útil del producto en refrigeración estándar, reduciendo la dependencia de redes de almacenamiento ultra-frío.
Última actualización de la página el:



