Tamaño y Participación del Mercado de Terapia Génica
Análisis del Mercado de Terapia Génica por Mordor Intelligence
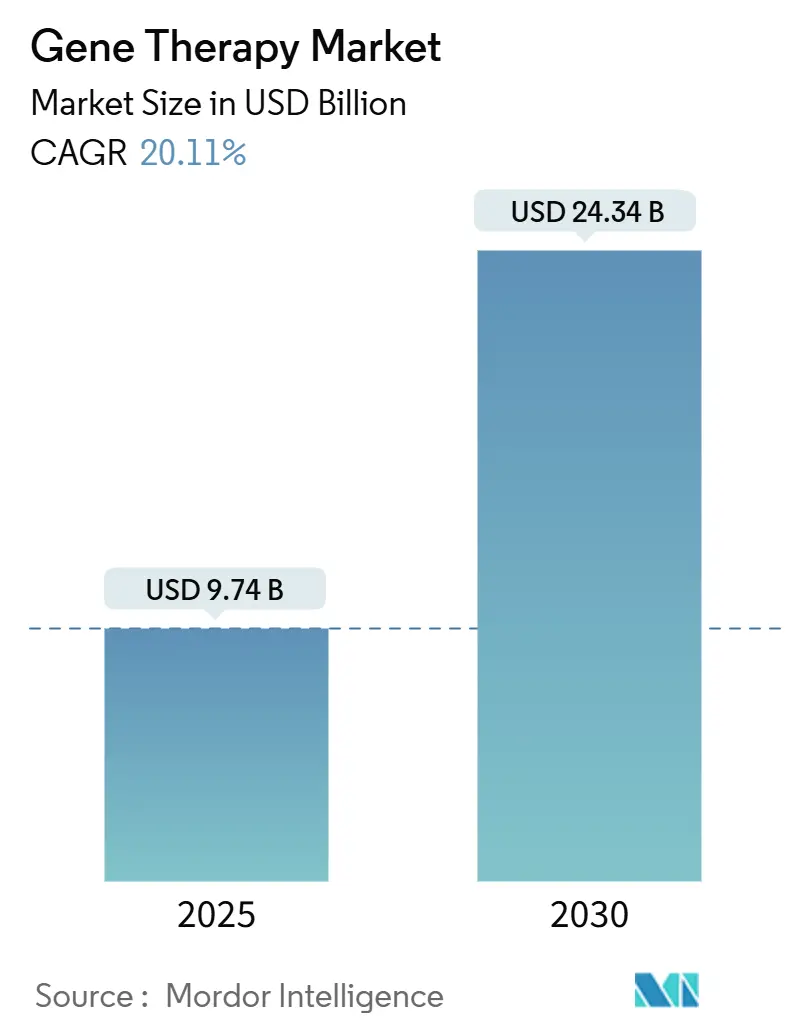
Se estima que el tamaño del Mercado de Terapia Génica es de USD 9,74 mil millones en 2025, y se espera que alcance USD 24,34 mil millones en 2030, a una TCAC del 20,11% durante el período de pronóstico (2025-2030).
Las autoridades regulatorias aprobaron nueve terapias celulares y génicas solo en 2024, señalando una creciente confianza en la viabilidad clínica y comercial y desbloqueando vías de reembolso más amplias en mercados clave. El incremento en la financiación biofarmacéutica y de capital privado está acelerando los activos en etapas avanzadas, mientras que la expansión de la capacidad de fabricación tanto viral como no viral reduce la fricción histórica de la cadena de suministro. Los rápidos avances en edición in vivo e ingeniería de vectores están ampliando el alcance terapéutico más allá de las enfermedades raras hacia trastornos de alta prevalencia, especialmente en neurología y oftalmología. El crecimiento de ensayos de dos dígitos en Asia-Pacífico y los incentivos políticos de América del Norte juntos aseguran una base de demanda diversificada, aun cuando los altos precios de productos y los requisitos de monitoreo de seguridad plantean obstáculos de acceso.
Conclusiones Clave del Informe
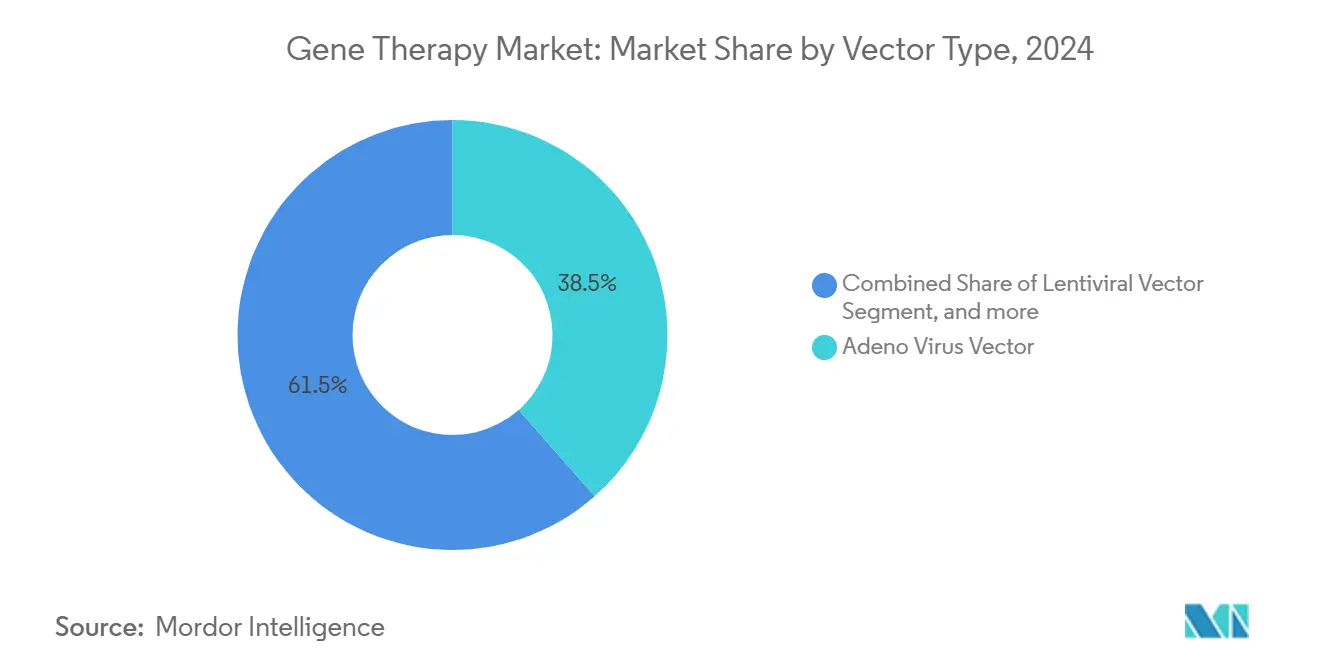
- Por tipo de vector, el Virus Adenoasociado capturó el 38,54% de la cuota del mercado de terapia génica en 2024, mientras que los métodos de administración no virales están preparados para expandirse a una TCAC del 24,34% hasta 2030.
- Por indicación, la oncología comandó el 42,92% de los ingresos en 2024; las aplicaciones neurológicas avanzan a una TCAC del 25,62% hasta 2030.
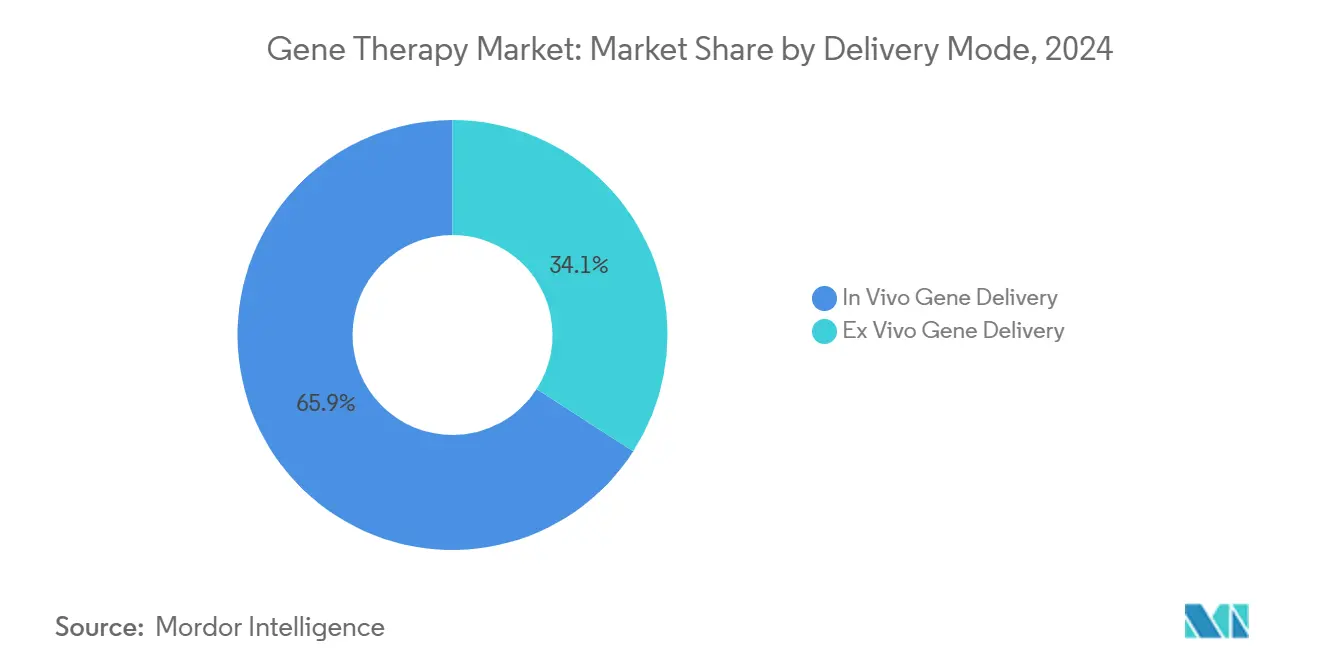
- Por modo de administración, los enfoques in vivo mantuvieron el 65,92% del tamaño del mercado de terapia génica en 2024, mientras que los métodos ex vivo progresarán a una TCAC del 23,07% entre 2025-2030.
- Por usuario final, los hospitales y clínicas representaron el 59,22% de la cuota del tamaño del mercado de terapia génica en 2024; los centros de tratamiento especializado están siguiendo una TCAC del 21,89% hasta 2030.
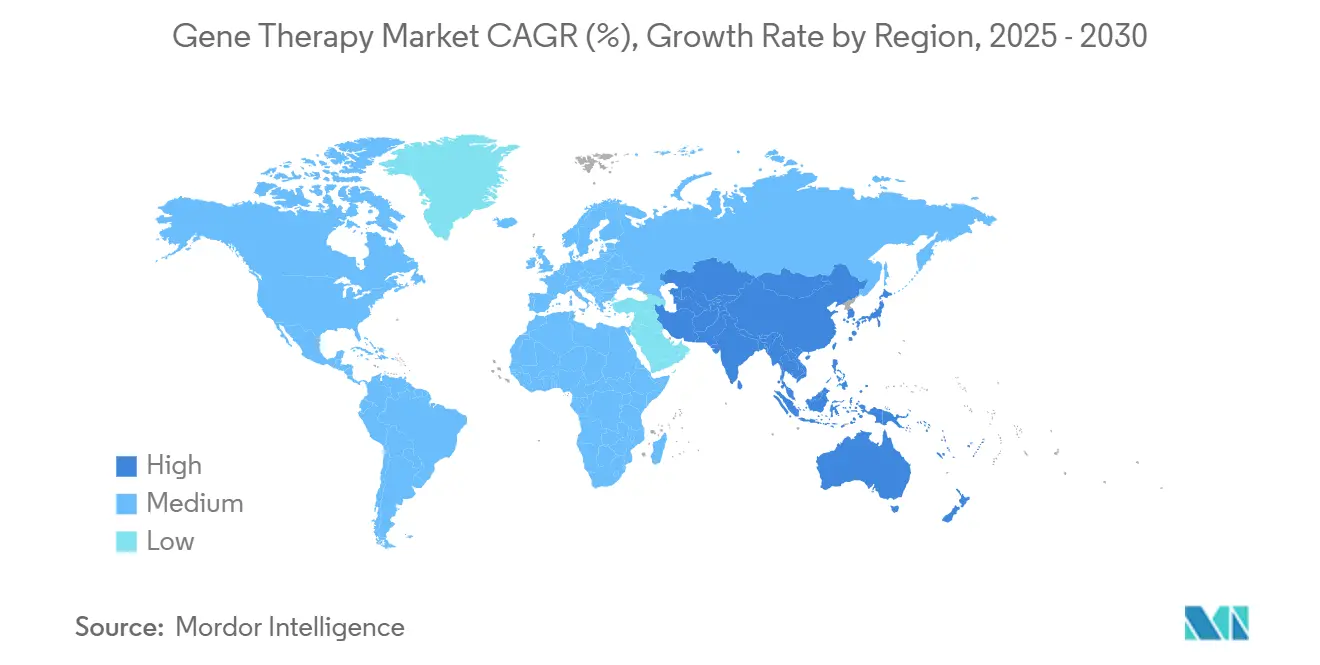
- Por geografía, América del Norte lideró con una cuota de ingresos del 41,78% en 2024; se pronostica que Asia-Pacífico acelere a una TCAC del 27,68% en el mismo horizonte.
Tendencias e Insights del Mercado Global de Terapia Génica
Análisis de Impacto de Impulsores
| Impulsor | (~) % Impacto en Pronóstico TCAC | Relevancia Geográfica | Cronología de Impacto |
|---|---|---|---|
| Aprobaciones regulatorias demostrando viabilidad | +5.2% | Global, concentrado en América del Norte y Europa | Corto plazo (≤ 2 años) |
| Avances en ingeniería de vectores y tecnología in vivo | +4.9% | Adopción temprana en América del Norte y Europa | Largo plazo (≥ 4 años) |
| Expansión de infraestructura de fabricación | +4.8% | América del Norte, Europa, Asia-Pacífico emergente | Mediano plazo (2-4 años) |
| Rápida ampliación de capacidad comercial de AAV CDMO | +3.8% | Global, América del Norte y Europa, expandiéndose a Asia-Pacífico | Mediano plazo (2-4 años) |
| Financiación biofarmacéutica y de capital privado | +3.5% | Centros de innovación en EE.UU., Europa y China | Mediano plazo (2-4 años) |
| Creciente inclusión de terapias génicas para enfermedades raras | +2.7% | Global, con mayor impacto en mercados desarrollados | Largo plazo (≥ 4 años) |
| Fuente: Mordor Intelligence | |||
Crecientes Aprobaciones Regulatorias Demostrando Viabilidad Clínica y Comercial
Las autorizaciones frecuentes de los principales reguladores están reduciendo el riesgo de desarrollo y comprimiendo los cronogramas de lanzamiento. El total acumulativo de la FDA de 37 productos celulares y génicos aprobados para 2024 muestra que los revisores de la agencia ahora aplican marcos dedicados como la designación de Terapia Avanzada de Medicina Regenerativa, que recorta el tiempo de desarrollo en aproximadamente un 40% para programas calificados.[1]Administración de Alimentos y Medicamentos de EE.UU., "Productos de Terapia Celular y Génica Aprobados," fda.govEl esquema PRIME de Europa y la regla de 2025 del Reino Unido para la fabricación en el punto de atención facilitan aún más la entrada al mercado. La aprobación de ZEVASKYN para epidermólisis bullosa distrófica recesiva en 2025 ejemplifica cómo las indicaciones se extienden más allá de las enfermedades ultra-raras hacia segmentos dermatológicos más amplios. Tal alcance terapéutico en expansión apoya el crecimiento multianual en el mercado de terapia génica y estimula la inversión de seguimiento de los pagadores que esperan beneficio clínico duradero.
Continuos Avances Tecnológicos en Ingeniería de Vectores y Plataformas de Edición In Vivo
Las bibliotecas de cápsidas mejoradas, la optimización de secuencias guiada por aprendizaje automático y las construcciones lipídicas novedosas están afilando el tropismo tisular y reduciendo la inmunogenicidad. Los investigadores de la Escuela de Medicina Perelman reportaron nanopartículas lipídicas cargadas de ADN que persisten in vivo durante meses, abriendo dosificación duradera para enfermedades crónicas.[2]Penn Medicine News, "Las Nanopartículas Lipídicas Cargadas de ADN Permanecen Activas Durante Meses," pennmedicine.orgLas plataformas de organoides ofrecen bancos de prueba específicos de tejido humano que mejoran la predictibilidad traslacional, respaldados por la aceptación de la Ley de Modernización de la FDA de modelos no animales. Los algoritmos asistidos por IA como OpenCRISPR-1 cortan ciclos de diseño y elevan la precisión de edición. Colectivamente, estas innovaciones desplazan el techo terapéutico hacia arriba, crean espacio para dosificación repetida y alimentan un bucle virtuoso de éxito clínico y despliegue de capital que amplía el mercado de terapia génica.
Expansión de la Infraestructura Global de Fabricación de Vectores Virales y No Virales
El despliegue de capital a gran escala está impulsando tanto la capacidad como la sofisticación de las líneas de producción. La compra de USD 16,5 mil millones de Catalent por parte de Novo Nordisk en 2024 subraya cómo las grandes farmacéuticas están asegurando el control integral de las cadenas de suministro. Las actualizaciones de vectores virales ahora incorporan biorreactores de flujo continuo y procesamiento descendente de sistema cerrado, reduciendo los tiempos de lote en dos dígitos. Las plataformas no virales de nanopartículas lipídicas reducen el costo de bienes hasta en un 60% y pueden empaquetar cargas útiles más grandes, eliminando barreras técnicas anteriores a indicaciones poligénicas.[3]Editores de Journal of Nanobiotechnology, "Avances en la Entrega de Nanopartículas Lipídicas," springeropen.com La automatización, el análisis de calidad habilitado por IA y los diseños modulares de salas limpias juntos mejoran la confiabilidad, alentando a los fabricantes por contrato a pre-construir suites que pueden ser rápidamente personalizadas para nuevos patrocinadores.
Escalante Financiación Biofarmacéutica y de Capital Privado en I+D de Terapia Génica
Las entradas de capital permanecen resistentes a pesar de la volatilidad del mercado más amplio. Los valores iniciales en acuerdos de licenciamiento externo de Fase II y III subieron un 35% en 2024 mientras se intensificaba la competencia por activos en etapas avanzadas. Sangamo Therapeutics aseguró USD 18 millones por adelantado y potencial de hitos de USD 1,4 mil millones por sus cápsidas dirigidas al SNC con Eli Lilly, ilustrando el apetito de los inversores por vectores de entrega diferenciados. Los grupos de capital privado también se están moviendo aguas abajo; la adquisición de bluebird bio por parte de Carlyle y SK Capital en 2025 inyecta fondos de comercialización en terapias aprobadas para la enfermedad de células falciformes y β-talasemia, demostrando el valor estratégico de los activos comercializados. Tal financiación sostenida acelera la diversificación de la pipeline y sostiene la demanda de servicios de fabricación, reforzando la expansión a largo plazo del mercado de terapia génica.
Análisis de Impacto de Restricciones
| Restricción | (~) % Impacto en Pronóstico TCAC | Relevancia Geográfica | Cronología de Impacto |
|---|---|---|---|
| Altos precios de terapias | -3,8% | Mayor efecto en mercados emergentes y regiones de reembolso restrictivo | Mediano plazo (2-4 años) |
| Complejidad de fabricación y límites de suministro de vectores | -2,6% | Varía según capacidad de producción regional | Corto plazo (≤ 2 años) |
| Preocupaciones de seguridad requiriendo monitoreo a largo plazo | -2,1% | Más intenso donde la supervisión regulatoria es estricta | Largo plazo (≥ 4 años) |
| Escasez de materias primas de plásmidos/cápsidas | -1,9% | Agudo en regiones con resistencia limitada de cadena de suministro | Corto plazo (≤ 2 años) |
| Fuente: Mordor Intelligence | |||
Altos Precios de Terapias Creando Barreras de Acceso y Asequibilidad
Las curas de dosis única comandam precios de lista entre USD 373.000 y USD 4,25 millones, tensionando los presupuestos de pagadores y probando la disposición social para financiar terapias curativas. Los proveedores citan brechas de apoyo social, distancia de viaje y obstáculos de autorización previa como los principales bloqueadores de acceso. Las opciones de reembolso innovadoras-contratos basados en resultados, modelos de amortización y garantías están emergiendo pero aún requieren intercambio de datos complejos e infraestructura de seguimiento a largo plazo. Los Centros de Servicios de Medicare y Medicaid lanzaron un Modelo de Acceso a Terapia Celular y Génica en 2025 que alienta las compras agrupadas a nivel estatal para temperar el impacto presupuestario. Estos vientos en contra financieros se espera que moderen la adopción en regiones sensibles a los costos, suavizando la curva de crecimiento del mercado de terapia génica a pesar de las fuertes proposiciones de valor clínico.
Complejidad de Fabricación y Suministro Limitado de Vectores de Grado GMP
Incluso con construcciones agresivas de capacidad, el suministro de vectores AAV y lentivirales de grado GMP cumple solo una cuarta parte de la demanda proyectada para 2025. Los ciclos de producción pueden exceder nueve meses, retrasando los cronogramas de lanzamiento y creando riesgo de inventario. Las soluciones descentralizadas emergentes como los pods modulares de salas limpias reducen los costos por dosis de aproximadamente USD 400.000 a menos de USD 35.000 en configuraciones piloto, aunque la armonización regulatoria sigue siendo un desafío. Hasta que tales modelos escalen, la disponibilidad limitada de vectores continuará actuando como un freno estructural en el mercado de terapia génica.
Análisis de Segmentos
Por Tipo de Vector: AAV Domina Mientras los Métodos No Virales Surgen
Los vectores AAV mantuvieron el 38,54% de la cuota del mercado de terapia génica en 2024 debido al perfil de seguridad favorable y la expresión sostenida de transgenes que sustentan múltiples productos aprobados para hemofilia y trastornos retinianos hereditarios. Este liderazgo se ve reforzado por el amplio tropismo tisular y un pool en expansión de serotipos modificados que mejoran la especificidad. Sin embargo, los sistemas no virales de nanopartículas lipídicas son la alternativa de más rápido crecimiento, pronosticada para registrar una TCAC del 24,34% hasta 2030 ya que transportan cargas genéticas más grandes y simplifican la economía de fabricación. Por tanto, el tamaño del mercado de terapia génica para plataformas no virales está preparado para cerrar parte de la brecha de ingresos actual. Los vectores lentivirales siguen siendo el pilar para la fabricación ex vivo de CAR-T, mientras que los sistemas basados en herpes ganan tracción en oncología por su capacidad de carga útil. La optimización continua de bibliotecas de cápsidas y promotores sintéticos determinará si los vectores virales pueden defender la cuota contra desafiantes no virales costo-eficientes.
El auge en enfoques no virales también alivia las limitaciones de materias primas porque los componentes lipídicos son susceptibles a cadenas de suministro farmacéutico estándar. Las nanopartículas cargadas de ADN que permanecen activas durante meses reducen los requerimientos de dosificación repetida y pueden ser ajustadas para captación selectiva de órganos. Tal flexibilidad atrae a desarrolladores que apuntan a trastornos neurológicos poligénicos donde el tamaño de la carga útil excede el límite de empaquetado del AAV. Consecuentemente, la dinámica competitiva dentro del mercado de terapia génica está cambiando de disponibilidad de vectores hacia precisión de entrega, creando espacio para CDMOs agnósticos de plataforma para capturar demanda emergente.

Por Indicación: Oncología Lidera Mientras Neurología Acelera
Las aplicaciones oncológicas generaron el 42,92% de los ingresos en 2024, respaldadas por un flujo constante de aprobaciones CAR-T y una pipeline profunda dirigida a tumores sólidos. La evidencia robusta para respuestas completas en malignidades hematológicas recidivantes sostiene la aceptación del pagador a pesar de las presiones de precios. Sin embargo, la neurología reclama la trayectoria de crecimiento más alta con una TCAC del 25,62% hasta 2030. Las cápsidas emergentes que cruzan la barrera hematoencefálica y las herramientas de edición in vivo precisas permiten intervención directa en trastornos como el síndrome de Rett y la enfermedad de Huntington. Se espera que el tamaño del mercado de terapia génica asignado a trastornos del SNC se multiplique mientras los incentivos regulatorios bilaterales comprimen el riesgo de desarrollo.
Las indicaciones metabólicas raras y de oftalmología continúan generando nuevas aprobaciones porque el privilegio inmune del tejido y los biomarcadores claros simplifican los puntos finales clínicos. Los objetivos cardiovasculares como la cardiomiopatía hipertrófica están ganando financiación de capital de riesgo, sugiriendo una absorción más amplia de enfermedades sistémicas. Mientras la amplitud terapéutica se amplía, la optimización del portafolio se vuelve crítica; los patrocinadores deben equilibrar los flujos de caja de oncología con activos de neurología de alto potencial pero científicamente complejos.
Por Modo de Administración: In Vivo Domina Mientras Ex Vivo Gana Impulso
La administración directa comandó el 65,92% de los ingresos en 2024, principalmente debido a aprobaciones para trastornos oculares, musculares y hepáticos donde la inyección localizada maximiza la eficiencia del vector. La dosificación in vivo elimina pasos de procesamiento celular, acorta los cronogramas de tratamiento y se ajusta a los flujos de trabajo hospitalarios existentes, manteniendo así su liderazgo. Sin embargo, la ingeniería ex vivo está en camino para una TCAC del 23,07% ya que la automatización de fabricación, la transducción viral mejorada y las plataformas alogénicas reducen los costos por paciente. La pipeline creciente de células inmunes modificadas para enfermedades autoinmunes muestra la versatilidad ex vivo más allá de la oncología. Como tal, el mercado de terapia génica se beneficia del crecimiento complementario a través de ambos canales de entrega, reduciendo la dependencia excesiva de cualquier modalidad única y suavizando los requerimientos de la cadena de suministro.
Los protocolos ex vivo optimizados ahora logran mayor viabilidad celular y eficiencia de transferencia génica, factores que previamente obstaculizaban los resultados clínicos. Las estrategias de scale-out y la producción en el punto de atención reducen aún más la complejidad logística, sentando las bases para centros de infusión basados en la comunidad. Con el tiempo, la convergencia de costos entre modalidades puede alentar a los patrocinadores a seleccionar la entrega basada únicamente en la idoneidad biológica en lugar de la practicabilidad de fabricación.

Por Usuario Final: Hospitales Lideran Mientras Centros Especializados Se Expanden Rápidamente
Los hospitales y centros médicos académicos representaron el 59,22% del volumen de administración en 2024 porque poseen equipos multidisciplinarios y ambientes controlados necesarios para la infusión de terapia génica. Estas instituciones a menudo sirven como sitios de ensayos, creando una transición sin problemas del estudio al estándar de atención. Sin embargo, se proyecta que las instalaciones de infusión especializadas crezcan a una TCAC del 21,89% hasta 2030. Sus modelos operativos lean reducen los costos del sitio de atención y mejoran la conveniencia del paciente, particularmente donde la distancia de viaje a centros terciarios es una barrera. Por tanto, el tamaño del mercado de terapia génica capturado por centros dedicados está preparado para subir mientras los pagadores incentivan entornos de menor costo.
Los institutos de investigación académica retienen influencia al hospedar estudios de primera-en-humanos y refinar protocolos de fabricación. Los hospitales comunitarios están integrando gradualmente flujos de trabajo de tratamiento validados, ayudados por plataformas de monitoreo remoto que minimizan visitas hospitalarias repetidas. La expansión del cuidado descentralizado amplía el acceso regional y apoya mayor rendimiento procesal, abordando una limitación crítica de capacidad mientras más productos ganan aprobación.
Análisis Geográfico
América del Norte mantuvo el 41,78% de los ingresos globales en 2024, sostenido por un ambiente regulatorio acomodativo, pools de capital de riesgo profundos y extensa infraestructura clínica. Estados Unidos aprobó 34 terapias génicas de primera en clase solo en 2024, destacando su papel central en la secuenciación de lanzamiento de productos. Las iniciativas federales como las subvenciones ARPA-H canalizan fondos significativos hacia la innovación de fabricación y vigilancia de seguridad, reforzando el liderazgo de la región en el mercado de terapia génica.
Europa mantiene una fuerte producción científica y se beneficia de las vías adaptativas de la EMA que aceleran tratamientos innovadores. El próximo marco del Reino Unido para fabricación descentralizada, efectivo en julio de 2025, puede reducir cargas logísticas y estimular la producción en el punto de atención. Sin embargo, las políticas de reembolso nacional desiguales prolongan el tiempo-al-paciente a través del bloque; la nueva regulación de Evaluación de Tecnología Sanitaria de la UE en 2025 busca armonizar los requisitos de evidencia pero también podría alargar las negociaciones. Los modelos de pago basados en resultados, como demuestran los acuerdos de Hemgenix en Inglaterra y Dinamarca, están aliviando gradualmente los obstáculos de adopción.
Asia-Pacífico registra el crecimiento más rápido con una TCAC del 27,68%. China hospeda más de 400 estudios basados en células e invierte fuertemente en plantas de vectores domésticas, posicionándose como motor tanto de demanda como de suministro. Las vías aceleradas de Japón para medicinas regenerativas y el portal de licenciamiento digital de Singapur agilizan aún más las aprobaciones. Mientras los estándares regulatorios convergen con las agencias occidentales, el reembolso variable y los controles de exportación sobre materiales genéticos siguen siendo desafíos. El apoyo político continuo y los CDMOs locales en maduración no obstante aseguran que Asia-Pacífico capturará una proporción creciente del mercado de terapia génica.
Panorama Competitivo
Principales Empresas en el Mercado de Terapia Génica
El terreno competitivo está moderadamente fragmentado, poblado por incumbentes farmacéuticos experimentados e innovadores biotecnológicos ágiles. Las casas de gran-pharma como Novartis, Pfizer y Roche están adquiriendo tecnologías de plataforma para compensar los acantilados de patentes; la asociación de Novo Nordisk con 2seventy bio ejemplifica la diversificación del portafolio hacia la edición génica. La actividad de asociación alcanzó 90 acuerdos en el Q1 2025, reflejando el intenso scouting para ingeniería de cápsidas, entrega no viral y fabricación escalable.
La diferenciación tecnológica impulsa la ventaja competitiva. Krystal Biotech aprovecha un vector HSV-1 patentado que permite administración tópica repetida; su producto VYJUVEK generó USD 341,2 millones desde el lanzamiento y logró una cobertura del 97% en EE.UU., demostrando prueba comercial de aplicaciones dermatológicas de enfermedades raras. La integración de IA es otro campo de batalla: la empresa conjunta de MeiraGTx con Hologen Neuro AI aplica bucles de diseño de aprendizaje profundo a cápsidas del SNC, mientras que Amgen reportó un aumento de ingresos del 19% en 2024 ayudado por cargas útiles de ARN modificadas que capitalizan la optimización guiada por aprendizaje automático.
Las oportunidades de espacio en blanco incluyen expansión de capacidad de vectores, indicaciones no oncológicas dirigidas y marcos de financiación novedosos que igualan los beneficios de terapia de una sola vez con ahorros de costos multianuales. Las organizaciones de desarrollo y fabricación por contrato que ofrecen servicios llave en mano, agnósticos de plataforma, están preparadas para ganar cuota mientras los patrocinadores más pequeños externalizan la producción. Mientras la pipeline se diversifica y proliferan las vías de aprobación regionales, el mercado de terapia génica recompensa a los jugadores que combinan profundidad científica con agilidad de cadena de suministro.
Líderes de la Industria de Terapia Génica
-
Gilead Sciences, Inc.
-
Amgen Inc.
-
Novartis AG
-
bluebird bio Inc.
-
Biogen Inc.
- *Nota aclaratoria: los principales jugadores no se ordenaron de un modo en especial


Desarrollos Recientes de la Industria
- Mayo 2025: Sarepta Therapeutics, Inc., un líder en medicina genética de precisión para enfermedades raras, ha asegurado una aprobación fundamental del Ministerio de Salud, Trabajo y Bienestar de Japón (MHLW) para su medicamento, ELEVIDYS (delandistrogeno moxeparvovec). Esta aprobación, otorgada bajo la vía condicional y de tiempo limitado de Japón, se dirige a la distrofia muscular de Duchenne (DMD). Específicamente, ELEVIDYS está sancionado para niños de 3 a menos de 8 años, siempre que carezcan de deleciones en el exón 8 y/o exón 9 del gen DMD y den negativo para anticuerpos anti-AAVrh74. Notablemente, esto marca el primer respaldo global para tratar DMD en niños menores de 4 años.
- Mayo 2025: Abeona Therapeutics recibió aprobación de la FDA para ZEVASKYN, la primera terapia génica basada en células para epidermólisis bullosa distrófica recesiva (RDEB), demostrando sanación efectiva de heridas en ensayos clínicos.
- Febrero 2025: Genprex, Inc., una firma de terapia génica en etapa clínica, está progresando en su programa de terapia génica para diabetes, reforzada por una colaboración con la Universidad de Pittsburgh. Las dos entidades han simplificado los acuerdos de licencia previos de Genprex con Pitt en un único acuerdo exclusivo. Este nuevo pacto abarca múltiples tecnologías dirigidas a crear un producto de terapia génica para diabetes Tipo 1 y Tipo 2. Además, Genprex ha establecido una subsidiaria de propiedad total, Convergen Biotech, Inc., dedicada a avanzar sus iniciativas de diabetes.
- Octubre 2024: El Gobernador Hochul anunció un desarrollo significativo para el mercado de terapia génica con el lanzamiento de la siguiente fase del Parque de Biogénesis de Nueva York de Long Island, un centro de innovación de terapia celular y génica líder en la nación. Este proyecto de USD 430 millones busca acelerar la investigación, desarrollo y comercialización de terapias que salvan vidas. El compromiso de USD 150 millones del estado marca la mayor inversión estatal en terapia celular y génica a nivel nacional, avanzando aún más la visión de Nueva York de establecer liderazgo en este campo crítico.
- Septiembre 2024: Genprex, Inc., una empresa de terapia génica en etapa clínica dedicada a ser pionera en terapias transformadoras para pacientes con cáncer y diabetes, ha revelado planes para transferir su programa de desarrollo clínico para diabetes y activos de terapia génica asociados a una subsidiaria de nueva creación y propiedad total. Esta nueva entidad, denominada "NewCo", se centrará en el avance y comercialización de GPX-002, un candidato de terapia génica dirigido tanto a diabetes Tipo 1 (T1D) como Tipo 2 (T2D).
Alcance del Informe Global del Mercado de Terapia Génica
Según el alcance de este informe, la terapia génica es un tratamiento médico avanzado que involucra la transferencia de un gen estándar o saludable para reemplazar un gen defectuoso en una célula. Puede curar varios trastornos crónicos y genéticos en seres humanos, para los cuales no se ha desarrollado cura final. El mercado se segmenta por Indicación (Cáncer, Trastornos Metabólicos, Trastornos Oculares, Atrofia Muscular Espinal y Otras Indicaciones), Tecnología (Vector de Adenovirus, Vector Virus Adenoasociado, Vector Lentiviral, Vector Retroviral, Vector de Virus Herpes y Otras Tecnologías), y Geografía (América del Norte, Europa, Asia-Pacífico, Oriente Medio y África, y América del Sur). El informe del mercado también cubre los tamaños de mercado estimados y tendencias para 17 países a través de las principales regiones globalmente. El informe ofrece el valor (en millones USD) para los segmentos anteriores.
| Vector de Adenovirus |
| Vector Virus Adenoasociado |
| Vector Lentiviral |
| Vector Retroviral |
| Vector de Virus Herpes |
| Otros Tipos de Vectores |
| Oncología |
| Trastornos Metabólicos Raros |
| Oftalmología |
| Neurología / SNC |
| Cardiovascular y Musculoesquelético |
| Otras Indicaciones |
| Administración Génica In Vivo |
| Administración Génica Ex Vivo |
| Hospitales y Clínicas |
| Centros de Tratamiento / Infusión Especializados |
| Institutos Académicos y de Investigación |
| América del Norte | Estados Unidos |
| Canadá | |
| México | |
| Europa | Alemania |
| Reino Unido | |
| Francia | |
| Italia | |
| España | |
| Resto de Europa | |
| Asia-Pacífico | China |
| Japón | |
| India | |
| Australia | |
| Corea del Sur | |
| Resto de Asia-Pacífico | |
| Oriente Medio y África | CCG |
| Sudáfrica | |
| Resto de Oriente Medio y África | |
| América del Sur | Brasil |
| Argentina | |
| Resto de América del Sur |
| Por Tipo de Vector | Vector de Adenovirus | |
| Vector Virus Adenoasociado | ||
| Vector Lentiviral | ||
| Vector Retroviral | ||
| Vector de Virus Herpes | ||
| Otros Tipos de Vectores | ||
| Por Indicación | Oncología | |
| Trastornos Metabólicos Raros | ||
| Oftalmología | ||
| Neurología / SNC | ||
| Cardiovascular y Musculoesquelético | ||
| Otras Indicaciones | ||
| Por Modo de Administración | Administración Génica In Vivo | |
| Administración Génica Ex Vivo | ||
| Por Usuario Final | Hospitales y Clínicas | |
| Centros de Tratamiento / Infusión Especializados | ||
| Institutos Académicos y de Investigación | ||
| Por Geografía | América del Norte | Estados Unidos |
| Canadá | ||
| México | ||
| Europa | Alemania | |
| Reino Unido | ||
| Francia | ||
| Italia | ||
| España | ||
| Resto de Europa | ||
| Asia-Pacífico | China | |
| Japón | ||
| India | ||
| Australia | ||
| Corea del Sur | ||
| Resto de Asia-Pacífico | ||
| Oriente Medio y África | CCG | |
| Sudáfrica | ||
| Resto de Oriente Medio y África | ||
| América del Sur | Brasil | |
| Argentina | ||
| Resto de América del Sur | ||


Preguntas Clave Respondidas en el Informe
¿Cuál es el valor actual del mercado de terapia génica?
El mercado de terapia génica está valorado en USD 9,74 mil millones en 2025 y se proyecta que suba a USD 24,34 mil millones en 2030.
¿Qué tipo de vector lidera las ventas globales?
Los vectores de Virus Adenoasociado representan el 38,54% de los ingresos de 2024 debido a su perfil de seguridad y expresión duradera.
¿Por qué Asia-Pacífico está creciendo tan rápidamente?
Asia-Pacífico registra una TCAC del 27,68% debido a la fuerte financiación gubernamental, el volumen en expansión de ensayos clínicos en China y las vías de aprobación simplificadas en Japón y Singapur.
¿Cómo están gestionando los pagadores los altos costos de terapias?
Los sistemas de salud emplean contratos basados en resultados, pagos amortizados y modelos de compra estatal agrupada como el Modelo de Acceso a Terapia Celular y Génica de CMS.
¿Qué factor más limita el crecimiento del mercado hoy?
La complejidad de fabricación y el suministro limitado de vectores de grado GMP continúan limitando la disponibilidad de productos a corto plazo y elevan el costo de bienes.
Última actualización de la página el:










