Taille et part du marché de la technologie de l'ADN recombinant (rDNA)
Analyse du marché de la technologie de l'ADN recombinant (rDNA) par Mordor Intelligence
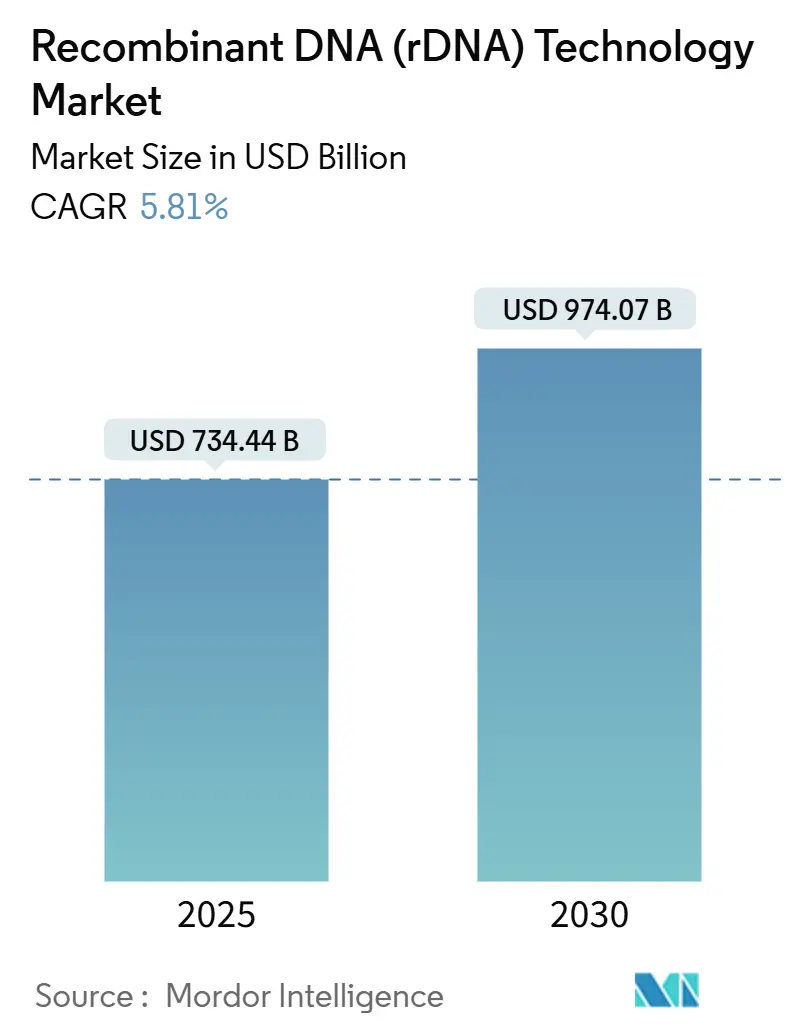
Le marché de la technologie de l'ADN recombinant un atteint 734,44 milliards USD en 2025 et devrait grimper à 974,07 milliards USD d'ici 2030, reflétant un TCAC de 5,81 %. La demande pour les thérapeutiques protéiques recombinantes, l'accélération des baisses de coûts CRISPR, et la démocratisation de la conception protéique assistée par IA continuent de remodeler l'économie de l'industrie, abaissant les barrières à l'entrée pour les petits innovateurs tout en récompensant les entreprises établies qui modernisent leurs empreintes de production. La baisse des prix pour les bioréacteurs à usage unique et les micro-usines de plasmides permet désormais aux développeurs de basculer entre les projets thérapeutiques et agricoles sans changements de ligne coûteux, encourageant l'expansion du portefeuille vers l'alimentation, l'alimentation animale et les services environnementaux. L'Amérique du Nord ancre toujours le financement et les essais de phase précoce, mais l'Asie-Pacifique installe des capacités à un rythme plus rapide, réduisant les écarts de compétences historiques et favorisant les chaînes d'approvisionnement locales qui diminuent le risque géopolitique pour les licenciés mondiaux. L'intensité concurrentielle monte alors que les leaders pharmaceutiques, les majors agricoles et les CDMO spécialisés en thérapie génique rivalisent tous pour les mêmes matières premières de vecteurs et la bande passante réglementaire.
Points clés du rapport
- Par produit, les applications médicales ont détenu 65,35 % de part de revenus en 2024, tandis que les produits non médicaux devraient croître à un TCAC de 12,25 % jusqu'en 2030.
- Par composant, les systèmes d'expression ont commandé 64,53 % de la part du marché de la technologie de l'ADN recombinant en 2024 ; les vecteurs de clonage s'étendent à un TCAC de 9,85 % jusqu'en 2030.
- Par application, la santé et les maladies ont représenté 46,62 % de part de la taille du marché de la technologie de l'ADN recombinant en 2024 ; les utilisations environnementales progressent à un TCAC de 12,52 % jusqu'en 2030.
- Par utilisateur final, les entreprises biotech et pharmaceutiques ont détenu 53,82 % de part en 2024, tandis que les instituts académiques et gouvernementaux sont projetés à augmenter à un TCAC de 9,61 % d'ici 2030.
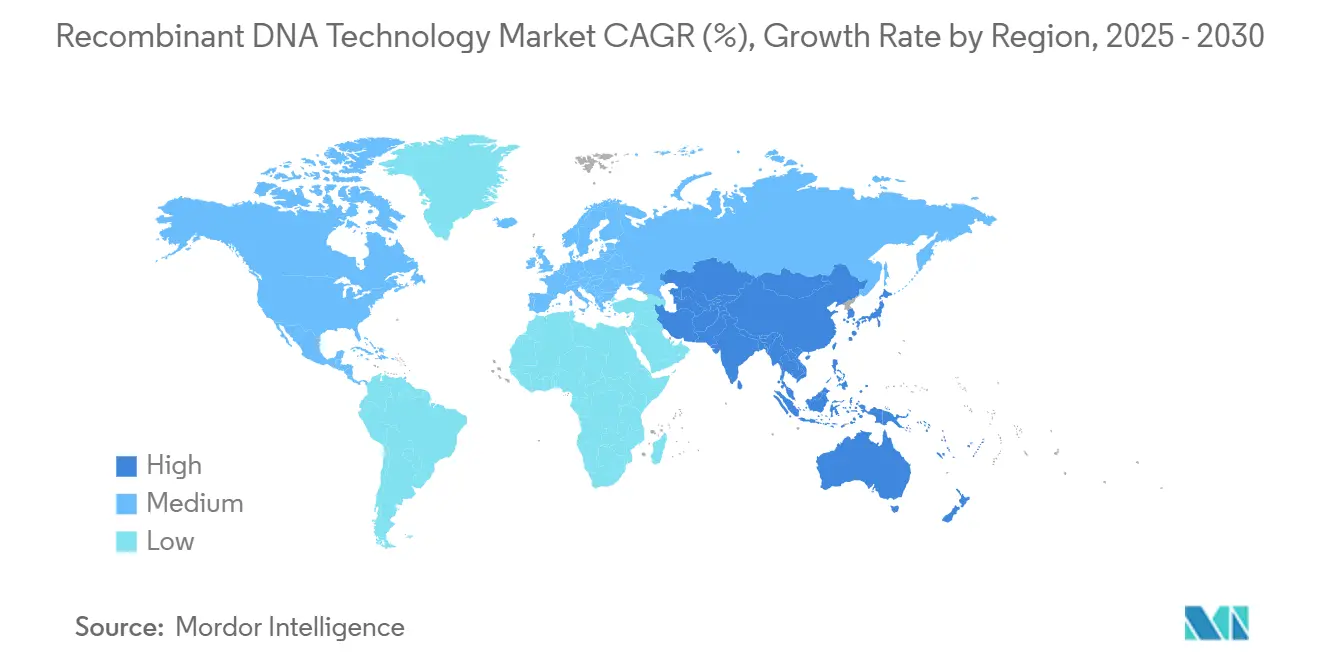
- Par géographie, l'Amérique du Nord menait avec 37,82 % de part en 2024, mais l'Asie-Pacifique est la région à croissance la plus rapide à un TCAC de 11,81 % jusqu'en 2030.
Tendances et perspectives du marché mondial de la technologie de l'ADN recombinant (rDNA)
Analyse d'impact des moteurs
| Moteur | (~) % Impact sur les prévisions TCAC | Pertinence géographique | Calendrier d'impact |
|---|---|---|---|
| La courbe de coût CRISPR-Cas continue de baisser | +1.2% | Mondiale, avec adoption précoce en Amérique du Nord et UE | Moyen terme (2-4 ans) |
| Demande biopharma pour les médicaments protéiques recombinants | +1.8% | Mondiale, concentrée dans les marchés développés | Long terme (≥ 4 ans) |
| Expansion de l'acreage de cultures GM dans les marchés émergents | +0.9% | Cœur APAC, débordement vers l'Amérique latine et l'Afrique | Long terme (≥ 4 ans) |
| Plateformes de conception protéique de novo pilotées par IA | +0.7% | Amérique du Nord et UE, expansion vers l'APAC | Moyen terme (2-4 ans) |
| Micro-usines d'ADN plasmidique distribuées à usage unique | +0.5% | Mondiale, avec adoption plus rapide dans les marchés émergents | Court terme (≤ 2 ans) |
| Source: Mordor Intelligence | |||
La courbe de coût CRISPR-Cas continue de baisser
L'élargissement de l'accès aux kits d'édition nucléase, la synthèse d'ARN guide moins chère, et l'augmentation des rendements de vecteurs ont poussé le coût entièrement chargé des thérapies CRISPR à la baisse fortement. Le succès clinique de CASGEVY dans la drépanocytose un validé la modalité, même à un prix initial proche de 3 millions USD par patient. Aldevron un ensuite réduit le temps de fabrication CRISPR personnalisé à six mois, prouvant que les gains de temps de cycle sont réalistes alors que les chaînes d'approvisionnement mûrissent[1]Aldevron, "World's First mRNA-Based Personalized CRISPR Therapy," aldevron.com. Un record de 14 désignations de révision américaines en 2024 un signalé que les régulateurs gagnent en confiance, réduisant les primes de risque de développement. Alors que les coûts tendent vers le bas, les développeurs pivotent des cibles de maladies ultra-rares vers les troubles prévalents, élargissant le bassin adressable du marché de la technologie de l'ADN recombinant.
Demande biopharma pour les médicaments protéiques recombinants
Novo Nordisk un alloué 4,1 milliards USD pour un nouveau site en Caroline du Nord axé sur les protéines recombinantes injectables, soulignant la demande persistante dans les soins du diabète et de l'obésité[2]CNBC, "Novo Nordisk to Build USD 4.1 Billion nord Carolina Installation," cnbc.com. L'investissement de 3 milliards USD d'Eli Lilly dans le Wisconsin et le bond de 35 % des revenus biosimilaires Q1 2025 d'Amgen à 700 millions USD suggèrent que l'offre, pas la demande, est le goulot d'étranglement actuel. Les bioréacteurs à flux continu et les lignes modulaires à usage unique abaissent l'échelle efficace minimale, permettant aux petites biotechs de commercialiser des protéines ciblées sans soutien de grande pharma, élargissant ainsi la participation concurrentielle dans le marché de la technologie de l'ADN recombinant.
Expansion de l'acreage de cultures GM dans les marchés émergents
La Chine un autorisé plusieurs cultures biotechnologiques en 2024 tandis que le Kenya un commercialisé le coton Bt, inversant l'hésitation réglementaire antérieure. La Loi britannique sur l'élevage de précision distingue désormais les traits édités génétiquement des transgéniques, une nuance attendue pour imprégner les débats politiques de l'UE. L'approbation par le Ghana du niébé GM riche en nutriments montre comment les objectifs de sécurité alimentaire peuvent accélérer les révisions. Le lancement par Bayer du soja Vyconic avec cinq tolérances aux herbicides souligne que l'empilement de traits avancés commande désormais un prix premium justifié par des pressions complexes de mauvaises herbes. Ces changements élargissent collectivement la demande agricole pour les vecteurs recombinants, soulevant les perspectives de croissance à long terme pour le marché de la technologie de l'ADN recombinant.
Plateformes de conception protéique de novo pilotées par IA
La série B de 73 millions USD de Cradle et le partenariat IA d'Illumina avec NVIDIA révèlent comment la conception guidée par algorithme comprime les délais de découverte. L'IA propose désormais des plis protéiques inatteignables par l'évolution naturelle, élargissant la portée thérapeutique. Le pacte de 1,9 milliard USD de Novo Nordisk et Moderna avec Life Edit reflète une tendance plus large de pharma externalisant la conception computationnelle vers des partenaires spécialisés. Les acteurs de la biotechnologie industrielle déploient des enzymes conçues par IA pour améliorer les rendements chimiques, prouvant la valeur commerciale hors des soins de santé. Alors que ces plateformes deviennent clés en main, elles formeront l'épine dorsale numérique des nouveaux entrants, accélérant la rivalité à travers chaque couche du marché de la technologie de l'ADN recombinant.
Analyse d'impact des contraintes
| Contrainte | (~) % Impact sur les prévisions TCAC | Pertinence géographique | Calendrier d'impact |
|---|---|---|---|
| Évolution des réglementations mondiales d'édition génique | -0.8% | Mondiale, avec variations régionales de rigueur | Moyen terme (2-4 ans) |
| Complexité de fabrication et CAPEX | -1.1% | Mondiale, concentrée dans les marchés développés | Long terme (≥ 4 ans) |
| Pénuries de matières premières de vecteurs de qualité pharmaceutique | -0.6% | Mondiale, aiguë en Amérique du Nord et UE | Court terme (≤ 2 ans) |
| Recul des consommateurs sur les aliments édités génétiquement | -0.4% | UE et marchés APAC sélectionnés, impact américain limité | Moyen terme (2-4 ans) |
| Source: Mordor Intelligence | |||
Évolution des réglementations mondiales d'édition génique
La supervision fragmentée force les développeurs à naviguer plusieurs formats de dossiers, protocoles cliniques parallèles, et mandats de surveillance post-commercialisation divergents. Le pilote CoGenT mondial de la FDA cherche l'alignement, pourtant le modèle d'évaluation des risques européen diffère encore de la pondération bénéfice-risque américaine[3]Greenberg Traurig LLP, "FDA Takes First Step Toward International Regulation of Gene Therapies," gtlaw.com. La Chine révise ses règles de thérapie génique, créant de l'incertitude pour les détenteurs de licences étrangères même en accélérant les voies pour les entreprises domestiques. Les exigences de suivi de quinze ans aux États-Unis étirent l'endurance financière des petits développeurs, consolidant le pouvoir parmi les incumbents riches en liquidités. Collectivement, la divergence réglementaire ralentit les lancements de produits et augmente les coûts de conformité, tempérant la croissance à court terme pour le marché de la technologie de l'ADN recombinant.
Complexité de fabrication et CAPEX
L'accord Solventum de 4,1 milliards USD de Thermo Fisher et le rachat Vacaville de 1,2 milliard USD de Lonza soulignent la prime sur la capacité cGMP existante. Les suites de vecteurs viraux exigent un zonage HEPA, une CVC séparée, et des systèmes d'élimination haute puissance, poussant les coûts de construction au-delà de 600 millions USD pour une installation de 30 000 litres. Le matériel à usage unique réduit le temps de mise en service mais gonfle les dépenses consommables, forçant les opérateurs à équilibrer les économies capex contre des coûts unitaires plus élevés. Même les grands acteurs biopharma verrouillent des créneaux CDMO multi-années pour couvrir le risque de capacité, un signe précoce que les contraintes d'offre pourraient plafonner les volumes à court terme dans le marché de la technologie de l'ADN recombinant.
Analyse par segment
Par produit : les applications médicales stimulent les revenus actuels
Les produits médicaux ont contribué 65,35 % des revenus globaux en 2024, ancrés par des protéines thérapeutiques matures qui bénéficient de décennies d'optimisation de processus et de canaux de remboursement bien établis. Le sous-ensemble d'agents thérapeutiques maintient l'élan grâce à l'expansion des pipelines GLP-1 et oncologiques, même alors que les entrants biosimilaires grignotent les monopoles hérités. Les vaccins ont gagné une nouvelle vie après que le COVID-19 ait validé les plateformes ARNm ; les essais de vaccins oncologiques exploitent désormais le même châssis lipide-nanoparticule, réduisant les budgets précliniques. En dehors des soins de santé, les produits non médicaux augmentent à un TCAC de 12,25 % sur le dos des cultures GM qui renforcent la tolérance à la sécheresse et des produits chimiques spécialisés qui remplacent les intermédiaires pétrochimiques. Les enzymes industrielles nettoient désormais les textiles à des températures plus basses, économisant l'énergie et créant des redevances récurrentes pour les concédants d'enzymes, une illustration de la résilience des revenus qui amortit la cyclicité des ventes de médicaments.
Les produits chimiques spécialisés exploitent les voies recombinantes pour produire des tensioactifs et des précurseurs de parfum dans des fermenteurs, produisant des émissions plus faibles par rapport aux voies pétrolières et s'alignant avec les engagements nets zéro des entreprises. Les organismes de remédiation environnementale digèrent les marées noires et les débris plastiques, lançant des niches de service entièrement nouvelles pour les startups de biologie synthétique. Cette diversification élargit le marché de la technologie de l'ADN recombinant, réduit la dépendance aux cycles de vie des médicaments blockbusters, et soutient des flux de trésorerie stables à travers les cycles économiques.
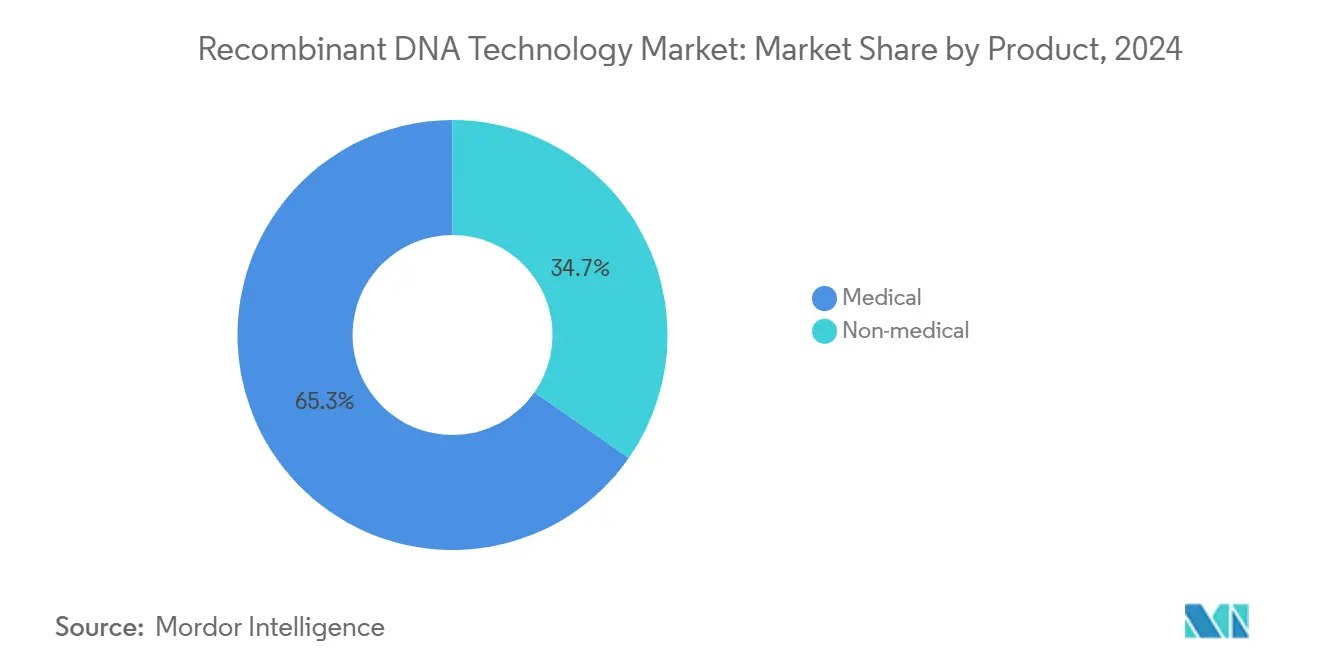
Note: Parts de segment de tous les segments individuels disponibles à l'achat du rapport
Par composant : les systèmes d'expression maintiennent la dominance
Les systèmes d'expression ont représenté une tranche de 64,53 % de la part du marché de la technologie de l'ADN recombinant en 2024, reflétant leur caractère indispensable à travers les thérapeutiques humaines, les vaccins animaux, et les enzymes industrielles. Les hôtes de cellules mammaliennes commandent une tarification premium parce qu'ils effectuent une glycosylation de type humain, un must pour les anticorps complexes. Les lignes bactériennes et de levure restent les chevaux de bataille pour la production d'insuline et d'enzymes, favorisées pour les temps de doublement rapides et les coûts de milieux plus bas. Les vecteurs de clonage, croissant à un TCAC de 9,85 %, sont propulsés par la montée en flèche des essais de thérapie génique qui nécessitent des plasmides de haute qualité et des épines dorsales virales.
Les micro-usines de plasmides à usage unique s'intègrent désormais dans les empreintes de laboratoire standard, permettant aux hôpitaux de créer des vecteurs personnalisés pour les cas d'usage compassionnel. Les vecteurs adéno-associés et lentiviraux atteignent des prix jusqu'à 200 000 USD par lot, créant des micro-segments lucratifs pour les CDMO spécialisés. La propagation de la fabrication distribuée est particulièrement prononcée dans les pipelines de maladies rares à faible volume, où la production localisée évite les retards de chaîne froide et allège les goulots d'étranglement douaniers.
Par application : la dominance santé fait face au défi environnemental
La santé et les maladies ont conservé 46,62 % des revenus en 2024 alors que les anticorps monoclonaux, les thérapies CAR-T, et les remplacements géniques ont sécurisé des victoires réglementaires à travers l'oncologie et l'hématologie. Les développeurs en oncologie prisent les anticorps recombinants pour leur spécificité, se traduisant par une survie sans progression supérieure dans les essais de phase tardive. Les traitements de maladies rares exploitent les incitations orphelines pour compenser les petites cohortes, résultant en des prix catalogue élevés qui soutiennent les marges. L'Amérique du Nord un commandé 37,82 % de la taille du marché de la technologie de l'ADN recombinant en 2024, montrant que le centre de gravité financier du segment reste dans les systèmes de santé des marchés développés.
Les applications environnementales évoluent le plus rapidement à un TCAC de 12,52 %, propulsées par les subventions gouvernementales pour la capture carbone, le traitement des eaux usées, et les services de dégradation plastique. Les microbes recombinants qui métabolisent le méthane en protéine alimentaire présentent des avantages doubles climat et sécurité alimentaire, attirant les afflux de capital d'impact. La variance réglementaire de la biotechnologie agricole à travers les pays tempère encore l'adoption universelle, pourtant les approbations des marchés émergents au Ghana et au Kenya font allusion à une acceptation accélérée.
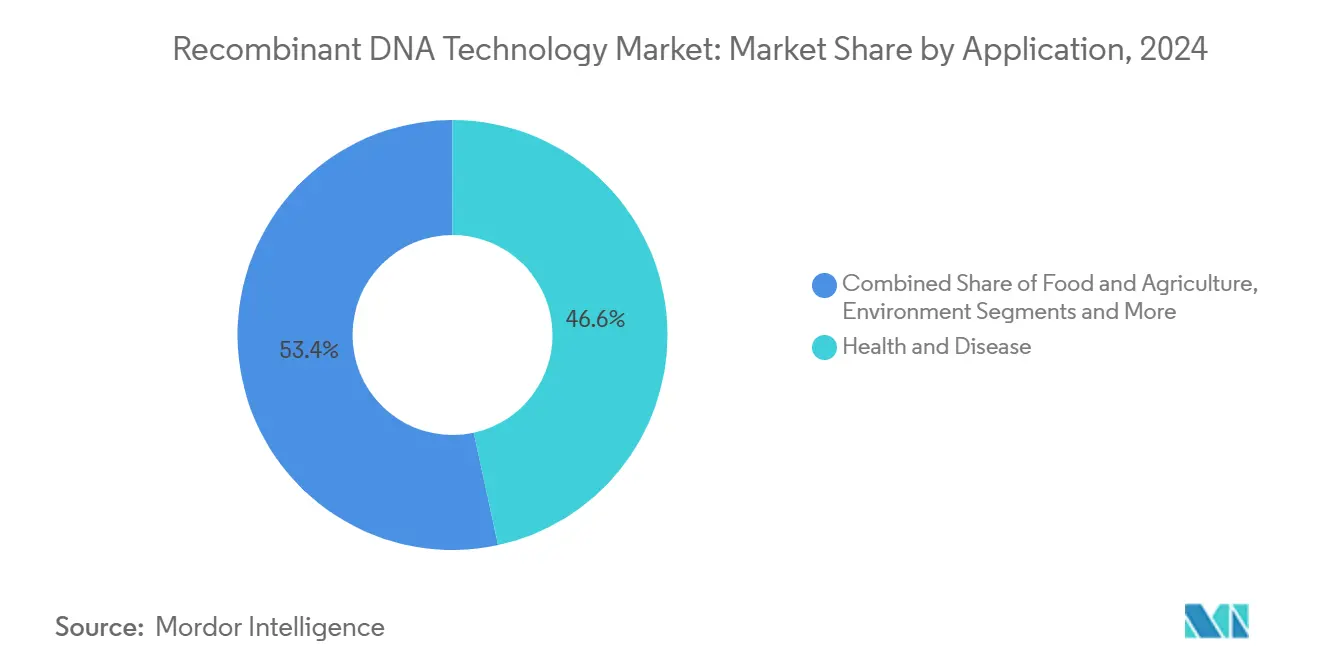
Note: Parts de segment de tous les segments individuels disponibles à l'achat du rapport
Par utilisateur final : la croissance académique défie le leadership industriel
Les entreprises biotech et pharmaceutiques ont contrôlé 53,82 % de part en 2024, exploitant les modèles intégrés découverte-à-commercial pour accélérer les lancements. Leur avance dans la conformité GMP et le marketing mondial leur donne un levier de négociation sur les payeurs et les fournisseurs de matières premières, renforçant les avantages d'incumbance. Les instituts académiques et gouvernementaux, cependant, s'étendent à un TCAC de 9,61 %, soutenus par le financement de l'ère pandémique qui un laissé des améliorations permanentes de laboratoires BSL-3 sur de nombreux campus. L'industrie de la technologie de l'ADN recombinant s'appuie désormais sur les spin-outs universitaires pour les technologies de livraison de niche et les analyses avancées que les entreprises plus grandes licencient sous des structures de jalons.
Les organisations de recherche contractuelle, les fournisseurs d'outillage, et les entreprises d'analyse complètent le paysage utilisateur, formant un écosystème interconnecté où les prestataires de services gagnent des revenus récurrents sans exposition directe au risque d'échec clinique. Cette démocratisation des capacités disperse l'innovation géographiquement et dilue le pouvoir de marché qui résidait autrefois seulement chez les pharmas multinationales, élargissant encore le marché de la technologie de l'ADN recombinant.
Analyse géographique
L'Amérique du Nord un commandé 37,82 % des revenus en 2024, soutenue par un financement de capital-risque robuste, un remboursement favorable, et des cadres FDA qui raccourcissent les cycles de révision pour les thérapies révolutionnaires. Les biofabricants américains bénéficient d'incitations fiscales et de réseaux laboratoire-université qui canalisent les diplômés qualifiés vers l'industrie. Les investissements du Canada dans les incubateurs de thérapie génique ajoutent une diversité régionale, particulièrement dans la R&D de vecteurs viraux. Le marché de la technologie de l'ADN recombinant voit désormais une forte concurrence au niveau des États pour la capacité, avec la Caroline du Nord, le Massachusetts, et la Californie offrant des subventions de contrepartie pour les constructions d'installations.
L'Asie-Pacifique un enregistré le TCAC le plus rapide à 11,81 % jusqu'en 2030, soutenue par le virage stratégique de la Chine vers les partenariats d'Asie du Sud-Est qui sécurisent les marchés en aval et les chaînes d'approvisionnement résilientes. Le gouvernement japonais un relancé les programmes de stimulation biotech, ciblant la biologie synthétique pour les produits chimiques durables, tandis que les groupes Chaebol de Corée du Sud co-investissent dans les CDMO pour capturer les revenus d'exportation de biologiques. La réforme par l'Inde de son Autorité de réglementation biotechnologique promet un dédouanement plus rapide pour les cultures éditées génétiquement, renforçant sa position comme hub de production de semences. Ensemble, ces mouvements réduisent l'écart de production historique avec les marchés occidentaux et renforcent la disponibilité locale des intrants recombinants.
L'Europe équilibre innovation et scepticisme des consommateurs, particulièrement pour les aliments OGM. La stratégie pharmaceutique UE à venir vise à rationaliser les approbations centralisées pour les thérapies avancées, pourtant les approbations de cultures font encore face aux opt-outs des États membres. Les fabricants contractuels en Irlande, Allemagne, et Suisse capitalisent sur cette division en offrant des bioréacteurs d'échelle pour les clients mondiaux, permettant aux sponsors de thérapie de contourner les accrocs réglementaires locaux en faveur de la production d'exportation uniquement. Le Moyen-Orient et l'Afrique sont à un stade naissant mais montrent une dynamique politique : l'Arabie Saoudite un budgété du capital de fonds souverain pour les centres de génomique, et l'autorisation du niébé GM du Ghana signale une position pragmatique sur la sécurité alimentaire. Les ceintures de soja et maïs d'Amérique du Sud fournissent un terrain fertile pour les traits GM, bien que la volatilité macroéconomique puisse tempérer l'investissement direct étranger. Ces trajectoires diverses assurent que le marché de la technologie de l'ADN recombinant reste géographiquement pluriel, réduisant le risque de concentration et permettant la collaboration transfrontalière.
Paysage concurrentiel
La concurrence s'étend sur les couches horizontales-outils de recherche, approvisionnement de vecteurs, capacité GMP-et les tranches verticales à travers les applications thérapeutiques, agricoles, et industrielles. Pfizer, Amgen, et Sanofi déploient la force du bilan pour sécuriser l'accès précoce aux créneaux CDMO à haut volume, évincant les petites entreprises des fenêtres de temps privilégié. L'expansion américaine de 2 milliards USD de Thermo Fisher regroupe les services R&D avec les consommables de purification, un mouvement conçu pour verrouiller les clients dans des chaînes d'approvisionnement de bout en bout. Lonza, Fujifilm Diosynth, et GenScript ont dimensionné les flottes de bioréacteurs au-delà de 500 000 litres, se positionnant comme indispensables aux sponsors de thérapie génique de phase tardive.
Les startups se différencient par le focus plateforme : Aldevron innove dans la fabrication rapide de plasmides ; Touchlight développe des vecteurs ADN doggybone ; Life Edit se spécialise dans l'édition de base. Beaucoup associent innovation et partenariats stratégiques-NEC Bio et AGC Biologics ont contracté pour produire des vaccins anticancéreux personnalisés, combinant la découverte d'antigènes IA avec la fabrication évolutive. Le marché de la technologie de l'ADN recombinant récompense de telles alliances en raccourcissant le temps-à-clinique tout en partageant le fardeau capital.
Les stratégies concurrentielles pivotent de plus en plus sur l'activation numérique. Les entreprises intègrent l'IA pour le criblage in-silico, les jumeaux numériques pour l'optimisation d'installation, et la blockchain pour la traçabilité des vecteurs pour satisfaire les audits de provenance plus stricts. Celles qui maîtrisent la fusion de données atteignent des cycles de libération de lots plus rapides et des variances de rendement plus serrées, se traduisant par un coût-des-marchandises plus bas qui défend les marges alors que l'érosion biosimilaire s'intensifie. Malgré les vagues de consolidation, le marché de la technologie de l'ADN recombinant compte encore des centaines d'entreprises soutenues par le capital-risque s'attaquant aux cibles étroites, soutenant un équilibre dynamique où les incumbents achètent ou s'associent avec les nouveaux venus les plus prometteurs plutôt que de s'appuyer uniquement sur la R&D interne.
Leaders de l'industrie de la technologie de l'ADN recombinant (rDNA)
-
New England Biolabs
-
Sanofi
-
GenScript
-
GSK plc
-
Pfizer Inc.
- *Avis de non-responsabilité : les principaux acteurs sont triés sans ordre particulier
Développements récents de l'industrie
- Avril 2025 : Thermo Fisher Scientific un dévoilé un plan d'investissement américain de 2 milliards USD couvrant les projets d'immobilisations et la R&D en sciences de la vie.
- Mars 2025 : Bayer un introduit le soja Vyconic avec cinq tolérances aux herbicides, ciblant les agriculteurs américains et canadiens d'ici 2027.
Portée du rapport mondial sur le marché de la technologie de l'ADN recombinant (rDNA)
Selon la portée du rapport, la technologie de l'ADN recombinant est un processus dans lequel la création et la manipulation de séquences d'ADN sont effectuées dans un ordre spécifique, résultant en la production d'organismes et de produits génétiquement modifiés. L'ADN recombinant est principalement utilisé dans des applications conventionnelles et non conventionnelles, telles que médicinales, agricoles, et industrielles. En médecine, l'ADN recombinant un été utilisé pour la production de masse d'insuline, Follistim, hormones de croissance humaine, anticorps monoclonaux, albumine humaine, vaccins, et autres médicaments. Le marché de la technologie de l'ADN recombinant (rDNA) est segmenté par produit (médical (agent thérapeutique, protéine humaine, et vaccin), non médical (cultures biotech, produits chimiques spécialisés, et autres produits non médicaux), composant (système d'expression, et vecteur de clonage), application (alimentation et agriculture, santé et maladie, environnement, et autres applications), utilisateur final (entreprises de biotechnologie et pharmaceutiques, instituts de recherche académiques et gouvernementaux, et autres utilisateurs finaux), et géographie (Amérique du Nord, Europe, Asie-Pacifique, Moyen-Orient et Afrique, et Amérique du Sud). Le rapport de marché couvre également les tailles de marché estimées et les tendances pour 17 pays différents à travers les principales régions mondialement. Le rapport offre la valeur (en millions USD) pour les segments susmentionnés.
| Médical | Agents thérapeutiques |
| Protéines humaines | |
| Vaccins | |
| Non médical | Cultures biotech |
| Produits chimiques spécialisés | |
| Autres produits non médicaux |
| Systèmes d'expression |
| Vecteurs de clonage |
| Alimentation et agriculture |
| Santé et maladie |
| Environnement |
| Autres applications |
| Entreprises biotech et pharma |
| Instituts académiques et gouvernementaux |
| Autres utilisateurs finaux |
| Amérique du Nord | États-Unis |
| Canada | |
| Mexique | |
| Europe | Allemagne |
| Royaume-Uni | |
| France | |
| Italie | |
| Espagne | |
| Reste de l'Europe | |
| Asie-Pacifique | Chine |
| Japon | |
| Inde | |
| Corée du Sud | |
| Australie | |
| Reste de l'Asie-Pacifique | |
| Moyen-Orient et Afrique | CCG |
| Afrique du Sud | |
| Reste du Moyen-Orient et de l'Afrique | |
| Amérique du Sud | Brésil |
| Argentine | |
| Reste de l'Amérique du Sud |
| Par produit | Médical | Agents thérapeutiques |
| Protéines humaines | ||
| Vaccins | ||
| Non médical | Cultures biotech | |
| Produits chimiques spécialisés | ||
| Autres produits non médicaux | ||
| Par composant | Systèmes d'expression | |
| Vecteurs de clonage | ||
| Par application | Alimentation et agriculture | |
| Santé et maladie | ||
| Environnement | ||
| Autres applications | ||
| Par utilisateur final | Entreprises biotech et pharma | |
| Instituts académiques et gouvernementaux | ||
| Autres utilisateurs finaux | ||
| Géographie | Amérique du Nord | États-Unis |
| Canada | ||
| Mexique | ||
| Europe | Allemagne | |
| Royaume-Uni | ||
| France | ||
| Italie | ||
| Espagne | ||
| Reste de l'Europe | ||
| Asie-Pacifique | Chine | |
| Japon | ||
| Inde | ||
| Corée du Sud | ||
| Australie | ||
| Reste de l'Asie-Pacifique | ||
| Moyen-Orient et Afrique | CCG | |
| Afrique du Sud | ||
| Reste du Moyen-Orient et de l'Afrique | ||
| Amérique du Sud | Brésil | |
| Argentine | ||
| Reste de l'Amérique du Sud | ||
Questions clés auxquelles répond le rapport
Quelle est la taille actuelle du marché de la technologie de l'ADN recombinant ?
Le marché était évalué à 734,44 milliards USD en 2025 et devrait atteindre 974,07 milliards USD d'ici 2030, affichant un TCAC de 5,81 %.
Quel segment de produit mène la génération de revenus ?
Les applications médicales ont représenté 65,35 % des revenus de 2024, principalement grâce aux protéines thérapeutiques et aux thérapies géniques en croissance rapide.
Quelle région croît le plus rapidement ?
L'Asie-Pacifique est projetée à croître à un TCAC de 11,81 % jusqu'en 2030, stimulée par l'expansion des empreintes de fabrication en Chine et en Asie du Sud-Est.
Quel facteur exerce l'impact positif le plus fort sur la croissance ?
La demande biopharma croissante pour les médicaments protéiques recombinants ajoute environ +1,8 points de pourcentage au TCAC prévisionnel.
Pourquoi les vecteurs de clonage dépassent-ils les systèmes d'expression en croissance ?
Les pipelines de thérapie génique nécessitent des vecteurs viraux et plasmidiques de haute qualité, poussant le segment vers un TCAC de 9,85 % jusqu'en 2030.
Comment les différences réglementaires affectent-elles l'entrée sur le marché ?
Les règles d'édition génique divergentes à travers les États-Unis, l'UE, et la Chine obligent les stratégies de conformité multi-juridictionnelles, ajoutant temps et coût avant le lancement.
Dernière mise à jour de la page le:



