Analyse du marché du traitement de la maladie de surcharge lysosomale
Le marché du traitement de la maladie lysosomale devrait enregistrer un TCAC de 8,2 % au cours de la période de prévision.
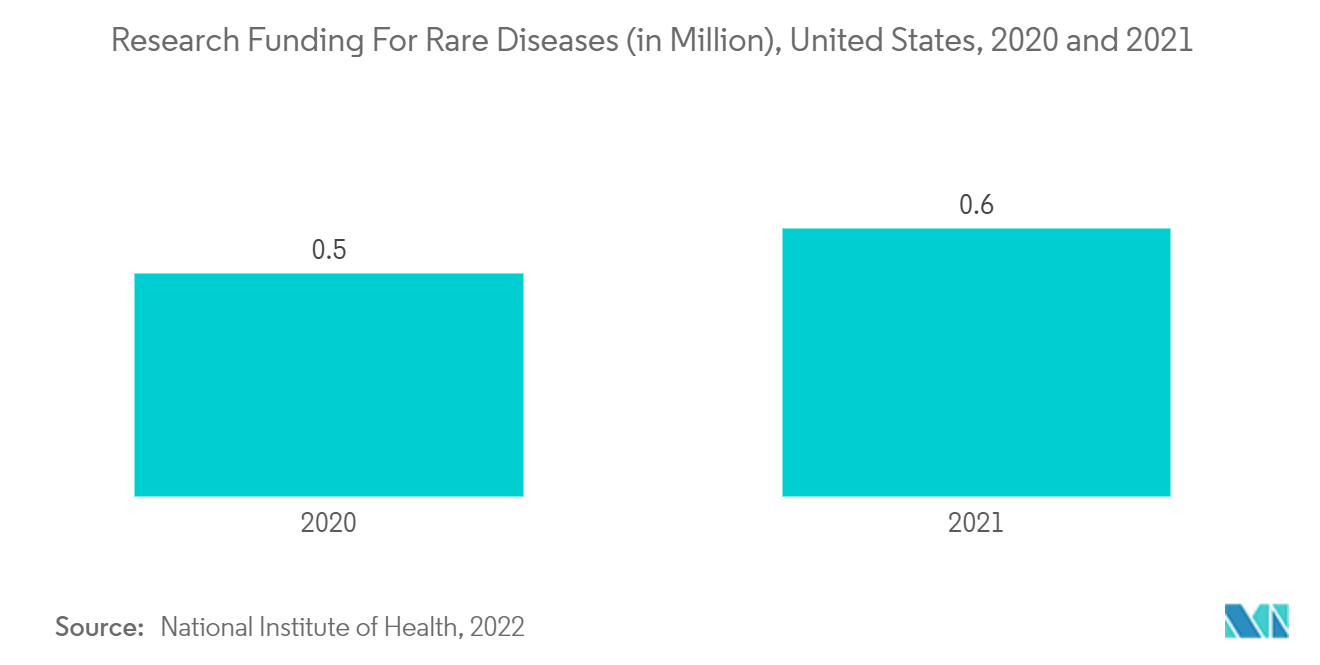
La croissance du traitement de la maladie lysosomale est motivée par l'augmentation de la recherche et du développement et par la sensibilisation de la population à la maladie lysosomale. En outre, les investissements croissants dans la recherche et le développement contribuent également à la croissance du marché. Selon létude publiée par la National Library of Medicine, en juillet 2022, considérés comme un groupe, les LSD sont beaucoup plus courants. L'incidence combinée se situe entre 1 sur 5 000 et 1 sur 8 000. Selon la même source, l'origine ethnique et la géographie jouent un rôle dans l'incidence des DSL. Par exemple, la maladie de Gaucher (MG) touche 1 personne sur 40 000 à 1 personne sur 60 000 dans la population générale. Chez les Juifs dEurope de lEst (Juifs ashkénazes), la maladie de GD atteint 1 sur 800 et la maladie de Tay-Sachs atteint 1 sur 3 900. Niemann-Pick A et la mucolipidose IV surviennent également avec une fréquence accrue dans cette population. Dans la population finlandaise, laspartylglucosaminurie survient à une fréquence de 1 sur 18500. Ainsi, la charge croissante des LSD devrait accroître la croissance du marché du traitement de la maladie lysosomale au cours de la période de prévision.
Le lancement de nouveaux médicaments dans le monde entier stimulera la demande de traitement de cette maladie et stimulera davantage la croissance des revenus du marché. De plus, laugmentation des dépenses de RD à léchelle mondiale favorisera également la recherche de nouveaux traitements et traitements des maladies lysosomales. Par exemple, Généthon a lancé en février 2021 un essai clinique de thérapie génique pour la maladie de Pompe à apparition tardive, mené par la société Spark Therapeutics, utilisant les technologies développées à Généthon.
De plus, la sensibilisation aux maladies lysosomales est cruciale pour les patients et le personnel soignant. Ces dernières années, il y a eu une sensibilisation accrue au traitement de la maladie de Fabry dans différents pays comme les États-Unis, le Royaume-Uni et dautres. Par exemple, selon la National Fabry Disease Foundation (NFDF), chaque année, le mois d'avril est le mois de la sensibilisation à la maladie de Fabry. En outre, d'autres organisations qui célèbrent officiellement le mois d'avril comme Mois de sensibilisation à la maladie de Fabry comprennent Fabry International Network (FIN), Fabry Australia et MPS Society au Royaume-Uni. De plus, courant avril, ces associations sensibilisent à la maladie de Fabry. Cela comprend léducation du public, des patients, des soignants et des professionnels de la santé. En outre, les activités de sensibilisation contribuent à améliorer la perception, le diagnostic et la gestion de ces maladies.
En outre, le développement croissant des thérapies enzymatiques de remplacement et de la thérapie génique créera également une opportunité lucrative pour le marché de la maladie de pompe au cours de la période de prévision, car ce sont les thérapies utilisées pour traiter ce trouble. Cependant, les coûts de traitement élevés associés aux maladies de stockage lysosomal peuvent dans une certaine mesure entraver le marché.
Tendances du marché du traitement de la maladie de surcharge lysosomale
Le segment de la maladie de Pompe devrait détenir une part de marché importante sur le marché du traitement de la maladie lysosomale
La maladie de Pompe est une maladie rare classée comme infantile précoce ou à apparition tardive, affectant principalement les muscles squelettiques, les malformations cardiaques et les problèmes respiratoires.
Selon le National Institute of Health, en avril 2022, la maladie de Pompe touche 1 individu sur 40 000 aux États-Unis. De plus, selon l'étude intitulée Fréquence des porteurs et prévalence génétique prédite de la maladie de Pompe basée sur une base de données de la population générale rapport sur la génétique moléculaire et le métabolisme de juin 2021, des variantes pathogènes ou probablement pathogènes (PLPV) ont été trouvées dans des proportions plus élevées en Asie de l'Est et en Asie de l'Est. Patients africains atteints de la maladie de Pompe classique à début infantile. Dans la population générale, la fréquence totale des porteurs (FC) et la prévalence génétique prévue (pGP) étaient respectivement de 1,3% (1 sur 77) et de 1:23232. Ainsi, la prévalence croissante de la maladie de pompe devrait stimuler la croissance du segment de marché au cours de la période de prévision.
De plus, les approbations et les lancements de produits par les principaux acteurs du marché en ce qui concerne le segment devraient stimuler le marché au cours de la période de prévision. Par exemple, en août 2021, la FDA américaine a approuvé un nouveau traitement enzymatique substitutif, lavalglucosidase alfa, pour les patients âgés dun an et plus atteints de la maladie de Pompe à apparition tardive.
Ainsi, tous les facteurs susmentionnés devraient stimuler la croissance du segment au cours de la période de prévision.
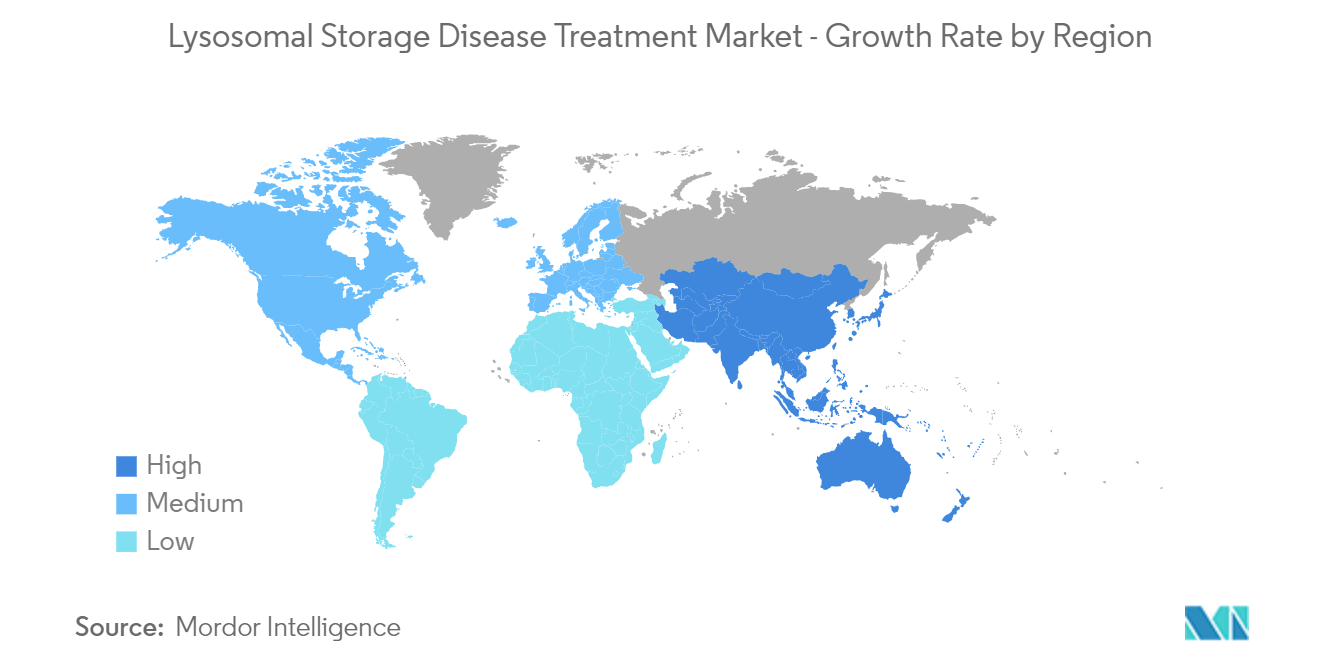
LAmérique du Nord devrait détenir une part importante du marché et devrait faire de même au cours de la période de prévision.
LAmérique du Nord devrait détenir une part de marché importante sur le marché mondial du traitement des maladies lysosomales en raison de lincidence croissante des troubles du stockage lysosomal dans cette région.
Selon NORD, données mises à jour en mars 2021, environ 6 000 personnes sont atteintes de la maladie de Gaucher aux États-Unis. De plus, la maladie de Gaucher de type 1 est la forme la plus courante de la maladie dans les pays occidentaux, représentant environ 95 % des patients. En outre, laugmentation de la recherche et du développement pour le diagnostic et le développement de médicaments pour le traitement des maladies lysosomales et la présence dinfrastructures de santé bien établies alimentent également dans une large mesure la croissance de lensemble du marché régional.
De plus, avec laugmentation des lancements de produits, lapprobation de la FDA américaine et les activités des principaux acteurs, le marché devrait connaître une forte augmentation. Par exemple, en août 2021, la FDA américaine a approuvé Nexviazyme pour la perfusion intraveineuse afin de traiter les patients âgés d'un an et plus atteints de la maladie de Pompe à apparition tardive. De plus, la FDA américaine a accordé la désignation de médicament orphelin (ODD) à l'AL01211 d'AceLink Therapeutics pour traiter la maladie de Fabry. De tels cas devraient stimuler la croissance du marché au cours de la période de prévision.
En outre, la sensibilisation croissante aux maladies rares et le développement des infrastructures de soins de santé devraient également alimenter la croissance du marché dans cette région.
Aperçu du marché du traitement des maladies lysosomales
Le marché du traitement de la maladie lysosomale est consolidé et se compose de quelques acteurs majeurs. En termes de part de marché, quelques-uns des principaux acteurs dominent actuellement le marché. Parmi les principaux acteurs du marché figurent Pfizer Inc, Takeda Pharmaceutical Company Limited (Shire Plc), Sanofi (Genzyme Corporation), BioMarin, Johnson Johnson (Actelion Pharmaceuticals Ltd), Amicus Therapeutics, Inc, Alexion Pharmaceuticals, Inc, Sigilon Therapeutics, Inc. et Orphazyme A/S.
Leaders du marché du traitement de la maladie de surcharge lysosomale
Pfizer Inc
Takeda Pharmaceutical Company Limited (Shire Plc)
Sanofi (Genzyme Corporation)
BioMarin
Johnson & Johnson (Actelion Pharmaceuticals Ltd)
- *Avis de non-responsabilité : les principaux acteurs sont triés sans ordre particulier
Actualités du marché du traitement de la maladie de surcharge lysosomale
- En août 2022, la Commission européenne a approuvé Galafold commercialisé par Amicus Therapeutics pour le traitement à long terme des patients atteints de la maladie de Fabry âgés de 12 ans et plus présentant une mutation sensible.
- En février 2022, Maze Therapeutics, une société qui transforme les connaissances génétiques en nouveaux médicaments de précision, a rapporté de nouvelles données précliniques soutenant l'avancement du MZE001, qui vise à lutter contre la maladie de Pompe en réduisant l'accumulation pathologique de glycogène grâce à l'inhibition de la glycogène synthase musculaire (GYS1).
Segmentation de lindustrie du traitement des maladies lysosomales
Selon la portée du rapport, les maladies de stockage lysosomal (LSD) sont des erreurs innées du métabolisme caractérisées par l'accumulation de substrats en excès dans les cellules de divers organes en raison du fonctionnement défectueux des lysosomes. Ils provoquent un dysfonctionnement des organes où ils saccumulent et contribuent à une grande morbidité et mortalité. Le marché du traitement de la maladie de surcharge lysosomale est segmenté par type de thérapie (thérapie de remplacement enzymatique, thérapie par réduction de substrat), par application (maladie de Gaucher, cystinose, maladie de Pompe, maladie de Fabry et autres applications) et par géographie (Amérique du Nord, Europe, Asie- Pacifique et Reste du monde). Le rapport propose la valeur (en millions de dollars) pour les segments ci-dessus.
| Thérapie de remplacement enzymatique | Vélaglucérase Alfa |
| Taliglucérase Alfa | |
| Agalsidase bêta | |
| Laronidase | |
| Imiglucérase | |
| Autres thérapies de remplacement enzymatique | |
| Thérapie de réduction de substrat | Éliglustat |
| Miglustat | |
| Autres thérapies de réduction de substrat |
| Maladie de Gaucher |
| Cystinose |
| Pompe Disease |
| Maladie de Fabry |
| Autres applications |
| Amérique du Nord | États-Unis |
| Canada | |
| Mexique | |
| L'Europe | Allemagne |
| Royaume-Uni | |
| France | |
| Italie | |
| Espagne | |
| Le reste de l'Europe | |
| Asie-Pacifique | Chine |
| Japon | |
| Inde | |
| Australie | |
| Corée du Sud | |
| Reste de l'Asie-Pacifique | |
| Reste du monde |
| Par type de thérapie | Thérapie de remplacement enzymatique | Vélaglucérase Alfa |
| Taliglucérase Alfa | ||
| Agalsidase bêta | ||
| Laronidase | ||
| Imiglucérase | ||
| Autres thérapies de remplacement enzymatique | ||
| Thérapie de réduction de substrat | Éliglustat | |
| Miglustat | ||
| Autres thérapies de réduction de substrat | ||
| Par candidature | Maladie de Gaucher | |
| Cystinose | ||
| Pompe Disease | ||
| Maladie de Fabry | ||
| Autres applications | ||
| Géographie | Amérique du Nord | États-Unis |
| Canada | ||
| Mexique | ||
| L'Europe | Allemagne | |
| Royaume-Uni | ||
| France | ||
| Italie | ||
| Espagne | ||
| Le reste de l'Europe | ||
| Asie-Pacifique | Chine | |
| Japon | ||
| Inde | ||
| Australie | ||
| Corée du Sud | ||
| Reste de l'Asie-Pacifique | ||
| Reste du monde | ||
FAQ sur les études de marché sur le traitement de la maladie de surcharge lysosomale
Quelle est la taille actuelle du marché du traitement de la maladie de surcharge lysosomale ?
Le marché du traitement de la maladie lysosomale devrait enregistrer un TCAC de 8,20 % au cours de la période de prévision (2024-2029)
Qui sont les principaux acteurs du marché Traitement de la maladie de surcharge lysosomale ?
Pfizer Inc, Takeda Pharmaceutical Company Limited (Shire Plc), Sanofi (Genzyme Corporation), BioMarin, Johnson & Johnson (Actelion Pharmaceuticals Ltd) sont les principales sociétés opérant sur le marché du traitement de la maladie de surcharge lysosomale.
Quelle est la région qui connaît la croissance la plus rapide sur le marché du traitement de la maladie de surcharge lysosomale ?
On estime que lAsie-Pacifique connaîtra la croissance du TCAC le plus élevé au cours de la période de prévision (2024-2029).
Quelle région détient la plus grande part du marché Traitement de la maladie de surcharge lysosomale ?
En 2024, lAmérique du Nord représente la plus grande part de marché sur le marché du traitement de la maladie lysosomale.
Quelles années couvre ce marché du traitement de la maladie de surcharge lysosomale ?
Le rapport couvre la taille historique du marché du traitement de la maladie de stockage lysosomal pour les années 2021, 2022 et 2023. Le rapport prévoit également la taille du marché du traitement de la maladie de stockage lysosomal pour les années 2024, 2025, 2026, 2027, 2028 et 2029.
Dernière mise à jour de la page le:
Rapport sur lindustrie du traitement des maladies lysosomales
Statistiques sur la part de marché, la taille et le taux de croissance des revenus du traitement de la maladie lysosomale de stockage 2024, créées par Mordor Intelligence™ Industry Reports. Lanalyse du traitement de la maladie lysosomale comprend des perspectives de marché pour 2024 à 2029 et un aperçu historique. Obtenez un échantillon de cette analyse de lindustrie sous forme de rapport PDF gratuit à télécharger.



