Taille et part du marché de l'expression protéique acellulaire
Analyse du marché de l'expression protéique acellulaire par Mordor Intelligence
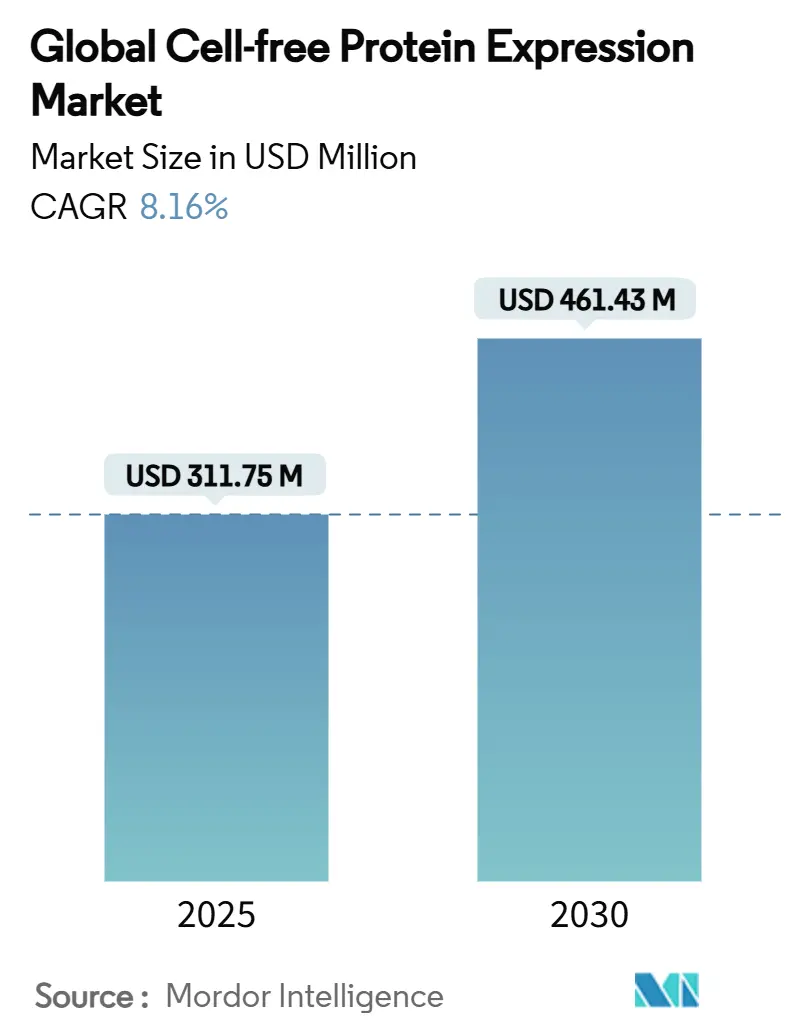
La taille du marché de l'expression protéique acellulaire s'élève à 311,75 millions USD en 2025 et devrait atteindre 461,43 millions USD d'ici 2030, reflétant un TCAC de 8,16 %. Le passage de la technologie des paillasses académiques aux suites cGMP redéfinit les flux de travail de biofabrication, particulièrement là où les délais rapides de conception-construction-test et les profils de protéines toxiques défient les systèmes basés sur les cellules. Le soutien réglementaire s'élargit, car les orientations de fabrication avancée de la FDA américaine décrivent des voies de validation claires pour les installations d'expression protéique acellulaire à échelle commerciale. Les flux de capitaux stratégiques vers la biologie synthétique, l'amélioration des rendements de lysat et une plus grande standardisation des réactifs élargissent le marché adressable bien au-delà de la recherche exploratoire. Entre-temps, la région Asie-Pacifique émerge comme la géographie à la croissance la plus rapide grâce aux programmes nationaux orientés vaccins, tandis que l'Amérique du Nord conserve la plus grande base de revenus en raison de la demande pharmaceutique établie. L'intensité concurrentielle reste modérée, avec des fournisseurs de plateformes intégrées se différenciant sur la qualité du lysat, l'automatisation et le support de flux de travail de bout en bout.
Points clés du rapport
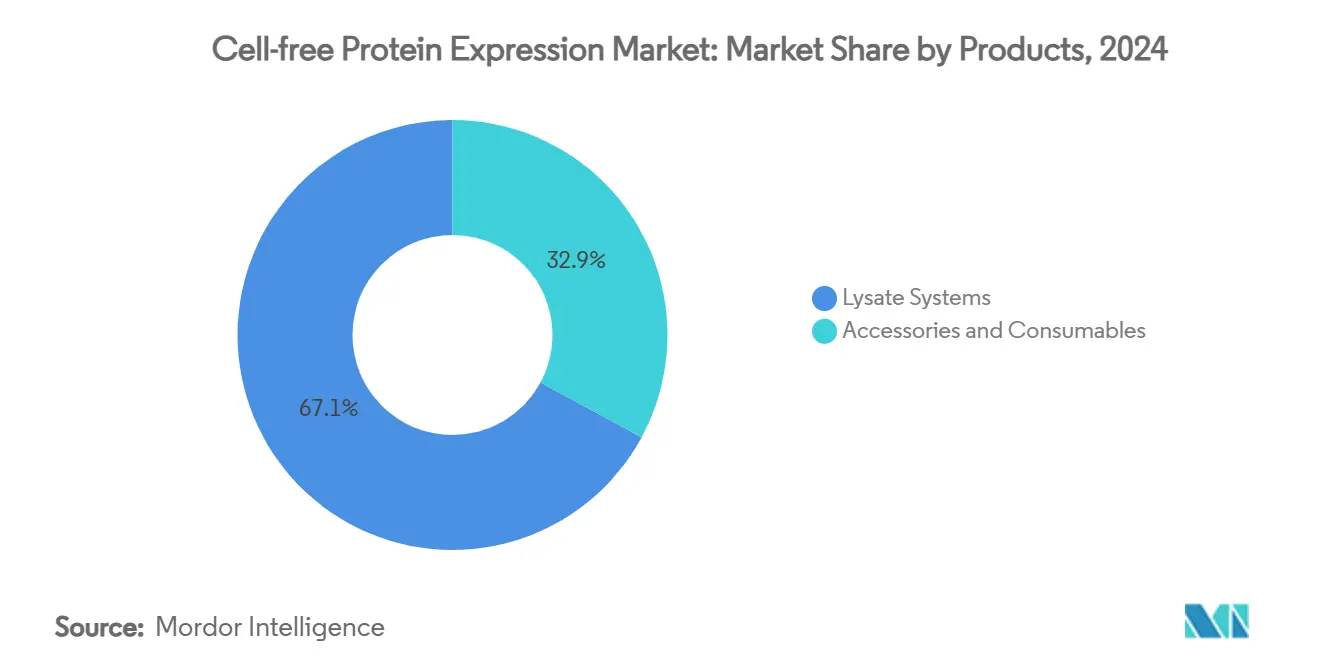
- Par type de produit, les systèmes de lysat détenaient 67,12 % de part de revenus du marché de l'expression protéique acellulaire en 2024, tandis que les accessoires et consommables devraient croître à un TCAC de 8,56 % jusqu'en 2030.
- Par méthode d'expression, les systèmes de traduction commandaient 56,65 % de la part du marché de l'expression protéique acellulaire en 2024 ; les plateformes de transcription-traduction couplées devraient enregistrer un TCAC de 9,71 % entre 2025-2030.
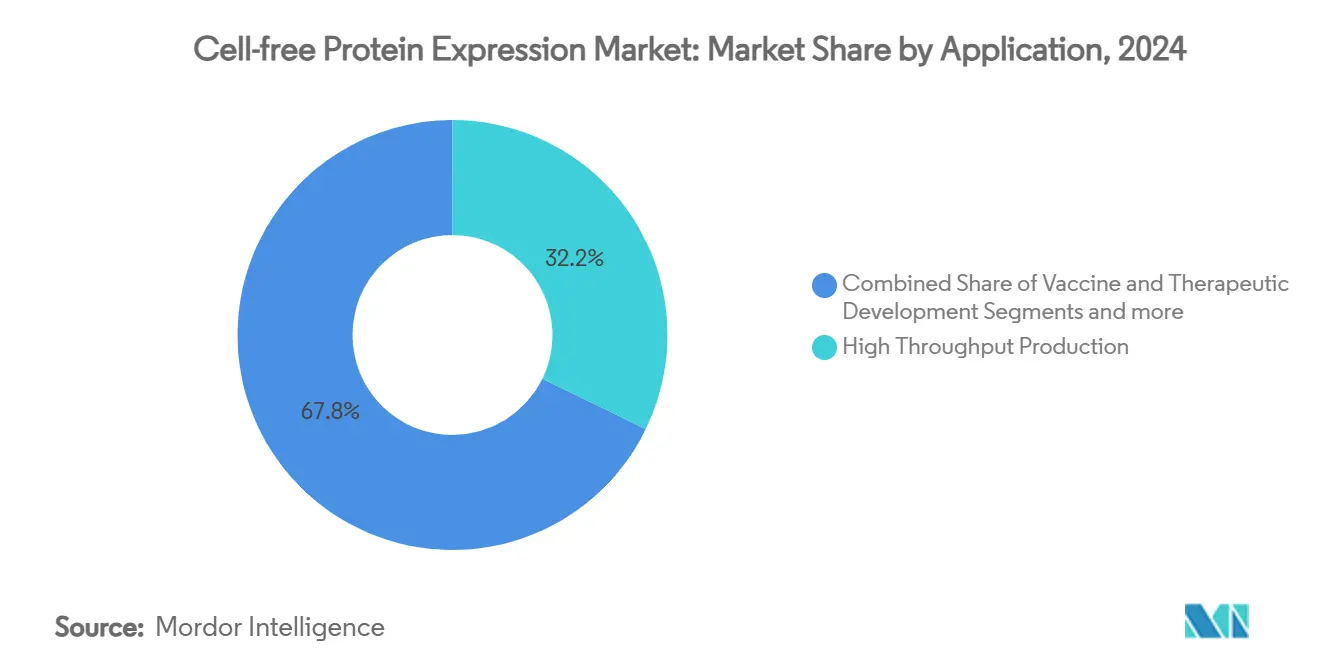
- Par application, le développement de vaccins et thérapeutiques a capturé 32,21 % de la taille du marché de l'expression protéique acellulaire en 2024 et progresse à un TCAC de 9,86 % jusqu'en 2030.
- Par utilisateur final, les entreprises pharmaceutiques et biotechnologiques représentaient 55,15 % de part de revenus en 2024, tandis que les CRO et CDMO sont positionnées pour la croissance la plus rapide à 9,55 % TCAC jusqu'en 2030.
- L'Amérique du Nord menait avec 41,44 % des revenus 2024 ; l'Asie-Pacifique devrait croître à un TCAC de 9,21 %, l'expansion régionale la plus rapide sur la période de prévision.
Tendances et perspectives du marché mondial de l'expression protéique acellulaire
Analyse d'impact des moteurs
| Moteur | (~) % Impact sur prévision TCAC | Pertinence géographique | Chronologie d'impact |
|---|---|---|---|
| Croissance du prototypage de vaccins personnalisés et rapides | +1.8% | Mondial ; gains précoces en Amérique du Nord et Europe | Moyen terme (2-4 ans) |
| Essor des plateformes d'expression protéique acellulaire pour la fabrication de produits biologiques à la demande | +1.5% | Amérique du Nord et UE ; extension vers APAC | Long terme (≥ 4 ans) |
| Recherche et développement croissants en protéomique et génomique | +1.2% | Mondial | Long terme (≥ 4 ans) |
| Investissements croissants dans les start-ups de biologie synthétique | +1.4% | Cœur Amérique du Nord ; expansion vers APAC | Court terme (≤ 2 ans) |
| Fardeau croissant du cancer et des maladies infectieuses | +0.9% | Mondial | Moyen terme (2-4 ans) |
| Avantages croissants des systèmes d'expression protéique acellulaire | +1.0% | Mondial | Moyen terme (2-4 ans) |
| Source: Mordor Intelligence | |||
Croissance du prototypage de vaccins personnalisés et rapides
Les stratégies vaccinales décentralisées mettent désormais l'accent sur la production sur site de conjugués spécifiques aux patients, et les systèmes d'expression protéique acellulaire livrent des coûts de dose aussi bas que 0,50 USD tout en éliminant les dépendances de chaîne du froid. La plateforme iVAX de l'Université Northwestern a augmenté les rendements de 91 % grâce à l'enrichissement vésiculaire, poussant les coûts par dose près de 1 USD. Cette économie, couplée à la stabilité de lysat lyophilisé, renforce les mesures de préparation pandémique de manières inaccessibles aux grands fermenteurs en acier inoxydable. Les régulateurs mondiaux répondent ; le cadre de fabrication avancée de la FDA cite explicitement les systèmes d'expression protéique acellulaire comme voie éligible pour les vaccins de réponse rapide, accélérant leur traduction clinique.
Essor des plateformes d'expression protéique acellulaire pour la fabrication de produits biologiques à la demande
Les fabricants contractuels mettent à l'échelle des installations flexibles alors que le pipeline thérapeutique se déplace vers des produits biologiques à faible volume et à mélange élevé. Samsung Biologics a engagé 6 milliards USD et Fujifilm Diosynth 3,2 milliards USD dans des usines multiproduits favorisant les technologies agiles. Les flux de travail d'expression protéique acellulaire s'alignent avec cette stratégie en découplant la synthèse protéique de la croissance cellulaire, permettant des changements de campagne quasi instantanés. Le jalon commercial est arrivé en 2025 quand Boehringer Ingelheim a exécuté le processus d'expression protéique acellulaire de Sutro Biopharma à pleine échelle BPF pour produire le luveltamab tazevibulin [1]Sutro Biopharma, "Fabrication commerciale Luveltamab Tazevibulin," sutrobio.com. Le succès a validé des rendements cohérents, confirmant que les lignes d'expression protéique acellulaire peuvent respecter les spécifications de qualité strictes requises pour les conjugués anticorps-médicament.
Recherche et développement croissants en protéomique et génomique
Les plateformes de conception protéique assistées par IA comme AlphaProteo de DeepMind produisent régulièrement des milliers de séquences hypothétiques, dont 84 % s'expriment avec succès dans les pipelines de laboratoire contre la norme historique de 20-30 %. Les systèmes d'expression protéique acellulaire accélèrent le criblage en exprimant des variants toxiques ou riches en membrane qui compromettent les hôtes vivants. Le monde académique exploite cette capacité pour la génomique fonctionnelle, où les systèmes d'expression protéique acellulaire automatisés en plaques caractérisent des bibliothèques entières de gènes en jours plutôt qu'en mois. La boucle de rétroaction entre la conception computationnelle et l'expression à la demande continue d'accélérer le débit de découverte et consolide les protocoles d'expression protéique acellulaire comme outil standard pour la protéomique de nouvelle génération.
Investissements croissants dans les start-ups de biologie synthétique
Le capital-risque alimente l'innovation d'expression protéique acellulaire dédiée. Exsilio Therapeutics a sécurisé 82 millions USD pour développer des éléments génétiques programmables optimisés via un prototypage de lysat rapide. Ces fonds stimulent l'automatisation, avec des start-ups intégrant des manipulateurs de liquides robotiques et des outils de conception basés sur le cloud pour raccourcir les cycles de développement. Les entreprises pharmaceutiques établies interviennent aussi ; l'alliance de GSK avec Elegen importe une plateforme avancée de production d'ADN d'expression protéique acellulaire directement dans ses centres R&D, soulignant un changement plus large vers des chaînes d'approvisionnement distribuées et centrées sur les réactifs. Les flux d'investissement se traduisent par une demande constante de réactifs et des mises à niveau de systèmes à travers le marché de l'expression protéique acellulaire [2]Wu, M, Un laboratoire expérimental natif IA pour l'ingénierie biomoléculaire autonome,
Université Cornell, arxiv.org.
Analyse d'impact des contraintes
| Contrainte | (~) % Impact sur prévision TCAC | Pertinence géographique | Chronologie d'impact |
|---|---|---|---|
| Écart persistant dans l'approvisionnement de lysat à gros volume | -1.1% | Mondial ; mise à l'échelle APAC contrainte | Moyen terme (2-4 ans) |
| Faible sensibilisation parmi les CRO des marchés émergents | -0.8% | Cœur APAC ; MEA émergent | Court terme (≤ 2 ans) |
| Capital initial élevé pour les postes de travail d'automatisation d'expression protéique acellulaire | -0.9% | Mondial ; marchés sensibles aux coûts | Long terme (≥ 4 ans) |
| Flux de travail de développement strict | -0.7% | Régions à réglementation intensive | Moyen terme (2-4 ans) |
| Source: Mordor Intelligence | |||
Écart persistant dans l'approvisionnement de lysat à gros volume
Alors que la demande migre des réactions de paillasse de 50 mL aux réacteurs cGMP de 1 000 L, la variabilité lot à lot dans l'activité de lysat reste le talon d'Achille. L'alliance de NIZO avec Enzymit se concentre sur les récoltes de fermentation continue pour stabiliser la composition enzymatique, mais les retards d'approvisionnement se répercutent encore dans les campagnes contractuelles Asie-Pacifique. Les systèmes de niche comme le germe de blé ou l'extrait de cellules humaines font face à des pénuries plus sévères en raison de flux de travail amont plus complexes, limitant leur disponibilité pour les cycles de production. Les avancées dans les modèles de réduction d'échelle de bioréacteur et les protocoles standardisés de lyophilisation atténuent la variabilité, mais la cohérence industrielle n'est pas encore pleinement réalisée.
Capital initial élevé pour les postes de travail d'automatisation d'expression protéique acellulaire
Les paillasses d'expression protéique acellulaire complètes et autonomes peuvent coûter plus de 500 000 USD, un chiffre hors de portée pour de nombreuses CRO des marchés émergents. Bien que les groupes de recherche aient démontré des réductions de coût de réactifs de 400 fois en utilisant le séchage par billes de silice et les stabilisateurs de lactose, les prix du matériel restent rigides. Les fournisseurs de plateformes lancent des modules skids modulaires qui intègrent manipulation de liquides, cyclage thermique et analytique en ligne dans un format de paiement à l'usage, mais l'adoption dépendra des modèles de financement et de cas ROI plus clairs dans les environnements à ressources contraintes.
Analyse par segment
Par produits : Les systèmes de lysat pilotent les fondements du marché
Les systèmes de lysat détenaient 67,12 % des revenus 2024, ancrant la taille du marché de l'expression protéique acellulaire au cœur du processus. Les lysats d'Escherichia coli dominent car ils exploitent le savoir-faire de fermentation mature et la scalabilité linéaire, tandis que les extraits de germe de blé offrent un repliement supérieur pour les protéines eucaryotes, un paramètre essentiel pour les études structurales. Les lysats de réticulocyte de lapin et de cellules d'insectes occupent des niches spécialisées où la machinerie de traduction mammalienne ou baculovirale offre une authenticité ajoutée. Le lysat de cellules humaines reste limité en capacité mais commande un prix premium pour les modifications post-traductionnelles qui reflètent la biologie native.
La standardisation autour des mélanges d'énergie pré-mélangés et des cocktails de chaperones améliorés déplace la capture de valeur vers les accessoires et consommables, le sous-segment à croissance la plus rapide à 8,56 % TCAC. Les réactifs représentent maintenant près de 40 % des coûts d'exploitation à vie, créant des flux de revenus annualisés pour les fournisseurs. Les cartouches de réaction à usage unique et les pastilles d'améliorateurs lyophilisées simplifient la reproductibilité du flux de travail, une caractéristique attrayante pour les lignes d'automatisation haut débit et les sites de fabrication distribués qui sous-tendent le marché de l'expression protéique acellulaire.
Par méthode d'expression : La dominance de la traduction fait face au défi du système couplé
Les kits de traduction uniquement représentaient 56,65 % des ventes 2024, favorisés pour leur simplicité et alignement avec les bibliothèques de modèles d'ARNm. Ils permettent un contrôle précis de l'optimisation des codons, des facteurs d'initiation et de la pause ribosomale, ce qui est précieux pour étudier les variants protéiques à l'échelle analytique. Cependant, les systèmes de transcription-traduction couplés s'étendent à un TCAC de 9,71 %, poussés par les avantages de coût des entrées ADN-directes et la réduction des étapes de flux de travail. Les protocoles d'ADN linéaire qui sautent le clonage plasmidique réduisent encore les délais d'exécution, tandis que les balayages de paramètres guidés par IA optimisent simultanément les concentrations de magnésium, NTP et acides aminés.
Cette convergence augmente les rendements plus près des titres cellulaires sans le fardeau métabolique ou les pénalités de temps des standards cellulaires. Alors que les installations haut débit poursuivent les métriques de coût par microgramme et de vitesse, les systèmes couplés sont positionnés pour absorber la part de volume, intensifiant la concurrence au niveau produit au sein du marché plus large de l'expression protéique acellulaire [3]Jacob T. Rapp, Laboratoires auto-pilotés pour naviguer de manière autonome dans le paysage de fitness protéique,
Nature Chemical Engineering, nature.com.
Par application : La production haut débit mène tandis que le développement de vaccins accélère
La production haut débit a conservé 32,21 % des revenus 2024 pour le marché de l'expression protéique acellulaire, surfant sur la demande des criblages de bibliothèques et programmes d'ingénierie enzymatique qui nécessitent des centaines d'expressions de variants en parallèle. La nature ouverte des réactions de lysat permet l'ajout direct de cofacteurs synthétiques, d'étiquettes isotopiques et d'acides aminés non canoniques, ouvrant des fenêtres d'investigation fermées aux cellules vivantes.
Le développement de vaccins et thérapeutiques est l'application à croissance la plus rapide à 9,86 % TCAC. Le segment exploite les capacités d'expression protéique acellulaire pour fabriquer des toxines oncolytiques et conjugués protéiques inadaptés aux cellules hôtes, effondrant ainsi les délais de développement à des semaines. Les jalons réglementaires, comme les cycles de production de conjugués anticorps-médicament qualifiés BPF, soulignent la préparation de production conforme cliniquement. Alors que les stratégies de personnalisation immunitaire progressent, les systèmes d'expression protéique acellulaire devraient sous-tendre les lots à délai d'exécution rapide, renforçant leur centralité pour le marché de l'expression protéique acellulaire.
Note: Parts de segment de tous les segments individuels disponibles à l'achat du rapport
Par utilisateur final : La dominance pharmaceutique défiée par la croissance CRO
Les entreprises pharmaceutiques et biotechnologiques ont contribué 55,15 % des dépenses 2024, intégrant des suites d'expression protéique acellulaire internes pour éliminer la dépendance au développement externe de lignées cellulaires et accélérer les molécules candidates. Les institutions académiques maintiennent une base constante de demande de réactifs pour le développement de méthodes et la formation d'étudiants.
Les organisations de recherche et fabrication contractuelles, cependant, exhibent un TCAC de 9,55 % alors que l'externalisation biopharma accélère. Les CRO exploitent les temps de configuration courts et les attributs plug-and-play des modules d'expression protéique acellulaire pour offrir des services d'expression avec des délais de deux semaines, un avantage concurrentiel sur les processus de culture cellulaire de plusieurs mois. Les procédures opérationnelles standard et les essais QC validés accompagnent maintenant de nombreux kits commerciaux, abaissant les barrières techniques pour l'entrée CRO et élargissant l'empreinte mondiale du marché de l'expression protéique acellulaire.
Analyse géographique
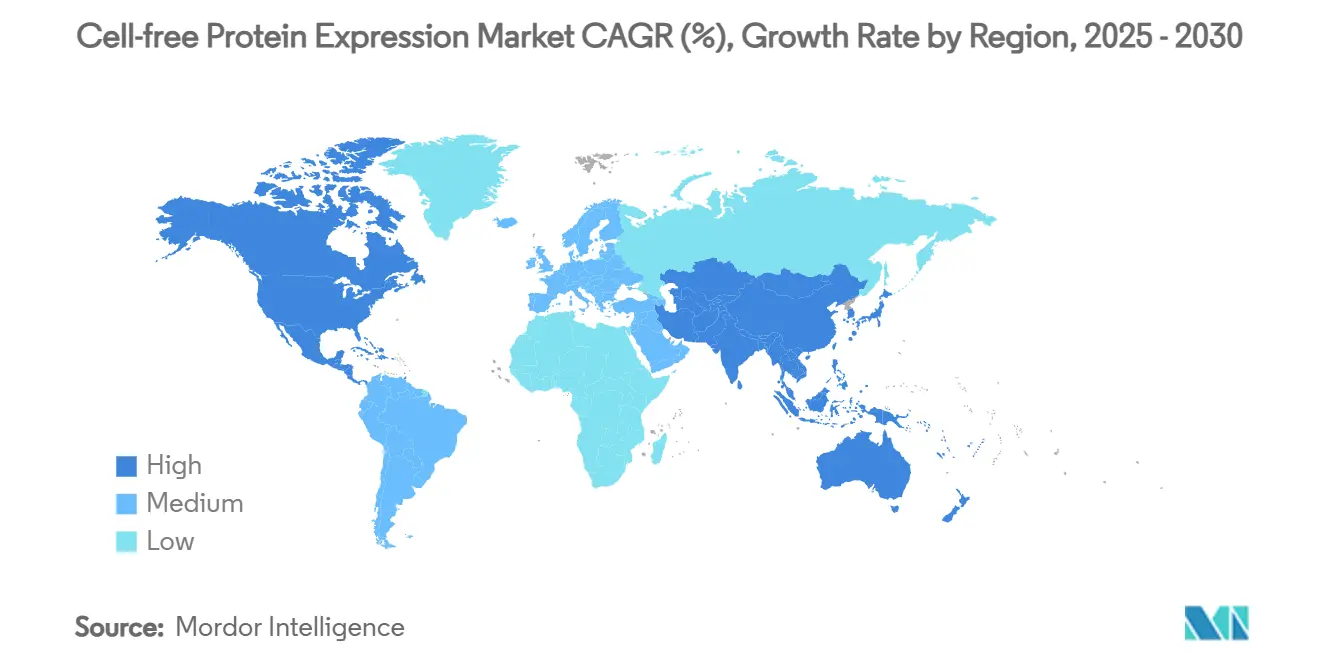
L'Amérique du Nord a maintenu 41,44 % des revenus 2024 pour le marché de l'expression protéique acellulaire, soutenue par les mécanismes de financement fédéral, les pools de capital-risque de biologie synthétique profonds et un climat réglementaire approuvant les technologies de fabrication nouvelles. La clarté de la FDA sur les voies de fabrication avancée a mécanisé la confiance de l'industrie et déclenché des partenariats de mise à l'échelle comme la production commerciale d'ADC de Boehringer Ingelheim et Sutro Biopharma.
L'Asie-Pacifique est la géographie en expansion la plus rapide à 9,21 % TCAC jusqu'en 2030. L'investissement de Singapour dans les usines pilotes de vaccins contre le cancer à ARNm et l'objectif politique explicite de la Corée du Sud d'un hub vaccinal mondial stimulent la demande localisée pour une production rapide et modulaire. Les cadres chinois émergents pour la thérapie cellulaire et génique, couplés à l'accent du Japon sur la transparence BPF, stimulent encore l'adoption. L'hétérogénéité génétique au sein des populations asiatiques encourage aussi les campagnes vaccinales personnalisées qui s'appuient fortement sur l'agilité de l'expression protéique acellulaire.
L'Europe avance régulièrement soutenue par les réglementations de fabrication modulaire de la MHRA qui encouragent la production ATMP au point de soins, un ajustement naturel pour les unités d'expression protéique acellulaire décentralisées. Les impératifs de durabilité et la préférence pour les entrées sans composants animaux résonnent avec le profil de réactifs de la plateforme, améliorant sa réception régionale. Les collaborations transfrontalières, comme les programmes de transfert de technologie de thérapie basée sur l'ARN, prolifèrent et renforcent le rôle de la région dans le marché de l'expression protéique acellulaire.
Paysage concurrentiel
Le champ concurrentiel est modérément fragmenté. Les fournisseurs de systèmes intégrés se différencient par la préparation de lysat propriétaire, les mélanges d'énergie haute densité et les paillasses robotiques entièrement fermées. Les acteurs leaders regroupent consommables, modules d'analytique de données et documentation réglementaire pour verrouiller les ventes de réactifs récurrentes. Les dépôts de brevets récents se concentrent sur la production continue de lysat, l'ingénierie de chaperones et le contrôle de réaction en temps réel basé sur capteurs.
Les alliances stratégiques deviennent le vecteur d'échelle principal. Le transfert de technologie de Sutro Biopharma vers Boehringer Ingelheim a fourni une preuve de concept pour la production d'expression protéique acellulaire BPF à volumes de lots commerciaux, perturbant les marchés traditionnels d'acier inoxydable. L'accord de GSK avec Elegen signale l'appétit des grandes pharmas pour l'approvisionnement externalisé d'ADN et ARNm d'expression protéique acellulaire, tandis que le réseau de distribution APAC de Nuclera élargit la portée géographique pour les systèmes d'automatisation de paillasse. Les opportunités d'espaces blancs persistent dans les diagnostics déployables sur le terrain et la surveillance environnementale, où les cartouches lyophilisées pourraient livrer des lectures protéiques à faible infrastructure, offrant de nouveaux pools de profit au sein du marché de l'expression protéique acellulaire.
Leaders de l'industrie de l'expression protéique acellulaire
-
Thermo Fisher Scientific Inc.
-
Promega Corporation
-
Merck KGaA (Sigma-Aldrich)
-
Takara Bio Inc.
-
New England Biolabs
- *Avis de non-responsabilité : les principaux acteurs sont triés sans ordre particulier
Développements récents de l'industrie
- Mai 2025 : Nuclera a établi un réseau de distribution à travers l'APAC et le Moyen-Orient, fournissant un support technique localisé pour sa gamme de produits d'expression protéique acellulaire.
- Avril 2025 : Nuclera a étendu son système eProtein Discovery avec un flux de travail de protéines membranaires permettant l'expression et la purification en 48 heures via la microfluidique numérique.
- Janvier 2025 : Sutro Biopharma et Boehringer Ingelheim BioXcellence ont annoncé la production commerciale réussie de luveltamab tazevibulin utilisant la plateforme d'expression protéique acellulaire de Sutro.
- Octobre 2024 : Nuclera a clôturé un tour de financement de 75 millions USD mené par Elevage Medical Technologies pour accélérer la commercialisation de son système d'expression d'expression protéique acellulaire de paillasse aux États-Unis et en Europe.
Portée du rapport mondial sur le marché de l'expression protéique acellulaire
Selon la portée de ce rapport, l'expression protéique acellulaire ou synthèse protéique in vitro est un processus qui implique la production de protéines recombinantes dans une solution de lysat cellulaire, sans utiliser de culture cellulaire ou de cellules vivantes. L'expression protéique acellulaire peut être réalisée en utilisant différents lysats cellulaires, comme ceux d'E. coli, de réticulocytes de lapin, de germes de blé, de cellules humaines et de cellules d'insectes.
Le marché de l'expression protéique acellulaire est segmenté par produits, méthode d'expression, application, utilisateur final et géographie. Par produits, le marché est segmenté en accessoires et consommables et systèmes de lysat. Les systèmes de lysat sont encore bifurqués en lysat E. Coli, lysat d'extrait de germe de blé, lysat de réticulocyte de lapin, lysat de cellules d'insectes, lysat de cellules humaines et autres systèmes de lysat. Par méthode d'expression, le marché est segmenté en transcription et traduction couplées et traduction. Par application, le marché est segmenté en ingénierie enzymatique, production haut débit, étiquetage protéique, études d'interaction protéine-protéine, développement de vaccins et thérapeutiques, et autres applications. Par utilisateur final, le marché est segmenté en entreprises pharmaceutiques et biotechnologiques, instituts académiques et de recherche, CRO et CDMO, et autres utilisateurs finaux. Par géographie, le marché est segmenté en Amérique du Nord, Europe, Asie-Pacifique, Moyen-Orient et Afrique, et Amérique du Sud. Le rapport offre la valeur (en millions USD) pour les segments ci-dessus.
| Accessoires et consommables | |
| Systèmes de lysat | Lysat E. coli |
| Lysat d'extrait de germe de blé | |
| Lysat de réticulocyte de lapin | |
| Lysat de cellules d'insectes | |
| Lysat de cellules humaines | |
| Autres systèmes de lysat |
| Transcription et traduction couplées |
| Traduction |
| Ingénierie enzymatique |
| Production haut débit |
| Étiquetage protéique |
| Études d'interaction protéine-protéine |
| Développement de vaccins et thérapeutiques |
| Autres applications |
| Entreprises pharmaceutiques et biotechnologiques |
| Instituts académiques et de recherche |
| CRO et CDMO |
| Autres utilisateurs finaux |
| Amérique du Nord | États-Unis |
| Canada | |
| Mexique | |
| Europe | Allemagne |
| Royaume-Uni | |
| France | |
| Italie | |
| Espagne | |
| Reste de l'Europe | |
| Asie-Pacifique | Chine |
| Japon | |
| Inde | |
| Australie | |
| Corée du Sud | |
| Reste de l'Asie-Pacifique | |
| Moyen-Orient et Afrique | CCG |
| Afrique du Sud | |
| Reste du Moyen-Orient et Afrique | |
| Amérique du Sud | Brésil |
| Argentine | |
| Reste de l'Amérique du Sud |
| Par produits | Accessoires et consommables | |
| Systèmes de lysat | Lysat E. coli | |
| Lysat d'extrait de germe de blé | ||
| Lysat de réticulocyte de lapin | ||
| Lysat de cellules d'insectes | ||
| Lysat de cellules humaines | ||
| Autres systèmes de lysat | ||
| Par méthode d'expression | Transcription et traduction couplées | |
| Traduction | ||
| Par application | Ingénierie enzymatique | |
| Production haut débit | ||
| Étiquetage protéique | ||
| Études d'interaction protéine-protéine | ||
| Développement de vaccins et thérapeutiques | ||
| Autres applications | ||
| Par utilisateur final | Entreprises pharmaceutiques et biotechnologiques | |
| Instituts académiques et de recherche | ||
| CRO et CDMO | ||
| Autres utilisateurs finaux | ||
| Par géographie | Amérique du Nord | États-Unis |
| Canada | ||
| Mexique | ||
| Europe | Allemagne | |
| Royaume-Uni | ||
| France | ||
| Italie | ||
| Espagne | ||
| Reste de l'Europe | ||
| Asie-Pacifique | Chine | |
| Japon | ||
| Inde | ||
| Australie | ||
| Corée du Sud | ||
| Reste de l'Asie-Pacifique | ||
| Moyen-Orient et Afrique | CCG | |
| Afrique du Sud | ||
| Reste du Moyen-Orient et Afrique | ||
| Amérique du Sud | Brésil | |
| Argentine | ||
| Reste de l'Amérique du Sud | ||
Questions clés auxquelles répond le rapport
Quelle est la taille du marché de l'expression protéique acellulaire en 2025 ?
La taille du marché de l'expression protéique acellulaire est de 311,75 millions USD en 2025 et devrait atteindre 461,43 millions USD d'ici 2030 à un TCAC de 8,16 %.
Quel segment croît le plus rapidement dans l'expression protéique acellulaire ?
Les accessoires et consommables croissent à un TCAC de 8,56 %, le rythme le plus rapide parmi les catégories de produits, alors que les laboratoires mettent à l'échelle des flux de travail standardisés.
Quelle est la région géographique leader pour les revenus d'expression protéique acellulaire ?
L'Amérique du Nord représente 41,44 % des revenus 2024 grâce à une infrastructure biotech forte et des voies réglementaires de soutien.
Pourquoi les CRO adoptent-elles les plateformes d'expression protéique acellulaire ?
Les CRO s'appuient sur les systèmes d'expression protéique acellulaire pour livrer des projets d'expression protéique en 2-4 semaines versus des mois pour les méthodes basées sur les cellules, gagnant un avantage de croissance TCAC de 9,55 %.
Comment la technologie d'expression protéique acellulaire bénéficie-t-elle au développement de vaccins personnalisés ?
L'expression protéique acellulaire permet des doses de vaccin spécifiques aux patients stables à température ambiante à 1 USD ou moins, accélérant les programmes de réponse pandémique et d'oncologie.
Quel reste le goulot d'étranglement principal pour l'expansion du marché ?
La cohérence et la disponibilité d'approvisionnement de lysat à gros volume restent les contraintes clés, réduisant l'impact TCAC des prévisions de 1,1 %.
Dernière mise à jour de la page le:



