Taille et part du marché de la production d'anticorps
Analyse du marché de la production d'anticorps par Mordor Intelligence
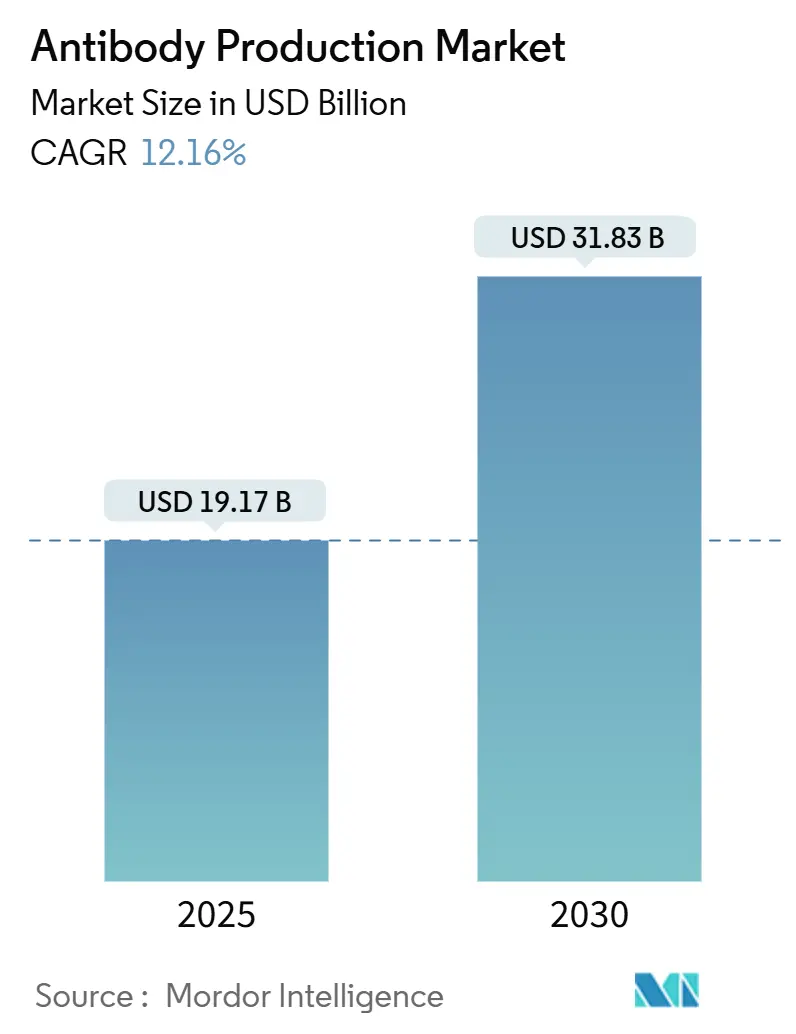
La taille du marché de la production d'anticorps est estimée à 19,17 milliards USD en 2025, et devrait atteindre 31,83 milliards USD d'ici 2030, à un TCAC de 12,16 % pendant la période de prévision (2025-2030).
L'adoption croissante de produits biologiques ciblés, l'adoption rapide de formats bispécifiques et des cas d'usage diagnostiques plus larges étendent la demande dans les domaines thérapeutiques, de recherche et des laboratoires cliniques. Les investissements continus dans les bioréacteurs à usage unique stimulent la flexibilité de production, tandis que les outils d'intelligence artificielle raccourcissent les cycles de développement de lignées cellulaires et améliorent la cohérence des lots. Les agences réglementaires soutiennent l'innovation par le biais de voies accélérées pour les biosimilaires et les nouvelles constructions d'anticorps, permettant aux petites entreprises et aux fabricants sous contrat de croître rapidement. La dynamique concurrentielle s'intensifie alors que les fournisseurs de services complets acquièrent des capacités spécialisées et que les organisations de développement et de fabrication sous contrat (CDMO) se différencient grâce à des plateformes bispécifiques propriétaires.
Points clés du rapport
- Par produit, les consommables ont dominé avec 62,54 % de la part du marché de la production d'anticorps en 2024 ; les instruments-bioréacteurs devraient croître à un TCAC de 11,98 % jusqu'en 2030.
- Par processus, les opérations en amont ont représenté 58,15 % de la part de la taille du marché de la production d'anticorps en 2024, tandis que la purification en aval progresse à un TCAC de 11,67 % jusqu'en 2030.
- Par type d'anticorps, les IgG monoclonaux ont détenu 70,67 % de la part du marché de la production d'anticorps en 2024 ; les anticorps bispécifiques enregistrent le TCAC le plus rapide de 12,04 % entre 2025-2030.
- Par utilisateur final, les entreprises pharmaceutiques et biotechnologiques ont commandé 63,34 % de la part de la taille du marché de la production d'anticorps en 2024 ; les CDMO enregistrent le TCAC projeté le plus élevé de 12,78 % jusqu'en 2030.
- Par géographie, l'Amérique du Nord un maintenu une part de 39,87 % en 2024, tandis que l'Asie-Pacifique est sur la voie d'un TCAC de 13,01 % jusqu'en 2030.
Tendances et perspectives du marché mondial de la production d'anticorps
Analyse d'impact des moteurs
| Moteur | (~) % Impact sur les prévisions TCAC | Pertinence géographique | Impact de pointe |
|---|---|---|---|
| Pipelines cliniques accélérés pour les ADC | ~+3,2 % | Amérique du Nord et Asie-Pacifique (États-Unis, Chine) | Moyen terme (3-4 ans) |
| Montée en puissance rapide de la capacité de bioréacteurs à usage unique | ~+2,8 % | Mondial, concentré en Amérique du Nord et en Europe | Court terme (≤ 2 ans) |
| Accélération réglementaire des mAb biosimilaires | ~+2,4 % | Mondial, prononcé dans l'UE, États-Unis, Chine | Moyen terme (3-4 ans) |
| Développement de lignées cellulaires assisté par IA réduisant la variabilité du titre | ~+2,1 % | Europe avec retombées en Amérique du Nord et Asie-Pacifique | Moyen terme (3-4 ans) |
| Poussée d'externalisation vers les CDMO | ~+1,9 % | Mondial, fort aux États-Unis, Chine, Inde | Moyen terme (3-4 ans) |
| Approbations croissantes d'anticorps bispécifiques | ~+2,0 % | Amérique du Nord et Europe, émergent en Asie | Moyen terme (3-4 ans) |
| Adoption de plateformes de bioprocédés continus | ~+1,6 % | Mondial, premiers adoptants aux États-Unis et UE | Long terme (≥ 5 ans) |
| Source: Mordor Intelligence | |||
Pipelines cliniques accélérés pour les conjugués anticorps-médicaments (ADC) aux États-Unis et en Chine
Plus de 600 candidats ADC sont en essais cliniques, et au moins 10 nouvelles approbations sont attendues d'ici 2027, soulignant l'élan soutenu dans les pipelines axés sur l'oncologie. L'approbation par la FDA en janvier 2025 du Datroway d'AstraZeneca et Daiichi Sankyo un réduit le risque de progression de la maladie dans le cancer du sein HR-positif, HER2-négatif de 37 % par rapport à la chimiothérapie AstraZeneca[1]Source : Samsung Biologics, "Installations optimisées pour une fabrication flexible et agile," samsungbiologics.com. L'expansion des capacités suit ; AstraZeneca s'est engagée à investir 1,5 milliard USD pour une installation ADC de bout en bout à Singapour qui sera opérationnelle en 2029 AstraZeneca. Des investissements similaires à grande échelle en Chine soutiennent des calendriers accélérés sous les priorités de l'Administration nationale des produits médicaux. Ces mouvements augmentent la demande pour des suites de conjugaison haute puissance, le confinement de vecteurs viraux et l'analyse avancée. Alors que les agences réglementaires affinent les directives pour les conjugués complexes, les fabricants adoptant des conceptions modulaires de salles blanches et des systèmes de purification à haut débit sont positionnés pour capturer les besoins cliniques émergents.
Montée en puissance rapide de la capacité de bioréacteurs à usage unique
Les bioréacteurs à usage unique (SUB) réduisent le risque de contamination croisée et permettent des changements plus rapides, essentiels pour les installations multi-produits. L'usine 5 de Samsung Biologics ajoutera des volumes SUB flexibles tout en raccourcissant le temps de construction de 30 % par rapport aux installations antérieures en acier inoxydable Samsung Biologics [2]Source : AstraZeneca, "Datroway approuvé aux États-Unis pour le cancer du sein HR-positif, HER2-négatif," astrazeneca.com. L'intégration du traitement continu avec les SUB génère des gains de productivité de 25-30 % et réduit l'empreinte des installations de 40 % Pharma Focus America. La miniaturisation des capteurs, les sondes à usage unique et le contrôle en boucle fermée permettent maintenant des ajustements qualité en temps réel, stimulant une adoption plus large au-delà des lots cliniques vers des programmes commerciaux à haut titre. La trajectoire soutient une forte demande pour les sacs de réacteurs stérilisés gamma, les unités d'entraînement et les voies d'écoulement auxiliaires jetables, renforçant la croissance des fournisseurs.
Accélération réglementaire des mAb biosimilaires
La désignation d'interchangeabilité de la FDA pour Yuflyma de Celltrion établit un nouveau précédent qui permet la substitution en pharmacie sans autorisation médicale FiercePharma. Des réformes parallèles en Chine ont réduit de moitié les délais d'approbation des biosimilaires, résultant en 51 lancements domestiques fin 2024, dont 31 sont basés sur des anticorps. Les voies accélérées intensifient la concurrence par les prix et stimulent les ajouts de capacité, notamment en Asie, où Henlius un expédié 5,5 millions d'unités de biosimilaires de trastuzumab vers 47 pays à la mi-2024 Henlius. Les fabricants optimisent la réutilisation de la Protéine un, adoptent la chromatographie multi-colonnes et déploient des systèmes d'ultrafiltration à passage unique plus grands pour rester compétitifs en coût tout en maintenant la comparabilité.
Développement de lignées cellulaires assisté par IA réduisant la variabilité du titre en Europe
Les groupes européens ont adopté des modèles d'apprentissage automatique qui identifient les nutriments du milieu influençant les variants de charge, resserrant le contrôle sur la glycosylation pour les bispécifiques complexes. Les études d'IA explicable ont souligné le rôle critique du Fe, Zn, Cu et Mn dans la modulation des profils post-traductionnels Springer. L'adoption de tels outils réduit les délais de développement jusqu'à 30 % tout en améliorant la prévisibilité du titre en phase précoce. L'Agence européenne des médicaments un répondu en mettant à jour les directives de validation pour inclure la conception d'expériences pilotée par IA ISPE. Les fournisseurs de services d'ingénierie vectorielle, de micro-bioréacteurs haut débit et d'analyses multi-omiques bénéficient alors que les producteurs se tournent vers des stratégies de développement riches en données.
Analyse d'impact des contraintes
| Contrainte | (~) % Impact sur les prévisions TCAC | Pertinence géographique | Impact de pointe | |
|---|---|---|---|---|
| CAPEX initial élevé pour les installations de biofabrication de grade GMP | ~-1,5 % | Mondial, frein plus fort dans les marchés émergents | Long terme (≥ 5 ans) | |
| Barrières de propriété intellectuelle pour les nouveaux formats bispécifiques | ~-1,2 % | Japon avec retombées mondiales pour les innovateurs bispécifiques | Moyen terme (3-4 ans) | |
| Complexité de conformité Qualité par conception (QbD) pour les petites et moyennes biotechs | ~-1,0 % | Mondial, surtout États-Unis et UE | Moyen terme (3-4 ans) | |
| Pénuries chroniques d'approvisionnement en composants de milieux sans protéines recombinantes | ~-0,7 % | Mondial, accentué en APAC lors des pics de demande | Court terme (≤ 2 ans) | |
| Source: Mordor Intelligence | ||||
CAPEX initial élevé pour les installations de biofabrication de grade GMP
Construire une usine d'anticorps de pointe peut dépasser 200 millions USD, les salles blanches et les services spécialisés représentant 60 % des dépenses BioProcess International. La récupération du capital s'étend sur 3-5 ans lorsque les permis, la validation et l'octroi de licences sont inclus. Les entrants des marchés émergents font face à des obstacles de financement plus raides et à la volatilité des taux d'intérêt, freinant les projets de terrain vierge. Les installations modulaires préfabriquées peuvent réduire le temps de construction de 30-50 %, mais le coût plus élevé des modules importés compense certaines économies Pharma Focus Asia. Par conséquent, la demande de capacité CDMO augmente alors que les innovateurs reportent la propriété en faveur de modèles de rémunération à l'acte, ralentissant marginalement l'expansion des revenus liés aux installations.
Barrières de propriété intellectuelle pour les nouveaux formats bispécifiques au Japon
L'office des brevets du Japon exige des données in vitro étendues pour soutenir les revendications bispécifiques larges, élevant la barre pour la reconnaissance de l'activité inventive. Ce régime strict un retardé les approbations locales par rapport aux États-Unis et à l'UE, contraignant l'accès des patients aux modalités de pointe. Les licences croisées entre les opérateurs historiques compliquent la complexité, forçant les petites entreprises à négocier des termes défavorables ou à contourner des fourrés de brevets denses. Les dépôts de Bristol-Myers Squibb illustrent une approche en couches combinant composition, procédé et couverture de formulation pour protéger les actifs sur le marché japonais. Les développeurs répondent avec des architectures bispécifiques structurellement distinctes, mais les cycles d'ingénierie itératifs allongent les délais de commercialisation, atténuant l'adoption à court terme.
Analyse par segment
Par produit : Les bioréacteurs à usage unique transforment l'économie de fabrication
Les consommables ont commandé 62,54 % de la part du marché de la production d'anticorps en 2024, reflétant la demande constante de milieux, résines, tampons et filtres qui soutiennent chaque lot de production. Les volumes récurrents élevés créent des flux de trésorerie prévisibles pour les fournisseurs mais ajoutent des dépenses opérationnelles pour les fabricants travaillant à améliorer le coût des marchandises. Les instruments-bioréacteurs constituent la catégorie à croissance la plus rapide, prévue pour progresser à un TCAC de 11,98 % alors que les conceptions à usage unique remplacent les systèmes en acier inoxydable et permettent l'agilité multi-produits. Les capteurs intégrés, les voies d'écoulement jetables et les plastiques prêts gamma atténuent le risque de contamination croisée et raccourcissent les changements, s'alignant avec les installations qui hébergent des programmes divers de bispécifiques et d'ADC.
Les stratégies de mise à l'échelle en amont s'appuient sur des trains SUB parallèles couplés à une capture continue, réduisant l'empreinte de l'installation tout en supportant des titres dépassant 10 g/L. Les avancées consommables, y compris les assemblages de tubes intelligents avec étiquettes RFID intégrées, rationalisent la traçabilité des matériaux et aident à la conformité. Alors que les cycles de vie des résines s'étendent grâce à de nouvelles chimies tolérantes aux alcalins, les opérateurs réduisent les volumes de tampon et diminuent les déchets, renforçant les métriques environnementales qui sont de plus en plus suivies dans les rapports ESG.
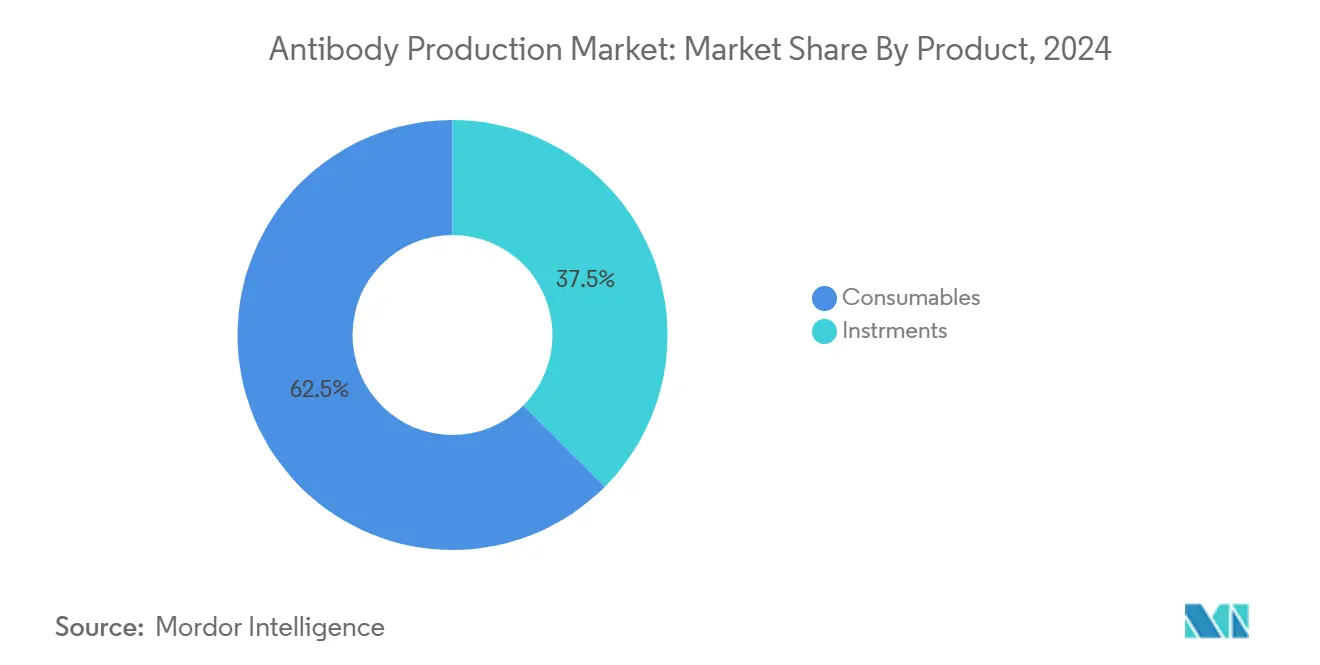
Note: Parts de segment de tous les segments individuels disponibles à l'achat du rapport
Par processus : Les innovations en aval traitent les goulots d'étranglement de purification
Les opérations en amont ont détenu 58,15 % de la taille du marché de la production d'anticorps en 2024, soulignant comment la productivité des lignées cellulaires et les performances des bioréacteurs pilotent l'économie globale. Les améliorations de titre émanent d'hôtes CHO modifiés délivrant des rendements >10 g/L et de stratégies fed-batch optimisées qui atténuent l'épuisement des nutriments. Ces gains déplacent le goulot d'étranglement vers la purification en aval, qui croît donc plus rapidement à un TCAC de 11,67 % jusqu'en 2030. Les résines de chromatographie multi-modale adaptées aux anticorps bispécifiques améliorent la résolution et les capacités de chargement, tandis que la filtration en profondeur de nouvelle génération se couple avec des réactifs de floculation pour clarifier les récoltes haute densité de SUB de 2 000 L.
L'intensification du processus incorpore l'inactivation virale continue et la filtration tangentielle à passage unique, créant des trains de purification directe qui réduisent le temps de traitement de 30 %. Les patins de gestion des tampons équipés de dilution en ligne freinent la consommation d'eau et les besoins d'espace au sol. Les fabricants poursuivant l'excellence opérationnelle intègrent des modèles de bilan massique en temps réel et un contrôle par rétroaction PAT, produisant des profils de glycosylation cohérents-un paramètre critique pour la comparabilité réglementaire. La convergence de l'intensification en amont et en aval débloque des économies de coûts et accélère la libération des lots, renforçant la compétitivité sur le marché de la production d'anticorps.
Par type d'anticorps : Les plateformes bispécifiques pilotent le pipeline d'innovation
Les anticorps IgG monoclonaux ont conservé 70,67 % de la part du marché de la production d'anticorps en 2024 en raison de cibles établies, de processus bien validés et d'une large expérience clinique. Les économies d'échelle et les chaînes d'approvisionnement robustes soutiennent des marges attractives pour les meilleurs vendeurs. En parallèle, les anticorps bispécifiques progressent à un TCAC de 12,04 % et devraient atteindre 50 milliards USD d'ici 2030, reflétant leur capacité à engager des cibles doubles pour une efficacité accrue Biointron. La complexité de fabrication se centre sur l'appariement correct des chaînes légères et l'assemblage d'hétérodimères, suscitant des innovations telles que Knobs-into-Holes et les cadres de chaînes légères communes.
Les plateformes propriétaires incluant le Columvi de Roche, approuvé pour le lymphome diffus à grandes cellules B en 2025, démontrent une réduction du risque de mortalité de 41 % par rapport aux soins standard FiercePharma. Les avancées dans le reciblage à double affinité et les technologies Beat® cherchent à simplifier la purification en permettant une capture en une seule étape. L'intensité R&D soutenue alimente la demande d'essais analytiques qui quantifient l'affinité cible et la fonction effectrice tôt dans le développement. Les construits basés sur des fragments et les conjugués anticorps-médicaments introduisent une diversité supplémentaire, mais chaque format exploite l'infrastructure partagée en amont et en aval, renforçant la croissance cohésive du marché de la production d'anticorps.
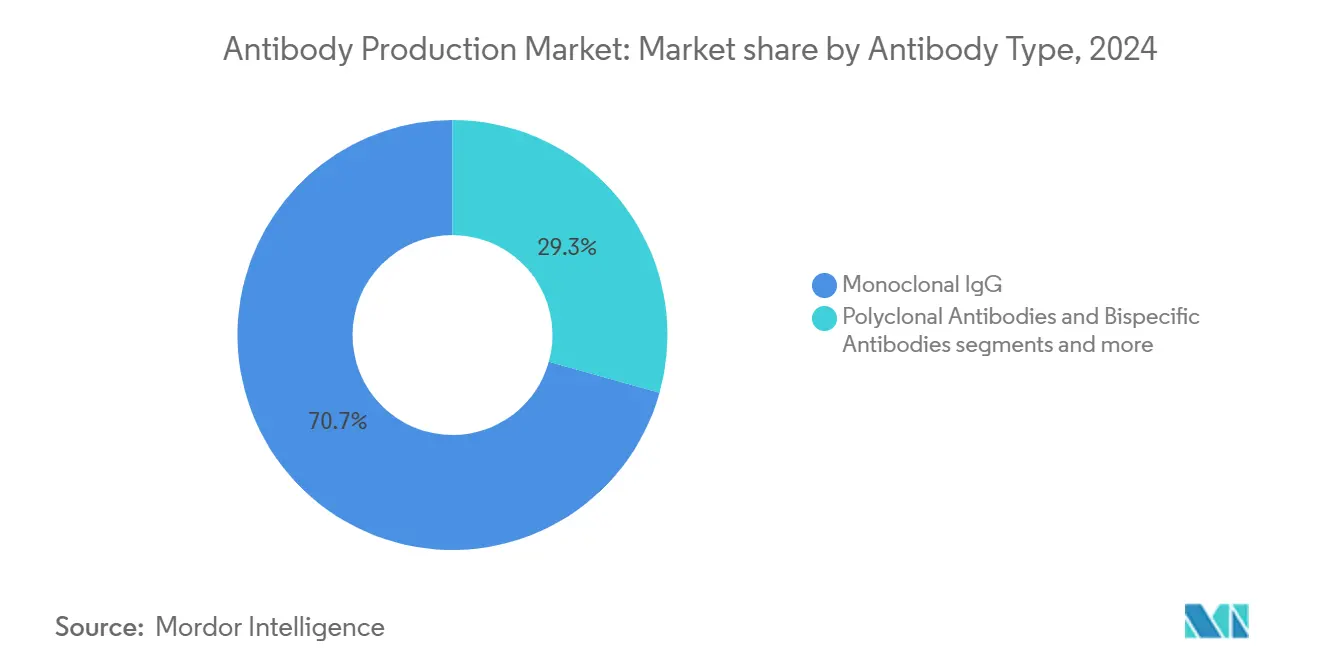
Note: Parts de segment de tous les segments individuels disponibles à l'achat du rapport
Par utilisateur final : Les CDMO capturent la tendance croissante d'externalisation
Les entreprises pharmaceutiques et biotechnologiques ont détenu 63,34 % de la taille du marché de la production d'anticorps en 2024, gérant d'vastes pipelines et l'approvisionnement commercial mondial. Néanmoins, la rationalisation des capacités et l'atténuation des risques motivent les grands sponsors à externaliser des programmes sélectionnés. Les CDMO affichent donc un TCAC leader de 12,78 %, soutenus par la demande de capacité flexible et de savoir-faire spécialisé. WuXi Biologics un rapporté un chiffre d'affaires de 18,7 milliards RMB en 2024, avec un carnet de commandes de 18,5 milliards USD soutenu par 151 nouveaux projets provenant principalement des États-Unis WuXi Biologics.
Les principaux fournisseurs de services exploitent des technologies propriétaires telles que WuXiBody™ pour résoudre les défis d'assemblage bispécifique, tandis que Lonza étend les suites de conjugaison pour capturer la vague ADC montante Lonza. Les laboratoires de diagnostic occupent une niche plus petite mais stable, appliquant des anticorps pour des tests compagnons et des essais de recherche qui éclairent les décisions de médecine de précision. Les instituts académiques et gouvernementaux restent vitaux pour l'innovation en phase précoce, s'associant souvent avec des CDMO pour traduire les découvertes en lots GMP. Le paradigme d'externalisation intensifie la concurrence, poussant les CDMO à investir dans les jumeaux numériques, l'intensification des processus et l'orchestration de projet de bout en bout
Par méthode : Les plateformes in vitro améliorent la reproductibilité
Les producteurs industriels s'appuient largement sur les systèmes d'expression in vitro car ils offrent des environnements contrôlés, une variabilité minimisée et des sorties évolutives. Les bibliothèques de présentation phagique englobant des milliards de variants accélèrent la sélection de candidats contre des épitopes difficiles, tandis que la présentation ribosomique ajoute une voie sans cellule qui accélère le criblage d'expression soluble. Le marché de la production d'anticorps bénéficie de ces plateformes qui rationalisent les pipelines de découverte précoce et alimentent des séquences de haute qualité dans le développement de processus. Les améliorations de conception vectorielle, l'optimisation des codons et l'ingénierie des cellules hôtes renforcent davantage la stabilité d'expression, réduisant l'attrition en phase tardive.
Les méthodes in vivo restent nécessaires pour les applications polyclonales à large spectre, mais les pressions éthiques et réglementaires limitent l'expansion future. Les souris humanisées et les souches transgéniques capables de produire des anticorps entièrement humains satisfont une partie de la demande tout en s'alignant avec les principes 3R (remplacement, réduction, raffinement). L'intégration de l'apprentissage automatique pour prédire la solubilité et le risque d'agrégation à partir des données de séquence raccourcit les délais de triage des candidats, renforçant les gains d'efficacité dans les flux de travail de l'industrie de production d'anticorps. Alors que les techniques computationnelles et de laboratoire humide convergent, le marché anticipe des taux de succès plus élevés et des transitions plus rapides de la découverte à la fabrication clinique.
Analyse géographique
L'Amérique du Nord un dominé le marché de la production d'anticorps avec une part de 39,87 % en 2024, soutenue par de solides marchés des capitaux, un dense cluster d'entreprises biopharmaceutiques et des cadres réglementaires avancés. Le raffinement continu par la FDA des voies accélérées favorise l'innovation en bispécifiques et biosimilaires, soutenant l'expansion du marché. L'intégration de l'intelligence artificielle dans l'analyse de production devient mainstream, permettant des stratégies de libération en temps réel qui réduisent les coûts d'inventaire.
L'Asie-Pacifique délivre le TCAC le plus rapide de 13,01 %, propulsé par l'expansion des écosystèmes de fabrication en Chine et en Inde et des politiques gouvernementales de soutien. L'approbation américaine de Jobevne par Biocon souligne les références qualité croissantes de l'Inde GaBIOnline. Les CDMO régionales augmentent le traitement continu et les constructions d'usines modulaires pour satisfaire les besoins domestiques et d'exportation. La position prudente du Japon sur la protection de la propriété intellectuelle pour les formats bispécifiques ralentit les lancements locaux mais encourage des contournements structurels inventifs.
L'Europe conserve un poids significatif grâce à son paysage biosimilaire mature, avec 64 approbations reflétant le leadership réglementaire précoce. L'accent sur la durabilité stimule l'adoption de la fabrication continue et des initiatives de réduction de solvants. La plateforme européenne de surveillance des pénuries et les directives GMP révisées pour l'IA signalent la vigilance réglementaire envers la sécurité d'approvisionnement et la surveillance numérique ISPE.
Paysage concurrentiel
Le marché de la production d'anticorps est modérément concentré, avec Thermo Fisher Scientific, Merck KGaA et Danaher ancrant la part de niveau supérieur grâce à des portefeuilles intégrés de réactifs, instruments et services. Les F&un stratégiques intensifient la pression concurrentielle ; l'acquisition de Seagen par Pfizer ajoute un pipeline ADC différencié et un savoir-faire de fabrication, remodelant la distribution des capacités BioPharma APAC. Les fournisseurs intégrés capitalisent sur les opportunités de vente croisée, regroupant le matériel à usage unique avec les consommables de chromatographie et les systèmes de contrôle numérique.
Les innovateurs spécialisés poursuivent les opportunités d'espaces blancs en bispécifiques, multispécifiques et ingénierie Fc. F-star Therapeutics exploite sa plateforme mAb²™ pour générer des bispécifiques tétravalents, tandis que Zymeworks avance les construits Azymetric qui conservent l'architecture IgG naturelle . Ces acteurs s'associent avec des CDMO pour compenser l'intensité capitalistique, échangeant l'accès technologique contre des créneaux de fabrication. L'étendue et la profondeur de la propriété intellectuelle définissent de plus en plus le levier de négociation, suscitant des dépôts de brevets robustes qui englobent les configurations de processus, formulation et dispositif.
Le leadership technologique est devenu un facteur de succès décisif. Les entreprises intègrent l'analyse prédictive dans les boucles de contrôle en temps réel, élevant les rendements de lots et diminuant les déviations. Les plateformes de bioprocédés continus, la sélection de lignées cellulaires guidée par IA et le criblage haut débit équipent les entreprises pour livrer des produits plus rapides et moins coûteux. Le paysage concurrentiel en évolution récompense l'agilité, la différenciation technologique et la maîtrise réglementaire mondiale, assurant un élan soutenu sur le marché de la production d'anticorps.
Leaders de l'industrie de la production d'anticorps
-
Sartorius AG
-
Danaher Corporation
-
Merck KGaA
-
Eppendorf AG
-
Thermo Fisher Scientific
- *Avis de non-responsabilité : les principaux acteurs sont triés sans ordre particulier
Développements récents de l'industrie
- Janvier 2025 : AstraZeneca un reçu l'approbation de la FDA pour Datroway (datopotamab deruxtecan) pour le cancer du sein métastatique HR-positif, HER2-négatif précédemment traité, réduisant le risque de progression de la maladie de 37 % .
- Mars 2025 : Lonza un étendu un partenariat pour la fabrication d'ADC à échelle commerciale et un commencé à construire une nouvelle suite de bioconjugaison à Visp, Suisse .
- Janvier 2025 : Le Columvi de Roche est devenu le premier anticorps bispécifique d'Europe approuvé pour le lymphome diffus à grandes cellules B, réduisant le risque de mortalité de 41 % FiercePharma.
Portée du rapport sur le marché mondial de la production d'anticorps
Selon la portée du rapport, la production d'anticorps fait référence au processus de création d'un anticorps spécifique. Au sens large, elle consiste en diverses méthodes, telles que l'amont, l'aval et la filtration. Le processus implique la préparation d'échantillons d'antigènes, qui sont injectés dans les animaux de laboratoire ou de ferme pour évoquer des niveaux d'expression élevés d'anticorps spécifiques à l'antigène dans le sérum, qui sont ensuite récupérés de l'animal. Le marché de la production d'anticorps est segmenté par type d'anticorps (anticorps monoclonaux, anticorps polyclonaux, autres types d'anticorps), processus (traitement en amont, traitement en aval, filtration), utilisateur final (entreprises pharmaceutiques et biotechnologiques, laboratoires de recherche, autres utilisateurs finaux), et géographie (Amérique du Nord, Europe, Asie-Pacifique, Moyen-Orient et Afrique, et Amérique du Sud). Le rapport couvre également les tailles de marché estimées et les tendances pour 17 pays dans les principales régions mondiales. Le rapport offre la valeur (en millions USD) pour les segments ci-dessus.
| Consommables | Milieux et sérums |
| Réactifs et suppléments | |
| Tampons et produits chimiques | |
| Instruments | Bioréacteurs |
| Systèmes de chromatographie | |
| Dispositifs de filtration et séparation | |
| Équipement de laboratoire de soutien |
| Traitement en amont | Développement de lignées cellulaires |
| Systèmes d'expansion de culture et d'expression | |
| Traitement en aval | Clarification et capture |
| Purification | |
| Formulation et remplissage-finition |
| Anticorps monoclonaux |
| Anticorps polyclonaux |
| Anticorps bispécifiques |
| Fragments d'anticorps |
| Entreprises pharmaceutiques et biotechnologiques |
| Organisations de fabrication/recherche sous contrat (CMO/CRO) |
| Instituts de recherche académiques et gouvernementaux |
| Laboratoires de diagnostic |
| Amérique du Nord | États-Unis |
| Canada | |
| Mexique | |
| Europe | Allemagne |
| Royaume-Uni | |
| France | |
| Italie | |
| Espagne | |
| Reste de l'Europe | |
| Asie-Pacifique | Chine |
| Japon | |
| Inde | |
| Corée du Sud | |
| Australie | |
| Reste de l'Asie | |
| Moyen-Orient et Afrique | CCG |
| Afrique du Sud | |
| Reste du Moyen-Orient et Afrique | |
| Amérique du Sud | Brésil |
| Argentine | |
| Reste de l'Amérique du Sud |
| Par produit | Consommables | Milieux et sérums |
| Réactifs et suppléments | ||
| Tampons et produits chimiques | ||
| Instruments | Bioréacteurs | |
| Systèmes de chromatographie | ||
| Dispositifs de filtration et séparation | ||
| Équipement de laboratoire de soutien | ||
| Par processus | Traitement en amont | Développement de lignées cellulaires |
| Systèmes d'expansion de culture et d'expression | ||
| Traitement en aval | Clarification et capture | |
| Purification | ||
| Formulation et remplissage-finition | ||
| Par type d'anticorps | Anticorps monoclonaux | |
| Anticorps polyclonaux | ||
| Anticorps bispécifiques | ||
| Fragments d'anticorps | ||
| Par utilisateur final | Entreprises pharmaceutiques et biotechnologiques | |
| Organisations de fabrication/recherche sous contrat (CMO/CRO) | ||
| Instituts de recherche académiques et gouvernementaux | ||
| Laboratoires de diagnostic | ||
| Par géographie | Amérique du Nord | États-Unis |
| Canada | ||
| Mexique | ||
| Europe | Allemagne | |
| Royaume-Uni | ||
| France | ||
| Italie | ||
| Espagne | ||
| Reste de l'Europe | ||
| Asie-Pacifique | Chine | |
| Japon | ||
| Inde | ||
| Corée du Sud | ||
| Australie | ||
| Reste de l'Asie | ||
| Moyen-Orient et Afrique | CCG | |
| Afrique du Sud | ||
| Reste du Moyen-Orient et Afrique | ||
| Amérique du Sud | Brésil | |
| Argentine | ||
| Reste de l'Amérique du Sud | ||
Questions clés auxquelles répond le rapport
Quelle est la taille actuelle du marché de la production d'anticorps ?
Le marché de la production d'anticorps s'élève à 19,17 milliards USD en 2025 et devrait croître à 31,83 milliards USD d'ici 2030.
Quelle catégorie de produits progresse le plus rapidement ?
Les instruments-bioréacteurs, particulièrement les systèmes à usage unique, montrent la croissance la plus élevée avec un TCAC de 11,98 % jusqu'en 2030.
Pourquoi les anticorps bispécifiques sont-ils importants ?
Les anticorps bispécifiques peuvent lier deux cibles distinctes simultanément, améliorant l'efficacité thérapeutique et stimulant un TCAC de 12,04 %, le plus élevé parmi les types d'anticorps.
À quelle vitesse l'Asie-Pacifique croît-elle ?
L'Asie-Pacifique devrait enregistrer un TCAC de 13,01 % de 2025-2030, en faisant le marché régional à croissance la plus rapide.
Pourquoi les entreprises externalisent-elles la production d'anticorps ?
L'externalisation vers les CDMO offre une capacité flexible et une expertise spécialisée, mise en évidence par le TCAC projeté de 12,78 % des CDMO.
Quel rôle jouent les bioréacteurs à usage unique dans l'expansion du marché ?
Les bioréacteurs à usage unique réduisent le risque de contamination et les coûts en capital, contribuant à ~+2,8 points de pourcentage au TCAC mondial du marché.
Dernière mise à jour de la page le:



