Influenza-Diagnostik-Marktgröße und -anteil
Influenza-Diagnostik-Marktanalyse von Mordor Intelligence
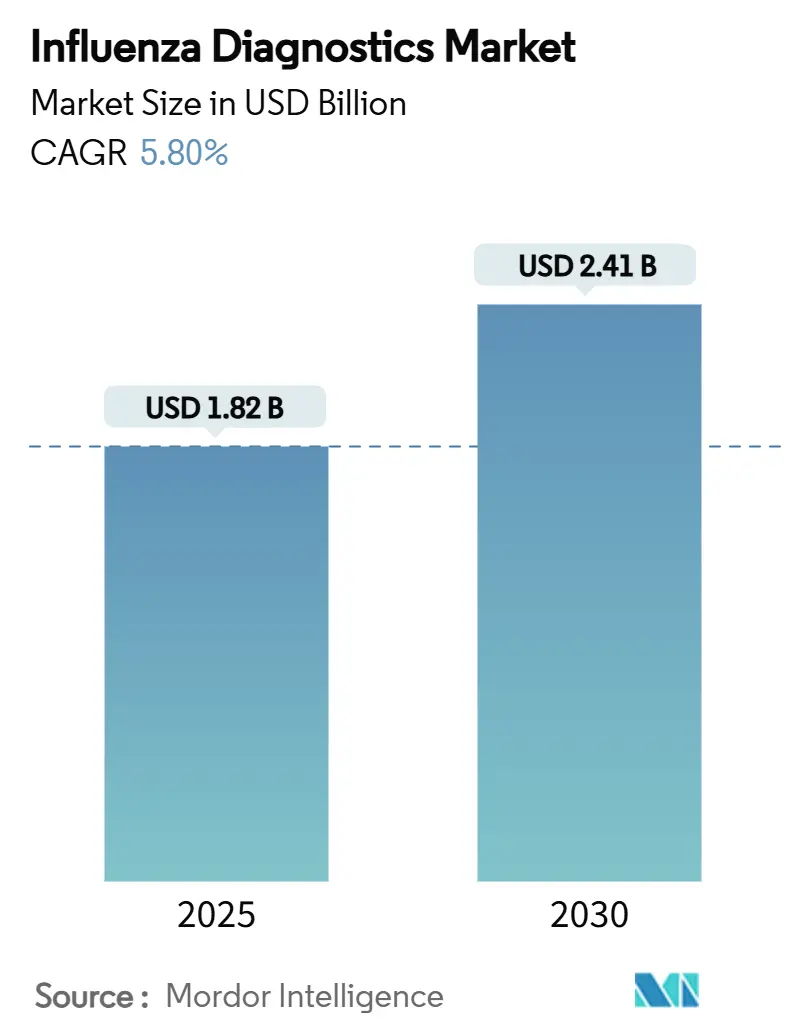
Die Influenza-Diagnostik-Marktgröße belief sich 2025 auf 1,82 Milliarden USD und wird voraussichtlich bis 2030 2,41 Milliarden USD erreichen, mit einem Wachstum von 5,8% CAGR über den Zeitraum. Diese gesunde Entwicklung folgt dem Übergang des Marktes von pandemischer Volatilität hin zu routinemäßigem, technologiegetriebenem Management von Atemwegserkrankungen. Das Wachstum wird durch die breitere Adoption molekularer Plattformen verankert, die höhere Genauigkeit als herkömmliche Schnellantigen-Tests bieten, stetige Regierungsfinanzierung für Überwachungsinfrastruktur und steigende Verbrauchernachfrage nach Heimtest- und Point-of-Care (POC)-Lösungen. Anbieter konsolidieren sich, um molekulare Genauigkeit mit patientennaher Geschwindigkeit zu kombinieren, während KI-gestützte Software die Laborumlaufzeiten verkürzt und die Qualitätskontrolle verbessert. Regionale Dynamiken formen die Nachfrage weiter: Nordamerika führt bei der installierten Basis und Erstattungsklarheit, während Asien-Pazifik die schnellste Aufnahme verzeichnet dank fortlaufender Investitionen in öffentliche Gesundheitslabore.
Wichtige Berichtsergebnisse
- Nach Testtyp erfassten schnelle Influenza-Diagnosetests 41,6% des Influenza-Diagnostik-Marktanteils in 2024, während CRISPR-basierte Assays eine CAGR von 9,7% bis 2030 projiziert werden.
- Nach Endnutzer hielten Krankenhäuser und klinische Labore 42,3% des Marktes in 2024; Point-of-Care-Einstellungen verzeichnen die höchste prognostizierte CAGR von 9,5% bis 2030.
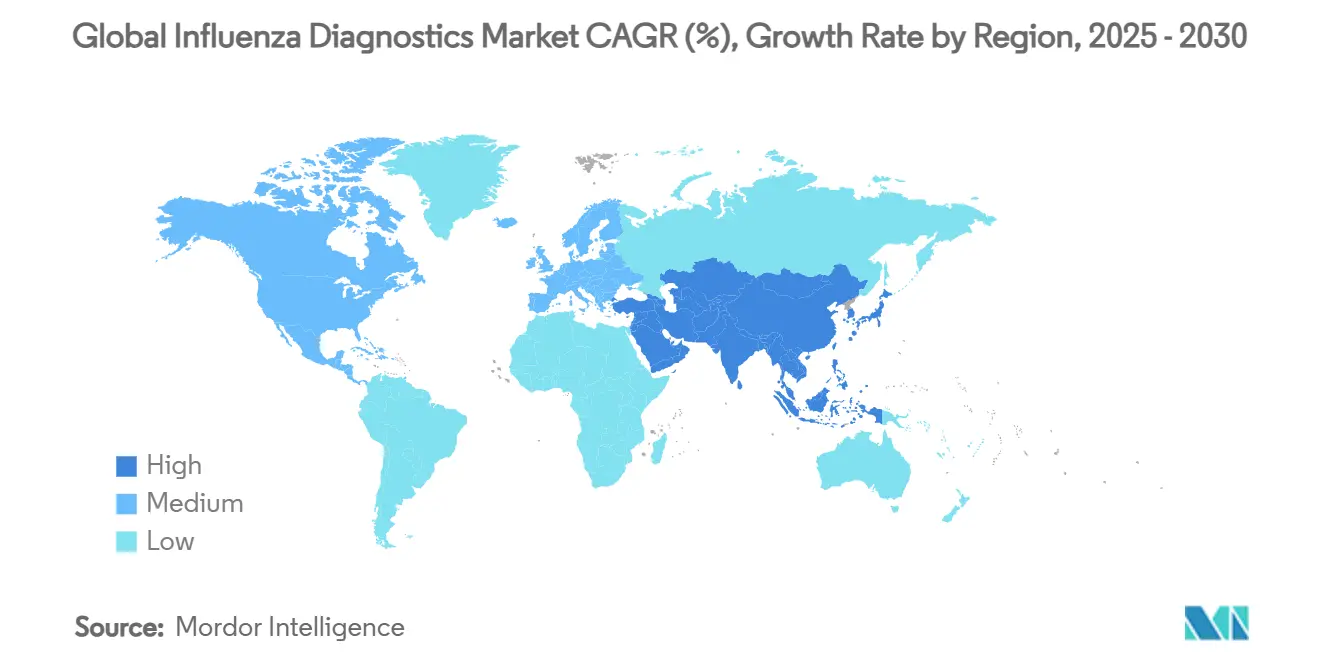
- Nach Geographie kommandierte Nordamerika 37,8% Umsatzanteil in 2024; Asien-Pazifik wird voraussichtlich mit 8,1% CAGR bis 2030 wachsen.
Globale Influenza-Diagnostik-Markttrends und Einblicke
Treiber-Auswirkungsanalyse
| Treiber | (~) % Auswirkung auf CAGR-Prognose | Geografische Relevanz | Auswirkungszeitrahmen |
|---|---|---|---|
| Steigende Prävalenz & Schwere von saisonalen und zoonotischen Influenza-Ausbrüchen | +1.20% | Global, mit verstärkter Auswirkung in Asien-Pazifik und Nordamerika | Mittelfristig (2-4 Jahre) |
| Wachsende Adoption von schnellen Point-of-Care (POC)-Tests in ambulanten Einrichtungen | +0.90% | Nordamerika & EU, expandierend nach APAC | Kurzfristig (≤ 2 Jahre) |
| Regierungsfinanzierte Überwachungsprogramme & Pandemie-Bereitschaftsbudgets | +0.80% | Global, konzentriert in entwickelten Märkten | Langfristig (≥ 4 Jahre) |
| KI-gestützte Ergebnis-Interpretationssoftware, die molekularen Workflow-Durchsatz steigert | +0.70% | Nordamerika & EU Kern, Übertragung auf APAC | Mittelfristig (2-4 Jahre) |
| Kommerzialisierung von Kombi-SARS-CoV-2/Grippe-Multiplex-Panels, die installierte Basis erweitern | +0.60% | Global, mit früher Adoption in Nordamerika | Kurzfristig (≤ 2 Jahre) |
| Zunehmende Integration von Telemedizin mit heimbasierten Grippe-Testkits | +0.50% | Nordamerika & EU, schrittweise APAC-Adoption | Mittelfristig (2-4 Jahre) |
| Quelle: Mordor Intelligence | |||
Steigende Prävalenz & Schwere von saisonalen und zoonotischen Influenza-Ausbrüchen
Ein Wiederaufleben der saisonalen Influenza-Aktivität hat die globale Diagnostik-Nachfrage intensiviert, wobei das CDC 39.053 laborbestätigte Krankenhausaufenthalte während der Saison 2024-2025 verzeichnete, die höchste Rate seit 2010-2011.[1]Centers for Disease Control and Prevention, "Weekly Flu Season Update," cdc.govGleichzeitig generierten hochpathogene H5N1-Ausbrüche 38 menschliche Fälle in Kalifornien unter Molkereiarbeitern und veranlassten erweiterte Viehüberwachung. Neue Kits, wie Singapurs Steadfast-Assay, unterscheiden hochpathogene und niedrigpathogene Stämme innerhalb von drei Stunden und verbessern die Ausbruchsreaktion. Diese Ereignisse drängen Gesundheitssysteme dazu, Notfall-Testkapazitäten das ganze Jahr über aufrechtzuerhalten und die Beschaffung hochgenauer molekularer Plattformen zu unterstützen.
Wachsende Adoption von schnellen Point-of-Care-Tests in ambulanten Einrichtungen
Krankenhausstudien der University of Southampton zeigten, dass POC-Influenza-Tests die Ergebniszeit auf unter eine Stunde verkürzen und schnellere antivirale Einleitung und kürzere Patientenaufenthalte ermöglichen. Plattformen umfassen jetzt molekulare Optionen wie Abbotts ID NOW, das Influenza A/B-Ergebnisse in 13 Minuten mit 96,3% Sensitivität liefert. KI-verbesserte Lesegeräte reduzieren die Interpretationszeit weiter auf zwei Minuten.[2]Baozhang Li, "TIMESAVER: Rapid Deep-Learning Interpretation of Lateral-Flow Assays," Nature Communications, nature.com Niedrigere Transportkosten und Behandlung beim selben Besuch unterstützen wirtschaftliche Argumente für weit verbreiteten POC-Einsatz in Kliniken und Einzelhandels-Gesundheitsstandorten.
Regierungsfinanzierte Überwachungsprogramme & Pandemie-Bereitschaftsbudgets
Lehren aus der COVID-Zeit führten zu höheren Zuweisungen, wobei das U.S. Department of Health and Human Services 172 Millionen USD für Influenza-Bereitschaft im Haushaltsjahr 2025 bereitstellte. Das CDC arbeitet jetzt mit kommerziellen Laboren wie Quest Diagnostics und Labcorp zusammen, um die Vogelgrippe-Testkapazität zu erweitern. Währenddessen erreichte die WHO eine vollständige nationale Influenza-Zentrum-Abdeckung in 11 südostasiatischen Ländern in 2024, ein Meilenstein, der die Grundnachfrage nach standardisierten Diagnostik-Kits erhöht. Diese Programme stabilisieren Beschaffungszyklen und setzen Leistungsmaßstäbe, die private F&E lenken.
KI-gestützte Ergebnis-Interpretationssoftware, die molekularen Workflow-Durchsatz steigert
Maschinenlern-Pipelines klassifizieren jetzt Virussequenzen und markieren Mutationen schneller als manuelle Prozesse, wodurch der Labordurchsatz ohne neue Hardware erhöht wird.[3]Hannah R. Meredith, "Machine-Learning Pipeline Accelerates Virus Detection and SNP Discovery," PubMed Central, ncbi.nlm.nih.govBugSeqs Zusammenarbeit mit BARDA bringt KI-gesteuerte Berichterstattung in die klinische Metagenomik und unterstützt pathogen-agnostische Überwachung. TIMESAVER, ein Deep-Learning-Algorithmus, hob die Sensitivität von Lateral-Flow-Assays für Influenza A/B auf 93,8%, während die Lesezeit auf zwei Minuten verkürzt wurde. Labore, die solche Tools einsetzen, verbessern die Qualitätskontroll-Konsistenz und können Kapazitäten während saisonaler Spitzen flexibel anpassen.
Hemmnis-Auswirkungsanalyse
| Hemmnis | (~) % Auswirkung auf CAGR-Prognose | Geografische Relevanz | Auswirkungszeitrahmen |
|---|---|---|---|
| Variable Sensitivität & Falsch-Negativ-Rate von RIDTs | -0.80% | Global, besonders in ressourcenarmen Gebieten | Kurzfristig (≤ 2 Jahre) |
| Hohe Kapital- & Betriebskosten molekularer Diagnostikplattformen | -0.60% | APAC und Schwellenmärkte, moderate Auswirkung in entwickelten Regionen | Mittelfristig (2-4 Jahre) |
| Regulatorische Unsicherheit für CRISPR-basierte Influenza-Assays | -0.40% | Global, mit variierenden regionalen Genehmigungszeitrahmen | Langfristig (≥ 4 Jahre) |
| Lieferkettenstörungen, die kritische Reagenzien für PCR-Assays betreffen | -0.50% | Global, mit verstärkter Auswirkung während geopolitischer Spannungen | Kurzfristig (≤ 2 Jahre) |
| Quelle: Mordor Intelligence | |||
Variable Sensitivität & Falsch-Negativ-Rate von RIDTs
Viele RIDTs übersehen frühe Infektionen, wenn die Viruslast niedrig ist; Studien setzen Falsch-Negativ-Raten über 30% für bestimmte kommerzielle Kits an. Das Panbio COVID-19/Flu A&B-Panel lieferte nur 80,8% Sensitivität für Influenza. Die WHO-Leitlinien von 2024 empfehlen jetzt Nukleinsäure-Tests für schwere oder Hochrisikofälle. Kliniken haben bestätigende PCR-Arbeitsabläufe eingeführt, die den Geschwindigkeitsvorteil von RIDTs zunichte machen und die Segmentexpansion eindämmen.
Hohe Kapital- & Betriebskosten molekularer Diagnostikplattformen
Umfassende Systeme wie Roches Cobas 6800 erfordern erhebliches Kapital plus Serviceverträge, die über die Budgets vieler mittelgroßen Krankenhäuser hinausgehen. Reagenzien, Wartung und qualifizierte Arbeitskräfte halten die Betriebsausgaben hoch; Lieferkettenschocks heben zusätzlich die Logistikausgaben an, die 2024 fast 20% des Umsatzes für Gerätehersteller erreichten. In einkommensschwächeren Märkten verlangsamt begrenzte Erstattung für syndromische Panels die Adoption trotz klinischer Vorteile.
Segmentanalyse
Nach Testtyp: CRISPR-Innovation fordert traditionelle Dominanz heraus
Schnellformate blieben mit 41,6% Umsatzanteil dominant, doch der Influenza-Diagnostik-Markt repositioniert sich, da Kliniker Sensitivität und Multiplexing priorisieren. CRISPR-Assays zeigen 9,7% CAGR bis 2030, angeführt vom SHINE-Test des Broad Institute, der Subtypen in 15 Minuten unterscheidet. Molekulare Panels, die Influenza A/B, RSV und SARS-CoV-2 bündeln, liefern operative Effizienz für Notaufnahmen. Die Influenza-Diagnostik-Marktgröße für CRISPR-Plattformen wird voraussichtlich am schnellsten unter allen Modalitäten expandieren, angetrieben von vereinfachten Arbeitsabläufen und schrumpfenden Instrumentenfußabdrücken. Direkte Fluoreszenzantikörper- und Viruskulturtests dienen weiterhin Forschungsnischen, wo Stammtypisierung oder antivirale Suszeptibilität erforderlich ist, beeinflussen aber nicht mehr mainstream-Kaufentscheidungen.
Molekulare Diagnostik, einschließlich RT-PCR und isothermer Formate, sehen beschleunigte Aufnahme, da KI-Tools die Ergebnisinterpretation rationalisieren. Multiplex-CRISPR-Cas13a-Streifen erreichten 100% Übereinstimmung mit RT-qPCR, während Amplifikationsschritte entfernt wurden. Krankenhäuser bevorzugen syndromische Panels, die überlappende Atemwegssymptome innerhalb einer einzigen Probe unterscheiden, während Einzelhandelskliniken CLIA-genehmigte molekulare Kartuschen für schnelle Walk-in-Begegnungen adoptieren. Diese Konvergenz von Genauigkeit und Geschwindigkeit positioniert molekulare Lösungen, um RIDT-Führerschaft zu erodieren, während Kapitalbarrieren abnehmen.
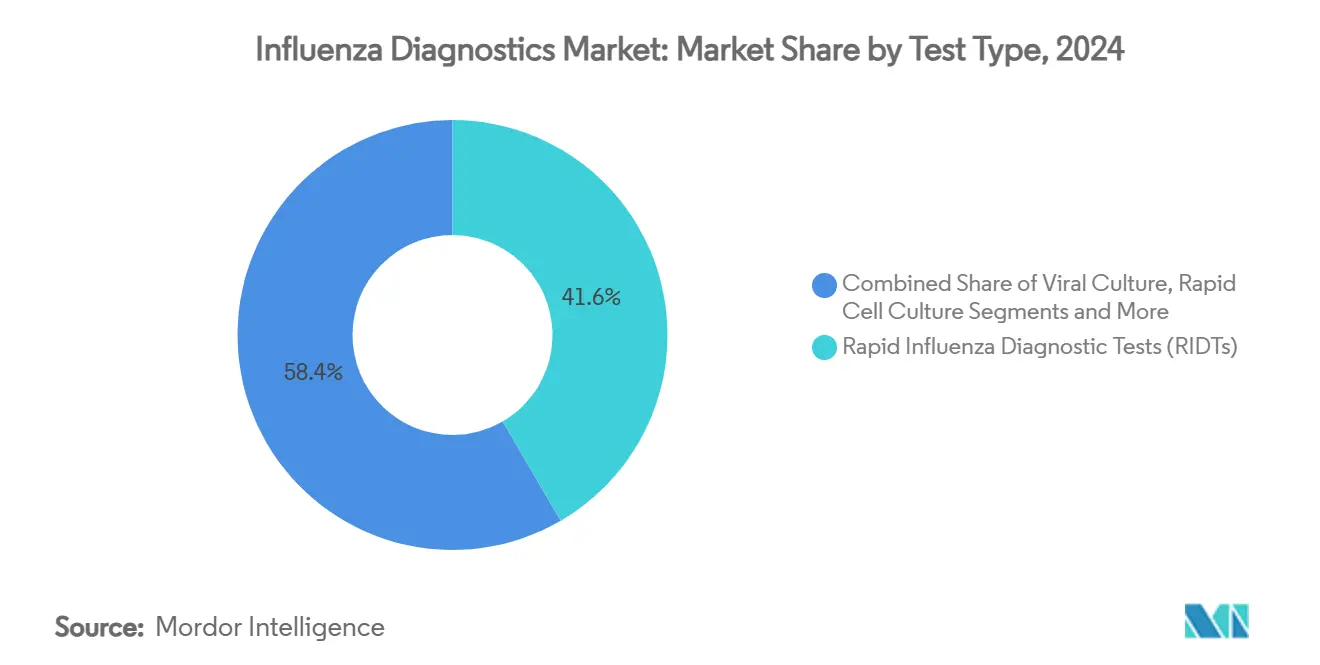
Notiz: Segmentanteile aller einzelnen Segmente beim Berichtkauf verfügbar
Nach Endnutzer: Krankenhaus-Konsolidierung gegen POC-Expansion
Krankenhäuser und klinische Labore generierten 42,3% der 2024-Umsätze durch Nutzung von Hochdurchsatz-Instrumenten und hauseigener Mikrobiologie-Expertise. Konsolidierung unter Gesundheitssystemen konzentriert Kaufkraft und ermöglicht Bulk-Reagenzienverträge, die Versorgung stabilisieren. Point-of-Care-Standorte zeigen jedoch die höchste 9,5% CAGR, da Ärzte sofortige Antworten für Behandlung während eines einzigen Besuchs benötigen. Der Influenza-Diagnostik-Marktanteil von Apotheken und Notfallzentren steigt weiter, da Einzelhändler wie CVS 3-in-1-Kombotests in 1.600 Standorten einsetzen.
Unabhängige Diagnoselabore behalten Relevanz durch Betreuung von ambulanten Kliniken und Fachpraxen, sehen aber Überweisungsrückgänge, wo Krankenhäuser Tests intern durchführen. Heimtests bilden ein aufkommendes Unter-Segment, nachdem die FDA 2024 den ersten OTC-Kombo-Grippe/COVID-Assay freigab. Über alle Einstellungen hinweg nutzt die Influenza-Diagnostik-Industrie Telemedizin-Verbindungen, um Ergebnisse direkt in elektronische Gesundheitsakten zu übertragen und antivirale E-Verschreibungen ohne zusätzliche Klinikbesuche zu unterstützen. Quelle: https://www.mordorintelligence.com/industry-reports/global-influenza-diagnostics-market
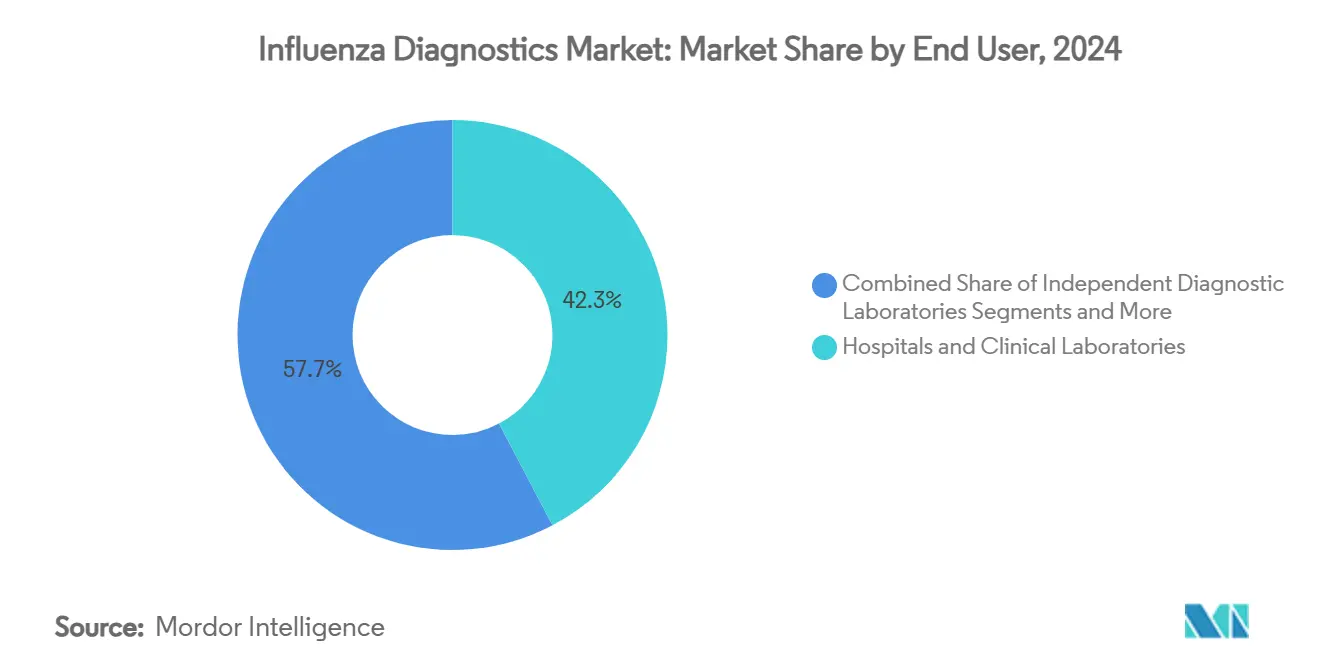
Notiz: Segmentanteile aller einzelnen Segmente beim Berichtkauf verfügbar
Geographieanalyse
Nordamerikas Führung stammt von umfassenden Überwachungssystemen und reifen Erstattungsmodellen. Das CDC koordiniert acht regionale Überwachungszentren, die 125 Länder umfassen, behält jedoch seinen größten Testfußabdruck im Inland. Die Influenza-Diagnostik-Marktgröße in Nordamerika profitiert von Thermo Fisher Scientifics 2-Milliarden-USD-Investition zur Erweiterung der inländischen Fertigung, die darauf abzielt, Lieferketten zu isolieren. Einzelhandelsapotheken integrieren CLIA-genehmigte molekulare Kartuschen für Behandlung beim selben Besuch, während Krankenversicherer zunehmend Heimsammlungskits erstatten und den Verbraucherzugang erweitern.
Asien-Pazifik verzeichnet die schnellste 8,1% CAGR aufgrund schneller Laboraufbauten und Regierungsfinanzierung. WHOs Meilenstein von 11 vollständig operativen nationalen Influenza-Zentren in Südostasien belegt diesen Fortschritt. Japan aktualisierte Qualitätsmanagementsbestimmungen zur Angleichung an ISO 13485:2016 und glättete Genehmigungswege für ausländische Assay-Entwickler. China und Indien kanalisieren impfstoffbezogene mRNA-Investitionen in die Diagnostik und fördern lokal hergestellte CRISPR-Kartuschen für regionale Verteilung.
Europa bleibt durch die In-vitro-Diagnostika-Verordnung (IVDR) einflussreich, die Konformitätsbewertungsanforderungen von 15% auf fast 90% der Assays erhöht. 2024 gewährte Übergangsextensionen verhindern sofortige Versorgungsengpässe, erhöhen aber Compliance-Kosten, die F&E zu weniger, höherwertigen Tests verschieben könnten. Naher Osten & Afrika und Südamerika verfolgen Kapazitätswachstum über multilaterale Hilfe und öffentlich-private Partnerschaften; die OECD drängt auf diversifizierte Beschaffung zur Minderung logistischer Schocks aus der Pandemie. Diese ungleiche Bereitschaft formt divergierende Adoptionskurven, doch gemeinsame Betonung der Atemwegsüberwachung unterhält globale Nachfrage nach robusten Assays. Quelle: https://www.mordorintelligence.com/industry-reports/global-influenza-diagnostics-market
Wettbewerbslandschaft
Der Influenza-Diagnostik-Markt zeigt moderate Konsolidierung: Die Top-5-Firmen verantworten fast 60% des globalen Umsatzes, doch agile Innovatoren erobern noch immer Weißraum-Nischen. Roches 295-Millionen-USD-Kauf von LumiraDx' POC-Technologie unterstreicht strategische Züge, molekulare Genauigkeit mit tragbarer Bequemlichkeit zu vereinen. bioMérieux' 111-Millionen-Euro-Akquisition von SpinChip bringt 10-Minuten-Vollblut-Immunoassays in sein Portfolio. Abbott und QuidelOrtho iterieren weiterhin CLIA-genehmigte Kombotests für Influenza A/B, RSV und SARS-CoV-2 in Einzelhandelseinstellungen, wo Durchsatz und Einfachheit breitere Panels übertrumpfen.
Aufkommende Wettbewerber differenzieren sich über CRISPR- oder KI-Fähigkeiten. Das Broad Institutes Papierstreifen-SHINE-Assay verspricht molekular-gradige Sensitivität in 15 Minuten ohne Instrumentierung. BugSeq integriert KI-Berichterstattung mit Nanopore-Sequenzierung für pathogen-agnostische Detektion. Lieferketten-Resilienz fließt jetzt in Wettbewerbsvorteile ein; Thermo Fishers Vier-Jahres-Plan widmet 1,5 Milliarden USD zur Steigerung der inländischen Produktion als Antwort auf 2024 erlebte PCR-Reagenzienmangel. Da Erstattung zu gebündelten Atemwegspanels wechselt, werden Plattformvielseitigkeit und Kosten-pro-berichtbares-Ergebnis zukünftige Marktanteilszuteilungen diktieren. Quelle: https://www.mordorintelligence.com/industry-reports/global-influenza-diagnostics-market
Influenza-Diagnostik-Industrieführer
-
Becton, Dickinson and Company
-
F. Hoffmann-La Roche Ltd
-
Thermo Fisher Scientific
-
Abbott Laboratories
-
QuidelOrtho Corporation
- *Haftungsausschluss: Hauptakteure in keiner bestimmten Reihenfolge sortiert
Jüngste Industrieentwicklungen
- Juni 2025: Thermo Fisher Scientific kündigte Pläne an, Teile seines Diagnostik-Geschäfts für etwa 4 Milliarden USD zu veräußern, einschließlich seiner Mikrobiologie-Sparte, die 1,4 Milliarden USD jährlichen Umsatz generiert
- Juni 2025: Illumina stimmte zu, SomaLogic für 350 Millionen USD zu akquirieren, um die Multiomik-Biomarker-Entdeckung zu beschleunigen.
- April 2025: HealthTrackRx und das CDC stellten einen schnellen H5N1-PCR-Test vor, um die Ausbruchsbereitschaft zu stärken.
- April 2025: Thermo Fisher Scientific verpflichtete sich zu 2 Milliarden USD für US-Fertigung und F&E-Expansion über vier Jahre.
- Februar 2025: Bio-Rad Laboratories bot an, Stilla Technologies zu akquirieren, um digitale PCR-Angebote zu stärken.
Globaler Influenza-Diagnostik-Marktberichtumfang
Influenza, auch als Grippe bekannt, ist eine hochansteckende Infektionskrankheit, die durch ein Virus verursacht wird. Dies ist eine Infektion der Atemwege, die Fieber und schwere Schmerzen verursacht. Der Influenza-Diagnostik-Markt umfasst die Tests, die zur Diagnose von Influenza-Fällen durchgeführt werden. Gemäß dem Umfang dieses Berichts wurden nur die Testkits und Reagenzien, die für die Diagnose von Influenza verwendet werden, zur Berechnung der Gesamtmarktgröße betrachtet. Der Influenza-Diagnostik-Markt ist segmentiert nach Testtyp (Traditioneller Diagnosetest und Molekularer Diagnose-Assay), Endnutzer (Krankenhaus, Labore, Andere Endnutzer) und Geographie (Nordamerika, Europa, Asien-Pazifik, Naher Osten und Afrika sowie Südamerika). Der Bericht deckt auch die geschätzten Marktgrößen und Trends für 17 Länder in bedeutenden Regionen weltweit ab. Der Bericht bietet den Wert (USD Millionen) für die oben genannten Segmente.
| Traditionelle Diagnosetests | Schnelle Influenza-Diagnosetests (RIDTs) |
| Direkte Fluoreszenzantikörper (DFA)-Tests | |
| Viruskultur | |
| Schnellzellkultur | |
| Molekulare Diagnosetests | Reverse-Transkriptase-PCR (RT-PCR) |
| Loop-vermittelte isotherme Amplifikation (LAMP) | |
| Nicking-Enzym-Amplifikationsreaktion (NEAR) | |
| CRISPR-basierte Assays | |
| Syndromische Multiplex-PCR-Panels |
| Krankenhäuser & Klinische Labore |
| Unabhängige Diagnoselabore |
| Point-of-Care-Einstellungen |
| Andere |
| Nordamerika | Vereinigte Staaten |
| Kanada | |
| Mexiko | |
| Europa | Deutschland |
| Vereinigtes Königreich | |
| Frankreich | |
| Italien | |
| Spanien | |
| Restliches Europa | |
| Asien-Pazifik | China |
| Japan | |
| Indien | |
| Südkorea | |
| Australien | |
| Restlicher Asien-Pazifik | |
| Naher Osten & Afrika | GCC |
| Südafrika | |
| Restlicher Naher Osten & Afrika | |
| Südamerika | Brasilien |
| Argentinien | |
| Restliches Südamerika |
| Nach Testtyp | Traditionelle Diagnosetests | Schnelle Influenza-Diagnosetests (RIDTs) |
| Direkte Fluoreszenzantikörper (DFA)-Tests | ||
| Viruskultur | ||
| Schnellzellkultur | ||
| Molekulare Diagnosetests | Reverse-Transkriptase-PCR (RT-PCR) | |
| Loop-vermittelte isotherme Amplifikation (LAMP) | ||
| Nicking-Enzym-Amplifikationsreaktion (NEAR) | ||
| CRISPR-basierte Assays | ||
| Syndromische Multiplex-PCR-Panels | ||
| Nach Endnutzer | Krankenhäuser & Klinische Labore | |
| Unabhängige Diagnoselabore | ||
| Point-of-Care-Einstellungen | ||
| Andere | ||
| Nach Geographie | Nordamerika | Vereinigte Staaten |
| Kanada | ||
| Mexiko | ||
| Europa | Deutschland | |
| Vereinigtes Königreich | ||
| Frankreich | ||
| Italien | ||
| Spanien | ||
| Restliches Europa | ||
| Asien-Pazifik | China | |
| Japan | ||
| Indien | ||
| Südkorea | ||
| Australien | ||
| Restlicher Asien-Pazifik | ||
| Naher Osten & Afrika | GCC | |
| Südafrika | ||
| Restlicher Naher Osten & Afrika | ||
| Südamerika | Brasilien | |
| Argentinien | ||
| Restliches Südamerika | ||
Wichtige im Bericht beantwortete Fragen
Wie hoch ist der aktuelle Wert des Influenza-Diagnostik-Marktes?
Die Influenza-Diagnostik-Marktgröße erreichte 1,82 Milliarden USD in 2025.
Wie schnell wird der Influenza-Diagnostik-Markt voraussichtlich wachsen?
Er wird voraussichtlich mit 5,8% CAGR von 2025 bis 2030 expandieren.
Welche Region hält den größten Anteil am globalen Influenza-Test-Umsatz?
Nordamerika führte mit 37,8% Marktanteil in 2024.
Warum gewinnen CRISPR-basierte Assays in Influenza-Tests an Zugkraft?
CRISPR-Plattformen kombinieren molekulare Genauigkeit mit schnellen, gerätearmen Arbeitsabläufen, die Point-of-Care-Bedürfnissen entsprechen.
Was hemmt breitere Adoption molekularer Plattformen in Schwellenmärkten?
Hohe Gerätkosten, laufende Reagenzienausgaben und spezialisierte Personalanforderungen begrenzen Aufnahme außerhalb gut finanzierter Gesundheitssysteme.
Wie transformieren KI-Tools die Influenza-Diagnostik?
KI-Pipelines beschleunigen Ergebnisinterpretation, erhöhen Sensitivität und automatisieren Qualitätsprüfungen, wodurch der Labordurchsatz während saisonaler Spitzen gesteigert wird.
Seite zuletzt aktualisiert am:



