Marktanalyse für Electronic Trial Master File (ETMF).
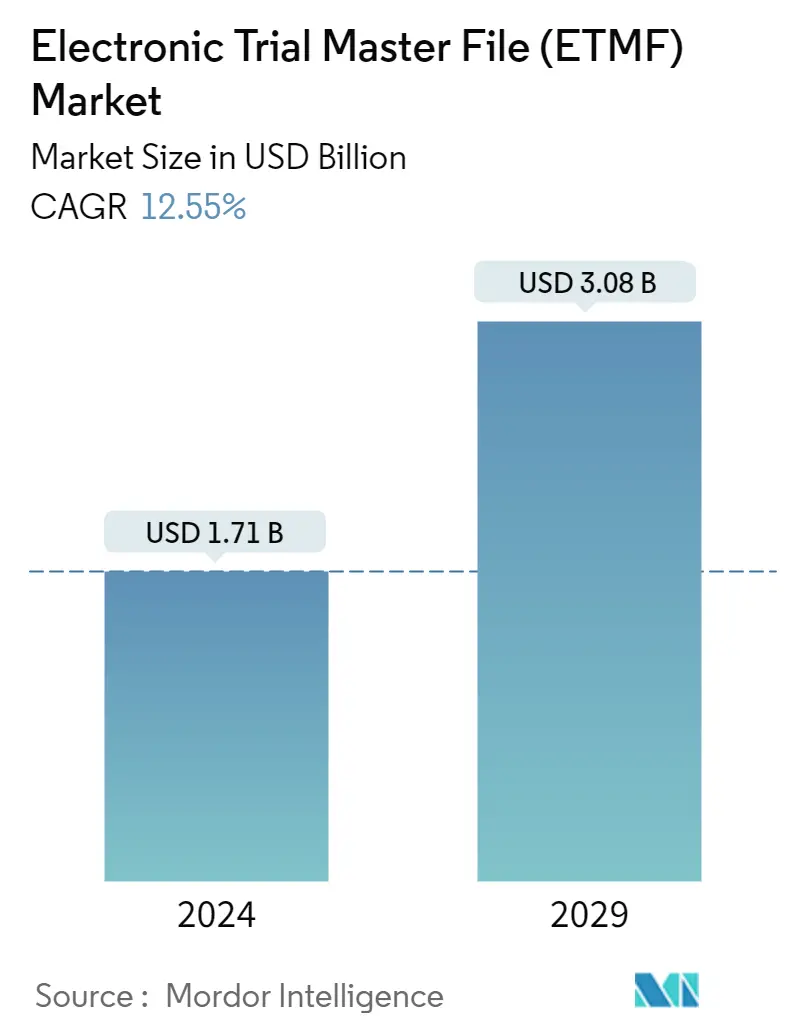
Die Größe des Marktes für elektronische Prozessstammdateien wird im Jahr 2024 auf 1,71 Milliarden US-Dollar geschätzt und soll bis 2029 3,08 Milliarden US-Dollar erreichen, was einem durchschnittlichen jährlichen Wachstum von 12,55 % im Prognosezeitraum (2024–2029) entspricht.
- Mit der COVID-19-Pandemie kam es weltweit zu einem sprunghaften Anstieg der Zahl klinischer Studien. Große Unternehmen konzentrierten sich auf die Entwicklung wirksamer Impfstoffe und Therapien zur Prävention und Behandlung der COVID-19-Krankheit. Den Daten von Clinicaltrials.gov aus dem Jahr 2022 zufolge waren bisher mehr als 8.283 Studien aus 150 Ländern auf Clinicaltrials.gov registriert. Die oben genannten Studien umfassten rund 777 Impfstoffstudien und 2.155 Arzneimittelstudien. Dies deutete auf den Anstieg der während der COVID-19-Pandemie generierten Daten zu klinischen Studien hin. Daher wurde die Nutzung der elektronischen Studienstammdatei verstärkt, um den Überblick über die während der Pandemie generierten klinischen Studiendaten zu behalten, was zu einem deutlichen Marktwachstum beitrug. Es wurde jedoch erwartet, dass Initiativen wichtiger Marktteilnehmer das Marktwachstum steigern würden.
- Beispielsweise gab Phlexglobal im April 2021 an, dass immer mehr Pharmaunternehmen, darunter fünf der weltweiten Top 10, die innovative TMF Quality Review-Lösung von Phlexglobal nutzten, um potenzielle regulatorische Risiken für Fusionen und Übernahmen zu identifizieren und zu mindern und die Inspektionsbereitschaft zu verbessern.
- Die elektronische Studienstammdatei ist eine neuartige Anwendung, die Software und Servertechnologie nutzt, um die Einrichtung, Sammlung, Speicherung, Nachverfolgung und Archivierung wesentlicher klinischer Studiendokumente zu unterstützen. Angesichts der zunehmenden Anzahl klinischer Studien auf der ganzen Welt ist es wichtig, klinische Daten sicher und in einer Form aufzubewahren, die leicht zugänglich und verständlich ist. Um mit der zunehmenden Zahl klinischer Studien zurechtzukommen, konzentrieren sich Unternehmen außerdem stärker auf die Bereitstellung fortschrittlicher und benutzerfreundlicher Software, die die Belastung durch riesige Datenmengen, die bei klinischen Studien anfallen, reduzieren kann. Darüber hinaus erlebt die Gesundheitsbranche einen Wandel im Hinblick auf die Digitalisierung in den Entwicklungs- und Industrieregionen, der die Einführung von Software wie einer elektronischen Studienstammdatei beschleunigt.
- Laut den von Clinicaltrials.gov veröffentlichten Daten für 2022 sind beispielsweise bisher rund 423.514 klinische Studien mit Standorten in allen 50 Bundesstaaten und 221 Ländern aufgeführt. Mit der zunehmenden Einführung der Informationstechnologie im Gesundheitswesen nimmt die Nutzung von ETMF zu. Die Verwendung einer elektronischen Teststammdatei bietet mehrere Vorteile, da sie nur einmal installiert und mehrmals wiederverwendet werden muss. Während die klinische Studie voranschreitet und sich ausdehnt, lässt sich außerdem die Last der riesigen Datenmengen mit der elektronischen Studienstammdateianwendung problemlos bewältigen.
- Es wird erwartet, dass Initiativen wichtiger Organisationen ein günstiges Umfeld für das Wachstum solcher Technologien schaffen. Beispielsweise hat die Food and Drug Administration (FDA oder die Agentur) am 15. März 2023 einen Leitlinienentwurf mit dem Titel Electronic Systems, Electronic Records, and Electronic Signatures in Clinical Investigations Questions and Answers (Leitlinienentwurf 2023) herausgegeben. Die FDA hat diese Fragen und Antworten in fünf Abschnitte unterteilt (A) elektronische Aufzeichnungen, (B) elektronische Systeme, die Sponsoren oder anderen regulierten Unternehmen gehören oder von diesen kontrolliert werden, (C) Anbieter und Dienste der Informationstechnologie, (D) digitale Gesundheitstechnologien und (E) elektronische Signaturen.
- Die FDA verfolgt weiterhin eine enge und praktische Auslegung von Teil 11, hat jedoch ihren risikobasierten Validierungsansatz durch zusätzliche Überlegungen und Empfehlungen erweitert. Daher wird erwartet, dass solche Richtlinien eine bessere Unterstützung für solche Plattformen bieten, was voraussichtlich das Marktwachstum im Prognosezeitraum steigern wird. Es wird jedoch erwartet, dass Budgetbeschränkungen das Marktwachstum behindern.
- Aufgrund der zunehmenden Verbreitung elektronischer Studienstammdateien (ETMF) aufgrund der zunehmenden Anzahl klinischer Studien weltweit und der zunehmenden Zahl von Forschungs- und Entwicklungsaktivitäten wird daher voraussichtlich die Nachfrage nach elektronischen Studienstammdateien (ETMF) im Laufe der Zeit zunehmen Prognosezeitraum. Es wird jedoch erwartet, dass Budgetbeschränkungen von Gesundheitsdienstleistern und Unternehmen das Wachstum des Marktes im Prognosezeitraum bremsen.
Markttrends für Electronic Trial Master File (ETMF).
Für das Segment der Pharma- und Biotechnologieunternehmen wird ein deutliches Wachstum erwartet
- Es wird erwartet, dass Pharma- und Biotechnologieunternehmen ein deutliches Marktwachstum verzeichnen werden, vor allem aufgrund der zunehmenden Investitionen in Forschungs- und Entwicklungsaktivitäten. Laut dem Bericht der India Brand Equity Foundation (IBEF) aus dem Jahr 2021 wurden im Jahr 2021 rund 1,206 Milliarden US-Dollar in die Pharmaindustrie investiert. Solch enorme Investitionen treiben die Zahl der durchgeführten klinischen Studien in die Höhe, was ein treibender Faktor ist für den untersuchten Markt.
- Darüber hinaus nimmt die Zahl der Studien zu, was das ETMF-System zur Verwaltung der Patienten- und Arzneimitteldaten erfordert. Nach Angaben der Europäischen Arzneimittel-Agentur wurden im Jahr 2021 in Europa 37.293 klinische Studien registriert. Daher wird erwartet, dass diese Faktoren die Nachfrage nach ETMF-Systemen in pharmazeutischen und biopharmazeutischen Unternehmen steigern werden.
- Darüber hinaus haben Eisai und Biogen laut dem von Biogen im Juli 2022 veröffentlichten Bericht Medikamente gegen die Alzheimer-Krankheit entwickelt und fordern eine beschleunigte Zulassung aufgrund ihrer Fähigkeit, toxische Plaques von einem Protein namens Amyloid zu entfernen. Ebenso sind in den Jahren 2022-2023 mehrere klinische Studien von verschiedenen Pharma- und Biotechnologieunternehmen geplant, was einen beflügelnden Faktor für den untersuchten Markt darstellt.
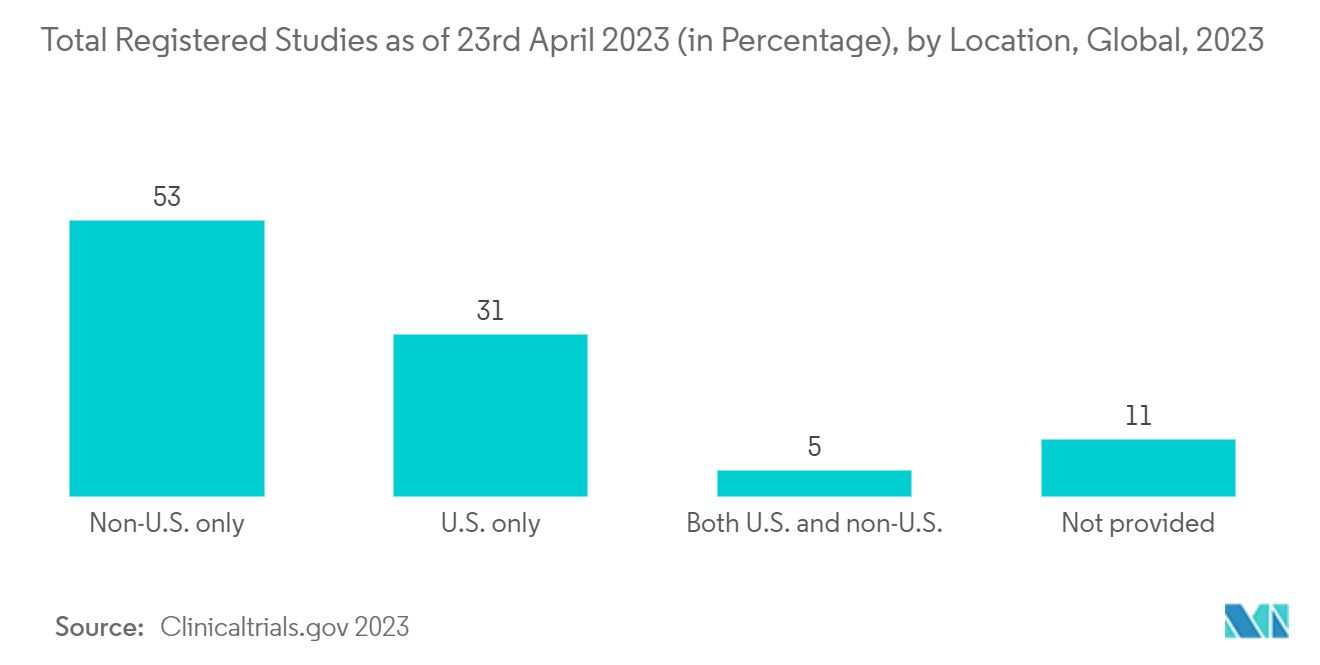
Es wird erwartet, dass Nordamerika einen erheblichen Anteil am Markt hält und dies auch im Prognosezeitraum tun wird
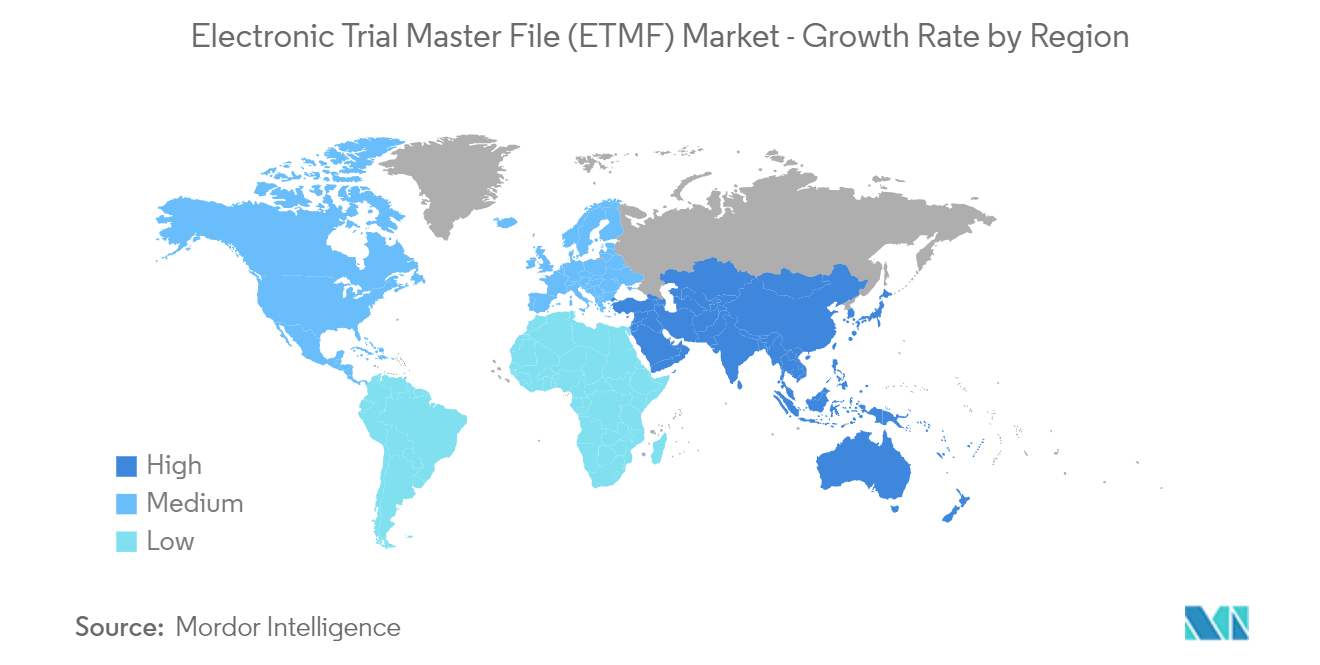
- Aufgrund der steigenden Investitionen und mehrerer Studien im Zusammenhang mit Forschung und Entwicklung wird erwartet, dass Nordamerika eine dominierende Region auf dem Electronic Trial Master File (ETMF)-Markt sein wird.
- Nach Angaben der Pharmaceutical Researchers and Manufacturers of America (PhRMA) hatten die Vereinigten Staaten im Jahr 2021 mit rund 58 % den höchsten Anteil an den FE-Ausgaben. Darüber hinaus beliefen sich die FE-Ausgaben biopharmazeutischer Unternehmen im Jahr 2021 auf rund 102,3 Milliarden US-Dollar Vereinigte Staaten, laut derselben Quelle.
- Darüber hinaus sind mit Stand 23. April 2023 rund 139.632 Studien in den Vereinigten Staaten registriert, diese Zahl wird bis Ende April 2023 ansteigen. Allein auf die Vereinigten Staaten entfallen 31 % der registrierten Studienorte. Dies weist darauf hin, dass im Land eine große Anzahl klinischer Studien stattfindet, was für den untersuchten Markt von Vorteil ist, da Bedarf an einem geeigneten Tool besteht, das Forschern dabei helfen kann, den Überblick über die Daten zu behalten und die Daten effektiv zu speichern.
- Darüber hinaus ist die Verbreitung von Informationstechnologie im Gesundheitswesen in den Vereinigten Staaten höher, was die Nachfrage nach Software erhöht, die die Arbeit mit riesigen Datenmengen, die jedes Jahr im Rahmen klinischer Studien generiert werden, erleichtern kann. Daher geht man davon aus, dass die Nachfrage nach ETMF-Software im Land steigen wird, da die Zahl der Versuche in den Vereinigten Staaten zunimmt.
- Aufgrund der oben genannten Faktoren wird daher davon ausgegangen, dass der untersuchte Markt einen hohen Marktanteil halten wird.
Branchenüberblick für Electronic Trial Master File (ETMF).
Der Markt für Electronic Trial Master Files (ETMF) ist mäßig wettbewerbsintensiv und mehrere auf dem Markt bekannte Unternehmen sind Veeva Systems, Aris Global LLC, Master Control, Inc., Clinevo Technology, Oracle Corporation, Phlexglobal, TransPerfect und Aurea Unter anderem Software, Labcorp (Covance, Inc.) und Sureclinical.
Marktführer im Bereich Electronic Trial Master File (ETMF).
Oracle Corporation
Clinevo Technologies
Master Control Inc
Veeva Systems
Aris Global LLC
- *Haftungsausschluss: Hauptakteure in keiner bestimmten Reihenfolge sortiert
Marktnachrichten für Electronic Trial Master File (ETMF).
- Im Februar 2023 unterzeichnete Vial, ein klinisches Forschungsunternehmen (CRO), eine Partnerschaftsvereinbarung mit Egnyte zur Integration der Life Sciences eTMF-Lösung (Electronic Trial Master File) in die Plattform von Vial. Nach Angaben des Unternehmens handelt es sich bei Egnyte eTMF um eine 21 CFR Part 11-konforme Plattform, die die Verarbeitungszeit für Dokumente und Daten verkürzt, die Compliance aufrechterhält und die Audit-Bereitschaft für Life-Science-Unternehmen verbessert.
- Im September 2022 führte Montrium seine von Experten geleiteten Trial Master File (TMF)-Dienste und seine neue TMF-Reifeschulung ein. Diese innovativen Angebote sind darauf ausgelegt, klinische Abläufe und TMF-Teams in jeder Phase der klinischen Entwicklung zu unterstützen.
Branchensegmentierung der Electronic Trial Master File (ETMF).
Die elektronische Studienstammdatei ist ein Verwaltungssystem, das eine strukturierte Möglichkeit zur Organisation, Speicherung und Verwaltung von Dokumenten, Bildern und anderen Inhalten im Zusammenhang mit klinischen Studien bietet.
Der Markt für elektronische Studienstammdateien ist nach Produkttyp (Software, Dienstleistungen), Endbenutzer (Pharma- und Biotechnologieunternehmen, Auftragsforschungsorganisationen, andere Endbenutzer) und Geografie (Nordamerika, Europa, Asien-Pazifik usw.) segmentiert Rest der Welt).
Der Bericht bietet den Wert (in USD) für die oben genannten Segmente.
| Dienstleistungen |
| Software |
| Pharma- und Biotechnologieunternehmen |
| Auftragsforschungsorganisationen |
| Andere Endbenutzer |
| Nordamerika | Vereinigte Staaten |
| Kanada | |
| Mexiko | |
| Europa | Deutschland |
| Großbritannien | |
| Frankreich | |
| Italien | |
| Spanien | |
| Rest von Europa | |
| Asien-Pazifik | China |
| Japan | |
| Indien | |
| Australien | |
| Südkorea | |
| Rest des asiatisch-pazifischen Raums | |
| Rest der Welt |
| Nach Produkttyp | Dienstleistungen | |
| Software | ||
| Vom Endbenutzer | Pharma- und Biotechnologieunternehmen | |
| Auftragsforschungsorganisationen | ||
| Andere Endbenutzer | ||
| Erdkunde | Nordamerika | Vereinigte Staaten |
| Kanada | ||
| Mexiko | ||
| Europa | Deutschland | |
| Großbritannien | ||
| Frankreich | ||
| Italien | ||
| Spanien | ||
| Rest von Europa | ||
| Asien-Pazifik | China | |
| Japan | ||
| Indien | ||
| Australien | ||
| Südkorea | ||
| Rest des asiatisch-pazifischen Raums | ||
| Rest der Welt | ||
Häufig gestellte Fragen zur Marktforschung im Bereich Electronic Trial Master File (ETMF).
Wie groß ist der Markt für elektronische Prozessstammdateien?
Die Größe des Marktes für elektronische Prozessstammdateien wird im Jahr 2024 voraussichtlich 1,71 Milliarden US-Dollar erreichen und bis 2029 mit einer jährlichen Wachstumsrate von 12,55 % auf 3,08 Milliarden US-Dollar wachsen.
Wie groß ist der Markt für elektronische Studienstammdateien derzeit?
Im Jahr 2024 wird die Größe des Marktes für elektronische Prozessstammdateien voraussichtlich 1,71 Milliarden US-Dollar erreichen.
Wer sind die Hauptakteure auf dem Markt für elektronische Studienstammdateien?
Oracle Corporation, Clinevo Technologies, Master Control Inc, Veeva Systems, Aris Global LLC sind die wichtigsten Unternehmen, die auf dem ETMF-Markt (Electronic Trial Master File) tätig sind.
Welches ist die am schnellsten wachsende Region im Markt für elektronische Prozessstammdateien?
Schätzungen zufolge wird der asiatisch-pazifische Raum im Prognosezeitraum (2024–2029) mit der höchsten CAGR wachsen.
Welche Region hat den größten Anteil am Markt für elektronische Studienstammdateien?
Im Jahr 2024 hat Nordamerika den größten Marktanteil am Markt für elektronische Prozessstammdateien.
Welche Jahre deckt dieser Markt für elektronische Prozessstammdateien ab und wie groß war der Markt im Jahr 2023?
Im Jahr 2023 wurde die Größe des Marktes für elektronische Prozessstammdateien auf 1,52 Milliarden US-Dollar geschätzt. Der Bericht deckt die historische Marktgröße des Marktes für elektronische Studienstammdateien für die Jahre 2019, 2020, 2021, 2022 und 2023 ab. Der Bericht prognostiziert auch die Marktgröße für elektronische Studienstammdateien für die Jahre 2024, 2025, 2026, 2027, 2028 und 2029.
Seite zuletzt aktualisiert am:
Globaler Electronic Trial Master File (ETMF)-Branchenbericht
Statistiken für den Marktanteil, die Größe und die Umsatzwachstumsrate der Electronic Trial Master File (ETMF) im Jahr 2024, erstellt von Mordor Intelligence™ Industry Reports. Die Analyse des Electronic Trial Master File (ETMF) umfasst eine Marktprognose für die Jahre 2024 bis 2029 und einen historischen Überblick. Holen Sie sich ein Beispiel dieser Branchenanalyse als kostenlosen PDF-Download.



