Globale Marktgröße und -anteil der Zelllinienentwicklung
Globale Marktanalyse für Zelllinienentwicklung von Mordor Intelligenz
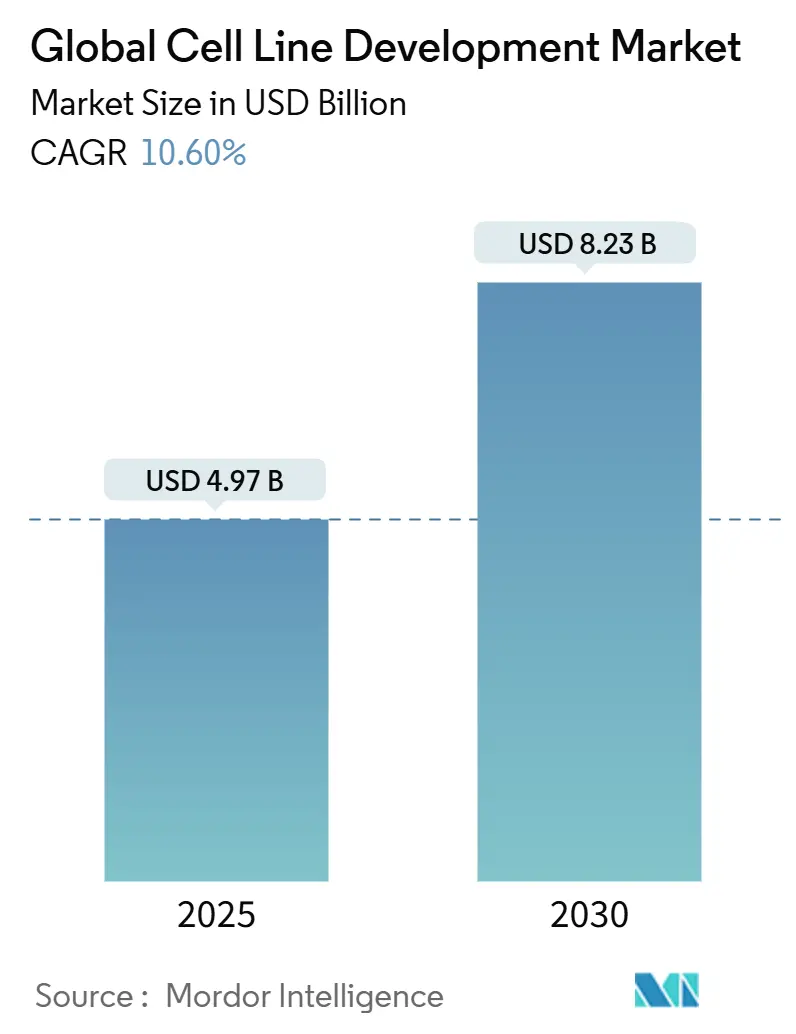
Der Markt für Zelllinienentwicklung erreichte USD 4,97 Milliarden im Jahr 2025 und wird voraussichtlich auf USD 8,23 Milliarden bis 2030 expandieren, was eine CAGR von 10,60% über den Zeitraum widerspiegelt. Die steigende Nachfrage nach Biologika, die mehr als 40% der Arzneimittelzulassungen 2024 ausmachten, ist der Anker dieses Wachstums, da komplexe Proteine, monoklonale Antikörper und Gentherapien alle hochentwickelte Zelllinien für die kommerzielle Produktion erfordern. Erhöhte Kapitalaufwendungen für kontinuierliche Bioprozessierung, eine beschleunigte Verlagerung zum Outsourcing und das Aufkommen von KI-gesteuerten Optimierungsplattformen haben bereits die Entwicklungszyklen von 6-9 Monaten auf 3-4 Monate verkürzt und geben den ersten Marktteilnehmern einen greifbaren Wettbewerbsvorteil. Regulatorische Reformen, die risikobasierte virale Sicherheitsbewertungen begünstigen, schaffen sowohl Einhaltung-Kosten als auch Qualitätsanreize, während geopolitische Spannungen regionale Produktionscluster fördern, die das Risiko von Abhängigkeiten von einzelnen Ländern reduzieren. Zusammengenommen verstärken diese strukturellen Kräfte die zentrale Rolle, die der Markt für Zelllinienentwicklung bei der Bereitstellung der nächsten Welle von Biologika spielen wird.
Wichtige Erkenntnisse des Berichts
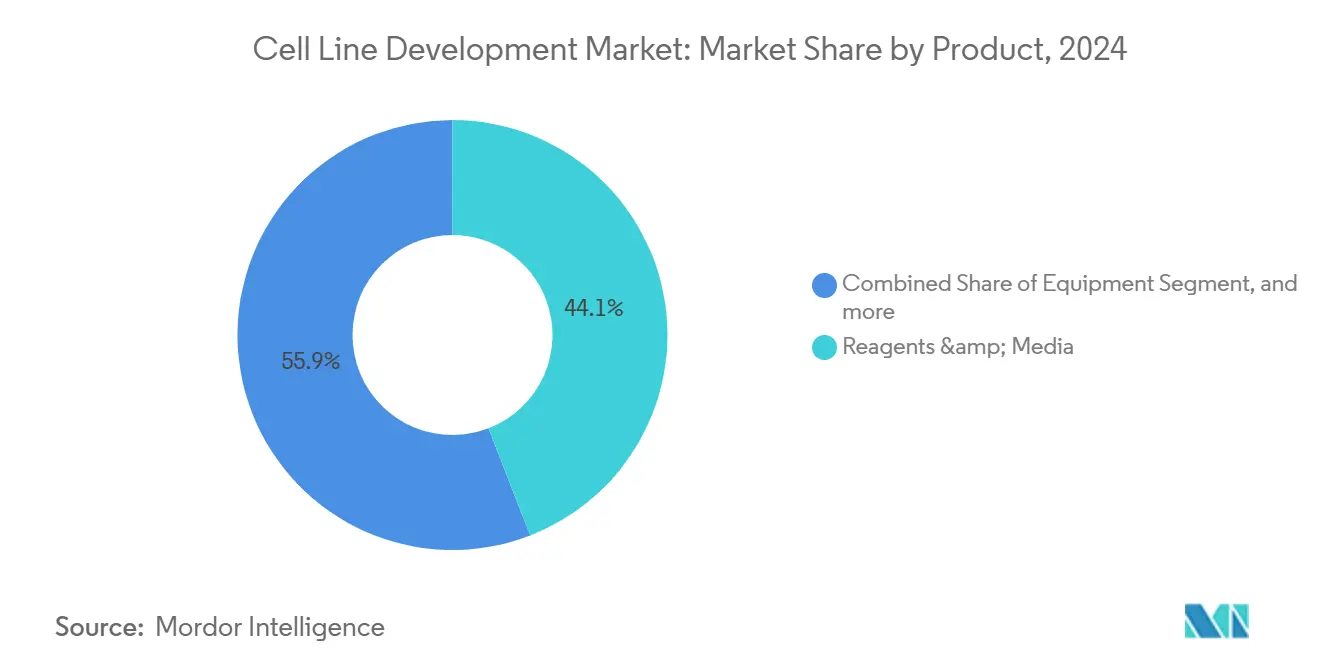
- Nach Produkt führten Reagenzien und Medien mit 44,12% Umsatzanteil In 2024, während Geräte voraussichtlich am schnellsten mit einer CAGR von 10,94% bis 2030 wachsen werden.
- Nach Quelle eroberten Säugetierplattformen 75,04% des Marktanteils für Zelllinienentwicklung In 2024, während Nicht-Säugetiersysteme eine CAGR von 11,35% über den Prognosezeitraum zeigen.
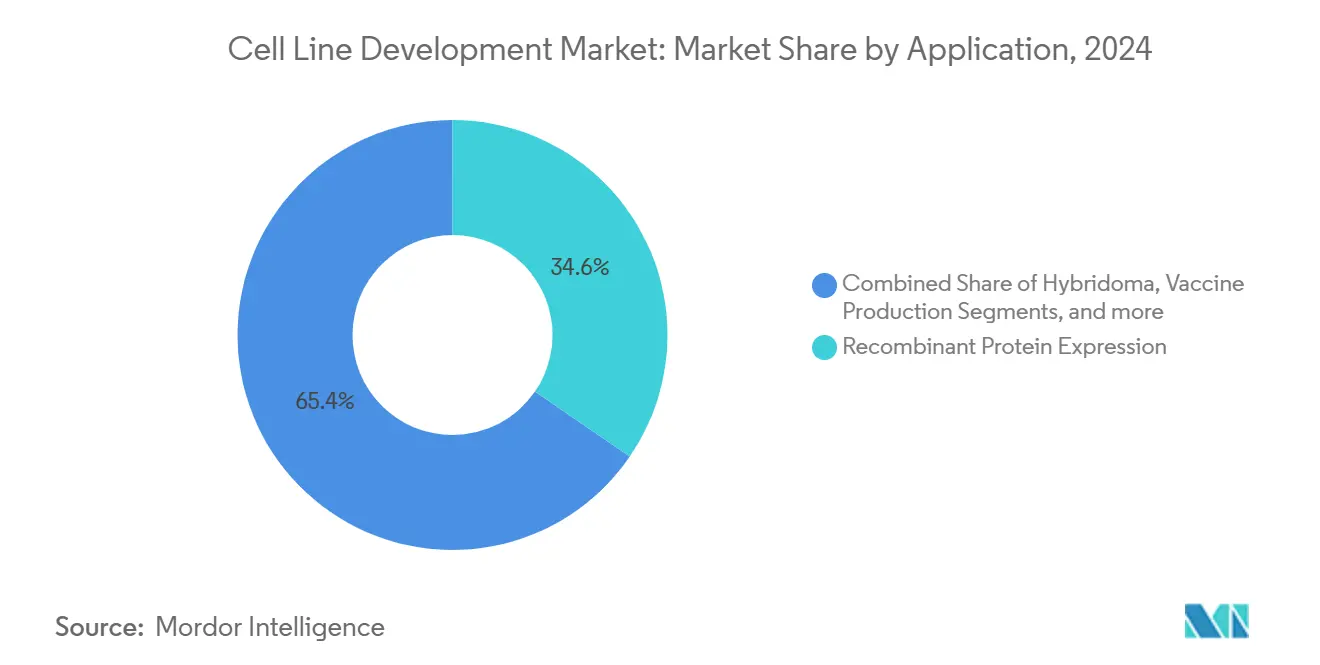
- Nach Anwendung hielt rekombinante Proteinexpression 34,56% Anteil der Marktgröße für Zelllinienentwicklung In 2024; Gen- und Zelltherapie-Herstellung expandiert mit einer CAGR von 11,14% bis 2030.
- Nach Endverbraucher kommandierten Biopharma- und Pharmaunternehmen 49,45% des Umsatzes In 2024, dennoch entwickeln sich CDMOs mit einer CAGR von 11,53% und werden die Lücke bis 2030 verringern.
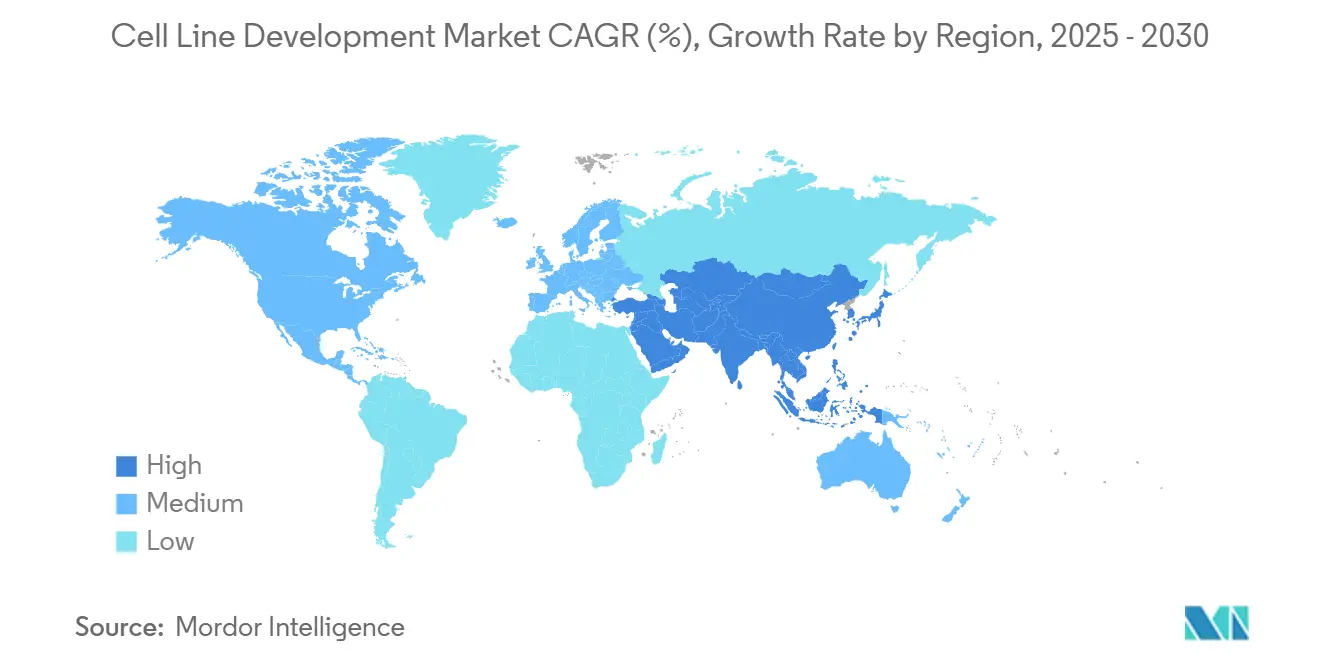
- Nach Geografie behielt Nordamerika 40,23% Anteil In 2024, während der Asien-Pazifik-Raum voraussichtlich die höchste regionale CAGR von 11,23% verzeichnen wird.
Globale Markttrends und Einblicke für Zelllinienentwicklung
Analyse der Treiber-Auswirkungen
| Treiber | (~) % Auswirkung auf CAGR-Prognose | Geografische Relevanz | Auswirkungs- zeitrahmen |
|---|---|---|---|
| Wachsende biopharmazeutische Nachfrage | +2.8% | Global, konzentriert In Nordamerika und EU | Mittelfristig (2-4 Jahre) |
| Expansion von monoklonalen Antikörper-Pipelines | +2.1% | Global, angeführt von Nordamerika, expandierend nach APAC | Langfristig (≥ 4 Jahre) |
| Investitionsausgaben- Rennen für kontinuierliche Bioprozessierung-Infrastruktur | +1.9% | Nordamerika und EU, aufkommend In APAC | Mittelfristig (2-4 Jahre) |
| KI-gesteuerte Zelllinien-Optimierungsplattformen | +1.4% | Global, frühe Einführung In Nordamerika und EU | Kurzfristig (≤ 2 Jahre) |
| Aufstieg regionaler Bio-CDMO-Cluster In MENA & ASEAN | +1.1% | MENA & ASEAN, mit Spillover-Effekten global | Langfristig (≥ 4 Jahre) |
| Anstieg der Biosimilar-Produktion nach Patent-Cliff | +0.9% | APAC Kern, Spillover zu MEA und Lateinamerika | Kurzfristig (≤ 2 Jahre) |
| Quelle: Mordor Intelligence | |||
Wachsende biopharmazeutische Nachfrage
Monoklonale Antikörper dominieren bereits biologische Pipelines, und ihr Wachstum In Autoimmun- und seltene Krankheitsindikationen hält den Druck auf die Zelllinienproduktivität aufrecht. Über 200 Antikörpertherapeutika sind zugelassen, mit fast 1.400 Kandidaten In aktiver Entwicklung, was Sponsoren dazu zwingt, robuste, hochproduktive Zelllinien früh In klinischen Programmen zu sichern. Der Markt für Zelllinienentwicklung fungiert daher als strategischer Engpass, der weitgehend die gesamten Projektzeitpläne und kommerzielle Rentabilität bestimmt. Steigende Volumina von bispezifischen Antikörpern und Antikörper-Wirkstoff-Konjugaten erfordern technisch entwickelte Zelllinien, die zu ausgewogener Kettenexpression fähig sind, was Prämie-Preise für spezialisierte Entwicklungsdienstleistungen antreibt. In allen wichtigen Geografien erhalten Große Moleküle nun bevorzugte Investitionen gegenüber kleinen Molekülen, was die langfristige Nachfrage nach ausgeklügelten Zellkultursystemen zementiert.
Expansion von monoklonalen Antikörper-Pipelines
Klinische Zulassungen von bispezifischen Antikörpern seit 2020 heben die Verschiebung zu Dual-Ziel-Formaten hervor, die die Komplexität der Zellentwicklungs-Workflows verdoppeln. Pharmazeutische Großunternehmen finanzieren weiterhin dedizierte Anlagen, wie AstraZenecas USD 1,5 Milliarden Singapur-Standort, um End-Zu-End-Antikörper-Wirkstoff-Konjugat-Produktionskapazitäten zu sichern. Da jedes neuartige Antikörperformat einzigartige Faltungs- und Glykosylierungsanforderungen mit sich bringt, bevorzugen Sponsoren zunehmend proprietäre Zellplattformen, die In langfristige Lieferverträge eingebunden werden können. Diese Dynamik intensiviert das Wettbewerbsrennen innerhalb des Marktes für Zelllinienentwicklung, insbesondere für Dienstleister, die schlüsselfertige Entwicklung plus nachgelagerte Analytik anbieten[1]AstraZeneca, "AstraZeneca Zu build end-Zu-end ADC Einrichtung In Singapur," astrazeneca.com.
CAPEX-Rennen für kontinuierliche Bioprozessierung-Infrastruktur
Investitionen von über USD 8 Milliarden bei Unternehmen wie Fujifilm Diosynth unterstreichen die Dynamik hin zu Perfusion und kontinuierlicher Chromatografie, die 2-3-fache Produktivitätssteigerungen liefern und gleichzeitig den Pufferverbrauch reduzieren. Anbieter von intensiven Prozessanalytik- und Hochdichte-Zellrückhaltungsgeräten erleben rapide Auftragsrückstände, und frühe Anwender berichten von 30-70% Kapitaleinsparungen In skalierten Anlagen. Zelllinien, die In kontinuierlichen Operationen verwendet werden, müssen die Produktivität über erweiterte Kulturdauern aufrechterhalten, was das Prämie auf genetische Stabilitätseigenschaften erhöht. Diese Anforderungen drängen Technologieanbieter zur Integration von Echtzeit-Datenanalytik, die metabolische Drift vorhersagt, wodurch die Verbindung des Marktes für Zelllinienentwicklung zu Industrie 4.0-Herstellungszielen verstärkt wird.
KI-gesteuerte Zelllinien-Optimierungsplattformen
Maschinelle Lernmodelle, die mehrere-Omics-Datensätze mit phänotypischen Ergebnissen korrelieren, können nun spezifische Genbearbeitungen und Mediumsformulierungen empfehlen, die höhere Titer In silico liefern. Frühe Anwender behaupten eine 40%ige Reduzierung der Laborexperimentierzeit und eine 20%ige Steigerung der Spitzenproduktivität. Große Biopharma-Unternehmen verfolgen Build-versus-Buy-Analysen, um zu bestimmen, ob sie externe Software lizenzieren oder proprietäre Modelle entwickeln sollen, während venture-kapitalfinanzierte Startups sich als datenreiche Servicepartner positionieren. Diese Plattformen verstärken das Wertversprechen des Marktes für Zelllinienentwicklung, indem sie Entwicklungszeitpläne komprimieren und kostspielige Sackgassen mildern.
Analyse der Hemmnisse-Auswirkungen
| Hemmnis | (~) % Auswirkung auf CAGR-Prognose | Geografische Relevanz | Auswirkungs- zeitrahmen |
|---|---|---|---|
| Strenge regulatorische Einhaltung | -1.8% | Global, am strengsten In Nordamerika und EU | Langfristig (≥ 4 Jahre) |
| Mangel an cGMP-konformen Rohstoff-Lieferketten | -1.5% | Global, akut In Schwellenmärkten | Kurzfristig (≤ 2 Jahre) |
| Langwierige Zelllinien-Stabilitätszeitpläne | -1.2% | Global, mit regionalen Variationen In Anforderungen | Mittelfristig (2-4 Jahre) |
| Geopolitische Exportkontrollrisiken für CHO/HEK-Zelllinien | -0.9% | uns-China Handelskorridore, Spillover global | Mittelfristig (2-4 Jahre) |
| Quelle: Mordor Intelligence | |||
Strenge regulatorische Compliance
Die aktualisierte Q5A(R2)-Leitlinie der FDA zur viralen Sicherheit erfordert erweiterte Charakterisierungsstudien und fügt bis zu einem Jahr zusätzlicher Tests für neue Zellsubstrate hinzu. Unternehmen ohne interne regulatorische Expertise müssen höhere Beratungsgebühren und mögliche Nacharbeiten absorbieren, wenn Einreichungen hinter sich entwickelnden Standards zurückbleiben. Abweichende regionale Erwartungen komplizieren die globale Markteinführungssequenzierung, da Europa oft zusätzliche Adventivagens-Screenings anfordert, die anderswo nicht verlangt werden. Diese Drücke erhöhen die Fixkosten des Betriebs im Markt für Zelllinienentwicklung und können kleinere Unternehmen zum Ausstieg oder zur Konsolidierung führen, wodurch die Verhandlungsmacht zu Großen, vertikal integrierten Anbietern verschoben wird[2]u.S. Lebensmittel Und Medikament Administration, "viral Sicherheit Evaluation von Biotechnologie Produkte abgeleitet From Zelle Lines," fda.gov.
Mangel an cGMP-konformen Rohstoff-Lieferketten
Rückgänge In uns-Rinderherden haben bereits die Verfügbarkeit von fötalem Kälberserum reduziert und zwingen viele Entwickler dazu, mehrere Lieferanten zu qualifizieren und Bestände zu erweitern. Lieferzeiten für Spezialmediumskomponenten erstrecken sich nun über mehrere Monate, was die Upstream-Prozessentwicklung verzögert und die Betriebskapitalanforderungen aufbläht. Einige Produzenten reagieren, indem sie zu chemisch definierten, tierursprungsfreien Formulierungen wechseln; diese Umstellung kann jedoch eine Re-Optimierung ganzer Zellkulturprozesse erfordern. Lieferkettenunsicherheit Dämpft daher ansonsten starke Wachstumsaussichten für den Markt für Zelllinienentwicklung In Regionen, wo die Logistik fragil bleibt[3]Corning Leben Wissenschaften, "Markt Alert An Serum liefern," corning.com.
Segmentanalyse
Nach Produkt: Reagenzien verankern Verbrauchsmaterial-Nachfrage
Reagenzien und Medien repräsentierten 44,12% des Umsatzes 2024, da jede Produktionscharge Große Volumina an Kulturmedium, Futter und Puffer verbraucht. Die prognostizierte CAGR des Segments von 10,94% übertrifft die der Investitionsgüter, weil jede neue Therapiezulassung wiederkehrende Verbrauchsmaterialbestellungen skaliert und vorhersagbare Nachfrage innerhalb des breiteren Marktes für Zelllinienentwicklung gewährleistet. Anbieter priorisieren chemisch definierte und serumfreie Formulierungen, die die Chargen-Konsistenz verbessern und gleichzeitig Kontaminationsrisiken reduzieren, und KI-gestützte Designtools optimieren Nährstoffmischungen zur Steigerung der Spitzentiter. Geräte, die Bioreaktoren und automatisierte Zellhandhabungssysteme umfassen, bleiben entscheidend, weil steigende Zelldichten präzise Prozesskontrolle erfordern, um Nährstoffmangel und Abfallakkumulation zu vermeiden. Nebendienstleistungen wie Zellbanking, analytische Tests und virale Freigabe-Studien runden eine wachsende Long-Tail-Kategorie ab, die von erhöhter regulatorischer Kontrolle profitiert.
Die Reagenzienkategorie profitiert weiter von abonnement-ähnlichen Kaufmustern, da Bioreaktoren kontinuierlich Futterkomponenten während erweiterten Perfusionsläufen ziehen. Spezialisierte Anbieter vermarkten nun modulare Medienkits, die auf Crisper-entwickelte Zelllinien zugeschnitten sind, die einzigartige metabolische Fingerabdrücke aufweisen. Da sich die Prozessintensivierung ausdehnt, wird die Nachfrage nach hochreinen Rohstoffen eskalieren, was Lieferanten ermutigt, Aminosäure- und Vitaminproduktion vertikal zu integrieren. Zusammengenommen konsolidieren diese Trends die wettbewerbliche Bedeutung von Verbrauchsmaterialien innerhalb des Marktes für Zelllinienentwicklung und straffen die Verbindungen zwischen Medieninnovation und der Gesamtanlagenleistung.
Notiz: Segmentanteile aller einzelnen Segmente verfügbar beim Berichtskauf
Nach Quelle: Säugetierplattformen dominieren kommerzielle Produktion
Säugetierlinien kontrollierten 75,04% des Marktanteils für Zelllinienentwicklung In 2024, und ihre CAGR von 11,35% unterstreicht die anhaltende Präferenz für menschenähnliche posttranslationale Modifikationen. Chinesische Hamster-Eierstockzellen bleiben der Goldstandard für monoklonale Antikörper, während Crisper-Knockouts, die wichtige Glykosylierungsgene löschen, homogenere Glykoformen mit reduzierter Immunogenität liefern. Humane embryonale Nierenzelllinien (HEK293), optimiert für Suspensionswachstum, stützen die meiste Adeno-assoziierte Viralvektorproduktion für Gentherapien und tragen nun bedeutsame Umsätze zur Marktgröße für Zelllinienentwicklung für virale Anwendungen bei. Nicht-Säugetiersysteme, einschließlich Hefe- und Insektenlinien, adressieren Nischenzym- und Impfstoffanwendungen, wo komplexe Glykosylierung unnötig ist.
Fortschritte beim Hochdurchsatz-Mikrofluidik-Screening ermöglichen die schnelle Isolierung von Spitze-produzierenden Säugetierklonen und verkürzen Wochen aus traditionellen Limiting-Dilution-Kampagnen. Neuartige genomische Instabilitätssensoren verfolgen chromosomale Aberrationen In Echtzeit und ermöglichen das frühe Aussortieren instabiler Klone. Bakterielle und Hefesysteme übertreffen immer noch bei einfachen Proteinprodukten, obwohl ihr Gesamtwachstum hinter Säugetierzuwächsen zurückbleibt. Diese Technologiemischung gewährleistet, dass der Markt für Zelllinienentwicklung eine vielfältige Toolbox aufrechterhält, die spezifische molekulare Anforderungen mit dem kostengünstigsten zellulären Chassis abgleichen kann.
Nach Anwendung: Gentherapie-Herstellung beschleunigt
Rekombinante Proteinexpression behielt 34,56% des Umsatzes 2024, da monoklonale Antikörper und Fusionsproteine weiterhin kommerzielle Pipelines dominieren. Dennoch wächst die Gen- und Zelltherapie-Herstellung mit einer CAGR von 11,14%, gestützt durch acht FDA-Zulassungen allein 2024, und ist bereit, größere Anteile des Marktes für Zelllinienentwicklung bis 2030 zu beanspruchen. Viralvektortiter haben sich bereits durch HEK293- und Sf9-basierte Suspensionsplattformen verdoppelt, während Automatisierung die Auto-T-Zellexpansion von 21 Tagen auf 14-17 Tage verkürzt. Hybridom-Anwendungen bleiben relevant für Entdeckungskampagnen, die Antikörperpipelines speisen, und Impfstoffentwickler erkunden Vero-abgeleitete Suspensionslinien, die Ertragsverbesserungen entsprechen, die In adhärenter Kultur erreicht wurden.
Wachsende klinische Nachfrage nach autologen Zelltherapien spornt auch Investitionen In geschlossene Herstellungshardware an, die Betreiberexposition reduziert. Diese Verschiebung zwingt Entwickler dazu, Zelllinienleistung mit Bioreaktorkonfiguration zu co-optimieren, was die integrierte Natur von Prozess- und Produktdesign In der Zelllinienentwicklungsbranche verstärkt. Über den Prognosehorizont erwarten Regulierungsbehörden jährlich 10-20 neue Gen- und Zelltherapiezulassungen, was den strategischen Wert spezialisierter vektorproduzierender Zellbanken und zugehöriger Analytik verstärkt.
Notiz: Segmentanteile aller einzelnen Segmente verfügbar beim Berichtskauf
Nach Endverbraucher: CDMOs erobern ausgelagertes Wachstum
Biopharma- und Pharma-Sponsoren machten 49,45% der Nachfrage 2024 aus, was interne Programme bei erstklassigen Innovatoren widerspiegelt. Dennoch verzeichnen CDMOs die schnellste CAGR von 11,53%, da Sponsoren Flexibilität inmitten ungewisser klinischer Ergebnisse und schwankender Kapazitätsanforderungen suchen. Samsung Biologika betreibt nun 784.000 L Kapazität, und Fujifilm Diosynths USD 8 Milliarden Expansionsplan demonstriert anhaltende Zuversicht In ausgelagertes Wachstum. Akademische und Forschungsinstitute tragen Entdeckungsphase-Zelllinien bei und arbeiten oft mit kommerziellen Einrichtungen zusammen, um Grundlagenforschung In klinische Kandidaten zu übersetzen. Startups und Diagnostikunternehmen bilden eine kleine, aber steigende Kundenschicht, da zellbasierte Tests an Traktion gewinnen.
Für CDMOs hängt die Differenzierung von Geschwindigkeit, bewährten regulatorischen Erfolgsbilanz und der Fähigkeit zur Integration digitaler Zwillinge ab, die Chargen-Ergebnisse vorhersagen. Sponsoren schätzen nahtlose Tech-überweisen-Pfade, die Validierungsausfallzeiten minimieren und regulatorische Dokumentation bewahren. Die Outsourcing-Welle strafft daher strategische Partnerschaften innerhalb des Marktes für Zelllinienentwicklung und drängt gleichzeitig Anbieter dazu, Serviceportfolios von Klonselektion bis zur kommerziellen Füllen-beenden zu erweitern.
Geografische Analyse
Nordamerika behielt einen Umsatzanteil von 40,23% In 2024, gestützt durch Großangelegte Investitionen wie Eli Lillys USD 9 Milliarden Indiana-Komplex und Novo Nordisks USD 4,1 Milliarden Norden Carolina-Erweiterung. Die Region profitiert von verwurzelter regulatorischer Expertise und robustem Venture Hauptstadt, sieht sich aber Rohstoffmangel und Exportkontrollunsicherheiten gegenüber, die die Versorgungskontinuität komplizieren. Kanadas OmniaBio baut ein KI-gestütztes Zelltherapie-Hub auf, das darauf ausgelegt ist, die Produktionskosten zu halbieren, was regionales Engagement für fortschrittliche Herstellung signalisiert. Mexiko zieht Nah-Shoring-Interesse an, da Unternehmen Nähe zu den Vereinigten Staaten suchen, ohne inländische Kostenstrukturen zu tragen. Zusammengenommen gewährleisten diese Dynamiken, dass der Markt für Zelllinienentwicklung In Nordamerika sowohl innovativ als auch kapitalintensiv bleibt.
Der Asien-Pazifik-Raum verzeichnet die schnellste CAGR von 11,23% bis 2030, angeheizt durch mehr als USD 3 Milliarden Biomanufacturing-Zusagen 2024 allein In Singapur. AstraZenecas USD 1,5 Milliarden ADC-Werk und BioNTechs erste Einrichtung außerhalb Deutschlands veranschaulichen den Aufstieg der Region als Prämie-Biomanufacturing-Destination. China und Indien behalten Kostenvorteile und Große interne Nachfrage, dennoch beschleunigt der vorgeschlagene uns BIOSECURE Act die Diversifizierung zu indischen CDMOs, Südkoreanischen Biologika-Clustern und ASEAN-Mitgliedsstaaten. Japan und Australien ergänzen das Ökosystem durch hochpräzise Analytik bzw. RNA-Therapeutikaplattformen. Diese Bewegungen verschieben kollektiv das Gravitätszentrum des Marktes für Zelllinienentwicklung zum Asien-Pazifik-Raum und schaffen multipolare Versorgungsnetzwerke, die geopolitische Risiken mindern.
Europa erlebt stetige, aber langsamere Expansion, unterstützt durch etablierte pharmazeutische Korridore In Deutschland, der Schweiz und Irland. Regierungsanreize für fortschrittliche Therapien und grenzüberschreitende regulatorische Harmonisierung bewahren Wettbewerbsfähigkeit, obwohl Energiekosten und Lohninflation die Margen relativ zu Asien verengen. Der Nahe Osten und Afrika verfolgen strategischen Eintritt, wobei Saudi-Arabien-Arabiens Nationale Biotechnologiestrategie globale Führung bis 2040 anstrebt und die VAE sich als regionaler Logistikknoten positionieren. Südamerika, angeführt von Brasilien, nutzt inländische Nachfrage und aufkommende Biosimilar-Gelegenheiten, jedoch begrenzt limitierte Venture-Finanzierung den schnellen Kapazitätsaufbau. Insgesamt entsteht ein ausgeglichener globaler Fußabdruck, In dem der Markt für Zelllinienentwicklung auf vielfältige Herstellungs-Hubs angewiesen ist, um lokale Nachfrage zu decken und Lieferketten zu de-risken.
Wettbewerbslandschaft
Wettbewerbslandschaft
Der Markt für Zelllinienentwicklung bleibt mäßig fragmentiert, weil kein einzelner Anbieter einen überdimensionierten Umsatzanteil kontrolliert. Thermo Fisher Scientific, Sartorius und Danaher verankern integrierte Portfolios, die von Medien bis zu analytischen Instrumenten reichen, dennoch disrupted aufkommende KI-zentrierte Unternehmen bei Prozessgeschwindigkeit und Kostenmetriken. Partnerschaften definieren Wettbewerbsgrenzen, da Bristol Myers Squibb sich mit Cellares für automatisierte Zelltherapieproduktion verbündet, während Scorpius Holdings Celltheons Transposase-basierte Plattform integriert, um die Generierung stabiler Zelllinien zu verkürzen. Technologierennen fokussieren auf Produktivitätssteigerungen, wobei Enduro Genetik 30% Ertragsverbesserungen durch Verknüpfung essentieller Gen mit Zielexpression berichtet, wodurch Zellwachstum mit Produktoutput ausgerichtet wird.
Regulatorische Expertise dient als wichtiger Differenziator, insbesondere unter den überarbeiteten FDA-Leitlinien zur viralen Sicherheit, die umfassende Adventivagens-Tests betonen. Unternehmen mit validierten Qualität-by-Design-Workflows können Prämie-Preise kommandieren und langfristige Lieferverträge sichern. Geopolitische Disruption fungiert sowohl als Bedrohung als auch als Gelegenheit: das vorgeschlagene BIOSECURE-Gesetz könnte WuXi Biologika' Zugang zu uns-Kunden beschränken und Verträge zu indischen und Südostasiatischen Anbietern lenken. Kontinuierliche Bioprozessierungs-Kompetenzen schaffen auch Schichtung; Unternehmen, die Perfusions-Bioreaktoren und Inline-Analytik integrieren, bieten überlegene Kosten pro Gramm und gewinnen Ausschreibungen für hochvolumige Antikörper-Projekte.
Kleinere Akteure spezialisieren sich oft auf Nischenmodalitäten wie Lentiviral-Vektorherstellung oder Crisper-bereite Suspensions-HEK293-Linien, die bestehende Patent-Dickichte umgehen. Diese Nischen, obwohl individuell klein, stützen kollektiv eine lebhafte Innovationsschicht, die proprietäre Zellbanken und Prozess-Know-how an größere CDMOs oder direkt an Sponsoren liefert. Da sich Biologika-Pipelines In mehrere-Spezifika und autologe Therapien diversifizieren, wird die Wettbewerbslandschaft des Marktes für Zelllinienentwicklung weiterhin agile Akteure belohnen, die schnell über Molekülklassen schwenken können, während sie starke Einhaltung-Aufzeichnungen beibehalten.
Globale Branchenführer der Zelllinienentwicklung
-
Promega Corporation
-
Danaher Corporation
-
Sartorius AG
-
Thermo Fisher Scientific
-
Merck KGaA
- *Haftungsausschluss: Hauptakteure in keiner bestimmten Reihenfolge sortiert
Jüngste Branchenentwicklungen
- Januar 2025: BioCina und NovaCina fusionierten, um ein globales Kraftzentrum In der biopharmazeutischen Herstellung zu etablieren, das Dienstleistungen von der Zelllinienentwicklung bis zur kommerziellen Substanzproduktion unter dem Namen BioCina integriert.
- Mai 2025: AstraZeneca erwarb das Zelltherapie-Startup EsoBiotec für USD 425 Millionen im Voraus und erweiterte seine Fähigkeiten In der Zelltherapieentwicklung.
- Oktober 2024: Matica Biotechnologie schloss sich mit KaliVir Immunotherapeutics zusammen, um die Entwicklung onkolytischer Viraltherapien mit MatiMax-Zelllinien zu verbessern.
- September 2024: Hovione und iBET gründeten ViSync Technologien, um Arzneimittelabgabe-Herausforderungen für komplexe Zell- und Gentherapien anzugehen.
Globaler Berichtsumfang für den Markt der Zelllinienentwicklung
Entsprechend dem Umfang dieses Berichts umfasst der Markt für Zelllinienentwicklung die Arten von Geräten, die im Prozess verwendet wurden, zusammen mit der Quelle, aus der die Zelle extrahiert wird. Weiterhin umfasst der untersuchte Markt verschiedene Arten von Zelllinien und deren Endverbraucher. Der Markt für Zelllinienentwicklung ist segmentiert nach Produkt (Reagenzien und Medien, Geräte, Fertigzellen und andere Produkte), Quelle (Säugetierzelllinien, Nicht-Säugetierzelllinien), Anwendung (Rekombinante Proteinexpression, Hybridom-Technologie, Impfstoffproduktion, Arzneimittelentdeckung, andere Anwendungen), Endverbraucher (Biotechnologie- und Pharmaunternehmen, Akademische und Forschungsinstitute, andere Endverbraucher) und Geografie (Nordamerika, Europa, Asien-Pazifik, Naher Osten & Afrika und Südamerika). Der Marktbericht deckt auch die geschätzten Marktgrößen und Trends für 17 verschiedene Länder In wichtigen Regionen weltweit ab. Der Bericht bietet den Wert (In USD Millionen) für die oben genannten Segmente.
| Reagenzien & Medien |
| Geräte |
| Andere Produkte |
| Säugetierzelllinien |
| Nicht-Säugetierzelllinien |
| Rekombinante Proteinexpression |
| Hybridom-Technologie |
| Impfstoffproduktion |
| Arzneimittelentdeckung & -screening |
| Gen- & Zelltherapie-Herstellung |
| Andere Anwendungen |
| Biopharma- & Pharmaunternehmen |
| Auftragsforschungs- & Herstellungsorganisationen (CDMOs) |
| Akademische & Forschungsinstitute |
| Andere Endverbraucher |
| Nordamerika | Vereinigte Staaten |
| Kanada | |
| Mexiko | |
| Europa | Deutschland |
| Vereinigtes Königreich | |
| Frankreich | |
| Italien | |
| Spanien | |
| Restliches Europa | |
| Asien-Pazifik | China |
| Japan | |
| Indien | |
| Südkorea | |
| Australien | |
| Restlicher Asien-Pazifik-Raum | |
| Naher Osten und Afrika | GCC |
| Südafrika | |
| Restlicher Naher Osten & Afrika | |
| Südamerika | Brasilien |
| Argentinien | |
| Restliches Südamerika |
| Nach Produkt | Reagenzien & Medien | |
| Geräte | ||
| Andere Produkte | ||
| Nach Quelle | Säugetierzelllinien | |
| Nicht-Säugetierzelllinien | ||
| Nach Anwendung | Rekombinante Proteinexpression | |
| Hybridom-Technologie | ||
| Impfstoffproduktion | ||
| Arzneimittelentdeckung & -screening | ||
| Gen- & Zelltherapie-Herstellung | ||
| Andere Anwendungen | ||
| Nach Endverbraucher | Biopharma- & Pharmaunternehmen | |
| Auftragsforschungs- & Herstellungsorganisationen (CDMOs) | ||
| Akademische & Forschungsinstitute | ||
| Andere Endverbraucher | ||
| Geografie | Nordamerika | Vereinigte Staaten |
| Kanada | ||
| Mexiko | ||
| Europa | Deutschland | |
| Vereinigtes Königreich | ||
| Frankreich | ||
| Italien | ||
| Spanien | ||
| Restliches Europa | ||
| Asien-Pazifik | China | |
| Japan | ||
| Indien | ||
| Südkorea | ||
| Australien | ||
| Restlicher Asien-Pazifik-Raum | ||
| Naher Osten und Afrika | GCC | |
| Südafrika | ||
| Restlicher Naher Osten & Afrika | ||
| Südamerika | Brasilien | |
| Argentinien | ||
| Restliches Südamerika | ||
Wichtige im Bericht beantwortete Fragen
Welcher prognostizierte Wert wird für den Markt für Zelllinienentwicklung bis 2030 erwartet?
Der Markt wird voraussichtlich USD 8,23 Milliarden bis 2030 erreichen und mit einer CAGR von 10,60% wachsen.
Welches Produktsegment hält heute den größten Anteil?
Reagenzien und Medien führen mit 44,12% Umsatzanteil, weil Verbrauchsmaterialien wiederkehrende Nachfrage In Zellkulturoperationen antreiben.
Warum werden Säugetierzelllinien für die Biologika-Herstellung bevorzugt?
Sie bieten menschenähnliche posttranslationale Modifikationen, die für die Sicherheit und Wirksamkeit komplexer Proteine wesentlich sind.
Wie wird das vorgeschlagene uns BIOSECURE-Gesetz den Markt beeinflussen?
Falls erlassen, könnte es Kollaborationen mit bestimmten chinesischen Lieferanten beschränken und Outsourcing nach Indien und Südostasien umleiten.
Welche Rolle spielen KI-gesteuerte Plattformen In der Zelllinienentwicklung?
Sie reduzieren Laborexperimentierung und verbessern die Produktivität, indem sie optimale Genbearbeitungen und Mediumsformulierungen aus mehrere-Omics-Daten vorhersagen.
Warum wachsen CDMOs schneller als interne Entwicklungsteams?
Outsourcing bietet Sponsoren Flexibilität, fortschrittliche Technologien und geringeres Startkapital, was eine CAGR von 11,53% für CDMOs bis 2030 antreibt.
Seite zuletzt aktualisiert am:



