Tamanho e Participação do Mercado Global de Biossimilares
Análise do Mercado Global de Biossimilares pela Mordor Intelligence
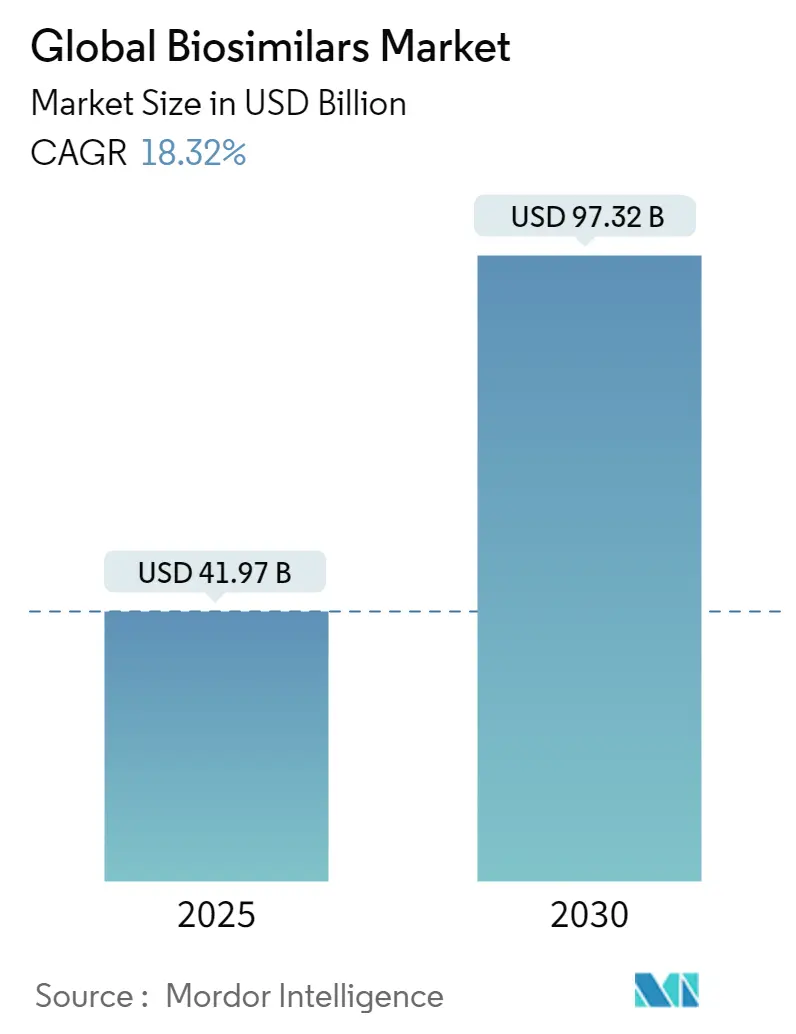
O tamanho do mercado de biossimilares está avaliado em USD 41,97 bilhões em 2025 e previsto para alcançar USD 97,32 bilhões até 2030, expandindo a uma TCAC de 18,32%. Esta curva de crescimento acentuada reflete a passagem da indústria de biossimilares de programas piloto cautelosos para uso clínico rotineiro, e sinaliza que os pagadores veem os biológicos de seguimento como uma alavanca estrutural para contenção de custos de longo prazo. Uma nova inferência que emerge dos números atuais é que o gasto global em biológicos de referência provavelmente não se estabilizará mesmo com a aceleração dos biossimilares, porque muitas novas moléculas originadoras estão simultaneamente entrando no mercado. A participação de 37% do mercado de biossimilares na Europa destaca como um marco regulatório precoce e claro pode se traduzir em escala comercial, mas também ilustra que posições de liderança não são imutáveis-Ásia-Pacífico agora registra a maior TCAC regional de 24%. Esta mudança regional implica que decisões da cadeia de suprimentos tomadas em Seul, Xangai e Hyderabad irão moldar cada vez mais os pontos de preço globais.
A perspectiva de cinco anos estabelecida antecipa que mais de USD 170 bilhões em receitas de biológicos perderão exclusividade até 2030, ampliando o conjunto de receitas acessível aos participantes de biossimilares. Esse único ponto de dados significa que o tamanho do mercado de biossimilares pode crescer mais rapidamente do que até mesmo a alta TCAC sugere, à medida que as políticas de substituição orientadas pelos pagadores se intensificam. Uma segunda inferência é que, embora os anticorpos monoclonais detenham uma participação de 48%, sua dominância relativa pode declinar porque heparinas de baixo peso molecular e proteínas de fusão inovadoras estão registrando curvas de crescimento mais acentuadas. Além disso, revisões recentes de políticas da Administração de Alimentos e Medicamentos dos EUA (FDA) que simplificam designações de intercambialidade provavelmente comprimirão cronogramas de lançamento, inclinando a vantagem competitiva para empresas com capacidade de fabricação em escala.
Principais Conclusões do Relatório
- O mercado de biossimilares está previsto para quase dobrar de USD 41,97 bilhões em 2025 para USD 97,32 bilhões até 2030, avançando a uma TCAC de 18,32%.
- A Europa mantém a maior participação regional com 37%, enquanto a Ásia-Pacífico registra o crescimento mais rápido com uma TCAC de 24% até 2030.
- Anticorpos monoclonais dominam a receita da classe de produtos com uma participação de 48% em 2024; heparinas de baixo peso molecular representam a classe de crescimento mais rápido a uma TCAC de 21%.
- Aplicações de oncologia lideram com 55% da receita de 2024, enquanto indicações autoimunes e inflamatórias crônicas crescem mais rapidamente a uma TCAC de 23%.
- Organizações de desenvolvimento e fabricação por contrato estão no caminho para controlar mais de 54% da capacidade global de biológicos até 2028, remodelando estratégias de fazer ou comprar.
Tendências e Insights do Mercado Global de Biossimilares
Análise de Impacto dos Impulsionadores
| Impulsionador | (~) % de Impacto na TCAC | Previsão de Relevância Geográfica | Cronograma de Impacto |
|---|---|---|---|
| Expiração iminente de patentes de múltiplos biológicos blockbuster | +3.8 % | Global | Prazo curto (≤ 2 anos) |
| Prevalência crescente de doenças crônicas e autoimunes | +2.9 % | América do Norte, Europa, Ásia-Pacífico | Prazo longo (≥ 4 anos) |
| Mandatos globais de contenção de custos e aquisições baseadas em licitações | +2.5 % | Europa, América Latina, MENA | Prazo médio (2-4 anos) |
| Crescente confiança de médicos e pacientes (evidência do mundo real) | +1.7 % | Global | Prazo médio (2-4 anos) |
| Investimento crescente de capital e expansões de capacidade CMO/CDMO | +1.4 % | Ásia-Pacífico, América do Norte | Prazo médio (2-4 anos) |
| Demanda crescente devido à eficácia de custos | +1.2 % | Global | Prazo longo (≥ 4 anos) |
| Fonte: Mordor Intelligence | |||
Expiração Iminente de Patentes de Múltiplos Biológicos Blockbuster
A expansão do tamanho do mercado está sendo impulsionada por uma onda sem precedentes de expirações de patentes que desbloqueará um estimado de USD 400 bilhões em vendas de produtos de referência entre 2029 e 2034. Como 25 biológicos de alto valor perdem exclusividade somente em 2025, desenvolvedores estão correndo para garantir slots de desenvolvimento e slots de fabricação simultaneamente. A inferência aqui é que pipelines de desenvolvimento estão agora tão congestionados que a capacidade de teste analítico, não financiamento, está emergindo como o fator limitante para alguns programas. Empresas como a Sandoz já divulgaram pipelines de 28 moléculas, demonstrando a escala da oportunidade [1]John Doe, "Novartis Expands Biosimilar Pipeline," Novartis, novartis.com. Anticorpos monoclonais focados em oncologia são os mais expostos, implicando preços médios de venda mais baixos para medicamentos blockbuster de câncer dentro do período de previsão. Esta disrupção reduzirá custos de tratamento e ampliará acesso, mas também aumenta a intensidade competitiva em áreas terapêuticas que anteriormente apresentavam apenas dois ou três fornecedores.
Prevalência Crescente de Doenças Crônicas e Autoimunes
Doenças crônicas e autoimunes estão aumentando mundialmente, e medicamentos especializados já representam mais da metade do gasto com prescrições nos EUA. Consequentemente, biossimilares direcionados a essas condições representam o grupo de indicações de crescimento mais rápido, registrando uma TCAC de 23% de 2025-2030. A inferência dos dados de prevalência crescente é que orçamentos de pagadores ficarão sob pressão crescente mesmo se biossimilares alcançarem ganhos de participação de mercado de dois dígitos, porque números absolutos de pacientes estão aumentando em paralelo. Oncologia permanece o maior conjunto de receitas hoje, mas prescrições autoimunes estão estreitando essa lacuna à medida que taxas de diagnóstico sobem. Evidências do mundo real de programas no Brasil mostram economias de custos superiores a 50% quando pacientes estáveis são trocados, sugerindo que resultados similares podem surgir em outros mercados emergentes. Migração constante de pacientes para terapias de manutenção de longo prazo aumenta a atratividade comercial de biossimilares de doenças crônicas e incentiva investimento em formulações subcutâneas.
Confiança Crescente de Médicos e Pacientes Impulsionada por Evidências do Mundo Real
Dados cumulativos de exposição de pacientes-quase 700 milhões de dias de terapia globalmente-dissiparam preocupações iniciais sobre a segurança de trocar para biossimilares. A orientação de junho de 2024 da FDA removeu a exigência rotineira de estudos de troca separados, efetivamente reduzindo custos de desenvolvimento e acelerando tempo até o mercado [2]Jane Smith, "Real-World Evidence Reinforces Biosimilar Safety," AJMC, ajmc.com. Uma inferência imediata é que empresas menores agora podem competir pelo status de primeira submissão porque a barreira financeira foi reduzida. O conforto dos médicos está claramente melhorando; biossimilares de adalimumabe capturaram 22% da participação do mercado dos EUA em nove meses de lançamento, um ritmo que teria sido implausível uma década antes. Importante, a confiança crescente se estende aos pagadores, que por sua vez fortalece o posicionamento de formulário para biossimilares. Como oncologia lidera com taxas de penetração de biossimilares acima de 80% em algumas indicações, prescritores estão começando a extrapolar experiências positivas para outras áreas terapêuticas.
Investimento de Capital Crescente, Alianças Estratégicas e Expansões de Capacidade CMO/CDMO
Organizações de fabricação por contrato (CMOs) e desenvolvedores híbridos estão previstos para controlar mais de 54% da capacidade global de biológicos até 2028. A Samsung Biologics sozinha está investindo USD 1,46 bilhão em capacidade adicional sul-coreana, enquanto a Fujifilm Diosynth está adicionando USD 3,2 bilhões em valor de instalações na Dinamarca e Carolina do Norte. A inferência que segue é que a diversificação geográfica de pegadas de fabricação desriscarizará cadeias de suprimentos e pode suavizar a volatilidade de preços ligada à escassez localizada. Alianças de grande escala, como as colaborações da Alvotech com Dr. Reddy's e Teva, ilustram como empresas estão reunindo recursos para acelerar cronogramas de lançamento. Essas parcerias frequentemente combinam know-how de acesso ao mercado ocidental com vantagens de custos asiáticos, remodelando limites competitivos. O aumento em estruturas de acordos híbridos-licenciamento mais fabricação conjunta-sinaliza que modelos de compartilhamento de PI estão se tornando mais normalizados na indústria de biossimilares.
Análise de Impacto das Restrições
| Restrição | (~) % de Impacto na TCAC | Previsão de Relevância Geográfica | Cronograma de Impacto |
|---|---|---|---|
| Complexidade intrínseca de fabricação e analítica | −2.3 % | Global | Prazo longo (≥ 4 anos) |
| Ceticismo sobre intercambialidade e substituição | −1.5 % | MENA, partes da Ásia e Europa Oriental | Prazo curto (≤ 2 anos) |
| Táticas defensivas do originador (litígio, barreiras de desconto) | −1.8 % | Estados Unidos | Prazo médio (2-4 anos) |
| Erosão severa de preços e margens estreitas | −2.1 % | Europa, Canadá | Prazo longo (≥ 4 anos) |
| Fonte: Mordor Intelligence | |||
Complexidade Intrínseca de Fabricação e Analítica
Desenvolver um biossimilar ainda custa USD 100-300 milhões e leva até sete a oito anos porque cada molécula deve passar por mais de 40 testes analíticos ortogonais. Uma inferência desses números é que racionamento de capital direcionará desenvolvedores menores para nichos estreitos e de alto valor em vez de portfólios amplos. Cultura de células mamárias, particularmente linhagens de Ovário de Hamster Chinês (CHO), permanece como o cavalo de batalha da produção por causa de seu perfil de glicosilação semelhante ao humano. A complexidade aumenta ainda mais quando desenvolvedores visam conjugados anticorpo-medicamento ou proteínas de fusão, ambos começando a aparecer em divulgações de pipeline. Desafios analíticos, incluindo perfil de glicanos e análise de variantes de carga, exigem instrumentação cara, empurrando muitas empresas a terceirizar para CDMOs especializados. Altas taxas de falha-pairando em torno de 50% para programas de biossimilares em estágio tardio-sinalizam que expertise, em vez de capital sozinho, determina probabilidades de sucesso.
Ceticismo Contínuo sobre Intercambialidade e Substituição em Certos Sistemas de Saúde
Apesar do progresso regulatório, ceticismo persiste em regiões com legislação limitada de biossimilares. Pesquisas em partes do Oriente Médio e Norte da África revelam que aproximadamente um terço dos médicos permanece desconfortável com substituição automática. A inferência aqui é que iniciativas educacionais, em vez de dados clínicos adicionais, poderiam desbloquear demanda significativa em mercados hesitantes. A designação da FDA do Simlandi (adalimumab-ryvk) como o primeiro biossimilar intercambiável de alta concentração e livre de citrato alivia algumas preocupações dos EUA, mas inércia persiste entre pacientes que têm estado estáveis em produtos de referência. Hesitação é mais evidente em biológicos de múltiplas indicações onde regimes de dosagem diferem entre doenças. Ao longo do tempo, mandatos de pagadores e evidências de economias do mundo real provavelmente corroerão resistência restante, mas fabricantes devem considerar curvas de adoção estendidas no planejamento de lançamentos.
Análise de Segmentos
Classe de Produto: Anticorpos Monoclonais Lideram Transformação do Mercado
O tamanho do mercado de biossimilares para anticorpos monoclonais está em 48% da receita total em 2024, e enquanto sua TCAC agregada modera para meados da adolescência, vendas absolutas continuam a subir. Uma inferência é que liderança de participação mascara fragmentação subjacente, pois dezenas de alvos mAb agora dividem o foco do fabricante. Heparinas de baixo peso molecular estão crescendo a 21% TCAC, sinalizando que anticoagulação pode se tornar o próximo campo de batalha competitivo. Aprovação pela FDA de cinco biossimilares de ustekinumabe em 2024 sublinha como agrupamento de lançamentos comprime pontos de preços e pode encurtar ciclos de vida do produto para cada participante sucessivo. Desenvolvedores estão priorizando mAbs como rituximabe e bevacizumabe porque endpoints clínicos são bem estabelecidos, reduzindo escopo de estudos comparativos. No entanto, anticorpos biespecíficos emergentes poderiam complicar trabalho futuro de equivalência, empurrando reguladores a refinar diretrizes novamente.
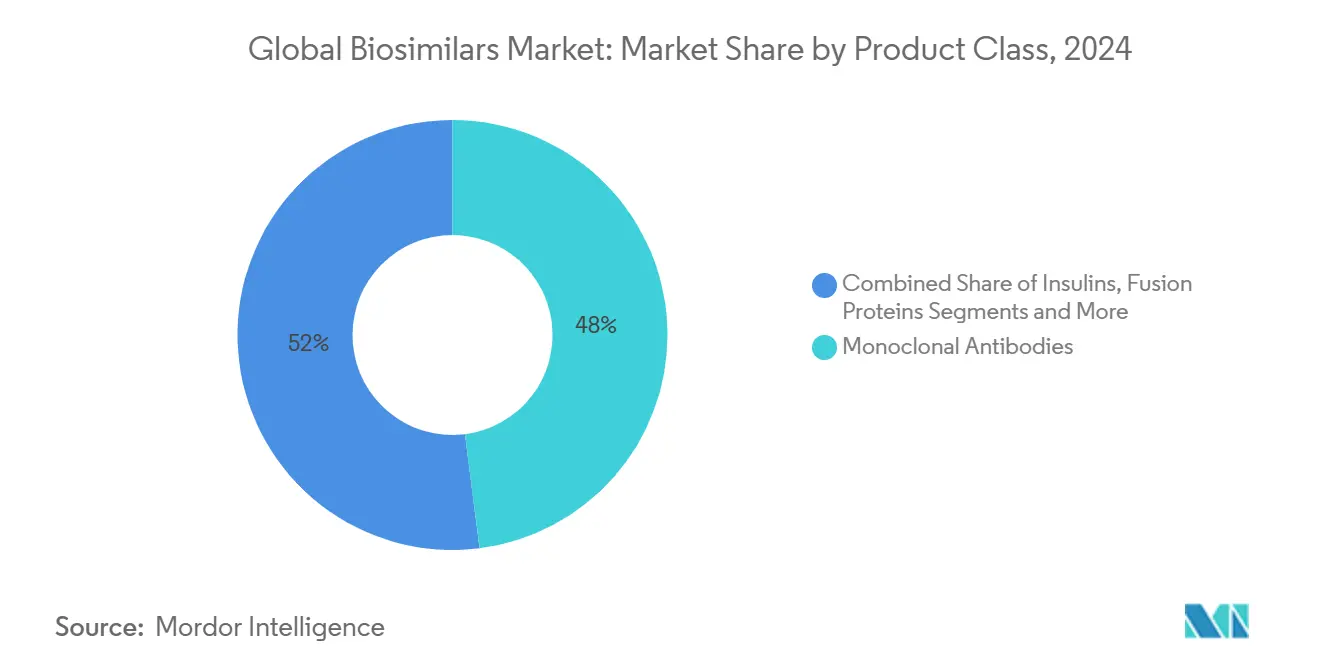
Nota: Participações de segmentos de todos os segmentos individuais disponíveis mediante compra do relatório
Indicação: Oncologia Domina Enquanto Autoimune Surge
O segmento de oncologia representa 55% da participação do mercado de biossimilares em 2024, comandando a maior fatia dos orçamentos de reembolso. Uma inferência imediata é que pagadores de oncologia possuem a maior alavancagem para impor troca, assim acelerando penetração. Doenças autoimunes e inflamatórias registram uma TCAC prevista de 23%, que implica que até 2030 a lacuna de receita entre as duas indicações pode estreitar consideravelmente. Lançamentos próximos de biossimilares visando inibidores de checkpoint como Yervoy sugerem um efeito de segunda ordem: se medicamentos caros de imuno-oncologia virem erosão de biossimilares, as economias poderiam financiar uso mais amplo de terapias de precisão. Por sua vez, essa dinâmica pode empurrar inovadores para construtos biológicos ainda mais complexos, renovando o ciclo de inovação.
Usuário Final: Hospitais Dominam Enquanto Canais de Varejo Expandem
Hospitais detêm 68% da participação do mercado de biossimilares em 2024 porque administração intravenosa (IV) e regimes de oncologia de alto custo ancoram gastos em centros de infusão. Inferência: poder de compra de grupos hospitalares molda negociações iniciais de preços, mas uma vez que formulações subcutâneas dominem, redes de farmácias de varejo exercerão mais influência. O canal de varejo e pedido por correspondência já mostra uma TCAC prevista de 22% até 2030, impulsionado por biossimilares auto-injetáveis que contornam cadeiras de infusão. Tyenne da Fresenius Kabi (tocilizumabe-aazg) fornece opções tanto IV quanto subcutâneas, evidenciando uma pivotagem estratégica para modelos de conveniência do paciente[3]Michael Brown, "Tyenne Biosimilar Receives FDA Approval," Fresenius Kabi, fresenius-kabi.com. Esta mudança também introduz desafios de gerenciamento de inventário, pois farmácias devem estocar múltiplos tamanhos de frasco e dispositivos, aumentando complexidade logística.
Tipo de Fabricação: Dominância Interna Enfrentando Desafio CDMO
Fabricação interna mantém 60% da participação do mercado de biossimilares em 2024, mas capacidade terceirizada cresce a uma TCAC de 20%. A inferência aqui é que diferenciais de custos sozinhos não podem explicar o aumento na terceirização; em vez disso, velocidade ao mercado e familiaridade regulatória impulsionam a tendência. CDMOs oferecem plataformas de processo prontas para uso e suítes analíticas validadas, tornando-os atraentes tanto para start-ups quanto para unidades de grandes farmacêuticas buscando flexibilidade. Conhecimento proprietário de processos permanece uma razão para algumas empresas manterem passos críticos internos, mas inovações de transferência de tecnologia estão reduzindo o risco de vazamento de conhecimento. Estratégias de integração vertical agora pesam a troca entre absorção de custos fixos e agilidade da cadeia de suprimentos.

Via de Administração: Preferências Evolutivas Remodelando Mercado
Infusões intravenosas permanecem dominantes hoje, mas biossimilares subcutâneos estão subindo na adoção, auxiliados por inovações de dispositivos que reduzem tempo de injeção. A nova inferência é que aprovações de dupla via aumentam participação de mercado porque permitem que médicos combinem preferências do paciente sem trocar produtos. A aprovação do Tyenne em ambas formulações exemplifica essa flexibilidade. Adoção subcutânea também se correlaciona com adoção de telemedicina, pois auto-administração permite monitoramento remoto de pacientes. Patentes para sistemas de entrega subcutânea como rituximabe SC expiram dentro da década, sugerindo que mais lançamentos multi-formato chegarão e poderão inclinar participação de mercado para farmácias de varejo.
Análise Geográfica
A Europa continua a liderar com 37% da participação do mercado de biossimilares, refletindo seu caminho regulatório pioneiro de 2006 e políticas de aquisição coordenadas. Muitos estados membros da UE instituíram esquemas de compartilhamento de ganhos, canalizando economias de volta para orçamentos hospitalares, o que encoraja engajamento de prescritores. A inferência é que a infraestrutura madura da Europa agora opera como um campo de teste para modelos de contratação avançados, como licitações multi-vencedores que preservam diversidade de fornecedores. Estudos de caso de infliximabe mostram que preços de originadores caíram drasticamente quando biossimilares chegaram, provando que competição funciona mesmo em terapêuticas especializadas. A região enfrenta um conjunto triplo de eventos de perda de exclusividade que acelerarão penetração de biossimilares mas também pode intensificar erosão de preços além de limiares confortáveis para fabricantes menores.
Ásia-Pacífico é o território de crescimento mais rápido com uma TCAC projetada de 24%, catalisada pelos gigantes sul-coreanos Samsung Bioepis e Celltrion e pelas reformas regulatórias da China. Uma inferência tirada de números de capacidade é que a Ásia está evoluindo de um hub de fabricação por contrato para uma potência de design e desenvolvimento, evidente na localização da infraestrutura de ensaios clínicos. A Índia aproveita sua herança de genéricos para acelerar submissões de biossimilares, enquanto Austrália e Japão estão investindo em bioprodução doméstica para resiliência da cadeia de suprimentos. A pandemia acelerou incentivos governamentais para autossuficiência em biológicos, sugerindo que a participação da Ásia em aprovações globais aumentará mais rapidamente do que apenas o crescimento da demanda global indicaria.
América do Norte-dominada pelos Estados Unidos-fica atrás da Europa em penetração, mas oferece o maior potencial de receita absoluta, apoiado por 56 aprovações da FDA e 41 lançamentos até julho de 2024. Uma inferência notável é que reformas de pagamento do Medicare embutidas na Lei de Redução da Inflação (IRA) podem realinhar incentivos para troca rápida de biossimilares em programas públicos. Economias projetadas dos EUA de USD 181 bilhões em cinco anos sublinham as apostas econômicas. Formulários provinciais canadenses também estão mandatando trocas não médicas, uma escolha política que pode harmonizar adoção através do continente. Coletivamente, esses fatores apontam para a América do Norte ultrapassando a Europa em tamanho de mercado no início dos anos 2030 se os diferenciais de crescimento atuais persistirem.

Cenário Competitivo
As 10 principais empresas controlam aproximadamente 70% da participação do mercado de biossimilares, mas essa concentração mascara estratégias divergentes. Samsung Bioepis superou KRW 1 trilhão em vendas com 12 moléculas comercializadas, sublinhando como fabricação em escala e portfólios focados podem flanquear Big Pharma diversificada. A inferência aqui é que players especializados ganham agilidade limitando competição interna por capital com medicamentos inovadores de alta margem. Oportunidades de espaço em branco também existem em oftalmologia, onde penetração de biossimilares é mínima mas preços de medicamentos de referência permanecem altos.
Diferenciação tecnológica está crescendo em importância; plataformas proprietárias S-AfuCHO e S-HiCon da Samsung Biologics visam encurtar ciclos de desenvolvimento e melhorar rendimentos. Triagem de moléculas assistida por IA e design de ensaios aumentam probabilidades de sucesso na primeira vez, sugerindo que capacidades digitais poderiam ampliar lacunas de desempenho. Alguns analistas preveem que Big Pharma pode recuar de biossimilares devido à pressão de preços, mas declarações da Amgen e Pfizer indicam compromisso contínuo, implicando que saídas competitivas, se ocorrerem, serão seletivas. A inferência é que mercados de capital podem recompensar empresas que dominam inovação ou se especializam em eficiência, penalizando modelos híbridos.
Integração vertical por gerentes de benefícios farmacêuticos (PBMs) na fabricação de biossimilares-através de entidades como Cordavis da CVS Health-pode redefinir economia de distribuição. Entrada de PBM pode apertar controle de formulário, reforçando sua alavancagem de negociação. A inferência é que desenvolvedores de biossimilares que carecem de parcerias PBM podem enfrentar acesso restrito ao mercado apesar da aprovação regulatória. Consequentemente, vantagem competitiva futura pode depender de integração downstream em vez de apenas escala de fabricação.
Líderes da Indústria Global de Biossimilares
-
Pfizer Inc
-
Novartis AG
-
Samsung Bioepies Co., Ltd
-
Coherus Biosciences, Inc.
-
Amgen Inc
- *Isenção de responsabilidade: Principais participantes classificados em nenhuma ordem específica

Desenvolvimentos Recentes da Indústria
- Março de 2025: A FDA aprovou Omlyclo (omalizumab-igec) da Celltrion USA como o primeiro biossimilar de referência ao Xolair (omalizumab). O biossimilar, concedido status de intercambialidade, é o primeiro biossimilar respiratório nos EUA. Omlyclo é aprovado para gerenciar asma moderada a severa em adultos e crianças de 6 anos ou mais com alergias não responsivas a esteroides inalados. Também é aprovado para adultos com inflamação sinusal crônica e pólipos nasais não responsivos a corticosteroides nasais.
- Janeiro de 2025: Amgen lançou Wezlana (ustekinumab-auub), o primeiro biossimilar intercambiável do Stelara, via plataforma Nuvaila da Optum, ampliando acesso ao tratamento autoimune.
- Outubro de 2024: A FDA aprovou Imuldosa (ustekinumab-srlf), o quinto biossimilar de ustekinumab nos EUA, com direitos de comercialização atribuídos à Intas Pharmaceuticals.
- Outubro de 2024: Biossimilar de denosumab TVB-009P da Teva entrou em revisão da FDA e EMA, com decisões esperadas para 2H 2025.
Escopo do Relatório do Mercado Global de Biossimilares
Conforme o escopo do relatório, um biossimilar é um biológico que é "similar" a outro medicamento biológico (conhecido como produto de referência) que já está licenciado pelos órgãos reguladores. Biossimilares são altamente similares ao produto de referência em termos de segurança, pureza e potência, mas podem ter diferenças menores em componentes clinicamente inativos. Ao aprovar biossimilares, o órgão regulador pode exigir que fabricantes conduzam um estudo clínico (ou estudos) suficiente para estabelecer segurança, pureza ou potência em um ou mais usos para os quais o produto de referência está licenciado, e o biossimilar busca licenciamento.
O mercado de biossimilares é segmentado por classe de produto (anticorpos monoclonais, hormônios recombinantes, imunomoduladores, agentes anti-inflamatórios e outras classes de produtos), aplicação (distúrbios sanguíneos, deficiência de hormônio do crescimento, distúrbios crônicos e autoimunes, oncologia e outras aplicações), e geografia (América do Norte, Europa, Ásia-Pacífico, Oriente Médio e África, e América do Sul). O relatório de mercado também cobre os tamanhos estimados do mercado global de biossimilares e tendências para 17 países em várias regiões. O relatório oferece o valor (USD milhões) para os segmentos acima mencionados.
| Anticorpos Monoclonais |
| Hormônios Recombinantes (EPO, G-CSF) |
| Insulinas |
| Heparinas de Baixo Peso Molecular |
| Proteínas de Fusão e Outros |
| Oncologia |
| Autoimune e Inflamatória Crônica |
| Distúrbios Metabólicos |
| Distúrbios Sanguíneos e de Coagulação |
| Outros |
| Hospitais |
| Clínicas Especializadas |
| Farmácias de Varejo e Pedido por Correspondência |
| Interna |
| Contrato/Terceirizada (CMO/CDMO) |
| Células Mamárias (CHO, SP2/0) |
| Microbiano (E. coli, Levedura) |
| Intravenosa |
| Subcutânea |
| América do Norte | Estados Unidos |
| Canadá | |
| México | |
| Europa | Alemanha |
| Reino Unido | |
| França | |
| Itália | |
| Espanha | |
| Resto da Europa | |
| Ásia-Pacífico | China |
| Japão | |
| Índia | |
| Coreia do Sul | |
| Austrália | |
| Resto da Ásia-Pacífico | |
| Oriente Médio | CCG |
| África do Sul | |
| Resto do Oriente Médio | |
| América do Sul | Brasil |
| Argentina | |
| Resto da América do Sul |
| Por Classe de Produto | Anticorpos Monoclonais | |
| Hormônios Recombinantes (EPO, G-CSF) | ||
| Insulinas | ||
| Heparinas de Baixo Peso Molecular | ||
| Proteínas de Fusão e Outros | ||
| Por Indicação | Oncologia | |
| Autoimune e Inflamatória Crônica | ||
| Distúrbios Metabólicos | ||
| Distúrbios Sanguíneos e de Coagulação | ||
| Outros | ||
| Por Usuário Final | Hospitais | |
| Clínicas Especializadas | ||
| Farmácias de Varejo e Pedido por Correspondência | ||
| Por Tipo de Fabricação | Interna | |
| Contrato/Terceirizada (CMO/CDMO) | ||
| Por Sistema de Expressão | Células Mamárias (CHO, SP2/0) | |
| Microbiano (E. coli, Levedura) | ||
| Por Via de Administração | Intravenosa | |
| Subcutânea | ||
| Por Geografia | América do Norte | Estados Unidos |
| Canadá | ||
| México | ||
| Europa | Alemanha | |
| Reino Unido | ||
| França | ||
| Itália | ||
| Espanha | ||
| Resto da Europa | ||
| Ásia-Pacífico | China | |
| Japão | ||
| Índia | ||
| Coreia do Sul | ||
| Austrália | ||
| Resto da Ásia-Pacífico | ||
| Oriente Médio | CCG | |
| África do Sul | ||
| Resto do Oriente Médio | ||
| América do Sul | Brasil | |
| Argentina | ||
| Resto da América do Sul | ||
Principais Questões Respondidas no Relatório
Qual é o tamanho do Mercado Global de Biossimilares?
O tamanho do Mercado Global de Biossimilares deve atingir USD 41,97 bilhões em 2025 e crescer a uma TCAC de 18,32% para alcançar USD 97,32 bilhões até 2030.
Qual região detém a maior participação do mercado de biossimilares?
A Europa lidera com uma participação de mercado de 37%, apoiada por seu marco regulatório precoce e altas taxas de adoção.
Qual é a região de crescimento mais rápido no Mercado Global de Biossimilares?
A Ásia-Pacífico está estimada para crescer na maior TCAC durante o período de previsão (2025-2030).
Por que biossimilares de anticorpos monoclonais são tão importantes?
Anticorpos monoclonais comandam 48% da receita de biossimilares porque seus produtos de referência são terapias de alto custo em oncologia e doenças autoimunes, criando fortes incentivos econômicos para versões de seguimento.
Página atualizada pela última vez em:


