小分子薬物探索市場規模・シェア
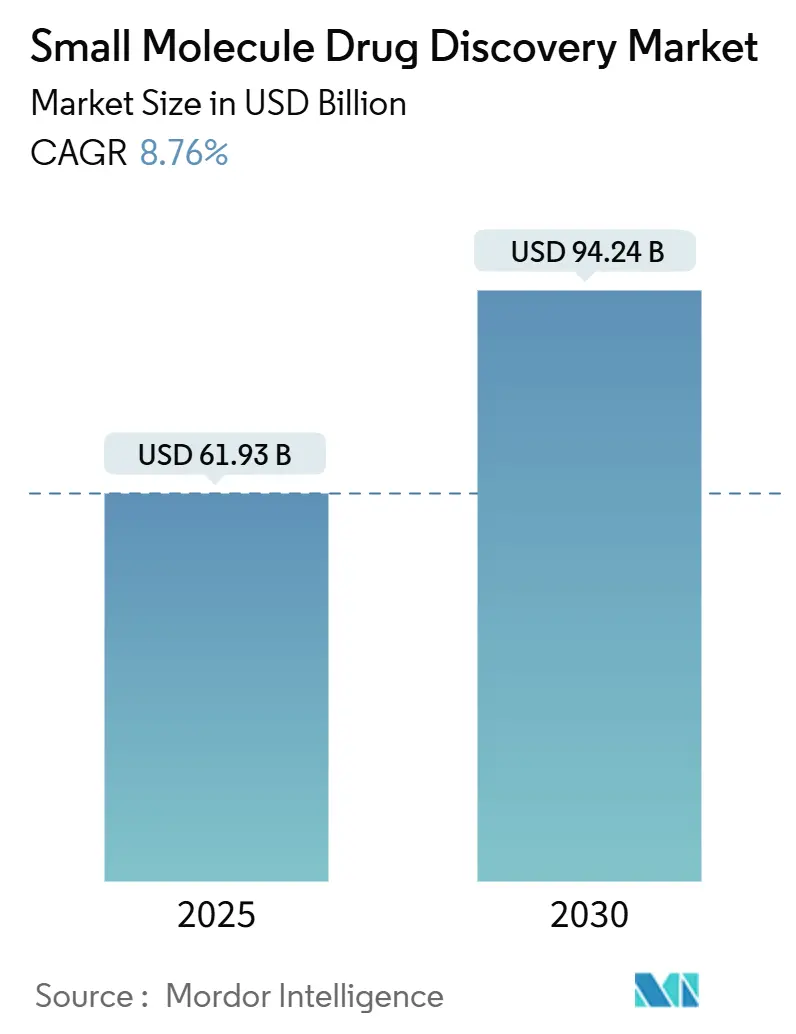
モルドール・インテリジェンスによる小分子薬物探索市場分析
小分子薬物探索市場規模は2025年に619億3000万米ドルとなり、2030年までに942億4000万米ドルに達し、年間平均成長率8.76%で成長すると予測される。経口投与治療薬への持続的依存、AI対応設計ツールの利用拡大、探索重視のCROへの安定したアウトソーシングにより、バイオ医薬品への投資増加にもかかわらず、小分子は製薬パイプラインの中心に位置している。北米は先進的な計算化学手法の採用をリードし、アジア太平洋地域はR&D能力の拡大が最も速い。オンコロジーは最大の治療用途であり続け、精密医療プログラムを引き続き誘致しているが、抗菌薬耐性が世界的な健康優先事項を先鋭化させる中、感染症プロジェクトはさらに速く成長している。技術専門企業、バーチャルバイオテクノロジー企業、従来の医薬品メーカーが差別化された専門知識とファーストインクラスの知的財産を求めて競争する中、競争激化が進んでいる。
主要レポートポイント
- 治療領域別では、オンコロジーが2024年の小分子薬物探索市場シェアの33.25%を占める一方、感染症は2030年まで年間平均成長率9.65%で拡大すると予測される。
- プロセス別では、リード最適化が2024年売上の29.74%を占め、標的同定・検証は2030年まで年間平均成長率9.5%で成長する見込み。
- 薬物タイプ別では、合成小分子が2024年売上の76.41%を占める一方、PROTACsと分子グルーは年間平均成長率9.37%で最も成長が速いカテゴリーとなっている。
- 技術別では、ハイスループットスクリーニングが2024年に35.43%のシェアでリードしているが、AI駆動設計プラットフォーム市場規模は年間平均成長率9.7%で進展している。
- エンドユーザー別では、製薬企業が2024年支出の44.34%を占め、バイオテクノロジー企業は年間平均成長率9.87%で最も急速な上昇を示している。
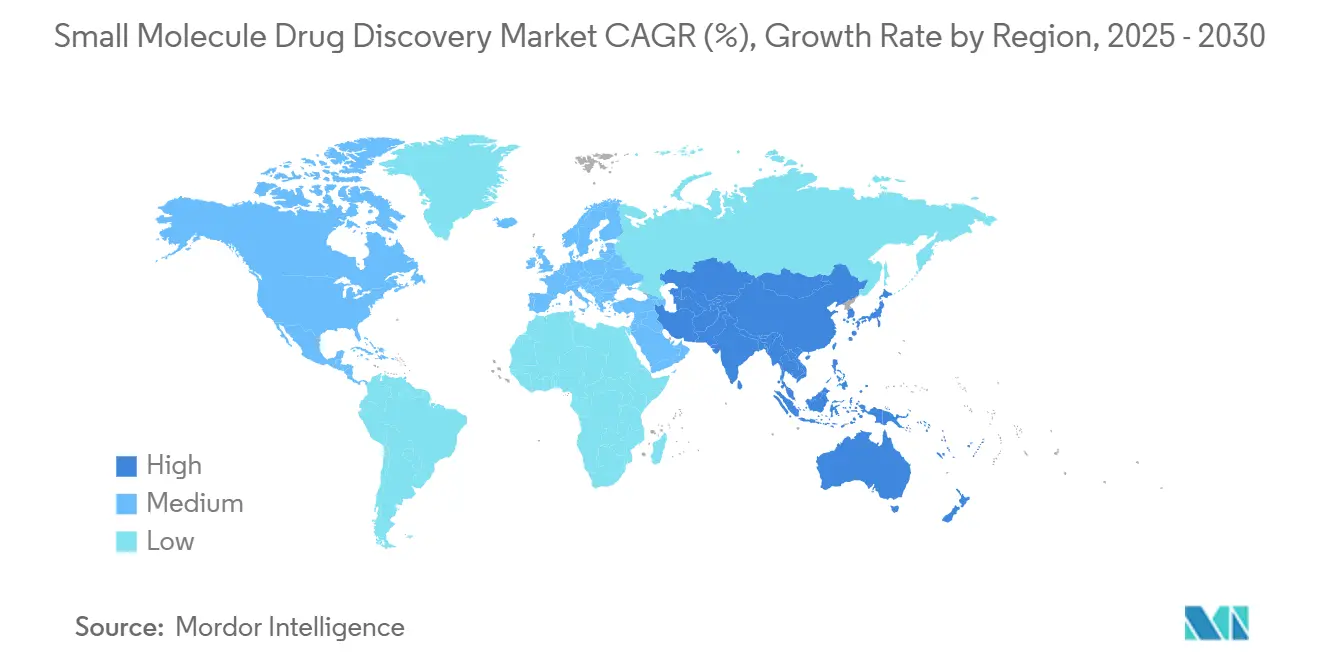
- 地域別では、北米が2024年に売上シェアの41.23%を占め、アジア太平洋地域は2030年まで年間平均成長率9.67%を記録すると予測される。
世界の小分子薬物探索市場トレンド・洞察
推進要因インパクト分析
| 推進要因 | (~) %のCAGR予測への影響 | 地理的関連性 | 影響時期 |
|---|---|---|---|
| 慢性・加齢関連疾患の世界的負担増加により 経口小分子治療薬需要を持続 | +2.1% | 世界的、北米・ヨーロッパで影響が高い | 長期(≥ 4年) |
| バイオ医薬品対比での化学合成の 製造効率・コスト効率の優位性が製薬R&D投資を方向付け | +1.8% | 世界的、新興市場で大きな影響 | 中期(2-4年) |
| AI駆動計算化学・予測モデリングの急速な成熟により ヒットからリードまでのタイムライン短縮 | +2.4% | 北米、ヨーロッパ、先進APAC市場 | 短期(≤ 2年) |
| 統合エンドツーエンドCRO/CDMOサービスモデルにより 資本軽量バーチャルバイオテック探索プログラムを可能に | +1.5% | 世界的、バイオテックハブに集中 | 中期(2-4年) |
| 規制迅速指定(ブレークスルー、希少疾病、 優先審査)により新規小分子薬の承認速度向上 | +1.2% | 北米・ヨーロッパ | 中期(2-4年) |
| 遺伝的に定義された患者集団に対する標的・精密 小分子治療薬の新出現増加 | +1.3% | 世界的、先進市場で早期採用 | 中期(2-4年) |
| 情報源: Mordor Intelligence | |||
慢性・加齢関連疾患の世界的負担増加により経口小分子治療薬需要を持続
人口高齢化とライフスタイル関連疾患が経口薬剤の長期使用を促進し、慢性ケアにおける小分子薬物探索市場を支えている。経口錠剤は注射可能なバイオ医薬品よりも輸送、保管、投与が容易であり、これはコールドチェーン能力が限られた医療システムにとって決定的な利点である。2024年に神経変性疾患に対して承認されたいくつかの脳透過性薬剤は、小分子がバイオ医薬品では到達できない標的に到達する方法を示し、中枢神経系治療における関連性を強化している[1]Zhonglei Wang, "Blockbuster Small-Molecule Drugs Approved by the FDA in 2024," MDPI, mdpi.com。支払者は糖尿病や高血圧などの広範囲疾患の治療費管理手段として経口投与薬を捉えている。
バイオ医薬品対比での化学合成の製造効率・コスト効率の優位性が製薬R&D投資を方向付け
化学合成プラットフォームは細胞培養ベースのバイオ医薬品製造より10~100倍低いコストで薬物原料をキログラム単位で製造できる。予測可能なスケールアップと長い保存期間により、企業は物流予算に負担をかけることなく幅広い患者集団にサービスを提供できる。価格圧力が強まる中、エグゼクティブは抗高血圧薬などの競争カテゴリーで持続可能な総利益をサポートする低いCOGSのため、探索ポートフォリオ内で小分子配分を維持または向上させている。
AI駆動計算化学・予測モデリングの急速な成熟によりヒットからリードまでのタイムライン短縮
深層学習モデルは数日でタンパク質ポケットに対して数十億の仮想構造をスクリーニングし、実験作業を最も有望なケモタイプに絞り込む。AtomNetは従来のハイスループットスクリーニングに匹敵するヒット率を実現したが、試薬と労働時間の消費量ははるかに少なかった[2]I. Wallach, "AI Is a Viable Alternative to High Throughput Screening," Nature, nature.com。これらのアルゴリズムは物理化学的性質予測も改善し、最適化された溶解性と毒性プロファイルで動物試験に入るリードを生み出す。より速い反復サイクルは、革新者が同等の支出で複数のプロジェクトを並行して進めることを可能にし、ファネルを拡大する。
統合エンドツーエンドCRO/CDMOサービスモデルによる資本軽量バーチャルバイオテック探索プログラムの実現
専門プロバイダーは現在、in-silico設計、薬用化学、ADME-Tox プロファイリング、前臨床製造を単一契約にバンドルしている。バーチャルバイオテックはこれらのネットワークを活用し、ベンチ活動の大部分をアウトソーシングしながら、生物学と戦略に焦点を当てた少数精鋭チームを運営する。これにより固定インフラが削減され、初期段階の支出を30-40%削減でき、シード資金が控えめな場合の重要な節約となる。同一パートナーが探索からIND対応研究にプログラムをシームレスに移行できるため、モデルはスケールアップも加速し、全体的なタイムラインを短縮する。
阻害要因インパクト分析
| 阻害要因 | (~) %のCAGR予測への影響 | 地理的関連性 | 影響時期 |
|---|---|---|---|
| 複雑な適応症における臨床開発コスト上昇と 後期段階失敗率の増大 | -1.6% | 世界的 | 長期(≥ 4年) |
| バイオ医薬品、細胞・遺伝子治療への パイプライン集中の急増により小分子プログラムから資本流出 | -1.4% | 北米・ヨーロッパ | 中期(2-4年) |
| 化学中間体の標的外毒性・環境影響に対する 世界的規制監視の強化 | -0.8% | 世界的、ヨーロッパ・北米で厳格執行 | 中期(2-4年) |
| 主要出発原料・高度中間体のサプライチェーン脆弱性により タイムラインリスクが拡大 | -0.7% | 世界的、アジア太平洋製造ハブで影響が高い | 短期(≤ 2年) |
| 情報源: Mordor Intelligence | |||
複雑な適応症における臨床開発コスト上昇と後期段階失敗率の増大
疾患関連モデルの進歩にもかかわらず、神経変性プログラムの第2相脱落率は依然として高く、失敗を含めて1つの薬剤を市場に出すための総支出を28億米ドルに押し上げている。単一資産パイプラインを保有する小規模企業は単一の期待外れな読み出しから存続リスクに直面し、多くが開発の早期段階でリスク分担アライアンスを求めるようになっている。スポンサーは翻訳バイオマーカーと適応設計試験を増々採用しているが、多因子疾患でのヒト有効性予測に依然として苦戦している。
バイオ医薬品、細胞・遺伝子治療へのパイプライン集中急増により小分子プログラムから資本流出
世界のバイオ医薬品売上は小分子売上の3倍の速度で拡大し、過度なベンチャーおよび企業資金を誘引している。米国における小分子の9年間価格交渉期間対バイオ医薬品の13年間などの規制規定が、取締役会の優先順位をさらに傾斜させている。大手製薬グループはそれに応じてポートフォリオを再調整し、高ボリュームのプライマリケア領域での特定の小分子フランチャイズを維持しながらも進めている。
セグメント分析
治療領域別:感染症上昇の中でオンコロジーが支配
オンコロジーは2024年の小分子薬物探索市場売上の33.25%を生み出し、免疫療法バックボーンとうまく組み合わせる変異特異的阻害剤から引き続き恩恵を受けている。KRAS、RET、FGFR変異を対象とするプログラムは早期治療設定に拡大しており、薬用化学需要を持続させている。より小規模ながら感染症探索は、公的民間パートナーシップが耐性脅威を標的とする抗生物質・抗ウイルスパイプラインに資金提供する中、予測年間平均成長率9.65%で加速している。中枢神経系候補は改善された血液脳関門透過化学を活用し、代謝・循環器疾患は次世代酵素調節薬を通じて安定した活動を維持している。消化器・呼吸器疾患は慢性炎症経路に標的メカニズムを適用するニッチ企業を惹きつけている[3]W. Zhang, "Global First-in-Class Drugs Approved in 2023-2024," ScienceDirect, sciencedirect.com。
パンデミック時代の監視インフラの回復は、広域抗ウイルス薬のスクリーニング取り組みを強化し、耐性メカニズムを回避する化学の長期機会を高めると予想される。オンコロジーの強力な知的財産ランドスケープは引き続きプレミアム価格設定とベンチャー支援を正当化し、そのシェアを際立たせている。しかし、併用レジメンが治療予算をシフトするため、抗体薬物複合体からの競争が2030年以降の成長を抑制する可能性がある。進化する病原体ランドスケープは、償還フレームワークが管理に配慮した薬剤を報奨する場合、感染症シェアが歴史的ベースラインに対して緩やかに上昇する可能性を示唆している。
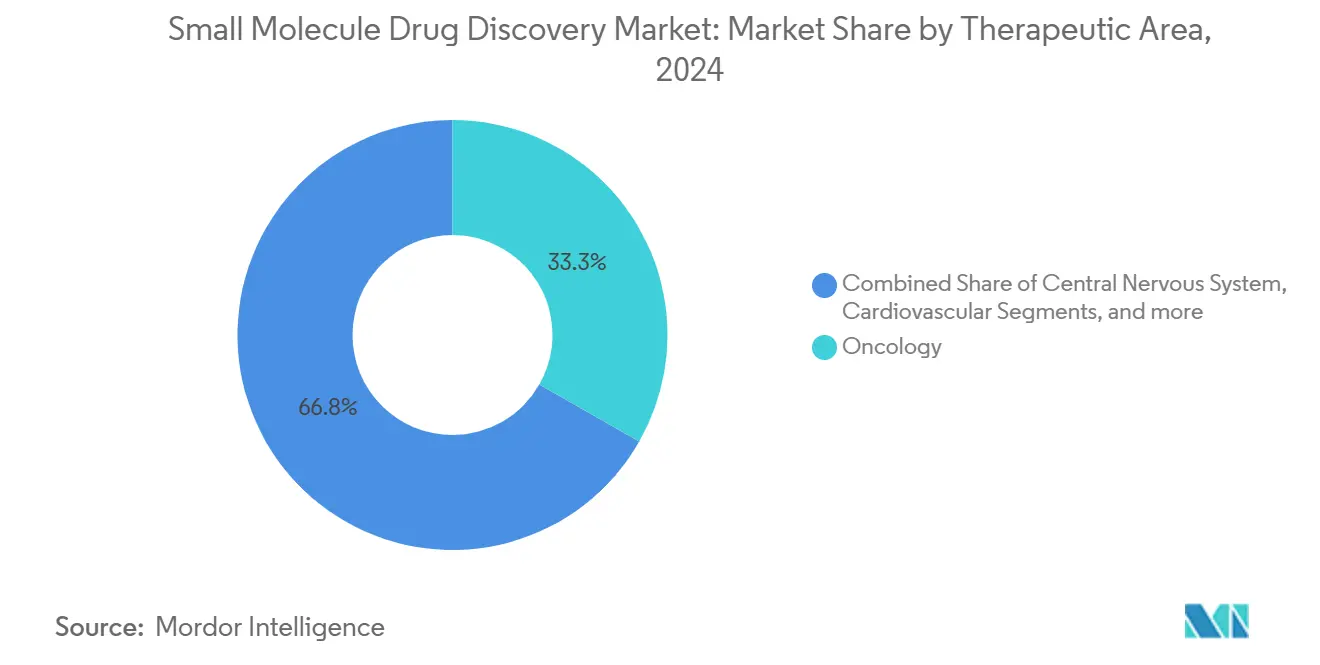
注記: すべての個別セグメントのセグメントシェアはレポート購入時に利用可能
プロセス・段階別:リード最適化の複雑性が売上を牽引
リード最適化は反復化学サイクル、SAR分析、並行ADME-Tox研究が最大の人件費と試薬予算を要求するため、小分子薬物探索市場規模の2024年支出の29.74%を占めた。新しい物理情報に基づく生成モデルは調整された効力と選択性を持つ類似体を提案するが、薬用化学者は臨床グレードプロファイルを達成するために多段階合成とスキャフォールドホッピングを依然として実行している。標的同定・検証は、タンパク質ドラッグ可能領域を拡大するCRISPR遺伝子編集スクリーン、単細胞オミクス、ネットワーク生物学により年間平均成長率9.5%で推移している。
ヒット生成は現在、膨大な化学空間をふるいにかけるためDNA符号化ライブラリーとバーチャルドッキングを組み合わせている。フラグメントベースキャンペーンは、最近承認されたFBDD由来化合物で実証されるように、従来は扱いにくい標的の出発点を供給している。前臨床候補選択段階は、早期に責任を除去する改善されたin-silico毒性学から恩恵を受けているが、決定的な動物研究は依然として必須である。スポンサーがスピードとリスク軽減されたワークフローを求める中、バイオインフォマティクス、化学、IND相談を統合するエンドツーエンドプラットフォームプロバイダーがシェアを獲得している。
薬物タイプ別:合成分子が大部分を維持、分解誘導薬が急増
合成小分子は2024年の小分子薬物探索市場シェアの76.41%を占め、拡張可能なプロセスと規制上の親しみやすさへの数十年の投資を強調している。多様なヘテロ環コア設計、フッ素化戦略、配座拘束は、経口バイオアベイラブルプロファイルを持つファーストインクラス薬剤を提供し続けている。PROTAC・分子グルー分解誘導薬は年間平均成長率9.37%で拡大し、内因性ユビキチン機構を活用して以前にドラッグ不可能だったタンパク質クラスを開放している。このモダリティはがん誘発ドライバーの酵素的・足場的機能の両方を中和でき、マルチターゲットプログラムを奨励している。
天然物誘導体は、その複雑な立体化学が高い標的親和性を与えるため、依然として革新をインスパイアしている。化学酵素合成とメタゲノムマイニングの進歩により、抗生物質・免疫調節キャンペーンのための海洋・植物代謝物への関心が復活している。ペプチド模倣薬と核苷類似体がポートフォリオを完成させ、選択性のために代謝活性化経路を活用できる抗ウイルス・オンコロジー適応症をサポートしている。総合的に、多様化はリスクプロファイル全体で探索パイプラインのバランスを保っている。
技術別:AI駆動設計がイノベーションを加速
ハイスループットスクリーニングは2024年に35.43%の売上シェアを維持し、予測計算モデルが不足するモダリティにとって不可欠であり続けている。しかし、AI駆動設計は年間平均成長率9.7%での拡大が予測され、多くのグリーンフィールド探索取り組みを支えている。物理ガイド神経ネットワークは現在、結合動態、標的外毒性、合成可能性を同時に予測し、化学者がマルチパラメーター最適化をデジタルファーストで評価することを可能にしている。フラグメントベース薬物探索は、効力を迅速に構築するためのcryo-EM構造と機械学習対応フラグメント連結から利益を得ている。
構造ベース設計は、AlphaFold予測を含む高解像度タンパク質データを活用し、従来のスクリーニングでは到達不可能なアロステリックポケットを可視化している。DNA符号化ライブラリーは共有結合・非共有結合メカニズムに対する迅速な親和性プロファイリングを促進している。これらのプラットフォームは一緒になってプロジェクトサイクルを短縮し、コストを圧縮し、資産軽量モデルを求める大手製薬とベンチャー支援スタートアップの両方からの関心を維持している。
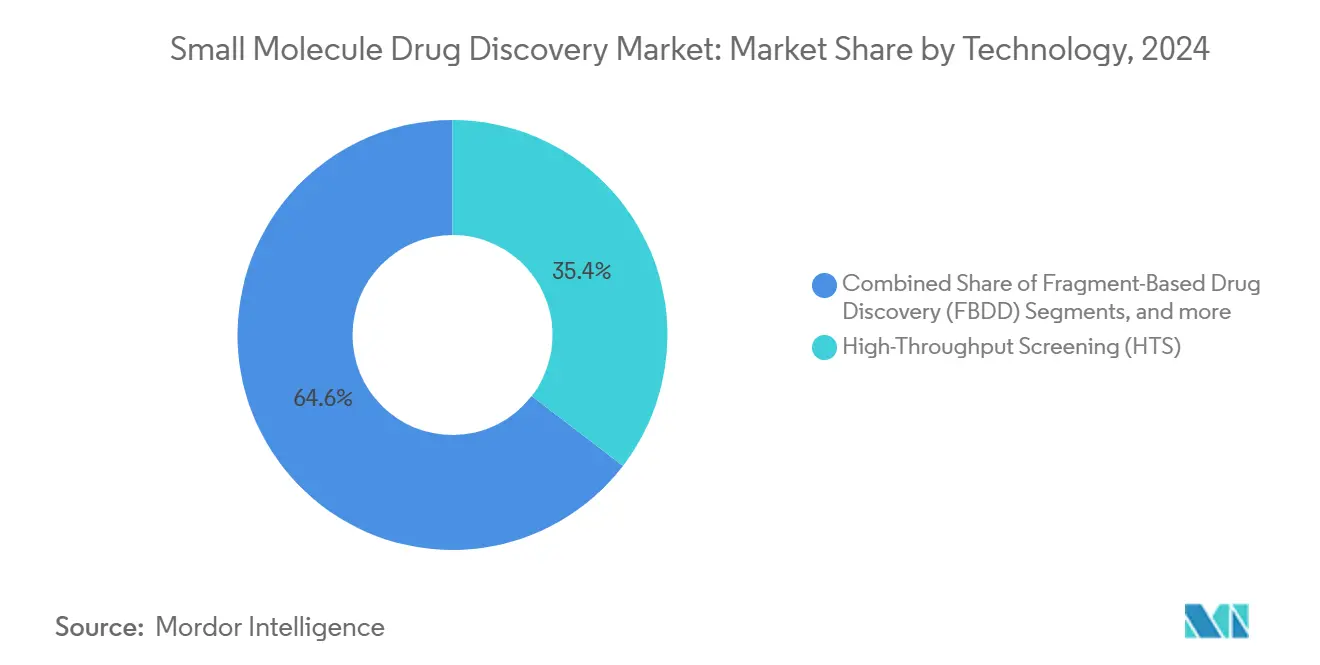
注記: すべての個別セグメントのセグメントシェアはレポート購入時に利用可能
エンドユーザー別:製薬リーダーが規模を保持、バイオテックが新規性を牽引
製薬企業は広範囲の化合物ライブラリー、グローバル化学チーム、統合規制専門知識を活用することにより、小分子薬物探索市場の2024年支出の44.34%を占めた。多くはインフラを複製することなくアルゴリズム馬力を供給するAI専門企業との株式指向取引を通じて社内能力を増強している。シリーズAやシリーズBラウンドで資金調達されることが多いバイオテクノロジー企業は、反復合成とバイオアッセイを信頼できるCROネットワークにアウトソーシングするバーチャルラボを運営している。彼らの年間平均成長率9.87%は、非従来的な標的とモダリティへの取り組みにおける機敏性を反映している。
学術センターは標的探索ブレークスルーにおいて極めて重要であり続け、ライセンスプログラムの安定した流れを供給している。NIHブループリント神経治療薬プログラムなどの政府資金による翻訳ネットワークは、非希釈資本と経験豊富なプロジェクト管理を提供し、引き渡し段階での科学的リスクを軽減している。一方、CROは化合物履歴、アッセイ性能、規制文書をリアルタイムで追跡する統合データプラットフォームを提供する戦略的パートナーに進化している。
地域分析
北米は成熟したベンチャー生態系、世界クラスの学術機関、ブレークスルー・希少疾病指定を通じた迅速審査をサポートする規制フレームワークにより、小分子薬物探索市場の2024年売上の41.23%を生み出した。インフレ削減法は小分子に償還不確実性をもたらすが、ボストン、サンディエゴ、トロントなどの技術豊富なハブはAI対応探索スタートアップを孵化し続けている。多くの世界企業が学際的人材と資本へのアクセスのため、米国に計算化学チームを拠点としている。
アジア太平洋地域は2025年から2030年まで年間平均成長率9.67%での拡大が予測される。中国のバイオテック企業は現在ファーストインクラスプログラムを開始し、2024年の世界インライセンス取引の31%が中国から調達された資産に関与した。政府インセンティブ、地方ベンチャーファンド、急速に拡大するCRO能力が地域の台頭を支えている。日本は数十年の薬用化学卓越性を活用し、インドは強力な合成化学教育とコスト優位から恩恵を受ける探索指向CROクラスターを構築している。
ヨーロッパは英国、ドイツ、スイスの活気あるバイオテック回廊と長年の製薬本社を融合している。ホライゾンヨーロッパ資金と官民イニシアティブは、AIモデリングと構造生物学を結合する国境を越えたコンソーシアムを維持している。大陸の規制当局は化学合成からの環境廃棄物の監視を強化しており、よりグリーンなプロセス化学技術を促している。中東・南米の新興市場は石油資金とバイオコモディティ収入を研究パークに投入しているが、人材不足と規制成熟が制限要因であり続けている。
競争環境
競争分野は大手製薬既存企業、中規模化学ハウス、AIネイティブスタートアップ、フルサービスCROを含む高度に断片化されている。パートナーがアルゴリズム設計と実証済みウェットラボ実行を組み合わせる中、戦略的アライアンスが増殖している。最近の取引には、Gilead SciencesがGenesis TherapeuticsとチームアップしてAI駆動ドッキングを抗ウイルス探索に活用することが含まれる。大手製薬は内部リソースと先行リスクを上限とするオプション取得構造のバランスを取っている。
専門企業は、かつてドラッグ不可能と考えられていた転写因子と足場タンパク質を標的とする分解誘導薬ライブラリーの特許取得を競っている。WuXi AppTecやCharles River Laboratoriesなどの大手CROは、彼らの化学者をスポンサースプリントチーム内に組み込む複数年探索フレームワークを確保し、これらのベンダーをフィー・フォー・サービス・サプライヤーではなく共同革新者として位置付けている。
ベンチャーキャピタルは桁違いの効率向上を約束するIsomorphic LabsやBenevolentAIなどのAIファーストプラットフォームへの資金提供を続けているが、臨床成功の証明はまだ新興段階である。予測毒性学、RNA結合小分子、環境配慮化学にホワイトスペースが残っており、ニッチ参入者を招いている。
小分子薬物探索業界リーダー
-
ICON Plc
-
Thermo Fisher Scientific Inc.
-
Eurofins Discovery
-
Labcorp Drug Development
-
Charles River Laboratories
- *免責事項:主要選手の並び順不同
最近の業界動向
- 2025年4月:マウントサイナイがオンコロジー・神経変性プログラムのため機械学習と薬用化学を融合するAI小分子薬物探索センターを立ち上げ。
- 2025年2月:Variational AIが迅速なヒット生成のためのEnki基盤モデルを拡大するため550万米ドルのシード延長ラウンドをクローズ。
- 2025年2月:BridGene BiosciencesがTakedaと神経学・免疫学探索パイプラインでの共有結合化学技術適用でパートナーシップ。
- 2024年9月:Gilead SciencesとGenesis Therapeuticsが先行3500万米ドル支払いと下流マイルストーンでマルチターゲットAI協力を開始。
世界小分子薬物探索市場レポート範囲
レポートの範囲により、小分子薬物探索は探索段階で薬物探索企業が負担するすべてのコストを表している。小分子は低分子量のため細胞に素早く侵入できる物質である。これらは治療目的で薬物として使用され、化学合成薬物分子とすべての生物学的合成薬物分子を含む。
小分子薬物探索市場は治療領域、プロセス・段階、地域でセグメント化されている。治療領域別では、市場はオンコロジー、中枢神経系、循環器、呼吸器、代謝障害、消化器、その他の治療領域にセグメント化されている。プロセス・段階別では、市場は標的ID・検証、ヒット生成・選択、リード同定、リード最適化にセグメント化されている。地域別では、市場は北米、ヨーロッパ、アジア太平洋、中東・アフリカ、南米にセグメント化されている。レポートは世界主要地域17か国の推定市場規模とトレンドもカバーしている。レポートは上記すべてのセグメントの価値(米ドル)を提供している。
| オンコロジー |
| 中枢神経系 |
| 循環器 |
| 呼吸器 |
| 代謝障害 |
| 消化器 |
| 感染症 |
| 自己免疫疾患 |
| その他の治療領域 |
| 標的同定・検証 |
| ヒット生成・選択 |
| リード同定 |
| リード最適化 |
| 前臨床候補選択 |
| 合成小分子 |
| 天然物誘導体 |
| ペプチド模倣薬 |
| PROTACs・分子グルー |
| 核苷類似体 |
| ハイスループットスクリーニング(HTS) |
| フラグメントベース薬物探索(FBDD) |
| 構造ベース薬物設計(SBDD) |
| 計算・AI駆動設計 |
| DNA符号化ライブラリースクリーニング |
| CRISPRベース標的検証 |
| バイオアッセイ開発・細胞ベースプラットフォーム |
| 製薬企業 |
| バイオテクノロジー企業 |
| 学術・研究機関 |
| 受託研究機関(CRO) |
| 北米 | 米国 |
| カナダ | |
| メキシコ | |
| ヨーロッパ | ドイツ |
| 英国 | |
| フランス | |
| イタリア | |
| スペイン | |
| その他のヨーロッパ | |
| アジア太平洋 | 中国 |
| 日本 | |
| インド | |
| オーストラリア | |
| 韓国 | |
| その他のアジア太平洋 | |
| 中東・アフリカ | GCC |
| 南アフリカ | |
| その他の中東・アフリカ | |
| 南米 | ブラジル |
| アルゼンチン | |
| その他の南米 |
| 治療領域別 | オンコロジー | |
| 中枢神経系 | ||
| 循環器 | ||
| 呼吸器 | ||
| 代謝障害 | ||
| 消化器 | ||
| 感染症 | ||
| 自己免疫疾患 | ||
| その他の治療領域 | ||
| プロセス・段階別 | 標的同定・検証 | |
| ヒット生成・選択 | ||
| リード同定 | ||
| リード最適化 | ||
| 前臨床候補選択 | ||
| 薬物タイプ別 | 合成小分子 | |
| 天然物誘導体 | ||
| ペプチド模倣薬 | ||
| PROTACs・分子グルー | ||
| 核苷類似体 | ||
| 技術別 | ハイスループットスクリーニング(HTS) | |
| フラグメントベース薬物探索(FBDD) | ||
| 構造ベース薬物設計(SBDD) | ||
| 計算・AI駆動設計 | ||
| DNA符号化ライブラリースクリーニング | ||
| CRISPRベース標的検証 | ||
| バイオアッセイ開発・細胞ベースプラットフォーム | ||
| エンドユーザー別 | 製薬企業 | |
| バイオテクノロジー企業 | ||
| 学術・研究機関 | ||
| 受託研究機関(CRO) | ||
| 地域別 | 北米 | 米国 |
| カナダ | ||
| メキシコ | ||
| ヨーロッパ | ドイツ | |
| 英国 | ||
| フランス | ||
| イタリア | ||
| スペイン | ||
| その他のヨーロッパ | ||
| アジア太平洋 | 中国 | |
| 日本 | ||
| インド | ||
| オーストラリア | ||
| 韓国 | ||
| その他のアジア太平洋 | ||
| 中東・アフリカ | GCC | |
| 南アフリカ | ||
| その他の中東・アフリカ | ||
| 南米 | ブラジル | |
| アルゼンチン | ||
| その他の南米 | ||
レポートで回答されている主要質問
低分子創薬市場の現在の価値は?
市場は2026年に674億2,000万米ドルであり、2031年までに1,030億6,000万米ドルに達すると予測されています。
収益をリードしている治療領域はどれですか?
腫瘍学(オンコロジー)は、継続的な精密医療への投資を反映し、2025年に31.55%のシェアでリードしています。
最も急速に成長しているセグメントはどれですか?
自己免疫プログラムは、2031年まで最高のCAGR 12.25%を示しています。
なぜ今PROTACsが重要なのか?
それらは標的タンパク質の分解を可能にし、これまで創薬困難とされていたタンパク質に対処することで、CAGR 17.87%で成長しています。
最も急速な成長が見込まれる地域はどこですか?
アジア太平洋地域は、中国での承認とインドのCRO(医薬品開発業務受託機関)の規模拡大により、CAGR 11.21%で拡大すると予測されています。
AIは創薬のタイムラインをどのように変えていますか?
REC-1245の急速な進展に示されるように、AIネイティブなプラットフォームはターゲットからIND(治験薬)までのタイムラインを最大40%短縮しました。
最終更新日:



