ヒト胚性幹細胞市場規模とシェア
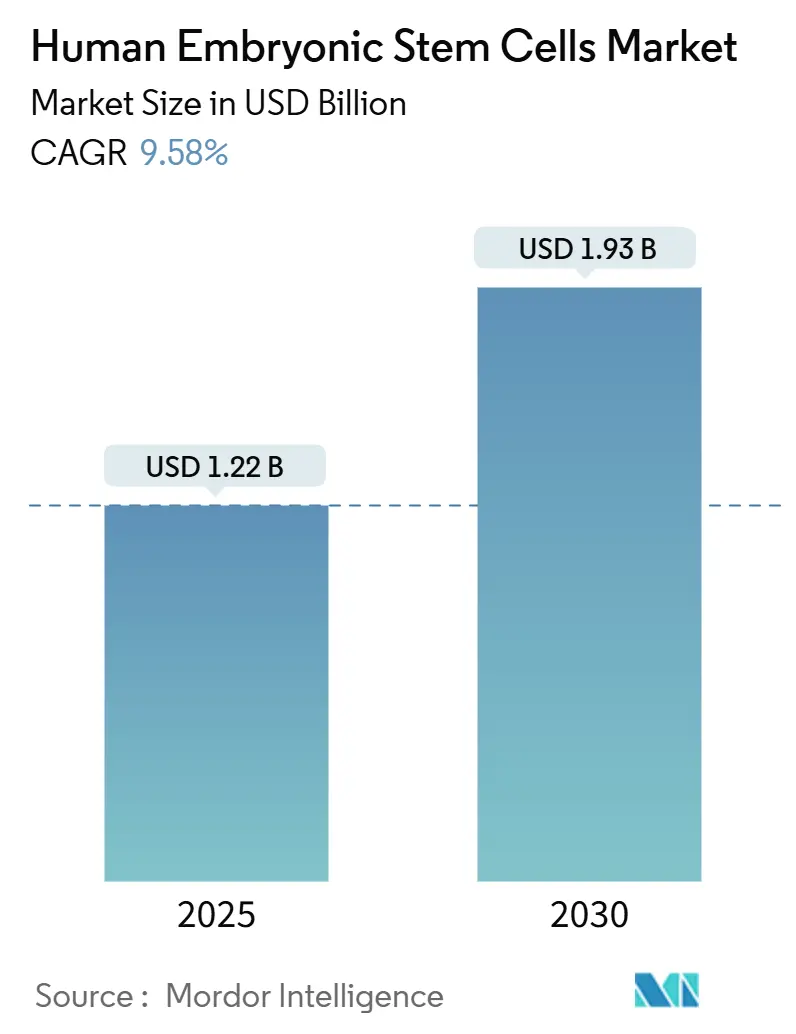
Mordor Intelligenceによるヒト胚性幹細胞市場分析
ヒト胚性幹細胞市場規模は2025年に12億2,000万米ドルと推定され、予測期間中(2025年~2030年)に年平均成長率9.58%で2030年までに19億3,000万米ドルに達すると予想されています。
CRISPR対応株工学の進歩、倫理的に調達された余剰IVF胚の着実に拡大するプール、および無異種成分GMP培養システムの商業利用により、心疾患、網膜疾患、および内分泌疾患にわたって治療の地平が集合的に拡大されています。自動化されたクローズドシステムバイオプロセシングが汚染リスクを削減し、バッチスループットを2倍にすることで産業導入が拡大し、ヒト胚性幹細胞市場での早期参入企業の競争優位性を高めています。[1]出典:Rebecca Ihilchik & Stacey Johnson、「AI対応バイオマニュファクチャリングイノベーションが細胞・遺伝子治療の手頃さとアクセスを向上」、ISCT Global、isctglobal.org FDAのRMAT経路と日本の迅速承認制度に例示される規制支援により、臨床から市場までのタイムラインが短縮され、数十億ドルの資金提供コミットメントが引き付けられています。一方、遺伝子編集パイオニアと製造スペシャリストとの学際的コラボレーションにより、開発サイクルが短縮され、ヒト胚性幹細胞市場内での知的財産防御可能性が拡大されています。高まる倫理活動とコスト圧力の増大は注視点ですが、技術主導の生産性向上により短期的な逆風を相殺する軌道にあります。
主要レポートポイント
- 用途別では、再生医療が2024年にヒト胚性幹細胞市場シェアの58.57%を占めており、幹細胞生物学研究は2030年まで年平均成長率10.86%で進歩しています。
- 製品タイプ別では、hESC株が2024年にヒト胚性幹細胞市場規模の53.12%のシェアを占めており、培養培地・試薬は2025年から2030年までの間に年平均成長率11.69%で拡大すると予測されています。
- 地域別では、北米が2024年に売上シェア42.16%で主導しており、一方アジア太平洋地域は2030年まで年平均成長率11.41%で最も速い成長を達成すると予測されています。
世界ヒト胚性幹細胞市場トレンドと洞察
要因インパクト分析
| 要因 | 年平均成長率予測への(~)%インパクト | 地理的関連性 | インパクト時間軸 |
|---|---|---|---|
| 心疾患および悪性疾患の高い有病率 | +1.8% | 世界的、北米・欧州に集中 | 中期(2~4年) |
| 再生医療への需要増加 | +2.1% | 世界的、APAC成長市場主導 | 長期(4年以上) |
| 政府および民間資金提供プログラムの拡大 | +1.5% | 北米、欧州、日本 | 短期(2年以内) |
| CRISPR対応hESC株工学 | +1.2% | 世界的、米国、英国、日本のR&Dセンター | 中期(2~4年) |
| 無異種成分GMP培養システムによる汚染リスク低減 | +0.9% | 世界的製造ハブ | 短期(2年以内) |
| 余剰IVF胚による倫理的hESC供給拡大 | +0.7% | 確立されたIVFインフラを持つ地域 | 長期(4年以上) |
| 情報源: Mordor Intelligence | |||
心疾患および悪性疾患の高い有病率
心血管疾患とがんは合わせて世界的な死因の大部分を占めており、多系統修復ソリューションへの持続的な臨床需要を生み出しています。ヒト胚性幹細胞由来心筋スフェロイドは豚梗塞モデルで収縮性を回復し、現在虚血性心筋症の初回ヒト試験に進んでいます。hESC由来膵島細胞(VX-880)は1型糖尿病患者12人中10人でインスリン非依存性を達成し、応用可能性の広さを強調しています。心疾患ケアへの人口レベル支出が3,500億米ドルを超える中、商業的関心が高まり、ヒト胚性幹細胞市場内で心代謝プログラムが主要価値推進要因として位置づけられています。hESCをシードした3Dプリント心筋足場などの付加製造技術の進歩により、トランスレーショナル経路がさらに短縮されています。[2]出典:Sena Quinn、「ヒト幹細胞による3D心臓組織プリンティング」、Lifeboat Foundation、lifeboat.com これらのデータは総合的に疾患修飾ポテンシャルを検証し、2030年までのプレミアム価格機会を強化しています。
再生医療への需要増加
米国で1,200を超える活発な細胞・遺伝子治療試験が実施されており、再生医療がニッチ領域から最前線のケアへと移行していることを示しています。ヒト胚性幹細胞に依存する同種プラットフォームにより、既製品投与が可能となり、自家移植手術の歴史的スケール制限を解決します。日本の60を超えるiPS細胞研究は、一貫性のある政策、償還の明確さ、製造インセンティブがいかに加速された導入を促進するかを示しています。FDAによる間葉系間質細胞治療の画期的承認は、規制当局が臨床的に検証された製品をクリアする準備ができていることを示し、間接的にhESC開発者に恩恵をもたらします。hESC由来角膜上皮を用いた視力回復成功(90%以上の有効性)により公衆の信頼が高まり、患者募集と投資家流入の好循環を促進しています。
政府および民間資金提供プログラムの拡大
CIRMの50億米ドル基金は、米国をトランスレーショナル研究のための資本豊富な環境として確立しています。公的助成金は早期研究のリスクを軽減し、ヒト胚性幹細胞市場全体でベンチャーキャピタルと戦略的製薬パートナーシップを誘い込んでいます。日本の条件付承認フレームワークは国家支援インフラ支出を補完し、グローバル企業がより迅速な市場参入のために東京近郊にGMPスイートを配置することを促しています。民間サイドでは、BARDAの幹細胞由来血小板プログラムなどの複数年代理店契約が、収益ストリームを多様化する防衛・緊急対応用途の拡大を示しています。これらの並行する資金チャネルは、発見速度を拡大し、商業化リスクを圧縮します。
CRISPR対応hESC株工学
CRISPRプライム編集は多能性細胞で36~73%のオンターゲット効率を達成し、アイソジェニック疾患モデルと低免疫原性治療株の迅速構築を可能にします。Cas12a-マルチプレックスシステムは現在、複数の編集の同時挿入を可能にし、候補スクリーニングサイクルを加速させています。HLA-A、-B、-Cアンチゲンを除去する概念実証作業は汎用ドナー細胞の有望性を示していますが、免疫適格マウスでの移植拒絶反応は、組み合わせ免疫回避戦略の必要性を強調しています。Wellcome Sanger Instituteで生成された大規模バリアントライブラリは、標的検証と毒性スクリーニングのための比類のないリソースを提供します。累積的に、精密編集は下流の減衰を低減し、ヒト胚性幹細胞市場全体で製品ポートフォリオの選択肢性を向上させます。
制約要因インパクト分析
| 制約要因 | 年平均成長率予測への(~)%インパクト | 地理的関連性 | インパクト時間軸 |
|---|---|---|---|
| 高い治療・製造コスト | -1.4% | 世界的、特にコスト敏感市場 | 中期(2~4年) |
| 厳格で不均一な世界規制 | -1.1% | 世界的、地域強度の変動あり | 長期(4年以上) |
| 急成長するiPSC代替品による資金の侵食 | -0.8% | 世界的R&Dセンター | 中期(2~4年) |
| ソーシャルメディア主導の倫理活動による導入抑制 | -0.6% | 主に欧米市場 | 短期(2年以内) |
| 情報源: Mordor Intelligence | |||
高い治療・製造コスト
現在のhESCベース治療は、手作業クリーンルーム作業と低いプロセス収率により、しばしば1回量あたり10万米ドルを超えます。AIガイドロボティクスは労働投入を50%削減し、ロット間一貫性を提供し、5年以内に5万米ドル未満での損益分岐点製造を示しています。Thermo Fisherのニュージャージー州にある4億7,500万米ドルのCDMOサイトは、コスト圧縮と規制遵守を目標とする業界規模の投資を例示しています。モジュラーロボティッククラスターは、拡張、収穫、最終充填・仕上げを再現可能に処理し、キャンペーン時間を短縮しバッチ失敗リスクを低減します。ノースイースタン大学の予測AIモデルがさらに栄養フィードと継代タイミングを最適化し、収率を産業ベンチマークに向けて押し上げています。これらの利得は、支払者の精査とコスト敏感な新興市場需要を相殺するために勢いを維持する必要があります。
厳格で不均一な世界規制
開発者は、EUの2027年SoHO規制からFDAの認可されていないクリニックに対する段階的執行まで、承認要件のパッチワークをナビゲートしています。[3]出典:Sarah Rosenthaler、「ヒト由来物質に関する新しいEU規制」、Schoenherr、schoenherr.eu 2025年に改定予定の日本の胚モデルガイドラインは、先進的な政策がいかに投資を促進できるか、また同時に遵守作業負荷をどう再形成するかを示しています。国際細胞・遺伝子治療学会のAPACロードマップは調和を目指していますが、採用されるまでは、異なる書類が管理コストを押し上げます。連邦資金禁止をめぐる米国の政治的議論が、長期資本計画に不確実性を追加しています。
セグメント分析
用途別:再生医療が臨床応用を推進
再生医療は2024年にヒト胚性幹細胞市場シェアの58.57%を獲得し、地理的萎縮患者におけるOpRegenの+5.5文字視力向上などの臨床結果に後押しされています。脊髄修復、膵島置換、心筋再筋肉化が現在多施設試験の見出しを飾り、セグメントの主要収益軌道を強化しています。より多くのプログラムがRMATまたはSAKIGAKE指定を確保するにつれ、支払者は償還を正当化するための実世界エビデンスを得、ヒト胚性幹細胞市場内で好循環の導入サイクルを促進しています。
幹細胞生物学研究は2030年まで年平均成長率10.86%を記録し、自動化ゲノム編集スクリーンとヒト組織複雑性を再現できるオルガノイドプラットフォームから恩恵を受けています。CRISPR駆動系譜追跡と高含有フェノミクスが標的同定タイムラインを短縮し、新規オルガノイド共培養システムが疾患モデル精度を5倍向上させます。学術コア施設が有料サービスモデルに移行するにつれ、研究支出が試薬と株ライセンスロイヤルティに還流し、サプライチェーン参加者の定期収益プールを拡大しています。発見応用のヒト胚性幹細胞市場規模は、マルチプレックススクリーンが精密医療パイプラインに不可欠になるにつれて着実に上昇すると予測されています。

注記: すべての個別セグメントのシェアはレポート購入時に利用可能
製品タイプ別:培養培地・試薬の成長にもかかわらずhESC株が優勢
商業的に確立されたhESC株は2024年にヒト胚性幹細胞市場規模の53.12%のシェアを占め、スケーラブルなマスター細胞バンクインフラと成熟した規制前例に支えられています。汎用ドナー編集戦略は、特注製造なしでより広範な患者カバレッジを約束し、迅速な参入を求めるビッグファーマにとって株ライセンシングを魅力的に保っています。LonzaからのGMP培養培地、試薬、補助キットは高マージンサプライ層を形成し、カスタマイズされた無異種成分製剤がプロセス検証サイクルを通じて定期需要をロックしています。
培養培地・試薬は年平均成長率11.69%で拡大し、特に拒絶リスクを最小化する患者固有の修正が可能な遺伝性疾患において、個別化医療の波に乗っています。機器・消耗品サプライヤーは、90%の労働削減を達成するTerumo-CiRAの自動化iPS細胞ワークステーションに例証されるように、ハードウェア・ソフトウェアスイートをバンドルすることでこのシフトを活用しています。COGSが低下するにつれ、自家移植パイプラインは大量市場同種製品を補完し、ニッチ希少疾患市場を獲得する可能性があります。

注記: すべての個別セグメントのシェアはレポート購入時に利用可能
地域分析
北米は、強固なNIHとCIRM資金、RMAT対応迅速審査、広範なCDMO能力に支えられ、2024年に世界収益の42.16%を維持しました。スタンフォード主導の心疾患試験、ノースウエスタンの脊髄イニシアティブ、Thermo Fisherの新プリンストンサイトが総合的にこの地域のラボから市場投入までの統合を展示しています。胚研究への連邦資金に関する政治的不確実性は戦略的リスクを呈しますが、多様化された民間投資が潜在的な公的予算変動を緩和しています。
アジア太平洋地域は最も急成長するクラスターで、日本の条件付承認制度と中国の国家支援研究パークを背景に2030年まで年平均成長率11.41%で進歩しています。60を超える活発な日本の臨床試験が規制の敏捷性を強調し、住友ファーマとニコン-ロンザ製造提携が多国籍パートナーからの資本流入を実証しています。政府助成金が施設建設と人材育成をカバーし、ヒト胚性幹細胞市場内でローカルサプライチェーン成熟度を拡大しています。
欧州の見通しは2027年のSoHO規制の効果的な展開にかかっています。ドイツと英国は主要な学術クラスターを維持しており、英国の合成胚に関する実践規範は大陸基準を形作る可能性のある政策革新を示しています。フランスとイタリアは眼科学と軟骨修復ニッチに焦点を当て、スカンジナビアコンソーシアムは患者アクセス拡大のための極低温物流に投資しています。西欧の償還ハードルは持続していますが、国境を越えたコラボレーションとEU全体のHTA改革により、認定製品の市場アクセスが合理化されると予想されます。

競合状況
競争は中程度で、ファーストインクラス適応症を追求する大手製薬と専門バイオテクノロジーの混在によって特徴づけられます。Vertex Pharmaceuticalsは、治療患者の83%でインスリン非依存性を示すVX-880データを提供するために集中的なR&D支出を活用し、単一資産の深さの価値を実証しました。Lineage Cell Therapeuticsは、開発リスクをヘッジするため、並行する後期眼科学と早期脊髄プログラムを実行し、パイプラインの幅を例示しています。アステラス製薬の安川電機とのロボティクス提携は、サイクル時間短縮が競争価格に直接変換される主要戦場としての製造スケーラビリティを指摘しています。
ニコンやOmniaBioを含む新興技術参入企業は、AI対応品質管理アルゴリズムを収益化し、百万細胞あたりコスト指標で差別化しています。汎用ドナー細胞工学はホワイトスペース領域で、学術産業コンソーシアムが補体とNK細胞応答を回避できる多遺伝子編集プラットフォームの精製を競っています。
第一世代hESC株の特許の崖が近づくにつれ、ブランドエクイティは基本的IP保護よりも製造能力と臨床結果データセットにますます依存するようになります。競争の全体的なトーンは、世界規模の規制分岐をナビゲートするためにスケールが不可欠になるため、さらなる統合を示唆しています。
ヒト胚性幹細胞産業リーダー
Merck KGaA
STEMCELL Technologies Inc.
Vertex Pharmaceuticals
Thermo Fisher Scientific Inc.
Lineage Cell Therapeutics Inc.
- *免責事項:主要選手の並び順不同

最近の業界動向
- 2024年9月:Allen InstituteとNYSCFが提携し、疾患モデルの包括性を改善するため、民族的に多様な幹細胞ライブラリに構造細胞タグを統合しました。
- 2024年9月:EPFLは、トランスレーショナル幹細胞プロジェクトのためのすべてのキャンパス研究グループが利用できる共有オルガノイドおよびiPSC施設、SCOLを開設しました。
世界ヒト胚性幹細胞市場レポート範囲
ヒト胚性幹細胞は、初期段階の着床前胚である胚盤胞の内細胞塊から抽出される多能性幹細胞です。これらの幹細胞は様々な疾患の治療に使用されます。
ヒト胚性幹細胞市場は用途と地域別にセグメント化されています。用途別では、市場は再生医療、幹細胞生物学研究、組織工学、毒性試験にセグメント化されています。地域別では、市場は北米、欧州、アジア太平洋、中東・アフリカ、南米にセグメント化されています。各セグメントについて、市場規模は米ドル価値の観点から提供されています。
| 再生医療 |
| 幹細胞生物学研究 |
| 組織工学 |
| 毒性試験 |
| hESC株 |
| 培養培地・試薬 |
| 機器・消耗品 |
| 北米 | 米国 |
| カナダ | |
| メキシコ | |
| 南米 | ブラジル |
| アルゼンチン | |
| その他の南米 | |
| 欧州 | ドイツ |
| 英国 | |
| フランス | |
| イタリア | |
| スペイン | |
| その他の欧州 | |
| APAC | 中国 |
| 日本 | |
| インド | |
| オーストラリア | |
| 韓国 | |
| その他のAPAC | |
| 中東・アフリカ | GCC |
| 南アフリカ | |
| その他のMEA |
| 用途別 | 再生医療 | |
| 幹細胞生物学研究 | ||
| 組織工学 | ||
| 毒性試験 | ||
| 製品タイプ別 | hESC株 | |
| 培養培地・試薬 | ||
| 機器・消耗品 | ||
| 地域別 | 北米 | 米国 |
| カナダ | ||
| メキシコ | ||
| 南米 | ブラジル | |
| アルゼンチン | ||
| その他の南米 | ||
| 欧州 | ドイツ | |
| 英国 | ||
| フランス | ||
| イタリア | ||
| スペイン | ||
| その他の欧州 | ||
| APAC | 中国 | |
| 日本 | ||
| インド | ||
| オーストラリア | ||
| 韓国 | ||
| その他のAPAC | ||
| 中東・アフリカ | GCC | |
| 南アフリカ | ||
| その他のMEA | ||
レポートで回答される主要質問
現在のヒト胚性幹細胞市場規模はどの程度ですか?
市場は2025年に12億2,000万米ドルに達し、着実な拡大軌道にあります。
2030年まで予測される年平均成長率(CAGR)は?
9.58%のCAGRが予測され、市場価値を2030年までに19億3,000万米ドルへと押し上げます。
今日最大の収益シェアを占める用途はどれですか?
再生医療が2024年に58.57%のシェアでリードし、進歩する心疾患、網膜、内分泌プログラムに支えられています。
最も速い成長が予想される地域はどこですか?
アジア太平洋地域は、日本の迅速承認制度と中国の拡大する研究インフラに推進され、2030年まで11.41%のCAGRで成長すると予測されています。
より広範な導入への主要なコスト障壁は何ですか?
GMP製造コストが投与価格を10万米ドル以上に保っていますが、AI主導の自動化が製造費を最大50%削減しています。
CRISPR技術はヒト胚性幹細胞製品をどう向上させていますか?
CRISPRプライム編集は36~73%の編集効率を提供し、低免疫原性汎用ドナー株と臨床応用を加速する高忠実度疾患モデルを可能にします。
最終更新日:



