Taille et Part du Marché des Tests de Toxicologie In Vitro
Analyse du Marché des Tests de Toxicologie In Vitro par Mordor Intelligence
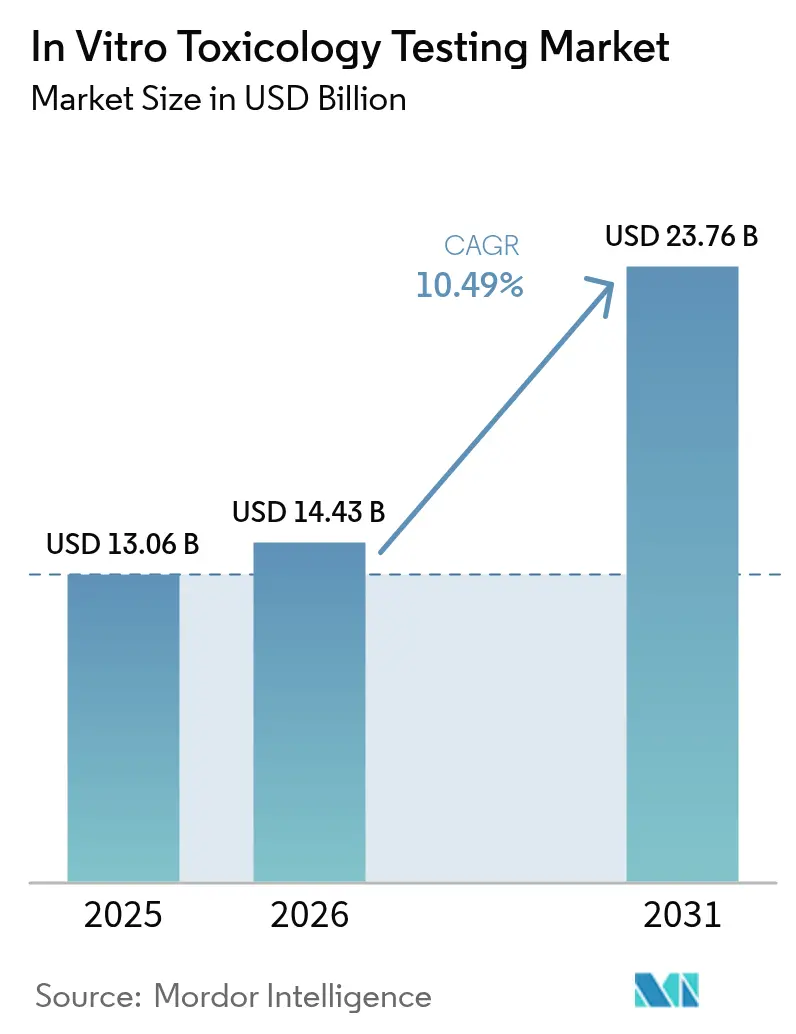
La taille du Marché des Tests de Toxicologie In Vitro était évaluée à 13,06 milliards USD en 2025 et devrait croître de 14,43 milliards USD en 2026 pour atteindre 23,76 milliards USD d'ici 2031, à un CAGR de 10,49 % durant la période de prévision (2026-2031).
Ce rythme souligne le rôle central du secteur dans la protection de la santé humaine dans les domaines pharmaceutique, cosmétique et chimique, tout en répondant aux réglementations mondiales qui découragent l'expérimentation animale. Des mandats de sécurité plus stricts, le programme de Nouvelles Méthodes Alternatives de la FDA et la feuille de route européenne visant à éliminer progressivement les modèles animaux stimulent la demande. Les avancées parallèles dans la culture cellulaire 3D, les systèmes organe-sur-puce et l'analyse assistée par IA améliorent la précision prédictive, réduisent les coûts de R&D et ouvrent de nouveaux flux de revenus pour les organisations de recherche sous contrat. L'intérêt des investisseurs reste fort, car la transition technologique promet une détection plus précoce de la toxicité, moins d'échecs en phase avancée et une mise sur le marché plus rapide des thérapeutiques innovantes.
Points Clés du Rapport
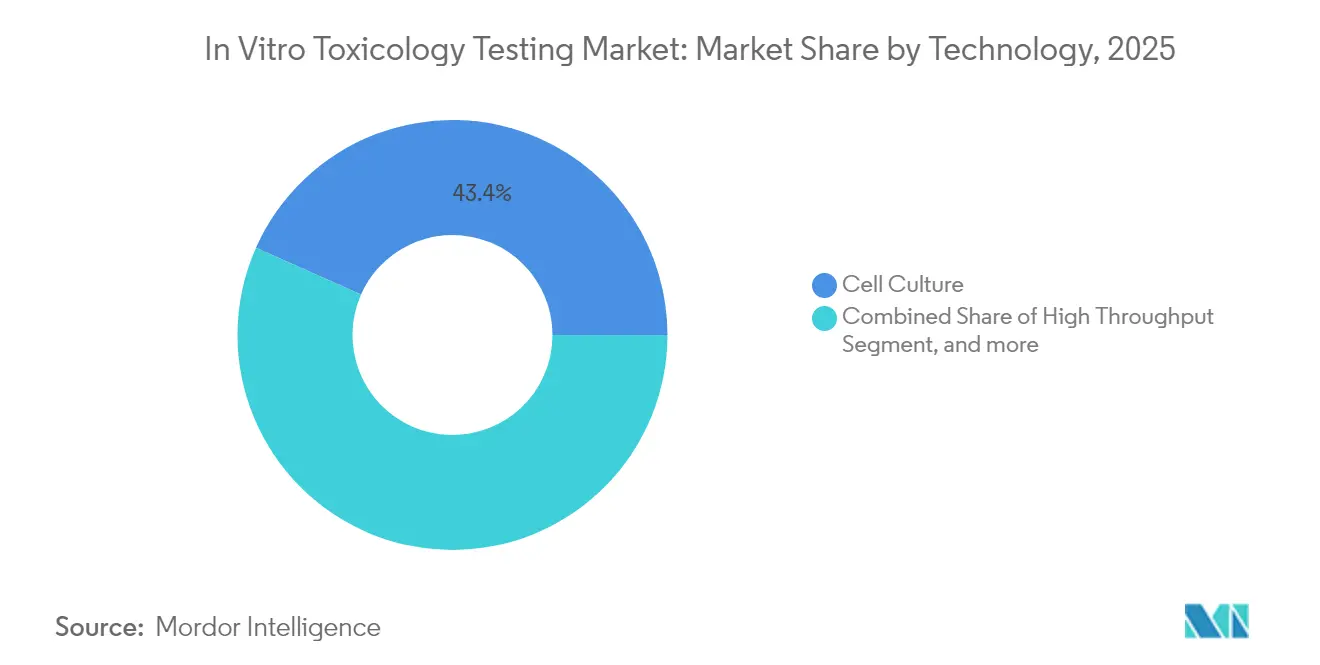
- Par technologie, la culture cellulaire a dominé avec 43,35 % de la part du marché des tests de toxicologie in vitro en 2025, tandis que les méthodes OMICS devraient croître à un CAGR de 13,61 % jusqu'en 2031.
- Par méthode, les dosages cellulaires représentaient 35,72 % de la taille du marché des tests de toxicologie in vitro en 2025 ; les techniques in silico devraient se développer à un CAGR de 14,03 % jusqu'en 2031.
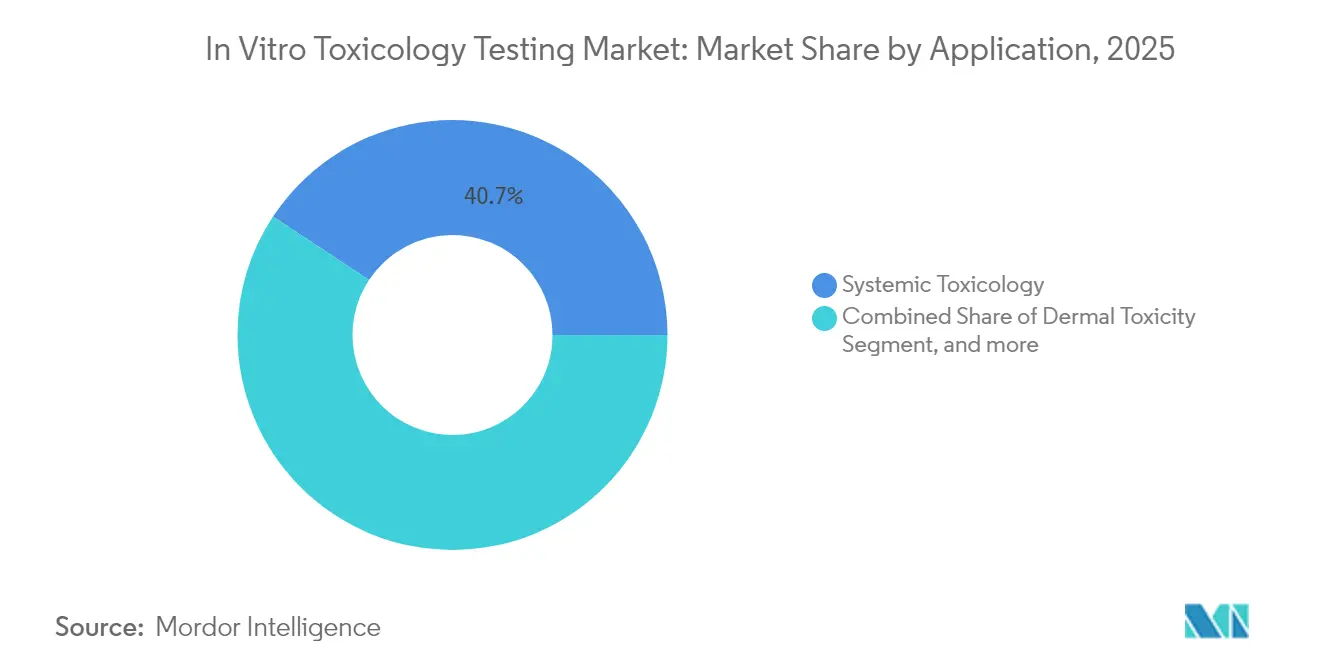
- Par application, la toxicologie systémique représentait 40,72 % de la taille du marché des tests de toxicologie in vitro en 2025, tandis que les tests de perturbation endocrinienne progressent à un CAGR de 12,33 % jusqu'en 2031.
- Par utilisateur final, l'industrie pharmaceutique détenait 47,78 % de la part du marché des tests de toxicologie in vitro en 2025, tandis que le diagnostic est le segment à la croissance la plus rapide avec un CAGR de 12,97 %.
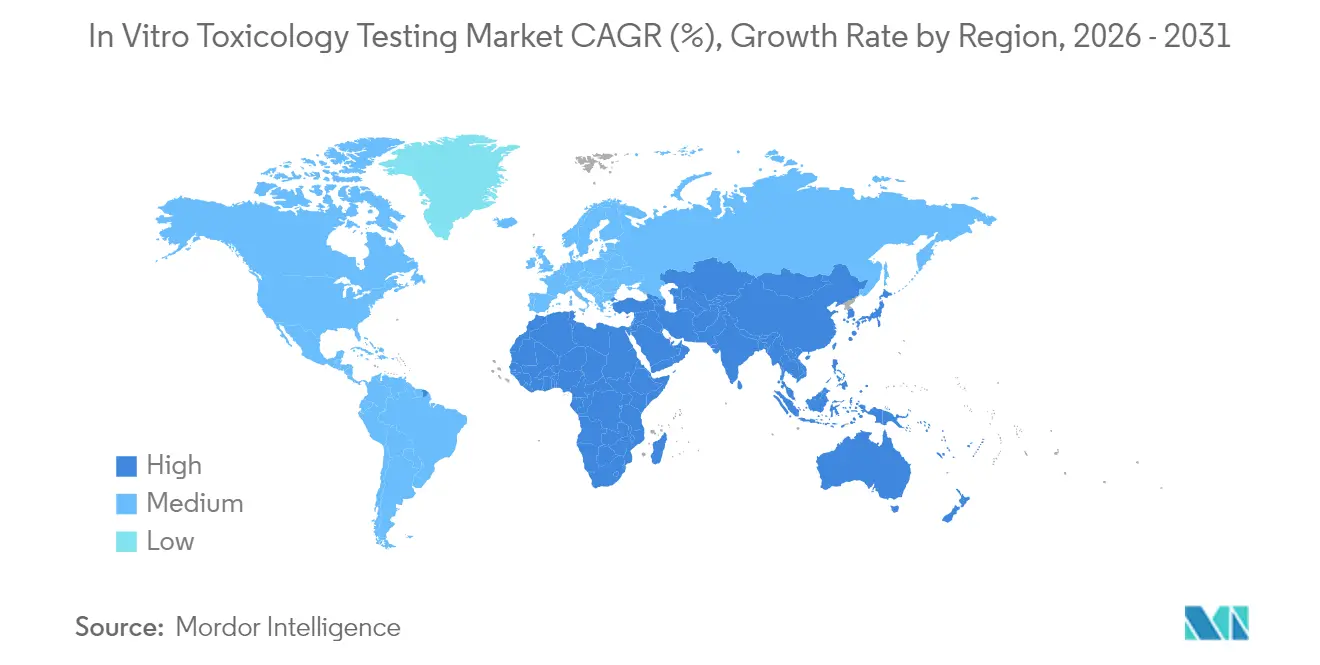
- Par géographie, l'Amérique du Nord a contribué à hauteur de 47,10 % des revenus en 2025 ; l'Asie-Pacifique devrait enregistrer un CAGR de 12,36 % de 2026 à 2031.
Remarque : Les chiffres de la taille du marché et des prévisions de ce rapport sont générés à l’aide du cadre d’estimation propriétaire de Mordor Intelligence, mis à jour avec les données et analyses les plus récentes disponibles en 2026.
Tendances et Perspectives du Marché Mondial des Tests de Toxicologie In Vitro
Analyse de l'Impact des Moteurs*
| Moteur | ( ~ ) % Impact sur les Prévisions de CAGR | Pertinence Géographique | Calendrier d'Impact |
|---|---|---|---|
| Réduction de l'utilisation des animaux dans la recherche préclinique | +3.2% | Europe, Amérique du Nord | Moyen terme (2-4 ans) |
| Développement avancé de dosages in vitro | +2.8% | Amérique du Nord, Europe | Long terme (≥4 ans) |
| Sensibilisation accrue à la sécurité des médicaments | +2.1% | Marchés développés dans le monde entier | Moyen terme (2-4 ans) |
| Adoption de la médecine personnalisée | +1.9% | Mondial | Long terme (≥4 ans) |
| Expansion du criblage à haut débit | +1.6% | Mondial | Moyen terme (2-4 ans) |
| Pression réglementaire en faveur des tests sans animaux | +1.4% | Europe, Amérique du Nord | Court terme (≤2 ans) |
| Source: Mordor Intelligence | |||
Opposition à l'Utilisation des Animaux dans la Recherche Préclinique
La pression éthique et les interdictions réglementaires continuent de supplanter les études animales. La Société de Toxicologie note que la directive européenne stricte sur les cosmétiques et le FDA Modernization Act 2.0 ont légitimé les approches sans animaux.[1]Société de Toxicologie, "Alternatives aux Tests sur les Animaux," toxicology.org À mesure que les entreprises s'alignent sur ces règles, la demande de dosages in vitro validés s'accélère. Les multinationales intègrent désormais des méthodes alternatives dans les dossiers de soumission mondiaux, créant des flux de travail unifiés entre les régions. Cette tendance catalyse également des partenariats public-privé qui partagent des données de référence pour accélérer la validation des dosages. La sensibilisation sociale croissante encourage en outre les investisseurs à privilégier les entreprises proposant des services de test sans cruauté.
Avancées Significatives dans les Dosages de Toxicologie In Vitro
Les percées dans les organoïdes 3D, la microfluidique et l'analyse unicellulaire fournissent des données plus riches et pertinentes pour l'humain. Les modèles microfluidiques de poumon-sur-puce évaluent désormais la toxicité particulaire avec un débit plus élevé que les tests classiques à l'interface air-liquide.[2]Toxicologie Environnementale, "Approches Microfluidiques pour la Toxicité des Particules," environmentaltox.com Combinés à l'imagerie en temps réel et à l'IA, les scientifiques peuvent détecter de subtils changements phénotypiques quelques heures après l'exposition. Ces outils soutiennent la prise de décision réglementaire pour des critères d'évaluation complexes tels que la neurotoxicité développementale, où les modèles rongeurs sont souvent insuffisants. À mesure que les protocoles mûrissent, les organisations de recherche sous contrat intègrent des ensembles de dosages pour fournir des informations mécanistiques complètes, augmentant ainsi leurs revenus par projet.
Sensibilisation Croissante à la Sécurité des Médicaments
Les échecs de toxicité en phase avancée coûtent des milliards au secteur pharmaceutique. Environ 30 % de l'attrition en phase II/III est due à des problèmes de sécurité imprévus.[3]ScienceDirect, "Attrition des Médicaments et Évaluation de la Sécurité," sciencedirect.com En réponse, les entreprises investissent dans des criblages multi-omiques prédictifs qui signalent les risques plus tôt. Les régulateurs encouragent l'intégration des données du monde réel, et les initiatives de médecine de précision s'appuient sur la corrélation génomique-clinique. Ensemble, ces facteurs poussent les commanditaires à adopter des tests in vitro à contenu plus élevé qui réduisent l'incertitude, satisfont les critères d'évaluation des technologies de santé et protègent la réputation de la marque.
Demande Croissante pour la Médecine Personnalisée
Adapter la thérapie nécessite de comprendre le risque de toxicité individuel. L'omique unicellulaire et les organoïdes dérivés de patients révèlent des réponses spécifiques au génotype, permettant des stratégies de dosage sur mesure. Les hôpitaux adoptent des panels de cytotoxicité au point de soin pour surveiller les événements indésirables en temps réel, créant une demande dérivée pour les kits commerciaux. Les acteurs du secteur répondent en co-développant des ensembles diagnostic compagnon-thérapie qui combinent les résultats d'efficacité et de sécurité.
Analyse de l'Impact des Freins*
| Frein | ( ~ ) % Impact sur les Prévisions de CAGR | Pertinence Géographique | Calendrier d'Impact |
|---|---|---|---|
| Modélisation limitée de l'auto-immunité et de l'immunostimulation | −1.8% | Centres de recherche avancée | Court terme (≤2 ans) |
| Voies réglementaires complexes pour les nouveaux dosages | −1.4% | Amérique du Nord, Europe | Moyen terme (2-4 ans) |
| Précision prédictive incomplète pour les toxicités systémiques | −1.2% | Mondial | Long terme (≥4 ans) |
| Difficultés de gestion et d'intégration des données | −1.0% | Mondial | Moyen terme (2-4 ans) |
| Source: Mordor Intelligence | |||
Incapacité des Modèles In Vitro à Déterminer l'Auto-immunité et l'Immunostimulation
Même les tissus 3D sophistiqués manquent de complexité immunitaire complète. AzoBioSciences souligne que les organoïdes sans composants vasculaires et lymphoïdes peinent à prédire les tempêtes de cytokines. Les développeurs de produits biologiques complètent donc encore les dosages par des études in vivo. Les systèmes multi-organes-sur-puce émergents sont prometteurs, mais la reproductibilité et la validation réglementaire restent des défis permanents, retardant l'adoption généralisée.
Cadre Réglementaire Strict pour les Tests In Vitro
La règle de la FDA de 2024 classifiant les tests développés en laboratoire comme dispositifs médicaux impose des obligations de contrôle de conception, de qualité et de surveillance post-commercialisation. Les petits innovateurs font face à des contraintes de ressources lors de la compilation des preuves de performance. L'absence de normes mondiales harmonisées complique davantage les approbations multi-régions, ralentissant le retour sur investissement pour les nouvelles plateformes. Les régulateurs signalent toutefois leur volonté d'accélérer l'approbation des dosages bien conçus et spécifiques au contexte d'utilisation.
*Nos prévisions mises à jour traitent les impacts des moteurs et des freins comme directionnels et non additifs. Les prévisions d’impact révisées reflètent la croissance de base, les effets de mix et les interactions entre variables.
Analyse des Segments
Par Technologie : Les Perspectives au Niveau Moléculaire Stimulent l'Adoption
La culture cellulaire a conservé la plus grande part à 43,35 % du marché des tests de toxicologie in vitro en 2025, bénéficiant de protocoles éprouvés et d'une large familiarité des utilisateurs. La force du segment réside dans sa polyvalence pour les criblages exploratoires, les dosages de puissance et les soumissions réglementaires. La taille du marché des tests de toxicologie in vitro pour les applications de Culture Cellulaire devrait rester supérieure à 9,12 milliards USD d'ici 2031, les améliorations telles que les lignées éditées par CRISPR et l'imagerie assistée par IA ouvrant de nouvelles perspectives mécanistiques. Les constructions 3D émergentes émulent davantage les organes humains, réduisant les faux négatifs souvent observés avec les monocouches bidimensionnelles.
Les approches OMICS, couvrant la transcriptomique, la protéomique et la métabolomique, ont enregistré le CAGR le plus rapide à 13,61 % jusqu'en 2031. La baisse rapide des coûts de séquençage et les avancées dans l'analyse unicellulaire élargissent l'adoption parmi les entreprises pharmaceutiques, biotechnologiques et académiques. L'intégration de couches multi-omiques offre des signatures toxicologiques au niveau des systèmes qui complètent les criblages phénotypiques, positionnant les OMICS comme pierre angulaire des pipelines de sécurité de nouvelle génération. À mesure que les ensembles de données s'élargissent, les modèles d'apprentissage automatique entraînés sur des empreintes OMICS affinent les relations structure-activité et prédisent plus tôt les toxicités idiosyncrasiques dans la découverte de médicaments.
Par Méthode : Les Modèles Numériques Progressent, les Dosages Classiques Persistent
Les dosages cellulaires représentaient 35,72 % de la part du marché des tests de toxicologie in vitro en 2025. Les systèmes rapporteurs fluorescents et la microscopie automatisée fournissent des données quantitatives sur l'apoptose, le stress oxydatif et les dommages à l'ADN, soutenant les soumissions de qualité réglementaire. Parallèlement, les techniques in silico devraient générer l'incrément de revenus le plus élevé, propulsées par des plateformes d'apprentissage automatique basées sur le cloud qui criblent des bibliothèques virtuelles à un coût incrémental minimal.
La taille du marché des tests de toxicologie in vitro pour les outils in silico croît à un CAGR de 14,03 % entre 2026 et 2031, portée par la rationalisation des portefeuilles pharmaceutiques et l'acceptation réglementaire des preuves computationnelles riches en données. Les dosages biochimiques et les préparations ex vivo continuent de répondre à des questions spécifiques aux voies et servent d'outils de transition pour les critères d'évaluation complexes où les modèles prédictifs manquent de validation.
Par Application : La Sécurité Hormonale sous les Projecteurs
La toxicologie systémique est restée le principal cas d'utilisation, contribuant à 40,72 % du chiffre d'affaires total en 2025. Les modèles intégrés du foie, des reins et du cœur permettent des lectures multi-organes simultanées, rationalisant les dossiers réglementaires pour les nouvelles entités chimiques.
En revanche, les tests de perturbation endocrinienne ont affiché le CAGR le plus rapide à 12,33 % face aux préoccupations croissantes concernant les polluants à activité hormonale. Les autorités européennes financent des projets tels qu'ENDpoiNTs pour affiner les dosages prédictifs intégrant les différences entre espèces et entre sexes. L'examen accru des ingrédients à activité endocrinienne dans les plastiques, les pesticides et les cosmétiques pousse le secteur à adopter des panels sensibles de liaison aux récepteurs et d'expression génique qui détectent de subtiles perturbations hormonales bien avant l'apparition de changements phénotypiques manifestes.
Par Utilisateur Final : Le Diagnostic s'Accélère, le Pharmaceutique Domine
Les entreprises pharmaceutiques ont conservé 47,78 % de part, ancrant les budgets de toxicologie de la découverte aux phases cliniques. La complexité accrue des pipelines et le virage vers les produits biologiques sollicitent les modèles traditionnels, alimentant la demande de plateformes in vitro avancées.
Pendant ce temps, le Diagnostic affiche la dynamique la plus rapide à un CAGR de 12,97 % alors que les hôpitaux mettent en œuvre des tests de cytotoxicité développés en laboratoire pour protéger les régimes personnalisés. Les organisations de recherche sous contrat saisissent cette opportunité en associant la toxicologie à la génomique et à la bioinformatique pour offrir des services clés en main, tandis que les institutions académiques restent essentielles dans les étapes d'invention des méthodes et de validation précoce.
Analyse Géographique
L'Amérique du Nord a dominé le marché des tests de toxicologie in vitro avec 47,10 % des revenus en 2025, soutenue par le financement de la FDA pour les méthodes alternatives et des dépenses élevées en R&D par habitant. La taille du marché des tests de toxicologie in vitro aux États-Unis est portée par l'adoption rapide de plateformes à haut débit guidées par l'IA et un environnement de remboursement favorable pour les diagnostics avancés. La clarté réglementaire autour des tests développés en laboratoire, bien que stricte, signale l'approbation officielle des technologies in vitro validées.
L'Asie-Pacifique est la région à la croissance la plus rapide, avec un CAGR prévu de 12,36 % de 2026 à 2031. Les multinationales établissent des pôles d'innovation régionaux pour exploiter le vaste bassin de patients et le vivier de talents rentable. Ces facteurs élèvent collectivement la demande locale de solutions de sécurité prédictives répondant aux critères réglementaires mondiaux.
L'Europe occupe une solide deuxième place, renforcée par des interdictions strictes des tests sur les animaux et des directives progressives sur la sécurité chimique. La feuille de route de la Commission européenne de novembre 2024 visant à éliminer les études animales propulse l'adoption précoce des dosages organe-sur-puce et multi-omiques. Les consortiums régionaux standardisent les voies de validation, offrant aux entreprises des voies de soumission plus fluides. Pendant ce temps, les marchés émergents d'Amérique du Sud et du Moyen-Orient et Afrique connaissent une adoption régulière à mesure que l'infrastructure de santé et les cadres de pharmacovigilance mûrissent, présentant des perspectives de croissance à long terme pour les fournisseurs de kits de test et les prestataires de services.
Paysage Concurrentiel
Le marché présente une concentration modérée, avec un mélange de conglomérats diversifiés des sciences de la vie, d'organisations de recherche sous contrat de taille moyenne et de start-ups agiles. Les acteurs établis élargissent leur offre de services par acquisition : l'achat en avril 2025 par Eurofins Scientific d'un laboratoire spécialisé dans les tests de perturbation endocrinienne élargit ses capacités de niche. Le lancement en janvier 2025 par Thermo Fisher d'un système de criblage automatisé renforce son offre groupée matériel-service, attirant les clients à la recherche de plateformes unifiées. Ces mouvements signalent un virage vers des offres verticalement intégrées couvrant la génération de données, l'analyse et le reporting réglementaire.
Les partenariats stratégiques entre spécialistes de l'IA et développeurs de dosages redéfinissent la dynamique concurrentielle. La fusion de Recursion et Exscientia vise à créer un moteur de découverte de médicaments par IA à grande échelle intégrant la prédiction de toxicité dès le premier jour. Les petites entreprises répliquent en se concentrant sur des domaines inexploités, notamment la neurotoxicité développementale et l'immunotoxicité, proposant des modèles haute fidélité que les acteurs établis ne possèdent pas. La pression sur les prix s'intensifie à mesure que l'automatisation réduit les coûts par échantillon, mais les fournisseurs se différencient par la qualité des données, les délais d'exécution et l'expertise consultative.
Les portefeuilles de propriété intellectuelle centrés sur la conception microfluidique, les algorithmes d'imagerie et l'analyse multi-omique deviennent des actifs critiques. Les entreprises exploitent ces brevets pour négocier des accords exclusifs avec les grandes entreprises pharmaceutiques, sécurisant des revenus récurrents grâce à des contrats de services-cadres pluriannuels. Dans l'ensemble, la concurrence repose désormais moins sur la capacité et davantage sur la validité scientifique et l'acceptation réglementaire des modèles avancés pertinents pour l'humain.
Leaders du Secteur des Tests de Toxicologie In Vitro
Charles River Laboratories International Inc.
Thermo Fisher Scientific Inc.
Eurofins Scientific SE
Merck KGaA
Agilent Technologies Inc.
- *Avis de non-responsabilité : les principaux acteurs sont triés sans ordre particulier


Développements Récents du Secteur
- Mai 2025 : Cocrystal Pharma a annoncé des avancées significatives dans le développement de ses médicaments antiviraux, son inhibiteur oral pan-viral de protéase CDI-988 démontrant une activité in vitro supérieure contre les souches de norovirus, soulignant le rôle critique des tests in vitro dans le développement thérapeutique.
- Avril 2025 : Eurofins Scientific a élargi ses capacités de tests de toxicologie in vitro par l'acquisition d'un laboratoire spécialisé dans les tests de perturbation endocrinienne, renforçant sa position dans ce segment d'application en croissance rapide.
- Février 2025 : Charles River Laboratories a dévoilé une plateforme avancée de culture cellulaire 3D pour l'évaluation de l'hépatotoxicité, intégrant une analyse d'images pilotée par IA pour améliorer la détection de subtils changements cellulaires indicatifs de la toxicité hépatique.
- Janvier 2025 : Thermo Fisher Scientific a lancé un nouveau système de criblage à haut débit spécialement conçu pour les applications de toxicologie in vitro, permettant l'évaluation simultanée de multiples critères de toxicité sur des milliers de composés.
Portée du Rapport sur le Marché Mondial des Tests de Toxicologie In Vitro
Les tests de toxicité in vitro désignent la méthode d'analyse scientifique des effets de substances chimiques létales ou toxiques sur des cellules de mammifères ou des bactéries en culture. Les méthodes de test in vitro sont réalisées principalement dans le but d'identifier des substances chimiques potentiellement nocives et/ou de confirmer l'absence de certaines propriétés toxiques aux stades initiaux du développement de nouvelles substances potentiellement utiles, notamment les médicaments thérapeutiques, les produits chimiques agricoles et même les additifs alimentaires.
| Culture Cellulaire |
| Haut Débit |
| Imagerie Moléculaire |
| OMICS |
| Culture Cellulaire 3D et Organoïdes |
| Dosage Cellulaire |
| Dosage Biochimique |
| In Silico |
| Ex Vivo |
| Toxicologie Systémique |
| Toxicité Dermique |
| Perturbation Endocrinienne |
| Toxicité Oculaire |
| Autres Applications |
| Industrie Pharmaceutique |
| Biotechnologie et Organisations de Recherche sous Contrat |
| Diagnostic |
| Instituts Académiques et de Recherche |
| Amérique du Nord | États-Unis |
| Canada | |
| Mexique | |
| Europe | Allemagne |
| Royaume-Uni | |
| France | |
| Italie | |
| Espagne | |
| Reste de l'Europe | |
| Asie-Pacifique | Chine |
| Japon | |
| Inde | |
| Australie | |
| Corée du Sud | |
| Reste de l'Asie-Pacifique | |
| Moyen-Orient et Afrique | CCG |
| Afrique du Sud | |
| Reste du Moyen-Orient et Afrique | |
| Amérique du Sud | Brésil |
| Argentine | |
| Reste de l'Amérique du Sud |
| Par Technologie | Culture Cellulaire | |
| Haut Débit | ||
| Imagerie Moléculaire | ||
| OMICS | ||
| Culture Cellulaire 3D et Organoïdes | ||
| Par Méthode | Dosage Cellulaire | |
| Dosage Biochimique | ||
| In Silico | ||
| Ex Vivo | ||
| Par Application | Toxicologie Systémique | |
| Toxicité Dermique | ||
| Perturbation Endocrinienne | ||
| Toxicité Oculaire | ||
| Autres Applications | ||
| Par Utilisateur Final | Industrie Pharmaceutique | |
| Biotechnologie et Organisations de Recherche sous Contrat | ||
| Diagnostic | ||
| Instituts Académiques et de Recherche | ||
| Par Géographie | Amérique du Nord | États-Unis |
| Canada | ||
| Mexique | ||
| Europe | Allemagne | |
| Royaume-Uni | ||
| France | ||
| Italie | ||
| Espagne | ||
| Reste de l'Europe | ||
| Asie-Pacifique | Chine | |
| Japon | ||
| Inde | ||
| Australie | ||
| Corée du Sud | ||
| Reste de l'Asie-Pacifique | ||
| Moyen-Orient et Afrique | CCG | |
| Afrique du Sud | ||
| Reste du Moyen-Orient et Afrique | ||
| Amérique du Sud | Brésil | |
| Argentine | ||
| Reste de l'Amérique du Sud | ||


Questions Clés Répondues dans le Rapport
Quelle est la taille actuelle du marché des tests de toxicologie in vitro ?
La taille du marché des tests de toxicologie in vitro s'élève à 14,43 milliards USD en 2026 et devrait atteindre 23,76 milliards USD d'ici 2031.
Quel segment technologique connaît la croissance la plus rapide ?
Les plateformes basées sur les OMICS mènent la croissance avec un CAGR projeté de 13,61 % jusqu'en 2031, car elles fournissent des informations moléculaires complètes et une détection plus précoce de la toxicité.
Pourquoi l'Amérique du Nord domine-t-elle ce marché ?
Les réglementations strictes de la FDA soutenant les méthodes alternatives, les dépenses élevées en R&D et l'adoption rapide des systèmes à haut débit guidés par l'IA confèrent à l'Amérique du Nord une part de revenus de 47,10 %.
Qu'est-ce qui freine le remplacement complet des tests sur les animaux ?
Les modèles in vitro actuels peinent à reproduire l'auto-immunité et l'immunostimulation systémique, nécessitant quelques études in vivo complémentaires pour les produits biologiques complexes.
Comment l'IA améliore-t-elle les tests de toxicologie ?
Les algorithmes d'IA analysent les données multi-omiques et d'imagerie, prédisent plus tôt les risques de toxicité et optimisent la sélection des composés, réduisant les délais et les coûts de développement.
Quel segment d'utilisateurs finaux se développe le plus rapidement ?
Le Diagnostic progresse à un CAGR de 12,97 % alors que les hôpitaux intègrent les dosages de toxicité dans la surveillance des traitements personnalisés.
Dernière mise à jour de la page le:











