Tamaño y Participación del Mercado de Cultivo Celular 3D
Análisis del Mercado de Cultivo Celular 3D por Mordor Intelligence
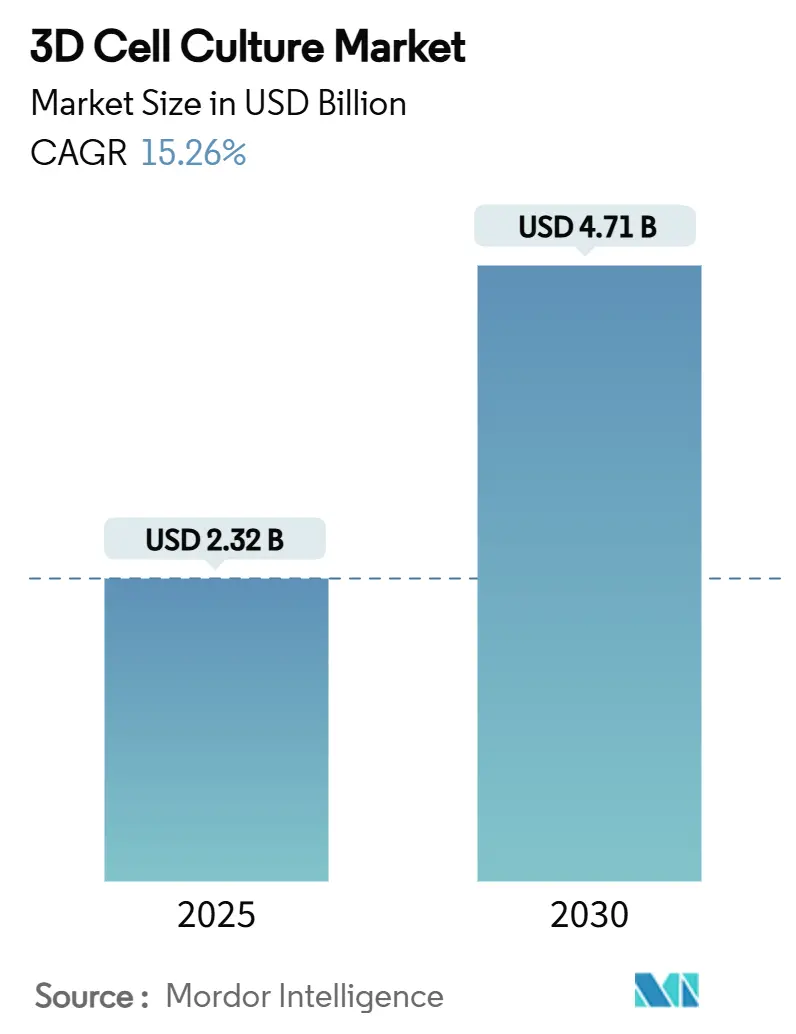
El tamaño del mercado de cultivo celular 3D está valorado en USD 2,32 mil millones en 2025 y se pronostica que alcance USD 4,71 mil millones en 2030, avanzando a una TCAC del 15,26% durante 2025-2030. América del Norte mantiene el liderazgo debido a pipelines farmacéuticos profundos, abundante financiación de capital de riesgo y el estímulo de la FDA de ensayos sin animales. Asia-Pacífico muestra la trayectoria más pronunciada ya que los gobiernos incorporan la biotecnología en las políticas industriales nacionales y expanden los clústeres de medicina traslacional. Los formatos basados en andamiaje aún dominan debido a protocolos listos para usar, sin embargo, los dispositivos microfluídicos de órgano en chip están escalando más rápido ya que reproducen la comunicación cruzada tejido-tejido y el cizallamiento impulsado por flujo esencial para el cribado de toxicidad confiable. Los complementos de inteligencia artificial que automatizan el análisis de imágenes y las lecturas multi-ómicas están convirtiendo los sistemas de cultivo 3D en motores de descubrimiento de alto contenido, cerrando las brechas históricas de datos entre el laboratorio y la clínica.
Conclusiones Clave del Informe
- Por tecnología, las plataformas basadas en andamiaje lideraron con una participación del 48,9% del mercado de cultivo celular 3D en 2024. Los sistemas microfluídicos de órgano en chip están avanzando a una TCAC del 18,9% hasta 2030.
- Por aplicación, la investigación del cáncer capturó el 45% de la participación del mercado de cultivo celular 3D en 2024. La medicina regenerativa se está expandiendo a una TCAC del 17,2% hasta 2030.
- Por usuario final, las empresas biotecnológicas y farmacéuticas mantuvieron el 46,8% del mercado de cultivo celular 3D en 2024. Se proyecta que las CRO y CDMO crezcan a una TCAC del 16,5% entre 2025-2030.
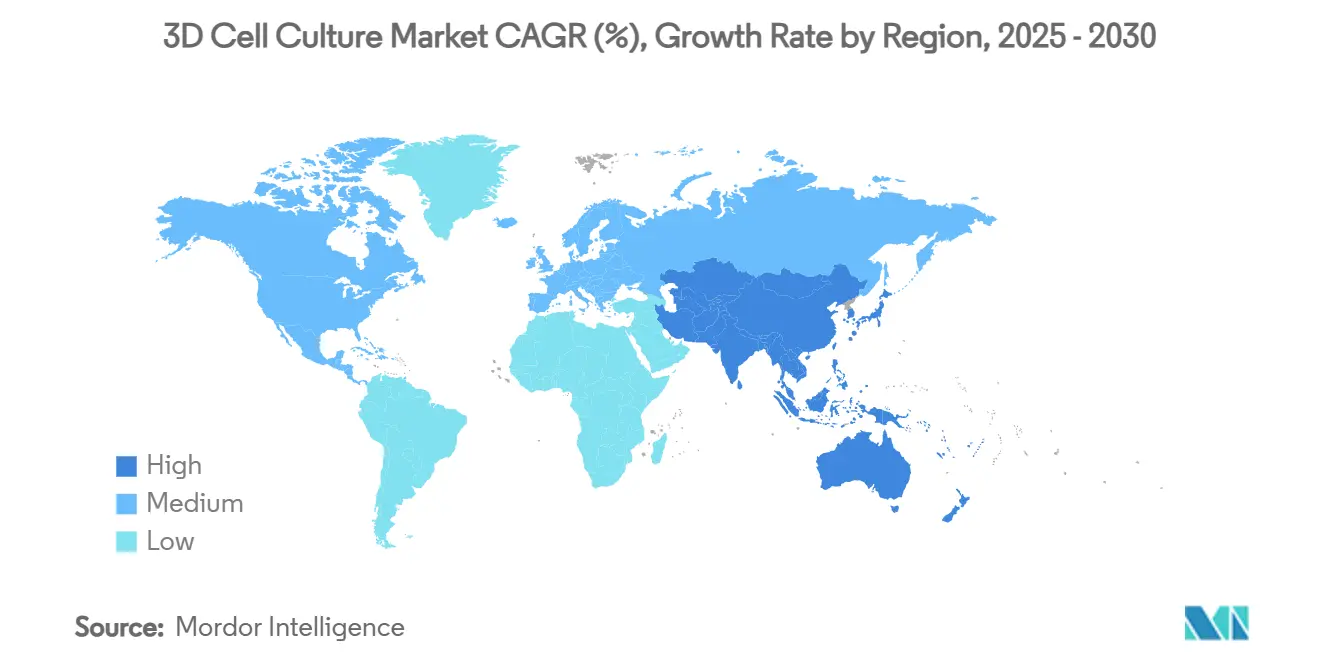
- Por geografía, América del Norte controló el 42% del mercado global de cultivo celular 3D en 2024. Se predice que Asia-Pacífico registre una TCAC del 16,8% hasta 2030.
Tendencias e Insights del Mercado Global de Cultivo Celular 3D
Análisis de Impacto de Factores Impulsores
| Factor Impulsor | (~) % Impacto en Pronóstico TCAC | Relevancia Geográfica | Cronología de Impacto |
|---|---|---|---|
| Demanda de modelos preclínicos fisiológicamente relevantes | +4.2% | América del Norte, Europa | Mediano plazo (2-4 años) |
| Aumento de inversión en medicina regenerativa y personalizada | +3.8% | América del Norte, Europa, Japón, Corea del Sur | Largo plazo (≥4 años) |
| Presión regulatoria para reemplazar las pruebas en animales | +3.1% | Europa, América del Norte, Asia-Pacífico | Mediano plazo (2-4 años) |
| Avances rápidos en materiales de andamiaje y biotintas | +2.5% | Global | Corto plazo (≤2 años) |
| Asociaciones llave en mano Farmacéutica-CRO | +1.7% | América del Norte, Europa, China, India | Corto plazo (≤2 años) |
| Fuente: Mordor Intelligence | |||
Expansión de la Demanda de Modelos Pre-clínicos Fisiológicamente Relevantes para Reducir Fallas de Fármacos en Etapa Tardía
El 90% de atrición de candidatos a fármacos en fase II y fase III ha hecho de la fidelidad predictiva un imperativo de I+D. Los tejidos tridimensionales que recapitulan la rigidez de la matriz extracelular, los gradientes de oxígeno y las interacciones multicelulares producen firmas de toxicidad frecuentemente perdidas en placas 2D. La Ley de Modernización de la FDA 3.0 ahora permite presentaciones de fármacos en investigación nuevos ancladas en datos sin animales, acelerando los ciclos de validación corporativa. Los organoides bioimprimidos derivados de pacientes permiten la estratificación en tiempo real de respondedores y no respondedores, reduciendo los costosos rediseños de ensayos. Los equipos farmacéuticos que desplegaron matrices de hígado en chip reportaron una caída del 30% en el retiro de candidatos relacionado con hepatotoxicidad en las presentaciones de 2024. Juntas, estas mejoras reducen el riesgo clínico y justifican un mayor gasto inicial en plataformas de cultivo avanzadas.
Escalada de Inversión Global en Medicina Regenerativa y Personalizada Acelerando la Adopción de Cultivo 3D
El capital privado y público dirigido a terapéuticas regenerativas excedió USD 30 mil millones globalmente en 2025, con el 35% destinado a kits de herramientas de ingeniería de tejidos. Debido a que los implantes autólogos demandan microambientes específicos del paciente, las empresas integran bioimpresión 3D con células madre pluripotentes inducidas para fabricar injertos inmuno-compatibles. La Fundación Nacional de Ciencias Naturales de China duplicó las subvenciones para parches de órganos basados en hidrogel, estimulando a proveedores domésticos de biotintas. Las inversiones paralelas en organoides editados con CRISPR están creando planos preclínicos para trastornos monogénicos una vez considerados intratables. Estos flujos de trabajo traslacionales dependen de químicas de andamiaje personalizables y biorreactores de perfusión, incorporando hardware de cultivo 3D en el núcleo de las cadenas de valor de medicina de precisión.
Intensificación de la Presión Regulatoria y Ética para Reemplazar las Pruebas en Animales en Cosméticos y Farmacia
La prohibición total de la directiva de cosméticos de la UE sobre pruebas en animales junto con las actualizaciones de REACH obliga a los fabricantes a obtener pipelines de toxicología alternativos. ISO, CEN y ASTM están estandarizando la terminología de órgano en chip, calibración de sensores y reportes de endpoints, proporcionando así a los reguladores una lista de verificación robusta para la presentación de expedientes[1]Joint Research Centre, "Setting Out a Roadmap for Standardisation of Organ-on-Chip Technology," ec.europa.eu. El Ministerio de Seguridad Alimentaria y de Medicamentos de Corea emitió una guía en 2025 permitiendo ensayos de piel en chip como pantallas de irritación independientes. Los modelos epidérmicos microfluídicos basados en papel reducen los costos consumibles en un 40% y se ajustan dentro de configuraciones de imágenes de alto rendimiento existentes. Cuando convergen las fechas límite de cumplimiento, se intensifica la demanda de construcciones 3D listas para validar que acorten la preparación de expedientes y reduzcan el riesgo de litigio relacionado con el bienestar animal.
Avances Rápidos en Materiales de Andamiaje y Biotintas Permitiendo Producción 3D a Escala Comercial
Los hidrogeles de próxima generación utilizan secuencias de péptidos modulares que regulan la rigidez, degradación y motivos de adhesión celular, permitiendo a los científicos adaptar matrices a fenotipos cardíacos, hepáticos o neurales sin reconfigurar instalaciones. Los andamiajes híbridos que combinan polietilenglicol con colágeno aumentan la resistencia a la tracción tres veces mientras mantienen baja inmunogenicidad, soportando cultivos de perfusión a largo plazo. Los biomateriales inteligentes que liberan factores de crecimiento en respuesta a pH o desencadenantes enzimáticos permiten control temporal de las vías de diferenciación. Acoplados con bioimpresoras de extrusión de bajo costo, estos materiales impulsan el rendimiento volumétrico a niveles compatibles con la fabricación por lotes de bibliotecas de esferoides para campañas de cribado. Los proveedores que escalan cartuchos de hidrogel liofilizado reportan costos operativos 25% más bajos versus mezclas personalizadas, eliminando una barrera económica clave para laboratorios de tamaño medio.
Análisis de Impacto de Restricciones
| Restricción | (~) % Impacto en Pronóstico TCAC | Relevancia Geográfica | Cronología de Impacto |
|---|---|---|---|
| Altos costos de capital y operación | -2.8% | Global (más fuerte en mercados emergentes) | Corto plazo (≤2 años) |
| Falta de estándares de validación armonizados | -2.3% | Global | Mediano plazo (2-4 años) |
| Escasez de talento técnico especializado | -1.5% | Asia-Pacífico, América Latina, MEA | Mediano plazo (2-4 años) |
| Fuente: Mordor Intelligence | |||
Altos Costos de Capital y Operación de Plataformas de Cultivo 3D Avanzadas vs. Sistemas 2D Convencionales
Las plataformas comerciales de órgano en chip controladas por flujo se listan entre USD 80.000 y USD 150.000, eclipsando el punto de entrada de USD 15.000 para incubadores 2D apilables. Los gastos operativos aumentan aún más una vez que se incluyen bombas microfluídicas, sensores en línea y captura de imágenes multiplex. Los institutos más pequeños posponen las actualizaciones, limitando la penetración regional en América del Sur y África. Los fabricantes están respondiendo con chips modulables producidos en impresoras de estereolitografía de escritorio, reduciendo los costos por ejecución en un 35%[2]Dasgupta I. et al., "Microfluidic Organ-on-Chip Technology," mdpi.com. Los acuerdos de suministro a granel para resinas fotocurables y software de control de código abierto reducen los gastos de propiedad y podrían neutralizar la restricción dentro de dos ciclos presupuestarios para muchos laboratorios.
Falta de Estándares Globales Armonizados para Validación y Reproducibilidad
Los formatos de reporte divergentes impiden la agrupación de datos entre sitios y complican las presentaciones regulatorias que abarcan jurisdicciones. El Centro de Investigación Conjunta de la Comisión Europea publicó una hoja de ruta de 2025 que describe materiales de referencia, endpoints de viabilidad y pruebas en anillo inter-laboratorio para sistemas de órgano en chip. El Instituto Nacional de Estándares y Tecnología de EE.UU. está coordinando con ISO TC 276 para unificar la terminología sobre integridad de barrera y cizallamiento fluídico. Hasta que los protocolos de consenso alcancen madurez, los patrocinadores deben sufragar estudios de verificación extra para satisfacer a los reguladores nacionales, inflando los cronogramas de proyectos. La situación debería aliviarse cuando los estándares de primera ola se conviertan en métodos compendiosos reconocidos para 2027.
Análisis de Segmentos
Por Tecnología: La Microfluídica Reforma las Plataformas Establecidas
Las plataformas de andamiaje mantuvieron una porción del 48,9% de la participación del mercado de cultivo celular 3D en 2024 y permanecieron indispensables para cultivos a largo plazo que requieren mimetismo de matriz extracelular. Esta categoría heredada se benefició de décadas de protocolos publicados, lo que facilitó la validación dentro de sistemas de calidad regulados. Sin embargo, el subsegmento microfluídico de órgano en chip está superando a todos los rivales con una TCAC del 18,9% ligada a su capacidad para flujo laminar, ventanas de imágenes en tiempo real y redes multi-órgano que desbloquean farmacocinética traslacional. Los proveedores están integrando flujo por gravedad libre de bombas peristálticas y válvulas acopladas magnéticamente, recortando el tiempo de inactividad por mantenimiento y aumentando la reproducibilidad del experimento. Un impulso adicional proviene de sensores conectados a la nube que transmiten flujo metabólico a modelos de aprendizaje automático, convirtiendo imágenes sin procesar en curvas dosis-respuesta en minutos en lugar de días. Esta eficiencia resuena con equipos de descubrimiento presionados por cronogramas de hitos agresivos, alentando la sustitución de insertos de hidrogel estáticos. A medida que los costos caen, se proyecta que el tamaño del mercado de cultivo celular 3D para microfluídica duplique su línea base de 2024 antes de 2029 sin canibalizar toda la demanda de andamiaje, porque los protocolos híbridos mezclan gotas de hidrogel dentro de chips para simular compartimentos estromales.
Los generadores de esferoides libres de andamiaje aprovechan fuerzas acústicas o magnéticas para ensamblar agregados celulares, apelando a grupos de cribado de alto rendimiento que necesitan rendimiento de 384 pocillos. Las estaciones de trabajo de bioimpresión 3D, una vez confinadas a departamentos de ingeniería, ahora se envían con recintos de grado GMP, posicionando la tecnología para fabricación comercial de tejido autólogo. Los biorreactores casados con sensores de perfusión entregan gradientes de nutrientes homogéneos requeridos para construcciones de tejido a escala de mililitros dirigidas a la fabricación de terapia celular. Los proveedores de servicios que ofrecen diseño de modelo de pila completa, validación e interpretación de datos compiten en velocidad de respuesta y profundidad de anotación molecular, una diferenciación que resuena con firmas biotecnológicas pequeñas con capacidades internas delgadas. Colectivamente, estos avances tecnológicos expanden la base de usuarios direccionable y consolidan el cultivo 3D como un elemento básico en lugar de un complemento exploratorio.
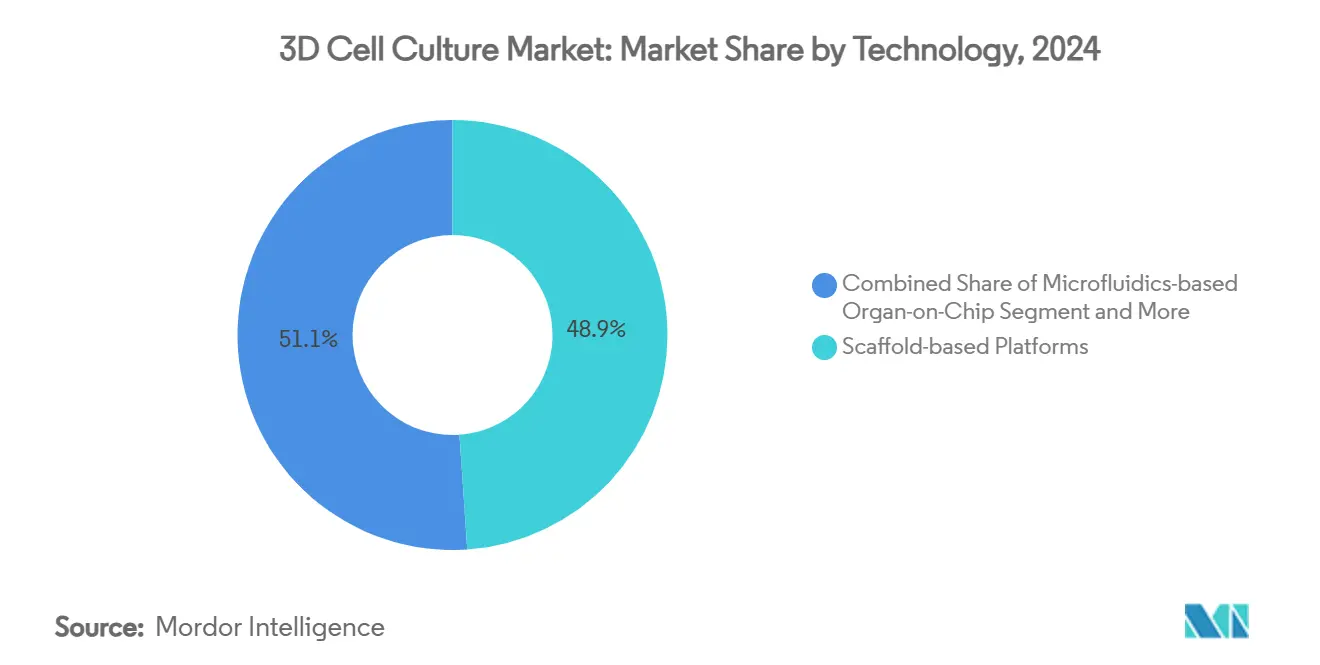
Nota: Participaciones de segmento de todos los segmentos individuales disponibles con la compra del informe
Por Aplicación: La Oncología Personalizada Impulsa la Innovación
La investigación del cáncer capturó el 45% del gasto total en 2024 porque los organoides tumorales heterotípicos revelan mecanismos de resistencia enmascarados en ensayos de monocapa. Los gradientes hipóxicos y co-cultivos de células inmunes dentro de matrices 3D permiten el cribado de inhibidores de puntos de control y transferencias de células adoptivas contra nichos de micro-tumores. La correlación positiva entre las respuestas a fármacos de organoides derivados de pacientes y los resultados clínicos alcanzó el 85% en estudios de validación de 2024, subrayando el valor traslacional. Consecuentemente, los grupos de oncología reasignan presupuesto de xenoinjertos murinos a matrices de chips de tumores de alto rendimiento, acelerando la priorización de candidatos.
Los flujos de trabajo de medicina regenerativa y terapéuticas personalizadas avanzan a una TCAC del 17,2% porque los andamiajes 3D guían decisiones de destino de células madre que los sustratos 2D no pueden soportar. Los parches de cartílago diseñados alcanzaron hitos de implantación en humanos por primera vez en ensayos de 2025, impulsados por gradientes de rigidez zonal logrados solo a través de impresión 3D. Más allá de usos terapéuticos, los organoides hepáticos y neurales entregan modelos de enfermedad para trastornos raros, atrayendo desarrolladores de fármacos huérfanos que necesitan sistemas de ensayo limitados pero mecánicamente ricos. Los laboratorios de descubrimiento de fármacos y toxicología aprecian que las construcciones 3D entregan concordancia cuatro veces mayor con bases de datos de eventos adversos que los cultivos planos, reduciendo la atrición en series químicas de alto valor. Las pruebas cosméticas y de virología son nichos pequeños pero en aumento, especialmente cuando la legislación impulsa alternativas animales y los brotes destacan la necesidad de modelos de infección relevantes para tejido humano.
Por Usuario Final: El Compromiso de CRO Se Dispara
Las empresas biotecnológicas y farmacéuticas consumieron el 46,8% de todos los pedidos de 2024 porque la economía de las fallas en etapa tardía justifica el gasto premium. Su adopción interna se aceleró después de que las promesas ESG corporativas incorporaron objetivos de reducción de animales. Sin embargo, las CRO y CDMO registran la tasa de crecimiento más alta del 16,5% porque agregan hardware especializado y personal multidisciplinario, amortizando costos entre muchos patrocinadores. Las alianzas estratégicas permiten a los clientes farmacéuticos externalizar el desarrollo de métodos, liberando científicos internos para tareas de optimización de candidatos. Los institutos académicos y de investigación siguen siendo crisoles de innovación, impulsando químicas de hidrogel novedosas y modalidades analíticas que luego migran a kits comerciales. Los hospitales y centros de diagnóstico pilotean programas de organoides derivados de pacientes que informan la selección terapéutica en casos refractarios, sugiriendo un futuro donde las estaciones de cultivo en el punto de atención ingresan a laboratorios de patología clínica. El modelo de negocio híbrido servicio-más-hardware que sustenta muchas startups convierte los gastos de capital en gastos operacionales que se alinean con las normas de presupuestación de CFO, alentando un compromiso más amplio.
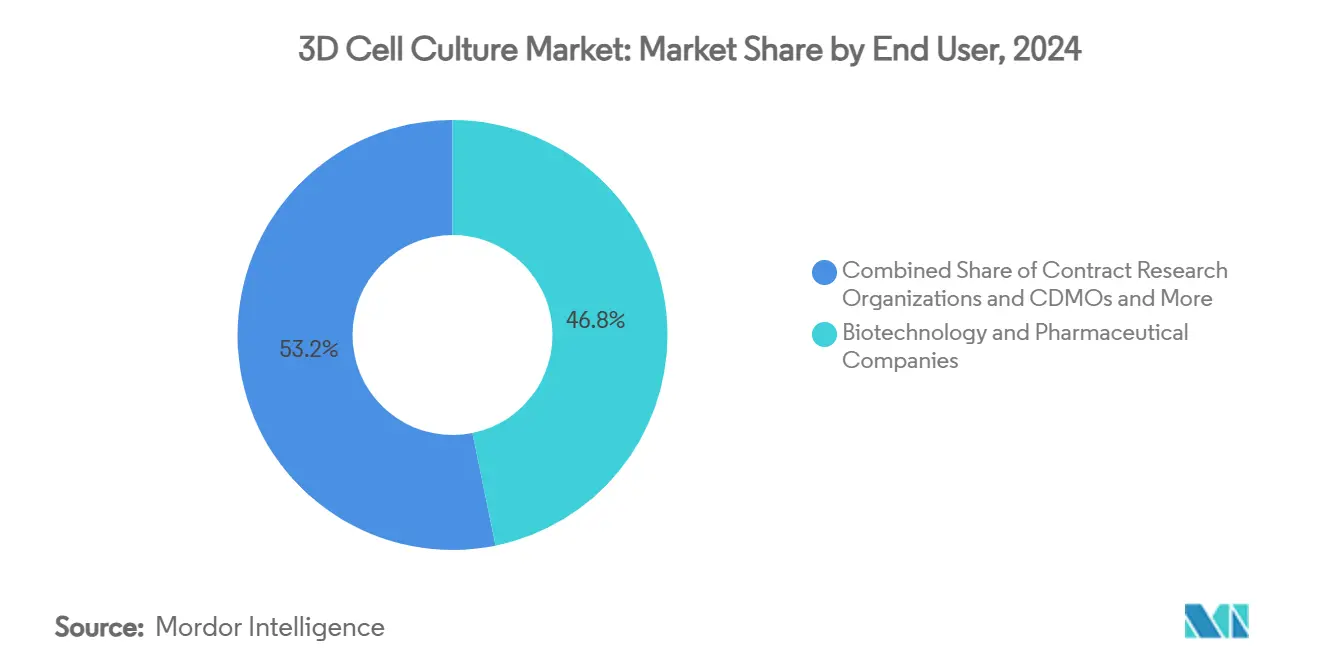
Nota: Participaciones de segmento de todos los segmentos individuales disponibles con la compra del informe
Análisis Geográfico
América del Norte representó el 42% de los ingresos globales en 2024, respaldada por subvenciones traslacionales del NIH, profundidad de capital de riesgo y vías aceleradas de la FDA para datos sin animales. Los laboratorios de Estados Unidos acumularon el 85% de la facturación regional, particularmente dentro de clústeres de Massachusetts y California que concentran innovadores de órgano en chip y proveedores de secuenciación. Canadá y México aumentaron los fondos para incubadoras biotecnológicas, ampliando el acceso de usuarios y complementando los flujos de importación de consumibles.
Europa se ubicó en segundo lugar y fortaleció el crecimiento a través de prohibiciones estrictas de pruebas en animales y subvenciones de Horizon Europe destinadas a métodos alternativos. Los institutos Fraunhofer de Alemania y los centros Catapult del Reino Unido colaboran con PYME para comercializar modelos óseos vascularizados que abordan pipelines de trastornos musculoesqueléticos. Los reguladores colaboran con organismos de desarrollo de estándares para armonizar marcos de validación, suavizando las comparaciones de estudios transfronterizos y reforzando la confianza en la demanda.
Asia-Pacífico registra la TCAC más rápida del 16,8% ya que China, Japón y Corea del Sur integran el cultivo 3D en hojas de ruta nacionales de medicina de precisión. El Ministerio de Ciencia y Tecnología de China subsidia pilotos de órgano en chip en laboratorios estatales clave, mientras que los consorcios japoneses se enfocan en soluciones de cerebro en chip para neurodegeneración. El Consejo de Investigación Científica e Industrial de India patrocina startups de hidrogel autóctonas para reducir la dependencia de importaciones. En otros lugares, el Medio Oriente, África y América del Sur registran pedidos incipientes pero en aumento a medida que se forman clústeres académico-industriales alrededor de hospitales universitarios. Brasil financia centros de bioimpresión 3D enfocados en pruebas de toxicidad dérmica para alinearse con nuevas regulaciones cosméticas. La creciente huella global magnifica el tamaño del mercado de cultivo celular 3D en desglosados regionales e impulsa la tecnología hacia ciclos de adopción mainstream.
Panorama Competitivo
La concentración del mercado permanece moderada porque nichos diferenciados coexisten dentro de una ola de adopción más amplia. Thermo Fisher Scientific y Merck KGaA anclan portafolios que abarcan plásticos, reactivos y software, capturando sinergia entre flujos de trabajo. Corning aprovecha la experiencia en sustratos de vidrio para suministrar placas de adherencia ultra-baja que siembran esferoides con varianza mínima por lote[3]Corning, "3D Cell Culture Models," corning.com. InSphero y MIMETAS explotan propiedad intelectual microfluídica estratificada con biología específica de enfermedad, ganando participación dentro de programas de oncología y enfermedad metabólica. Jugadores emergentes como Emulate, CN Bio y TissUse son pioneros en chips multi-órgano, posicionándose para modelado de exposición sistémica.
Las presentaciones de patentes se expandieron 35% entre 2023-2025, especialmente alrededor de microcanales resistentes al cizallamiento y biotintas foto-reticulables. Los movimientos estratégicos incluyen la adquisición de USD 420 millones de Merck KGaA de OrganoTech Biosciences para integrar servicios de organoides derivados de pacientes. Thermo Fisher lanzó una suite de imágenes habilitada por IA que se empareja con sus chips de perfusión para puntuación automatizada de endpoints. Las asociaciones con proveedores de software de análisis simplifican pipelines de datos, un impulsor clave de adopción. Los proveedores que agrupan chips, medios y análisis en contratos de suscripción construyen flujos de ingresos recurrentes, protegiendo el flujo de efectivo de presupuestos de capital cíclicos.
Las oportunidades de espacio en blanco giran alrededor de kits de validación llave en mano y materiales de grado GMP compatibles con fabricación de terapia celular. Los proveedores que proporcionen documentación lista para consenso se beneficiarán cuando ISO y ASTM finalicen estándares. La entrada de firmas de análisis nativas de la nube acelera la interpretación de lecturas multiplex, forjando colaboraciones intersectoriales entre fabricantes de herramientas de ciencias de la vida y especialistas en ciencia de datos.
Líderes de la Industria de Cultivo Celular 3D
-
Merck KGaA
-
MIMETAS BV
-
Lonza Group AG
-
Thermo Fisher Scientific Inc.
-
Corning Incorporated
- *Nota aclaratoria: los principales jugadores no se ordenaron de un modo en especial
Desarrollos Recientes de la Industria
- Mayo 2025: PL BioScience y DewCell Biotherapeutics iniciaron una asociación de USD 12 millones para co-desarrollar SynthaPLT, un lisado de plaquetas libre de animales optimizado para expansión 3D de tipos celulares de medicina regenerativa.
- Enero 2025: Merck KGaA compró OrganoTech Biosciences por USD 420 millones, agregando organoides derivados de pacientes a su catálogo de oncología de precisión.
Alcance del Informe Global del Mercado de Cultivo Celular 3D
Según el alcance del informe, el cultivo celular tridimensional (3D) es un ambiente artificialmente creado en el que las células biológicas pueden crecer o interactuar con su entorno en las tres dimensiones. El mercado de cultivo celular 3D está segmentado por producto, aplicación, usuario final y geografía. Por producto, el mercado está segmentado como cultivos celulares 3D basados en andamiaje, cultivos celulares 3D libres de andamiaje, microchips y biorreactores 3D. Por aplicación, el mercado está segmentado como descubrimiento de fármacos, ingeniería de tejidos, aplicaciones clínicas y otras aplicaciones. Por usuario final, el mercado está segmentado como laboratorios e institutos de investigación, empresas biotecnológicas y farmacéuticas y otros usuarios finales. Por geografía, el mercado está segmentado como América del Norte, Europa, Asia-Pacífico, Medio Oriente y África, y América del Sur. El informe de mercado también cubre los tamaños de mercado estimados y tendencias para 17 países en las principales regiones globalmente. El informe ofrece el valor (en USD) para los segmentos anteriores.
| Plataformas Basadas en Andamiaje | Microplacas de Superficie Microestampada |
| Hidrogeles (Naturales, Sintéticos, Híbridos) | |
| Andamiajes Derivados de MEC | |
| Microportadores Porosos | |
| Plataformas Libres de Andamiaje | Placas de Gota Colgante |
| Esferoides Levitados Magnéticamente | |
| Sistemas de Órgano en Chip Basados en Microfluídica | |
| Biorreactores 3D (Agitador, Perfusión, Pared Rotatoria) | |
| Sistemas y Reactivos de Bioimpresión 3D | |
| Servicios (Desarrollo de Ensayos Personalizados, Modelos Externalizados) |
| Investigación del Cáncer y Detección de Fármacos Oncológicos |
| Investigación de Células Madre e Ingeniería de Tejidos |
| Descubrimiento de Fármacos y Detección de Toxicología |
| Medicina Regenerativa / Terapéuticas Personalizadas |
| Otras Aplicaciones (Virología, Seguridad Cosmética) |
| Empresas Biotecnológicas y Farmacéuticas |
| Institutos Académicos y de Investigación |
| Organizaciones de Investigación por Contrato y CDMO |
| Hospitales y Centros de Diagnóstico |
| América del Norte | Estados Unidos |
| Canadá | |
| México | |
| Europa | Alemania |
| Reino Unido | |
| Francia | |
| Italia | |
| España | |
| Resto de Europa | |
| Asia-Pacífico | China |
| Japón | |
| India | |
| Corea del Sur | |
| Australia | |
| Resto de Asia-Pacífico | |
| Medio Oriente y África | CCG |
| Sudáfrica | |
| Resto de Medio Oriente y África | |
| América del Sur | Brasil |
| Argentina | |
| Resto de América del Sur |
| Por Tecnología | Plataformas Basadas en Andamiaje | Microplacas de Superficie Microestampada |
| Hidrogeles (Naturales, Sintéticos, Híbridos) | ||
| Andamiajes Derivados de MEC | ||
| Microportadores Porosos | ||
| Plataformas Libres de Andamiaje | Placas de Gota Colgante | |
| Esferoides Levitados Magnéticamente | ||
| Sistemas de Órgano en Chip Basados en Microfluídica | ||
| Biorreactores 3D (Agitador, Perfusión, Pared Rotatoria) | ||
| Sistemas y Reactivos de Bioimpresión 3D | ||
| Servicios (Desarrollo de Ensayos Personalizados, Modelos Externalizados) | ||
| Por Aplicación | Investigación del Cáncer y Detección de Fármacos Oncológicos | |
| Investigación de Células Madre e Ingeniería de Tejidos | ||
| Descubrimiento de Fármacos y Detección de Toxicología | ||
| Medicina Regenerativa / Terapéuticas Personalizadas | ||
| Otras Aplicaciones (Virología, Seguridad Cosmética) | ||
| Por Usuario Final | Empresas Biotecnológicas y Farmacéuticas | |
| Institutos Académicos y de Investigación | ||
| Organizaciones de Investigación por Contrato y CDMO | ||
| Hospitales y Centros de Diagnóstico | ||
| Geografía | América del Norte | Estados Unidos |
| Canadá | ||
| México | ||
| Europa | Alemania | |
| Reino Unido | ||
| Francia | ||
| Italia | ||
| España | ||
| Resto de Europa | ||
| Asia-Pacífico | China | |
| Japón | ||
| India | ||
| Corea del Sur | ||
| Australia | ||
| Resto de Asia-Pacífico | ||
| Medio Oriente y África | CCG | |
| Sudáfrica | ||
| Resto de Medio Oriente y África | ||
| América del Sur | Brasil | |
| Argentina | ||
| Resto de América del Sur | ||
Preguntas Clave Respondidas en el Informe
¿Qué ingresos genera América del Norte del cultivo celular 3d en 2025?
América del Norte entrega el 42% de las ventas globales, traduciéndose a aproximadamente USD 0,97 mil millones basado en el tamaño de mercado de 2025.
¿Qué segmento está creciendo más rápido dentro de la categoría de tecnología?
Plataformas microfluídicas de órgano en chip, pronosticadas para avanzar a una TCAC del 18,9% hasta 2030.
¿Cómo mejoran los cultivos 3D el descubrimiento de fármacos oncológicos?
Reproducen factores del microambiente tumoral como hipoxia y contacto estromal, produciendo 85% de concordancia con resultados clínicos reportados en estudios de 2024.
¿Por qué son las CRO fundamentales para la adopción?
Las CRO agrupan hardware especializado, protocolos y análisis de IA, permitiendo a los patrocinadores acceder a modelos avanzados sin fuertes inversiones de capital, impulsando una TCAC del 16,5%.
¿Cuál es la restricción primaria que obstaculiza la adopción en mercados emergentes?
Los altos costos iniciales de dispositivos relativos a sistemas 2D reducen la adopción donde los presupuestos de investigación son limitados; nuevos chips imprimibles de bajo costo están aliviando esta brecha.
¿Cómo están evolucionando los estándares?
ISO, ASTM y la Comisión Europea están redactando normas de validación armonizadas que deberían madurar para 2027, simplificando las presentaciones regulatorias globales.
Última actualización de la página el:



