Marktgröße und Marktanteil für Pharmakovigilanz
Pharmakovigilanz-Marktanalyse von Mordor Intelligence
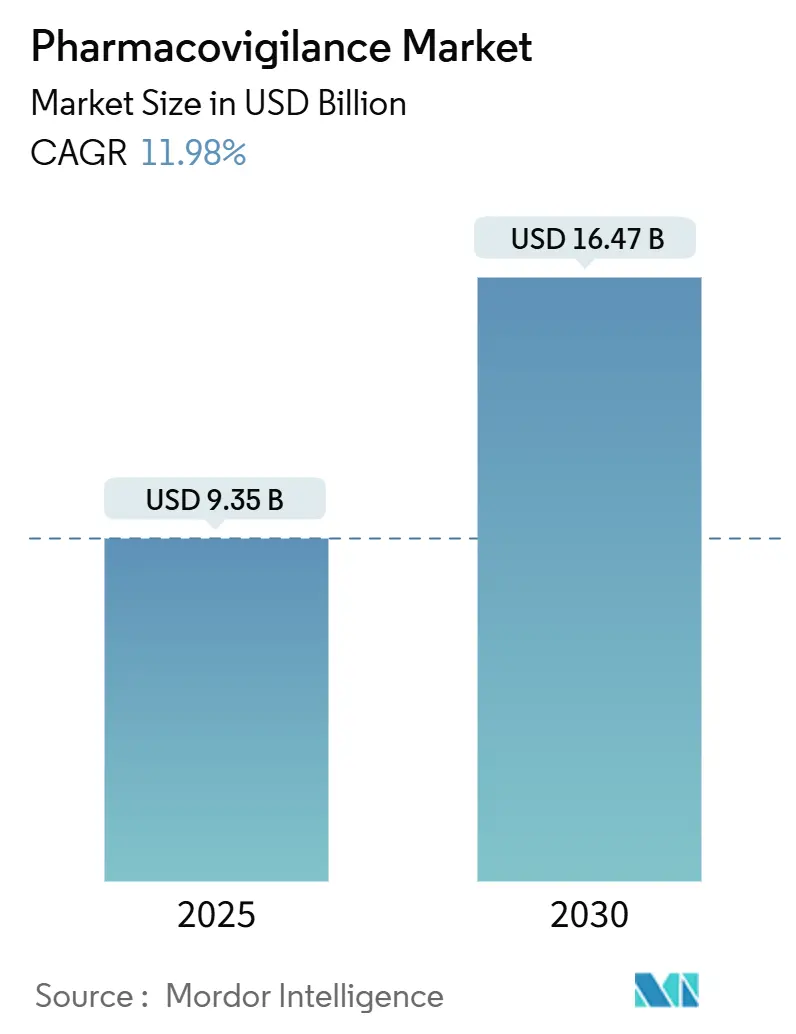
Der Pharmakovigilanz-Markt wird 2025 auf 9,35 Milliarden USD geschätzt und soll bis 2030 16,47 Milliarden USD erreichen, mit einer CAGR von 11,98%. Expandierende Arzneimittel-Pipelines, strengere Post-Marketing-Überwachungsvorschriften und die schnelle Einführung künstlicher Intelligenz (KI) in Sicherheitsüberwachungs-Workflows erhalten diese Dynamik aufrecht.[1]European Medicines Agency, "Guidance on the Application of the Amended Variations Regulation," ema.europa.eu Pharmaunternehmen lenken Ressourcen in Richtung proaktives Sicherheitsmanagement um, da Biologika, Gentherapien und andere komplexe Modalitäten in den kommerziellen Einsatz gelangen. Contract Research Organizations (CROs) mit cloud-basierten KI-Plattformen bieten kosteneffiziente Compliance und beschleunigen den Outsourcing-Trend. Post-Marketing-Überwachungspflichten vergrößern Datenvolumen, wodurch das Electronic Health Record (EHR) Mining zur am schnellsten wachsenden Berichtsmethode wird. Nordamerika behält die Führung aufgrund ausgereifter Regulierungswissenschaft, aber Harmonisierungsinitiativen im asiatisch-pazifischen Raum (APAC) treiben das zweistellige Wachstum dieser Region voran.[2]Food and Drug Administration, "International Regulatory Harmonization," fda.gov
Wichtige Erkenntnisse des Berichts
- Nach Dienstleistern führte die Vertragsauslagerung 2024 mit 55,46% Umsatzanteil; das Segment expandiert bis 2030 mit einer CAGR von 13,73%.
- Nach klinischen Studienphasen hielten Phase-IV-Post-Marketing-Studien 2024 32,18% des Pharmakovigilanz-Marktanteils, während präklinische Aktivitäten die höchste CAGR von 13,13% bis 2030 verzeichnen.
- Nach Art der Berichterstattung kommandierte die Spontanberichterstattung 2024 43,45% Anteil der Pharmakovigilanz-Marktgröße; EHR Mining soll zwischen 2025-2030 mit einer CAGR von 14,36% wachsen.
- Nach Endnutzern machten Pharmaunternehmen 2024 59,53% Anteil der Pharmakovigilanz-Marktgröße aus und Krankenhäuser verzeichnen bis 2030 eine CAGR von 14,45%.
- Nach Geografie hielt Nordamerika 2024 44,18% des Pharmakovigilanz-Marktanteils, während APAC die schnellste CAGR von 13,64% bis 2030 verzeichnet.
Globale Pharmakovigilanz-Markttrends und Einblicke
Treiber-Auswirkungsanalyse
| Treiber | (~) % Auswirkung auf CAGR-Prognose | Geografische Relevanz | Auswirkungszeitrahmen |
|---|---|---|---|
| Eskalierender Arzneimittelkonsum & Entwicklungs-Pipeline | +2.1% | Global | Langfristig (≥ 4 Jahre) |
| Wachsende Inzidenz unerwünschter Arzneimittelwirkungen (UAW) | +1.8% | Global, alternde Bevölkerungen | Mittelfristig (2-4 Jahre) |
| Outsourcing von PV-Dienstleistungen an CRO/BPO-Anbieter | +2.3% | Nordamerika & EU, steigend in APAC | Kurzfristig (≤ 2 Jahre) |
| KI-gestützte Signaldetektion & prädiktive Analytik | +1.9% | Nordamerika & EU Kern, Übertragung APAC | Mittelfristig (2-4 Jahre) |
| Ausbau von Real-World-Evidence (RWE) Plattformen | +1.7% | USA & EU führend, globale Verbreitung | Langfristig (≥ 4 Jahre) |
| Strenge regulatorische Vorschriften für proaktive Post-Marketing-Sicherheit | +2.0% | Global | Langfristig (≥ 4 Jahre) |
| Quelle: Mordor Intelligence | |||
Zunehmender Arzneimittelkonsum und Entwicklungs-Pipeline
Die FDA genehmigte 2024 50 neue molekulare Einheiten, was unterstreicht, wie Durchbruch-Zulassungen die Post-Marketing-Sicherheitspflichten für jeden Sponsor erweitern.[3]Food and Drug Administration, "Drug and Biologic Approvals," fda.gov Gentherapien, CAR-T-Behandlungen und Kombinationsprodukte weisen einzigartige Risikoprofile auf, die eine wachsame Überwachung während des gesamten Produktlebenszyklus erfordern. Bedingte Zulassungen verstärken zusätzlich die Real-World-Evidence (RWE) Erwartungen und lenken Budgets in Richtung kontinuierlicher Überwachungsinfrastrukturen um. Diese Dynamiken binden Pharmakovigilanz-Teams in einen langfristigen Expansionszyklus, der das Arbeitsaufkommen über die klinische Entwicklung hinaus erhält.
Wachsende Inzidenz unerwünschter Arzneimittelwirkungen (UAW)
Das Pharmacovigilance Risk Assessment Committee (PRAC) der Europäischen Arzneimittelagentur (EMA) betonte kürzlich die lebenslange Überwachung für CAR-T-Empfänger nach der Beobachtung potenzieller sekundärer Malignome.[4]European Medicines Agency, "PRAC Meeting Highlights," ema.europa.eu Polypharmazie in älteren Bevölkerungen multipliziert Arzneimittel-Arzneimittel-Interaktionen und treibt UAW-Fallvolumen höher. Der Impfstoff-Rollout der Pandemiezeit validierte die Wichtigkeit großangelegter Signaldetektions-Netzwerke, die Millionen von Sicherheitsberichten innerhalb von Wochen verarbeiten können.
Outsourcing von PV-Dienstleistungen an CRO/BPO-Anbieter
Sponsoren übertragen zunehmend vollständige Pharmakovigilanz-Operationen an CROs, die globale Compliance-Zentren und speziell entwickelte KI-Engines unterhalten. Solche Anbieter skalieren nahtlos über Jurisdiktionen hinweg und ermöglichen mittelgroßen Biotechnologie-Firmen, komplexe Regeln zu erfüllen, ohne schwere Fixkosten zu tragen. Arbeitskosten-Arbitrage-Modelle in Indien und Osteuropa sind ebenfalls attraktiv, doch die Differenzierung beruht nun auf automatisierter Aufnahme und prädiktiver Signaldetektion statt auf reinen Kosteneinsparungen.
KI-gestützte Signaldetektion und prädiktive Analytik
IQVIA zielt auf eine 50%ige Reduzierung der Ausgaben für Routine-Fallbearbeitung durch Integration von Large-Language-Model (LLM) Copilots in tägliche Arbeitsabläufe. Währenddessen bettete Oracle erweiterte Machine-Learning-Features in seine Sicherheitsplattform ein, um Literatur-Alerts zu triagieren und Narrativ-Schreibung zu automatisieren. Regulierungsbehörden haben mit Entwurfsleitlinien reagiert, die Validierungserwartungen für KI-Einsatz im Sicherheitsmanagement setzen.
Beschränkungen-Auswirkungsanalyse
| Beschränkung | (~) % Auswirkung auf CAGR-Prognose | Geografische Relevanz | Auswirkungszeitrahmen |
|---|---|---|---|
| Cybersicherheits- und Datenschutz- risiken | -1.4% | Global, hoch in EU & USA | Kurzfristig (≤ 2 Jahre) |
| Mangel an globaler regulatorischer Harmonisierung & Datenstandards | -1.2% | Global, Schwellenmärkte am stärksten betroffen | Langfristig (≥ 4 Jahre) |
| Mangel an spezialisierten PV-Talenten & hohe Fluktuation | -1.6% | Nordamerika & EU akut | Mittelfristig (2-4 Jahre) |
| Komplexität von Kombinations- & ATMP Therapien | -1.1% | Nordamerika & EU, sich ausweitend | Langfristig (≥ 4 Jahre) |
| Quelle: Mordor Intelligence | |||
Cybersicherheits- und Datenschutzrisiken
Cloud-Deployment sensibler Patientendaten setzt Sicherheitssysteme Ransomware und nationalstaatlichen Intrusion aus. Jüngste Gesundheitswesen-Datenschutzverletzungen zwangen mehrere Sponsoren, EHR-Integrationen auszusetzen, während Audits sicherstellten, dass keine Manipulation von Sicherheitssignalen stattfand. Die Datenschutz-Grundverordnung (DSGVO) und ähnliche Gesetze verlangen Datenminimierungs- und Lokalisierungsstrategien, die manchmal mit globalen Analytics-Ambitionen in Konflikt stehen.
Mangel an spezialisierten PV-Talenten und hohe Mitarbeiterfluktuation
Branchenumfragen prognostizieren einen 35%igen Mangel an qualifizierten Pharmakovigilanz-Fachkräften bis 2030, da KI-Fähigkeiten, regulatorisches Wissen und therapeutische Spezialisierung in ein einziges Profil konvergieren. Organisationen reagieren mit Ausbildungsprogrammen und internen Akademien, doch Anlaufzeiten können zwei Jahre übersteigen und schaffen kurzfristige Engpässe.
Segmentanalyse
Nach klinischen Studienphasen: Post-Marketing-Überwachung treibt Wachstum
Phase-IV-Studien hielten 2024 32,18% des Pharmakovigilanz-Marktanteils und spiegeln die Forderung der Regulierungsbehörden nach lebenslanger Überwachung innovativer Therapien wider. Die Pharmakovigilanz-Marktgröße für präklinische Sicherheitsbewertungen soll dank risikobasierter Frühphasen-Analytik mit einer CAGR von 13,13% expandieren. Adaptive Studiendesigns verkürzen Phasen II und III, erhöhen aber die Bedeutung hochauflösender Signaldetektion, sobald Produkte breite Bevölkerungen erreichen. Aktualisierte ICH E6(R3) Leitlinien verpflichten Sponsoren, Quality-by-Design-Metriken in allen Phasen einzubetten und sicherzustellen, dass nachverfolgbare Sicherheitsdatenerfassung ab der ersten Dosierung am Menschen erfolgt.
Der Pharmakovigilanz-Markt reagiert durch Integration dezentraler Studien mit direkter Patientenprobenahme und tragbaren Sensoren. KI-Modelle simulieren Off-Target-Effekte vor der ersten Patientendosierung und geben Unternehmen einen Vorsprung in der Risikomanagement-Planung. Da bedingte Zulassungen zunehmen, übersteigen Post-Authorization Safety Studies (PASS) Budgets traditionelle Phase-III-Ausgaben und sichern Phase-IV-Dominanz in den langfristigen Ausblick.
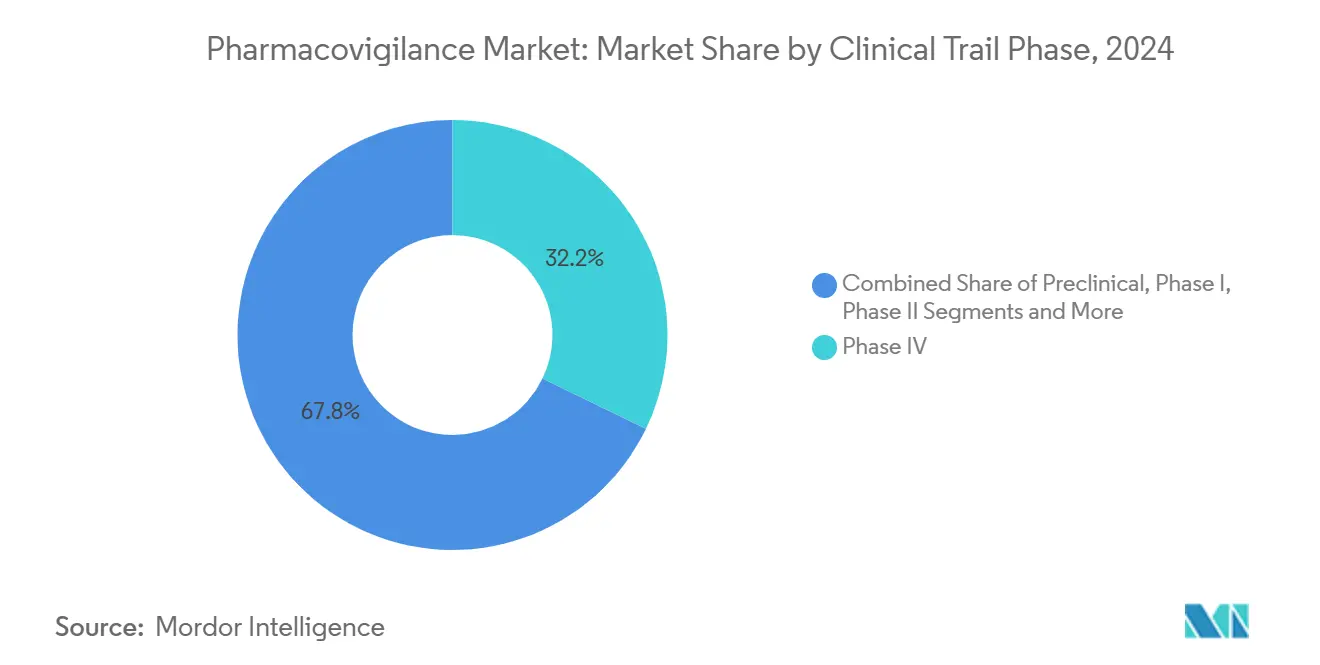
Notiz: Segmentanteile aller einzelnen Segmente verfügbar beim Kauf des Berichts
Nach Dienstleistern: Outsourcing beschleunigt durch Technologieintegration
Vertragsauslagerung kontrollierte 2024 55,46% des Gesamtumsatzes und soll bis 2030 mit 13,73% wachsen, wodurch der größte Anteil des Pharmakovigilanz-Marktes erhalten bleibt. Inhouse-Einheiten behalten kritische Entscheidungsfindung, verlassen sich aber zunehmend auf Hybrid-Modelle, bei denen CRO-Plattformen Routineaufgaben verarbeiten. Strategische Allianzen wie Parexels mehrjähriger KI-Pakt mit Palantir veranschaulichen, wie technisch erweiterte CROs Wettbewerbsvorteile kultivieren.
Die Pharmakovigilanz-Industrie schätzt nun skalierbare Data Lakes, Natural Language Processing (NLP) für wissenschaftliche Literatur und Robotic Process Automation bei der Aufnahme. Infolgedessen migrieren selbst große Pharmaunternehmen Arbeitslasten zu externen Zentren in Indien, Irland und Osteuropa und konsolidieren fragmentierte Anbieterlisten zu Master Service Agreements, die KI-Investitions-Roadmaps garantieren.
Nach Art der Berichterstattung: EHR Mining entsteht als Technologie-Disruptor
Spontanberichterstattung blieb 2024 mit 43,45% das Rückgrat, doch die Pharmakovigilanz-Marktgröße für EHR Mining soll die schnellste CAGR von 14,36% verzeichnen. Finale FDA-Leitlinien zu RWE öffnen die Tür für automatisierte Extraktion strukturierter und unstrukturierter klinischer Daten zur Ergänzung traditioneller Falleinreichungen.
KI-Algorithmen analysieren Arztnotizen, Laborbefunde und Bildgebungs-Repositories, um verborgene Sicherheitstrends Wochen früher als Spontanberichte zu enthüllen. Projekte wie Sanofis ARTEMIS verarbeiten jährlich mehr als 700.000 Fälle mit NLP-Engines und befreien menschliche Experten für Ursachenanalysen. Standardisierungshürden bestehen fort, insbesondere um Datenprovenienz, aber die Trajektorie hin zur automatisierten RWE-Aufnahme ist klar.
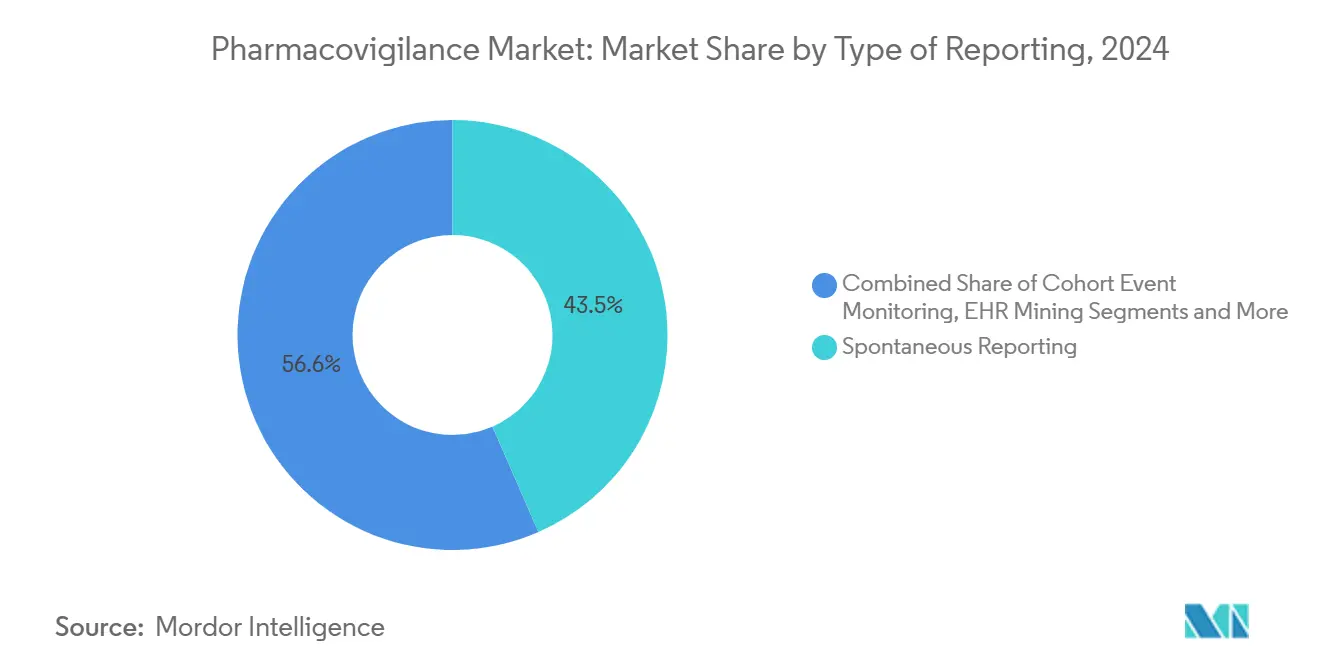
Notiz: Segmentanteile aller einzelnen Segmente verfügbar beim Kauf des Berichts
Nach Endnutzern: Krankenhaus-Integration transformiert Sicherheitsüberwachung
Pharmaunternehmen hielten 2024 59,53% der Ausgaben, doch Krankenhaus-Systeme verzeichnen die höchste CAGR von 14,45%, da dezentrale und pragmatische Studien Sicherheitsverantwortlichkeiten näher an den Versorgungsort legen. Die Pharmakovigilanz-Marktgröße für integrierte Versorgungsnetzwerke steigt, da Krankenhäuser RWE-Plattformen einsetzen, die nahezu Echtzeit-Sicherheitsdaten an Sponsoren weiterleiten.
BARDAs fünfjähriger Pakt mit Allucent illustriert, wie staatliche Finanzierung Krankenhaus-Teilnahme an Gegenmaßnahme-Studien beschleunigt. Doch Interoperabilitätslücken und Datenschutzvorschriften verlangsamen grenzübergreifenden Datenaustausch und verlängern die Übergangsperiode.
Geografieanalyse
Nordamerika eroberte 2024 44,18% des Pharmakovigilanz-Marktes aufgrund hoher F&E-Intensität, fortgeschrittener EHR-Durchdringung und klarer regulatorischer Erwartungen. KI-Pilotprojekte finden schnelle Akzeptanz, da die FDA schrittweise Validierungsrahmen veröffentlicht und die Region als globale Referenz für digitale Pharmakovigilanz positioniert.
Europa folgt mit ausgereifter Gesetzgebung, die das EudraVigilance-Netzwerk unterstützt, und neuen KI-Reflexionspapieren, die Innovation fördern, während sie Algorithmus-Transparenz verlangen. Der Fokus auf Advanced Therapy Medicinal Products bringt spezialisierte Überwachungsbedarfe mit sich und erhält Investitionen bis 2030. Die Pharmakovigilanz-Marktgröße für EU-basierte PASS wächst neben Orphan-Drug-Zulassungen.
Der asiatisch-pazifische Raum soll mit 13,64% CAGR die schnellste weltweit verzeichnen, da Chinas Regulierungsreformen und Indiens erweiterte klinische Studienlandschaft konvergieren. ASEAN-Nationen gleichen Kennzeichnungs- und elektronische Einreichungsstandards an und vereinfachen multinationale Sicherheitskampagnen. Investitionen in heimische Biotech-Fertigung stimulieren Nachfrage nach lokalisierten Fallbearbeitungszentren. Naher Osten & Afrika und Südamerika fügen inkrementelles Wachstum hinzu, wo Pharmakovigilanz-Infrastruktur mit pharmazeutischen Importvolumen und entstehenden Fertigungsclustern skaliert.
Wettbewerbslandschaft
Der Pharmakovigilanz-Markt zeigt moderate Fragmentierung. IQVIA, ICON und Parexel unterhalten beträchtliche globale Präsenzen, doch Software-first-Anbieter wie ArisGlobal und Oracle schließen die Lücke durch KI-zentrierte Angebote. ArisGlobal aktualisierte seine LifeSphere-Suite mit LLM-gestützter Triage und sah 2024 eine Rekordwelle neuer Kunden.
Strategische Deals definieren die Wettbewerbserzählung. ICONs Akquisition von PRA Health Sciences konsolidierte zwei Full-Service-CROs unter einer KI-Plattform und erhöhte die Größenordnung sowohl in Post-Marketing- als auch in Real-World-Studien. Sanofis Zusammenarbeit mit OpenAI und Formation Bio signalisiert Big-Pharma-Interesse an vertikal integrierter KI-Software-Entwicklung.
White-Space-Nischen bestehen fort in fortgeschrittener Zell- und Gentherapie-Überwachung, pädiatrischer Arzneimittelsicherheit und NLP-Lösungen für japanische und Mandarin-Quelldokumente. Neue Marktteilnehmer mit Plug-and-Play-Sicherheits-Clouds oder token-basierten Datenaustausch-Modellen könnten Marktanteile von langsam modernisierenden Legacy-Plattform-Incumbents erobern.
Pharmakovigilanz-Industrieführer
-
Cognizant
-
Capgemini
-
Accenture
-
Wipro Limited
-
IBM
- *Haftungsausschluss: Hauptakteure in keiner bestimmten Reihenfolge sortiert
Jüngste Industrieentwicklungen
- Januar 2025: ArisGlobal berichtete über signifikantes Kundenwachstum und Produktverbesserungen in seiner LifeSphere-Plattform.
- September 2024: IQVIA startete seinen KI-Assistenten zur Beschleunigung der Signaldetektion durch Synthese umfangreicher Gesundheitsdatensätze.
- September 2024: Boehringer Ingelheim erweiterte die LifeSphere MultiVigilance-Plattform nach Japan und verstärkte APAC-Fähigkeiten.
- Mai 2024: Sanofi, Formation Bio und OpenAI enthüllten eine KI-Partnerschaft zur Verkürzung von Arzneimittelentwicklungs- und Sicherheitszeitplänen.
Globaler Pharmakovigilanz-Marktbericht Umfang
Pharmakovigilanz ist die Wissenschaft und Gruppe von Aktivitäten im Zusammenhang mit der Erkennung, Bewertung, dem Verständnis und der Prävention unerwünschter Wirkungen oder anderer arzneimittelbezogener Probleme. Pharmakovigilanz konzentriert sich auf UAW (unerwünschte Arzneimittelreaktionen) und Arzneimitteltoxizität. Der Pharmakovigilanz-Markt umfasst alle Arten von Berichterstattung unerwünschter Ereignisse, die während klinischer Studien in Krankenhäusern, Apotheken und anderen Gesundheitssektoren durchgeführt werden. Der Pharmakovigilanz-Markt ist nach klinischen Studienphasen (Präklinisch, Phase I, Phase II, Phase III und Phase IV), Dienstleistern (Inhouse und Vertragsauslagerung), Art der Berichterstattung (Spontanberichterstattung, intensivierte UAW-Berichterstattung, gezielte Spontanberichterstattung, Kohorten-Event-Monitoring und EHR Mining), Endnutzern (Krankenhäuser, Pharmaunternehmen und andere Endnutzer) und Geografie (Nordamerika, Europa, Asien-Pazifik, Naher Osten und Afrika und Südamerika) segmentiert. Der Marktbericht deckt auch die geschätzten Marktgrößen und Trends für 17 verschiedene Länder in wichtigen Regionen weltweit ab. Der Bericht bietet den Wert (in Milliarden USD) für die oben genannten Segmente.
| Präklinisch |
| Phase I |
| Phase II |
| Phase III |
| Phase IV |
| Inhouse |
| Vertragsauslagerung |
| Spontanberichterstattung |
| Intensivierte UAW-Berichterstattung |
| Gezielte Spontanberichterstattung |
| Kohorten-Event-Monitoring |
| EHR Mining |
| Krankenhäuser |
| Pharmaunternehmen |
| CROs und andere Endnutzer |
| Nordamerika | Vereinigte Staaten |
| Kanada | |
| Mexiko | |
| Europa | Deutschland |
| Vereinigtes Königreich | |
| Frankreich | |
| Italien | |
| Spanien | |
| Restliches Europa | |
| Asien-Pazifik | China |
| Japan | |
| Indien | |
| Australien | |
| Südkorea | |
| Restlicher asiatisch-pazifischer Raum | |
| Naher Osten und Afrika | GCC |
| Südafrika | |
| Restlicher Naher Osten und Afrika | |
| Südamerika | Brasilien |
| Argentinien | |
| Restliches Südamerika |
| Nach klinischen Studienphasen | Präklinisch | |
| Phase I | ||
| Phase II | ||
| Phase III | ||
| Phase IV | ||
| Nach Dienstleistern | Inhouse | |
| Vertragsauslagerung | ||
| Nach Art der Berichterstattung | Spontanberichterstattung | |
| Intensivierte UAW-Berichterstattung | ||
| Gezielte Spontanberichterstattung | ||
| Kohorten-Event-Monitoring | ||
| EHR Mining | ||
| Nach Endnutzern | Krankenhäuser | |
| Pharmaunternehmen | ||
| CROs und andere Endnutzer | ||
| Nach Geografie | Nordamerika | Vereinigte Staaten |
| Kanada | ||
| Mexiko | ||
| Europa | Deutschland | |
| Vereinigtes Königreich | ||
| Frankreich | ||
| Italien | ||
| Spanien | ||
| Restliches Europa | ||
| Asien-Pazifik | China | |
| Japan | ||
| Indien | ||
| Australien | ||
| Südkorea | ||
| Restlicher asiatisch-pazifischer Raum | ||
| Naher Osten und Afrika | GCC | |
| Südafrika | ||
| Restlicher Naher Osten und Afrika | ||
| Südamerika | Brasilien | |
| Argentinien | ||
| Restliches Südamerika | ||
Im Bericht beantwortete Schlüsselfragen
Wie hoch ist der aktuelle Wert des Pharmakovigilanz-Marktes?
Der Pharmakovigilanz-Markt wird 2025 auf 9,35 Milliarden USD geschätzt.
Wie schnell wird der Pharmakovigilanz-Markt bis 2030 wachsen?
Er soll mit einer CAGR von 11,98% expandieren und bis 2030 16,47 Milliarden USD erreichen.
Welches Servicemodell hält den größten Pharmakovigilanz-Marktanteil?
Vertragsauslagerung führt mit 55,46% des 2024er Umsatzes.
Warum ist der asiatisch-pazifische Raum die am schnellsten wachsende Region?
Regulatorische Harmonisierung in China, Indien und ASEAN-Nationen plus große Fertigungsinvestitionen treiben APACs CAGR von 13,64% an.
Seite zuletzt aktualisiert am: