Tamanho e Participação do Mercado de Terapia Gênica
Análise do Mercado de Terapia Gênica pela Mordor Intelligence
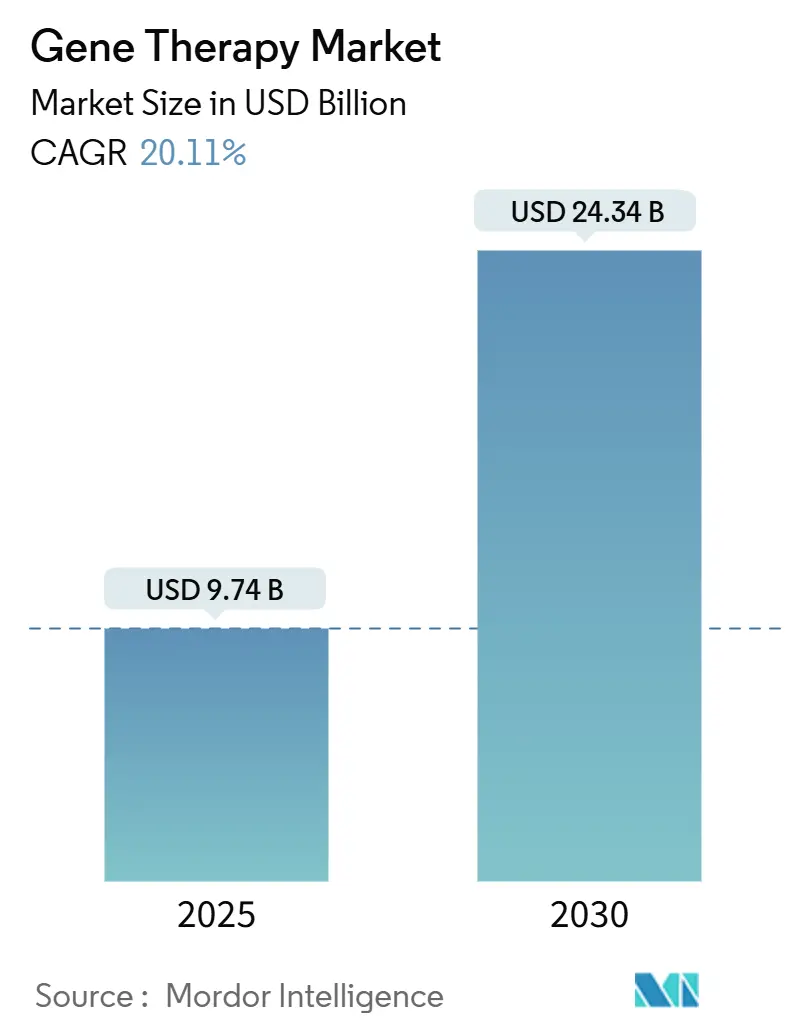
O tamanho do Mercado de Terapia Gênica é estimado em USD 9,74 bilhões em 2025, e espera-se que alcance USD 24,34 bilhões até 2030, a uma CAGR de 20,11% durante o período de previsão (2025-2030).
As autoridades regulamentadoras aprovaram nove terapias celulares e gênicas apenas em 2024, sinalizando crescente confiança na viabilidade clínica e comercial e desbloqueando caminhos de reembolso mais amplos em mercados-chave. O financiamento intensificado de biofarmacêuticas e private equity está acelerando ativos em estágio avançado, enquanto a capacidade de fabricação em expansão, tanto viral quanto não viral, reduz o atrito histórico da cadeia de suprimentos. Avanços rápidos na edição in vivo e engenharia de vetores estão ampliando o escopo terapêutico além de doenças raras para distúrbios de alta prevalência, especialmente em neurologia e oftalmologia. O crescimento de ensaios de dois dígitos na Ásia-Pacífico e os incentivos políticos da América do Norte juntos garantem uma base de demanda diversificada, mesmo enquanto preços altos de produtos e requisitos de monitoramento de segurança representam obstáculos de acesso.
Principais Destaques do Relatório
- Por tipo de vetor, o Vírus Adeno-associado capturou 38,54% da participação do mercado de terapia gênica em 2024, enquanto os métodos de entrega não virais estão posicionados para expandir a uma CAGR de 24,34% até 2030.
- Por indicação, oncologia comandou 42,92% da receita em 2024; aplicações neurológicas estão avançando a uma CAGR de 25,62% até 2030.
- Por modo de entrega, abordagens in vivo detiveram 65,92% do tamanho do mercado de terapia gênica em 2024, enquanto métodos ex vivo progredirão a uma CAGR de 23,07% entre 2025-2030.
- Por usuário final, hospitais e clínicas representaram 59,22% da participação do tamanho do mercado de terapia gênica em 2024; centros de tratamento especializados estão registrando uma CAGR de 21,89% até 2030.
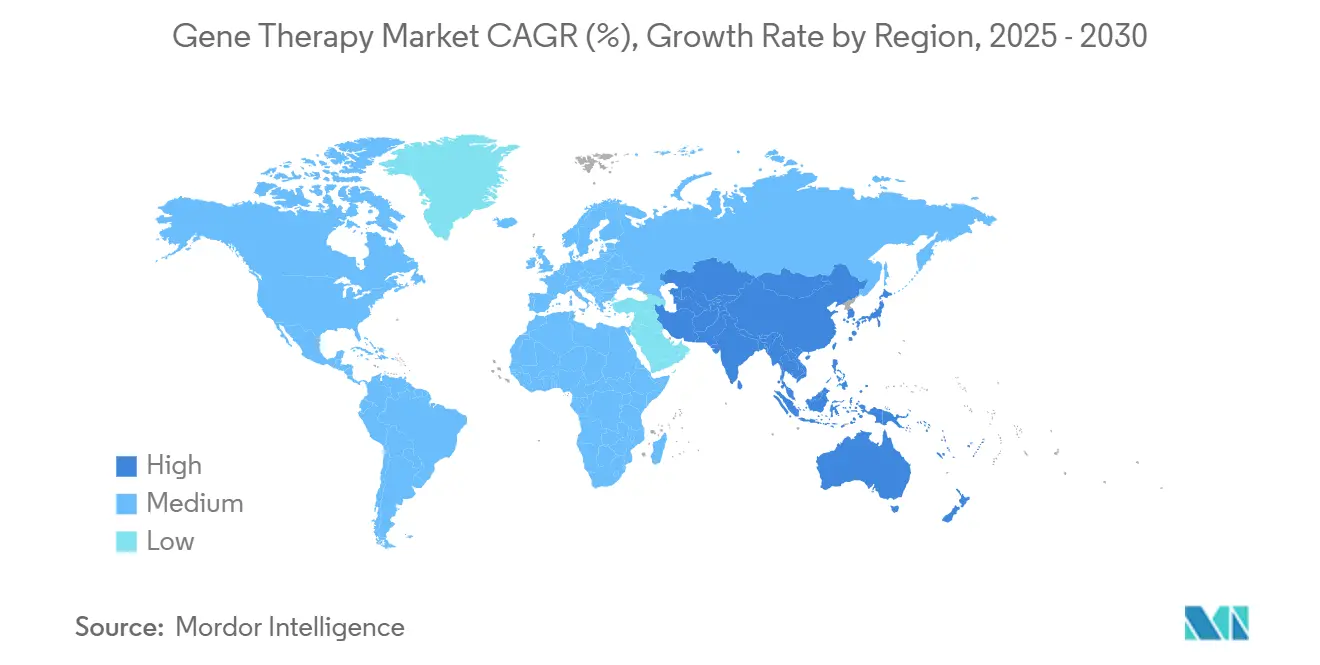
- Por geografia, a América do Norte liderou com 41,78% da participação de receita em 2024; a Ásia-Pacífico está prevista para acelerar a uma CAGR de 27,68% no mesmo horizonte.
Tendências e Insights do Mercado Global de Terapia Gênica
Análise do Impacto dos Impulsionadores
| Impulsionador | (~) % Impacto na Previsão CAGR | Relevância Geográfica | Cronograma de Impacto |
|---|---|---|---|
| Aprovações regulamentadoras demonstrando viabilidade | +5.2% | Global, concentrado na América do Norte e Europa | Curto prazo (≤ 2 anos) |
| Avanços em engenharia de vetores e tecnologia in vivo | +4.9% | Adoção precoce na América do Norte e Europa | Longo prazo (≥ 4 anos) |
| Expansão da infraestrutura de fabricação | +4.8% | América do Norte, Europa, Ásia-Pacífico emergente | Médio prazo (2-4 anos) |
| Rápida ampliação da capacidade comercial de AAV CDMO | +3.8% | Global, América do Norte e Europa, expandindo para Ásia-Pacífico | Médio prazo (2-4 anos) |
| Financiamento de biofarmacêuticas e private equity | +3.5% | Centros de inovação nos EUA, Europa e China | Médio prazo (2-4 anos) |
| Crescente inclusão de terapias gênicas para doenças raras | +2.7% | Global, com maior impacto em mercados desenvolvidos | Longo prazo (≥ 4 anos) |
| Fonte: Mordor Intelligence | |||
Crescentes Aprovações Regulamentadoras Demonstrando Viabilidade Clínica e Comercial
Aprovações frequentes de grandes reguladores estão reduzindo o risco de desenvolvimento e comprimindo cronogramas de lançamento. O total cumulativo da FDA de 37 produtos celulares e gênicos aprovados até 2024 mostra que os revisores da agência agora aplicam estruturas dedicadas como a designação Regenerative Medicine Advanced Therapy, que reduz o tempo de desenvolvimento em cerca de 40% para programas qualificados.[1]U.S. Food and Drug Administration, "Approved Cellular and Gene Therapy Products," fda.govO esquema PRIME da Europa e a regra de 2025 do Reino Unido para fabricação no ponto de atendimento facilitam ainda mais a entrada no mercado. A aprovação do ZEVASKYN para epidermólise bolhosa distrófica recessiva em 2025 exemplifica como as indicações estão se estendendo além de doenças ultra-raras para segmentos dermatológicos mais amplos. Tal ampliação do alcance terapêutico apoia o crescimento multi-anual no mercado de terapia gênica e estimula investimento de seguimento de pagadores esperando benefício clínico duradouro.
Avanços Tecnológicos Contínuos em Engenharia de Vetores e Plataformas de Edição In Vivo
Bibliotecas de capsídeos aprimoradas, otimização de sequência guiada por aprendizado de máquina e construtos lipídicos novos estão aguçando o tropismo tecidual e reduzindo a imunogenicidade. Pesquisadores da Escola de Medicina Perelman relataram nanopartículas lipídicas carregadas com DNA que persistem in vivo por meses, abrindo dosagem durável para doenças crônicas.[2]Penn Medicine News, "DNA-Loaded Lipid Nanoparticles Remain Active for Months," pennmedicine.orgPlataformas de organoides oferecem leitos de teste específicos de tecido humano que melhoram a previsibilidade translacional, apoiados pela aceitação da Lei de Modernização da FDA de modelos não-animais. Algoritmos assistidos por IA como o OpenCRISPR-1 cortam ciclos de design e elevam a precisão de edição. Coletivamente, essas inovações elevam o teto terapêutico, criam espaço para dosagem repetida e alimentam um ciclo virtuoso de sucesso clínico e implantação de capital que amplia o mercado de terapia gênica.
Expansão da Infraestrutura Global de Fabricação de Vetores Virais e Não Virais
O investimento de capital em larga escala está impulsionando tanto a capacidade quanto a sofisticação das linhas de produção. A compra de USD 16,5 bilhões da Catalent pela Novo Nordisk em 2024 sublinha como a grande farmacêutica está garantindo controle ponta a ponta das cadeias de suprimentos. Atualizações de vetores virais agora incorporam biorreatores de fluxo contínuo e processamento downstream de sistema fechado, cortando tempos de lote por dígitos duplos. Plataformas de nanopartículas lipídicas não virais reduzem o custo dos produtos em até 60% e podem embalar cargas maiores, removendo barreiras técnicas anteriores para indicações poligênicas.[3]Journal of Nanobiotechnology editors, "Advances in Lipid Nanoparticle Delivery," springeropen.com Automação, análise de qualidade habilitada por IA e designs modulares de salas limpas juntos aprimoram a confiabilidade, encorajando fabricantes contratados a pré-construir suítes que podem ser rapidamente personalizadas para novos patrocinadores.
Crescente Financiamento de Biofarmacêuticas e Private Equity em P&D de Terapia Gênica
Os influxos de capital permanecem resilientes apesar da volatilidade mais ampla do mercado. Valores antecipados em acordos de licenciamento de Fase II e III subiram 35% em 2024 à medida que a competição por ativos em estágio avançado se intensificou. A Sangamo Therapeutics garantiu USD 18 milhões antecipados e potencial de marcos de USD 1,4 bilhão por seus capsídeos direcionados ao SNC com a Eli Lilly, ilustrando o apetite do investidor por vetores de entrega diferenciados. Grupos de private equity também estão se movendo a jusante; a aquisição da bluebird bio pela Carlyle e SK Capital em 2025 injeta fundos de comercialização em terapias aprovadas para doença falciforme e β-talassemia, demonstrando o valor estratégico de ativos comercializados. Tal financiamento sustentado acelera a diversificação do pipeline e sustenta a demanda por serviços de fabricação, reforçando a expansão de longo prazo do mercado de terapia gênica.
Análise do Impacto das Restrições
| Restrição | (~) % Impacto na Previsão CAGR | Relevância Geográfica | Cronograma de Impacto |
|---|---|---|---|
| Preços altos das terapias | -3,8% | Maior efeito em mercados emergentes e regiões de reembolso restritivo | Médio prazo (2-4 anos) |
| Complexidade de fabricação e limites de suprimento de vetores | -2,6% | Varia por capacidade de produção regional | Curto prazo (≤ 2 anos) |
| Preocupações de segurança exigindo monitoramento de longo prazo | -2,1% | Mais intenso onde a supervisão regulamentadora é rigorosa | Longo prazo (≥ 4 anos) |
| Escassez de matérias-primas de plasmídeo/capsídeo | -1,9% | Aguda em regiões com resiliência limitada da cadeia de suprimentos | Curto prazo (≤ 2 anos) |
| Fonte: Mordor Intelligence | |||
Preços Altos das Terapias Criando Barreiras de Acesso e Acessibilidade
Curas de dose única comandam preços de lista entre USD 373.000 e USD 4,25 milhões, tensionando orçamentos de pagadores e testando a disposição social de financiar terapias curativas. Provedores citam lacunas de apoio social, distância de viagem e obstáculos de autorização prévia como os principais bloqueadores de acesso. Opções inovadoras de reembolso-contratos baseados em resultados, modelos de amortização e garantias estão emergindo, mas ainda requerem compartilhamento de dados complexo e infraestrutura de acompanhamento de longo prazo. Os Centros de Serviços Medicare e Medicaid lançaram um Modelo de Acesso a Terapia Celular e Gênica em 2025 que encoraja compras agrupadas em nível estadual para amenizar o impacto orçamentário. Esses ventos contrários financeiros devem moderar a adoção em regiões sensíveis a custos, suavizando a curva de crescimento do mercado de terapia gênica apesar das fortes proposições de valor clínico.
Complexidade de Fabricação e Suprimento Restrito de Vetores Grau GMP
Mesmo com expansões agressivas de capacidade, o suprimento de vetores AAV e lentivirais grau GMP atende apenas um quarto da demanda projetada para 2025. Ciclos de produção podem exceder nove meses, retardando cronogramas de lançamento e criando risco de inventário. Soluções descentralizadas emergentes como pods modulares de salas limpas cortam custos por dose de cerca de USD 400.000 para menos de USD 35.000 em configurações piloto, embora a harmonização regulamentadora permaneça um desafio. Até que tais modelos escalem, a disponibilidade restrita de vetores continuará a agir como um freio estrutural no mercado de terapia gênica.
Análise de Segmento
Por Tipo de Vetor: AAV Domina Enquanto Métodos Não Virais Crescem
Vetores AAV detiveram 38,54% da participação do mercado de terapia gênica em 2024 devido à segurança favorável e expressão sustentada de transgenes que fundamentam múltiplos produtos aprovados para hemofilia e distúrbios retinianos hereditários. Esta liderança é reforçada pelo amplo tropismo tecidual e um pool em expansão de sorotipos engenheirados que melhoram a especificidade. No entanto, sistemas de nanopartículas lipídicas não virais são a alternativa que mais cresce, prevista para registrar uma CAGR de 24,34% até 2030, pois carregam cargas genéticas maiores e simplificam a economia de fabricação. O tamanho do mercado de terapia gênica para plataformas não virais está, portanto, configurado para fechar parte da atual lacuna de receita. Vetores lentivirais permanecem o esteio para fabricação ex vivo de CAR-T, enquanto sistemas baseados em herpes ganham tração em oncologia por sua capacidade de carga. A otimização contínua de bibliotecas de capsídeos e promotores sintéticos determinará se vetores virais podem defender participação contra desafiantes não virais eficientes em custo.
O aumento em abordagens não virais também alivia restrições de matérias-primas porque componentes lipídicos são suscetíveis a cadeias de suprimentos farmacêuticos padrão. Nanopartículas carregadas com DNA que permanecem ativas por meses reduzem requisitos de dosagem repetida e podem ser ajustadas para captação seletiva por órgão. Tal flexibilidade atrai desenvolvedores visando distúrbios neurológicos poligênicos onde o tamanho da carga excede o limite de empacotamento do AAV. Consequentemente, a dinâmica competitiva dentro do mercado de terapia gênica está mudando da disponibilidade de vetores para precisão de entrega, criando espaço para CDMOs agnósticas de plataforma capturarem demanda emergente.
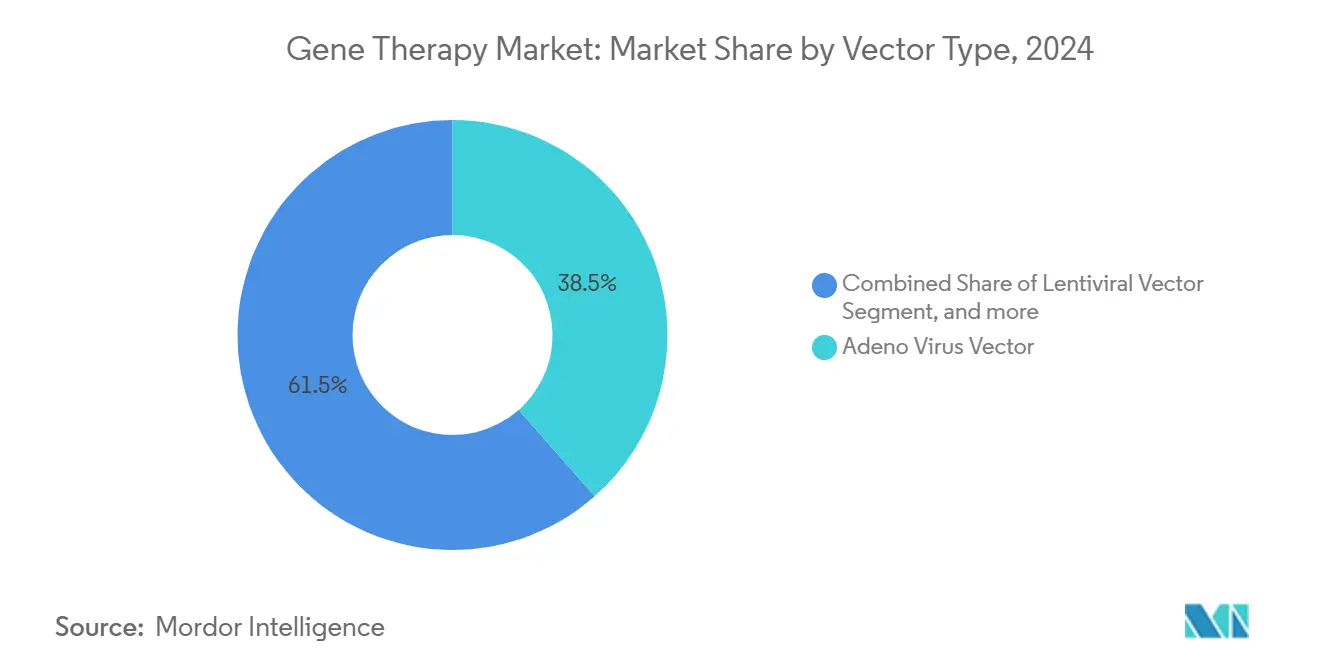
Nota: Participações de segmento de todos os segmentos individuais disponíveis na compra do relatório
Por Indicação: Oncologia Lidera Enquanto Neurologia Acelera
Aplicações oncológicas geraram 42,92% da receita em 2024, apoiadas por um fluxo constante de aprovações de CAR-T e um pipeline profundo voltado para tumores sólidos. Evidência robusta para respostas completas em malignidades hematológicas recidivas sustenta a aceitação do pagador apesar das pressões de preço. No entanto, neurologia reivindica a maior trajetória de crescimento a uma CAGR de 25,62% até 2030. Capsídeos emergentes que cruzam a barreira hematoencefálica e ferramentas precisas de edição in vivo permitem intervenção direta em distúrbios como síndrome de Rett e doença de Huntington. O tamanho do mercado de terapia gênica alocado para distúrbios do SNC deve se multiplicar à medida que incentivos regulamentadores bilaterais comprimem o risco de desenvolvimento.
Indicações metabólicas raras e oftalmológicas continuam a render novas aprovações porque o privilégio imunológico tecidual e biomarcadores claros simplificam endpoints clínicos. Alvos cardiovasculares como cardiomiopatia hipertrófica estão ganhando financiamento de venture capital, sugerindo captação mais ampla de doenças sistêmicas. À medida que a amplitude terapêutica se amplia, a otimização de portfólio torna-se crítica; patrocinadores devem equilibrar fluxos de caixa de oncologia com ativos de neurologia de alto potencial, mas cientificamente complexos.
Por Modo de Entrega: In Vivo Domina Enquanto Ex Vivo Ganha Momentum
A administração direta comandou 65,92% da receita em 2024, principalmente devido a aprovações para distúrbios oculares, musculares e hepáticos onde a injeção localizada maximiza a eficiência do vetor. A dosagem in vivo elimina etapas de processamento celular, encurta cronogramas de tratamento e se adapta aos fluxos de trabalho hospitalares existentes, mantendo assim sua liderança. No entanto, a engenharia ex vivo está no caminho para uma CAGR de 23,07% à medida que automação de fabricação, transdução viral melhorada e plataformas alogênicas reduzem custos por paciente. O pipeline crescente de células imunes engenheiradas para doenças autoimunes mostra versatilidade ex vivo além da oncologia. Como tal, o mercado de terapia gênica se beneficia do crescimento complementar em ambos os canais de entrega, reduzindo dependência excessiva de qualquer modalidade única e suavizando requisitos da cadeia de suprimentos.
Protocolos ex vivo otimizados agora alcançam maior viabilidade celular e eficiência de transferência gênica, fatores que anteriormente dificultavam resultados clínicos. Estratégias de escala e produção no ponto de atendimento reduzem ainda mais a complexidade logística, estabelecendo as bases para centros de infusão baseados na comunidade. Com o tempo, a convergência de custos entre modalidades pode encorajar patrocinadores a selecionar entrega baseada apenas na adequação biológica em vez de praticabilidade de fabricação.
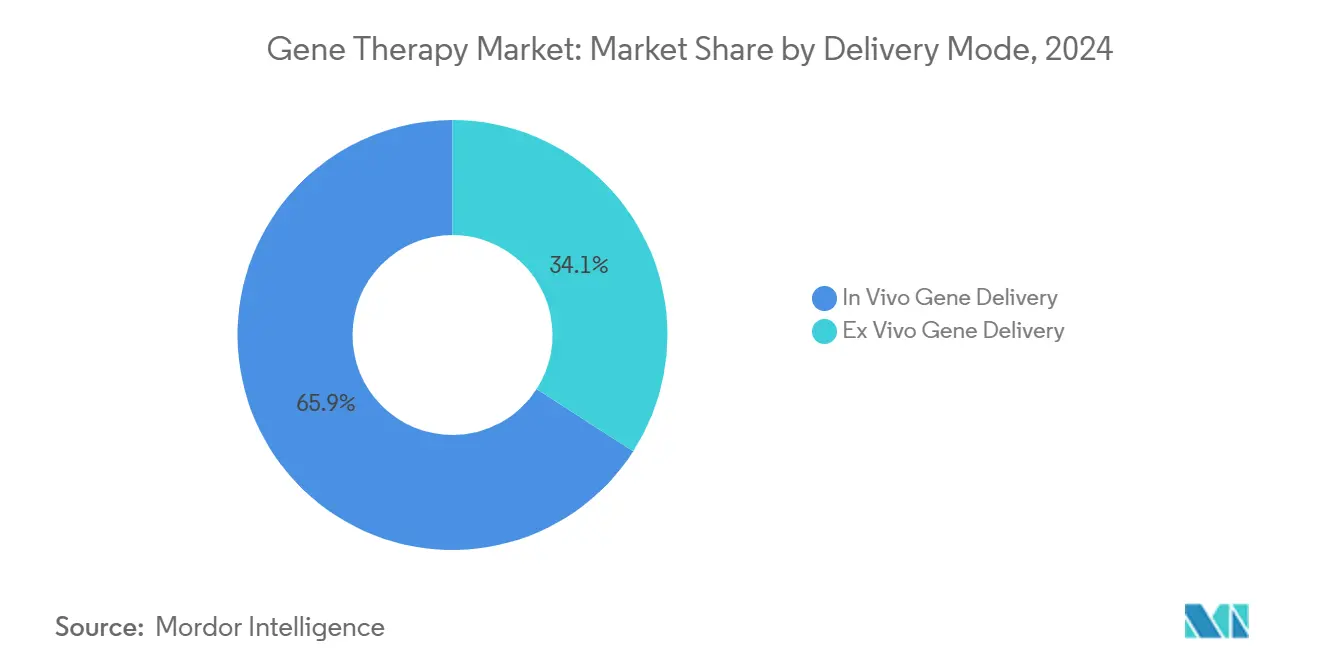
Nota: Participações de segmento de todos os segmentos individuais disponíveis na compra do relatório
Por Usuário Final: Hospitais Lideram Enquanto Centros Especializados Expandem Rapidamente
Hospitais e centros médicos acadêmicos representaram 59,22% do volume de administração em 2024 porque possuem equipes multidisciplinares e ambientes controlados necessários para infusão de terapia gênica. Essas instituições frequentemente servem como locais de ensaio, criando transição perfeita do estudo para padrão de cuidado. No entanto, instalações especializadas de infusão são projetadas para crescer a 21,89% CAGR até 2030. Seus modelos operacionais enxutos reduzem custos do local de cuidado e melhoram a conveniência do paciente, particularmente onde a distância de viagem para centros terciários é uma barreira. O tamanho do mercado de terapia gênica capturado por centros dedicados está, portanto, posicionado para subir à medida que pagadores incentivam configurações de menor custo.
Institutos de pesquisa acadêmica mantêm influência hospedando estudos first-in-human e refinando protocolos de fabricação. Hospitais comunitários estão gradualmente integrando fluxos de trabalho de tratamento validados, ajudados por plataformas de monitoramento remoto que minimizam visitas hospitalares repetidas. A expansão do cuidado descentralizado amplia o acesso regional e apoia maior throughput processual, abordando uma restrição crítica de capacidade à medida que mais produtos ganham aprovação.
Análise Geográfica
A América do Norte deteve 41,78% da receita global em 2024, sustentada por um ambiente regulamentador acomodativo, pools profundos de venture capital e extensa infraestrutura clínica. Os Estados Unidos aprovaram 34 terapias gênicas first-in-class apenas em 2024, destacando seu papel central no sequenciamento de lançamento de produtos. Iniciativas federais como subsídios ARPA-H canalizam fundos significativos para inovação de fabricação e vigilância de segurança, reforçando a liderança da região no mercado de terapia gênica.
A Europa mantém forte produção científica e se beneficia das vias adaptativas da EMA que expedem tratamentos revolucionários. A estrutura futura do Reino Unido para fabricação descentralizada, efetiva em julho de 2025, pode reduzir encargos logísticos e estimular produção no ponto de atendimento. No entanto, políticas nacionais de reembolso desiguais prolongam o tempo até o paciente em todo o bloco; a nova regulamentação de Avaliação de Tecnologia de Saúde da UE em 2025 visa harmonizar requisitos de evidência, mas também pode prolongar negociações. Modelos de pagamento baseados em resultados, como demonstrado por acordos Hemgenix na Inglaterra e Dinamarca, estão gradualmente facilitando obstáculos de adoção.
A Ásia-Pacífico registra o crescimento mais rápido a uma CAGR de 27,68%. A China hospeda mais de 400 estudos baseados em células e investe pesadamente em plantas de vetores domésticas, posicionando-se como motor tanto de demanda quanto de suprimento. As vias aceleradas do Japão para medicamentos regenerativos e o portal de licenciamento digital de Singapura agilizam ainda mais as aprovações. Embora os padrões regulamentadores convirjam com agências ocidentais, reembolso variável e controles de exportação em materiais genéticos permanecem desafios. O apoio político contínuo e CDMOs locais amadurecendo asseguram que a Ásia-Pacífico capturará uma proporção crescente do mercado de terapia gênica.
Panorama Competitivo
Principais Empresas no Mercado de Terapia Gênica
O terreno competitivo é moderadamente fragmentado, povoado por farmacêuticas incumbentes experientes e inovadores biotecnológicos ágeis. Casas de grande farmacêutica como Novartis, Pfizer e Roche estão adquirindo tecnologias de plataforma para compensar penhascos de patentes; a parceria da Novo Nordisk com 2seventy bio exemplifica diversificação de portfólio em edição gênica. A atividade de parceria alcançou 90 acordos no Q1 2025, refletindo prospecção intensa por engenharia de capsídeos, entrega não viral e fabricação escalável.
A diferenciação tecnológica impulsiona vantagem competitiva. A Krystal Biotech alavanca um vetor HSV-1 proprietário permitindo administração tópica repetida; seu produto VYJUVEK gerou USD 341,2 milhões desde o lançamento e alcançou 97% de cobertura dos EUA, demonstrando prova comercial de aplicações dermatológicas de doenças raras. A integração de IA é outro campo de batalha: a joint venture da MeiraGTx com Hologen Neuro AI aplica loops de design de deep learning a capsídeos do SNC, enquanto a Amgen relatou um aumento de receita de 19% em 2024 auxiliado por cargas de RNA engenheiradas que capitalizam na otimização guiada por aprendizado de máquina.
Oportunidades de espaço em branco incluem expansão de capacidade de vetores, indicações não oncológicas direcionadas e estruturas de financiamento inovadoras que correspondem benefícios de terapia única com economias de custo multi-anuais. Organizações de desenvolvimento e fabricação contratadas oferecendo serviços turnkey, agnósticos de plataforma, estão posicionadas para ganhar participação à medida que patrocinadores menores terceirizam produção. À medida que o pipeline se diversifica e caminhos de aprovação regionais proliferam, o mercado de terapia gênica recompensa jogadores que combinam profundidade científica com agilidade da cadeia de suprimentos.
Líderes da Indústria de Terapia Gênica
-
Gilead Sciences, Inc.
-
Amgen Inc.
-
Novartis AG
-
bluebird bio Inc.
-
Biogen Inc.
- *Isenção de responsabilidade: Principais participantes classificados em nenhuma ordem específica
Desenvolvimentos Recentes da Indústria
- Maio de 2025: Sarepta Therapeutics, Inc., líder em medicina genética de precisão para doenças raras, garantiu aprovação pivotal do Ministério da Saúde, Trabalho e Bem-Estar do Japão (MHLW) para seu medicamento, ELEVIDYS (delandistrogene moxeparvovec). Esta aprovação, concedida sob o caminho condicional e limitado no tempo do Japão, visa a distrofia muscular de Duchenne (DMD). Especificamente, ELEVIDYS é sancionado para crianças de 3 a menos de 8 anos, desde que não tenham deleções no exon 8 e/ou exon 9 do gene DMD e testem negativo para anticorpos anti-AAVrh74. Notavelmente, isso marca o primeiro endosso global para tratar DMD em crianças menores de 4 anos.
- Maio de 2025: Abeona Therapeutics recebeu aprovação da FDA para ZEVASKYN, a primeira terapia gênica baseada em células para epidermólise bolhosa distrófica recessiva (RDEB), demonstrando cicatrização efetiva de feridas em ensaios clínicos.
- Fevereiro de 2025: Genprex, Inc., uma empresa de terapia gênica em estágio clínico, está fazendo progressos em seu programa de terapia gênica para diabetes, reforçado por uma colaboração com a Universidade de Pittsburgh. As duas entidades simplificaram os acordos de licença anteriores da Genprex com Pitt em um único acordo exclusivo. Este novo pacto abrange múltiplas tecnologias voltadas para criar um produto de terapia gênica para diabetes Tipo 1 e Tipo 2. Além disso, a Genprex estabeleceu uma subsidiária integral, Convergen Biotech, Inc., dedicada ao avanço de suas iniciativas de diabetes.
- Outubro de 2024: O Governador Hochul anunciou um desenvolvimento significativo para o mercado de terapia gênica com o lançamento da próxima fase do New York Biogenesis Park de Long Island, um centro de inovação de terapia celular e gênica líder nacional. Este projeto de USD 430 milhões visa acelerar pesquisa, desenvolvimento e comercialização de terapias que salvam vidas. O compromisso de USD 150 milhões do estado marca o maior investimento estadual em terapia celular e gênica nacionalmente, avançando ainda mais a visão de Nova York de estabelecer liderança neste campo crítico.
- Setembro de 2024: Genprex, Inc., uma empresa de terapia gênica em estágio clínico dedicada a pioneirar terapias transformadoras para pacientes com câncer e diabetes, revelou planos para transferir seu programa de desenvolvimento clínico de diabetes e ativos de terapia gênica associados para uma subsidiária integral recém-estabelecida. Esta nova entidade, apelidada de "NewCo", focará no avanço e comercialização de GPX-002, um candidato a terapia gênica visando diabetes Tipo 1 (T1D) e Tipo 2 (T2D).
Escopo do Relatório Global do Mercado de Terapia Gênica
Conforme o escopo deste relatório, terapia gênica é um tratamento médico avançado que envolve a transferência de um gene padrão ou saudável para substituir um gene defeituoso em uma célula. Pode curar vários distúrbios crônicos e genéticos em seres humanos, para os quais nenhuma cura final foi desenvolvida. O mercado é segmentado por Indicação (Câncer, Distúrbios Metabólicos, Distúrbios Oculares, Atrofia Muscular Espinhal e Outras Indicações), Tecnologia (Vetor de Adenovírus, Vetor de Vírus Adeno-associado, Vetor Lentiviral, Vetor Retroviral, Vetor de Vírus Herpes e Outras Tecnologias) e Geografia (América do Norte, Europa, Ásia-Pacífico, Oriente Médio e África e América do Sul). O relatório de mercado também cobre os tamanhos de mercado estimados e tendências para 17 países em grandes regiões globalmente. O relatório oferece o valor (em milhões de USD) para os segmentos acima.
| Vetor de Adenovírus |
| Vetor de Vírus Adeno-associado |
| Vetor Lentiviral |
| Vetor Retroviral |
| Vetor de Vírus Herpes |
| Outros Tipos de Vetores |
| Oncologia |
| Distúrbios Metabólicos Raros |
| Oftalmologia |
| Neurologia / SNC |
| Cardiovascular e Musculoesquelético |
| Outras Indicações |
| Entrega Gênica In Vivo |
| Entrega Gênica Ex Vivo |
| Hospitais e Clínicas |
| Centros de Tratamento Especializado / Infusão |
| Institutos Acadêmicos e de Pesquisa |
| América do Norte | Estados Unidos |
| Canadá | |
| México | |
| Europa | Alemanha |
| Reino Unido | |
| França | |
| Itália | |
| Espanha | |
| Resto da Europa | |
| Ásia-Pacífico | China |
| Japão | |
| Índia | |
| Austrália | |
| Coreia do Sul | |
| Resto da Ásia-Pacífico | |
| Oriente Médio e África | CCG |
| África do Sul | |
| Resto do Oriente Médio e África | |
| América do Sul | Brasil |
| Argentina | |
| Resto da América do Sul |
| Por Tipo de Vetor | Vetor de Adenovírus | |
| Vetor de Vírus Adeno-associado | ||
| Vetor Lentiviral | ||
| Vetor Retroviral | ||
| Vetor de Vírus Herpes | ||
| Outros Tipos de Vetores | ||
| Por Indicação | Oncologia | |
| Distúrbios Metabólicos Raros | ||
| Oftalmologia | ||
| Neurologia / SNC | ||
| Cardiovascular e Musculoesquelético | ||
| Outras Indicações | ||
| Por Modo de Entrega | Entrega Gênica In Vivo | |
| Entrega Gênica Ex Vivo | ||
| Por Usuário Final | Hospitais e Clínicas | |
| Centros de Tratamento Especializado / Infusão | ||
| Institutos Acadêmicos e de Pesquisa | ||
| Por Geografia | América do Norte | Estados Unidos |
| Canadá | ||
| México | ||
| Europa | Alemanha | |
| Reino Unido | ||
| França | ||
| Itália | ||
| Espanha | ||
| Resto da Europa | ||
| Ásia-Pacífico | China | |
| Japão | ||
| Índia | ||
| Austrália | ||
| Coreia do Sul | ||
| Resto da Ásia-Pacífico | ||
| Oriente Médio e África | CCG | |
| África do Sul | ||
| Resto do Oriente Médio e África | ||
| América do Sul | Brasil | |
| Argentina | ||
| Resto da América do Sul | ||
Principais Perguntas Respondidas no Relatório
Qual é o valor atual do mercado de terapia gênica?
O mercado de terapia gênica está avaliado em USD 9,74 bilhões em 2025 e está projetado para subir para USD 24,34 bilhões até 2030.
Qual tipo de vetor lidera as vendas globais?
Vetores de Vírus Adeno-associado respondem por 38,54% da receita de 2024 devido ao seu perfil de segurança e expressão duradoura.
Por que a Ásia-Pacífico está crescendo tão rapidamente?
A Ásia-Pacífico registra uma CAGR de 27,68% devido ao forte financiamento governamental, volume crescente de ensaios clínicos na China e caminhos de aprovação simplificados no Japão e Singapura.
Como os pagadores estão gerenciando altos custos de terapia?
Sistemas de saúde empregam contratos baseados em resultados, pagamentos amortizados e modelos de compra agrupada estadual como o Modelo de Acesso a Terapia Celular e Gênica do CMS.
Qual fator mais limita o crescimento do mercado hoje?
A complexidade de fabricação e suprimento limitado de vetores grau GMP continuam a limitar a disponibilidade de produtos de curto prazo e elevar o custo dos produtos.
Página atualizada pela última vez em:



