Taille et part du marché de la génomique spatiale et de la transcriptomique

Analyse du marché de la génomique spatiale et de la transcriptomique par Mordor Intelligence
La taille du marché de la génomique spatiale et de la transcriptomique s'élève à 673 millions USD en 2025 et est en passe d'atteindre 1 207,39 millions USD d'ici 2030, affichant un TCAC de 12,40 %. Cette forte augmentation reflète la demande croissante des entreprises pharmaceutiques qui s'appuient désormais sur le contexte spatial pour expliquer les interactions cellulaires au sein de tissus intacts. L'intégration constante de l'intelligence artificielle avec les plateformes de biologie spatiale permet l'identification automatisée des types cellulaires, une découverte de biomarqueurs plus riche et des flux de travail translationnels plus rapides. Les initiatives au niveau des consortiums, y compris le NIH BRAIN Cell Census Network, ont sécurisé un financement public à long terme et consolidé la pertinence de recherche de la technologie. Simultanément, les instruments de séquençage de quatrième génération repoussent les seuils de débit et de coût, élargissant la faisabilité clinique. Les acquisitions stratégiques telles que Bruker-NanoString et la transaction en cours Quanterix-Akoya signalent que les solutions spatiales clé en main attirent des valorisations premium et accélèrent la consolidation des plateformes. Dans l'ensemble, l'intensité concurrentielle se déplace vers la différenciation logicielle et les partenariats d'écosystème.
Principales conclusions du rapport
- Par technologie, la transcriptomique spatiale détenait 54,8 % de la part de marché de la génomique spatiale et de la transcriptomique en 2024, tandis que la génomique spatiale devrait se développer à un TCAC de 23,0 % jusqu'en 2030.
- Par produit, les consommables représentaient 46,3 % de la part de la taille du marché de la génomique spatiale et de la transcriptomique en 2024 ; les logiciels devraient enregistrer un TCAC de 21,4 % jusqu'en 2030.
- Par type d'échantillon, le tissu FFPE menait avec une part de 49,1 % du marché de la génomique spatiale et de la transcriptomique en 2024, tandis que les organoïdes et cultures 3D progressent à un TCAC de 24,6 %.
- Par application, l'oncologie représentait 47,6 % du marché de la génomique spatiale et de la transcriptomique en 2024 ; l'immunologie et les maladies infectieuses représentent la trajectoire la plus rapide, avec un TCAC de 22,2 % jusqu'en 2030.
- Par utilisateur final, les entreprises pharmaceutiques et biotechnologiques contrôlaient 44,8 % du marché de la génomique spatiale et de la transcriptomique en 2024, les CRO et laboratoires de diagnostic croissant à un TCAC de 20,5 %.
- Par géographie, l'Amérique du Nord menait avec une part de 46,6 % du marché des désinfectants de surface en 2024, tandis que l'Asie-Pacifique devrait enregistrer la croissance la plus rapide à un TCAC de 23,4 % entre 2025 et 2030.
Tendances et perspectives du marché mondial de la génomique spatiale et de la transcriptomique
Analyse d'impact des moteurs
| Moteur | (~) % d'impact sur les prévisions TCAC | Pertinence géographique | Calendrier d'impact |
|---|---|---|---|
| Potentiel émergent des analyses spatiales comme diagnostics du cancer | +2.80% | Mondial, avec adoption précoce en Amérique du Nord et UE | Moyen terme (2-4 ans) |
| Avancées rapides en imagerie haute résolution et chimies de code-barres | +2.10% | Mondial, concentré dans les pôles technologiques | Court terme (≤ 2 ans) |
| Avènement des plateformes de séquençage de quatrième génération | +1.90% | Cœur Amérique du Nord et UE, expansion vers APAC | Moyen terme (2-4 ans) |
| Adoption croissante de la multi-omique unicellulaire dans la découverte de médicaments | +2.30% | Centres pharmaceutiques mondiaux | Court terme (≤ 2 ans) |
| Pipelines de pathologie spatiale activés par l'IA | +1.70% | Régions technologiquement avancées mondialement | Long terme (≥ 4 ans) |
| Chimies de capture in-situ compatibles FFPE | +1.60% | Environnements cliniques mondiaux | Moyen terme (2-4 ans) |
| Source: Mordor Intelligence | |||
Potentiel émergent des analyses spatiales comme diagnostics du cancer
Les technologies d'analyse spatiale transforment les diagnostics du cancer en révélant les complexités du microenvironnement tumoral que la génomique traditionnelle ne peut capturer. Des études récentes utilisant la transcriptomique spatiale Visium HD ont identifié des sous-populations distinctes de macrophages avec des fonctions pro-tumorales dans le cancer colorectal, démontrant comment le contexte spatial influence les stratégies de ciblage thérapeutique.[1]Stephane Plaisance, "La transcriptomique spatiale dissèque les niches tumeur-immune," Nature Genetics, nature.com La capacité de la technologie à cartographier les interactions cellulaires à résolution unicellulaire permet des approches d'oncologie de précision qui associent les patients aux immunothérapies basées sur des signatures de biomarqueurs spatiaux plutôt que sur la génétique tumorale en vrac. Les études de validation clinique montrent que la transcriptomique spatiale peut prédire les réponses aux traitements dans le cancer du foie et caractériser des microenvironnements tumoraux complexes dans le glioblastome, soutenant directement les voies de développement de diagnostics compagnons FDA. Ce potentiel diagnostique s'étend au-delà des applications de recherche, avec des entreprises pharmaceutiques intégrant l'analyse spatiale dans la conception d'essais cliniques pour identifier les populations de patients les plus susceptibles de répondre aux thérapies ciblées. La convergence de la biologie spatiale avec les flux de travail de pathologie pilotés par l'IA promet de révolutionner le diagnostic du cancer en fournissant aux cliniciens des insights sans précédent sur la biologie tumorale et les mécanismes de résistance au traitement.
Avancées rapides en imagerie haute résolution et chimies de code-barres
Les percées technologiques en résolution d'imagerie et code-barres moléculaire étendent les capacités de transcriptomique spatiale au-delà des limitations actuelles. Le dévoilement par Illumina de la technologie de transcriptomique spatiale de nouvelle génération en février 2025 promet une résolution cellulaire avec des zones de capture neuf fois plus grandes que les solutions existantes, permettant l'analyse de millions de cellules en une seule expérience. Les chimies de code-barres avancées supportent désormais la détection simultanée d'ARN et de protéines, avec le flux de travail multi-omique RNAscope sans protéase de Bio-Techne préservant la morphologie tissulaire tout en permettant un profilage moléculaire complet. Ces avancées traitent des goulots d'étranglement critiques dans l'analyse spatiale, particulièrement le compromis entre résolution et débit qui a limité l'adoption clinique. Les plateformes haute définition comme Visium HD de 10x Genomics atteignent une résolution subcellulaire tout en maintenant des capacités de profilage du transcriptome entier, permettant aux chercheurs d'identifier des phénotypes cellulaires rares et des interactions critiques pour la compréhension des maladies. L'intégration d'imagerie avancée avec des outils d'analyse computationnelle crée des opportunités d'analyse spatiale en temps réel dans les environnements cliniques, transformant potentiellement les flux de travail diagnostiques en oncologie et neurologie.
Avènement des plateformes de séquençage de quatrième génération
Les séquenceurs de quatrième génération tels que le G4X de Singular Genomics traitent plus de 6,2 millions de cellules et 438 millions de transcrits par cellule de flux, redéfinissant le débit pour les essais spatiaux. La chimie Direct-Seq superpose la cartographie des récepteurs des cellules T et B sur le contexte tissulaire, enrichissant les pipelines d'immuno-oncologie. La chimie génome HiFi à faible coût de PacBio abaisse les barrières par échantillon, facilitant les études translationnelles dans les laboratoires hospitaliers. En éliminant la préparation d'échantillons destructive et en supportant la reconstruction 3D, ces systèmes apportent une fidélité sans précédent à l'analyse de l'architecture tissulaire.
Adoption croissante de la multi-omique unicellulaire dans la découverte de médicaments
Les développeurs de médicaments exploitent la multi-omique unicellulaire pour connecter l'action des composés avec les changements moléculaires spatialement résolus. La collaboration d'Absci et Owkin fusionne la conception de médicaments par IA avec des données multi-omiques spatiales pour rationaliser la validation de cibles. Le séquençage VDJ spatial cartographie les dynamiques du répertoire immunitaire à l'intérieur des tumeurs, mettant en évidence des clones spécifiques d'antigène pour l'exploitation thérapeutique.[2]Nikolaus Rajewsky, "LifeTime : Construire un atlas européen de données spatiales unicellulaires," Max Delbrück Center, mdc-berlin.de Une telle profondeur accélère l'optimisation des pistes et réduit l'attrition en phase tardive en révélant les voies de résistance précocement.
Analyse d'impact des contraintes
| Contrainte | (~) % d'impact sur les prévisions TCAC | Pertinence géographique | Calendrier d'impact |
|---|---|---|---|
| Mise en œuvre lente dans les laboratoires cliniques | -1.80% | Mondiale, particulièrement dans les régions à ressources limitées | Moyen terme (2-4 ans) |
| Flux de travail génomiques conventionnels bien établis | -1.40% | Marchés établis en Amérique du Nord et UE | Long terme (≥ 4 ans) |
| Évolutivité du fardeau de stockage de données et de calcul | -1.20% | Mondiale, concentrée dans les applications intensives en données | Court terme (≤ 2 ans) |
| Réactifs à code-barres limités pour les organismes non-modèles | -0.90% | Institutions de recherche mondiales, marchés émergents | Moyen terme (2-4 ans) |
| Source: Mordor Intelligence | |||
Mise en œuvre lente dans les laboratoires cliniques
L'adoption dans les laboratoires de diagnostic traîne parce que les flux de travail spatiaux nécessitent du matériel d'imagerie spécialisé, une bioinformatique avancée et une manipulation tissulaire standardisée. De nombreuses installations manquent de budgets d'équipement et de personnel formé, forçant la dépendance sur des centres de référence. De plus, les codes de remboursement pour les essais spatiaux restent non définis sur plusieurs marchés, limitant le retour sur investissement. La clarté réglementaire autour de la validité analytique et de l'utilité clinique progresse, mais les laboratoires naviguent encore des voies d'approbation incertaines. Jusqu'à ce que l'harmonisation des protocoles arrive à maturité, la variabilité échantillon-à-échantillon peut entraver la reproductibilité des résultats et la confiance des opérateurs.
Flux de travail génomiques conventionnels bien établis
Les hôpitaux ont investi massivement dans les plateformes NGS en vrac et les configurations LIMS adaptées aux essais établis. La transition vers des solutions spatiales exige de ré-ingénierie des pipelines informatiques et de reformation du personnel, créant une inertie même dans les systèmes à hautes ressources. Les dirigeants de laboratoire citent l'intégration avec les dossiers de santé électroniques comme une barrière clé parce que les schémas de données actuels accueillent rarement les coordonnées spatiales multi-couches. Les modèles de pratique conservateurs découragent davantage le remplacement d'essais avec de longs antécédents de validation clinique, malgré des preuves croissantes de la valeur incrémentale de la technologie spatiale.
Analyse des segments
Par technologie : Les plateformes de séquençage dirigent le leadership du marché
La transcriptomique spatiale représentait 54,8 % du marché de la génomique spatiale et de la transcriptomique en 2024, soutenue par une couverture du transcriptome entier et la compatibilité avec les pipelines RNA-seq existants. Les approches basées sur l'imagerie telles que MERFISH et Xenium ajoutent une précision subcellulaire, élargissant l'adoption parmi les neurologues recherchant des détails au niveau synaptique. La génomique spatiale devrait croître à un TCAC de 23,0 %, rétrécissant l'écart alors que les groupes pharmaceutiques réalisent le bénéfice du contexte ADN direct lors du profilage de l'évolution tumorale. La taille du marché de la génomique spatiale et de la transcriptomique pour les plateformes centrées sur le séquençage devrait dépasser les systèmes d'imagerie de 2025 à 2030 en raison de la baisse des coûts de cellules de flux et des flux de travail logiciels intégrés.
La concurrence pivote autour du débit et de la résolution. 10x Genomics étend Xenium à la détection de molécule unique, tandis que Vizgen défend les stratégies de code-barres brevetées. Les acteurs de quatrième génération comme Singular Genomics emploient des cycles de réaction in-situ qui réduisent considérablement les temps d'exécution, défiant les titulaires. L'analytique activée par l'IA reste un différenciateur universel ; les fournisseurs associant le matériel avec des pipelines cloud capturent des revenus de licence récurrents et verrouillent les utilisateurs dans les paramètres de découverte et cliniques.
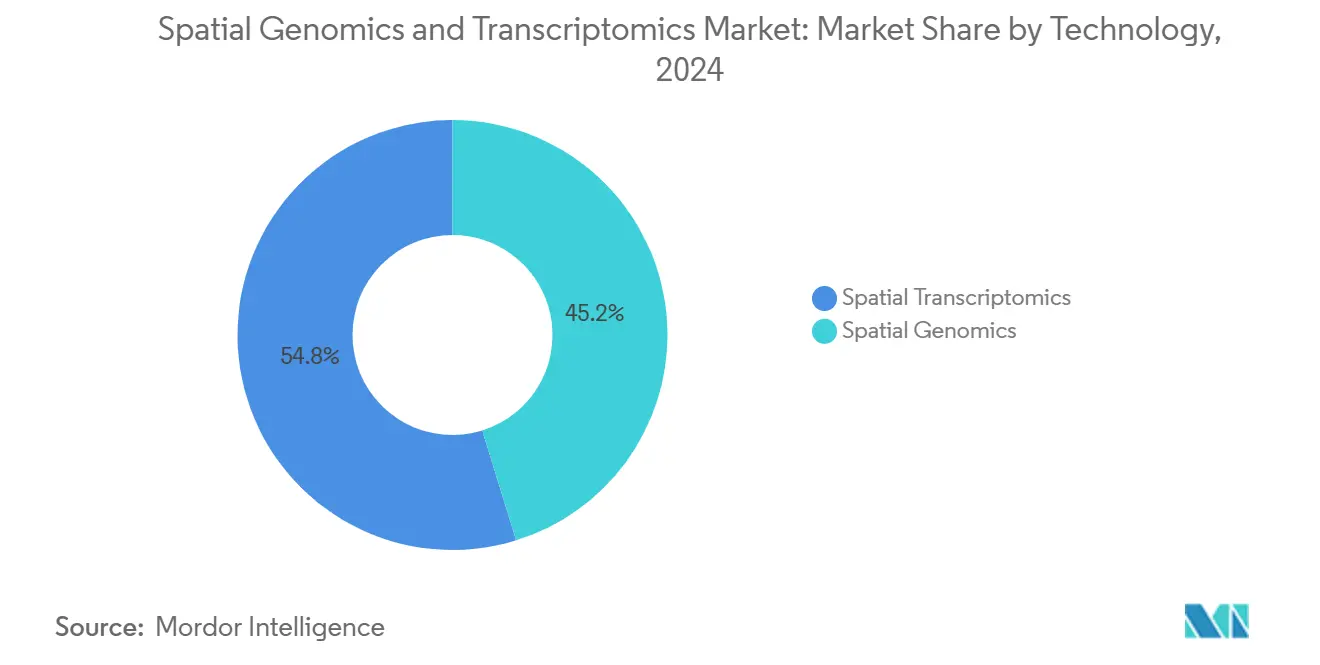
Note: Les parts de segments de tous les segments individuels disponibles à l'achat du rapport
Par produit : L'innovation logicielle accélère la transformation du marché
Les consommables ont généré 46,3 % des revenus du marché de la génomique spatiale et de la transcriptomique en 2024, soutenus par la demande récurrente de sondes, kits de lames et réactifs tissulaires. Les laboratoires traitant des centaines de sections hebdomadairement considèrent les dépenses de réactifs comme le coût opérationnel dominant. Cependant, les logiciels évoluent le plus rapidement à un TCAC de 21,4 % parce que l'expansion des tailles de jeux de données exige une interprétation automatisée. Les modules de segmentation d'image et d'intégration multimodale atteignent des frais d'abonnement qui rivalisent avec les coûts de réactifs par exécution, prouvant leur valeur stratégique. Les ventes d'instruments catalysent l'entrée sur la plateforme mais contribuent à une tranche de revenus plus petite, bien que les placements de matériel verrouillent l'entraînement futur des consommables.
Les développeurs se différencient par des pipelines clé en main. SpatialX de BioTuring combine la réduction de dimensionnalité avec des tableaux de bord intuitifs, réduisant le temps d'analyse pour les non-bioinformaticiens. La livraison cloud abaisse les seuils d'entrée pour les hôpitaux de niveau intermédiaire manquant de calcul sur site. À mesure que les directives réglementaires évoluent, la conformité.
Par type d'échantillon : La compatibilité FFPE stimule l'adoption clinique
Les blocs FFPE représentaient 49,1 % de la part de marché de la génomique spatiale et de la transcriptomique en 2024 parce que la plupart des archives de pathologie hospitalière sont fixées au formol. Les chimies optimisées récupèrent maintenant de l'ARN de haute qualité sans compromettre la morphologie, transformant les biobanques existantes en riches actifs de recherche. Le tissu frais-congelé conserve un rôle dans les programmes de découverte nécessitant de l'ARN intact, mais les améliorations de protocole rétrécissent les écarts de performance. Les organoïdes et cultures 3D présentent une croissance de 24,6 % depuis que les écrans pharmaceutiques favorisent de plus en plus les modèles qui imitent l'architecture in vivo. La taille du marché de la génomique spatiale et de la transcriptomique pour les applications d'organoïdes devrait donc s'étendre régulièrement jusqu'en 2030 alors que les plateformes d'automatisation réduisent la variabilité de culture.
L'adoption de méthodes de tissu clarifié et d'imagerie par nappe de lumière enrichit davantage les flux de travail de culture 3D, permettant l'interrogation complète d'organoïdes sans sectionnement. Les suspensions unicellulaires restent utiles pour valider les sondes de capture et référencer les pipelines analytiques ; cependant, leur manque de coordonnées spatiales limite leur utilité autonome en dehors du développement de méthodes.
Par application : Le leadership en oncologie fait face au défi neurologique
L'oncologie a contribué à 47,6 % des revenus du marché de la génomique spatiale et de la transcriptomique en 2024, une fonction de la cartographie du microenvironnement tumoral et de la stratification de l'immunothérapie. Les pipelines pharmaceutiques s'appuient sur des signatures spatiales pour identifier les répondeurs et surveiller la résistance, intégrant les essais dans chaque essai majeur de tumeur solide. La recherche en immunologie et maladies infectieuses devrait grimper à un TCAC de 22,2 % alors que les laboratoires cartographient la chorégraphie des cellules immunitaires dans les troubles inflammatoires chroniques et la pathogenèse virale. Les cas d'usage en neurologie grimpent fortement alors que les cartes spatiales illuminent la pathogenèse d'Alzheimer et de Parkinson. Le financement NIH de 867 millions USD vers les atlas cérébraux spatiaux assure un élan continu.[3]Instituts nationaux de santé, "Prix de financement du réseau de recensement cellulaire de l'initiative BRAIN," nih.gov
La biologie du développement exploite les outils de suivi de lignée pour décoder les motifs embryonnaires, tandis que les équipes de microbiologie tracent les niches hôte-pathogène pour concevoir des antimicrobiens de précision. Collectivement, les applications émergentes diversifient la base de clients, amortissant les fournisseurs contre les fluctuations de remboursement en oncologie.
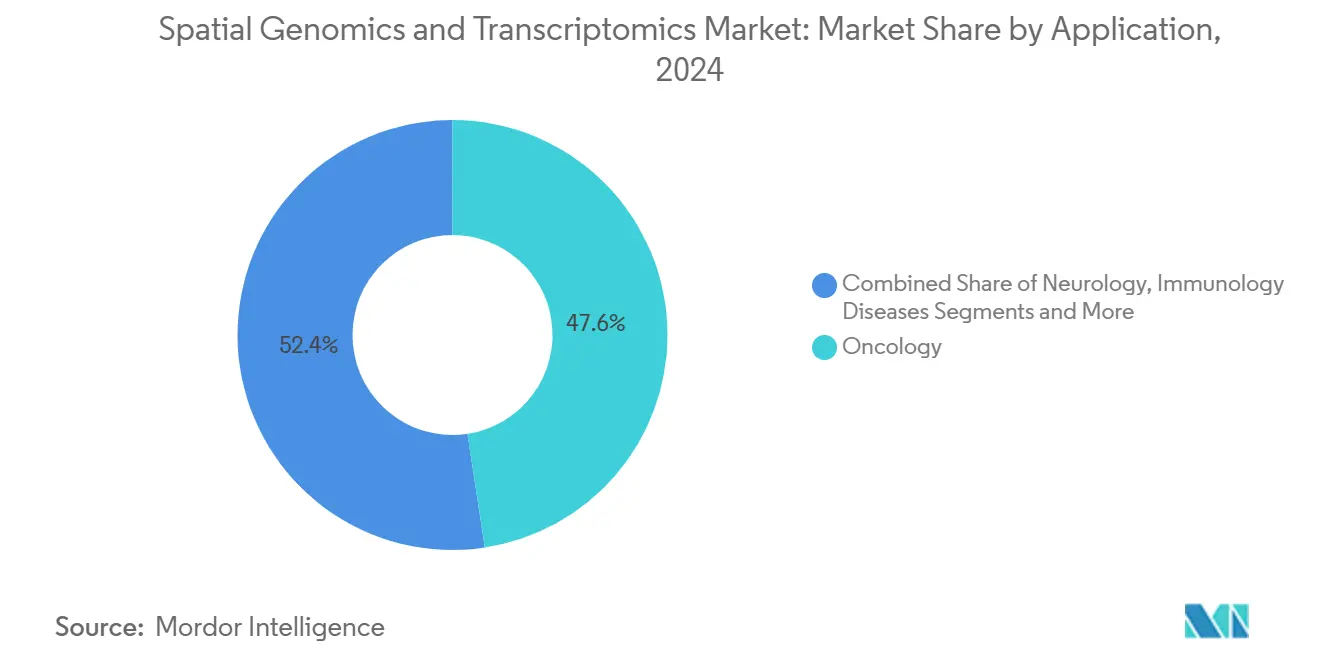
Note: Les parts de segments de tous les segments individuels disponibles à l'achat du rapport
Par utilisateur final : L'intégration pharmaceutique accélère la traduction clinique
Les entreprises pharmaceutiques et biotechnologiques détenaient 44,8 % des revenus du marché de la génomique spatiale et de la transcriptomique en 2024 parce que le profilage spatial à haut débit dé-risque la sélection de cibles et valide le mécanisme d'action. Les CRO et laboratoires de diagnostic s'étendent à un TCAC de 20,5 % alors que la demande d'externalisation croît des petites biotechs manquant de capacités internes. Les centres académiques restent critiques pour l'innovation de méthodes, mais font face à des cycles budgétaires qui influencent la cadence d'achat. L'industrie de la génomique spatiale et de la transcriptomique bénéficie de fournisseurs de services spécialisés offrant des tableaux de bord interactifs qui convertissent les cartes complexes en rapports prêts pour la décision, abaissant le seuil de compétences pour les cliniciens.
Les laboratoires hospitaliers lancent des pilotes diagnostiques précoces, particulièrement dans les centres de cancer tertiaires, mais le remboursement complet déterminera la vitesse de mise à l'échelle. La collaboration entre les entreprises de plateforme et les réseaux de santé intégrés vise à co-développer des packages de preuves cliniques, lissant les soumissions réglementaires.
Analyse géographique
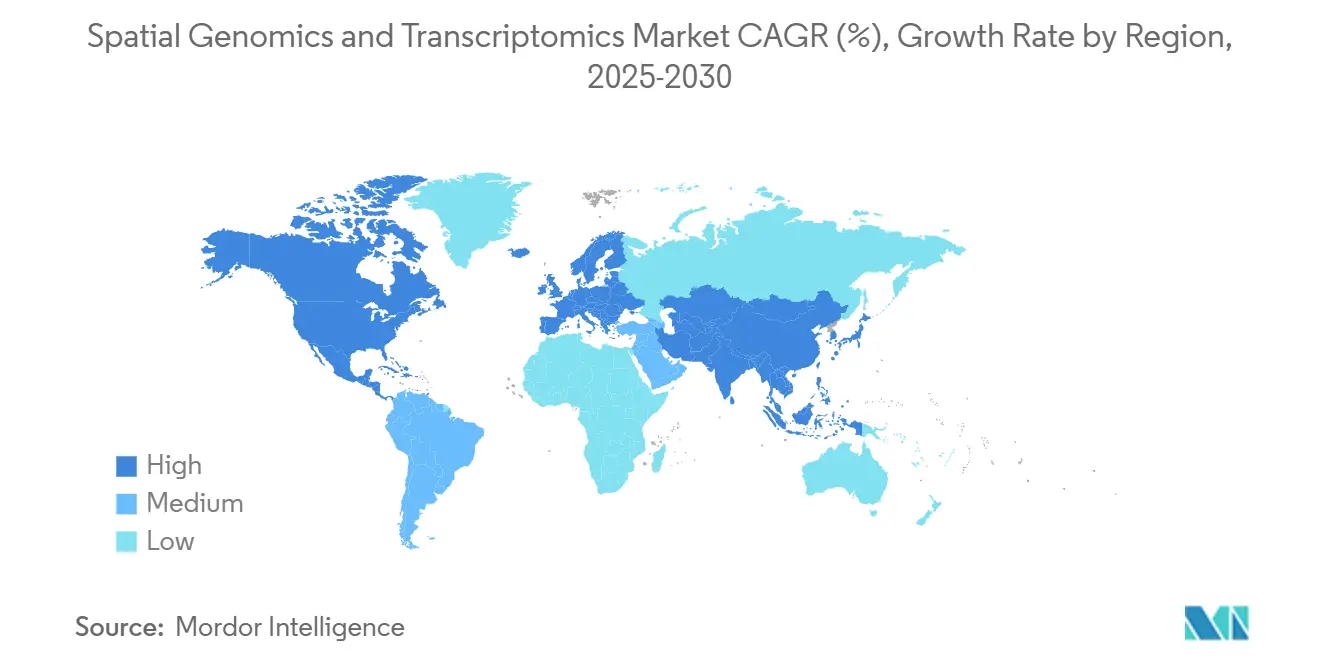
L'Amérique du Nord a mené le marché de la génomique spatiale et de la transcriptomique en 2024, catalysée par les allocations NIH dépassant 867 millions USD qui soutiennent les consortiums multi-centres et les subventions d'équipement. La densité de fournisseurs de plateformes tels que 10x Genomics, Illumina et PacBio assure un accès précoce aux prototypes et au support technique. Le financement robuste de capital-risque continue de faire naître des start-ups de logiciels analytiques, renforçant la maturité de l'écosystème. Les régulateurs américains élaborent des voies de diagnostic compagnon qui, une fois finalisées, pourraient davantage ancrer la dominance régionale.
L'Europe démontre une croissance cohésive à travers des programmes phares comme LifeTime, qui canalise 1 million EUR (1,2 million USD) pour harmoniser la multi-omique spatiale à travers 100 institutions. Les cadres éthiques harmonisés et les accords de partage de données pan-UE rationalisent les études multi-sites. L'Allemagne, le Royaume-Uni et la France hébergent de solides clusters pharmaceutiques qui traduisent les découvertes en essais, tandis que les pays nordiques fournissent l'innovation d'imagerie. Les directives pilotées par l'EMA sur la pathologie numérique devraient raccourcir les cycles d'approbation pour les tests spatiaux, favorisant l'expansion du marché.
L'Asie-Pacifique est la région à croissance la plus rapide alors que les plans nationaux de médecine de précision mettent à l'échelle l'infrastructure génomique. La Chine verse des fonds d'État dans la génomique oncologique, stimulant l'approvisionnement en vrac de plateformes spatiales pour les centres de cancer provinciaux. La démographie vieillissante du Japon élève les budgets de recherche neurodégénérative, stimulant l'adoption d'essais spatiaux centrés sur le cerveau. Les nations d'Asie du Sud-Est intègrent des modules spatiaux dans la surveillance des maladies infectieuses. Bien que les cadres réglementaires pour les tests spatiaux cliniques traînent derrière les homologues occidentaux, la présence croissante de CRO accélère l'externalisation pharmaceutique, alimentant la demande régionale.
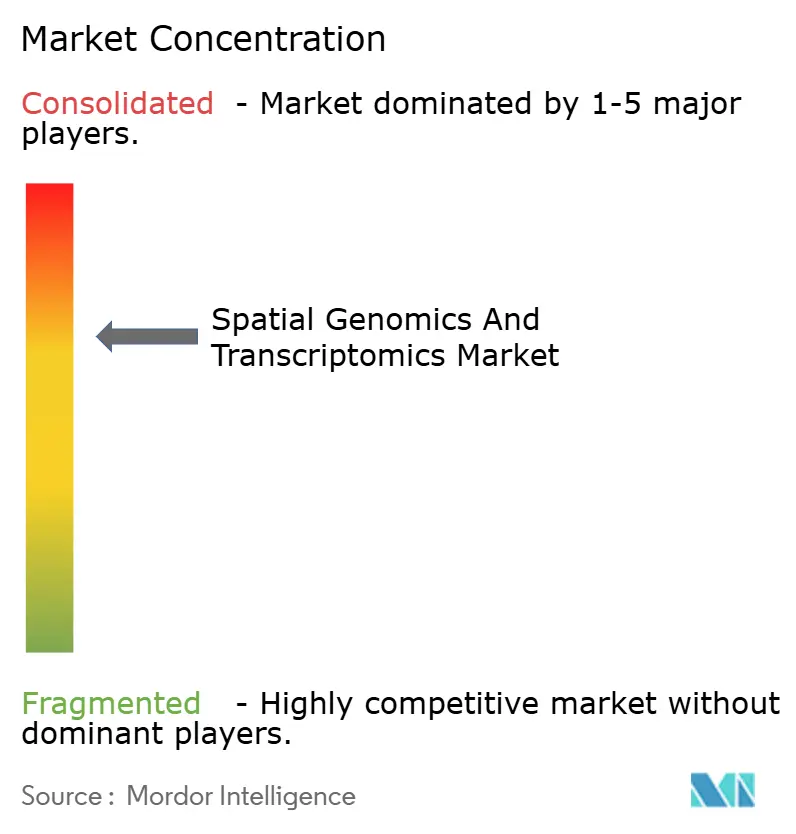
Paysage concurrentiel
Le marché de la génomique spatiale et de la transcriptomique affiche une consolidation modérée. Après l'achat de NanoString pour son portefeuille GeoMx, Bruker s'est élargi dans la co-détection ARN-protéine, intégrant des pipelines d'analyse qui raccourcissent le temps échantillon-à-insight. L'acquisition en cours de Quanterix d'Akoya promet une plateforme de bout en bout s'étendant des essais ultrasensibles basés sur le sang à la protéomique tissulaire. 10x Genomics conserve le leadership en itérant Visium HD et Xenium, exploitant une base installée et un modèle de réactifs en boucle fermée. Les disputes de propriété intellectuelle telles que Vizgen contre 10x indiquent de hautes barrières pour les nouveaux entrants.
Les feuilles de route technologiques convergent sur des plex plus élevés, des temps d'exécution plus rapides et l'analytique pilotée par l'IA. Singular Genomics positionne le débit comme un différenciateur, tandis que PacBio mise sur la précision de lecture.
Les entreprises axées sur les logiciels comme Nucleai s'associent avec les fabricants d'instruments pour regrouper les algorithmes prédictifs, capturant la valeur sans fabriquer de matériel. La capacité de validation clinique reste un goulot d'étranglement ; les entreprises capables de financer des essais multi-sites gagneront l'avantage du premier arrivé dans les diagnostics réglementés.
Leaders de l'industrie de la génomique spatiale et de la transcriptomique
-
10x Genomics
-
NanoString Technologies, Inc.
-
Dovetail Genomics
-
S2 Genomics, Inc.
-
Illumina, Inc.
- *Avis de non-responsabilité : les principaux acteurs sont triés sans ordre particulier
Développements récents de l'industrie
- Juin 2025 : Caris Life Sciences a clôturé un tour de croissance de 168 millions USD pour étendre les offres de médecine de précision et de génomique spatiale.
- Mai 2022 : Quanterix et Akoya Biosciences ont modifié les termes de leur fusion, projetant 40 millions USD de synergies annuelles d'ici 2026.
- Février 2025 : Illumina a dévoilé une plateforme de transcriptomique spatiale avec une zone de capture 9× et une amélioration de résolution 4×, prévue pour un lancement en 2026.
- Février 2025 : Bruker a introduit le panneau CosMx Whole Transcriptome et le visualiseur de génome 3D PaintScape à l'AGBT 2025.
Portée du rapport mondial du marché de la génomique spatiale et de la transcriptomique
Selon la portée de la génomique spatiale et de la transcriptomique, une discipline relativement nouvelle qui implique la détermination de données à haut débit sur la structure organisationnelle du contenu cellulaire à partir d'échantillons de tissus et de cellules Technologie (transcriptomique spatiale et génomique spatiale), Produit (instruments, logiciels et consommables), Utilisateur final (fabricants pharmaceutiques, clients de diagnostic et autres), et Géographie (Amérique du Nord, Europe, Asie-Pacifique, Moyen-Orient et Afrique, et Amérique du Sud) sont les segments du marché de la génomique spatiale et de la transcriptomique. Le rapport de marché couvre également les tailles de marché estimées et les tendances pour 17 pays différents à travers les principales régions mondiales. Le rapport offre la valeur (en millions USD) pour les segments ci-dessus.
| Transcriptomique spatiale | Basé sur le séquençage |
| Basé sur l'imagerie | |
| Génomique spatiale | Séquençage in-situ |
| Hybridation fluorescente in situ (FISH) | |
| Capture in-situ |
| Instruments |
| Consommables |
| Logiciels et services |
| Tissu FFPE |
| Tissu frais-congelé |
| Organoïdes et cultures cellulaires 3D |
| Oncologie |
| Neurologie |
| Immunologie et maladies infectieuses |
| Biologie du développement |
| Découverte et criblage de médicaments |
| Entreprises pharmaceutiques et biotechnologiques |
| Instituts académiques et de recherche |
| CRO et laboratoires de diagnostic |
| Amérique du Nord | États-Unis |
| Canada | |
| Mexique | |
| Europe | Allemagne |
| Royaume-Uni | |
| France | |
| Italie | |
| Espagne | |
| Reste de l'Europe | |
| Asie-Pacifique | Chine |
| Japon | |
| Inde | |
| Corée du Sud | |
| Australie | |
| Reste de l'Asie-Pacifique | |
| Moyen-Orient et Afrique | CCG |
| Afrique du Sud | |
| Reste du Moyen-Orient et Afrique | |
| Amérique du Sud | Brésil |
| Argentine | |
| Reste de l'Amérique du Sud |
| Par technologie | Transcriptomique spatiale | Basé sur le séquençage |
| Basé sur l'imagerie | ||
| Génomique spatiale | Séquençage in-situ | |
| Hybridation fluorescente in situ (FISH) | ||
| Capture in-situ | ||
| Par produit | Instruments | |
| Consommables | ||
| Logiciels et services | ||
| Par type d'échantillon | Tissu FFPE | |
| Tissu frais-congelé | ||
| Organoïdes et cultures cellulaires 3D | ||
| Par application | Oncologie | |
| Neurologie | ||
| Immunologie et maladies infectieuses | ||
| Biologie du développement | ||
| Découverte et criblage de médicaments | ||
| Par utilisateur final | Entreprises pharmaceutiques et biotechnologiques | |
| Instituts académiques et de recherche | ||
| CRO et laboratoires de diagnostic | ||
| Géographie | Amérique du Nord | États-Unis |
| Canada | ||
| Mexique | ||
| Europe | Allemagne | |
| Royaume-Uni | ||
| France | ||
| Italie | ||
| Espagne | ||
| Reste de l'Europe | ||
| Asie-Pacifique | Chine | |
| Japon | ||
| Inde | ||
| Corée du Sud | ||
| Australie | ||
| Reste de l'Asie-Pacifique | ||
| Moyen-Orient et Afrique | CCG | |
| Afrique du Sud | ||
| Reste du Moyen-Orient et Afrique | ||
| Amérique du Sud | Brésil | |
| Argentine | ||
| Reste de l'Amérique du Sud | ||
Questions clés auxquelles répond le rapport
Quelle est la valeur actuelle du marché de la génomique spatiale et de la transcriptomique ?
La taille du marché de la génomique spatiale et de la transcriptomique est de 673 millions USD en 2025.
À quelle vitesse le marché devrait-il croître ?
Il devrait enregistrer un TCAC de 12,40 %, atteignant 1 207,39 millions USD d'ici 2030.
Quel segment technologique mène aujourd'hui ?
La transcriptomique spatiale mène avec 54,8 % des revenus de 2024, grâce aux flux de travail de séquençage établis.
Pourquoi les entreprises pharmaceutiques sont-elles des adopteurs majeurs ?
Elles s'appuient sur le contexte spatial pour sélectionner des cohortes de patients réactifs et dé-risquer les programmes de médicaments, leur donnant 44,8 % de part de marché en 2024.
Qu'est-ce qui limite l'adoption clinique des essais spatiaux ?
Les coûts d'équipement élevés, le manque de protocoles standardisés et les voies de remboursement non définies ralentissent la mise en œuvre en laboratoire.
Dernière mise à jour de la page le:



