Taille et part du marché du marquage protéique
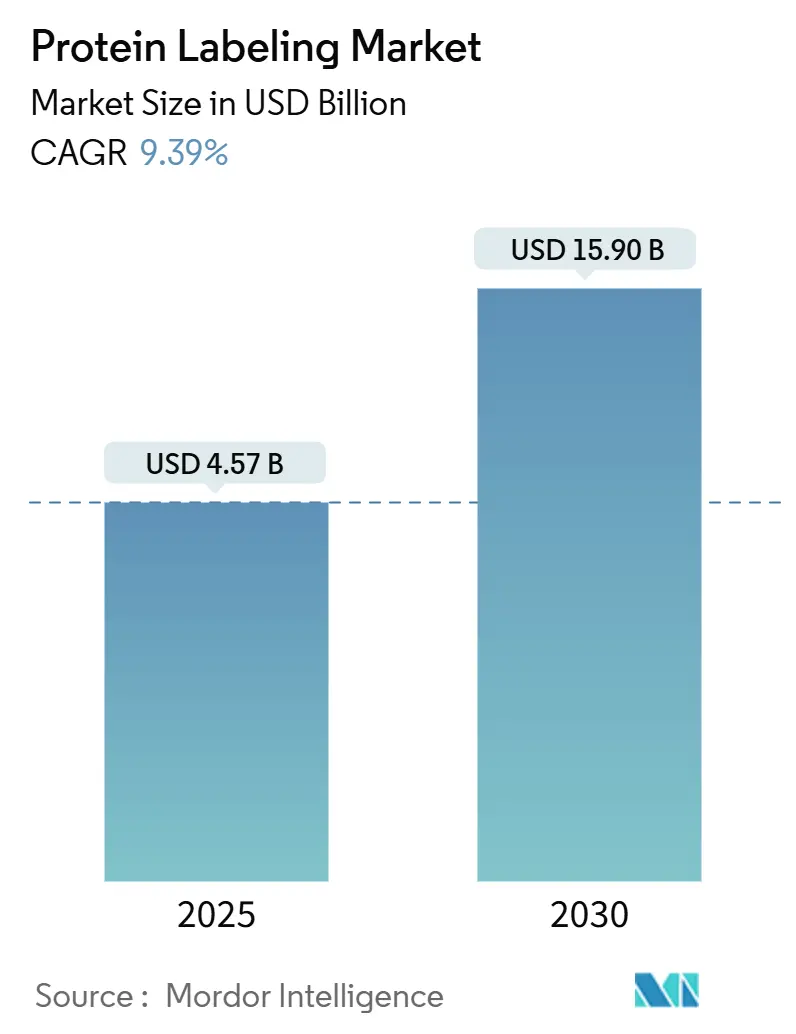
Analyse du marché du marquage protéique par Mordor Intelligence
Le marché du marquage protéique est actuellement valorisé à 2,92 milliards USD en 2025 et devrait atteindre 4,57 milliards USD d'ici 2030, se traduisant par un TCAC stable de 9,39 %. La demande est propulsée par des percées qui permettent des étiquetages spécifiques au site avec un impact minimal sur la conformation protéique, une exigence essentielle pour les flux de travail avancés actuels de protéomique, d'imagerie cellulaire vivante et de biothérapeutique. L'utilisation élargie d'outils d'intelligence artificielle pour la prédiction de structure, un pipeline croissant de conjugués anticorps-médicaments et la migration de tâches complexes de bioconjugaison vers des CDMOs spécialisés élargissent conjointement les opportunités commerciales. Dans le même temps, les plateformes analytiques à forte intensité capitalistique et l'évolution des réglementations autour des conjugués radio-marqués demeurent des obstacles pratiques. L'intensité concurrentielle augmente alors que les acteurs établis cherchent à se différencier via des chimies propriétaires, des modèles de service intégrés et des alliances stratégiques avec les développeurs de médicaments.
Points clés à retenir
- Par type de produit : Les réactifs et kits ont dominé avec 71,13 % de la part de marché du marquage protéique en 2024, tandis que les services devraient s'étendre à un TCAC de 10,47 % jusqu'en 2030.
- Par application : Les techniques immunologiques représentaient 34,37 % de la part de la taille du marché du marquage protéique en 2024, mais les dosages cellulaires progressent à un TCAC de 11,13 % entre 2025-2030.
- Par méthode de marquage : Les approches in vitro détenaient 60,07 % de la taille du marché du marquage protéique en 2024 ; les techniques in vivo croissent plus rapidement à un TCAC de 12,23 %.
- Par utilisateur final : Les entreprises pharmaceutiques et biotechnologiques commandaient 44,90 % de la part de la taille du marché du marquage protéique en 2024, tandis que les CRO/CDMO enregistrent le TCAC projeté le plus élevé à 13,07 % jusqu'en 2030.
- Par géographie : L'Amérique du Nord menait avec 37,90 % de part de revenus en 2024 ; l'Asie-Pacifique devrait afficher le TCAC régional le plus rapide de 11,57 % sur 2025-2030.
Tendances et perspectives du marché mondial du marquage protéique
Analyse d'impact des moteurs
| Contrainte | ( ~ ) % Impact sur les prévisions de TCAC | Pertinence géographique | Calendrier d'impact |
|---|---|---|---|
| Limitations associées aux dosages et méthodes de marquage protéique | -0.7% | Mondial | Moyen terme (2-4 ans) |
| Complexité réglementaire autour des conjugués protéine-radioisotope | -0.6% | Amérique du Nord, Europe, Japon | Long terme (≥ 4 ans) |
| Coût en capital élevé des flux de travail de spectrométrie de masse haute résolution | -0.5% | Marchés émergents, petites institutions de recherche mondiales | Moyen terme (2-4 ans) |
| Durée de conservation limitée et problèmes de stabilité de nombreux réactifs marqués | -0.4% | Mondial, plus prononcé dans les régions avec infrastructure difficile | Court terme (≤ 2 ans) |
| Source: Mordor Intelligence | |||
Expansion de la R&D en protéomique et génomique
Les avancées en spectrométrie de masse haute résolution et en modélisation basée sur l'IA ont fortement augmenté le volume et la profondeur des études de caractérisation protéique. La sortie d'ESM-3 et AlphaFold 3 en 2024 un amélioré la précision de prédiction de structure, permettant aux chercheurs d'identifier des résidus accessibles pour un marquage sélectif haute production. Les programmes de financement aux États-Unis et en Europe privilégient maintenant les pipelines multi-omiques qui dépendent de chimies de marquage robustes pour la quantification et la cartographie spatiale. Ces dynamiques maintiennent une tarification premium pour les sondes de nouvelle génération et annoncent une adoption plus large de flux de travail haute production dans les centres académiques et de médecine translationnelle.
Application croissante dans la découverte et le développement de médicaments
Environ 40 % des médicaments expérimentaux se concentrent maintenant sur des protéines historiquement non-médicamentables, élevant le rôle du marquage homogène et spécifique au site. Les pipelines de conjugués anticorps-médicaments, dépassant actuellement 360 études cliniques, nécessitent des ratios linker-charge précis pour l'efficacité. Les plateformes de dégradation protéique ciblée dépendent de même d'étiquettes cellulaires vivantes qui surveillent la protéolyse en temps réel. Ces cas d'usage élargissent la demande adressable à travers les réactifs, l'instrumentation et les services de conjugaison personnalisée.
Externalisation croissante vers les CDMOs/CRO
Les compagnies pharmaceutiques rationalisent les dépenses d'investissement en déléguant la conjugaison, le remplissage-finition et l'analytique à des partenaires spécialisés. L'accord 2024 de Samsung Biologics pour fournir des services ADC de bout en bout pour AstraZeneca illustre le modèle, assurant l'accès au marquage de grade GMP tout en comprimant les délais. Les fournisseurs d'Asie-Pacifique gagnent du terrain en couplant les efficacités de coût avec des références réglementaires en expansion, accélérant une croissance de revenus à deux chiffres.
Utilisation croissante des techniques basées sur la fluorescence
La microscopie super-résolution atteint maintenant couramment des détails sub-10 nm grâce aux innovations de points quantiques et de colorants organiques[1].Source: "Site-specific protein labeling strategies for super-resolution microscopy," ScienceDirect, sciencedirect.com Les chercheurs intègrent des panneaux multiplexés pour visualiser les réseaux protéiques, stimulant la consommation de réactifs et ajoutant une impulsion aux mises à niveau d'instruments.
Analyse d'impact des contraintes
| Contrainte | ( ~ ) % Impact sur les prévisions de TCAC | Pertinence géographique | Calendrier d'impact |
|---|---|---|---|
| Limitations associées aux dosages et méthodes de marquage protéique | -0.7% | Mondial | Moyen terme (2-4 ans) |
| Complexité réglementaire autour des conjugués protéine-radioisotope | -0.6% | Amérique du Nord, Europe, Japon | Long terme (≥ 4 ans) |
| Coût en capital élevé des flux de travail de spectrométrie de masse haute résolution | -0.5% | Marchés émergents, petites institutions de recherche mondiales | Moyen terme (2-4 ans) |
| Durée de conservation limitée et problèmes de stabilité de nombreux réactifs marqués | -0.4% | Mondial, plus prononcé dans les régions avec infrastructure difficile | Court terme (≤ 2 ans) |
| Source: Mordor Intelligence | |||
Limitations des dosages et méthodes de marquage protéique
Les étiquettes fluorescentes larges au-dessus de 25 kDa ont altéré la localisation sub-cellulaire chez 42 % des protéines testées, et les conjugués nanobody ont montré 38 % de variabilité dans l'efficacité de liaison entre laboratoires. De telles inconsistances augmentent les exigences de validation, prolongent les délais de projet et augmentent l'usage de consommables, particulièrement dans les environnements réglementés.
Obstacles réglementaires pour les conjugués protéine-radioisotope
La supervision par phases de la FDA des tests développés en laboratoire commençant en juillet 2024 introduit de nouveaux points de contrôle de conformité pour les flux de travail radio-marqués[2].Source: "Medical Devices; Laboratory Developed Tests," Federal Register, federalregister.gov Des dispositions comparables dans l'UE augmentent les coûts de documentation et de licence d'installation, restreignant l'adoption aux centres bien financés.
Analyse par segment
Par produit : Les services accélèrent tandis que les réactifs ancrent la croissance
Les réactifs et kits représentaient 71,13 % des revenus du marché du marquage protéique en 2024, soulignant leur rôle essentiel dans les flux de travail quotidiens à travers la découverte, les diagnostics et la fabrication. Les chimies prêtes à l'emploi simplifient la standardisation de protocole et soutiennent la reproductibilité, gardant la demande résiliente même alors que de nouvelles techniques émergent. Les améliorations continues de la luminosité des colorants et des poignées prêtes au clic maintiennent un pouvoir de tarification incrémental et incitent aux achats répétés.
Le segment des services, cependant, dépasse la croissance principale à un TCAC de 10,47 %. Cette poussée reflète la complexité technique croissante de la conjugaison anticorps-médicament, des sondes de dégradation ciblée et des agents d'imagerie animale vivante qui dépassent beaucoup de capacités internes. Les CDMOs ajoutent des suites dédiées de 1 000-2 000 L, comme l'expansion 2024 de Lonza à Visp, pour accommoder la conjugaison de charge à grande échelle et les tâches de remplissage-finition. La taille du marché du marquage protéique pour les projets externalisés devrait s'étendre régulièrement alors que les sponsors de pipeline cherchent des solutions rapides conformes aux GMP.
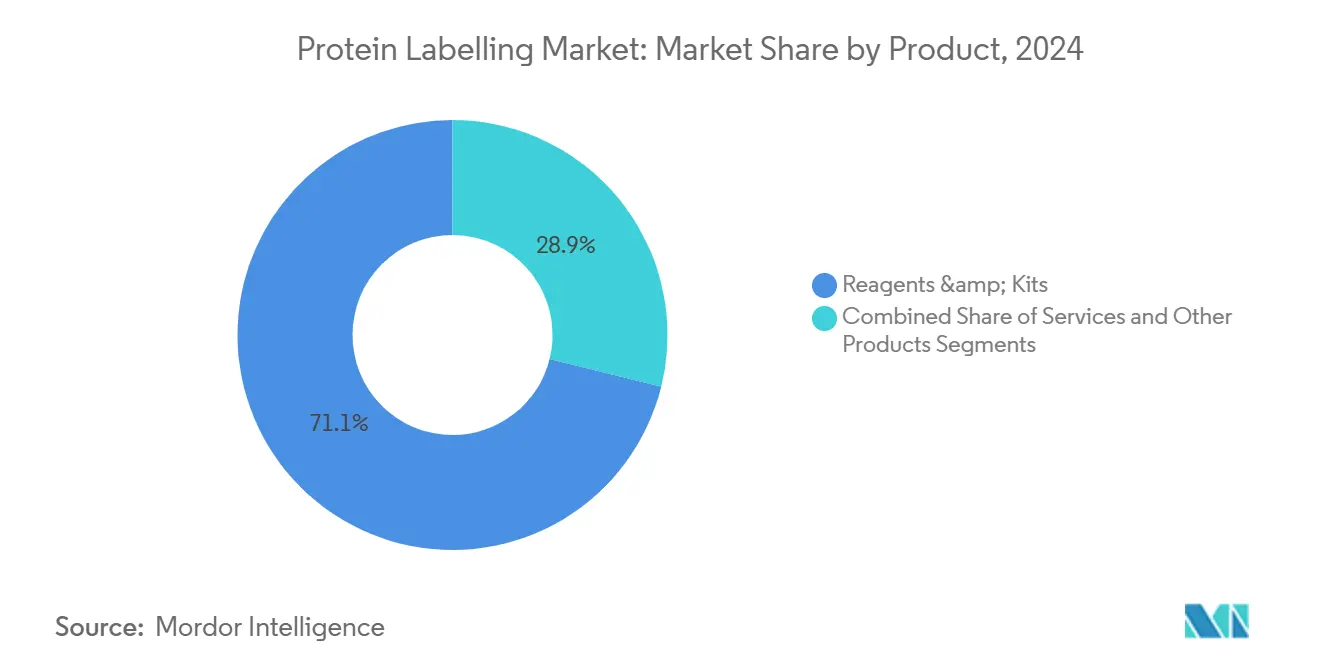
Note: Parts de segment de tous les segments individuels disponibles lors de l'achat du rapport
Par application : Les dosages cellulaires gagnent en dynamisme aux côtés des piliers immunologiques
Les techniques immunologiques sont restées la plus grande tranche du marché du marquage protéique avec une part de 34,37 % en 2024, bénéficiant de décennies d'optimisation en ELISA, Occidental blot et immunohistochimie. Le débit élevé et les protocoles cliniquement validés assurent une pertinence durable dans la vérification de biomarqueurs, les tests de libération de lots et la pathologie de routine.
Les dosages cellulaires, cependant, enregistrent l'avance la plus rapide à 11,13 % de TCAC alors que les chercheurs privilégient les lectures physiologiquement pertinentes en oncologie, neurologie et médecine régénérative. Les portefeuilles de sondes fluorescentes de Thermo Fisher permettent la surveillance en temps réel de l'activation, du trafic et de l'assemblage de complexes des récepteurs. La part de marché du marquage protéique capturée par les plateformes cellulaires vivantes dynamiques devrait s'élargir alors que l'imagerie automatisée et l'analytique haute teneur pénètrent les laboratoires de criblage.
Par méthode de marquage : Les approches in vivo remodèlent la visualisation en temps réel
Les chimies in vitro continuent de dominer avec 60,07 % du marché du marquage protéique en 2024, valorisées pour la stœchiométrie précise et la quantification directe. Les diagnostics et la biologie structurale s'appuient encore fortement sur les modifications de protéines purifiées qui demandent des environnements contrôlés.
Le marquage in vivo enregistre un TCAC plus rapide de 12,23 %, porté par les avancées en expansion de code génétique, marquage médié par enzyme et marquage CuRVE ultra-rapide qui couvre les tissus 3D intacts.[3]Source: "MIT method enables ultrafast protein labeling of tens of millions of cells in 3D tissues," MIT News, news.mit.edu Ces techniques permettent aux chercheurs de cartographier la dynamique protéique dans des contextes cellulaires natifs, critiques pour la neurobiologie et les études de micro-environnement tumoral. La taille du marché du marquage protéique attachée aux applications intracellulaires en temps réel s'élargira donc progressivement jusqu'en 2030.
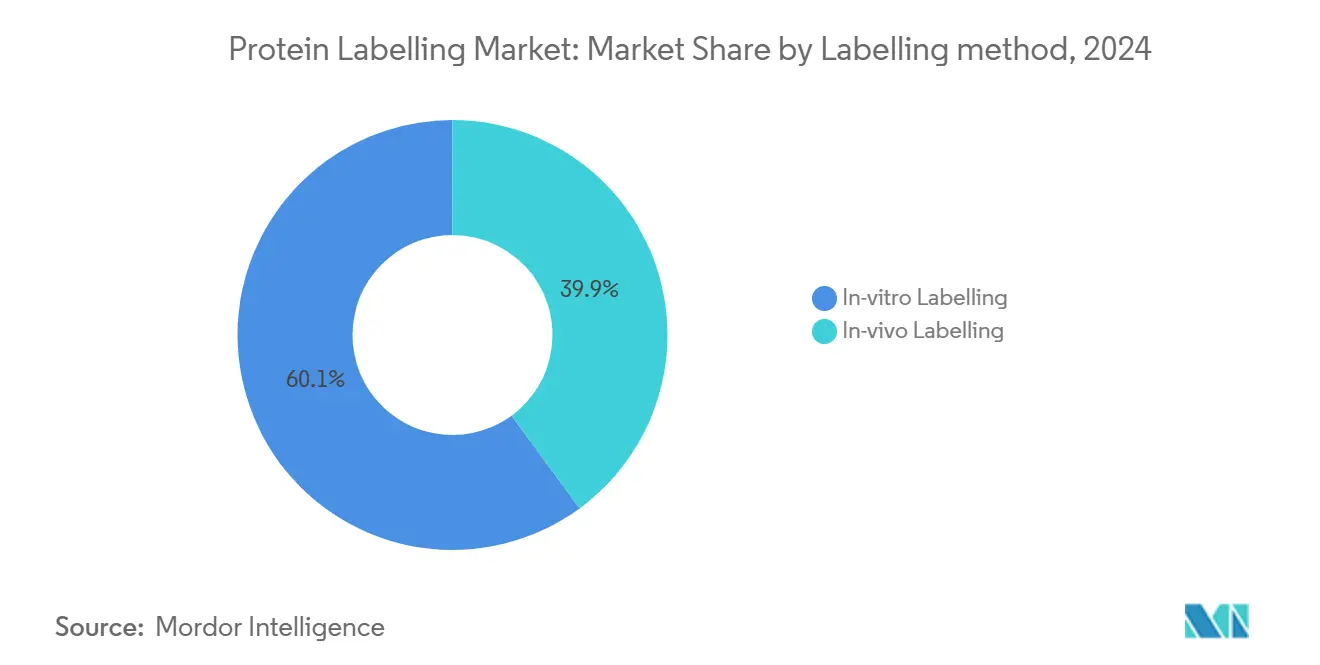
Note: Parts de segment de tous les segments individuels disponibles lors de l'achat du rapport
Par utilisateur final : Les CRO/CDMOs émergent comme moteur de croissance principal
Les firmes pharmaceutiques et biotech détenaient 44,90 % des revenus 2024, validant la centralité du marquage protéique de l'identification de cible au développement en phase tardive. Le financement de capital-risque croissant, comme les 15 millions USD de Série un de Syncell pour étendre sa plateforme de protéomique spatiale Microscoop, injecte une demande fraîche pour les réactifs personnalisés et l'analytique.
Néanmoins, les CRO et CDMOs montrent la montée la plus vive à 13,07 % de TCAC alors que les sponsors externalisent la conjugaison et l'analytique GMP. Les partenariats comme GenNext-Thermo Fisher qui intègrent l'empreinte avancée et la LC-MS Orbitrap combinent les meilleurs outils de classe avec l'expertise réglementaire, cimentant l'attrait du modèle d'externalisation. Les instituts académiques restent des consommateurs essentiels pour les enquêtes fondamentales, tandis que les laboratoires de diagnostics favorisent les immunodosages à délai rapide utilisant des kits de marquage pré-validés.
Analyse géographique
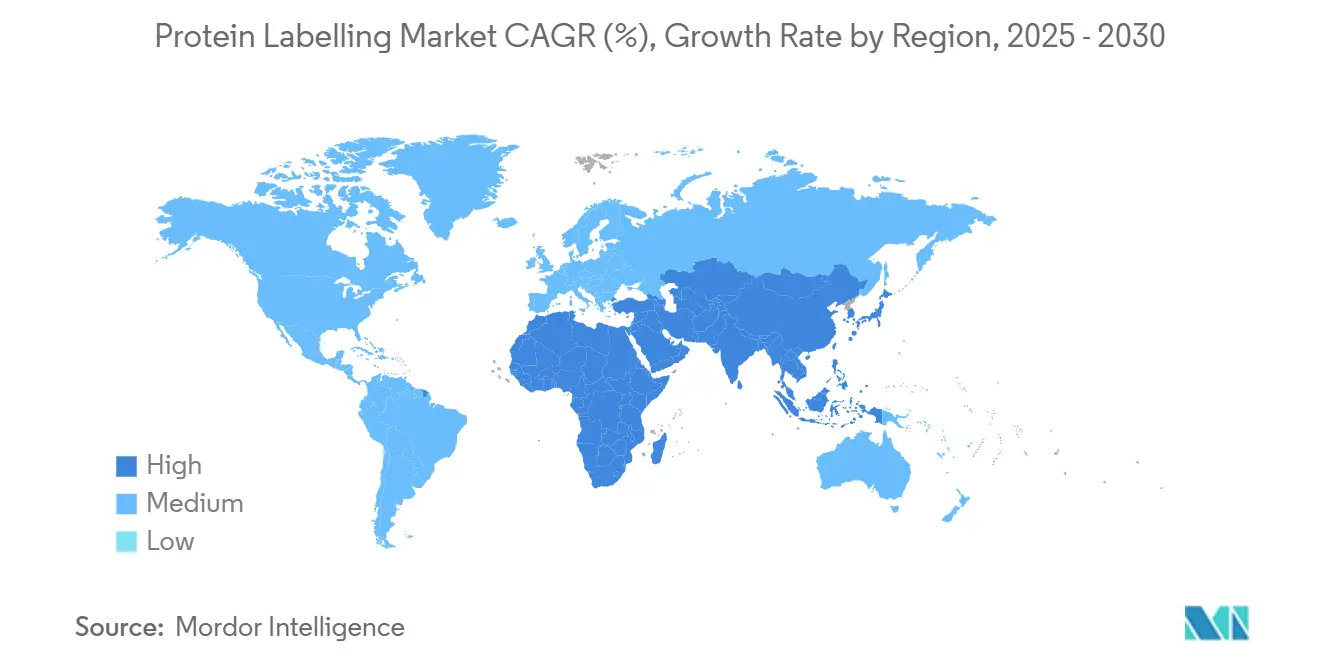
L'Amérique du Nord un généré 37,90 % des revenus 2024, soutenue par un financement NIH robuste, un cluster biopharma dense et une adoption précoce des technologies de marquage de nouvelle génération. La percée CuRVE du MIT, capable de marquer des dizaines de millions de cellules en une seule journée, illustre le leadership régional en méthodologie disruptive[3]Source: "MIT method enables ultrafast protein labeling of tens of millions of cells in 3D tissues," MIT News, news.mit.edu. Une haute cadence d'approbations FDA pour les ADC et radio-immunoconjugués ancre davantage l'élan commercial.
L'Europe se classe seconde, soutenue par les subventions Horizon Europe et de forts corridors de biofabrication en Allemagne, au Royaume-Uni et en France. L'acquisition de Polyplus par Sartorius un étendu les capacités de production de vecteur du continent, nécessitant un marquage avancé pour les protéines d'enveloppe virale. L'harmonisation réglementaire progresse, pourtant les approches divergentes de manipulation de radio-isotopes maintiennent les coûts d'entrée sur le marché élevés.
L'Asie-Pacifique est l'arène à croissance la plus rapide, avançant à un TCAC de 11,57 %. Les CDMOs chinois comme WuXi Biologics rapportent une demande vibrante pour les formats de conjugaison marqués sous WuXiBody et chimies de linker associées. Les politiques industrielles nationales, incluant le 14ème plan quinquennal de Chine et les initiatives BIRAC de l'Inde, canalisent le capital vers l'infrastructure protéomique, bien que l'accès inégal aux plateformes MS haut de gamme persiste. La montée en puissance rapide des installations de conjugués anticorps-médicament de Corée du Sud, soutenue par Samsung Biologics, cimente davantage l'ascension régionale.
Paysage concurrentiel
Les cinq premiers fournisseurs capturent collectivement près de la moitié des revenus mondiaux, pointant vers un champ modérément concentré. Thermo Fisher Scientific mène avec un portefeuille de bout en bout de sondes fluorescentes, kits de chimie click, microscopes et systèmes LC-MS. Merck KGaA suit, exploitant ses marques de réactifs historiques pour fournir des substrats haute pureté pour le marquage bioorthogonal. Les unités Cytiva et Beckman Coulter de Danaher renforcent sa position via des solutions de bioprocédés et une analytique de cytométrie en flux avancée.
La différenciation stratégique dépend des chimies spécifiques au site propriétaires et des offres de service intégrées. Les suites jumelles de conjugaison de 1 200 L de Lonza permettent une montée en puissance transparente des lots précliniques aux commerciaux, tandis que Bio-Rad élargit ses réactifs d'imagerie super-résolution pour la conception de Panneaux multiplex. Les mouvements récents incluent le lancement par Sartorius du système Octet R8e BLI qui capture les données de cinétique de liaison plus rapidement que les modèles précédents.
Les alliances entre innovateurs technologiques et développeurs de médicaments continuent de proliférer. La licence d'EditCo Bio des plateformes HiBiT, HaloTag et NanoLuc de Promega rationalise les flux de travail CRISPR knock-in, raccourcissant les itérations build-test. Le partenariat de Prism BioLab avec Elix intègre la conception de composés basée sur l'IA avec le criblage de peptides-mimétiques, élargissant la base client adressable pour les inhibiteurs PPI sélectifs.
Leaders de l'industrie du marquage protéique
-
Thermo Fisher Scientific Inc
-
Merck KGaA
-
Perkinelmer Inc
-
Danaher Corporation
-
F. Hoffmann-La Roche AG
- *Avis de non-responsabilité : les principaux acteurs sont triés sans ordre particulier
Développements récents de l'industrie
- Mai 2025 : GenNext Technologies s'associe avec Thermo Fisher pour intégrer l'empreinte AutoFox avec les solutions Orbitrap LC-MS
- Mai 2025 : Sartorius introduit le système d'interférométrie par couche biologique Octet R8e pour l'analyse cinétique haute production
- Avril 2025 : EditCo Bio sécurise les droits aux technologies HiBiT, HaloTag et NanoLuc de Promega pour améliorer les knock-ins CRISPR.
- Avril 2025 : Prism BioLab et Elix collaborent sur la découverte de médicaments peptides-mimétiques accélérée par l'IA.
Portée du rapport sur le marché mondial du marquage protéique
Selon la portée du rapport, le marquage protéique fait référence à l'utilisation d'étiquettes moléculaires appropriées pour détecter ou purifier la protéine marquée et ses partenaires de liaison. Les stratégies de marquage résultent en l'attachement covalent de différentes molécules, incluant la biotine, les enzymes rapporteuses, les fluorophores et les isotopes radioactifs, à la protéine cible ou séquence nucléotidique
| Réactifs et kits |
| Services |
| Autres produits (colonnes de spin, résines, etc.) |
| Techniques immunologiques |
| Dosages cellulaires |
| Microscopie de fluorescence |
| Microarrays protéiques |
| Spectrométrie de masse |
| Marquage in vitro |
| Marquage in vivo |
| Entreprises pharmaceutiques et biotechnologiques |
| Organismes de recherche contractuelle et de fabrication (CRO/CDMO) |
| Instituts académiques et de recherche |
| Laboratoires de diagnostics cliniques |
| Amérique du Nord | États-Unis |
| Canada | |
| Mexique | |
| Europe | Allemagne |
| Royaume-Uni | |
| France | |
| Italie | |
| Espagne | |
| Reste de l'Europe | |
| Asie-Pacifique | Chine |
| Japon | |
| Inde | |
| Corée du Sud | |
| Australie | |
| Reste de l'Asie-Pacifique | |
| Moyen-Orient et Afrique | CCG |
| Afrique du Sud | |
| Reste du Moyen-Orient et Afrique | |
| Amérique du Sud | Brésil |
| Argentine | |
| Reste de l'Amérique du Sud |
| Par produit | Réactifs et kits | |
| Services | ||
| Autres produits (colonnes de spin, résines, etc.) | ||
| Par application | Techniques immunologiques | |
| Dosages cellulaires | ||
| Microscopie de fluorescence | ||
| Microarrays protéiques | ||
| Spectrométrie de masse | ||
| Par méthode de marquage | Marquage in vitro | |
| Marquage in vivo | ||
| Par utilisateur final | Entreprises pharmaceutiques et biotechnologiques | |
| Organismes de recherche contractuelle et de fabrication (CRO/CDMO) | ||
| Instituts académiques et de recherche | ||
| Laboratoires de diagnostics cliniques | ||
| Par géographie | Amérique du Nord | États-Unis |
| Canada | ||
| Mexique | ||
| Europe | Allemagne | |
| Royaume-Uni | ||
| France | ||
| Italie | ||
| Espagne | ||
| Reste de l'Europe | ||
| Asie-Pacifique | Chine | |
| Japon | ||
| Inde | ||
| Corée du Sud | ||
| Australie | ||
| Reste de l'Asie-Pacifique | ||
| Moyen-Orient et Afrique | CCG | |
| Afrique du Sud | ||
| Reste du Moyen-Orient et Afrique | ||
| Amérique du Sud | Brésil | |
| Argentine | ||
| Reste de l'Amérique du Sud | ||
Questions clés répondues dans le rapport
1. Quelle est la valeur projetée du marché du marquage protéique d'ici 2030 ?
Le marché devrait atteindre 4,57 milliards USD d'ici 2030, reflétant un TCAC de 9,39 %
2. Quelle région montre la croissance la plus rapide dans le marché du marquage protéique ?
L'Asie-Pacifique mène avec un TCAC de 11,57 %, alimenté par l'expansion des capacités CDMO et les initiatives gouvernementales de soutien.
3. Pourquoi les CRO et CDMOs gagnent-ils en traction dans l'industrie du marquage protéique ?
Les sponsors externalisent la conjugaison complexe pour accéder à une expertise spécialisée, réduire les dépenses d'investissement et comprimer les délais de développement, conduisant un TCAC de 13,07 % pour ce segment.
4. Comment les technologies de marquage spécifique au site bénéficient-elles à la découverte de médicaments ?
Les étiquettes précises améliorent l'homogénéité dans les conjugués anticorps-médicaments et permettent la surveillance en temps réel de la dégradation protéique ciblée, améliorant ainsi l'efficacité thérapeutique.
5. Quelles avancées techniques sous-tendent la montée du marquage in vivo ?
L'expansion du code génétique, les chimies médiées par enzyme et la méthode CuRVE du MIT permettent un marquage rapide et uniforme dans les tissus vivants sans perturber la fonction protéique.
6. Quelle contrainte limite le plus significativement l'adoption plus large d'outils avancés de marquage protéique ?
Les coûts en capital élevés pour les plateformes de spectrométrie de masse de premier niveau restent la barrière principale, particulièrement dans les marchés émergents avec des budgets de recherche contraints.
Dernière mise à jour de la page le:



