Taille et part du marché des thérapeutiques de la myasthénie grave
Analyse du marché des thérapeutiques de la myasthénie grave par Mordor Intelligence
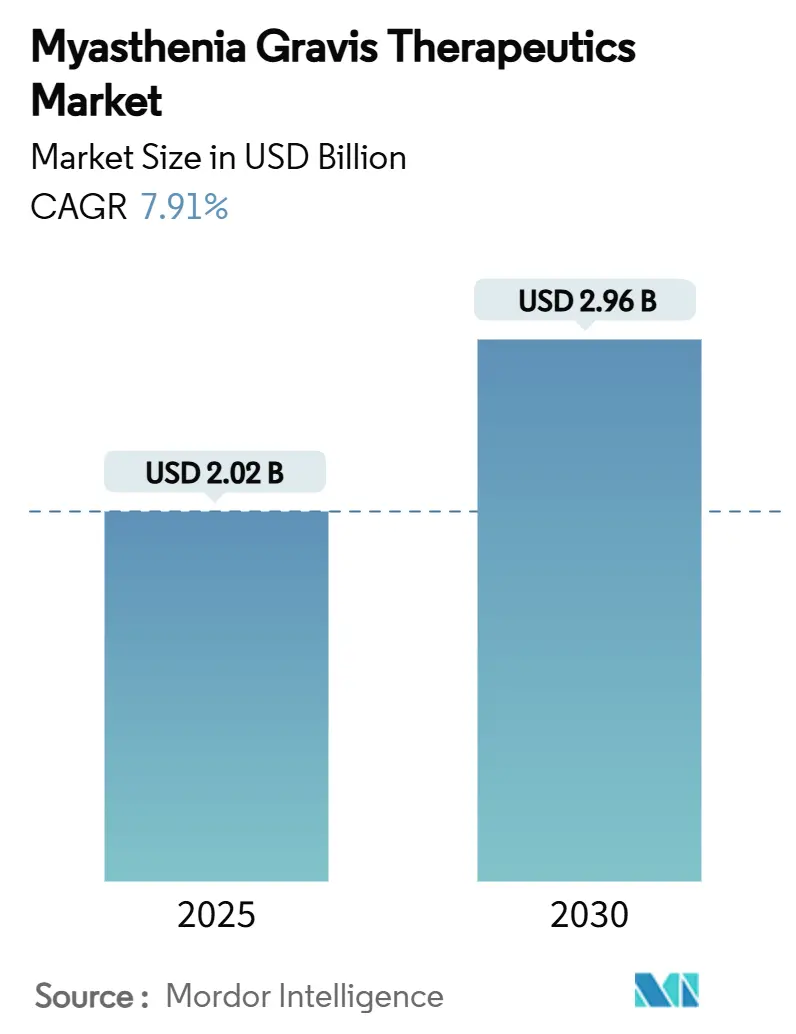
Le marché des thérapeutiques de la myasthénie grave s'établissait à 2,02 milliards USD en 2025 et devrait atteindre 2,96 milliards USD d'ici 2030 avec un TCAC de 7,91 %. L'adoption croissante de biologiques, notamment les antagonistes du FcRn et les inhibiteurs du complément, redéfinit les parcours de soins et incite les payeurs à réévaluer les cadres de remboursement. La maturation du pipeline, les incitations pour les médicaments orphelins et les collaborations soutenues par le capital-risque ont raccourci les cycles de développement, tandis que les formulations sous-cutanées (SC) accélèrent la décentralisation des traitements. Une forte croissance de la prévalence, un diagnostic plus précoce grâce aux outils assistés par IA et une latitude tarifaire premium renforcent davantage les perspectives de revenus. L'intensité concurrentielle devrait augmenter alors que Johnson & Johnson, argenx et UCB développent de nouveaux lancements et que les programmes de biosimilaires préparent leurs entrées post-2030.
Points clés du rapport
- Par traitement, les thérapies médicamenteuses ont dominé avec 69,37 % de part de revenus en 2024 ; les thérapies géniques et cellulaires progressent à un TCAC de 9,73 % jusqu'en 2030.
- Par voie d'administration, la délivrance intraveineuse détenait 63,56 % de la part du marché des thérapeutiques de la myasthénie grave en 2024, tandis que le segment SC progresse à un TCAC de 10,12 % jusqu'en 2030.
- Par classe de médicaments, les inhibiteurs de la cholinestérase représentaient 46,56 % de la taille du marché des thérapeutiques de la myasthénie grave en 2024 ; les anticorps monoclonaux croissent à un TCAC de 11,34 % jusqu'en 2030.
- Par utilisateur final, les hôpitaux détenaient 59,52 % de part en 2024, tandis que les soins à domicile progressent à un TCAC de 10,89 % car les biologiques SC permettent l'auto-administration.
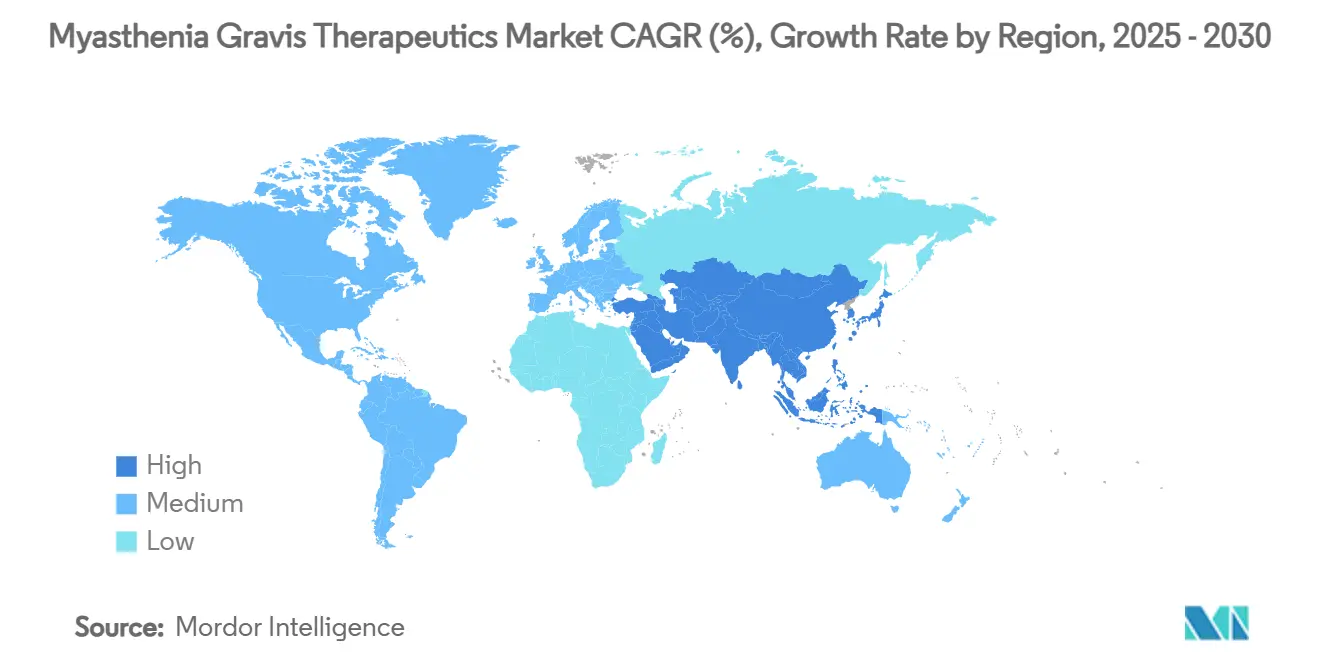
- Par géographie, l'Amérique du Nord commandait 44,43 % des revenus en 2024 ; l'Asie-Pacifique est la région à la croissance la plus rapide avec un TCAC de 9,78 % jusqu'en 2030.
Tendances et insights du marché mondial des thérapeutiques de la myasthénie grave
Analyse d'impact des moteurs
| Moteur | (~) % d'impact sur les prévisions TCAC | Pertinence géographique | Calendrier d'impact |
|---|---|---|---|
| Incidence croissante et diagnostic plus précoce de la MG | +1.2% | Mondial, avec des gains concentrés en Amérique du Nord et UE | Moyen terme (2-4 ans) |
| Approbations accélérées de biologiques ciblant le complément et le FcRn | +2.1% | Mondial, mené par les voies réglementaires US et UE | Court terme (≤ 2 ans) |
| Incitations pour maladies rares et effet de levier tarifaire premium | +1.8% | Marchés cœurs Amérique du Nord et UE | Long terme (≥ 4 ans) |
| Pipeline d'essais cliniques robuste alimenté par des accords venture/big pharma | +1.5% | Mondial, avec R&D concentrée en Amérique du Nord | Moyen terme (2-4 ans) |
| Biologiques SC auto-administrés améliorant l'observance | +0.9% | Mondial, avec adoption précoce dans les marchés développés | Court terme (≤ 2 ans) |
| Analytics d'électromyographie basées sur IA permettant une intervention plus précoce | +0.6% | Amérique du Nord et UE, s'étendant à APAC | Long terme (≥ 4 ans) |
| Source: Mordor Intelligence | |||
Incidence croissante et diagnostic plus précoce
L'incidence est passée à 68,5 nouveaux cas américains par million en 2024, reflétant une sensibilisation croissante et une meilleure couverture d'assurance pour les tests neuromusculaires. L'analytique oculo-motrice assistée par IA confirme désormais les signatures de fatigue en moins de 60 secondes, réduisant le retard diagnostique moyen de 2,3 ans à moins de 12 mois dans les cliniques tertiaires.[1]Yun Ye, "Epidemiology of myasthenia gravis in the United States," Frontiers in Neurology, frontiersin.org La confirmation précoce permet aux cliniciens de commencer la thérapie immuno-modificatrice plus tôt, et les centres qui atteignent un diagnostic sub-annuel rapportent des taux de manifestations minimales 40 % plus élevés au suivi de deux ans. Un accès élargi à la télé-neurologie, couplé aux incitations des payeurs pour des bilans rapides, continue d'élargir le bassin de patients du marché des thérapeutiques de la myasthénie grave.
Approbations accélérées de biologiques FcRn/complément
Entre 2023 et 2025, quatre médicaments révolutionnaires-rozanolixizumab, zilucoplan, nipocalimab et SC efgartigimod-ont terminé l'examen réglementaire en seulement 6-8 mois sous des voies prioritaires. Les délais condensés raccourcissent les périodes de consommation de liquidités, encourageant les investisseurs en capital-risque et favorisant l'activité d'accords big pharma. Les approbations parallèles dans l'UE, au Japon et en Australie permettent des lancements quasi simultanés, accélérant la capture de revenus mondiaux pendant les fenêtres d'exclusivité. Ces dynamiques ajoutent ampleur et profondeur au marché des thérapeutiques de la myasthénie grave et valident l'immunologie de précision comme thème de croissance cœur.
Incitations pour maladies rares et tarification premium
Le statut de médicament orphelin accorde une exclusivité de sept ans, un crédit d'impôt R&D de 25 % et supprime les frais d'utilisateur FDA, éliminant des coûts réglementaires considérables. Les prix catalogue dépassent 800 000 USD par patient-année, pourtant les contrats basés sur les résultats atténuent la résistance des payeurs tout en préservant de solides flux de revenus nets. Les fabricants canalisent les marges élevées vers des programmes de nouvelle génération tels que CAART et les anticorps bispécifiques, renforçant un cycle d'investissement vertueux qui maintient l'industrie des thérapeutiques de la myasthénie grave attrayante pour les acteurs établis et nouveaux entrants.
Biologiques SC améliorant l'observance
L'autorisation EMA pour le rozanolixizumab auto-injecté et l'approbation FDA des seringues pré-remplies Vyvgart Hytrulo déplacent le traitement des suites de perfusion vers le domicile, élevant l'observance de 65 % à 89 % dans les six mois du déploiement. Le dosage à domicile élimine les contraintes de déplacement, un avantage cité par 83 % des répondants d'enquête. Une meilleure persistance produit une suppression IgG plus stable, moins d'exacerbations et moins d'hospitalisations liées aux crises, renforçant la justification clinique et économique pour l'utilisation de biologiques sur le marché des thérapeutiques de la myasthénie grave.
Analyse d'impact des contraintes
| Contrainte | (~) % d'impact sur les prévisions TCAC | Pertinence géographique | Calendrier d'impact |
|---|---|---|---|
| Coût élevé de la thérapie biologique à long terme | -1.8% | Mondial, plus aigu dans les marchés émergents | Long terme (≥ 4 ans) |
| Faible sensibilisation à la maladie dans les économies émergentes | -1.1% | APAC, Amérique latine, MEA | Moyen terme (2-4 ans) |
| Complexité de la chaîne du froid et AQ d'essai pour les mAbs | -0.7% | Mondial, régions dépendantes des infrastructures | Court terme (≤ 2 ans) |
| Risque d'érosion des prix post-Soliris LOE et entrée de biosimilaires | -0.9% | Principalement Amérique du Nord et UE | Long terme (≥ 4 ans) |
| Source: Mordor Intelligence | |||
Coût élevé de la thérapie biologique
La dépense annuelle d'inhibiteur FcRn approche 833 000 USD, tandis que les études coût-utilité suggèrent que les prix doivent chuter jusqu'à 88 % pour respecter les seuils de consentement à payer aux États-Unis et en Europe.[2] Young-Ah Heo, "Efgartigimod: A Review in Generalized Myasthenia Gravis," Journal of Managed Care & Specialty Pharmacy, jmcp.org Les plafonds budgétaires déclenchent des retards d'autorisation préalable de quatre à six semaines, et les patients des marchés émergents optent souvent par défaut pour les stéroïdes ou la plasmaphérèse à cause des co-paiements élevés. De larges écarts d'accessibilité tempèrent donc la croissance de la demande pour le marché des thérapeutiques de la myasthénie grave malgré la supériorité clinique des agents nouveaux.
Faible sensibilisation à la maladie dans les économies émergentes
La reconnaissance de la myasthénie grave en soins primaires s'établit en moyenne en dessous de 30 % dans de nombreux environnements APAC et d'Amérique latine, avec un mauvais diagnostic à la présentation initiale dépassant 60 %.[3]Yasar Zorlu, "Decoding myasthenia gravis with infrared spectroscopy," Scientific Reports, nature.com Les patients peuvent circuler entre les services d'ophtalmologie et ORL jusqu'à un an avant l'orientation neurologique, retardant l'accès à la thérapie modificatrice de maladie. Ces facteurs restreignent la pénétration du marché, maintenant les volumes de prescription bas même lorsque les produits reçoivent l'approbation réglementaire.
Analyse de segments
Par traitement : les thérapies géniques accélèrent les soins de précision
Les thérapies géniques et cellulaires constituent la catégorie de traitement à la croissance la plus rapide avec un TCAC de 9,73 %, bien que les régimes médicamenteux aient encore capturé 69,37 % des revenus 2024. Les premières études de cas CAR-T montrent les scores MG quantitatifs chutant de 21 à 5, soutenant les gains de force musculaire sans immunosuppression continue. La réponse MG-ADL de 98,1 % du télitacicept dans les essais de phase tardive et la technologie CAART qui épuise sélectivement les cellules B pathogènes renforcent la confiance croissante dans les approches curatives. Le capital-risque et les subventions de fondations de maladies fournissent un financement critique, tandis que les régulateurs familiers avec les vecteurs AAV rationalisent les examens IND. Alors que les interventions uniques mûrissent, le marché des thérapeutiques de la myasthénie grave peut évoluer vers des revenus en front-loaded, avec des budgets de médicaments chroniques pivotant progressivement vers la surveillance post-traitement.
Le segment médicamenteux existant reste important parce que les stéroïdes, inhibiteurs de la cholinestérase et IVIg continuent de gérer les épisodes légers ou rapidement progressifs. Néanmoins, les antagonistes FcRn et inhibiteurs du complément permettent désormais un sevrage stéroïdien chez près de la moitié des patients, érodant la dépendance aux immunosuppresseurs larges. Les protocoles combinés mélangeant biologiques avec édition génique ciblée peuvent créer des modèles hybrides de soins qui préservent les marges de maintenance tout en débloquant une rémission durable pour les groupes à haut risque. Une telle innovation maintient la diversité des revenus sur le marché des thérapeutiques de la myasthénie grave et amortit les fabricants de médicaments contre les résultats réglementaires binaires.
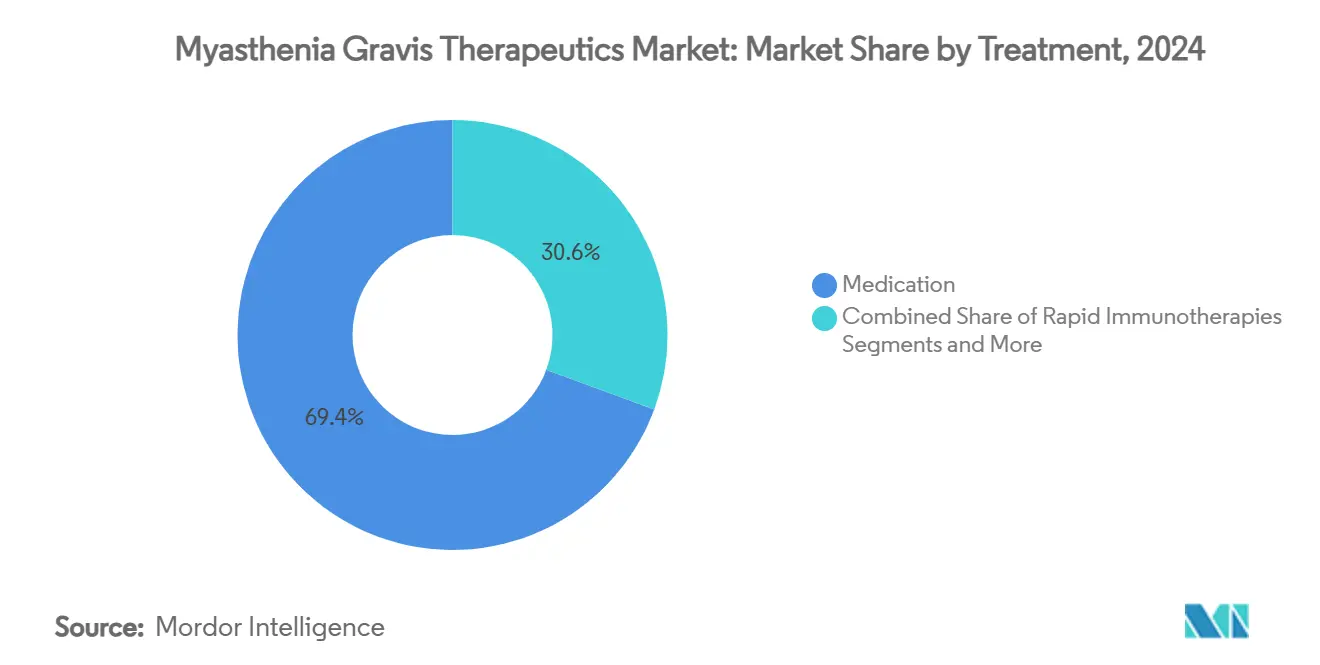
Note: Parts de segments de tous les segments individuels disponibles à l'achat du rapport
Par voie d'administration : la délivrance SC redéfinit la commodité
L'administration sous-cutanée croît de 10,12 % annuellement et est prête à grignoter la dominance intraveineuse, qui représentait 63,56 % des revenus en 2024. L'endorsement EMA du rozanolixizumab auto-injecté et l'autorisation FDA pour les seringues pré-remplies Vyvgart Hytrulo confirment la sécurité et l'efficacité de la délivrance contrôlée par le patient. Le dosage SC peut être complété en cinq minutes à domicile, comparé aux visites de perfusion de plusieurs heures, élevant l'observance à 89 % et conduisant au basculement parmi les patients désireux de réduire le temps clinique. Une telle commodité élargit la taille du marché des thérapeutiques de la myasthénie grave en engageant les résidents ruraux et patients à mobilité limitée qui sautaient auparavant la thérapie biologique.
Les partenariats technologiques, comme l'expansion de 30 millions USD d'argenx avec Halozyme, ciblent des concentrations médicamenteuses plus élevées et des volumes d'injection plus petits, améliorant le confort et la logistique. Le changement libère les chaises de perfusion pour d'autres spécialités, un avantage valorisé par les administrateurs hospitaliers, et abaisse les coûts d'installation des payeurs. Les formulations orales restent confinées aux inhibiteurs de cholinestérase hérités et stéroïdes, pourtant les biologiques futurs à libération prolongée ou nanoparticules pourraient déplacer des thérapies supplémentaires vers les soins à domicile. Une pénétration SC plus large continuera donc de remodeler l'allocation des revenus au sein du marché des thérapeutiques de la myasthénie grave.
Par classe de médicaments : les anticorps monoclonaux surpassent les médicaments hérités
Les anticorps monoclonaux ont affiché la trajectoire de croissance la plus élevée avec un TCAC de 11,34 % jusqu'en 2030, bien que les inhibiteurs de cholinestérase aient encore généré 46,56 % des revenus 2024. Les antagonistes FcRn tels qu'efgartigimod, rozanolixizumab et nipocalimab délivrent une réduction IgG rapide, améliorant les scores MG-ADL et QMG en semaines. Les inhibiteurs du complément restent critiques pour les patients avec pathologie médiée par le complément, offrant des perspectives de rémission lorsque les titres d'auto-anticorps restent élevés malgré la thérapie FcRn. Le rituximab conserve une niche dans la maladie MuSK-positive, avec 97 % des receveurs atteignant un statut clinique amélioré mais limité par les obstacles de remboursement hors-indication.
La diversification du pipeline inclut des inhibiteurs C2 et agonistes MuSK, suggérant de nouvelles vagues de lancements qui maintiennent les décisions de prescription fluides et compétitives. La méta-analyse en réseau souligne la réponse QMG supérieure du batoclimab et les gains MG-ADL leaders du rozanolixizumab, impliquant une sélection médicamenteuse éventuelle basée sur l'algorithme. Une telle personnalisation basée sur les données soutient l'expansion soutenue de la part biologique à l'intérieur du marché des thérapeutiques de la myasthénie grave tout en donnant aux payeurs des leviers pour négocier des contrats basés sur la valeur.
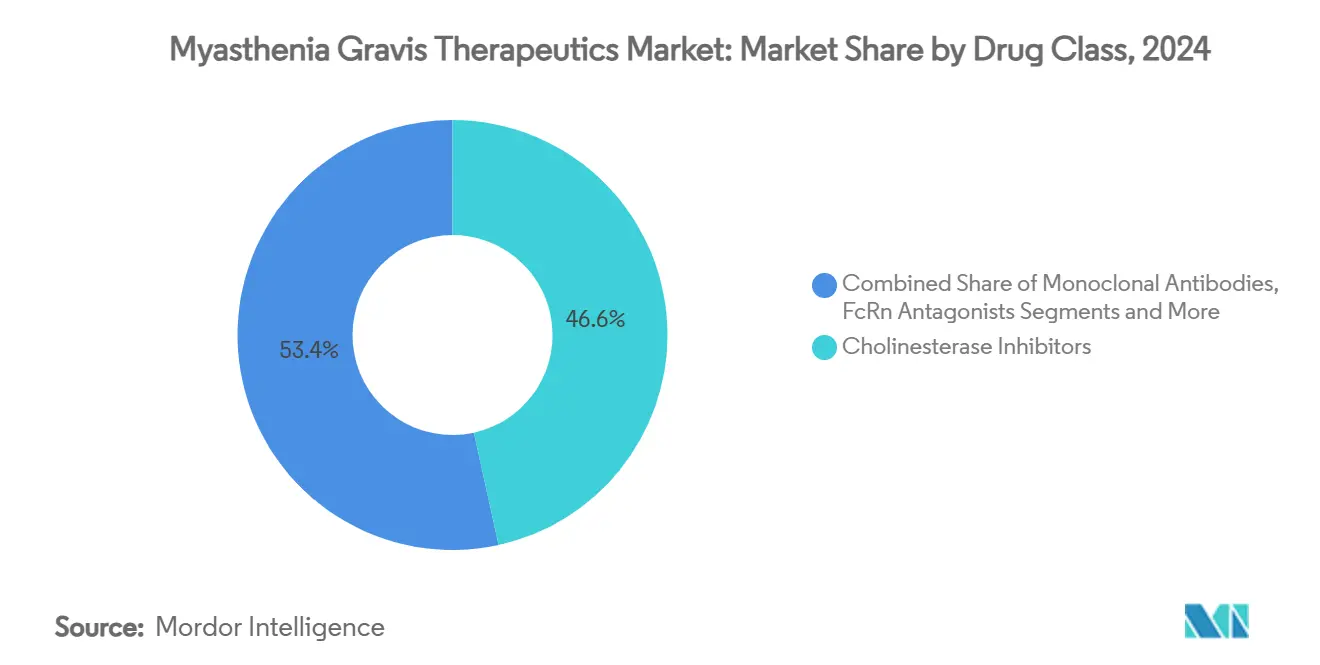
Note: Parts de segments de tous les segments individuels disponibles à l'achat du rapport
Par utilisateur final : les soins à domicile capturent la croissance la plus rapide
Les soins à domicile s'étendent à un TCAC de 10,89 %, défiant les hôpitaux qui détenaient 59,52 % de part en 2024. L'expérience COVID-19 a normalisé l'auto-injection et la télé-surveillance, réduisant l'anxiété des patients concernant l'administration de biologiques de haute valeur à domicile. Les plateformes assistées par IA automatisent désormais les examens neuromusculaires avec 95 % de précision, permettant aux cliniciens d'ajuster le dosage basé sur les scores de performance à distance. Sur l'horizon de prévision, le marché des thérapeutiques de la myasthénie grave attend une migration stable du dosage de maintenance des cliniques spécialisées vers les salons.
Les hôpitaux dominent encore l'initiation parce que les neurologues effectuent les évaluations de base, titrages de perfusion et gestion des crises. Les centres de chirurgie ambulatoire conservent un rôle pour la thymectomie et électrophysiologie, pourtant les volumes de facturation glissent car les biologiques abaissent la demande procédurale. Les payeurs endorsent la décentralisation lorsque les métriques d'observance se prouvent stables, et certains assureurs offrent des remises premium aux patients qui transitionnent vers l'administration à domicile. Ce changement réalloue les flux de revenus mais élargit le marché global des thérapeutiques de la myasthénie grave en supprimant les barrières logistiques aux soins chroniques.
Analyse géographique
L'Amérique du Nord a généré 44,43 % des revenus 2024, soutenue par une large couverture d'assurance et une adoption biologique rapide suivant les désignations révolutionnaires FDA. L'incidence se situe maintenant à 68,5 par million, équivalant à environ 82 700 adultes américains nécessitant une thérapie continue. Les tests oculo-moteurs assistés par IA et la télé-neurologie réduisent les goulots d'étranglement spécialisés, promouvant des démarrages précoces qui élèvent l'exposition médicamenteuse cumulative. L'intensité concurrentielle a augmenté en 2025 lorsque Johnson & Johnson a lancé nipocalimab, ajoutant une tension prix qui peut élargir l'accès patient en tempérant les escalateurs de coûts annuels.
L'Europe suit avec un environnement réglementaire cohésif qui a approuvé rozanolixizumab en janvier 2024 et l'auto-administration SC en février 2025. Les évaluations technologiques de santé sécurisent des remises de prix catalogue de 20-30 %, pourtant reconnaissent encore la valeur du médicament orphelin où les données du monde réel montrent un sevrage stéroïdien plus rapide et moins de crises. Les études de préférence confirment que 83 % des patients européens favorisent le dosage SC, permettant aux payeurs de réallouer les budgets de perfusion vers l'acquisition médicamenteuse. Les approbations conditionnelles nécessitent une surveillance post-marché, assurant la transparence sécuritaire tout en permettant le flux de revenus pendant la collecte de données. Les programmes biosimilaires croissants pour les inhibiteurs du complément pourraient générer des économies supplémentaires, finançant potentiellement une adoption FcRn plus large à travers les formulaires nationaux.
L'Asie-Pacifique est la région à croissance la plus rapide avec un TCAC de 9,78 %, soutenue par les examens PMDA et NMPA qui traînent maintenant les autorisations américaines de moins de six mois. Le Japon a approuvé efgartigimod comme VYVDURA pour la myasthénie grave généralisée et thrombocytopénie immune, tandis que la Chine a autorisé les formes IV et SC pour gMG et CIDP. Malgré ces gains, les coûts out-of-pocket s'élèvent encore en moyenne à 40 % du revenu annuel du ménage en Chine, ce qui plafonne l'utilisation pour les biologiques à prix élevé. La télé-médecine et la spectroscopie infrarouge basée sur IA avec 100 % de précision diagnostique commencent à combler les écarts spécialisés. L'investissement continu dans l'infrastructure de soins de santé et les initiatives de fabrication locale, incluant les biosimilaires FcRn planifiés, devraient élever la contribution régionale au marché des thérapeutiques de la myasthénie grave sur la prochaine décennie.
Paysage concurrentiel
Le marché des thérapeutiques de la myasthénie grave montre une consolidation modérée. Argenx reste le leader des revenus, affichant 573 millions USD de ventes Vyvgart au T3 2024 et ciblant 50 000 patients mondiaux d'ici 2030. L'approbation nipocalimab de Johnson & Johnson en mai 2025 fournit de solides données head-to-head montrant une amélioration soutenue quatre fois supérieure versus placebo, approvisionnant une échelle immédiate via sa franchise d'immunologie globale. Le rozanolixizumab d'UCB se différencie avec auto-injection et une indication AChR/MuSK double, attirant les patients recherchant le dosage à domicile.
La ligne d'inhibiteur du complément d'AstraZeneca est vulnérable à l'empiètement FcRn mais maintient la loyauté parmi les sous-groupes complément-positifs. Le batoclimab d'Immunovant, maintenant en Phase 3, a affiché un bénéfice MG-ADL de 5,6 points qui peut élever la compétition sur la profondeur de réduction IgG. Les alliances technologiques continuent de remodeler le domaine ; le partenariat Enhanze d'argenx avec Halozyme cible quatre nouveaux candidats SC qui pourraient étendre ses douves de marque. Les entrants de thérapie génique, incluant les développeurs CAART, sont probablement des cibles d'acquisition pour les big pharma recherchant des actifs de rémission durable, renforçant davantage le pipeline futur pour le marché des thérapeutiques de la myasthénie grave.
L'image tarifaire est fluide. Les études coût-efficacité pressent de larges remises, pourtant les contrats basés sur les résultats et modèles de soins chroniques groupés accordent aux fabricants une latitude s'ils peuvent documenter la réduction de crise et l'épargne stéroïdienne. Alors que plus d'agents entrent, les systèmes nationaux peuvent tirer parti des appels d'offres concurrentiels pour faire chuter les prix nets, mais les marges d'immunologie élevées et la capacité de fabrication rare favorisent encore les originateurs sur les biosimilaires avant 2030.
Leaders de l'industrie des thérapeutiques de la myasthénie grave
-
argenx SE
-
UCB Pharma
-
Johnson & Johnson
-
Novartis AG
-
AstraZeneca
- *Avis de non-responsabilité : les principaux acteurs sont triés sans ordre particulier
Développements récents de l'industrie
- Avril 2025 : Johnson & Johnson a obtenu l'approbation FDA pour nipocalimab (Imaavy) dans la myasthénie grave généralisée, montrant un contrôle symptomatique soutenu quatre fois supérieur au placebo.
- Avril 2025 : Argenx a reçu l'autorisation FDA pour les seringues pré-remplies Vyvgart Hytrulo, qui permettent l'auto-administration par le patient à domicile.
- Avril 2025 : RemeGen a annoncé une réponse MG-ADL de 98,1 % pour télitacicept en Phase 3, avec l'approbation chinoise attendue T2 2025.
- Mars 2025 : Immunovant a rapporté des données Phase 3 batoclimab, atteignant une amélioration MG-ADL de 5,6 points à 680 mg hebdomadaire.
Portée du rapport mondial sur le marché des thérapeutiques de la myasthénie grave
La myasthénie grave est un trouble auto-immun neuromusculaire qui cause une faiblesse dans les muscles squelettiques, qui sont les muscles que votre corps utilise pour le mouvement. Elle se produit lorsque la communication entre les cellules nerveuses et les muscles devient altérée. Cette altération empêche les contractions musculaires cruciales de se produire, résultant en une faiblesse musculaire. Bien qu'il n'existe pas de cure pour le trouble, des médicaments peuvent être utilisés pour prévenir l'exacerbation des symptômes.
| Médicaments | |
| Immunothérapies rapides | Immunoglobuline intraveineuse (IVIg) |
| Plasmaphérèse | |
| Thérapies géniques et cellulaires | |
| Autres thérapies émergentes |
| Orale |
| Intraveineuse |
| Sous-cutanée |
| Inhibiteurs de la cholinestérase |
| Corticostéroïdes et autres immunosuppresseurs |
| Anticorps monoclonaux |
| Inhibiteurs du complément |
| Antagonistes FcRn |
| Autres |
| Hôpitaux |
| Cliniques de neurologie spécialisées |
| Soins à domicile |
| Centres de chirurgie ambulatoire |
| Amérique du Nord | États-Unis |
| Canada | |
| Mexique | |
| Europe | Allemagne |
| Royaume-Uni | |
| France | |
| Italie | |
| Espagne | |
| Reste de l'Europe | |
| Asie-Pacifique | Chine |
| Japon | |
| Inde | |
| Australie | |
| Corée du Sud | |
| Reste de l'Asie-Pacifique | |
| Moyen-Orient et Afrique | CCG |
| Afrique du Sud | |
| Reste du Moyen-Orient et Afrique | |
| Amérique du Sud | Brésil |
| Argentine | |
| Reste de l'Amérique du Sud |
| Par traitement | Médicaments | |
| Immunothérapies rapides | Immunoglobuline intraveineuse (IVIg) | |
| Plasmaphérèse | ||
| Thérapies géniques et cellulaires | ||
| Autres thérapies émergentes | ||
| Par voie d'administration | Orale | |
| Intraveineuse | ||
| Sous-cutanée | ||
| Par classe de médicaments | Inhibiteurs de la cholinestérase | |
| Corticostéroïdes et autres immunosuppresseurs | ||
| Anticorps monoclonaux | ||
| Inhibiteurs du complément | ||
| Antagonistes FcRn | ||
| Autres | ||
| Par utilisateur final | Hôpitaux | |
| Cliniques de neurologie spécialisées | ||
| Soins à domicile | ||
| Centres de chirurgie ambulatoire | ||
| Par géographie | Amérique du Nord | États-Unis |
| Canada | ||
| Mexique | ||
| Europe | Allemagne | |
| Royaume-Uni | ||
| France | ||
| Italie | ||
| Espagne | ||
| Reste de l'Europe | ||
| Asie-Pacifique | Chine | |
| Japon | ||
| Inde | ||
| Australie | ||
| Corée du Sud | ||
| Reste de l'Asie-Pacifique | ||
| Moyen-Orient et Afrique | CCG | |
| Afrique du Sud | ||
| Reste du Moyen-Orient et Afrique | ||
| Amérique du Sud | Brésil | |
| Argentine | ||
| Reste de l'Amérique du Sud | ||
Questions clés répondues dans le rapport
1. Quelle est la valeur actuelle du marché des thérapeutiques de la myasthénie grave ?
Le marché s'établit à 2,02 milliards USD en 2025 et devrait atteindre 2,96 milliards USD d'ici 2030 avec un TCAC de 7,91 %.
2. Quelle catégorie de traitement croît le plus rapidement ?
Les thérapies géniques et cellulaires mènent, s'étendant à un TCAC de 9,73 % jusqu'en 2030 alors que CAR-T et télitacicept montrent des taux de réponse élevés.
3. Pourquoi les biologiques SC gagnent-ils en popularité ?
Les approbations EMA et FDA pour les formulations auto-injectées élèvent l'observance à 89 % et éliminent les visites de suite de perfusion, améliorant la commodité patient et les profils de coût des payeurs.
4. Quelle région offre le plus haut potentiel de croissance ?
L'Asie-Pacifique montre un TCAC de 9,78 % grâce aux examens PMDA et NMPA plus rapides, bien que l'accessibilité reste un défi.
5. Quelles sont les principales barrières à l'adoption biologique ?
Les coûts annuels près de 833 000 USD et la faible sensibilisation à la maladie dans les économies émergentes ralentissent l'adoption malgré une forte efficacité clinique.
Dernière mise à jour de la page le:



