Tamaño y Participación del Mercado de Diagnósticos Complementarios
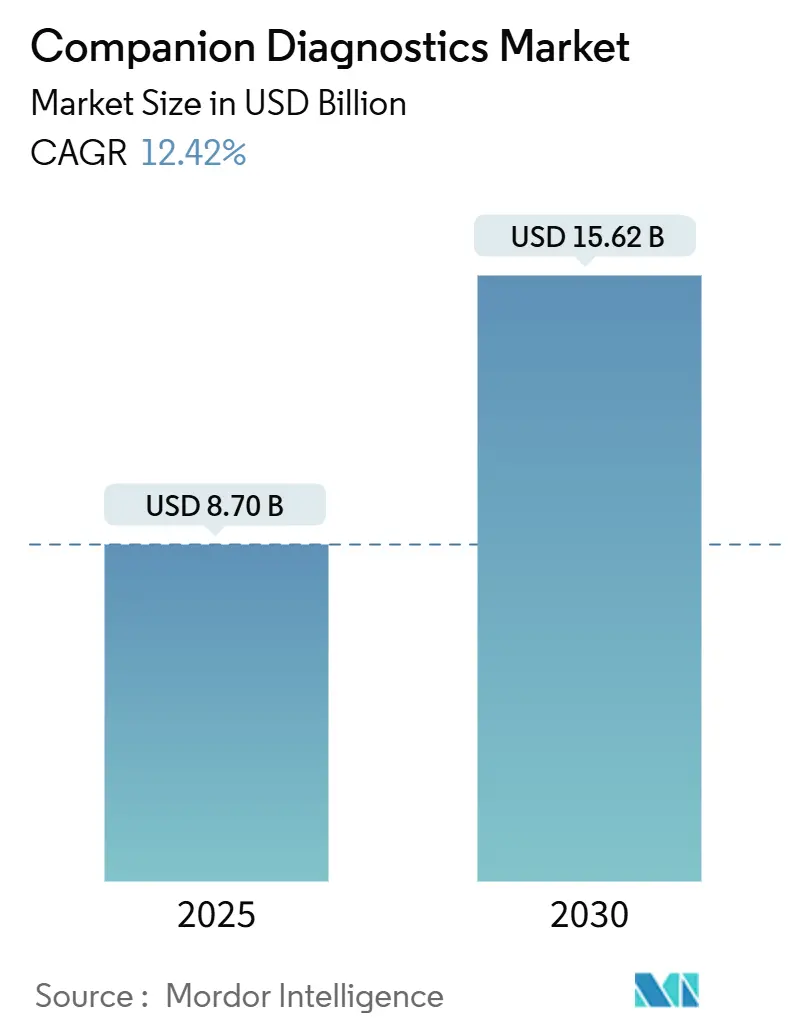
Análisis del Mercado de Diagnósticos Complementarios por Mordor Intelligence
El tamaño del mercado está valorado en USD 8,70 mil millones en 2025 y se pronostica que se expanda a USD 15,62 mil millones en 2030, reflejando una TCAC del 12,42%. Los diagnósticos complementarios integran pruebas moleculares con terapéuticas dirigidas, alineando la información diagnóstica con las opciones terapéuticas óptimas. La creciente aplicación de la medicina de precisión está simultáneamente cambiando las prioridades de inversión para los fabricantes de medicamentos y remodelando los modelos de reembolso de los pagadores, ya que los responsables de políticas reconocen los diagnósticos como herramientas fundamentales de contención de costos.
Puntos Clave del Informe
- PCR aún posee la mayor participación de 2024 con un 22,2% de participación de mercado, mientras que se pronostica que los diagnósticos complementarios superarán a las alternativas basadas en PCR, expandiéndose a una TCAC del 14,3% entre 2025-2030.
- Por Indicación, se espera que el Melanoma crezca con una TCAC del 13,6%, mientras que el Cáncer de Pulmón mantuvo una participación del 22,5% en 2024
- Los ensayos y kits representan el 66,3% del gasto de 2024, impulsados por su vinculación uno a uno con lanzamientos de medicamentos específicos. Sin embargo, las plataformas interpretativas impulsadas por software representan la categoría de producto de crecimiento más rápido con una TCAC del 15,8% (2025-2030).
- La biopsia de tejido aún representa el 78,5% de los volúmenes de 2024 porque la histología confirmatoria sigue siendo el estándar de oro regulatorio. Se proyecta que el tamaño del mercado de biopsia líquida se expanda una TCAC del 18,9% hasta 2030.
- Por Usuario Final, se establece que el tamaño del mercado de diagnósticos complementarios de las CRO ascienda una TCAC del 13,2% (2025-2030). y las Empresas Farmacéuticas y Biotecnológicas mantuvieron una participación del 45,2% en 2024.
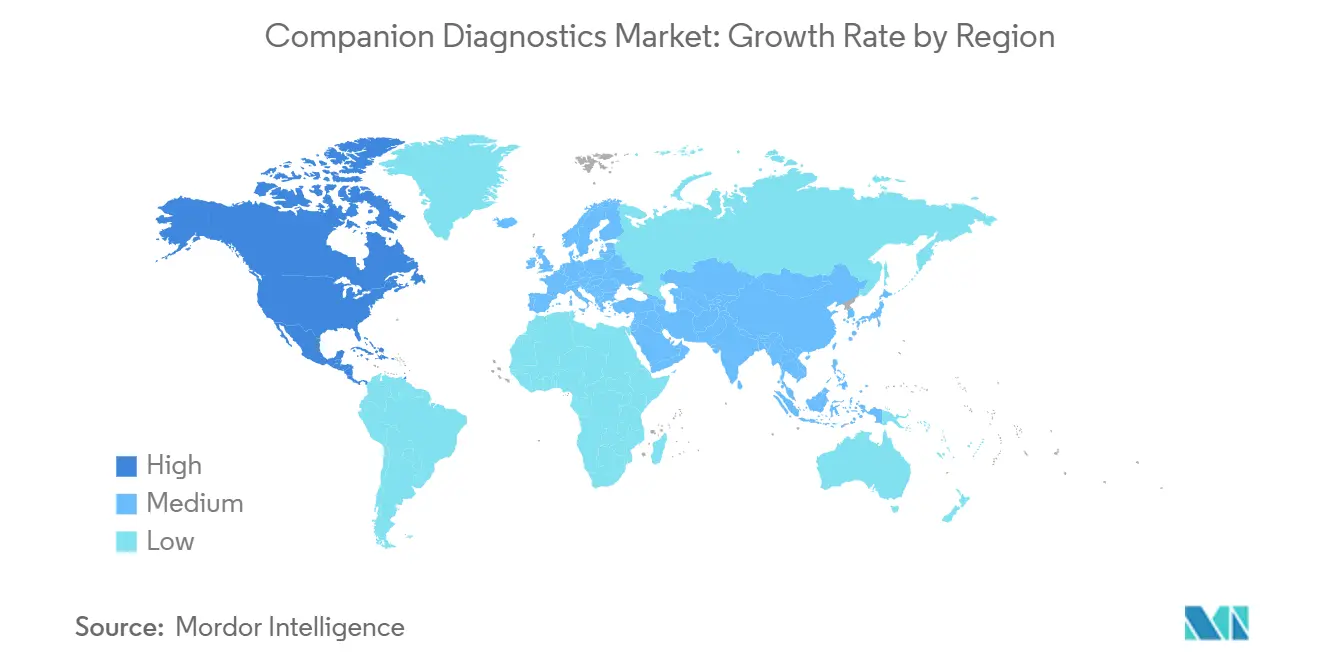
- América del Norte mantiene una participación de mercado del 40,4% en 2024 y se proyecta que Asia-Pacífico registre una TCAC del 12,7% de 2025-2030
Tendencias e Insights del Mercado Global de Diagnósticos Complementarios
Análisis de Impacto de Impulsores
| Impulsor | % Aproximado de Impacto en la TCAC General (2025-2030) | Regiones Primarias Afectadas | Cronología de Impacto |
|---|---|---|---|
| Expansión de etiquetas de medicamentos de medicina de precisión | ~+2,0% | América del Norte, Europa, Japón | Largo plazo (≥4 años) |
| Adopción rápida de biopsia líquida | ~+1,6% | Centros oncológicos urbanos globales; más rápido en Asia-Pacífico | Mediano plazo (2-4 años) |
| Pipeline oncológico enfocado en ADC que requiere plataformas CDx multiplex | +0.8% | América del Norte, Europa, Japón | Mediano plazo (2-4 años) |
| Curva de costo decreciente de NGS | ~+1,3% | Centros comunitarios de cáncer en América del Norte y Europa Occidental | Largo plazo (≥4 años) |
| Alineación de pagadores con pruebas aprobadas por FDA | ~+1,1% | Estados Unidos; derrame hacia Canadá y CCG | Corto plazo (≤2 años) |
| Integración de IA para interpretación de variantes | ~+0,7% | Laboratorios de referencia de alto rendimiento mundialmente | Mediano plazo (2-4 años) |
| Fuente: Mordor Intelligence | |||
Tendencias e Insights del Mercado de Diagnósticos Complementarios Adopción Rápida de CDx de Biopsia Líquida en Prácticas Oncológicas
Los diagnósticos complementarios de biopsia líquida están redefiniendo el manejo del cáncer al proporcionar una ruta mínimamente invasiva para pruebas repetidas que capturan la heterogeneidad tumoral en tiempo real. Los clínicos ahora rastrean la evolución de la enfermedad a través del ADN tumoral circulante, ajustando dinámicamente la terapia en lugar de depender de instantáneas estáticas de tejido. Una implicación de segundo orden es que los laboratorios hospitalarios deben recalibrar el rendimiento y la logística de cadena fría para acomodar volúmenes más grandes de ensayos basados en sangre, afectando las cronologías de asignación de capital a través de toda la línea de servicio oncológico. FoundationOne Liquid CDx, que obtuvo múltiples aprobaciones de la FDA en 2024, ilustra el impulso regulatorio que está acelerando la adopción del mercado [1]U.S. Food and Drug Administration - Companion Diagnostics Table . Sin embargo, la sensibilidad de la biopsia líquida aún varía según el estadio del cáncer y la biología de derramamiento tumoral, lo que significa que los proveedores están presionados a adoptar estrategias híbridas de tejido-más-sangre que preserven la precisión diagnóstica mientras controlan la redundancia de pruebas.
Avances en Medicina Personalizada y Oncología de Precisión
Los diagnósticos complementarios han pasado de ser complementos opcionales; son requisitos codificados para el acceso a muchos medicamentos dirigidos. La FDA enumera 168 emparejamientos de biomarcador-medicamento vinculados a pruebas aprobadas, señalando que las agencias de reembolso progresivamente retendrán el pago por cursos de terapia que carezcan de confirmación molecular. Esta vinculación está dirigiendo a las empresas farmacéuticas a co-desarrollar pruebas más temprano en ensayos de Fase I, comprimiendo las cronologías totales del programa pero aumentando la complejidad preclínica. Un efecto inmediato de rebote es que las organizaciones de investigación por contrato (CRO) están expandiendo los bancos de validación de biomarcadores para asegurar contratos estratégicos de subcontratación multianual, posicionándose como guardianes moleculares de facto para los pipelines biofarmacéuticos.
Innovaciones Tecnológicas en Herramientas Diagnósticas
La secuenciación de nueva generación (NGS) está entregando insights genómicos comprehensivos en un solo flujo de trabajo, con su segmento proyectado a crecer un 14,3% entre 2025 y 2030. Los laboratorios están superponiendo algoritmos de inteligencia artificial sobre la salida de NGS para hacer triage del flujo de variantes, un movimiento que sutilmente cambia la demanda de trabajo diagnóstico de tecnólogos de laboratorio húmedo hacia científicos de datos. Este reequilibrio de fuerza laboral, inferido del aumento en ofertas de trabajo de bioinformática, está influyendo los currículos universitarios y las startups respaldadas por capital de riesgo que proporcionan motores de anotación automatizada. Dado que los paneles de NGS de cáncer de pulmón identifican mutaciones accionables en hasta el 65% de los pacientes, los pagadores ya están redactando niveles de reembolso variable vinculados al número de hallazgos clínicamente accionables, presagiando modelos de precios basados en valor para diagnósticos.
Prevalencia Creciente de Enfermedades Crónicas
La incidencia de cáncer continúa escalando, con la American Cancer Society proyectando aproximadamente dos millones de nuevos casos en Estados Unidos para 2024 [2]European Medicines Agency, "In Vitro Diagnostic Regulation Guidance," European Medicines Agency, ema.europa.eu. El aumento de volumen fuerza a los centros oncológicos a rediseñar los protocolos de triage de pacientes, reconociendo que el tiempo de respuesta diagnóstico ahora influye directamente el tiempo hasta el tratamiento y, por extensión, los reembolsos de métricas de calidad. Los patrocinadores farmacéuticos responden integrando diagnósticos complementarios más temprano para aumentar el poder del ensayo, reconociendo que las poblaciones enriquecidas reducen el ruido estadístico. Esta dinámica está impulsando a las juntas de revisión institucional a actualizar el lenguaje de consentimiento informado, ya que los pacientes ahora deben reconocer que el perfilado molecular determina la elegibilidad para terapia-un cambio sutil pero significativo en el discurso de autonomía.
Análisis de Impacto de Restricciones
| Restricción | (~) % de Arrastre en la TCAC General (2025-2030) | Regiones Primarias Afectadas | Cronología de Impacto |
|---|---|---|---|
| Altos costos de desarrollo (USD 50-100 millones) | ~-1,8% | Universal; más agudo en mercados emergentes | Largo plazo (≥4 años) |
| Cuellos de botella regulatorios IVDR | ~-1,3% | Unión Europea | Mediano plazo (2-4 años) |
| Sensibilidad variable del ensayo en tumores de ctDNA bajo | ~-0,9% | Global; mayor impacto en programas oncológicos de estadio temprano | Corto plazo (≤2 años) |
| Reembolso inconsistente fuera de mercados principales | ~-0,8% | América Latina, partes de ASEAN, Europa Oriental | Largo plazo (≥4 años) |
| Escasez de fuerza laboral de bioinformática | ~-0,4% | Laboratorios de rápida escala en Asia-Pacífico y MENA | Mediano plazo (2-4 años) |
| Fuente: Mordor Intelligence | |||
Altos Costos de Desarrollo
Desarrollar un diagnóstico complementario puede requerir USD 50-100 millones y 3-5 años, enmarcando los diagnósticos como proyectos de capital de ciclo largo. Las empresas más pequeñas cada vez más atan sus fortunas a alianzas con grandes farmacéuticas, intercambiando participaciones de capital por financiamiento de desarrollo. La consecuencia de segundo orden es una consolidación de portafolios de propiedad intelectual: a medida que las grandes empresas absorben derechos de dispositivos, la libertad de operación para recién llegados se estrecha. Este paisaje de PI que se aprieta empuja a los inversionistas de capital de riesgo a favorecer empresas de plataforma con menús de ensayos expandibles en lugar de conceptos de biomarcadores únicos, sutilmente migrando dólares de capital de riesgo lejos de biomarcadores de nicho hacia soluciones escalables impulsadas por informática.
Políticas Regulatorias Estrictas
El Reglamento de Diagnóstico In Vitro (IVDR) de la Unión Europea introdujo consultas obligatorias de cuerpo notificado y Agencia Europea de Medicamentos para diagnósticos complementarios en 2022 [3]American Cancer Society, "Cancer Facts & Figures 2024," American Cancer Society, cancer.org. Porque solo un puñado de cuerpos están completamente designados, las colas de revisión se están alargando, obligando a las empresas a desviar la secuenciación de lanzamiento hacia Estados Unidos o Japón primero. Como efecto de ondas, los oncólogos europeos pueden experimentar acceso retardado a pruebas novedosas, planteando debates éticos sobre equidad geográfica en el cuidado del cáncer. En Estados Unidos, el piloto de la FDA que publica públicamente las características de rendimiento de pruebas ha catalizado transparencia pero simultáneamente expone ensayos de bajo rendimiento, creando riesgo reputacional para empresas de diagnósticos y agudizando el escrutinio del comprador.
Análisis de Segmentos
Análisis de Segmentos Tecnología: NGS Interrumpe Paradigmas de Pruebas Tradicionales
PCR aún posee la mayor participación de 2024 con un 22,2% de participación de mercado, sin embargo se espera que NGS supere a todas las otras tecnologías. El tamaño del mercado de NGS en diagnósticos complementarios se pronostica que supere a las alternativas basadas en PCR, expandiéndose a una TCAC del 14,3% entre 2025-2030. Los comités de adquisiciones hospitalarias cada vez más ejecutan análisis de costo total de propiedad que revelan que el alto rendimiento de muestras compensa los costos de consumibles NGS más altos sobre una ventana de amortización de tres años. Consecuentemente, los vendedores de instrumentos ahora agrupan software de análisis en contratos de reactivos, un arreglo que cambia el reconocimiento de ingresos de ventas de hardware de una sola vez a flujos de servicio recurrentes-remodelando la visibilidad de ganancias trimestrales.
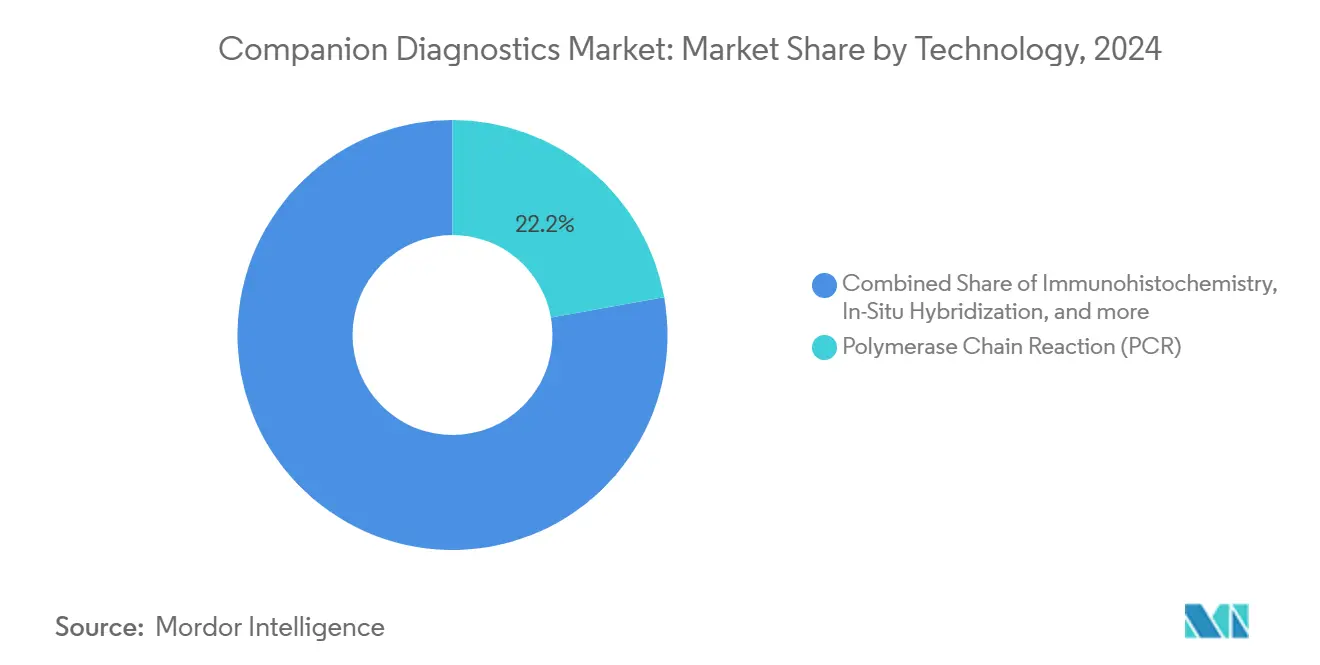
Nota: Participaciones de segmentos de todos los segmentos individuales disponibles con la compra del informe
Indicación: Melanoma Emerge como Frontera de Crecimiento
Los diagnósticos complementarios de melanoma capturarán una aceleración de participación de mercado a una TCAC del 13,6% hasta 2030 mientras proliferan las combinaciones de inmunoterapia. El impacto downstream es que las clínicas de dermatología deben coordinar estrechamente con laboratorios moleculares para asegurar pruebas de reflejo rápido, efectivamente mezclando dos silos clínicos históricamente separados. Esta integración fuerza a los vendedores de registros médicos electrónicos a adaptar módulos de entrada de órdenes para acomodar paneles moleculares de reflejo, un ajuste de TI que, aunque menor en la superficie, representa una inversión administrativa notable a través de los sistemas de salud.
Producto y Servicio: Soluciones de Software Aceleran el Crecimiento
Los ensayos y kits representan el 66,3% del gasto de 2024, impulsados por su vinculación uno a uno con lanzamientos de medicamentos específicos. Sin embargo, las plataformas interpretativas impulsadas por software representan la categoría de producto de crecimiento más rápido con una TCAC del 15,8% (2025-2030). La precisión diagnóstica depende de pipelines de clasificación de variantes que ahora están sujetos a actualizaciones continuas de aprendizaje automático, impulsando a los reguladores a contemplar controles de cambio de algoritmo post-mercado. Una consecuencia empresarial paralela está emergiendo: los laboratorios pueden incurrir en responsabilidad si declinan actualizaciones de software que podrían mejorar materialmente las llamadas clínicas, implícitamente enhilaando cláusulas de mantenimiento de software en auditorías de acreditación de laboratorio.
Tipo de Muestra: Biopsia Líquida Transforma Paradigmas de Pruebas
La biopsia de tejido aún representa el 78,5% de los volúmenes de 2024 porque la histología confirmatoria permanece como el estándar de oro regulatorio. Se proyecta que el tamaño del mercado de biopsia líquida se expanda una TCAC del 18,9% hasta 2030. Las prácticas oncológicas ya están reasignando personal de flebotomía para acomodar el aumento, sutilmente incrementando la demanda de dispositivos de procesamiento de sangre en punto de atención. Los laboratorios que históricamente se especializaron en histopatología de tejidos ahora deben invertir en sistemas de extracción de ADN de plasma, creando tensión de gastos operativos que influye los ciclos de presupuesto de capital.
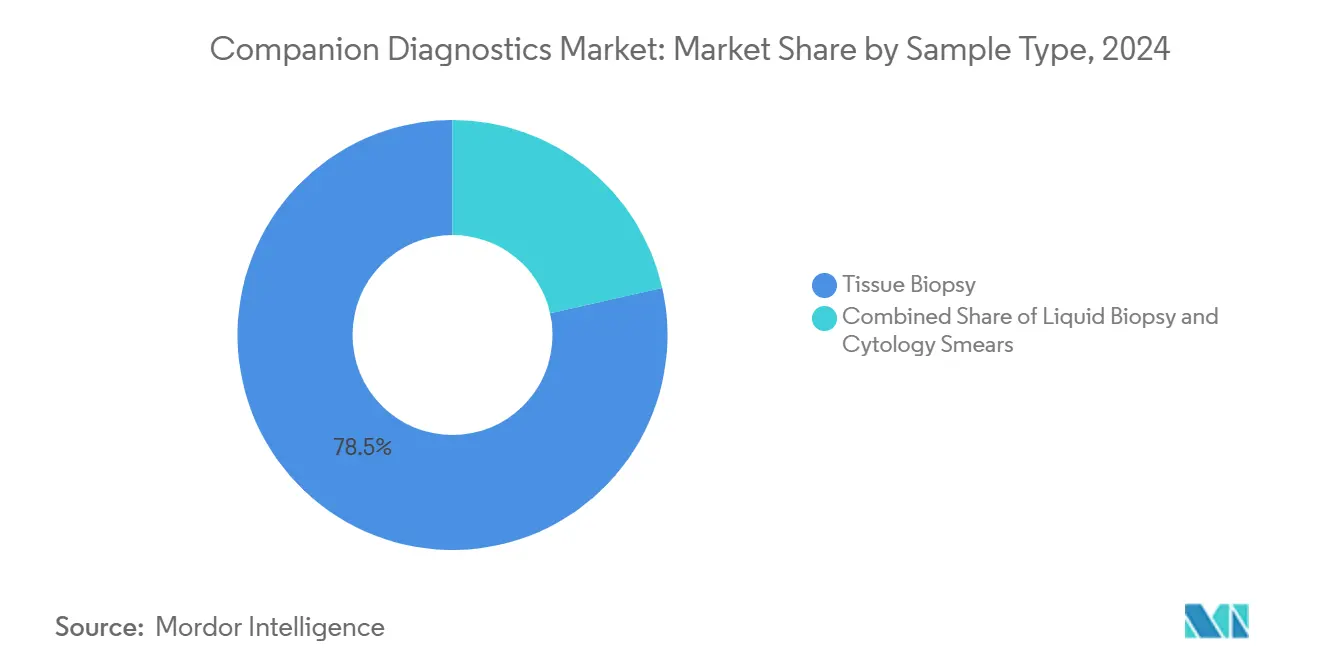
Nota: Participaciones de segmentos de todos los segmentos individuales disponibles con la compra del informe
Usuario Final: CRO Emergen como Socios Estratégicos
El tamaño del mercado de diagnósticos complementarios de las CRO está establecido para ascender una TCAC del 13,2% (2025-2030). Su amplitud de experiencia en validación de biomarcadores permite a biotecnológicas más pequeñas acceder a vías regulatorias que de otra manera serían prohibitivas. Este posicionamiento da a las CRO apalancamiento para negociar modelos de tarifas de compartir riesgo atados a hitos de ensayo, cambiándolos de vendedores de servicio hacia socios cuasi-desarrollo-un matiz que altera el reconocimiento de ingresos y podría mejorar la estabilidad del margen.
Análisis Geográfico
América del Norte mantiene una participación de mercado del 40,4% en 2024. La política de UnitedHealthcare de cubrir diagnósticos complementarios aprobados por la FDA cuando se emparejan con el medicamento correspondiente señala el respaldo del pagador que influye directamente la velocidad de adopción. Un resultado inferido es que los aseguradores privados fuera del paraguas de UnitedHealthcare pueden emular la política para permanecer competitivos, llevando a una cascada que puede estabilizar las tasas de reembolso de pruebas a nivel de industria. [4]UnitedHealthcare, "Coverage Summary: Molecular Diagnostics and Genetic Testing," UnitedHealthcare, uhc.com
Se proyecta que Asia-Pacífico registre una TCAC del 12,7% de 2025-2030. El programa de perfilado del genoma del cáncer (CGP) apoyado por el gobierno de Japón pronostica un mercado CGP de 54 mil millones de yenes para 2035, impulsando a los laboratorios domésticos a escalar la capacidad de secuenciación. Este compromiso gubernamental establece un precedente que países vecinos pueden replicar, armonizando expectativas regulatorias y estimulando la inscripción de ensayos clínicos transfronterizos que acelera la acumulación de datos en poblaciones asiáticas sub-estudiadas.
El ambiente del Reglamento de Diagnóstico In Vitro de Europa está impulsando a las empresas a reexaminar estrategias de lanzamiento. La capacidad limitada de cuerpos notificados amplifica el riesgo de tiempo al mercado, causando que las empresas de diagnósticos consideren modelos de pruebas centralizadas como soluciones interinas. Tal centralización puede inadvertidamente fortalecer laboratorios de referencia selectos, creando un cuasi-oligopolio que podría influir dinámicas de precios una vez que los volúmenes de pruebas alcancen su pico.
Panorama Competitivo
El ambiente competitivo mezcla jugadores diversificados como Roche con especialistas ágiles como Guardant Health. Los acuerdos de co-desarrollo estratégico permanecen fundamentales: el portafolio de Roche de más de 200 colaboraciones farmacéuticas ancla sus diagnósticos en muchos protocolos de ensayos clínicos, asegurando adopción casi automática en el lanzamiento comercial. Un vector competitivo sutil está emergiendo alrededor de la propiedad de datos; las empresas que controlan grandes conjuntos de datos genómicos del mundo real pueden refinar algoritmos predictivos más rápido, otorgándoles una ventaja iterativa poco probable de ser replicada por competidores de solo reactivos.
Líderes de la Industria de Diagnósticos Complementarios
-
Qiagen NV
-
Agilent Technologies Inc.
-
Abbott
-
Biomerieux
-
F. Hoffmann-La Roche Ltd
- *Nota aclaratoria: los principales jugadores no se ordenaron de un modo en especial
Desarrollos Recientes de la Industria
- Enero 2025: Roche recibió expansión de etiqueta de la FDA para el anticuerpo PATHWAY anti-HER2/neu para incluir cáncer de mama metastásico HR-positivo, HER2-ultrabajo
- Diciembre 2024: El PD-L1 IHC 28-8 pharmDx de Agilent aseguró certificación EU IVDR.
- Noviembre 2024: Roche obtuvo marca CE para el Ensayo VENTANA FOLR1 RxDx.
Alcance del Informe del Mercado Global de Diagnósticos Complementarios
Según el alcance del informe, las pruebas de diagnósticos complementarios proporcionan información esencial para usar de manera segura y efectiva un producto farmacológico o biológico correspondiente.
El mercado de diagnósticos complementarios está segmentado por tecnología, indicación y geografía. El segmento de tecnología se divide en inmunohistoquímica (IHC), reacción en cadena de la polimerasa (PCR), hibridización in-situ (ISH), PCR en tiempo real (RT-PCR), secuenciación génica, y otras tecnologías. El segmento de indicación se divide en cáncer de pulmón, cáncer de mama, cáncer colorrectal, leucemia, melanoma, y otras indicaciones. El informe también cubre los tamaños de mercado estimados y tendencias para 17 países a través de las principales regiones globalmente. El informe ofrece el valor en USD para estos segmentos.
| Inmunohistoquímica (IHC) |
| Reacción en Cadena de la Polimerasa (PCR) |
| PCR en Tiempo Real (RT-PCR) |
| Hibridización In-Situ (ISH) |
| Secuenciación de Nueva Generación / Génica (NGS) |
| Otras Tecnologías |
| Cáncer de Pulmón |
| Cáncer de Mama |
| Cáncer Colorrectal |
| Leucemia |
| Melanoma |
| Cáncer Gástrico |
| Cáncer de Próstata |
| Otras Indicaciones |
| Ensayos y Kits |
| Instrumentos y Analizadores |
| Software y Servicios |
| Biopsia de Tejido |
| Biopsia Líquida |
| Frotis de Citología |
| Empresas Farmacéuticas y Biotecnológicas |
| Organizaciones de Investigación por Contrato (CRO) |
| Laboratorios de Referencia Clínica |
| Hospitales y Centros de Cáncer |
| América del Norte | Estados Unidos |
| Canadá | |
| México | |
| Europa | Alemania |
| Reino Unido | |
| Francia | |
| Italia | |
| España | |
| Resto de Europa | |
| Asia-Pacífico | China |
| Japón | |
| India | |
| Corea del Sur | |
| Australia | |
| Resto de Asia-Pacífico | |
| Medio Oriente | CCG |
| Sudáfrica | |
| Resto del Medio Oriente | |
| América del Sur | Brasil |
| Argentina | |
| Resto de América del Sur |
| Por Tecnología | Inmunohistoquímica (IHC) | |
| Reacción en Cadena de la Polimerasa (PCR) | ||
| PCR en Tiempo Real (RT-PCR) | ||
| Hibridización In-Situ (ISH) | ||
| Secuenciación de Nueva Generación / Génica (NGS) | ||
| Otras Tecnologías | ||
| Por Indicación | Cáncer de Pulmón | |
| Cáncer de Mama | ||
| Cáncer Colorrectal | ||
| Leucemia | ||
| Melanoma | ||
| Cáncer Gástrico | ||
| Cáncer de Próstata | ||
| Otras Indicaciones | ||
| Por Producto y Servicio | Ensayos y Kits | |
| Instrumentos y Analizadores | ||
| Software y Servicios | ||
| Por Tipo de Muestra | Biopsia de Tejido | |
| Biopsia Líquida | ||
| Frotis de Citología | ||
| Por Usuario Final | Empresas Farmacéuticas y Biotecnológicas | |
| Organizaciones de Investigación por Contrato (CRO) | ||
| Laboratorios de Referencia Clínica | ||
| Hospitales y Centros de Cáncer | ||
| Por Geografía | América del Norte | Estados Unidos |
| Canadá | ||
| México | ||
| Europa | Alemania | |
| Reino Unido | ||
| Francia | ||
| Italia | ||
| España | ||
| Resto de Europa | ||
| Asia-Pacífico | China | |
| Japón | ||
| India | ||
| Corea del Sur | ||
| Australia | ||
| Resto de Asia-Pacífico | ||
| Medio Oriente | CCG | |
| Sudáfrica | ||
| Resto del Medio Oriente | ||
| América del Sur | Brasil | |
| Argentina | ||
| Resto de América del Sur | ||
Preguntas Clave Respondidas en el Informe
¿Qué tan grande es el Mercado de Diagnósticos Complementarios?
Se espera que el tamaño del Mercado de Diagnósticos Complementarios alcance USD 8,70 mil millones en 2025 y crezca a una TCAC del 12,42% para alcanzar USD 15,62 mil millones en 2030.
¿Cuál es el tamaño actual del Mercado de Diagnósticos Complementarios?
En 2025, se espera que el tamaño del Mercado de Diagnósticos Complementarios alcance USD 8,70 mil millones.
¿Quiénes son los jugadores clave en el Mercado de Diagnósticos Complementarios?
Qiagen NV, Agilent Technologies Inc., Abbott, Biomerieux y F. Hoffmann-La Roche Ltd son las principales empresas que operan en el Mercado de Diagnósticos Complementarios.
¿Cuál es la región de crecimiento más rápido en el Mercado de Diagnósticos Complementarios?
Se estima que Asia-Pacífico crezca a la TCAC más alta durante el período de pronóstico (2025-2030).
¿Qué región tiene la mayor participación en el Mercado de Diagnósticos Complementarios?
En 2025, América del Norte representa la mayor participación de mercado en el Mercado de Diagnósticos Complementarios.
¿Qué años cubre este Mercado de Diagnósticos Complementarios, y cuál fue el tamaño del mercado en 2024?
En 2024, el tamaño del Mercado de Diagnósticos Complementarios se estimó en USD 7,62 mil millones. El informe cubre el tamaño histórico del Mercado de Diagnósticos Complementarios para los años: 2019, 2020, 2021, 2022, 2023 y 2024. El informe también pronostica el tamaño del Mercado de Diagnósticos Complementarios para los años: 2025, 2026, 2027, 2028, 2029 y 2030.
Última actualización de la página el: