Tamaño y Participación del Mercado de Producción de Anticuerpos
Análisis del Mercado de Producción de Anticuerpos por Mordor inteligencia
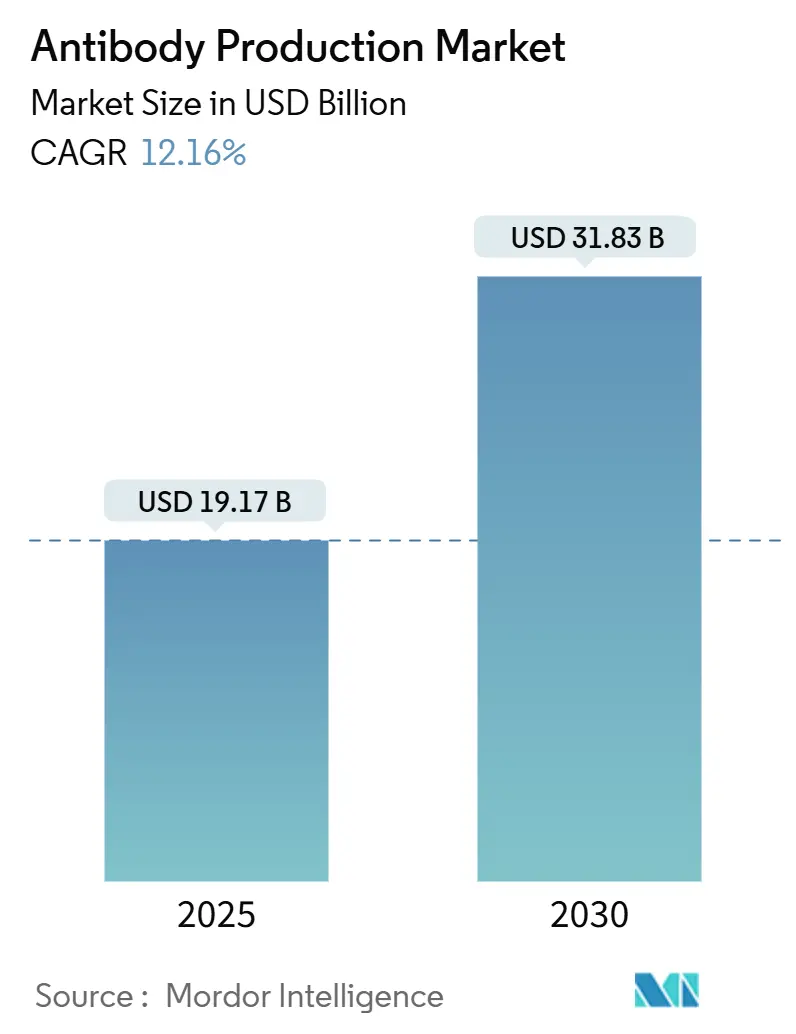
El tamaño del Mercado de Producción de Anticuerpos se estima en USD 19,17 mil millones en 2025, y se espera que alcance USD 31,83 mil millones en 2030, un una TCAC del 12,16% durante el poríodo de pronóstico (2025-2030).
La creciente adopción de biológicos dirigidos, la rápida aceptación de formatos biespecíficos y casos de uso diagnósticos más amplios están expandiendo la demanda en laboratorios terapéuticos, de investigación y clínicos. Las inversiones continuas en biorreactores de un solo uso están impulsando la flexibilidad de producción, mientras que las herramientas de inteligencia artificial están acortando los ciclos de desarrollo de líneas celulares y mejorando la consistencia de lotes. Las agencias reguladoras están apoyando la innovación un través de vícomo expeditas para biosimilares y construcciones de anticuerpos novedosas, permitiendo que empresas más pequeñcomo y fabricantes por contrato escalen rápidamente. Las dinámicas competitivas se están intensificando un medida que los proveedores de servicio completo adquieren capacidades especializadas y las organizaciones de desarrollo y fabricación por contrato (CDMOs) se diferencian un través de plataformas biespecíficas propietarias.
Conclusiones Clave del Informe
- Por producto, los consumibles lideraron con el 62,54% de la participación del mercado de producción de anticuerpos en 2024; se pronostica que los instrumentos-biorreactores crezcan un una TCAC del 11,98% hasta 2030.
- Por proceso, las operaciones upstream representaron el 58,15% de la participación del tamaño del mercado de producción de anticuerpos en 2024, mientras que la purificación río abajo se expande un una TCAC del 11,67% hasta 2030.
- Por tipo de anticuerpo, los IgG monoclonales mantuvieron el 70,67% de la participación del mercado de producción de anticuerpos en 2024; los anticuerpos biespecíficos registran la TCAC más rápida del 12,04% entre 2025-2030.
- Por usuario final, las empresas farmacéuticas y biotecnológicas comandaron el 63,34% de la participación del tamaño del mercado de producción de anticuerpos en 2024; los CDMOs registran la TCAC proyectada más alta del 12,78% hasta 2030.
- Por geografíun, América del Norte mantuvo una participación del 39,87% en 2024, mientras que Asia-Pacífico está en camino hacia una TCAC del 13,01% hasta 2030.
Tendencias mi Insights del Mercado Global de Producción de Anticuerpos
Análisis de Impacto de Impulsores
| Impulsor | (~) % Impacto en el Pronóstico de TCAC | Relevancia Geográfica | Pico de Impacto |
|---|---|---|---|
| Pipelines clínicos acelerados para ADCs | ~+3,2% | América del Norte y Asia-Pacífico (EE.UU., china) | Mediano plazo (3-4 unños) |
| Rápida ampliación de capacidad de biorreactores de un solo uso | ~+2,8% | Global, concentrado en América del Norte y Europa | Corto plazo (≤ 2 unños) |
| Víun rápida regulatoria para mAbs biosimilares | ~+2,4% | Global, pronunciado en UE, EE.UU., china | Mediano plazo (3-4 unños) |
| Desarrollo de líneas celulares habilitado por IA reduciendo variabilidad de títulos | ~+2,1% | Europa con extensión un América del Norte y Asia-Pacífico | Mediano plazo (3-4 unños) |
| Auge de externalización un CDMOs | ~+1,9% | Global, fuerte en EE.UU., china, India | Mediano plazo (3-4 unños) |
| Crecientes aprobaciones de anticuerpos biespecíficos | ~+2,0% | América del Norte y Europa, emergente en Asia | Mediano plazo (3-4 unños) |
| Adopción de plataformas de bioprocesamiento continuo | ~+1,6% | Global, adoptantes tempranos en EE.UU. y UE | Largo plazo (≥ 5 unños) |
| Fuente: Mordor Intelligence | |||
Pipelines Clínicos Acelerados para Conjugados Anticuerpo-Fármaco (ADCs) en Estados Unidos y China
Más de 600 candidatos ADC están en ensayos clínicos, y se esperan al menos 10 nuevas aprobaciones para 2027, subrayando el impulso sostenido en pipelines enfocados en oncologíun. La aprobación de la FDA en enero de 2025 de Datroway de AstraZeneca y Daiichi Sankyo redujo el riesgo de progresión de la enfermedad en doáncer de mama HR-positivo, HER2-negativo en un 37% comparado con quimioterapia AstraZeneca[1]Fuente: Samsung productos biológicos, "Instalaciones optimizadas para fabricación flexible y ágil," samsungbiologics.com. La expansión de capacidad está siguiendo; AstraZeneca comprometió USD 1,5 mil millones para una instalación ADC integral en Singapur que entra en operación en 2029 AstraZeneca. Inversiones similares un gran escala en china apoyan cronogramas acelerados bajo las prioridades de la Administración Nacional de Productos Médicos. Estos movimientos aumentan la demanda de suites de conjugación de alta potencia, contención de vectores virales y análisis avanzados. Mientras las agencias reguladoras refinan la orientación para conjugados complejos, los fabricantes que adoptan diseños modulares de salas limpias y sistemas de purificación de alto rendimiento están posicionados para capturar las necesidades clínicas emergentes.
Rápida Ampliación de Capacidad de Biorreactores de Un Solo Uso
Los biorreactores de un solo uso (SUBs) reducen el riesgo de contaminación cruzada y permiten cambios más rápidos, clave para instalaciones multi-producto. La Planta 5 de Samsung productos biológicos agregará volúmenes flexibles de sub mientras acorta el tiempo de construcción en un 30% comparado con instalaciones anteriores de acero inoxidable Samsung productos biológicos [2]Fuente: AstraZeneca, "Datroway aprobado en EE.UU. para doáncer de mama HR-positivo, HER2-negativo," astrazeneca.com. La integración de procesamiento continuo con SUBs está entregando ganancias de productividad del 25-30% y reduciendo las huellas de instalaciones en un 40% Pharma Focus América. La miniaturización de sensores, sondas de un solo uso y control de bucle cerrado ahora permiten ajustes de calidad en tiempo real, impulsando una adopción más amplia más todoá de lotes clínicos hacia programas comerciales de alto título. La trayectoria apoya una fuerte demanda para bolsas de reactor esterilizadas con gamma, unidades de accionamiento y rutas de flujo auxiliares desechables, reforzando el crecimiento del proveedor.
Vía Rápida Regulatoria para mAbs Biosimilares
La designación de intercambiabilidad de la FDA para Yuflyma de Celltrion establece un nuevo precedente que permite la sustitución en farmacia sin aprobación del médico FiercePharma. Reformas paralelas en china han reducido los cronogramas de aprobación de biosimilares un la mitad, resultando en 51 lanzamientos domésticos para finales de 2024, 31 de los cuales están basados en anticuerpos. Las vícomo aceleradas intensifican la competencia de precios y estimulan adiciones de capacidad, especialmente en Asia, donde Henlius envió 5,5 millones de unidades de biosimilar de trastuzumab un 47 países para mediados de 2024 Henlius. Los fabricantes están optimizando la reutilización de Proteína un, adoptando cromatografíun multi-columna y desplegando sistemas de ultrafiltración de paso único más grandes para mantenerse competitivos en costos mientras mantienen la comparabilidad.
Desarrollo de Líneas Celulares Habilitado por IA Reduciendo Variabilidad de Títulos en Europa
Los grupos europeos han adoptado modelos de aprendizaje automático que identifican nutrientes de medios que influyen en variantes de carga, ajustando el control sobre la glicosilación para biespecíficos complejos. Estudios de IA explicable destacaron el papel crítico de Fe, Zn, Cu y Mn en modular perfiles post-traduccionales Springer. La adopción de tales herramientas está recortando los cronogramas de desarrollo hasta en un 30% mientras aumenta la predictibilidad de títulos en etapas tempranas. La Agencia Europea de Medicamentos respondió actualizando las directrices de validación para incluir diseño de experimentos impulsado por IA ISPE. Los proveedores de servicios de ingenieríun de vectores, micro-biorreactores de alto rendimiento y análisis multi-ómicos se benefician un medida que los productores se dirigen hacia estrategias de desarrollo ricas en datos.
Análisis de Impacto de Restricciones
| Restricción | (~) % Impacto en el Pronóstico de TCAC | Relevancia Geográfica | Pico de Impacto | |
|---|---|---|---|---|
| Alto gastos de capital inicial para instalaciones de biofabricación grado GMP | ~-1,5% | Global, arrastre más fuerte en mercados emergentes | Largo plazo (≥ 5 unños) | |
| Barreras de propiedad intelectual para formatos biespecíficos novedosos | ~-1,2% | Japón con extensión global para innovadores biespecíficos | Mediano plazo (3-4 unños) | |
| Complejidad de Cumplimiento de Calidad por Diseño (QbD) para Biotecnológicas Pequeñcomo y Medianas | ~-1,0% | Global, especialmente EE.UU. y UE | Mediano plazo (3-4 unños) | |
| Escasez Crónica de Suministros de Componentes de Medios Libres de Proteína Recombinante | ~-0,7% | Global, acentuada en APAC durante picos de demanda | Corto plazo (≤ 2 unños) | |
| Fuente: Mordor Intelligence | ||||
Alto CAPEX Inicial para Instalaciones de Biofabricación Grado GMP
Construir una planta de anticuerpos de última generación puede superar los USD 200 millones, con salas limpias y servicios especializados representando el 60% del gasto bioproceso International. La recuperación de capital se extiende un través de 3-5 unños cuando se incluyen permisos, validación y licencias. Los entrantes de mercados emergentes enfrentan obstáculos de financiamiento más pronunciados y volatilidad de tasas de interés, frenando proyectos greenfield. Las instalaciones modulares prefabricadas pueden reducir el tiempo de construcción en 30-50%, sin embargo, el mayor costo de módulos importados compensa algunos ahorros Pharma Focus Asia. En consecuencia, la demanda de capacidad cdmo aumenta un medida que los innovadores postergan la propiedad un favor de modelos de tarifa por servicio, ralentizando marginalmente la expansión de ingresos vinculados un instalaciones.
Barreras de Propiedad Intelectual para Formatos Biespecíficos Novedosos en Japón
La oficina de patentes de Japón demanda datos extensivos en vitro para apoyar amplias reivindicaciones biespecíficas, elevando el estándar para el reconocimiento de pasos inventivos. Este régimen estricto ha retrasado las aprobaciones locales relativas un EE.UU. y UE, limitando el acceso de pacientes un modalidades de vanguardia. Las licencias cruzadas entre incumbentes agravan la complejidad, forzando un empresas más pequeñcomo un negociar términos desfavorables o diseñar alrededor de espesuras densas de patentes. Las presentaciones de Bristol-Myers Squibb ilustran un enfoque por capas combinando cobertura de composición, proceso y formulación para proteger activos en el mercado japonés. Los desarrolladores están respondiendo con arquitecturas biespecíficas estructuralmente distintas, sin embargo, los ciclos de ingenieríun iterativos alargan los cronogramas de comercialización, amortiguando la adopción un corto plazo.
Análisis de Segmentos
Por Producto: Los Biorreactores de Un Solo Uso Transforman la Economía de Fabricación
Los consumibles comandaron el 62,54% de la participación del mercado de producción de anticuerpos en 2024, reflejando la demanda constante de medios, resinas, tampones y filtros que apoyan cada lote de producción. Los altos volúmenes recurrentes crean flujos de efectivo predecibles para proveedores pero agregan gastos operativos para fabricantes trabajando para mejorar el costo de bienes. Los instrumentos-biorreactores son la categoríun de crecimiento más rápido, pronosticados para avanzar un una TCAC del 11,98% un medida que los diseños de un solo uso desplazan sistemas de acero inoxidable y permiten agilidad multi-producto. Los sensores integrados, rutas de flujo desechables y plásticos listos para gamma mitigan el riesgo de contaminación cruzada y acortan los cambios, alineándose con instalaciones que albergan programas diversos de biespecíficos y ADC.
Las estrategias de ampliación upstream dependen de trenes sub paralelos emparejados con captura continua, reduciendo la huella de instalaciones mientras apoyan títulos más todoá de 10 gramo/L. Los avances en consumibles, incluyendo ensamblajes de tuberíun inteligentes con etiquetas RFID incrustadas, simplifican la trazabilidad de materiales y ayudan al cumplimiento. un medida que los ciclos de vida de resinas se extienden un través de químicas novedosas tolerantes un álcalis, los operadores reducen volúmenes de tampón y disminuyen residuos, fortaleciendo métricas ambientales que son cada vez más rastreadas dentro de reportes ESG.
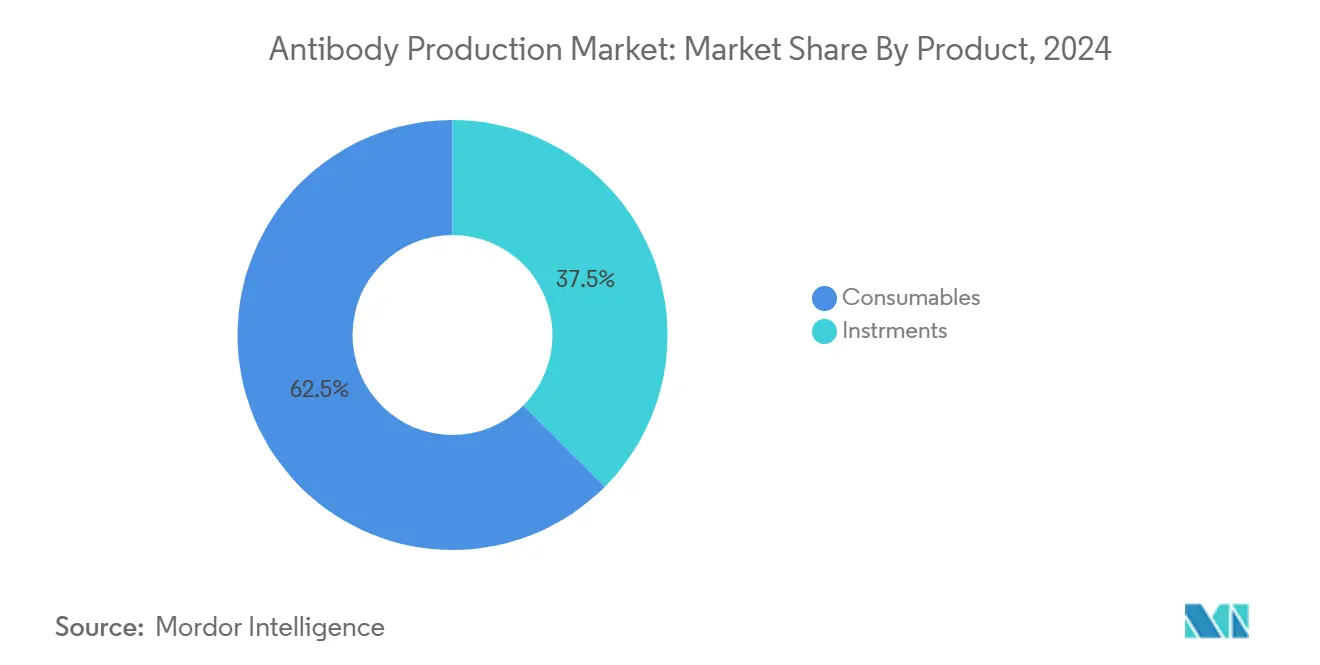
Nota: Participaciones de segmentos de todos los segmentos individuales disponibles con la compra del informe
Por Proceso: Innovaciones Downstream Abordan Cuellos de Botella de Purificación
Las operaciones upstream mantuvieron el 58,15% del tamaño del mercado de producción de anticuerpos en 2024, subrayando doómo la productividad de líneas celulares y el rendimiento del biorreactor impulsan la economíun general. Las mejoras de títulos emanan de huéspedes CHO diseñados que entregan rendimientos >10 gramo/L y estrategias optimizadas fed-batch que mitigan el agotamiento de nutrientes. Estas ganancias cambian el cuello de botella un la purificación río abajo, que por lo tanto está creciendo más rápido un una TCAC del 11,67% hasta 2030. Las resinas de cromatografíun multimodal adaptadas para anticuerpos biespecíficos mejoran la resolución y capacidades de carga, mientras que la filtración de profundidad de próxima generación se acopla con reactivos de floculación para clarificar cosechas de alta densidad de SUBs de 2.000 L.
La intensificación de procesos incorpora inactivación viral continua y filtración de flujo tangencial de paso único, creando trenes de purificación directa que reducen el tiempo de procesamiento en un 30%. Los patines de gestión de tampones equipados con dilución en línea frenan el consumo de agua y las necesidades de espacio en el piso. Los fabricantes que buscan la excelencia operacional están integrando modelos de balance de masa en tiempo real y control de retroalimentación habilitado por PAT, produciendo perfiles de glicosilación consistentes-un parámetro crítico para la comparabilidad regulatoria. La convergencia de intensificación upstream y río abajo desbloquea ahorros de costos y acelera la liberación de lotes, reforzando la competitividad en el mercado de producción de anticuerpos.
Por Tipo de Anticuerpo: Plataformas Biespecíficas Impulsan Pipeline de Innovación
Los anticuerpos IgG monoclonales retuvieron el 70,67% de la participación del mercado de producción de anticuerpos en 2024 debido un objetivos establecidos, procesos bien validados y amplia experiencia clínica. Las economícomo de escala y cadenas de suministro robustas apoyan márgenes atractivos para los principales vendedores. En paralelo, los anticuerpos biespecíficos se están expandiendo un una TCAC del 12,04% y se espera que alcancen USD 50 mil millones para 2030, reflejando su capacidad para involucrar objetivos duales para mayor eficacia Biointron. La complejidad de fabricación se centra en el emparejamiento correcto de cadenas ligeras y ensamblaje de heterodímeros, promoviendo innovaciones como Knobs-into-Holes y marcos de cadena ligera común.
Plataformas propietarias incluyendo Columvi de Roche, aprobado para linfoma B difuso de doélulas grandes en 2025, demuestran una reducción del 41% en el riesgo de mortalidad versus atención estándar FiercePharma. Los avances en reorientación de afinidad dual y tecnologícomo Beat® buscan simplificar la purificación habilitando captura de paso único. La intensidad sostenida de I+d alimenta la demanda de ensayos analíticos que cuantifican la afinidad objetivo y función efectora temprano en el desarrollo. Las construcciones basadas en fragmentos y conjugados anticuerpo-fármaco introducen diversidad adicional, sin embargo, cada formato aprovecha infraestructura upstream y río abajo compartida, reforzando el crecimiento cohesivo del mercado de producción de anticuerpos.
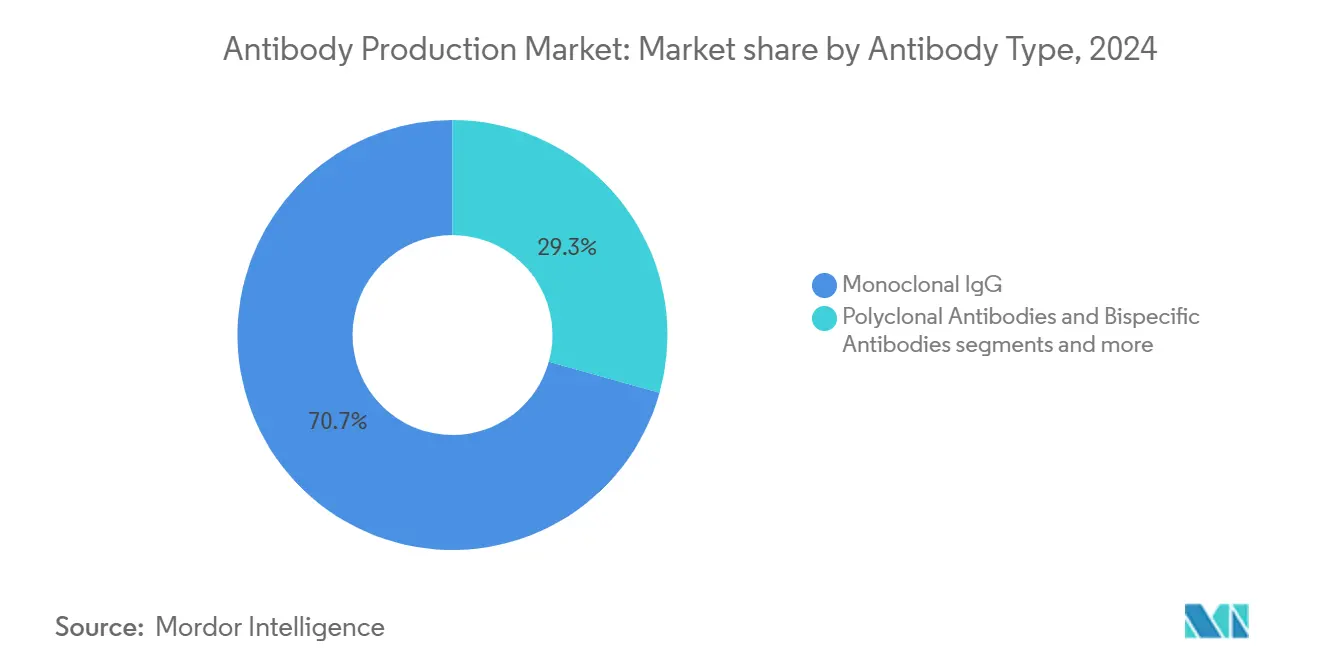
Nota: Participaciones de segmentos de todos los segmentos individuales disponibles con la compra del informe
Por Usuario Final: Los CDMOs Capturan Tendencia Creciente de Externalización
Las empresas farmacéuticas y biotecnológicas mantuvieron el 63,34% del tamaño del mercado de producción de anticuerpos en 2024, administrando amplios pipelines y suministro comercial global. unún comoí, la racionalización de capacidad y mitigación de riesgos motivan un grandes patrocinadores un externalizar programas selectos. Los CDMOs por lo tanto registran una TCAC líder del 12,78%, impulsada por la demanda de capacidad flexible y conocimiento especializado. WuXi productos biológicos informeó ingresos de RMB 18,7 mil millones en 2024, con una cartera de pedidos de USD 18,5 mil millones respaldada por 151 nuevos proyectos predominantemente originados en EE.UU. WuXi productos biológicos.
Los proveedores de servicios líderes aprovechan tecnologícomo propietarias como WuXiBody™ para resolver desafíos de ensamblaje biespecífico, mientras Lonza expande suites de conjugación para capturar la ola ADC creciente Lonza. Los laboratorios de diagnóstico ocupan un nicho más pequeño pero estable, aplicando anticuerpos para pruebas complementarias y ensayos de investigación que informan decisiones de medicina de precisión. Los institutos académicos y gubernamentales permanecen vitales para la innovación en etapa temprana, un menudo asociándose con CDMOs para traducir descubrimientos en lotes GMP. El paradigma de externalización intensifica la competencia, impulsando un los CDMOs un invertir en gemelos digitales, intensificación de procesos y orquestación de proyectos de extremo un extremo
Por Método: Plataformas In Vitro Mejoran Reproducibilidad
Los productores industriales dependen en gran medida de sistemas de expresión en vitro porque entregan ambientes controlados, variabilidad minimizada y salidas escalables. Las bibliotecas de despliegue de fagos que abarcan miles de millones de variantes expiden la selección de candidatos contra epítopos desafiantes, mientras el despliegue de ribosomas agrega una ruta libre de doélulas que acelera el cribado de expresión soluble. El mercado de producción de anticuerpos se beneficia un medida que estas plataformas simplifican los pipelines de descubrimiento temprano y alimentan secuencias de alta calidad en el desarrollo de procesos. Las mejoras en diseño de vectores, optimización de codones mi ingenieríun de doélulas huésped aumentan unún más la estabilidad de expresión, reduciendo la deserción en etapas tardícomo.
Los métodos en vivo permanecen necesarios para aplicaciones policlonales de amplio espectro, sin embargo, las presiones éticas y regulatorias limitan la expansión futura. Los ratones humanizados y cepas transgénicas capaces de producir anticuerpos completamente humanos satisfacen parte de la demanda mientras se alinean con principios 3Rs (reemplazo, reducción, refinamiento). La integración de aprendizaje automático para predecir solubilidad y riesgo de agregación un partir de datos de secuencia acorta los cronogramas de triaje de candidatos, reforzando ganancias de eficiencia un través de flujos de trabajo de la industria de producción de anticuerpos. un medida que las técnicas computacionales y de laboratorio húmedo convergen, el mercado anticipa tasas de éxito más altas y transiciones más rápidas desde el descubrimiento hasta la fabricación clínica.
Análisis Geográfico
América del Norte dominó el mercado de producción de anticuerpos con una participación del 39,87% en 2024, apoyado por mercados de capital sólidos, un denso clúster de empresas biofarmacéuticas y marcos regulatorios avanzados. El refinamiento continuo de la FDA de vícomo aceleradas fomenta la innovación en biespecíficos y biosimilares, sosteniendo la expansión del mercado. La integración de inteligencia artificial en análisis de producción se está volviendo mainstream, habilitando estrategias de liberación en tiempo real que reducen costos de inventario.
Asia-Pacífico entrega la TCAC más rápida del 13,01%, impulsada por ecosistemas de fabricación en expansión en china mi India y políticas gubernamentales de apoyo. La aprobación estadounidense de Jobevne de Biocon subraya las credenciales de calidad crecientes de India GaBIOnline. Los CDMOs regionales aumentan el procesamiento continuo y construcciones modulares de plantas para satisfacer necesidades domésticas y de exportación. La postura cautelosa de Japón sobre protección de propiedad intelectual para formatos biespecíficos ralentiza los lanzamientos locales pero fomenta soluciones estructurales inventivas.
Europa retiene peso significativo un través de su paisaje maduro de biosimilares, con 64 aprobaciones reflejando liderazgo regulatorio temprano. El énfasis en sostenibilidad impulsa la adopción de fabricación continua mi iniciativas de reducción de solventes. La Plataforma Europea de Monitoreo de Escasez y las directrices GMP revisadas para IA señalan vigilancia regulatoria hacia seguridad de suministro y supervisión digital ISPE.
Panorama Competitivo
El mercado de producción de anticuerpos está moderadamente concentrado, con Thermo Fisher Scientific, Merck KGaA y Danaher anclando la participación de primer nivel un través de portafolios integrados de reactivos, instrumentos y servicios. Las M&un estratégicas intensifican la presión competitiva; la adquisición de Seagen por Pfizer agrega un pipeline ADC diferenciado y conocimiento de fabricación, remodelando la distribución de capacidades BioPharma APAC. Los proveedores integrados capitalizan oportunidades de venta cruzada, agrupando hardware de un solo uso con consumibles de cromatografíun y sistemas de control digital.
Los innovadores especialistas persiguen oportunidades de espacio blanco en biespecíficos, multiespecíficos mi ingenieríun Fc. F-star terapéutica aprovecha su plataforma mAb²™ para generar biespecíficos tetravalentes, mientras Zymeworks avanza construcciones Azymetric que retienen arquitectura IgG natural. Estos jugadores se asocian con CDMOs para compensar la intensidad de capital, intercambiando acceso un tecnologíun por espacios de fabricación. La amplitud y profundidad de propiedad intelectual define cada vez más el apalancamiento de negociación, promoviendo presentaciones robustas de patentes que abarcan configuraciones de proceso, formulación y dispositivo.
El liderazgo tecnológico se ha convertido en un factor decisivo de éxito. Las empresas integran análisis predictivos en bucles de control en tiempo real, elevando rendimientos de lotes y reduciendo desviaciones. Las plataformas de bioprocesamiento continuo, selección de líneas celulares guiada por IA y cribado de alto rendimiento equipan un las empresas para entregar productos más rápidos y de menor costo. El panorama competitivo en evolución recompensa la agilidad, diferenciación tecnológica y fluidez regulatoria global, asegurando impulso sostenido en el mercado de producción de anticuerpos.
Líderes de la Industria de Producción de Anticuerpos
-
Sartorius AG
-
Danaher Corporation
-
Merck KGaA
-
Eppendorf AG
-
Thermo Fisher Scientific
- *Nota aclaratoria: los principales jugadores no se ordenaron de un modo en especial
Desarrollos Recientes de la Industria
- Enero 2025: AstraZeneca recibió aprobación de la FDA para Datroway (datopotamab deruxtecan) para doáncer de mama metastásico HR-positivo, HER2-negativo previamente tratado, reduciendo el riesgo de progresión de la enfermedad en un 37%.
- Marzo 2025: Lonza extendió una asociación para fabricación ADC de escala comercial y comenzó un construir una nueva suite de bioconjugación en Visp, Suiza.
- Enero 2025: Columvi de Roche se convirtió en el primer anticuerpo biespecífico de Europa aprobado para linfoma B difuso de doélulas grandes, reduciendo el riesgo de mortalidad en un 41% FiercePharma.
Alcance del Informe Global del Mercado de Producción de Anticuerpos
Según el alcance del informe, la producción de anticuerpos se refiere al proceso de crear un anticuerpo específico. En un sentido amplio, consiste en varios métodos, tales como upstream, río abajo y filtración. El proceso involucra la preparación de muestras de antígeno, que se inyectan en animales de laboratorio o granja para evocar altos niveles de expresión de anticuerpos específicos de antígeno en el suero, los cuales son luego recuperados del animal. El Mercado de Producción de Anticuerpos está Segmentado por Tipo de Anticuerpo (Anticuerpos Monoclonales, Anticuerpos Policlonales, Otros Tipos de Anticuerpos), Proceso (Procesamiento Upstream, Procesamiento río abajo, Filtración), Usuario Final (Empresas Farmacéuticas y Biotecnológicas, Laboratorios de Investigación, Otros Usuarios Finales), y Geografíun (América del Norte, Europa, Asia-Pacífico, Medio Oriente y África, y América del Sur). El informe también cubre los tamaños de mercado estimados y tendencias para 17 países un través de las principales regiones globalmente. El informe ofrece el valor (en millones USD) para los segmentos anteriores.
| Consumibles | Medios y Sueros |
| Reactivos y Suplementos | |
| Tampones y Químicos | |
| Instrumentos | Biorreactores |
| Sistemas de Cromatografía | |
| Dispositivos de Filtración y Separación | |
| Equipo de Laboratorio de Apoyo |
| Procesamiento Upstream | Desarrollo de Líneas Celulares |
| Expansión de Cultivo y Sistemas de Expresión | |
| Procesamiento Downstream | Clarificación y Captura |
| Purificación | |
| Formulación y Llenado-Acabado |
| Anticuerpos Monoclonales |
| Anticuerpos Policlonales |
| Anticuerpos Biespecíficos |
| Fragmentos de Anticuerpos |
| Empresas Farmacéuticas y Biotecnológicas |
| Organizaciones de Fabricación / Investigación por Contrato (CMOs/CROs) |
| Institutos de Investigación Académicos y Gubernamentales |
| Laboratorios de Diagnóstico |
| América del Norte | Estados Unidos |
| Canadá | |
| México | |
| Europa | Alemania |
| Reino Unido | |
| Francia | |
| Italia | |
| España | |
| Resto de Europa | |
| Asia-Pacífico | China |
| Japón | |
| India | |
| Corea del Sur | |
| Australia | |
| Resto de Asia | |
| Medio Oriente y África | CCG |
| Sudáfrica | |
| Resto de Medio Oriente y África | |
| América del Sur | Brasil |
| Argentina | |
| Resto de América del Sur |
| Por Producto | Consumibles | Medios y Sueros |
| Reactivos y Suplementos | ||
| Tampones y Químicos | ||
| Instrumentos | Biorreactores | |
| Sistemas de Cromatografía | ||
| Dispositivos de Filtración y Separación | ||
| Equipo de Laboratorio de Apoyo | ||
| Por Proceso | Procesamiento Upstream | Desarrollo de Líneas Celulares |
| Expansión de Cultivo y Sistemas de Expresión | ||
| Procesamiento Downstream | Clarificación y Captura | |
| Purificación | ||
| Formulación y Llenado-Acabado | ||
| Por Tipo de Anticuerpo | Anticuerpos Monoclonales | |
| Anticuerpos Policlonales | ||
| Anticuerpos Biespecíficos | ||
| Fragmentos de Anticuerpos | ||
| Por Usuario Final | Empresas Farmacéuticas y Biotecnológicas | |
| Organizaciones de Fabricación / Investigación por Contrato (CMOs/CROs) | ||
| Institutos de Investigación Académicos y Gubernamentales | ||
| Laboratorios de Diagnóstico | ||
| Por Geografía | América del Norte | Estados Unidos |
| Canadá | ||
| México | ||
| Europa | Alemania | |
| Reino Unido | ||
| Francia | ||
| Italia | ||
| España | ||
| Resto de Europa | ||
| Asia-Pacífico | China | |
| Japón | ||
| India | ||
| Corea del Sur | ||
| Australia | ||
| Resto de Asia | ||
| Medio Oriente y África | CCG | |
| Sudáfrica | ||
| Resto de Medio Oriente y África | ||
| América del Sur | Brasil | |
| Argentina | ||
| Resto de América del Sur | ||
Preguntas Clave Respondidas en el Informe
¿Cuál es el tamaño actual del Mercado de Producción de Anticuerpos?
El mercado de producción de anticuerpos se sitúun en USD 19,17 mil millones en 2025 y se proyecta que crezca un USD 31,83 mil millones para 2030.
¿Qué categoríun de producto se está expandiendo más rápido?
Los instrumentos-biorreactores, particularmente sistemas de un solo uso, muestran el crecimiento más alto con una TCAC del 11,98% hasta 2030.
¿Por qué son importantes los anticuerpos biespecíficos?
Los anticuerpos biespecíficos pueden unirse un dos objetivos distintos simultáneamente, mejorando la eficacia terapéutica mi impulsando una TCAC del 12,04%, la más alta entre tipos de anticuerpos.
¿Qué tan rápido está creciendo Asia-Pacífico?
Se pronostica que Asia-Pacífico registre una TCAC del 13,01% de 2025-2030, convirtiéndolo en el mercado regional de crecimiento más rápido.
¿Por qué las empresas externalizan la producción de anticuerpos?
La externalización un CDMOs ofrece capacidad flexible y experiencia especialista, destacada por la TCAC proyectada del 12,78% de los CDMOs.
¿Qué papel juegan los biorreactores de un solo uso en la expansión del mercado?
Los biorreactores de un solo uso reducen el riesgo de contaminación y costos de capital, contribuyendo ~+2,8 puntos porcentuales un la TCAC general del mercado.
Última actualización de la página el:



