Mäusemodell-Marktgröße und -anteil
Mäusemodell-Marktanalyse von Mordor Intelligence
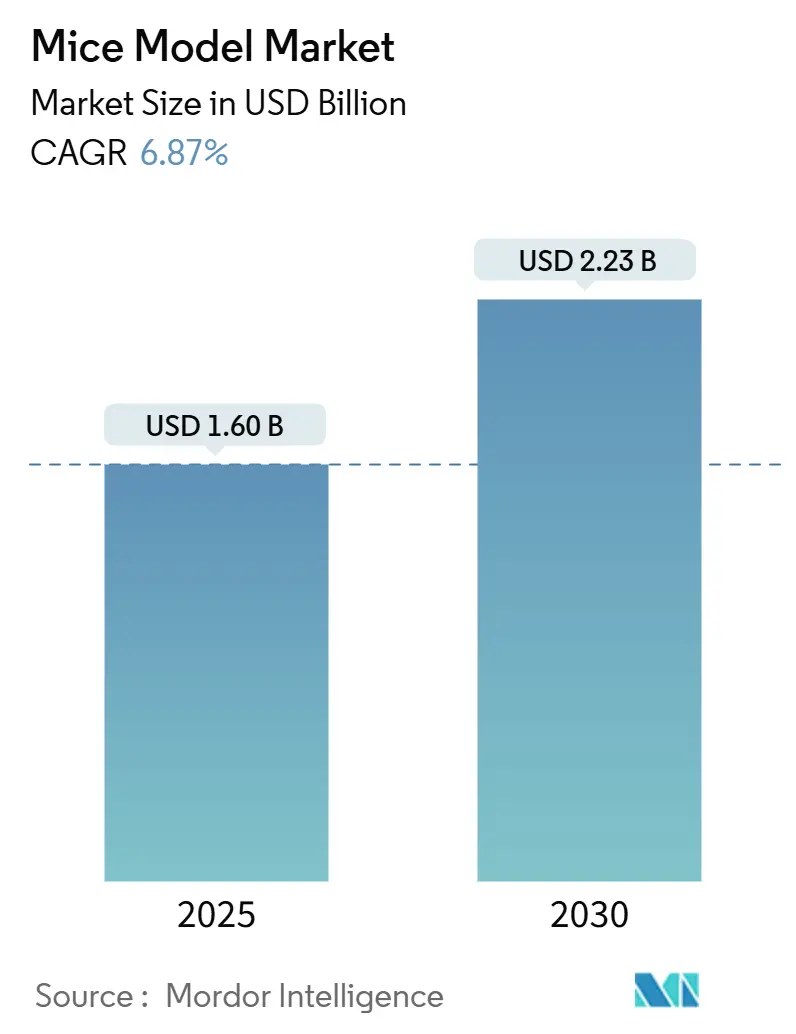
Die Mäusemodell-Marktgröße wird auf 1,60 Milliarden USD im Jahr 2025 geschätzt und soll bis 2030 2,23 Milliarden USD erreichen, mit einer CAGR von 6,87%. Die stetige Nachfrage stammt aus Onkologie-, Immunologie- und Seltene-Krankheiten-Pipelines, die auf gentechnisch veränderte Stämme mit größerer translationaler Validität angewiesen sind. CRISPR/Cas9 behält den größten Technologie-Fußabdruck und ist gleichzeitig die am schnellsten wachsende Methode, verkürzt Modellgenerierungs-Zeitpläne und senkt Kosten. Nordamerika behält die Führung dank konzentrierter F&E-Finanzierung und intensiver pharmazeutischer Aktivität, dennoch schließt Asien-Pazifik die Lücke, während China, Japan und Südkorea Kapital in lokale Zuchtinfrastruktur investieren. Auftragsforschungsorganisationen (CROs) erobern einen wachsenden Anteil ausgelagerter Studien, während humanisierte Immunsystem- und patientenabgeleitete Xenotransplantat (PDX)-Bibliotheken für Immuno-Onkologie-Validierung an Bedeutung gewinnen. Regulatorische Dynamik hin zu alternativen Methoden führt zu Gegenwind, drängt aber auch Modellentwickler dazu, höher-treue, ethisch verfeinerte Linien zu liefern.
Wichtige Berichts-Erkenntnisse
- Nach Maustyp führten Inzuchtmäuse mit 31,67% des Mäusemodell-Marktanteils in 2024; gentechnisch veränderte Mäuse werden voraussichtlich mit einer CAGR von 10,00% bis 2030 expandieren.
- Nach Service beherrschten Zuchtdienste 44,59% des Mäusemodell-Marktes in 2024, während genetische Tests am schnellsten mit 9,20% CAGR bis 2030 wachsen werden.
- Nach Technologie hielt CRISPR/Cas9 38,21% der Mäusemodell-Marktgröße in 2024 und wird mit einer CAGR von 13,90% über den Prognosezeitraum voranschreiten.
- Nach Anwendung entfielen 41,44% des Mäusemodell-Marktes in 2024 auf die Onkologie, während Infektionskrankheitsstudien für eine CAGR von 11,00% zwischen 2025-2030 positioniert sind.
- Nach Endverbraucher kontrollierten Pharma- und Biopharma-Unternehmen 48,53% des Mäusemodell-Marktes in 2024; CROs verzeichnen die höchsten Wachstumsaussichten mit 9,00% CAGR.
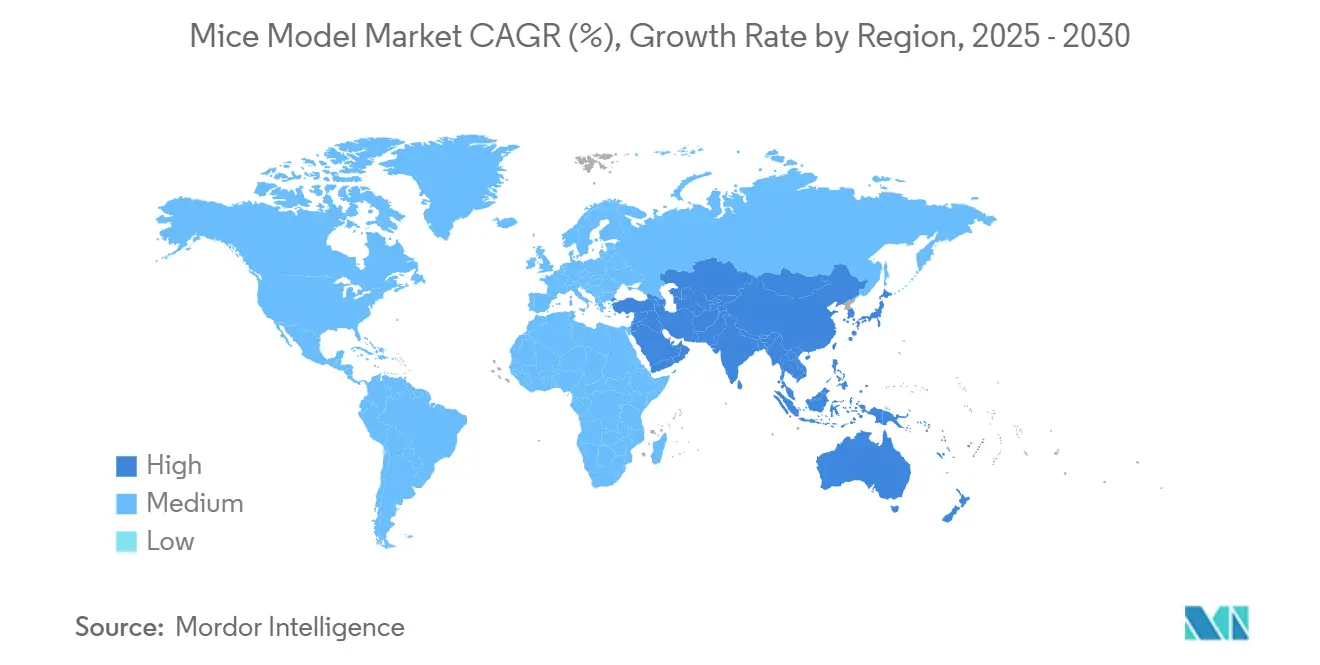
- Geografisch behielt Nordamerika 41,92% des globalen Mäusemodell-Marktes in 2024; Asien-Pazifik verzeichnet die schnellste regionale CAGR mit 8,26% bis 2030.
Globale Mäusemodell-Markttrends und Einblicke
Treiber-Auswirkungsanalyse
| Treiber | (~) % Auswirkung auf CAGR-Prognose | Geografische Relevanz | Auswirkungszeitplan |
|---|---|---|---|
| Proliferation von humanisierten Mäusen für Immuno-Onkologie-Arzneimittel- Validierung | +1.7% | Nordamerika, Europa, China | Mittelfristig (2-4 Jahre) |
| Schnelle Einführung von CRISPR-editierten Knock-In-Modellen für Zielgen- Funktionsstudien | +1.4% | Global, mit Konzentration in USA, Europa, Japan | Kurzfristig (≤ 2 Jahre) |
| Expansion von Auftrags-Zuchtdiensten zur Unterstützung des Big-Pharma-Pipeline-Anstiegs | +1.2% | Nordamerika, Europa, aufkommend in APAC | Mittelfristig (2-4 Jahre) |
| Beschleunigende Nachfrage nach patientenabgeleiteten Xenotransplantat (PDX)- Bibliotheken bei CROs | +1.0% | Nordamerika, Europa, China, Japan | Mittelfristig (2-4 Jahre) |
| Hochdurchsatz-In-Vivo-Screening-Präferenz in präklinischer Toxikologie | +0.8% | Global, mit früher Einführung in USA und Europa | Kurzfristig (≤ 2 Jahre) |
| Staatlich finanzierte Konsortien fördern Seltene-Krankheiten-Mausmodell- Repositories | +0.7% | Nordamerika, Europa, Japan | Langfristig (≥ 4 Jahre) |
| Quelle: Mordor Intelligence | |||
Humanisierte Mäuse revolutionieren Immuno-Onkologie-Validierung
Humanisierte Modelle, die durch Transplantation menschlicher Immunkomponenten in immundefiziente Stämme erzeugt werden, ersetzen traditionelle Xenotransplantate rasch. Diese Mäuse replizieren Checkpoint-Inhibitor- und CAR-T-Reaktionen treuer und verkürzen Spätstadium-Ausfälle. BioDuro berichtet von einer 70%igen Steigerung der Vorhersagegenauigkeit für Immuntherapien, was die Verwendung über Wirksamkeitsstudien hinaus auf Sicherheit und Biomarker-Entdeckung ausdehnt. Harvard-Wissenschaftler identifizierten kürzlich neuartige PD-1-Resistenzmechanismen in solchen Modellen und verdeutlichten deren analytische Tiefe. Pharmazeutische Sponsoren weisen daher größere Budgets für humanisierte Kohorten zu, was die wiederkehrende Nachfrage in Nordamerika, Europa und China steigert.
CRISPR-Technologie beschleunigt genetische Modellentwicklung
CRISPR/Cas9 hat die Mauslinien-Erstellung von mehrjährigen Projekten zu mehrmonatigen Unternehmungen verändert. Yales 2025 Cas12a-Plattform[1]Yale News, 'New CRISPR Tool Enables More Seamless Gene Editing,' news.yale.edu ermöglicht multiplexe Editierungen in einer Generation, während Taconic 40% niedrigere Produktionskosten im Vergleich zu embryonalen Stammzell-Methoden zeigt. Mehr als 60% der kundenspezifischen Bestellungen spezifizieren jetzt CRISPR-Designs, was Lieferanten dazu drängt, automatisierte Mikroinjektion und Elektroporation zu skalieren. Mit steigender Komplexität werden multiplexe Editierungen für polygene Störungen wesentlich, was den Wachstumspfad der Technologie verstärkt.
Auftrags-Zuchtdienste unterstützen Big-Pharma-Pipeline-Anstieg
Pharma-Sponsoren kürzen zunehmend fixe Infrastrukturkosten und lagern Kolonie-Expansion und Qualitätskontrolle aus. Boston Children's Mouse Gene Manipulation Core veranschaulicht integrierte Angebote, die CRISPR-Knock-ins, Embryo-Mikroinjektion, Quarantäne und Kryokonservierung umfassen.[2]Boston Children's Hospital, 'Research Cores,' Boston Children's Hospital, research.childrenshospital.org Outsourcing liefert 30-40% operative Einsparungen und beschleunigt Studienstarts durch Vermeidung von Facility-Aufbauten. Lieferanten investieren in hochdurchsätzige genetische Überwachung zur Eindämmung von Drift, in Übereinstimmung mit Reproduzierbarkeitsmandaten. Während Arzneimittel-Pipelines anschwellen, rüsten sich mittelgroße CROs in Nordamerika und Europa um, um der Nachfrage gerecht zu werden, während APAC-Einsteiger Preisflexibilität hinzufügen.
Patientenabgeleitete Xenotransplantat-Bibliotheken werden wesentlich für Onkologie-Arzneimittelentwicklung
PDX-Modelle behalten Patiententumor-Heterogenität bei und ermöglichen genauere Wirksamkeits-Screenings. Crown Biosciences Sammlung umfasst jetzt über 3.000 Modelle, und die XENTURION-Biobank[3]Franco Bertotti, 'XENTURION: Matched PDX and Tumoroid Resource for Metastatic Colorectal Cancer,' Nature Communications, nature.com integriert 128 kolorektale PDXs mit Omik-Annotationen und schärft Patientenstratifizierungs-Einblicke. Sponsoren schreiben PDX-geleiteter Auswahl 15-20% weniger Phase-II/III-Ausfälle zu, was sich in Multi-Milliarden-Dollar-F&E-Einsparungen niederschlägt. CROs skalieren daher dedizierte PDX-Einrichtungen und kombinieren sie mit Tumoroid-Screening, insbesondere für Immuno-Onkologie-Kombinationen.
Hemmnisse-Auswirkungsanalyse
| Hemmnis | (~) % Auswirkung auf CAGR-Prognose | Geografische Relevanz | Auswirkungszeitplan |
|---|---|---|---|
| Fortschritte bei In-Silico-Organ-on-Chip-Alternativen reduzieren Tierverwendung | -1.0% | Nordamerika, Europa, aufkommend in APAC | Mittelfristig (2-4 Jahre) |
| Strenge 3Rs-Compliance und Ethikprüfungs-Verzögerungen | -0.8% | Global, mit stärkster Auswirkung in Europa | Kurzfristig (≤ 2 Jahre) |
| Lieferstörungen durch Pathogen-freie Kolonie-Wartungskosten | -0.7% | Global | Kurzfristig (≤ 2 Jahre) |
| Steigender öffentlicher Druck treibt Investor-ESG-Beschränkungen an | -0.5% | Europa, Nordamerika | Mittelfristig (2-4 Jahre) |
| Quelle: Mordor Intelligence | |||
Fortschritte bei In-Silico- und Organ-on-Chip-Alternativen reduzieren Tierverwendung
Künstliche Intelligenz-Modellierung und mikrofluidische Organ-Chips gewinnen regulatorische Ermutigung, wobei die FDA einen Fahrplan zum Ausstieg aus bestimmten monoklonalen Antikörper-Assays skizziert.[4]U.S. Food and Drug Administration, 'Roadmap to Reducing Animal Testing in Preclinical Safety Studies,' fda.gov Diese Plattformen bieten schnelle Toxizitätsdaten und ethische Vorteile und ziehen Risikokapital in Nordamerika und Europa an. Dennoch bleibt die Komplexität ganzer Organismen schwer nachzuahmen, was Forscher dazu veranlasst zu bemerken, dass systemische Immun- und Stoffwechselwechselwirkungen noch immer murine Bestätigung erfordern. Folglich werden alternative Werkzeuge mittelfristig als ergänzend und nicht als völliger Ersatz betrachtet.
Strenge 3Rs-Compliance schafft regulatorische Hürden
Globale Ethikkomitees setzen jetzt strengere Ersatz-, Reduzierungs- und Verfeinerungs-Standards durch. Europa hat unter der aktualisierten Richtlinie 2010/63/EU zusätzliche Dokumentationsebenen hinzugefügt, während das FDA-Modernisierungsgesetz 2.0 Nicht-Tierdatenpakete in einigen Fällen erlaubt. Prüfungen verlängern Studien-Zeitpläne und erhöhen Verwaltungskosten, insbesondere für kleinere Labore mit begrenztem regulatorischem Personal. Große akademische Zentren reagieren mit Trainingsprogrammen und digitalen Tracking-Tools, dennoch belasten Verzögerungen weiterhin Projektstarts und können kurzfristiges Wachstum dämpfen.
Segmentanalyse
Nach Maustyp: Gentechnisch veränderte Mäuse treiben Präzisionsmedizin voran
Genetisch einheitliche Inzuchtstämme eroberten 31,67% des Mäusemodell-Marktanteils in 2024 und verstärkten ihre Rolle bei der Assay-Reproduzierbarkeit. Dennoch entwickeln sich gentechnisch veränderte Mäuse mit einer CAGR von 10,00% weiter, da CRISPR-Multiplexing komplexe Allel-Kombinationen vereinfacht. Die Mäusemodell-Marktgröße, die mit diesen gentechnisch veränderten Linien verbunden ist, soll zwischen 2025 und 2030 etwa 430 Millionen USD hinzufügen, angetrieben von Onkologie- und neurodegenerativen Studien, die polygene Konstrukte erfordern. Forscher schätzen schnelle Knockout-, Knock-in- und bedingte Systeme, die Genfunktion in Echtzeit klären. Auszucht-Bestände bleiben für Populationsvielfalt-Modellierung relevant, während Hybrid-/kongene Linien Immunologie-Nischen bedienen, wo MHC-Kompatibilität von größter Bedeutung ist. Lieferanten bündeln zunehmend Genotypisierung, Phänotypisierung und Kolonie-Management, um wissenschaftliche Strenge zu gewährleisten und geistiges Eigentum zu schützen, das mit maßgeschneiderten Stämmen verbunden ist. Kollaborative Konsortien erweitern globale Repositories, demokratisieren den Zugang und reduzieren Duplikation von Bemühungen zwischen Laboratorien.
Langfristig wird erwartet, dass multigene humanisierte Plattformen Einzelgen-Mutanten überholen, da Sponsoren größere menschliche Übertragbarkeit fordern. Partnerschaften zwischen akademischen Genomzentren und kommerziellen Züchtern haben Linien-Validierung beschleunigt und geholfen, frühere Engpässe bei Embryo-Verfügbarkeit zu vermeiden. Fortgeschrittene Kryokonservierung reduziert Drift und ermöglicht es Laboren, kritische Allele ohne aktive Zucht zu speichern. Vor diesem Hintergrund werden gentechnisch veränderte Murin-Modelle für mechanismus-fokussierte Präzisionsmedizin-Pipelines unverzichtbar und unterstützen therapeutische Modalitäten von Gen-Editierung bis zu Antikörper-Arzneimittel-Konjugaten.
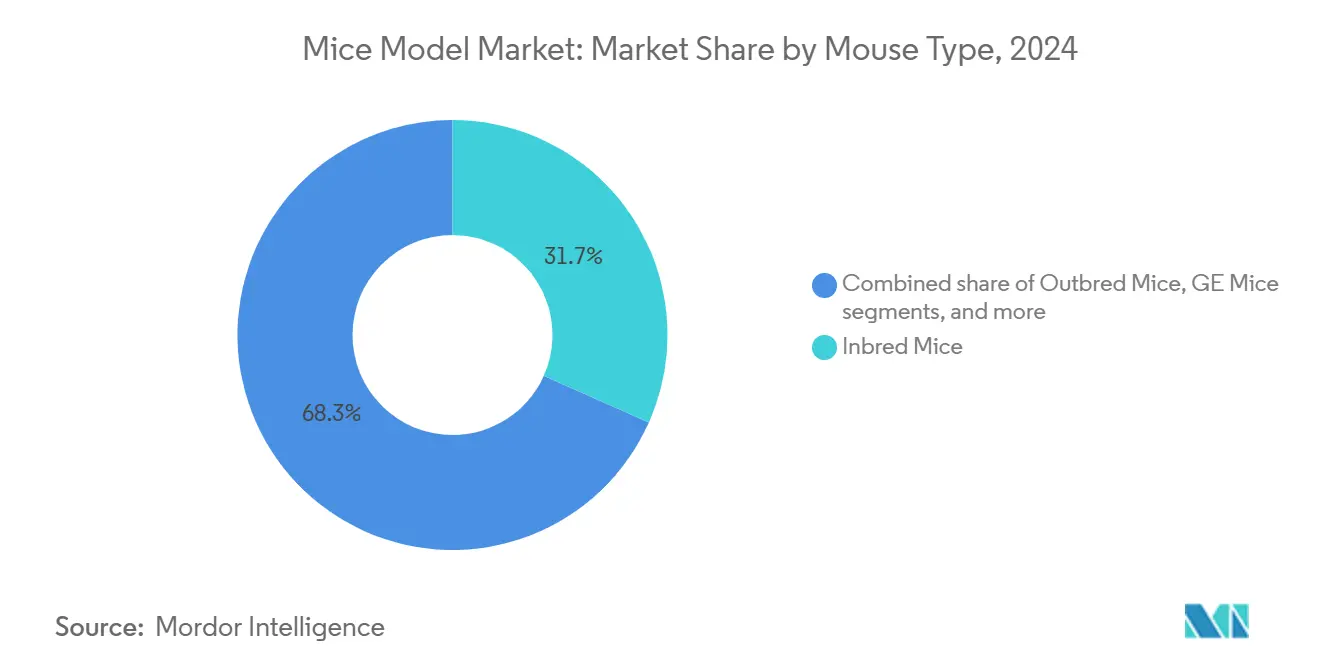
Notiz: Segmentanteile aller individuellen Segmente verfügbar beim Berichtskauf
Nach Service: Genetische Tests entstehen als Wachstumsmotor
Zuchtdienste hielten 44,59% des Mäusemodell-Marktes in 2024 und unterstrichen den grundlegenden Bedarf für zuverlässige Kolonie-Expansion. Dennoch steigen genetische Tests am schnellsten mit einer CAGR von 9,20%, da Sponsoren molekulare Bestätigung jeder Editierung benötigen, bevor sie sich zu GLP-Toxikologie-Studien verpflichten. Die Mäusemodell-Marktgröße, die mit Tests verbunden ist, sollte bis 2030 220 Millionen USD erreichen und spezialisierte Laboratorien mit Next-Generation-Sequenzierungs-Plattformen begünstigen. Kryokonservierungsdienste fügen Widerstandsfähigkeit hinzu, bewahren hochwertiges Keimplasma und gleichen Pathogen-Risiken aus. Rederivation und Quarantäne bleiben Compliance-Grundpfeiler, insbesondere nach hochkarätigen Kontaminationsereignissen, die strengere Vivarium-Audits auslösten.
Service-Anbieter differenzieren sich durch integrierte Dashboards, die Zucht-Metriken, Genotyp-Ergebnisse und Gesundheitsstatus in Echtzeit verfolgen. Führende Unternehmen setzen Barcoding und KI-gestützte Bilderkennung ein, um phänotypische Drift früh zu kennzeichnen. Pharmazeutische Kunden schätzen diese Transparenz und integrieren oft Qualitätsklauseln in Master-Service-Vereinbarungen. Folglich migriert das Service-Ökosystem von transaktionalen Aufgaben hin zu datenreichen, beratenden Engagements, die genetische Einblicke in jede Phase der Modellnutzung einweben.
Nach Technologie: CRISPR/Cas9 revolutioniert Modellgenerierung
CRISPR/Cas9 beherrschte 38,21% des Mäusemodell-Marktes in 2024 und wird voraussichtlich mit 13,90% CAGR beschleunigen. Seine Dominanz stammt aus unübertroffener Editierungseffizienz, validiert durch Yales Cas12a-System, das Multiplex-Editierungen in einer einzigen Generation ausführt. Embryonale Stammzell-Injektion dient weiterhin großen Fragment-Integrationen, die für Reporter-Konstrukte kritisch sind, während Kerntransfer Nischen-Klonierungskapazitäten trotz technischem Overhead bietet. Automatisierte Mikroinjektionssysteme erreichen jetzt 94% Pipetten-Insertionsgenauigkeit und reduzieren Variabilität und Arbeitskosten.
In der Zukunft reduziert CRISPR-VIM-virusähnliche Partikel-Abgabe-Embryo-Handling und könnte den Zugang für Labore ohne fortgeschrittene Mikromanipulationsausrüstung erweitern. Lieferanten nutzen cloud-basierte Design-Pipelines, die Guide-RNA-Off-Target-Scores berechnen und Angebot-zu-Konstrukt-Zyklen verkürzen. Während sich geistiges Eigentum-Streitigkeiten beilegen, ebnet Kreuzlizenzierung den Weg für standardisierte Protokolle, gewährleistet Reproduzierbarkeit über Kontinente hinweg und skaliert den gesamten Mäusemodell-Markt.
Nach Anwendung: Infektionskrankheitsforschung beschleunigt nach der Pandemie
Die Onkologie behielt 41,44% der Einnahmen in 2024 bei und spiegelte die Abhängigkeit des Sektors von PDX- und humanisierten Modellen wider, um Checkpoint-Inhibitor-Wirksamkeit vorherzusagen. Dennoch verzeichnet die Infektionskrankheitsforschung die schnellste CAGR von 11,00%, angetrieben von Pandemie-Bereitschaftsfinanzierung und antimikrobiellen Resistenz-Programmen. Die Mäusemodell-Marktgröße für infektiöse Verwendungen wird voraussichtlich bis 2030 400 Millionen USD übertreffen, da Sponsoren Next-Generation-Antivirale und pathogen-spezifische Impfstoffe bewerten.
Immunologie-Studien verlassen sich auf verfeinerte Modelle, die Zytokin-Netzwerke replizieren, während Neurowissenschafts-Forscher longitudinale Bildgebung integrieren, um Degenerationspfade zu kartieren. Herz-Kreislauf- und Stoffwechsel-Bereiche profitieren von Telemetrie-Implantaten und diät-induzierten Krankheits-Settings, die klinische Heterogenität approximieren. Dieses sich erweiternde Anwendungsspektrum unterstreicht die Anpassungsfähigkeit und Bedeutung des Mäusemodell-Marktes für diverse therapeutische Portfolios.
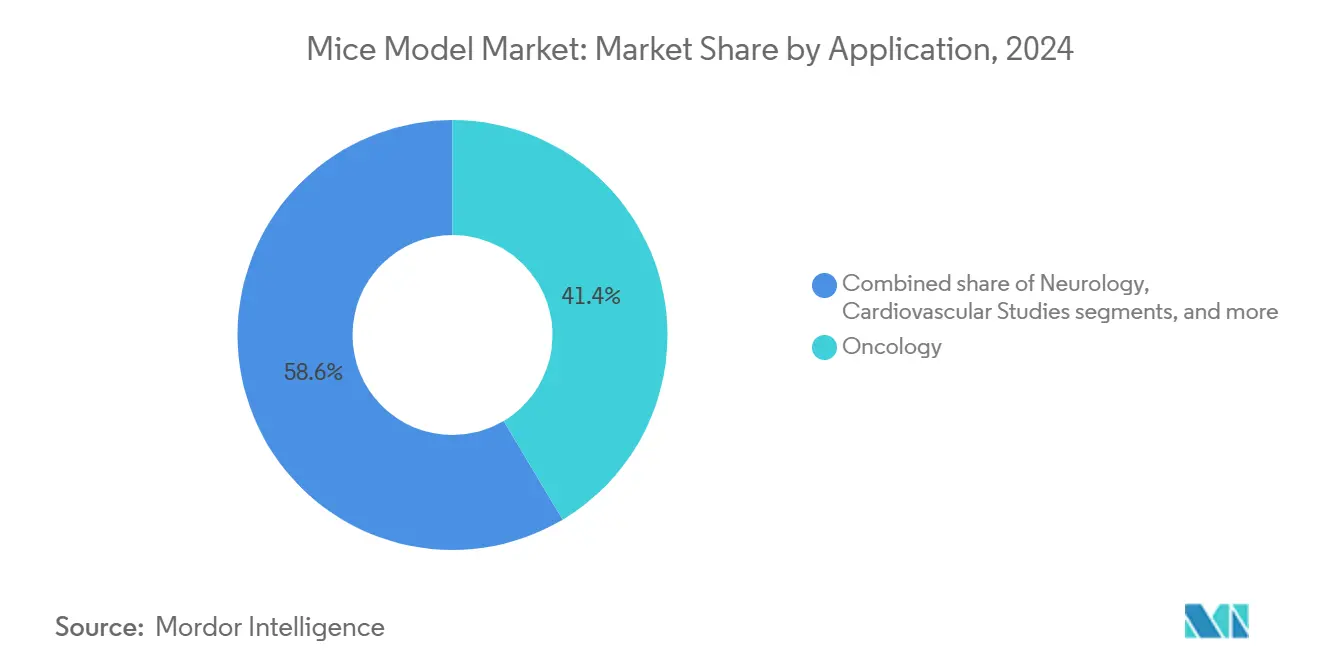
Notiz: Segmentanteile aller individuellen Segmente verfügbar beim Berichtskauf
Nach Endverbraucher: CROs gewinnen Boden durch spezialisierte Expertise
Pharma- und Biopharma-Unternehmen besaßen 48,53% des Mäusemodell-Marktes in 2024 und leiteten Modelle in Zielvalidierung und IND-ermöglichende Studien. CROs liefern jedoch das schnellste Wachstum mit 9,00% CAGR und reiten auf der Nachfrage nach schlüsselfertigen Wirksamkeits- und Sicherheitspaketen. Einige CROs betreiben jetzt Kolonie-Kapazitäten, die mittelgroße Pharma-Unternehmen übertreffen und Größenvorteile bieten, die mehrjährige Framework-Deals verankern. Akademische Institute bleiben wichtige Innovatoren und beherbergen transgene Kern-Einrichtungen, die neuartige Konstrukte pilotieren, bevor kommerzielle Skalierung auftritt.
Regierungsprogramme wie der NIH-PAR-25-327-Grant leiten Ressourcen in ultra-seltene Krankheitslinie-Entwicklung und übertragen oft validierte Stämme an öffentliche Repositories für breiteren Zugang. Gemeinnützige Organisationen wie die Michael J. Fox Foundation unterversichern Parkinson-Krankheitslinien und gewährleisten schnelle Verbreitung an Forscher. Kollektiv verstärken diese Benutzersegmente ein kollaboratives Ökosystem, das den Mäusemodell-Markt vorantreibt.
Geografie-Analyse
Nordamerika hielt 41,92% des Mäusemodell-Marktes in 2024, gestützt von National Institutes of Health-Stipendien, die gen-basierte Therapien und translationale Modelle priorisieren. Der NIH-PAR-25-327-Mechanismus finanziert speziell ultra-seltene neurologische Störungsforschung mit sophistizierten Murin-Systemen. Regionale Lieferanten setzen CRISPR-Hochdurchsatz-Kerne und pathogen-freie Einrichtungen ein und zementieren First-to-Market-Vorteile. Regulatorische Verschiebungen wie der FDA-Plan zum Ausstieg aus bestimmten Tiertests belasten Legacy-Modelle, spornen aber gleichzeitig Nachfrage nach fortgeschrittenen Linien mit erhöhter Vorhersagekraft an.
Asien-Pazifik verzeichnet die höchste CAGR von 8,26% dank aggressiver nationaler Investitionen. Chinas National Resource Center for Mutant Mice produzierte bis Mitte 2024 Knockouts für 10.881 Gene und schuf eine inländische Pipeline, die CRO-Expansion nährt. Japan verfeinert Qualitätsprotokolle für PDX-Adoption, und Südkorea leitet Smart-Farm-Finanzierung in keim-freie Barriere-Einrichtungen. Multinationale Sponsoren partnern mit lokalen Züchtern wie GemPharmatech, das einen San Diego-Knoten eröffnete, um US-APAC-Nachfrage zu überbrücken.
Europa hält eine CAGR von 5,81% aufrecht, unterstützt von kollaborativer Finanzierung und starker Ethik-Governance. Die European Medicines Agency's Regulatory Science to 2025-Agenda ermutigt innovative nicht-klinische Modelle, während sie das 3Rs-Prinzip aufrechterhält. Naher Osten & Afrika und Südamerika repräsentieren zusammen aufkommende Korridore mit CAGRs von 7,57% bzw. 7,04%. Golfnationen finanzieren translationale Zentren, die sich auf Stoffwechselstörungen konzentrieren, die in lokalen Bevölkerungen vorherrschen, während brasilianische Institute tropische Krankheitsmodelle vorantreiben, die sich mit regionaler Epidemiologie abstimmen. Globale Pharmas klinischer Fußabdruck in diesen Bereichen steigert Nachfrage nach standardisierten Murin-Assays und gewährleistet harmonisierte Daten über multizentrische Studien hinweg.
Wettbewerbslandschaft
Der Mäusemodell-Markt zeigt moderate Konzentration: Die fünf größten Lieferanten-Charles River Laboratories, Taconic Biosciences, The Jackson Laboratory, GenOway und Inotiv, Inc.-kontrollieren einen erheblichen Teil der Marktgröße. Diese Marktführer integrieren Zucht, Gentechnik, Gesundheitsüberwachung und globale Logistik. Charles River verstärkt Differenzierung durch interne CRISPR-Dienste und Immuno-Onkologie-Studien-Suiten. Taconic nutzt lizenzfreie Stämme und schnellen CRISPR-Editierung-Zugang, um schnell bewegende Biotech-Kunden anzusprechen, während The Jackson Laboratory mit Krankheitsstiftungen partnert, um neuartige Linien effizient zu verbreiten.
Strategische Allianzen intensivieren sich. Biocytogens RenLite-Antikörper-Plattform sicherte sich eine Lizenzvereinbarung mit Janssen und paarte proprietäre humanisierte Mäuse mit nachgeschalteter therapeutischer Entdeckung. Unterdessen nähren akademische Pipelines kommerzielle Kataloge; Yale überträgt Cas12a-gentechnisch veränderte Stämme unter nicht-exklusiven Bedingungen und erweitert Marktzugang.
Nischenspezialistos wachsen um PDX- und organ-spezifische humanisierte Modelle und erobern oft Geschäft von kleinen Biotech-Unternehmen, die maßgeschneiderte translationale Auslesungen suchen. Wettbewerbsspannung entsteht auch von alternativen Methoden-Entwicklern im Organ-on-Chip-Bereich; jedoch koppeln die meisten Sponsoren diese Plattformen noch immer mit muriner Validierung und erhalten Kernnachfrage. Preise bleiben für Standardlinien stabil, dennoch befehlen Premium-humanisierte Stämme Aufschläge von über 150% aufgrund komplexer Lizenzierung und Zuchtkosten.
Mäusemodell-Branchenführer
Charles River Laboratories International Inc.
GenOway
Inotiv, Inc.
Taconic Biosciences, Inc.
The Jackson Laboratory
- *Haftungsausschluss: Hauptakteure in keiner bestimmten Reihenfolge sortiert
Jüngste Branchenentwicklungen
- April 2025: GemPharmatech erweiterte seine US-Operationen mit einer neuen San Diego-Einrichtung, die Laborvermietung, Zucht und In-Vivo-präklinische Studien anbietet und Kunden Zugang zu einer umfangreichen Bibliothek gentechnisch veränderter Linien gibt.
- März 2025: Yale University-Forscher entwickelten neue CRISPR-Cas12a-Mauslinien, die gleichzeitige Bewertung mehrerer genetischer Veränderungen in Bezug auf verschiedene Krankheiten ermöglichen und Forschungskapazitäten in immunologischen Reaktionen und genetischen Störungen erheblich verbessern.
- März 2025: Ein Nature Communications-Paper stellte CRISPR-VLP-induzierte gezielte Mutagenese vor, eine virusähnliche Partikel-Methode, die Generierung gentechnisch veränderter Mausmodelle vereinfacht.
- Februar 2025: Die Chan Zuckerberg Initiative veröffentlichte den Rare As One Network Cycle 1 Impact Report und hob patienten-geleitete Bemühungen zum Aufbau von Tiermodell-Infrastruktur für seltene Krankheitsforschung hervor.
Globaler Mäusemodell-Marktberichtsumfang
Mäusemodelle sind biologische Darstellungen menschlicher Krankheiten oder Syndrome. Mäuse und Menschen haben ungefähr 99% Ähnlichkeit in ihrer DNA. Durch das Studium von Mäusen, die Symptome von Krankheiten wie Alzheimer, Diabetes oder Krebs haben, können wir viel mehr über die Behandlung dieser Krankheiten bei Patienten lernen.
Der Mäusemodell-Markt ist segmentiert nach Typ (Inzuchtmäuse, Auszuchtmäuse, gentechnisch veränderte Mäuse, Hybrid-Mäuse, chirurgisch modifizierte Mäuse und spontane Mutant-Mäuse), Service (Zucht, Kryokonservierung, Modell-In-Lizenzierung, genetische Tests und andere Services), Technologie (CRISPR/CAS9, embryonale Stammzell-Injektion, Kerntransfer und andere Technologien), Anwendung (Onkologie, Herz-Kreislauf-Studien, Neurologie und andere Anwendungen) und Geografie (Nordamerika, Europa, Asien-Pazifik, Naher Osten und Afrika und Südamerika). Der Marktbericht deckt auch die geschätzten Marktgrößen und Trends für 17 verschiedene Länder in wichtigen Regionen weltweit ab.
Der Bericht bietet den Wert (in USD) für die oben genannten Segmente.
| Inzuchtmäuse |
| Auszuchtmäuse |
| Gentechnisch veränderte Mäuse |
| Hybrid-/Kongene Mäuse |
| Zucht |
| Kryokonservierung |
| Rederivation & Quarantäne |
| Genetische Tests |
| Andere Services |
| CRISPR/Cas9 |
| Embryonale Stammzell-Injektion |
| Kerntransfer |
| Mikroinjektion |
| Andere Technologien |
| Onkologie |
| Immunologie & Entzündung |
| Neurologie |
| Herz-Kreislauf-Studien |
| Stoffwechselkrankheiten |
| Infektionskrankheiten |
| Andere Anwendungen |
| Pharma- & Biopharma-Unternehmen |
| Auftragsforschungsorganisationen (CROs) |
| Akademische & Forschungsinstitute |
| Andere Endverbraucher |
| Nordamerika | Vereinigte Staaten |
| Kanada | |
| Mexiko | |
| Europa | Deutschland |
| Vereinigtes Königreich | |
| Frankreich | |
| Italien | |
| Spanien | |
| Restliches Europa | |
| Asien-Pazifik | China |
| Indien | |
| Japan | |
| Australien | |
| Südkorea | |
| Restliches Asien-Pazifik | |
| Naher Osten & Afrika | GCC |
| Südafrika | |
| Restlicher Naher Osten & Afrika | |
| Südamerika | Brasilien |
| Argentinien | |
| Restliches Südamerika |
| Nach Maustyp | Inzuchtmäuse | |
| Auszuchtmäuse | ||
| Gentechnisch veränderte Mäuse | ||
| Hybrid-/Kongene Mäuse | ||
| Nach Service | Zucht | |
| Kryokonservierung | ||
| Rederivation & Quarantäne | ||
| Genetische Tests | ||
| Andere Services | ||
| Nach Technologie | CRISPR/Cas9 | |
| Embryonale Stammzell-Injektion | ||
| Kerntransfer | ||
| Mikroinjektion | ||
| Andere Technologien | ||
| Nach Anwendung | Onkologie | |
| Immunologie & Entzündung | ||
| Neurologie | ||
| Herz-Kreislauf-Studien | ||
| Stoffwechselkrankheiten | ||
| Infektionskrankheiten | ||
| Andere Anwendungen | ||
| Nach Endverbraucher | Pharma- & Biopharma-Unternehmen | |
| Auftragsforschungsorganisationen (CROs) | ||
| Akademische & Forschungsinstitute | ||
| Andere Endverbraucher | ||
| Nach Geografie | Nordamerika | Vereinigte Staaten |
| Kanada | ||
| Mexiko | ||
| Europa | Deutschland | |
| Vereinigtes Königreich | ||
| Frankreich | ||
| Italien | ||
| Spanien | ||
| Restliches Europa | ||
| Asien-Pazifik | China | |
| Indien | ||
| Japan | ||
| Australien | ||
| Südkorea | ||
| Restliches Asien-Pazifik | ||
| Naher Osten & Afrika | GCC | |
| Südafrika | ||
| Restlicher Naher Osten & Afrika | ||
| Südamerika | Brasilien | |
| Argentinien | ||
| Restliches Südamerika | ||
Wichtige im Bericht beantwortete Fragen
Warum wird CRISPR/Cas9 als Gamechanger für Mausmodell-Entwicklung betrachtet?
Es ermöglicht schnelle, hochpräzise Gen-Editierungen, lässt Forscher komplexe Multigen-Modelle in Monaten statt Jahren erstellen, was Zielvalidierungs-Zyklen in der Arzneimittelentdeckung beschleunigt.
Was macht humanisierte Mäuse für Immuno-Onkologie-Studien zunehmend wichtig?
Diese Modelle integrieren menschliche Immunkomponenten und ermöglichen es, Checkpoint-Inhibitor- und CAR-T-Therapien in einem lebenden System zu testen, das Patientenimmunreaktionen genauer als traditionelle Xenotransplantate nachahmt.
Wie gestalten Auftragsforschungsorganisationen (CROs) die Mäusemodell-Landschaft um?
CROs bündeln jetzt Zucht, genetische Tests und Phänotypisierung in schlüsselfertige Pakete und geben Pharma-Unternehmen schnellere Projektstarts und eliminieren den Bedarf für kostspielige interne Vivarium-Erweiterung.
Auf welche Weise verbessern patientenabgeleitete Xenotransplantat (PDX)-Bibliotheken Onkologie-Arzneimittel-Screening?
PDX-Modelle bewahren die genetische Heterogenität ursprünglicher Tumoren und helfen Forschern, biomarker-getriebene Untergruppen zu identifizieren und späte klinische Ausfälle zu reduzieren, die mit schlechter translationaler Relevanz verbunden sind.
Welche Rolle spielen Seltene-Krankheiten-Konsortien bei der Förderung neuer Mausmodelle?
Staatlich finanzierte Initiativen bündeln Ressourcen, um Knockout-Stämme für wenig erforschte Störungen zu erstellen und zu teilen, füllen Lücken, denen kommerzielle Anreize fehlen und ermöglichen präklinische Tests für ultra-seltene Zustände.
Warum werden Organ-on-Chip- und In-Silico-Tools sowohl als Bedrohung als auch als Chance für den Mäusemodell-Markt betrachtet?
Sie versprechen ethische, hochdurchsätzige Alternativen für bestimmte Assays und ermutigen zur Verfeinerung von Tierstudien; dennoch ergänzen sie derzeit eher als vollständig Ganzorganismus-Modelle zu ersetzen, die für systemische Sicherheits- und Wirksamkeitsbewertung benötigt werden.
Seite zuletzt aktualisiert am:



