Gen Therapie Marktgröße und -anteil
Gen Therapie Marktanalyse von Mordor Intelligenz
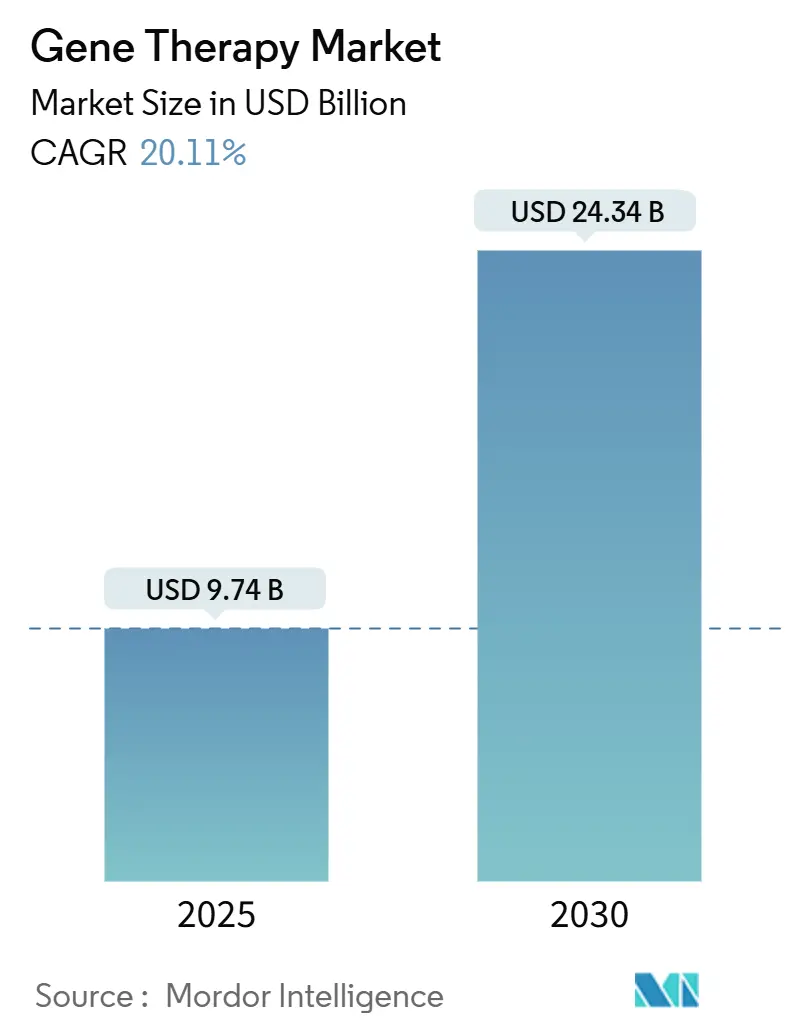
Die Gen Therapie Marktgröße wird auf USD 9,74 Milliarden im Jahr 2025 geschätzt und soll USD 24,34 Milliarden bis 2030 erreichen, bei einer CAGR von 20,11% während des Prognosezeitraums (2025-2030).
Regulierungsbehörden genehmigten allein im Jahr 2024 neun Zell- und Gentherapien, was ein steigendes Vertrauen In die klinische und kommerzielle Durchführbarkeit signalisiert und breitere Erstattungswege In Schlüsselmärkten freischaltet. Verstärkte Biopharma- und Privat-Eigenkapital-Finanzierung beschleunigt Assets In der späten Phase, während der Ausbau der Herstellungskapazitäten sowohl viral als auch nicht-viral historische Lieferketten-Reibungen reduziert. Schnelle Fortschritte bei In-Vivo-Editierung und Vektor-Maschinenbau erweitern den therapeutischen Anwendungsbereich über seltene Krankheiten hinaus auf häufige Erkrankungen, insbesondere In Neurologie und Ophthalmologie. Asien-Pazifiks zweistelliges Studienwachstum und Nordamerikas politische Anreize sichern gemeinsam eine diversifizierte Nachfragebasis, auch wenn hohe Produktpreise und Sicherheitsüberwachungsanforderungen Zugangsbarrieren darstellen.
Wichtige Erkenntnisse des Berichts
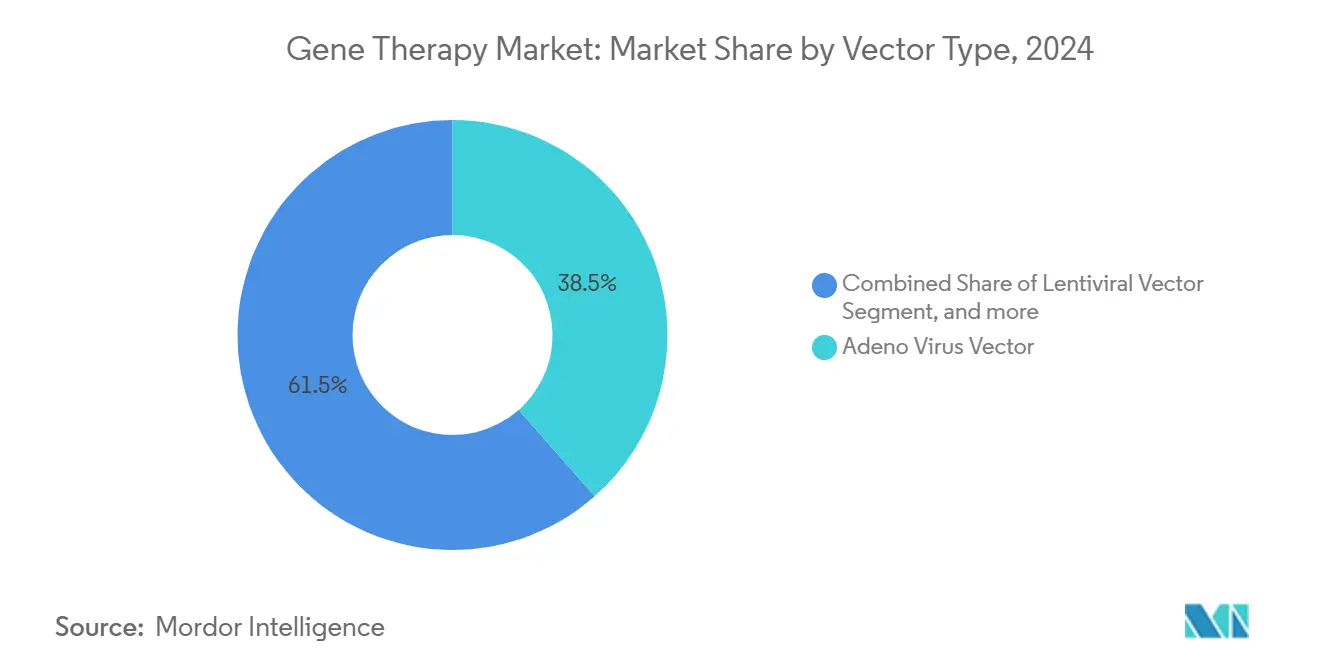
- Nach Vektortyp eroberte Adeno-assoziierte Viren 38,54% des Gen Therapie Marktanteils In 2024, während nicht-virale Verabreichungsmethoden bereit sind, mit einer CAGR von 24,34% bis 2030 zu expandieren.
- Nach Indikation kommandierte Onkologie 42,92% Umsatz In 2024; neurologische Anwendungen entwickeln sich mit einer CAGR von 25,62% bis 2030.
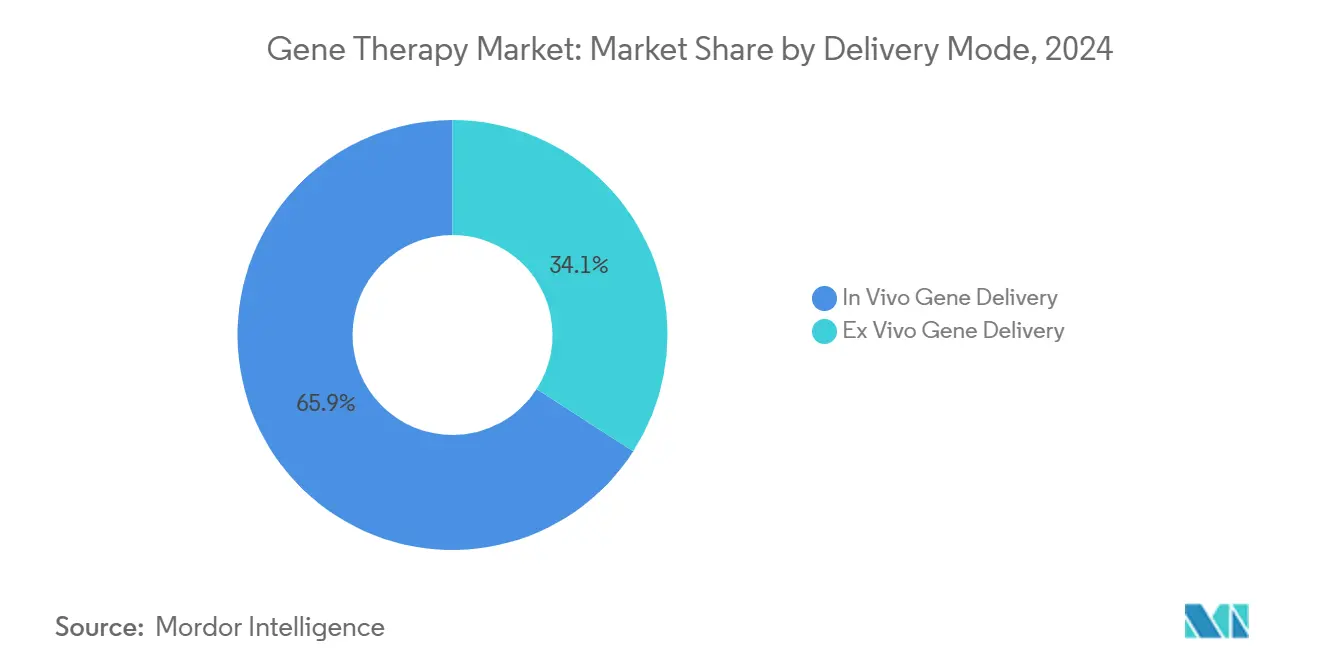
- Nach Verabreichungsart hielten In-Vivo-Ansätze 65,92% der Gen Therapie Marktgröße In 2024, wohingegen Ex-Vivo-Methoden mit einer CAGR von 23,07% zwischen 2025-2030 voranschreiten werden.
- Nach Endnutzer entfielen auf KrankenhäBenutzer und Kliniken 59,22% Anteil der Gen Therapie Marktgröße In 2024; spezialisierte Behandlungszentren verfolgen eine CAGR von 21,89% bis 2030.
- Nach Geografie führte Nordamerika mit 41,78% Umsatzanteil In 2024; Asien-Pazifik wird voraussichtlich mit einer CAGR von 27,68% über denselben Zeitraum beschleunigen.
Globale Gen Therapie Markttrends und Einblicke
Treiber-Impact-Analyse
| Treiber | (~) % Auswirkung auf CAGR-Prognose | Geografische Relevanz | Auswirkung Zeitrahmen |
|---|---|---|---|
| Regulatorische Zulassungen, die Durchführbarkeit demonstrieren | +5.2% | Global, konzentriert In Nordamerika und Europa | Kurzfristig (≤ 2 Jahre) |
| Fortschritte bei Vektor-Maschinenbau & In-Vivo-Technologie | +4.9% | Frühe Adaption In Nordamerika und Europa | Langfristig (≥ 4 Jahre) |
| Ausbau der Herstellungsinfrastruktur | +4.8% | Nord amerika, Europa, aufstrebendes Asien-Pazifik | Mittelfristig (2-4 Jahre) |
| Schnelle Hochskalierung kommerzieller AAV-CDMO-Kapazitäten | +3.8% | Global, Nord amerika und Europa, Expansion nach Asien-Pazifik | Mittelfristig (2-4 Jahre) |
| Biopharma- und Privat-Eigenkapital-Finanzierung | +3.5% | Innovations hubs In den USA, Europa und China | Mittelfristig (2-4 Jahre) |
| Wachsende Einbeziehung von Gentherapien für seltene Krankheiten | +2.7% | Global, mit höherer Auswirkung In entwickelten Märkten | Langfristig (≥ 4 Jahre) |
| Quelle: Mordor Intelligence | |||
Steigende regulatorische Zulassungen demonstrieren klinische und kommerzielle Durchführbarkeit
Häufige Freigaben von Großen Regulierungsbehörden reduzieren Entwicklungsrisiken und verkürzen Markteinführungszeiten. Die kumulierte Gesamtzahl von 37 genehmigten Zell- und Genprodukten der FDA bis 2024 zeigt, dass Behördenprüfer nun spezielle Rahmenwerke wie die Regenerativ Medizin Fortgeschritten Therapie-Bezeichnung anwenden, die die Entwicklungszeit für qualifizierte Programme um etwa 40% verkürzt.[1]u.S. Lebensmittel Und Medikament Administration, "Approved Zellulär Und Gen Therapie Produkte," fda.govEuropas PRIME-System und die 2025er Regel des Vereinigten Königreichs für Punkt-von-Pflege-Herstellung erleichtern den Markteintritt weiter. Die Zulassung von ZEVASKYN für rezessive dystrophische Epidermolysis bullosa In 2025 veranschaulicht, wie sich Indikationen über ultra-seltene Krankheiten hinaus auf breitere dermatologische Segmente ausdehnen. Eine solche Erweiterung der therapeutischen Reichweite unterstützt mehrjähriges Wachstum im Gen Therapie Markt und stimuliert Folgeinvestitionen von Kostenträgern, die dauerhaften klinischen Nutzen erwarten.
Kontinuierliche technologische Fortschritte bei Vektor-Engineering und In-Vivo-Editierungsplattformen
Erweiterte Kapsid-Bibliotheken, maschinenlerngesteuerte Sequenzoptimierung und neuartige Lipid-Konstrukte schärfen Gewebetropismus und reduzieren Immunogenität. Forscher an der Perelman School von Medizin berichteten über DNA-beladene Lipid-Nanopartikel, die monatelang In vivo persistieren und dauerhafte Dosierung für chronische Krankheiten ermöglichen.[2]Penn Medizin News, "DNA-Loaded Lipid Nanopartikel Remain Aktiv für Months," pennmedicine.orgOrganoid-Plattformen bieten menschliche gewebespezifische Testbetten, die translationale Vorhersagbarkeit verbessern, unterstützt durch die Akzeptanz nicht-tierischer Modelle des FDA Modernization Act. KI-unterstützte Algorithmen wie OpenCRISPR-1 verkürzen Designzyklen und erhöhen Editierpräzision. Gemeinsam verschieben diese Innovationen die therapeutische Obergrenze höher, schaffen Raum für Wiederholungsdosierung und befeuern einen positiven Kreislauf aus klinischem Erfolg und Kapitalanlage, der den Gen Therapie Markt vergrößert.
Ausbau der globalen Viralvektor- und nicht-viralen Herstellungsinfrastruktur
Großangelegte Kapitalanlagen steigern sowohl Kapazität als auch Raffinesse der Produktionslinien. Novo Nordisks USD 16,5 Milliarden Kauf von Catalent In 2024 unterstreicht, wie Groß Pharma die End-Zu-End-Kontrolle über Lieferketten sichert. Viralvektor-Upgrades umfassen jetzt kontinuierliche Durchflussbioraktoren und geschlossene stromabwärts-Verarbeitung, wodurch Batch-Vorlaufzeiten um zweistellige Prozentsätze gesenkt werden. Nicht-virale Lipid-Nanopartikel-Plattformen senken die Herstellungskosten um bis zu 60% und können größere Payloads verpacken, wodurch frühere technische Barrieren für polygene Indikationen beseitigt werden.[3]Journal von Nanobiotechnology editors, "Advances In Lipid Nanoparticle Lieferung," springeropen.com Automatisierung, KI-gestützte Qualitätsanalytik und modulare Reinraum-Designs verbessern gemeinsam die Zuverlässigkeit und ermutigen Auftragshersteller, vorgefertigte Suiten zu bauen, die schnell für neue Sponsoren angepasst werden können.
Eskalierende Biopharma- & Private-Equity-Finanzierung in Gene Therapy F&E
Kapitalzuflüsse bleiben trotz breiterer Marktvolatilität robust. Vorabwerte bei Phase-II- und III-Auslizenzierungsdeals stiegen 2024 um 35%, da der Wettbewerb um späte Assets intensivierte. Sangamo Therapeutika sicherte sich USD 18 Millionen im Voraus und Meilenstein-Potenzial von USD 1,4 Milliarden für seine ZNS-gezielten Kapside mit Eli Lilly, was den Investorenappetit für differenzierte Liefervektoren illustriert. Privat-Eigenkapital-Gruppen bewegen sich auch stromabwärts; Carlyles und SK Capitals Akquisition von bluebird Bio In 2025 injiziert Kommerzialisierungsmittel In genehmigte Therapien für Sichelzellkrankheit und β-Thalassämie und demonstriert den strategischen Wert vermarkteter Assets. Solche anhaltende Finanzierung beschleunigt Pipeline-Diversifikation und erhält die Nachfrage nach Herstellungsdienstleistungen aufrecht, was die langfristige Expansion des Gen Therapie Marktes verstärkt.
Beschränkungen-Impact-Analyse
| Beschränkung | (~) % Auswirkung auf CAGR-Prognose | Geografische Relevanz | Auswirkung Zeitrahmen |
|---|---|---|---|
| Hohe Therapiepreise | -3,8% | Größere Auswirkung In Schwellenmärkten und restriktiven Erstattungsregionen | Mittelfristig (2-4 Jahre) |
| Herstellungs komplexität & Vektor-Versorgungslimits | -2,6% | Variiert je regionaler Produktionskapazität | Kurzfristig (≤ 2 Jahre) |
| Sicherheits bedenken, die langfristige Überwachung erfordern | -2,1% | Am intensivsten wo regulatorische Aufsicht streng ist | Langfristig (≥ 4 Jahre) |
| Mangel an Plasmid-/Kapsid-Rohmaterialien | -1,9% | Akut In Regionen mit begrenzter Lieferketten-Resilienz | Kurzfristig (≤ 2 Jahre) |
| Quelle: Mordor Intelligence | |||
Hohe Therapiepreise schaffen Zugangs- und Erschwinglichkeitsbarrieren
Einzeldosis-Heilungen kosten zwischen USD 373.000 und USD 4,25 Millionen und belasten Kostenträger-Budgets und testen die gesellschaftliche Bereitschaft, kurative Therapien zu finanzieren. Anbieter nennen soziale Unterstützungslücken, Reiseentfernungen und Vorautorisierungshürden als die wichtigsten Zugangsblockaden. Innovative Erstattungsoptionen - ergebnisbasierte Verträge, Amortisierungsmodelle und Garantien - entstehen, erfordern aber noch komplexe Datenteilung und langfristige Nachverfolgungsinfrastruktur. Die Zentren für Medicare & Medicaid Dienstleistungen starteten 2025 ein Zelle Und Gen Therapie Zugang Modell, das staatliche gepoolte Beschaffung fördert, um Budgetauswirkungen zu mildern. Diese finanziellen Gegenwinds werden voraussichtlich die Adoption In kostensensitiven Regionen moderieren und die Gen Therapie Marktwachstumskurve trotz starker klinischer Wertversprechen Dämpfen.
Herstellungskomplexität und begrenzte Versorgung mit GMP-Grade-Vektoren
Selbst mit aggressivem Kapazitätsausbau erfüllt die Versorgung mit GMP-Grad-AAV- und lentiviralen Vektoren nur ein Viertel der projizierten 2025er Nachfrage. Produktionszyklen können neun Monate überschreiten, wodurch Markteinführungszeiten verlangsamt und Bestandsrisiken geschaffen werden. Aufkommende dezentralisierte Lösungen wie modulare Reinraum-Pods senken die Kosten pro Dosis von etwa USD 400.000 auf unter USD 35.000 In Piloteinstellungen, obwohl regulatorische Harmonisierung eine Herausforderung bleibt. Bis solche Modelle skalieren, wird begrenzte Vektorverfügbarkeit weiterhin als strukturelle Bremse für den Gen Therapie Markt wirken.
Segmentanalyse
Nach Vektortyp: AAV dominiert, während nicht-virale Methoden aufholen
AAV-Vektoren hielten 38,54% des Gen Therapie Marktanteils In 2024 aufgrund Günstiger Sicherheit und anhaltender Transgen-Ausdruck, die mehrere genehmigte Produkte für Hämophilie und vererbte Netzhauterkrankungen untermauern. Diese Führung wird durch breiten Gewebetropismus und einen erweiterten Pool von konstruierten Serotypen verstärkt, die Spezifität verbessern. Jedoch sind nicht-virale Lipid-Nanopartikel-Systeme die am schnellsten steigende Alternativ, prognostiziert mit einer CAGR von 24,34% bis 2030, da sie größere genetische Payloads tragen und Herstellungsökonomie vereinfachen. Die Gen Therapie Marktgröße für nicht-virale Plattformen ist daher darauf ausgelegt, einen Teil der aktuellen Umsatzlücke zu schließen. Lentivirale Vektoren bleiben die Hauptstütze für Ex-Vivo-Auto-T-Herstellung, während Herpes-basierte Systeme In der Onkologie für ihre Nutzlast-Kapazität an Zugkraft gewinnen. Kontinuierliche Optimierung von Kapsid-Bibliotheken und synthetischen Promotern wird bestimmen, ob virale Vektoren Anteile gegen kosteneffiziente nicht-virale Herausforderer verteidigen können.
Der Anstieg nicht-viraler Ansätze lindert auch Rohmaterialbeschränkungen, da Lipid-Komponenten für standardmäßige pharmazeutische Lieferketten geeignet sind. DNA-beladene Nanopartikel, die monatelang aktiv bleiben, senken Wiederholungsdosierungsanforderungen und können für organselektive Aufnahme abgestimmt werden. Solche Flexibilität zieht Entwickler an, die polygene neurologische Störungen anvisieren, wo Nutzlast-Größe AAVs Verpackungsgrenze überschreitet. Folglich verschiebt sich die Wettbewerbsdynamik im Gen Therapie Markt von Vektorverfügbarkeit hin zu Lieferpräzision und schafft Raum für plattform-agnostische CDMOs, aufkommende Nachfrage zu erfassen.
Notiz: Segmentanteile aller individuellen Segmente verfügbar beim Berichtkauf
Nach Indikation: Onkologie führt, während Neurologie beschleunigt
Onkologie-Anwendungen generierten 42,92% des Umsatzes In 2024, unterstützt durch einen stetigen Fluss von Auto-T-Zulassungen und eine tiefe Pipeline für solide Tumore. Robuste Evidenz für komplette Remissionen bei refraktären hämatologischen Malignomen erhält Kostenträger-Akzeptanz trotz Preisdrucks aufrecht. Dennoch beansprucht Neurologie die höchste Wachstumstrajektorie mit einer CAGR von 25,62% bis 2030. Aufkommende Kapside, die die Blut-Hirn-Schranke überqueren, und präzise In-Vivo-Editierungswerkzeuge ermöglichen direkte Intervention bei Störungen wie Rett-Syndrom und Huntington-Krankheit. Die Gen Therapie Marktgröße, die ZNS-Störungen zugeordnet ist, wird sich voraussichtlich vervielfachen, da bilaterale regulatorische Anreize Entwicklungsrisiken komprimieren.
Seltene metabolische und ophthalmologische Indikationen liefern weiterhin neue Zulassungen, da Gewebeimmunprivileg und klare Biomarker klinische Endpunkte vereinfachen. Kardiovaskuläre Ziele wie hypertrophe Kardiomyopathie gewinnen Venture-Finanzierung und deuten auf breitere systemische Krankheitsaufnahme hin. Da therapeutische Breite zunimmt, wird Portfolio-Optimierung kritisch; Sponsoren müssen Onkologie-Cashflows mit hohem Potenzial aber wissenschaftlich komplexen Neurologie-Assets balancieren.
Nach Verabreichungsart: In Vivo dominiert, während Ex Vivo an Schwung gewinnt
Direkte Verabreichung kommandierte 65,92% des Umsatzes In 2024, primär aufgrund von Zulassungen für okuläre, muskuläre und hepatische Störungen, wo lokalisierte Injektion Vektoreffizienz maximiert. In-Vivo-Dosierung eliminiert Zellverarbeitungsschritte, verkürzt Behandlungszeiten und passt In bestehende Krankenhausworkflows, wodurch ihre Führung erhalten bleibt. Jedoch ist Ex-Vivo-Maschinenbau auf Kurs für eine CAGR von 23,07%, da Herstellungsautomatisierung, verbesserte virale Transduktion und allogene Plattformen Kosten pro geduldig senken. Die wachsende Pipeline konstruierter Immunzellen für Autoimmunerkrankungen zeigt Ex-Vivo-Vielseitigkeit jenseits der Onkologie. Als solches profitiert der Gen Therapie Markt von komplementärem Wachstum über beide Lieferkanäle, wodurch Überabhängigkeit von einer einzelnen Modalität reduziert und Lieferketten-Anforderungen geglättet werden.
Optimierte Ex-Vivo-Protokolle erreichen jetzt höhere Zellviabilität und Gen-überweisen-Effizienz, Faktoren, die zuvor klinische Ergebnisse behinderten. Skala-out-Strategien und Punkt-von-Pflege-Produktion reduzieren weiter logistische Komplexität und legen Grundlagen für gemeindebasierte Infusionszentren. Über Zeit kann Kostenkonvergenz zwischen Modalitäten Sponsoren ermutigen, Lieferung allein basierend auf biologischer Eignung statt Herstellungspraktikabilität auszuwählen.
Notiz: Segmentanteile aller individuellen Segmente verfügbar beim Berichtkauf
Nach Endnutzer: Krankenhäuser führen, während Spezialkliniken schnell expandieren
KrankenhäBenutzer und akademische Medizinzentren repräsentierten 59,22% des Verabreichungsvolumens In 2024, da sie multidisziplinäre Teams und kontrollierte Umgebungen besitzen, die für Gen Therapie Infusion notwendig sind. Diese Institutionen dienen oft als Studienstätten und schaffen nahtlose Übergänge von Studie zu Standardversorgung. Dennoch werden spezialisierte Infusionseinrichtungen voraussichtlich mit 21,89% CAGR bis 2030 wachsen. Ihre schlanken Betriebsmodelle reduzieren Versorgungskosten und verbessern Patientenkomfort, besonders wo Reiseentfernung zu tertiären Zentren eine Barriere darstellt. Die Gen Therapie Marktgröße, die von spezialisierten Zentren erfasst wird, steht daher vor einem Anstieg, da Kostenträger kostengünstigere Settings incentivieren.
Akademische Forschungsinstitute behalten Einfluss, indem sie First-In-Menschlich-Studien hosten und Herstellungsprotokolle verfeinern. GemeindekrankenhäBenutzer integrieren allmählich validierte Behandlungsworkflows, unterstützt durch Fernbedienung-Überwachungsplattformen, die wiederholte Krankenhausbesuche minimieren. Die Expansion dezentralisierter Versorgung erweitert regionalen Zugang und unterstützt höheren Verfahrensdurchsatz, wodurch eine kritische Kapazitätsbeschränkung adressiert wird, da mehr Produkte Zulassungen gewinnen.
Geografieanalyse
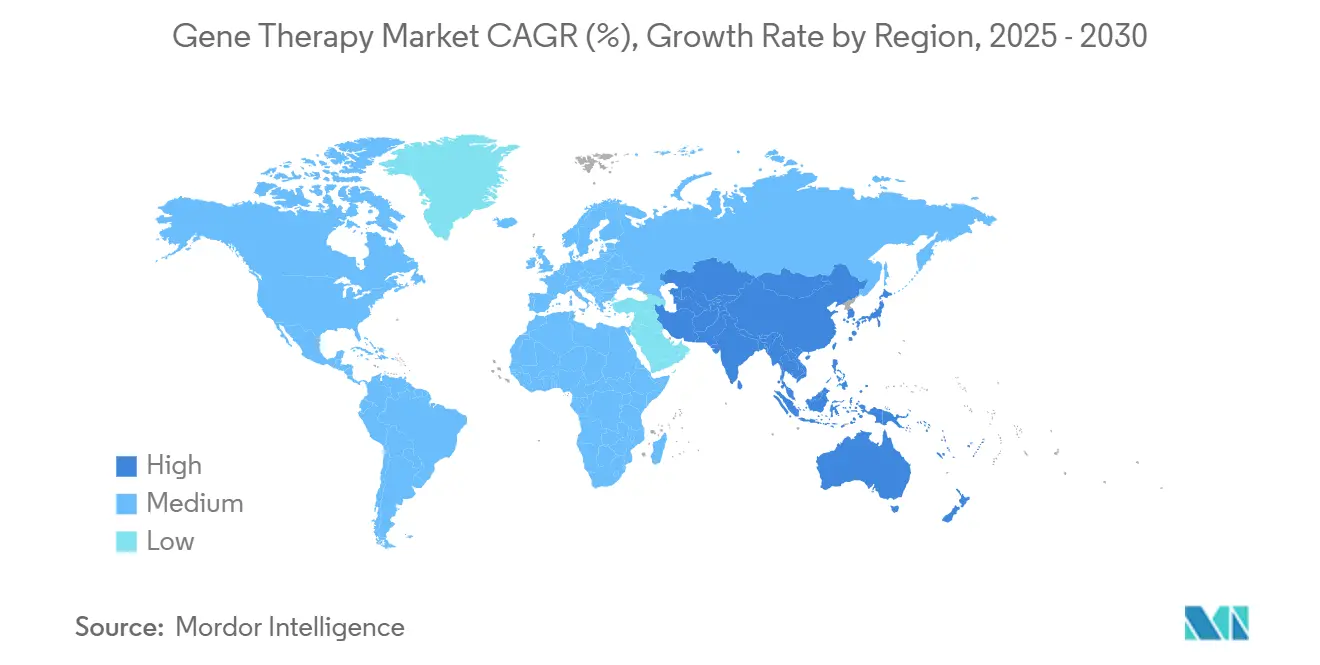
Nordamerika hielt 41,78% des globalen Umsatzes In 2024, getragen von einer entgegenkommenden regulatorischen Umgebung, tiefen Venture-Hauptstadt-Pools und umfangreicher klinischer Infrastruktur. Die Vereinigten Staaten genehmigten 2024 allein 34 First-In-Class-Gentherapien und unterstreichen ihre zentrale Rolle In der Produkteinführungssequenzierung. Bundesinitiativen wie ARPA-H-Grants leiten erhebliche Mittel zu Herstellungsinnovation und Sicherheitsüberwachung und verstärken die Führung der Region im Gen Therapie Markt.
Europa hält starke wissenschaftliche Leistung aufrecht und profitiert von EMAs adaptiven Pfaden, die Durchbruchbehandlungen beschleunigen. Das kommende Vereinigtes Königreich-Framework für dezentralisierte Herstellung, wirksam ab Juli 2025, kann logistische Belastungen reduzieren und Punkt-von-Pflege-Produktion stimulieren. Jedoch verlängern ungleiche nationale Erstattungsrichtlinien die Zeit-bis-geduldig über den Block hinweg; die neue EU Gesundheit Technologie Bewertung-Regulierung 2025 zielt darauf ab, Evidenzanforderungen zu harmonisieren, könnte aber auch Verhandlungen verlängern. Ergebnisbasierte Zahlungsmodelle, wie durch Hemgenix-Vereinbarungen In England und Dänemark demonstriert, mildern allmählich Adoptionshürden.
Asien-Pazifik verzeichnet das schnellste Wachstum mit einer CAGR von 27,68%. China hostet mehr als 400 zellbasierte Studien und investiert stark In inländische Vektoranlagen, wodurch es sich als sowohl Nachfrage- als auch Versorgungsmotor positioniert. Japans beschleunigte Pfade für Regenerativ Medizin und Singapurs digitales Lizenzportal straffen Zulassungen weiter. Während regulatorische Standards mit westlichen Behörden konvergieren, bleiben Variabel Erstattung und Exportkontrollen für genetische Materialien Herausforderungen. Kontinuierliche politische Unterstützung und reifende lokale CDMOs versichern dennoch, dass Asien-Pazifik einen steigenden Anteil des Gen Therapie Marktes erfassen wird.
Wettbewerbslandschaft
Top-Unternehmen im Gene Therapy Markt
Das Wettbewerbsfeld ist mäßig fragmentiert, bevölkert von erfahrenen Pharma-Etablierten und agilen Biotechnologie-Innovatoren. Groß-Pharma-HäBenutzer wie Novartis, Pfizer und Roche akquirieren Plattformtechnologien, um Patentklippen auszugleichen; Novo Nordisks Zusammenschluss mit 2seventy Bio veranschaulicht Portfolio-Diversifikation In Geneditierung. Partnerschaftsaktivität erreichte 90 Deals In Q1 2025, was intensives Scouting für Kapsid-Maschinenbau, nicht-virale Lieferung und skalierbare Herstellung widerspiegelt.
Technologiedifferenzierung treibt Wettbewerbsvorteil an. Krystal Biotechnologie nutzt einen proprietären HSV-1-Vektor, der wiederholte topische Verabreichung ermöglicht; ihr Produkt VYJUVEK generierte USD 341,2 Millionen seit der Markteinführung und erreichte 97% uns-Abdeckung, was kommerziellen Beweis seltener dermatologischer Anwendungen demonstriert. KI-Integration ist ein weiteres Schlachtfeld: MeiraGTx'S Gelenk Venture mit Hologen Neuro KI wendet Tief-Lernen-Design-Loops auf ZNS-Kapside an, während Amgen einen 19%igen Umsatzanstieg 2024 berichtete, unterstützt durch konstruierte RNA-Payloads, die maschinenlerngesteuerte Optimierung kapitalisieren.
Weiß-Raum-Möglichkeiten umfassen Vektorkapazitätserweiterung, gezielte nicht-onkologische Indikationen und neuartige Finanzierungsrahmen, die einmalige Therapievorteile mit mehrjährigen Kosteneinsparungen matchen. Vertrag Entwicklung Und Herstellung Organizations, die schlüsselfertige, plattform-agnostische Dienstleistungen anbieten, sind bereit, Anteile zu gewinnen, da kleinere Sponsoren Produktion outsourcen. Da sich die Pipeline diversifiziert und regionale Zulassungspfade proliferieren, belohnt der Gen Therapie Markt Spieler, die wissenschaftliche Tiefe mit Lieferketten-Agilität kombinieren.
Gen Therapie Industrieführer
-
Gilead Wissenschaften, Inc.
-
Amgen Inc.
-
Novartis AG
-
bluebird Bio Inc.
-
Biogen Inc.
- *Haftungsausschluss: Hauptakteure in keiner bestimmten Reihenfolge sortiert


Aktuelle Industrieentwicklungen
- Mai 2025: Sarepta Therapeutika, Inc., ein Vorreiter In der Präzisionsgenetikmedizin für seltene Krankheiten, hat eine entscheidende Zustimmung von Japans Ministerium für Gesundheit, Arbeit und Wohlfahrt (MHLW) für sein Medikament ELEVIDYS (delandistrogene moxeparvovec) erhalten. Diese Zulassung, gewährt unter Japans bedingtem und zeitlich begrenztem Pfad, zielt auf Duchenne-Muskeldystrophie (DMD) ab. Speziell ist ELEVIDYS für Kinder im Alter von 3 bis unter 8 Jahren genehmigt, vorausgesetzt sie weisen keine Deletionen In Exon 8 und/oder Exon 9 des DMD-Gens auf und testen negativ auf Anti-AAVrh74-Antikörper. Bemerkenswert ist dies die erste globale Billigung zur Behandlung von DMD bei Kindern unter 4 Jahren.
- Mai 2025: Abeona Therapeutika erhielt FDA-Zulassung für ZEVASKYN, die erste zellbasierte Gentherapie für rezessive dystrophische Epidermolysis bullosa (RDEB), die effektive Wundheilung In klinischen Studien demonstrierte.
- Februar 2025: Genprex, Inc., ein klinisches Gentherapie-Unternehmen, macht Fortschritte In seinem Diabetes-Gentherapie-Programm, gestärkt durch eine Zusammenarbeit mit der University von Pittsburgh. Die beiden Einheiten haben Genprex'S vorherige Lizenzvereinbarungen mit Pitt zu einer einzigen exklusiven Vereinbarung gestrafft. Dieser neue Pakt umfasst mehrere Technologien zur Erstellung eines Gentherapie-Produkts für sowohl Typ-1- als auch Typ-2-Diabetes. Weiterhin hat Genprex eine vollständig eigene Tochtergesellschaft, Convergen Biotechnologie, Inc., gegründet, die sich der Weiterentwicklung seiner Diabetes-Initiativen widmet.
- Oktober 2024: Gouverneur Hochul kündigte eine bedeutende Entwicklung für den Gen Therapie Markt mit der Einführung der nächsten Phase von Long Islands neu York Biogenesis Park an, einem landesweit führenden Zell- und Gentherapie-Innovationshub. Dieses USD 430 Millionen Projekt zielt darauf ab, Forschung, Entwicklung und Kommerzialisierung lebensrettender Therapien zu beschleunigen. Das USD 150 Millionen Engagement des Staates markiert die größte staatliche Investition In Zell- und Gentherapie landesweit und treibt neu Yorks Vision weiter voran, Führerschaft In diesem kritischen Feld zu etablieren.
- September 2024: Genprex, Inc., ein klinisches Gentherapie-Unternehmen, das sich transformativen Therapien für Krebs- und Diabetespatienten widmet, hat Pläne enthüllt, sein Diabetes-klinisches Entwicklungsprogramm und zugehörige Gentherapie-Assets In eine neu gegründete, vollständig eigene Tochtergesellschaft zu verschieben. Diese neue Einheit, "NewCo" genannt, wird sich auf die Weiterentwicklung und Kommerzialisierung von GPX-002 konzentrieren, einem Gentherapie-Kandidaten für sowohl Typ-1- (T1D) als auch Typ-2-Diabetes (T2D).
Globaler Gen Therapie Marktbericht Umfang
Gemäß dem Umfang dieses Berichts ist Gen Therapie eine fortgeschrittene medizinische Behandlung, die den überweisen eines Standard- oder gesunden Gens beinhaltet, um ein defektes Gen In einer Zelle zu ersetzen. Sie kann verschiedene chronische und genetische Störungen bei Menschen heilen, für die keine endgültige Heilung entwickelt wurde. Der Markt ist segmentiert nach Indikation (Krebs, Stoffwechselstörungen, Augenerkrankungen, Spinale Muskelatrophie und andere Indikationen), Technologie (Adenovirus-Vektor, Adeno-assoziierter Virus-Vektor, Lentiviraler Vektor, Retroviraler Vektor, Herpesvirus-Vektor und andere Technologien) sowie Geografie (Nordamerika, Europa, Asien-Pazifik, Naher Osten und Afrika und Südamerika). Der Marktbericht deckt auch die geschätzten Marktgrößen und Trends für 17 Länder über Große Regionen global ab. Der Bericht bietet den Wert (In USD Millionen) für die oben genannten Segmente.
| Adenovirus-Vektor |
| Adeno-assoziierter Virus-Vektor |
| Lentiviraler Vektor |
| Retroviraler Vektor |
| Herpesvirus-Vektor |
| Andere Vektortypen |
| Onkologie |
| Seltene Stoffwechselstörungen |
| Ophthalmologie |
| Neurologie / ZNS |
| Kardiovaskuläre und Muskelskeletale |
| Andere Indikationen |
| In-Vivo-Gentherapie |
| Ex-Vivo-Gentherapie |
| Krankenhäuser und Kliniken |
| Spezialisierte Behandlungs-/Infusionszentren |
| Akademische und Forschungsinstitute |
| Nordamerika | Vereinigte Staaten |
| Kanada | |
| Mexiko | |
| Europa | Deutschland |
| Vereinigtes Königreich | |
| Frankreich | |
| Italien | |
| Spanien | |
| Restliches Europa | |
| Asien-Pazifik | China |
| Japan | |
| Indien | |
| Australien | |
| Südkorea | |
| Restliches Asien-Pazifik | |
| Naher Osten & Afrika | GCC |
| Südafrika | |
| Restlicher Naher Osten & Afrika | |
| Südamerika | Brasilien |
| Argentinien | |
| Restliches Südamerika |
| Nach Vektortyp | Adenovirus-Vektor | |
| Adeno-assoziierter Virus-Vektor | ||
| Lentiviraler Vektor | ||
| Retroviraler Vektor | ||
| Herpesvirus-Vektor | ||
| Andere Vektortypen | ||
| Nach Indikation | Onkologie | |
| Seltene Stoffwechselstörungen | ||
| Ophthalmologie | ||
| Neurologie / ZNS | ||
| Kardiovaskuläre und Muskelskeletale | ||
| Andere Indikationen | ||
| Nach Verabreichungsart | In-Vivo-Gentherapie | |
| Ex-Vivo-Gentherapie | ||
| Nach Endnutzer | Krankenhäuser und Kliniken | |
| Spezialisierte Behandlungs-/Infusionszentren | ||
| Akademische und Forschungsinstitute | ||
| Nach Geografie | Nordamerika | Vereinigte Staaten |
| Kanada | ||
| Mexiko | ||
| Europa | Deutschland | |
| Vereinigtes Königreich | ||
| Frankreich | ||
| Italien | ||
| Spanien | ||
| Restliches Europa | ||
| Asien-Pazifik | China | |
| Japan | ||
| Indien | ||
| Australien | ||
| Südkorea | ||
| Restliches Asien-Pazifik | ||
| Naher Osten & Afrika | GCC | |
| Südafrika | ||
| Restlicher Naher Osten & Afrika | ||
| Südamerika | Brasilien | |
| Argentinien | ||
| Restliches Südamerika | ||


Wichtige Fragen im Bericht beantwortet
Was ist der aktuelle Wert des Gen Therapie Marktes?
Der Gen Therapie Markt ist mit USD 9,74 Milliarden In 2025 bewertet und soll auf USD 24,34 Milliarden bis 2030 steigen.
Welcher Vektortyp führt globale Verkäufe an?
Adeno-assoziierte Virus-Vektoren machen 38,54% des 2024er Umsatzes aufgrund ihres Sicherheitsprofils und dauerhafter Ausdruck aus.
Warum wächst Asien-Pazifik so schnell?
Asien-Pazifik verzeichnet eine CAGR von 27,68% aufgrund starker Regierungsfinanzierung, expandierender klinischer Studienvolumen In China und gestraffte Zulassungspfade In Japan und Singapur.
Wie handhaben Kostenträger hohe Therapiekosten?
Gesundheitssysteme setzen ergebnisbasierte Verträge, amortisierte Zahlungen und gepoolte staatliche Beschaffungsmodelle wie das CMS Zelle Und Gen Therapie Zugang Modell ein.
Welcher Faktor beschränkt das Marktwachstum heute am meisten?
Herstellungskomplexität und begrenzte Versorgung mit GMP-Grad-Vektoren begrenzen weiterhin kurzfristige Produktverfügbarkeit und erhöhen Herstellungskosten.
Seite zuletzt aktualisiert am:










