Marktgröße und Marktanteil für Colorektale Krebsdiagnostik und -therapeutika
Marktanalyse für Colorektale Krebsdiagnostik und -therapeutika von Mordor Intelligence
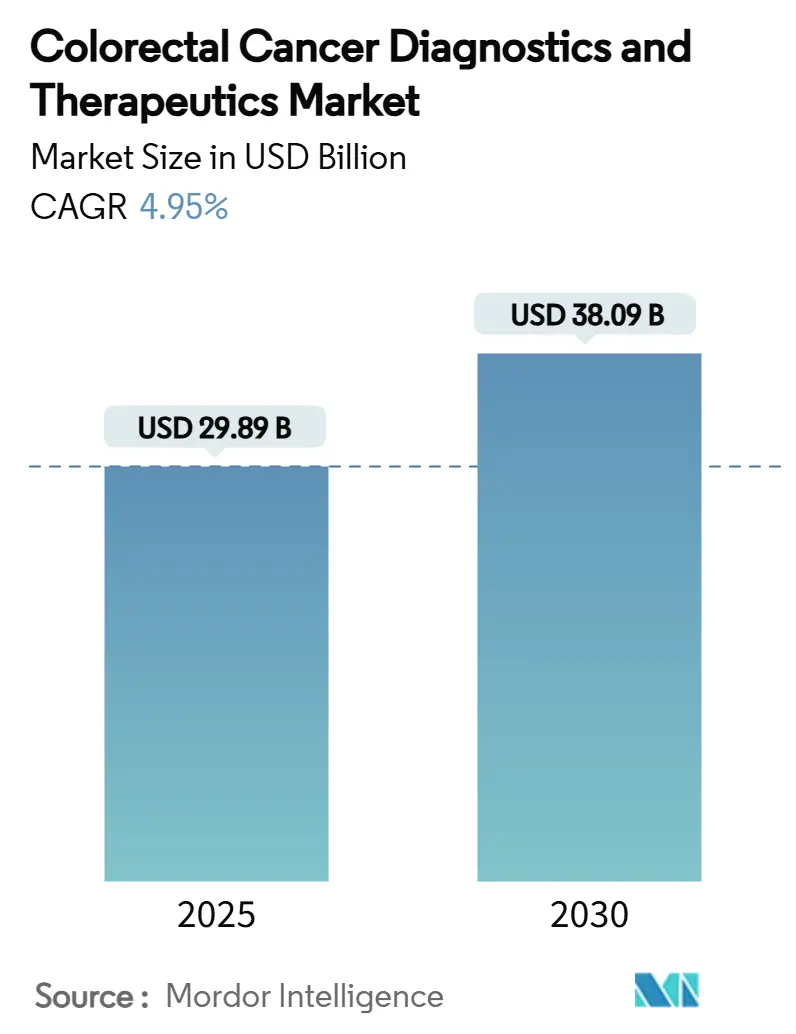
Der Markt für colorektale Krebsdiagnostik und -therapeutika wird mit 29,89 Milliarden USD im Jahr 2025 bewertet und soll bis 2030 38,09 Milliarden USD erreichen, mit einer CAGR von 4,95%. Das aktuelle Wachstum wird durch Präzisionsmedizin, KI-gestützte Screening-Verfahren und die kontinuierliche Einführung von Immuntherapie-Optionen vorangetrieben, die Überlebensraten verbessern und gleichzeitig Premiumpreise aufrechterhalten. Nicht-invasive Tests - Stuhl-DNA, blutbasierte Assays und KI-unterstützte Koloskopie - bringen bisher ungetestete Bevölkerungsgruppen in klinische Behandlungspfade, während Dual-Checkpoint-Blockade die Erstlinientherapie für Biomarker-definierte Patienten neu gestaltet. Erstattungsanpassungen in den Vereinigten Staaten und Politikkonvergenz in Europa beschleunigen die Adoption, und Asien-Pazifik überwindet Altlasten-Engpässe durch staatlich finanzierte Technologieprogramme. Kostendruck und Kapazitätsbeschränkungen bleiben bestehen, dennoch monetarisiert der Markt für colorektale Krebsdiagnostik und -therapeutika Innovationen schneller, als Screening-Volumina in reifen Volkswirtschaften stagnieren.
Wichtige Berichtserkenntnisse
- Nach Modalität hielten diagnostische Verfahren 27,9% des Marktanteils für colorektale Krebsdiagnostik und -therapeutika im Jahr 2024, während Therapeutika auf Kurs sind, die schnellste CAGR von 13,6% bis 2030 zu verzeichnen.
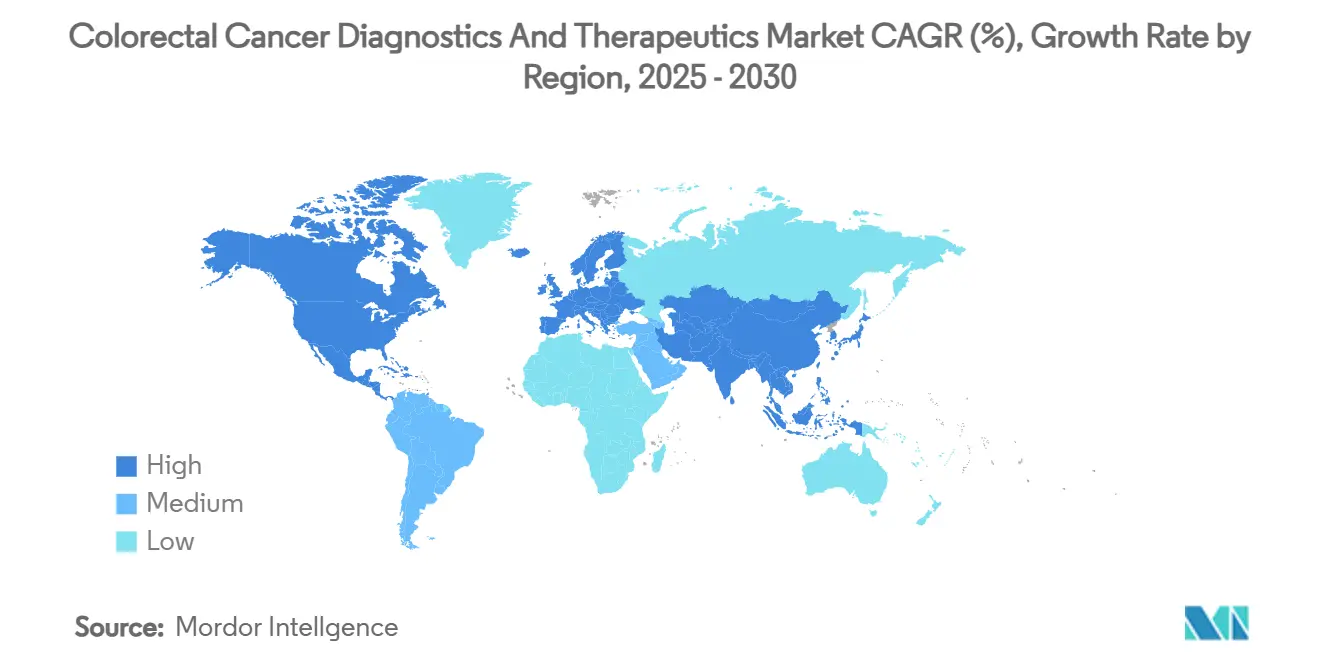
- Nach Geografie führte Nordamerika mit 34,6% Umsatzanteil im Jahr 2024, während Asien-Pazifik voraussichtlich mit einer CAGR von 7,70% bis 2030 wachsen wird.
Globale Trends und Erkenntnisse des Marktes für Colorektale Krebsdiagnostik und -therapeutika
Analyse der Treiber-Auswirkungen
| Treiber | (~) % Auswirkung auf CAGR-Prognose | Geografische Relevanz | Auswirkungszeitraum |
|---|---|---|---|
| Steigende Inzidenz und Prävalenz von Darmkrebs | +1.20% | Global, mit höchster Auswirkung in APAC und MEA | Langfristig (≥ 4 Jahre) |
| Rasche Adoption von Next-Generation Stuhl-DNA und blutbasierten Screening-Tests | +0.80% | Nordamerika & EU, expandierend nach APAC | Mittelfristig (2-4 Jahre) |
| Technologische Durchbrüche bei zielgerichteten Therapien und Immuntherapie-Pipelines | +1.10% | Global, angeführt von Nordamerika und Europa | Mittelfristig (2-4 Jahre) |
| Ausweitung des leitlinienbasierten Screenings auf 45-Jährige in Schlüsselmärkten | +0.60% | Nordamerika, Europa, ausgewählte APAC-Länder | Kurzfristig (≤ 2 Jahre) |
| Molekulare Resterkrankung (MRD)-Tests verändern Adjuvant-Therapie-Entscheidungen | +0.40% | Nordamerika, Europa, Premium-APAC-Märkte | Langfristig (≥ 4 Jahre) |
| Wertbasierte Erstattung, die Früherkennung belohnt | +0.30% | Nordamerika, ausgewählte europäische Märkte | Mittelfristig (2-4 Jahre) |
| Quelle: Mordor Intelligence | |||
Steigende Inzidenz von Darmkrebs
Die Früh-Onset-Inzidenz stieg von 5,43 auf 6,13 pro 100.000 zwischen 1990 und 2021, und Modellierungen signalisieren eine kontinuierliche Beschleunigung bis 2030.[1]B. Siegel et al., "Global Trends in Early-Onset Colorectal Cancer," bmcmedicine.biomedcentral.com Einkommensstarke Länder zeigen Lebensstilkonvergenz, die das Risiko in jüngeren Jahren erhöht, während Asien-Pazifik Inzidenzraten von 7,51 pro 100.000 für Männer und 6,22 für Frauen verzeichnet. Längere Überlebenszeiten steigern die lebenslange Screening- und Nachsorgenachfrage und verankern anhaltende Umsatzsichtbarkeit im Markt für colorektale Krebsdiagnostik und -therapeutika.
Rasche Adoption von Next-Generation Stuhl-DNA und blutbasierten Screening-Tests
FDA-Zulassungen für Shield (83,1% Sensitivität), Cologuard Plus (93,9%) und ColoSense (94,4%) im Jahr 2024 erweiterten das nicht-invasive Test-Toolkit.[2]FDA, "Blood-Based and Stool-Based Colorectal Cancer Screening Tests," fda.gov Diese Modalitäten adressieren die 40% der berechtigten Erwachsenen, die historisch die Koloskopie übersprungen haben, und könnten potenziell 15-20 Millionen US-amerikanische Leben zum jährlichen Screening-Pool hinzufügen. Das Vertrauen der Investoren festigte sich mit Genoscopys 105 Millionen USD Series C-Runde im Januar 2025.
Technologische Durchbrüche bei zielgerichteten Therapien und Immuntherapie-Pipelines
KRAS G12C-Inhibitor-Kombinationen wurden 2024-2025 zugelassen und erschlossen Optionen für 40% der mutationspositiven Tumore, während Dual-Checkpoint-Blockade (Opdivo + Yervoy) ein medianes progressionsfreies Überleben lieferte, das noch nicht erreicht wurde gegenüber 39,3 Monaten für Monotherapie bei MSI-H-Erkrankung.[3]Bristol Myers Squibb, "Opdivo + Yervoy Receives FDA Approval for Metastatic Colorectal Cancer," bms.com Begleitdiagnostika sind nun in Verschreibungsabläufe eingebettet und erhöhen die Nachfrage nach Biomarker-Assays innerhalb des Marktes für colorektale Krebsdiagnostik und -therapeutika.
Ausweitung des leitlinienbasierten Screenings auf 45-Jährige in Schlüsselmärkten
Medicares Adoption 2025 und die Ausrichtung privater Kostenträger öffnete die Screening-Berechtigung für 19 Millionen zusätzliche Amerikaner und verbesserte Kosten-pro-QALY-Verhältnisse über Risiko-Kohorten hinweg. Die Niederlande und Dänemark spiegelten die Politik wider und unterstrichen die transatlantische Dynamik für frühere Erkennung.
Analyse der Beschränkungen-Auswirkungen
| Beschränkung | (~) % Auswirkung auf CAGR-Prognose | Geografische Relevanz | Auswirkungszeitraum |
|---|---|---|---|
| Hohe Medikamentenkosten und behandlungsbezogene Toxizitäten | -0.70% | Global, am schwerwiegendsten in Schwellenmärkten | Mittelfristig (2-4 Jahre) |
| Suboptimale Screening-Adhärenz in ressourcenarmen Umgebungen | -0.50% | APAC, MEA, Lateinamerika | Langfristig (≥ 4 Jahre) |
| Begrenzte Immuntherapie-Wirksamkeit bei MSS-Tumoren verursacht hohe Studien-Ausfallrate | -0.40% | Global, besonders Nordamerika und Europa | Mittelfristig (2-4 Jahre) |
| Datenintegrations- und Datenschutzhürden für KI-gestützte Diagnostikplattformen | -0.30% | Nordamerika, Europa, ausgewählte APAC-Märkte | Kurzfristig (≤ 2 Jahre) |
| Quelle: Mordor Intelligence | |||
Hohe Medikamentenkosten und behandlungsbezogene Toxizitäten
Zielgerichtete Therapie-Regime kosten durchschnittlich 150.000-200.000 USD pro Jahr, eine Belastung, die die Aufnahme einschränkt, wo Eigenanteile 60% der gesamten Gesundheitskosten übersteigen. Kombinationsimmuntherapie erfordert intensive Sicherheitsüberwachung, da Grad 3/4 unerwünschte Ereignisse 81% erreichen können, was Onkologie-Budgets und Versorgungsinfrastruktur in der colorektalen Krebsdiagnostik und -therapeutika-Branche strapaziert.
Suboptimale Screening-Adhärenz in ressourcenarmen Umgebungen
Screening-Raten reichen von 75% in Dänemark bis 6,3% in Ländern ohne organisierte Programme. In Saudi-Arabien wurden 62% der berechtigten Personen nie gescreent, hauptsächlich aufgrund von Koloskopie-Angst und begrenztem geografischem Zugang. Diese Lücken führen zu Spätstadiumpräsentationen, die die Mortalität erhöhen und Wachstumsaussichten für den Markt für colorektale Krebsdiagnostik und -therapeutika dämpfen.
Segmentanalyse
Nach Modalität: Therapeutika treiben Wachstum trotz Diagnostik-Dominanz
Therapeutika erzeugten starken Rückenwind mit einer CAGR von 13,6%, die Screening-Aktivitäten überholte. Opdivo + Yervoy sicherte sich Erstlinienstatus für MSI-H/dMMR-Erkrankung und setzte Umsatzerwartungen zu Premiumpreisen neu. KRAS-, EGFR- und HER2-Ziele erweitern adressierbare Pools und steigern die Marktgröße für colorektale Krebsdiagnostik und -therapeutika bei personalisierten Regimen. Diagnostik behielt 27,9% des Marktanteils für colorektale Krebsdiagnostik und -therapeutika im Jahr 2024, unterstützt durch Multitarget-Stuhl-DNA, Blutbiomarker und KI-Koloskopie, die Screening bequemer machen. Medtronics GI Genius erhöhte die Adenom-Erkennung um 14,4% und sicherte sich einen dreijährigen VA-Vertrag für fast 100 zusätzliche Einheiten. Shield und ColoSense erweiterten blut- und RNA-basierte Tests, doch Kostenträger kalibrieren noch die Abdeckung für ihre höheren Pro-Test-Kosten.
Diagnostik-Monetarisierung schwenkt von Volumen zu Diversifizierung. Exact Sciences führte Cologuard Plus mit 93,9% Sensitivität ein, reduzierte falsch positive Ergebnisse und verstärkte seine Führung. Blutbasierte Assays wachsen schnell bei jüngeren Kohorten, die Nadelstiche invasiven Spiegelungen vorziehen, eine Ausrichtung, die Adhärenz verbessert. Molekulare Resterkrankungs-Tests erweitern den Wert über das Behandlungskontinuum durch Markierung minimaler Erkrankung nach Operation und vergrößern weitere Marktgrößenchancen für colorektale Krebsdiagnostik und -therapeutika durch Nachfolge-Tests.
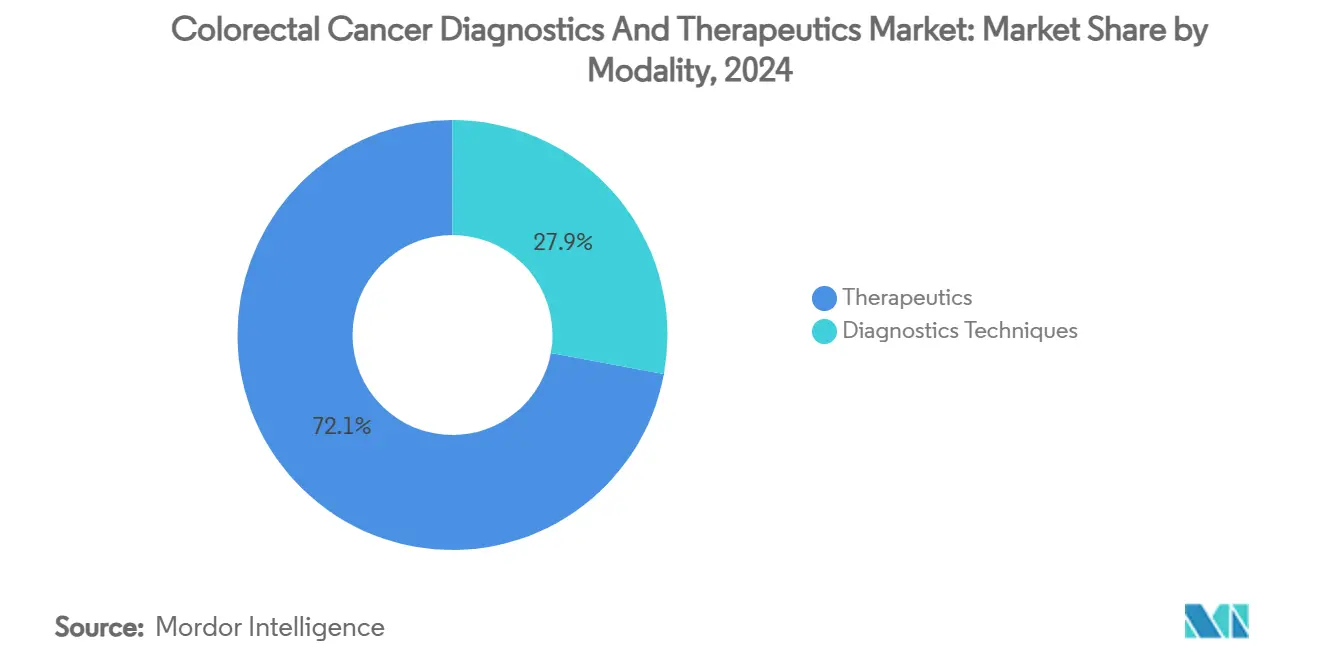
Notiz: Segmentanteile aller einzelnen Segmente verfügbar beim Berichtskauf
Geografische Analyse
Nordamerikas Führung ist in Erstattungsbreite und Innovationsgeschwindigkeit verankert. Medicare-Abdeckung für CT-Kolonografie im Jahr 2025 beseitigt eine prozedurale Kostenhürde und ergänzt Blut- und Stuhltests, die bereits unter Präventivkodes erstattet werden. Sechzig Prozent der Darmkrebs-Medikamentenstudien laufen in US- und kanadischen Zentren und beschleunigen FDA-Zulassungen, die weltweit ausstrahlen. VA-Einsatz von 100 GI Genius-Einheiten unterstreicht institutionelle Migration zu KI-Diagnostik. Regulatorische Pfade wie Breakthrough Device und Priority Review verkürzen Zeitlinien, doch steigende Prüfung der Therapiekosten erhöht Zeit-zu-Gewinn-Hürden für kürzliche Markteinführungen.
Asien-Pazifik überholt alle Regionen mit 7,70% CAGR. Regierungsprogramme erweitern Screening auf das ländliche China und subventionieren KI-Koloskopie in Japan, was Technologie traditionelle Engpässe überspringen lässt. Inzidenzraten von 7,51 pro 100.000 für Männer und 6,22 für Frauen drängen Politiker zum Handeln. Fertigungscluster reduzieren Ausrüstungskosten, während Medizintourismus regionale Patienten zu Technologiezentren in Thailand und Indien lenkt und die Nachfrage innerhalb des Marktes für colorektale Krebsdiagnostik und -therapeutika verstärkt.
Europas Trajektorie ist stabil, angetrieben durch gut etablierte nationale Programme. Die Nutzung variiert noch: 75% in Dänemark, aber unter 10% in einkommensschwächeren Mitgliedern. EMA-zentralisierte Zulassungen verlängern Pipeline-Zeitlinien im Vergleich zur FDA; jedoch führt nach erteilter Zulassung die Erstattungsabdeckung durch universelle Systeme zu rascher Durchdringung. Naher Osten & Afrika versprechen zukünftige Aufwärtspotenziale, besonders in GCC-Staaten, wo Öleinnahmen Krebszentren finanzieren, die mit KI-Bildgebung und Immuntherapien ausgestattet sind.
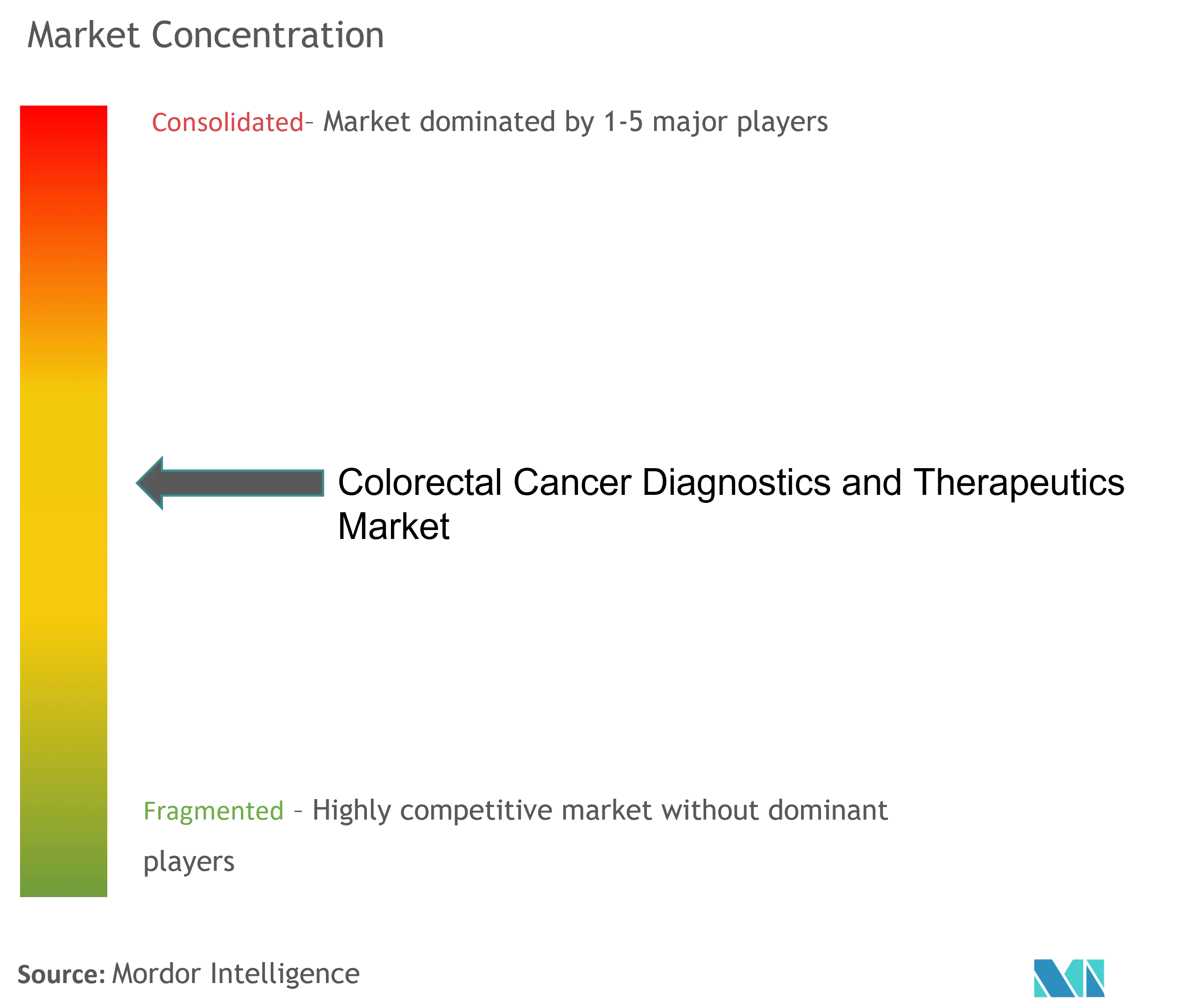
Wettbewerbslandschaft
Die Wettbewerbsintensität ist moderat. Exact Sciences, Guardant Health und Bristol Myers Squibb repräsentierten gemeinsam mehr als 42% des Umsatzes von 2024 innerhalb der Marktgröße für colorektale Krebsdiagnostik und -therapeutika. Exact Sciences steigerte den Q1 2025-Umsatz auf 707 Millionen USD mit 14% Cologuard-Volumenwachstum. Guardant Healths Shield-Bluttest fordert Stuhl-DNA-Incumbenz heraus und zielt auf nicht-konforme Patienten mit einem 83,1% Sensitivitätsprofil.
Auf der Therapieseite erweiterte Bristol Myers Squibb sein Immuno-Onkologie-Franchise mit Dual-Checkpoint-Blockade, die Progressionsrisiko um 79% gegenüber Chemotherapie reduziert. Johnson & Johnsons RYBREVANT-Programm adressiert EGFR-getriebene Erkrankung und verzeichnete 49% Gesamtansprechrate bei RAS/BRAF-Wildtyp-Tumoren. Medtronic nutzt KI-Differenzierung, wobei GI Genius übersehene Polyp-Raten um 50% in klinischer Praxis senkte und VA-Expansionsauszeichnungen gewann.
Aufkommende Marktteilnehmer fokussieren sich auf molekulare Resterkrankung, Multiomik und digitale Pathologie. Tagomics sicherte sich 860.000 GBP Innovate UK-Förderung zur Validierung eines epigenetischen Panels, während PathPresenter FDA 510(k)-Zulassung für einen Cloud-Viewer erhielt, der Pathologie-Arbeitsabläufe rationalisiert. M&A bleibt aktiv, da Merck Prometheus Biosciences übernahm, um Präzisionsmedizin-Pipelines bei colorektalen Indikationen zu stärken. Das Feld bevorzugt Unternehmen, die Diagnostik und Therapeutika unter einheitlichen Kommerzialisierungsschirmen integrieren.
Branchenführer für Colorektale Krebsdiagnostik und -therapeutika
-
Epigenomics AG
-
Abbott Laboratories
-
F. Hoffmann-La Roche AG
-
Novigenix SA
-
Amgen Inc
- *Haftungsausschluss: Hauptakteure in keiner bestimmten Reihenfolge sortiert
Aktuelle Branchenentwicklungen
- Juni 2025: Tagomics erhielt eine 860.000 GBP (1,1 Millionen USD) Innovate UK Biomedical Catalyst-Förderung zur Entwicklung einer Multiomik-Plattform für frühe Darmkrebs-Erkennung.
- Juni 2025: PathPresenter erhält FDA 510(k)-Zulassung für einen digitalen Pathologie-Viewer kompatibel mit Hamamatsu NanoZoomer S360MD.
- April 2025: Bristol Myers Squibb gewinnt FDA-Zulassung für Opdivo + Yervoy bei Erstlinien-MSI-H/dMMR metastasierendem Darmkrebs.
- März 2025: Mainz Biomed rekrutiert den ersten Patienten in eAArly DETECT 2 zur Weiterentwicklung RNA-basierter Darmkrebs-Diagnostik.
- Januar 2025: Geneoscopy schließt 105 Millionen USD Series C-Finanzierung unter Führung von Bio-Rad zur Kommerzialisierung von ColoSense und Expansion in IBD-Tests ab.
Umfang des globalen Berichts zum Markt für Colorektale Krebsdiagnostik und -therapeutika
Entsprechend dem Umfang des Berichts ist Darmkrebs, auch bekannt als Darmkrebs, Kolonkarzinom oder Rektumkarzinom, jede Form von Krebs, die Kolon und Rektum betrifft. Die Diagnostik und Therapeutika zur Behandlung von Darmkrebs sind verschiedene Screening-Tests, Kits und medizinische Geräte.
Der Markt für colorektale Krebsdiagnostik und -therapeutika ist segmentiert nach Modalität (diagnostische Verfahren (Stuhltests, Immunhistochemie, Koloskopie, flexible Sigmoidoskopie und andere diagnostische Verfahren) und Therapeutika (Chemotherapie, Immuntherapie und andere Therapeutika)) und Geografie (Nordamerika, Europa, Asien-Pazifik, Naher Osten und Afrika, und Südamerika). Der Bericht deckt auch die geschätzten Marktgrößen und Trends für 17 Länder in wichtigen Regionen weltweit ab.
Der Bericht bietet den Wert (in USD) für die oben genannten Segmente.
| Diagnostische Verfahren | Stuhlbasierte Tests | Fäkaler Immunchemischer Test (FIT) |
| Guajak-FOBT | ||
| Multitarget-Stuhl-DNA (mt-sDNA) | ||
| Blutbasierte Biomarker-Tests | ctDNA-Assays | |
| Epigenetische Methylierungs-Panels | ||
| Endoskopie-basierte Bildgebung | Koloskopie | |
| KI-unterstützte Koloskopie | ||
| Flexible Sigmoidoskopie | ||
| Radiologie und Molekulare Endoskopie | ||
| Histopathologie / Digitale Pathologie | ||
| Therapeutika | Chemotherapie | Fluoropyrimidine (5-FU, Capecitabin) |
| Oxaliplatin-basierte Regime (FOLFOX) | ||
| Irinotecan-basierte Regime (FOLFIRI) | ||
| Zielgerichtete Therapie | Anti-EGFR (Cetuximab, Panitumumab) | |
| Anti-VEGF (Bevacizumab, Aflibercept) | ||
| BRAF / HER2 / KRAS G12C-Inhibitoren | ||
| Immuntherapie | PD-1 / PD-L1-Inhibitoren | |
| CTLA-4-Kombinationen | ||
| CAR-T / Onkolytische Viren | ||
| Andere Therapeutika (Radioembolisation, Impfstoffe) | ||
| Nordamerika | Vereinigte Staaten |
| Kanada | |
| Mexiko | |
| Europa | Deutschland |
| Vereinigtes Königreich | |
| Frankreich | |
| Italien | |
| Spanien | |
| Übriges Europa | |
| Asien-Pazifik | China |
| Japan | |
| Indien | |
| Südkorea | |
| Australien | |
| Übriges Asien-Pazifik | |
| Naher Osten und Afrika | GCC |
| Südafrika | |
| Übriger Naher Osten und Afrika | |
| Südamerika | Brasilien |
| Argentinien | |
| Übriges Südamerika |
| Nach Modalität | Diagnostische Verfahren | Stuhlbasierte Tests | Fäkaler Immunchemischer Test (FIT) |
| Guajak-FOBT | |||
| Multitarget-Stuhl-DNA (mt-sDNA) | |||
| Blutbasierte Biomarker-Tests | ctDNA-Assays | ||
| Epigenetische Methylierungs-Panels | |||
| Endoskopie-basierte Bildgebung | Koloskopie | ||
| KI-unterstützte Koloskopie | |||
| Flexible Sigmoidoskopie | |||
| Radiologie und Molekulare Endoskopie | |||
| Histopathologie / Digitale Pathologie | |||
| Therapeutika | Chemotherapie | Fluoropyrimidine (5-FU, Capecitabin) | |
| Oxaliplatin-basierte Regime (FOLFOX) | |||
| Irinotecan-basierte Regime (FOLFIRI) | |||
| Zielgerichtete Therapie | Anti-EGFR (Cetuximab, Panitumumab) | ||
| Anti-VEGF (Bevacizumab, Aflibercept) | |||
| BRAF / HER2 / KRAS G12C-Inhibitoren | |||
| Immuntherapie | PD-1 / PD-L1-Inhibitoren | ||
| CTLA-4-Kombinationen | |||
| CAR-T / Onkolytische Viren | |||
| Andere Therapeutika (Radioembolisation, Impfstoffe) | |||
| Geografie | Nordamerika | Vereinigte Staaten | |
| Kanada | |||
| Mexiko | |||
| Europa | Deutschland | ||
| Vereinigtes Königreich | |||
| Frankreich | |||
| Italien | |||
| Spanien | |||
| Übriges Europa | |||
| Asien-Pazifik | China | ||
| Japan | |||
| Indien | |||
| Südkorea | |||
| Australien | |||
| Übriges Asien-Pazifik | |||
| Naher Osten und Afrika | GCC | ||
| Südafrika | |||
| Übriger Naher Osten und Afrika | |||
| Südamerika | Brasilien | ||
| Argentinien | |||
| Übriges Südamerika | |||
Wichtige im Bericht beantwortete Fragen
Wie groß ist der Markt für colorektale Krebsdiagnostik und -therapeutika im Jahr 2025?
Der Markt wird mit 29,89 Milliarden USD im Jahr 2025 bewertet und soll 38,09 Milliarden USD bis 2030 bei einer CAGR von 4,95% erreichen.
Welches Segment wächst am schnellsten?
Therapeutika führen das Wachstum mit einer CAGR von 13,6% bis 2030 an, angetrieben von Immuntherapie- und zielgerichteten kleinmolekularen Zulassungen.
Welchen Anteil hält Nordamerika?
Nordamerika macht 34,6% des globalen Umsatzes aus, eine Position, die durch breite Erstattung und hohe Innovationsdichte unterstützt wird.
Warum expandiert Asien-Pazifik schnell?
Staatlich finanzierte Screening-Programme, KI-gestützte Koloskopie-Adoption und kosteneffiziente Fertigung treiben eine CAGR von 7,70% in Asien-Pazifik an.
Was sind die wichtigsten Kostenhürden?
Zielgerichtete Therapiekurse kosten durchschnittlich 150.000-200.000 USD jährlich und bringen hohe Toxizitäts-Management-Kosten mit sich, die Schwellenmarkt-Budgets belasten.
Seite zuletzt aktualisiert am:



