Marktgröße und Marktanteil für Gehirntumorbehandlungen
Marktanalyse für Gehirntumorbehandlungen von Mordor Intelligence
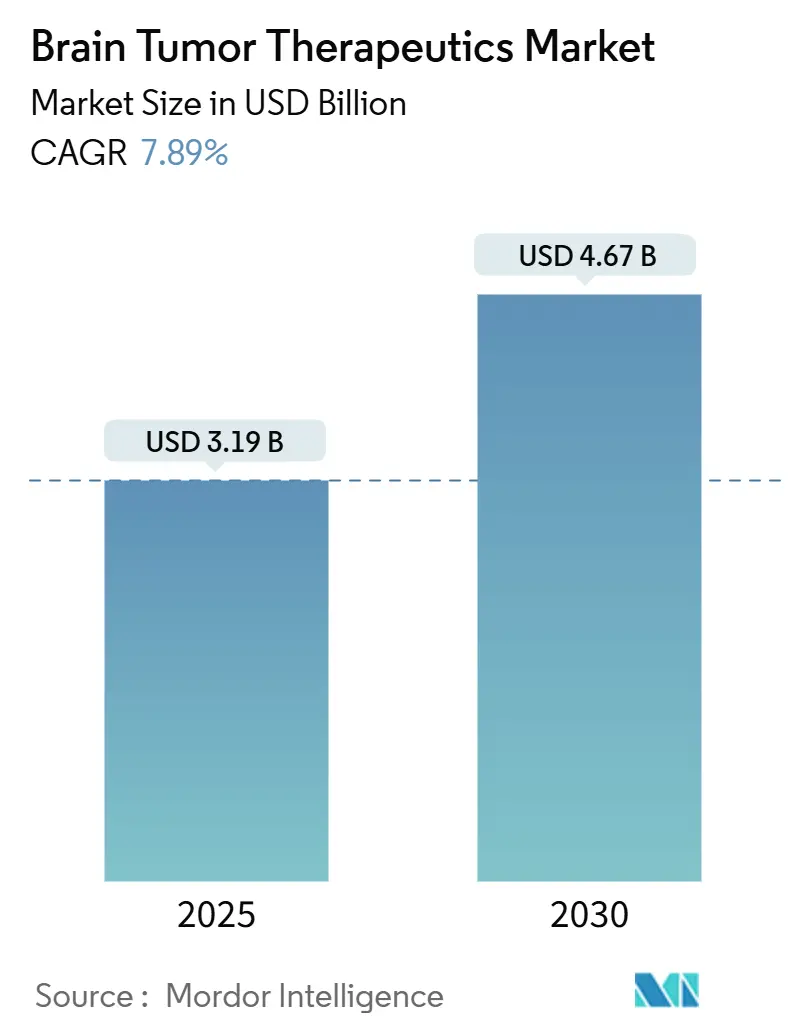
Der Markt für Gehirntumorbehandlungen erreichte 3,19 Milliarden USD im Jahr 2025 und soll bis 2030 auf 4,67 Milliarden USD ansteigen, mit einer Expansion von 7,89% CAGR. Das robuste Wachstum spiegelt die Konvergenz von Präzisionsmedizin-Durchbrüchen, beschleunigten Zulassungen und einer stetigen Pipeline von späten Entwicklungsphasen wider, die den Weg vom Labor zum Krankenbett verkürzen. Die kommerzielle Einführung der Borneutroneneinfangtherapie (BNCT) zusammen mit KI-gestützten Wirkstoff-Repositionierungs-Tools verändert die therapeutischen Erwartungen, insbesondere bei Gliomen und anderen hochgradigen Tumoren. Intravenöse Behandlungsregime dominieren weiterhin die klinische Praxis, da sie eine präzise pharmakokinetische Kontrolle ermöglichen, doch gewinnen orale zielgerichtete Wirkstoffe an Boden, da sich Blut-Hirn-Schranken-Lösungen verbessern. Investoren leiten weiterhin Rekordsummen in die Neuroonkologie, wobei große Biopharma-Konzerne in den letzten zwei Jahren mehr als 53 Milliarden USD für neurologische Assets bereitgestellt haben. Allerdings bremsen Störungen der Radioisotop-Lieferkette und erhöhte Therapiekosten die kurzfristige Dynamik.
Wichtigste Erkenntnisse des Berichts
- Nach Krebsart führte das Glioblastom mit 51,23% Marktanteil für Gehirntumorbehandlungen im Jahr 2024 und ist auch für die schnellste CAGR von 8,45% bis 2030 positioniert.
- Nach Therapie hielt die Immuntherapie 32,56% Umsatzanteil im Jahr 2024; zielgerichtete niedermolekulare Behandlungen werden voraussichtlich die höchste CAGR von 8,52% bis 2030 verzeichnen.
- Nach Verabreichungsweg kommandierte das intravenöse Segment 56,34% Anteil der Marktgröße für Gehirntumorbehandlungen im Jahr 2024.
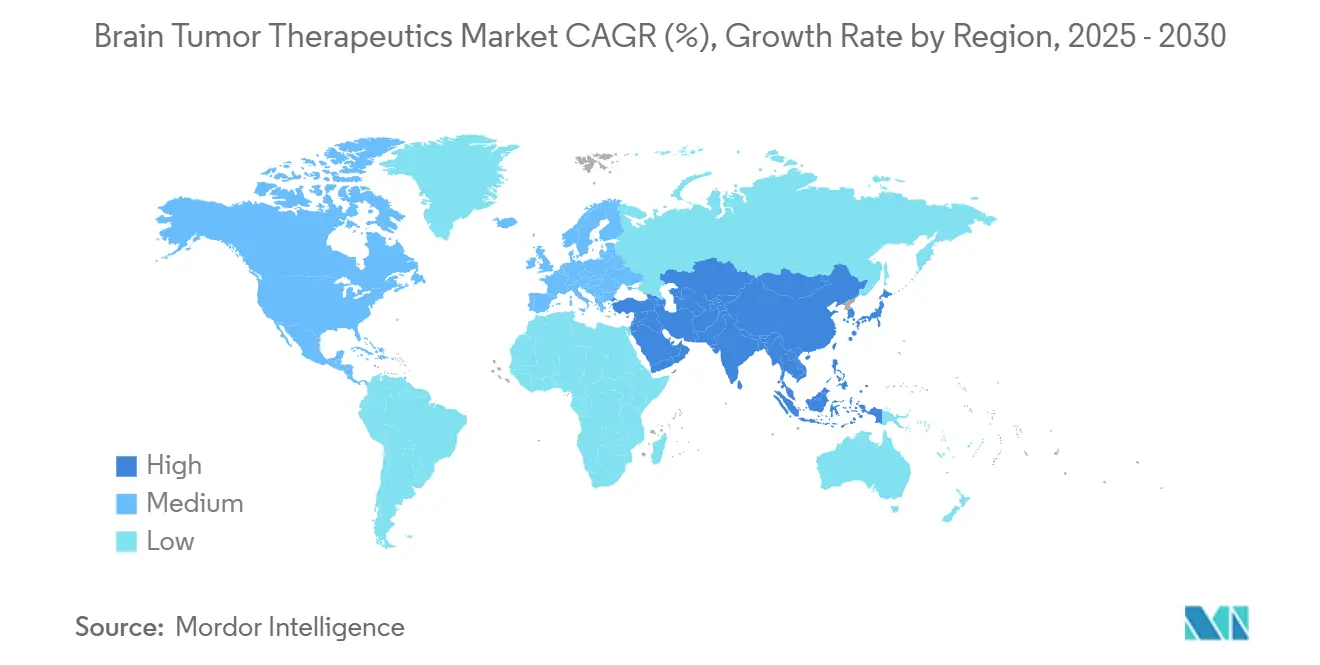
- Nach Geografie entfielen auf Nordamerika 40,34% Umsatzanteil im Jahr 2024, während für Asien-Pazifik eine CAGR von 8,54% bis 2030 prognostiziert wird.
Globale Markttrends und Einblicke für Gehirntumorbehandlungen
Auswirkungsanalyse der Treiber
| Treiber | (≈) % Auswirkung auf CAGR-Prognose | Geografische Relevanz | Auswirkungszeitraum |
|---|---|---|---|
| Steigende Inzidenz primärer und metastatischer Hirntumoren | +1.8% | Global | Mittelfristig (2-4 Jahre) |
| Erweiterung der späten Pipeline und beschleunigte FDA-Zulassungen | +2.1% | Nordamerika & EU, Übertragung auf APAC | Kurzfristig (≤ 2 Jahre) |
| Präzisionsmedizin-Wandel hin zu biomarker-geleiteten Therapien | +1.6% | Global; frühe Gewinne in USA, Deutschland, Japan | Mittelfristig (2-4 Jahre) |
| Staatlich geförderte Hirnkrebs-Initiativen und Finanzierungsschübe | +1.2% | Nordamerika & EU Kernbereich | Langfristig (≥ 4 Jahre) |
| Kommerzielle BNCT-Einführungsdynamik | +0.9% | APAC Kernbereich; Übertragung auf MEA | Langfristig (≥ 4 Jahre) |
| KI-gestützte Wirkstoff-Repositionierung beschleunigt Waisen-Tumor-Kandidaten | +1.4% | Global | Kurzfristig (≤ 2 Jahre) |
| Quelle: Mordor Intelligence | |||
Erweiterung der späten Pipeline und beschleunigte FDA-Zulassungen
Die Regulierungsgeschwindigkeit formt weiterhin den Markt für Gehirntumorbehandlungen um. Vorasidenibs Zulassung 2024 für Grad-2-IDH-mutante Gliome verdoppelte das mediane progressionsfreie Überleben gegenüber Placebo und validierte biomarker-geleitete Entwicklungspfade[1]Drugs.com, "FDA Approves Vorasidenib for Low-Grade Glioma," drugs.com. Durchbruchstherapie-Bezeichnungen verkürzen Zeitpläne, während Ausnahmen für Untersuchungsgeräte nun neuartige Strahlentherapie-Plattformen wie Alpha DaRTs Radium-224-Seeds für rezidivierende Glioblastome abdecken. Die kollektive Dynamik verkürzt Kommerzialisierungszyklen und ermutigt zu mehrmäßigen Master-Studien, die molekulare Untergruppen mit zielgerichteten Wirkstoffen abgleichen.
Präzisionsmedizin-Wandel hin zu biomarker-geleiteten Therapien
Routinetests für IDH-Mutation, MGMT-Promotor-Methylierung und 1p/19q-Kodeletion leiten nun die Regimen-Auswahl in führenden Zentren. Flüssigbiopsie-Plattformen bieten molekulare Echtzeitauslesungen und ermöglichen Therapiewechsel vor radiographischer Progression. Maschinenlern-Algorithmen, die Multi-Omics-Profile integrieren, sagen bereits Immuntherapie-Antworten mit über 90% Genauigkeit voraus, eine Fähigkeit, die Eignungskriterien für Checkpoint-Blockaden verfeinert.
Kommerzielle Einführung kompakter BNCT-Plattformen
Japan hat die Borneutroneneinfangtherapie von experimenteller Nutzung zu routinemäßigem Krankenhausservice bewegt, indem kompakte beschleunigerbasierte Neutronquellen installiert wurden, die die großen Forschungsreaktoren ersetzen, die in früheren Studien verwendet wurden. Mehr als 500 Patienten haben bereits die Therapie erhalten und etablieren eine erste reale Sicherheits- und Wirksamkeitsaufzeichnung für die Modalität. Klinische Programme erweitern sich nun über rezidivierende Kopf-Hals-Tumoren hinaus auf Hirnmalignome, unterstützt von Bor-Trägern der nächsten Generation wie Peptid-konjugierten Verbindungen, die sich selektiver im Tumorgewebe ansammeln. Parallele Monte-Carlo-Studien zeigen, dass neu gestaltete Neutronengeneratoren thermische-zu-epithermische Flussverhältnisse erreichen können, die IAEA-Behandlungsrichtlinien entsprechen, ein technischer Meilenstein, der die Tür zu breiteren Krankheitsanwendungen und Installation in regionalen Krebszentren öffnet.
KI-unterstützte Wirkstoff-Repositionierung für Waisen-Hirntumoren
Maschinenlern-Plattformen, die Legacy-Verbindungsbibliotheken gegen Multi-Omics-Krebsdatensätze durchsuchen, komprimieren die Entdeckungszeitlinie für seltene Hirntumorbehandlungen von Jahrzehnten auf nur wenige Jahre. Musterkennungsalgorithmen haben bereits neue Anwendungen für vertraute Moleküle hervorgehoben, einschließlich der Repositionierung des Anthelmintikums Mebendazol für Glioblastom, das nun in einer kürzlichen Patentanmeldung geschützt ist. Die Modellgenauigkeit verbessert sich weiter, da Trainingssätze genomische, transkriptomische und reale Behandlungsergebnis-Daten kombinieren, wodurch Entwickler Medikamentenreaktionen auf Tumor-Subtyp-Ebene mit hohem Vertrauen vorhersagen können. Der Ansatz ist besonders wertvoll für ultra-seltene Hirntumoren, deren kleine Patientenpools konventionelle prospektive Studien unpraktisch machen; KI-geleitete Repositionierung liefert klinisch umsetzbare Kandidaten bei minimalen Kosten und Zeitaufwand.
Auswirkungsanalyse der Beschränkungen
| Beschränkung | (≈) % Auswirkung auf CAGR-Prognose | Geografische Relevanz | Auswirkungszeitraum |
|---|---|---|---|
| Hohe Kosten neuartiger Therapeutika und Kombinationsregime | -1.4% | Global | Kurzfristig (≤ 2 Jahre) |
| Blut-Hirn-Schranke begrenzt niedermolekulare und biologische Penetration | -1.1% | Global | Mittelfristig (2-4 Jahre) |
| Tumor-Mikroumgebung-getriebene Immuntherapie-Resistenz | -0.8% | Global | Mittelfristig (2-4 Jahre) |
| Radioisotop-Lieferengpässe für BNCT-Einrichtungen | -0.6% | APAC Kernbereich; aufkommend in Nordamerika | Langfristig (≥ 4 Jahre) |
| Quelle: Mordor Intelligence | |||
Hohe Kosten neuartiger Therapeutika und Kombinationsregime
Erstklassige Zell- und Gentherapien überschreiten oft 400.000 USD pro Behandlungsverlauf, während Multi-Agent-Kombinationen weitere 300.000 USD jährlich hinzufügen können, was Kostenträger-Budgets belastet. Gesundheitssysteme verknüpfen nun Erstattungen mit realen Ergebnissen, was Abdeckungsverzögerungen schafft, die frühe Adoption in einkommensschwächeren Umgebungen begrenzen.
Blut-Hirn-Schranke begrenzt niedermolekulare und biologische Penetration
Nur 2% systemischer Moleküle erreichen therapeutische Konzentrationen im Gehirn, was zur Abhängigkeit von hohen Dosen zwingt, die systemische Toxizität erhöhen. Fokussierter Ultraschall, konvektionsgestützte Verabreichung und Nanopartikel-Träger machen Fortschritte, doch Kapitalintensität und spezialisierte Ausbildung verlangsamen die Einführung über tertiäre Zentren hinaus.
Segmentanalyse
Nach Art der Hirnkrebserkrankung: Glioblastom treibt Innovation trotz therapeutischer Hürden voran
Das Glioblastom hielt 51,23% Marktanteil für Gehirntumorbehandlungen im Jahr 2024 und wird mit einer CAGR von 8,45% prognostiziert, wodurch es den größten Anteil der Marktgröße für Gehirntumorbehandlungen bis 2030 behält. Hohe Sterblichkeit, begrenzte Standardbehandlungsoptionen und das Aufkommen von Tumor-behandelnden Feldern helfen, Investorenfokus zu erhalten.
Fortgesetzte Gerät-Medikament-Paarungen, Peptid-Impfstoffe und IDH-selektive Inhibitoren illustrieren Kapitalkonzentration in diesem Segment. Meningiom folgt in Werttermen dank verfeinerten Radiochirurgie-Protokollen, während Hypophysentumoren von neuartigen endokrinen Modulatoren profitieren, die Hormonspiegel vorhersagbarer normalisieren. Pädiatrisch-orientierte Subtypen wie Medulloepitheliom und Ependymom integrieren nun risiko-angepasste Strahlentherapie mit Molekulardiagnostik, verbessern das Fünf-Jahres-Überleben, lassen aber rezidivierte Erkrankung als dringende Forschungspriorität.
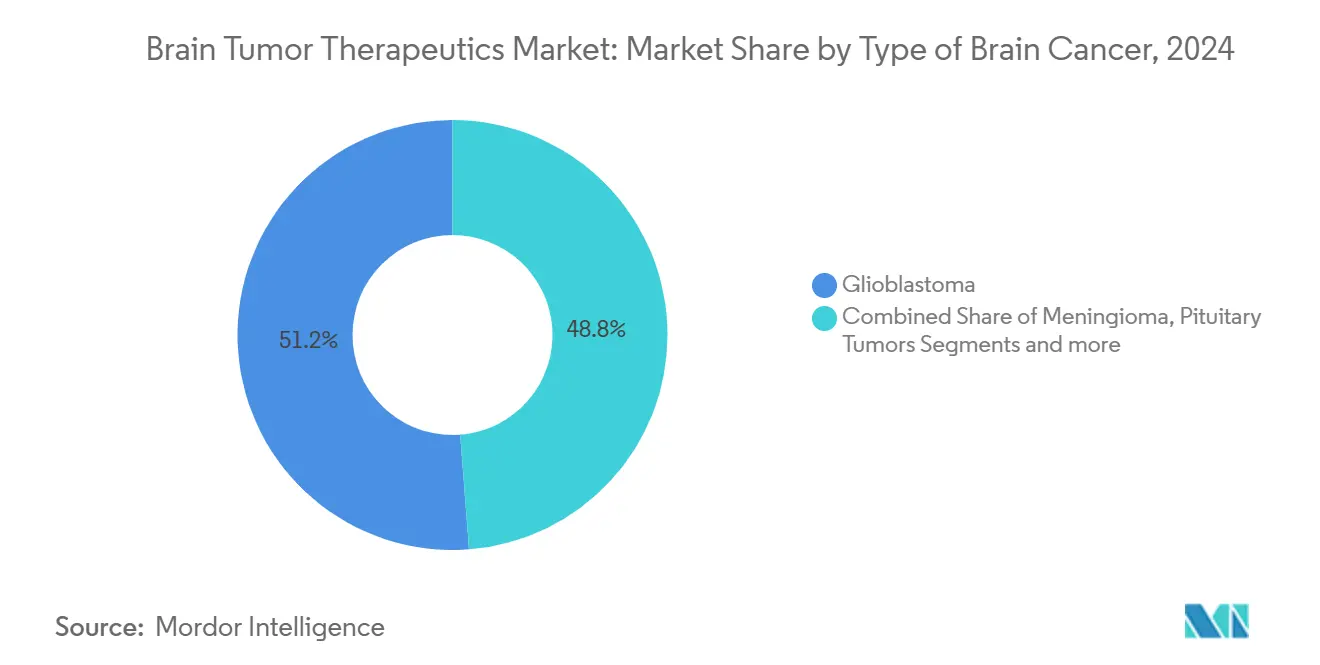
Notiz: Segmentanteile aller einzelnen Segmente bei Berichtskauf verfügbar
Nach Therapie: Zielgerichtete niedermolekulare Substanzen überholen Immuntherapie im Wachstumstempo
Die Immuntherapie kommandierte 32,56% Umsatz im Jahr 2024 und bleibt integral für Tumoren mit hoher Mutationslast. Dennoch positioniert die präzisionsgeleitete Zulassungswelle nun zielgerichtete niedermolekulare Therapie als die am schnellsten wachsende Kategorie mit einer erwarteten CAGR von 8,52%, was den Appetit des Marktes für Gehirntumorbehandlungen auf oral dosierte, biomarker-abgestimmte Wirkstoffe widerspiegelt.
Die Chemotherapie hält als adjuvante oder Rettungstherapie an, doch dosisdichte Regime stehen vor Ersatz, da mutationsspezifische Inhibitoren Erstattung gewinnen. Gen- und Zelltherapien führen kurative Potentiale ein, konfrontieren jedoch Skalierbarkeit und Kosten. Währenddessen erweitern strahlentherapeutische Adjuvante wie BNCT über Kopf- und Halsindikationen hinaus und verstärken multimodale Protokolle.
Nach Verabreichungsweg: Intravenös bleibt dominant inmitten von Verabreichungsinnovation
Das intravenöse Segment deckte 56,34% der Marktgröße für Gehirntumorbehandlungen im Jahr 2024 ab und sollte mit einer CAGR von 8,34% bis 2030 steigen. Kliniker verlassen sich auf IV-Verabreichung für präzise Dosistitration und Echtzeit-Toxizitätsmanagement bei Medikamenten mit engem therapeutischem Index.
Orale zielgerichtete Wirkstoffe skalieren dank verbesserter Permeabilität und Patientenkomfort, während intrathekale und intraventrikuläre Methoden nischige Anwendung bei leptomeningealer Ausbreitung sehen. Konvektionsgestützte Verabreichungsstudien zeigen 100-fach höhere Tumorkonzentrationen versus systemische Infusion, doch technische Komplexität beschränkt sie auf Überweisungszentren.
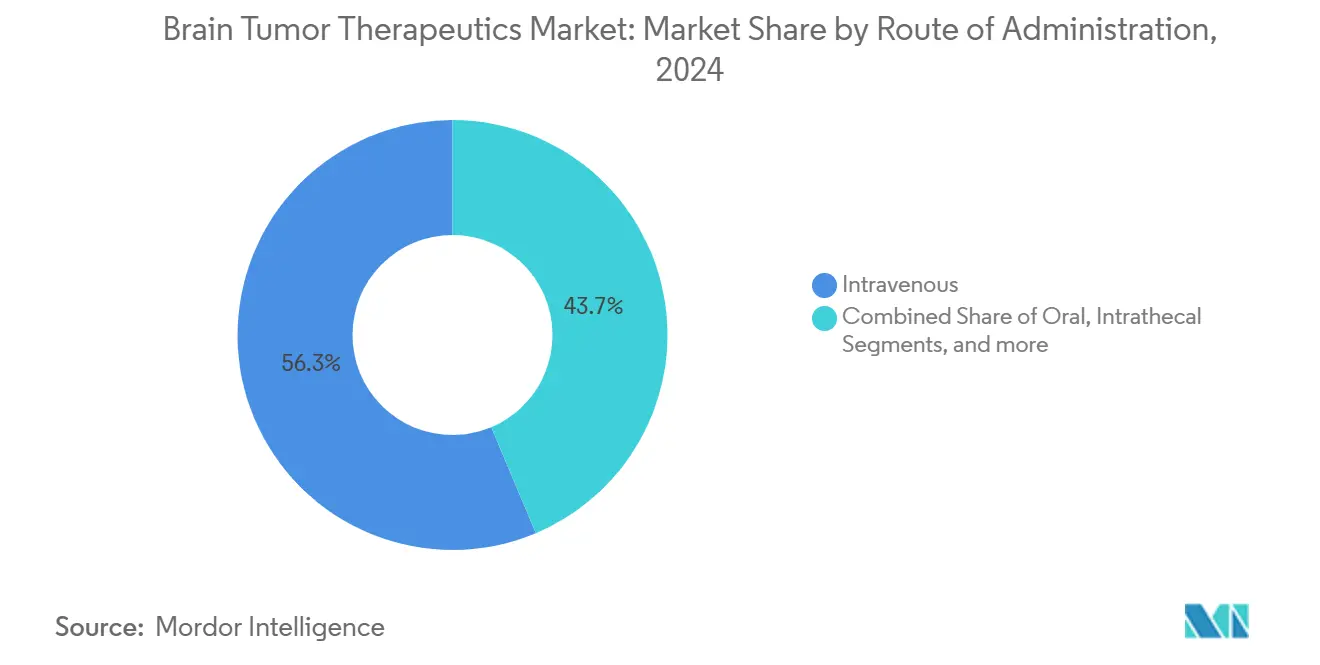
Notiz: Segmentanteile aller einzelnen Segmente bei Berichtskauf verfügbar
Geografieanalyse
Nordamerika behielt 40,34% Marktanteil im Jahr 2024 und genießt unvergleichliche klinische Studiendichte, Genomtest-Adoption und Kostenträger-Mechanismen, die neue Produktaufnahme beschleunigen[2]U.S. Food and Drug Administration, "Drugs@FDA Database," fda.gov. Die große installierte Basis der Region von Gamma Knife und BNCT-Systemen unterstützt Kombinationsregime, und philanthropische Finanzierung vom Biden Cancer Moonshot erhält Translationsforschungsprogramme[3]White House, "Cancer Moonshot Fact Sheet," whitehouse.gov .
Europa folgt mit stetigen Beiträgen, da EMA-zentralisierte Zulassungen den Zugang über Mitgliedstaaten hinweg straffen, und öffentlich-private Partnerschaften Waisen-Tumor-Projekte kofinanzieren. Deutschland, Frankreich und Italien beherbergen kollektiv mehr als 120 laufende interventionelle Hirntumor-Studien, während pan-europäische Register reale Evidenz an Gesundheitstechnologie-Bewertungsagenturen liefern.
Asien-Pazifik, die am schnellsten wachsende Region mit 8,54% CAGR, profitiert von Chinas regulatorischer Modernisierung, wo 60+ innovative Medikamente unter beschleunigten Wegen im Jahr 2024 Freigabe gewannen. Japans frühe BNCT-Adoption macht das Land zu einem regionalen Überweisungszentrum, und australische Institutionen nutzen günstige Ethik-Zeitpläne zur Rekrutierung internationaler Patienten. Verbessernde Erstattungsrahmen in Südkorea und Singapur erweitern weiter den Patientenzugang zu führenden Regimen.
Wettbewerbslandschaft
Der Wettbewerb ist intensiv, aber moderat konzentriert, wobei globale pharmazeutische Marktführer und agile Biotechs um die Sicherung von Erstklassen-Labels wetteifern. Novartis, Roche und Bristol-Myers Squibb nutzen diversifizierte Pipelines und Präzisionsonkologie-Expertise, um das hochwertige Gliom-Franchise zu verankern. Novocure eroberte die Tumor-behandelnde Felder-Nische, nachdem Gesamtüberlebens-Gewinne in mehreren randomisierten Studien demonstriert wurden.
Akquisitionsaktivität ist lebhaft. Mercks 30-Millionen-USD-Kauf von Modifi Biosciences lieferte einen DNA-Schäden-Verstärker, der darauf ausgelegt ist, Temozolomid-Resistenz zu umgehen. Bristol-Myers Squibbs 4,1-Milliarden-USD-Bewegung für RayzeBio sicherte eine Actinium-225-Radiopharmaeutika-Plattform, obwohl globale Isotopen-Engpässe die Versorgungskonsistenz bedrohen[4]Fierce Pharma, "Radiopharmaceutical Supply Headwinds Stall Clinical Programs," fiercepharma.com.
Entwickler jagen auch seltene Tumor-Weißräume, wo Wettbewerbsdichte niedrig bleibt und Regulatoren Prioritätsprüfungsgutscheine anbieten. Unternehmen mit adaptiven Studienfähigkeiten und Patientenvertretungs-Allianzen sichern schnellere Rekrutierung und differenzierte reale Datensätze, die Erstattungsdossiers stärken.
Branchenführer für Gehirntumorbehandlungen
-
Bayer AG
-
F. Hoffmann-La Roche Ltd
-
Eisai Inc.
-
Novartis AG
-
Merck & Co. Inc.
- *Haftungsausschluss: Hauptakteure in keiner bestimmten Reihenfolge sortiert
Jüngste Branchenentwicklungen
- Januar 2025: Novocure berichtete, dass TTFields plus Gemcitabin/nab-Paclitaxel das Gesamtüberleben auf 16,2 Monate in der Phase-3-PANOVA-3-Studie erhöhte, mit einer für Ende 2025 geplanten regulatorischen Einreichung.
- April 2025: Die FDA gewährte eine Untersuchungsgerät-Ausnahme für Alpha DaRT Radium-224-Therapie in einer rezidivierenden Glioblastom-Pilotstudie und führte lokalisierte Alpha-Strahlung in US-Studien ein.
- Januar 2025: Elicio Therapeutics sicherte FDA-Abstimmung über einen ELI-002-Registrationsweg bei Hirnkrebs und brachte eine amphiphil-basierte Immuntherapie in Richtung potentieller Zulassung voran.
- August 2024: Vorasidenib (Voranigo) erhielt FDA-Zulassung für Grad-2-IDH-mutante Gliome und verdoppelte das mediane progressionsfreie Überleben auf 27,7 Monate.
Globaler Marktberichtsumfang für Gehirntumorbehandlungen
Gemäß dem Berichtsumfang entstehen Hirntumoren aus dem abnormalen Wachstum von Krebszellen im Gehirn. Ein Hirntumor ist eine der führenden Todesursachen weltweit. Das Meningiom ist die häufigste Art von Hirntumor und am schwersten zu behandeln, während Behandlungen für Gliome meist bessere Ergebnisse haben. Der Markt für Gehirntumorbehandlungen ist segmentiert nach Art der Hirnkrebserkrankung (Glioblastom, Meningiom, Hypophysentumoren und andere Arten von Hirnkrebserkrankungen), Therapie (Chemotherapie, Immuntherapie, Gentherapie und andere Therapien) und Geografie (Nordamerika, Europa, Asien-Pazifik, Naher Osten und Afrika sowie Südamerika). Der Bericht deckt auch die geschätzten Marktgrößen und Trends für 17 Länder in großen Regionen weltweit ab. Der Bericht bietet den Wert (in USD) für die oben genannten Segmente.
| Glioblastom |
| Meningiom |
| Hypophysentumoren |
| Ependymom |
| Medulloepitheliom |
| Andere seltene Tumoren |
| Chemotherapie |
| Immuntherapie |
| Gen- und Zelltherapie |
| Zielgerichtete niedermolekulare Therapie |
| Tumor-behandelnde Felder (TTF) und Elektrotherapie |
| Strahlentherapie-Adjuvante |
| Oral |
| Intravenös |
| Intrathekal / Intraventrikulär |
| Konvektionsgestützte Verabreichung |
| Nordamerika | Vereinigte Staaten |
| Kanada | |
| Mexiko | |
| Europa | Deutschland |
| Vereinigtes Königreich | |
| Frankreich | |
| Italien | |
| Spanien | |
| Restliches Europa | |
| Asien-Pazifik | China |
| Japan | |
| Indien | |
| Südkorea | |
| Australien | |
| Restlicher Asien-Pazifik-Raum | |
| Naher Osten und Afrika | GCC |
| Südafrika | |
| Restlicher Naher Osten und Afrika | |
| Südamerika | Brasilien |
| Argentinien | |
| Restliches Südamerika |
| Nach Art der Hirnkrebserkrankung | Glioblastom | |
| Meningiom | ||
| Hypophysentumoren | ||
| Ependymom | ||
| Medulloepitheliom | ||
| Andere seltene Tumoren | ||
| Nach Therapie | Chemotherapie | |
| Immuntherapie | ||
| Gen- und Zelltherapie | ||
| Zielgerichtete niedermolekulare Therapie | ||
| Tumor-behandelnde Felder (TTF) und Elektrotherapie | ||
| Strahlentherapie-Adjuvante | ||
| Nach Verabreichungsweg | Oral | |
| Intravenös | ||
| Intrathekal / Intraventrikulär | ||
| Konvektionsgestützte Verabreichung | ||
| Geografie | Nordamerika | Vereinigte Staaten |
| Kanada | ||
| Mexiko | ||
| Europa | Deutschland | |
| Vereinigtes Königreich | ||
| Frankreich | ||
| Italien | ||
| Spanien | ||
| Restliches Europa | ||
| Asien-Pazifik | China | |
| Japan | ||
| Indien | ||
| Südkorea | ||
| Australien | ||
| Restlicher Asien-Pazifik-Raum | ||
| Naher Osten und Afrika | GCC | |
| Südafrika | ||
| Restlicher Naher Osten und Afrika | ||
| Südamerika | Brasilien | |
| Argentinien | ||
| Restliches Südamerika | ||
Im Bericht beantwortete Schlüsselfragen
Wie hoch ist der aktuelle Wert des Marktes für Gehirntumorbehandlungen?
Der Markt generierte 3,19 Milliarden USD im Jahr 2025 und ist auf Kurs, 4,67 Milliarden USD bis 2030 zu erreichen, mit einem Wachstum von 7,89% CAGR.
Welche Krebsart trägt den meisten Umsatz bei?
Das Glioblastom trägt den höchsten Umsatz bei und macht 51,23% des Marktes 2024 aus und expandiert mit einer CAGR von 8,45% bis 2030.
Warum gewinnen zielgerichtete niedermolekulare Therapien an Tempo?
Biomarker-abgestimmte niedermolekulare Substanzen wie IDH-Inhibitoren bieten orale Bequemlichkeit und verbesserte Wirksamkeit und machen sie zur am schnellsten wachsenden Therapieklasse mit 8,52% CAGR.
Welche Region bietet die schnellste Wachstumschance?
Asien-Pazifik ist die am schnellsten wachsende Region mit 8,54% CAGR, unterstützt von beschleunigten Zulassungen in China und BNCT-Adoption in Japan.
Welche Faktoren begrenzen Behandlungserfolg trotz neuer Zulassungen?
Hohe Therapiekosten, Blut-Hirn-Schranken-Penetrationsgrenzen und Versorgungseinschränkungen für Radioisotope beschränken breiteren Patientenzugang und konsistente Behandlungsergebnisse.
Wie konzentriert ist die Wettbewerbslandschaft?
Der Markt erhält einen Konzentrationsscore von 6, was moderate Dominanz der Top-5-Unternehmen anzeigt, während Raum für innovative Biotechs bleibt, Anteile zu sichern.
Seite zuletzt aktualisiert am:



