Taille et part de marché des tests de validité d'échantillons
Analyse du marché des tests de validité d'échantillons par Mordor Intelligence
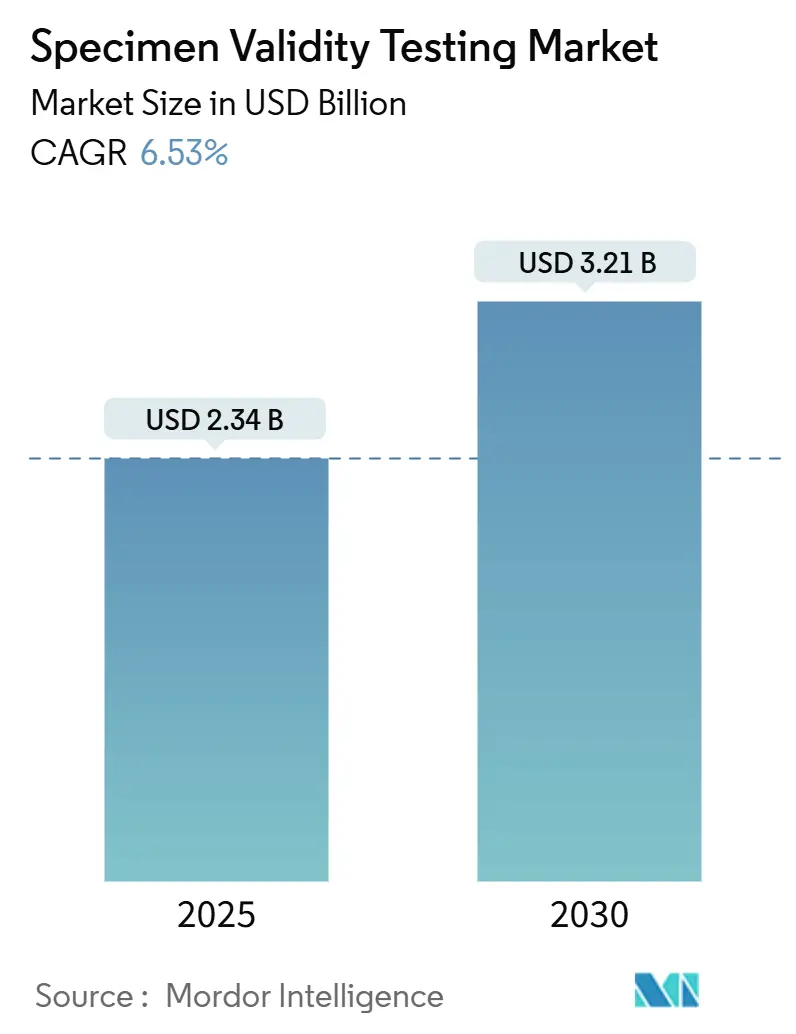
La taille du marché des tests de validité d'échantillons est évaluée à 2,34 milliards USD en 2025 et devrait atteindre 3,21 milliards USD d'ici 2030, progressant à un TCAC de 6,53 %. Cette trajectoire reflète le renforcement des mandats de sécurité au travail, l'adoption accélérée des plateformes de tests au point de service (POC), et les mises à niveau technologiques qui détectent les tentatives de falsification sophistiquées. Les employeurs dans les transports, l'énergie et la santé continuent d'élargir la couverture des tests, tandis que les mises à jour gouvernementales-telles que l'expansion du panel fédéral de janvier 2025 qui inclut désormais le fentanyl et le norfentanyl-élèvent la barre d'intégrité pour tous les laboratoires. L'utilisation croissante de la télésanté un également ouvert un nouveau canal de collecte à distance, stimulant la demande pour des dispositifs inviolables et des analyses pilotées par IA qui vérifient l'intégrité des échantillons en temps réel. Bien que les matrices non urinaires gagnent en popularité, le marché des tests de validité d'échantillons reste soutenu par les programmes urinaires à haut volume qui dominent encore les environnements réglementés.
Points clés du rapport
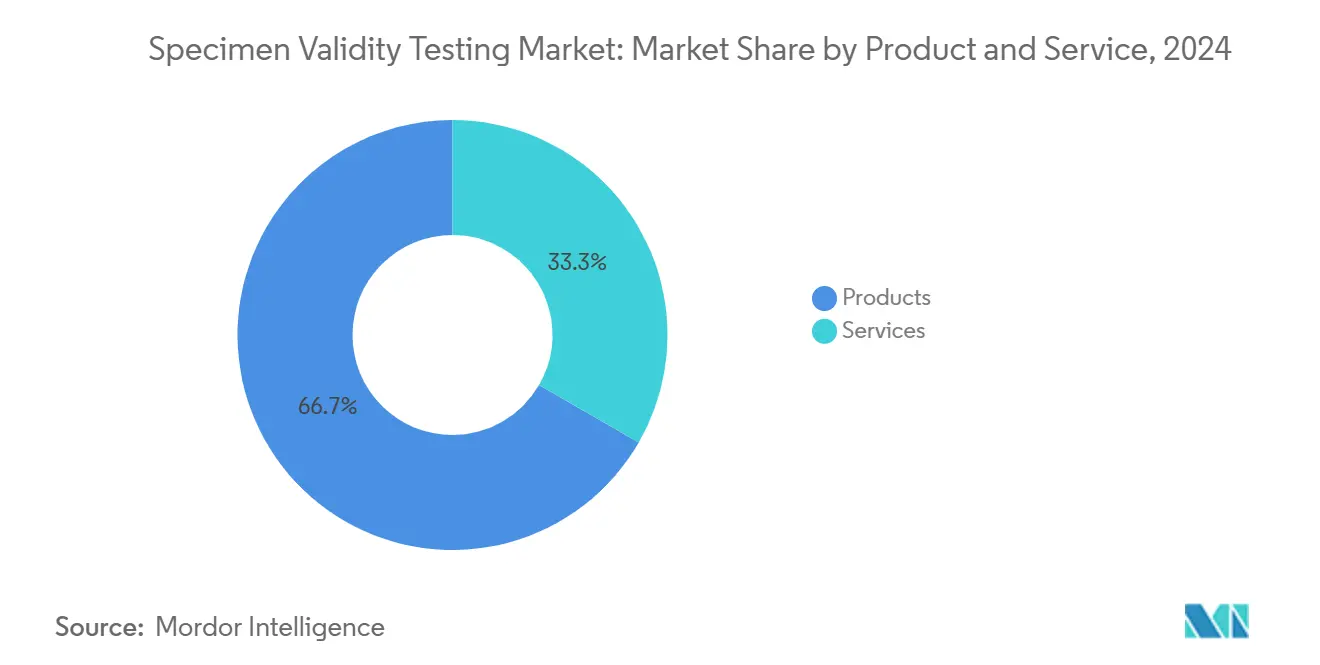
- Par produit et service, les produits consommables ont maintenu 66,67 % de part de revenus en 2024, tandis que les services devraient afficher le TCAC le plus rapide de 7,21 % jusqu'en 2030.
- Par type, les tests de laboratoire ont détenu 59,65 % de la part de marché des tests de validité d'échantillons en 2024, tandis que les plateformes POC devraient s'étendre à un TCAC de 7,29 % jusqu'en 2030.
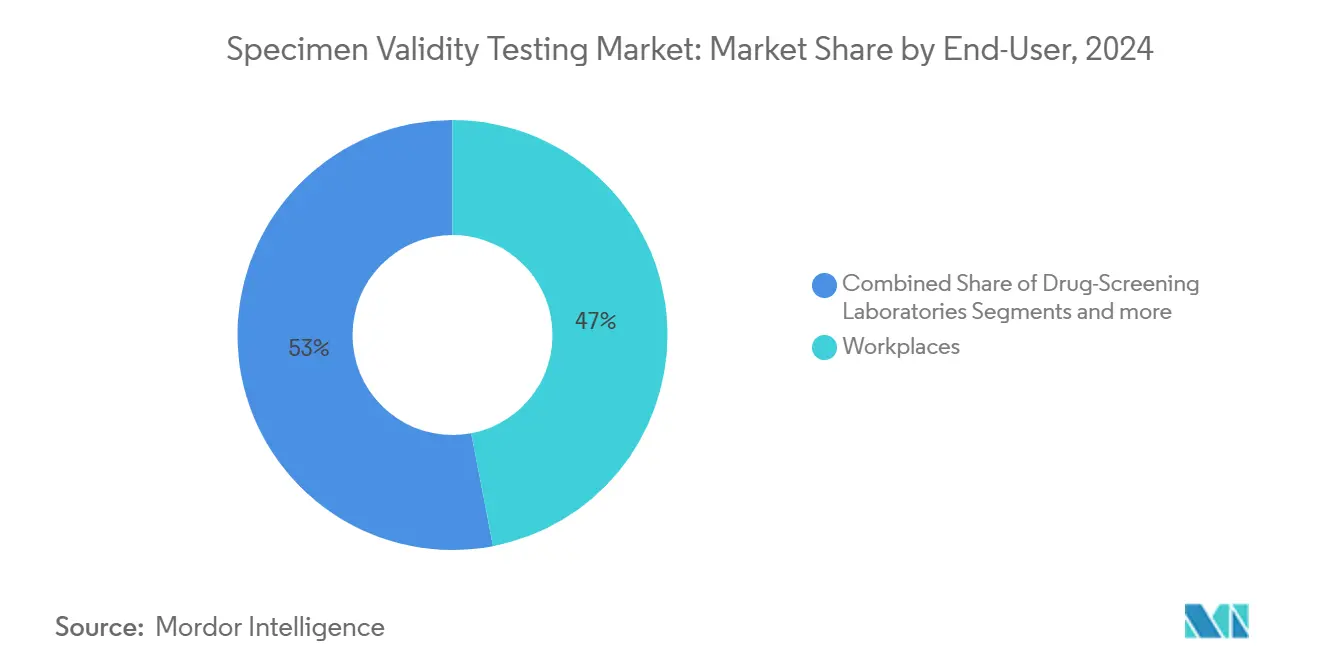
- Par utilisateur final, les programmes en milieu de travail ont mené avec 46,98 % de part de revenus en 2024 ; les laboratoires de dépistage de drogues enregistrent le TCAC projeté le plus élevé de 7,33 % jusqu'en 2030.
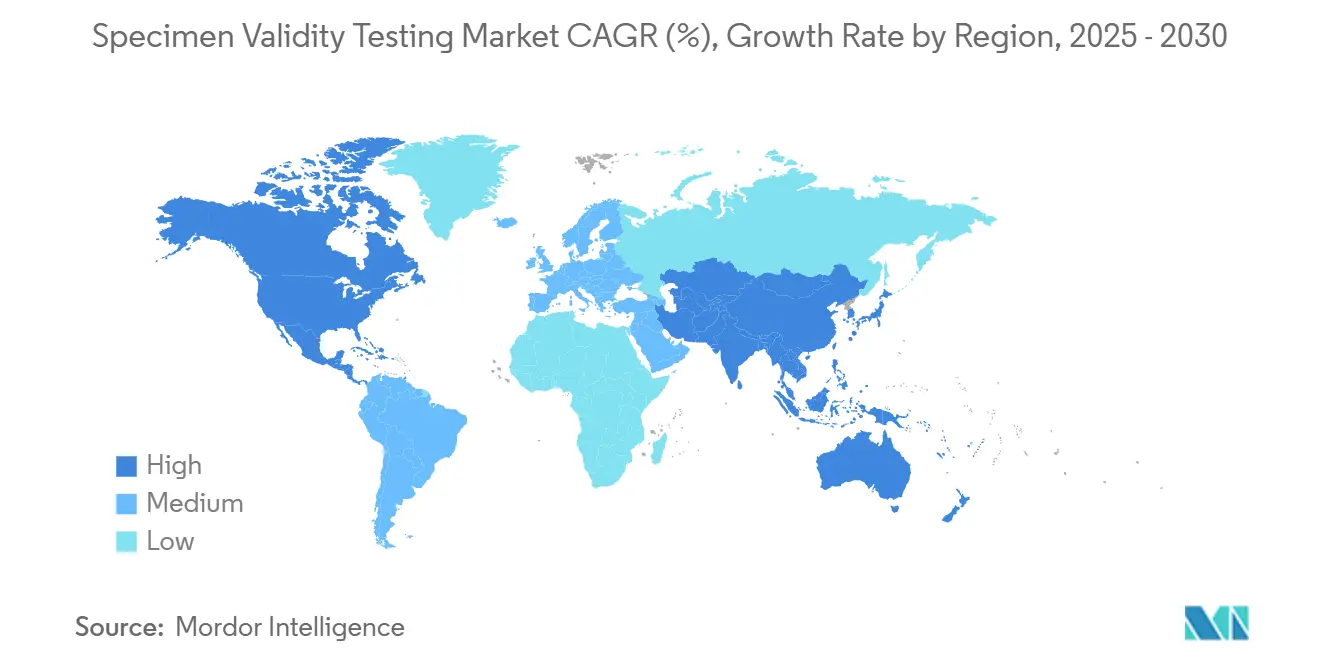
- Par géographie, l'Amérique du Nord un commandé 41,34 % de part de la taille du marché des tests de validité d'échantillons en 2024 ; l'Asie-Pacifique devrait croître à un TCAC de 7,41 % de 2025 à 2030.
Tendances et insights du marché mondial des tests de validité d'échantillons
Analyse d'impact des moteurs
| Moteur | (~) % Impact sur les prévisions TCAC | Pertinence géographique | Chronologie d'impact |
|---|---|---|---|
| Mandats croissants de dépistage de drogues en milieu de travail | +1.2% | Mondial, concentré en Amérique du Nord et UE | Moyen terme (2-4 ans) |
| Adoption rapide des dispositifs SVT POC | +0.9% | Amérique du Nord et Asie-Pacifique | Court terme (≤ 2 ans) |
| Expansion de la télésanté stimulant les kits à domicile | +0.7% | Amérique du Nord et UE | Moyen terme (2-4 ans) |
| Algorithmes d'apprentissage automatique pour la détection de falsification en direct | +0.6% | Mondial, mené par l'Amérique du Nord | Long terme (≥ 4 ans) |
| Légalisation du cannabis stimulant les Panneaux différenciés | +0.5% | Amérique du Nord, s'étendant à l'UE | Court terme (≤ 2 ans) |
| Sécurité de la chaîne d'approvisionnement renforçant les contrôles stériles | +0.4% | Mondial | Moyen terme (2-4 ans) |
| Source: Mordor Intelligence | |||
Mandats croissants de dépistage de drogues en milieu de travail
Les régulateurs sur six continents renforcent les règles de sécurité d'entreprise, poussant les employeurs à vérifier non seulement la présence de drogues mais l'authenticité de chaque échantillon. Les directives alignées sur l'OSHA aux États-Unis, le Règlement sur le transport des marchandises dangereuses du Canada, et l'ordre de test obligatoire pour le pétrole et le gaz du Ministère de la Main-d'œuvre d'Oman soulignent un mouvement collectif vers des vérifications de validité d'échantillons plus strictes. Les grandes conglomérats intègrent de plus en plus les logiciels de chaîne de possession et la surveillance des Officiers de Révision Médicale (ORM) dans les procédures opérationnelles standard, atténuant le risque de litige après les accidents. Le multiplicateur de demande résultant élève les ventes récurrentes de bandes de température, de dosages d'oxydants, et de systèmes de garde numérique [1]General Civil Aviation Authority, ACCEPTABLE MEANS OF COMPLIANCE,
gcaa.gov.ae.
Adoption rapide des dispositifs SVT POC
Les analyseurs portables nouvellement autorisés complètent désormais les dépistages d'adultérants en moins de six minutes, répondant à la norme d'' immédiateté ' requise dans les enquêtes post-incident. L'autorisation de la Food and Drug Administration (FDA) américaine pour les dosages de fentanyl sur site un établi un précédent pour intégrer les vérifications de validité dans des coupelles POC en une étape. Les employeurs valorisent la réduction des temps d'arrêt, tandis que les laboratoires voient moins d'échantillons rejetés, raccourcissant les cycles de facturation. Les fournisseurs répondent avec des lecteurs modulaires qui impriment des rapports prêts pour la conformité, renforçant les revenus récurrents de consommables.
Expansion de la télésanté stimulant les kits SVT à domicile
La gestion à distance des patients dépendants aux opioïdes et de gestion de la douleur exige des kits d'auto-collecte qui protègent contre la substitution. Les essais académiques montrent des taux d'achèvement supérieurs à 80 % pour les soumissions d'urine à distance lorsque les paramètres de validité-température, pH, créatinine-sont intégrés dans les dispositifs de collecte. Les assureurs santé exigent désormais une preuve documentaire de validité avant de rembourser les codes de haute complexité, poussant les cliniques à adopter des tubes de transport inviolables et des capteurs de température Bluetooth.
Algorithmes d'apprentissage automatique pour la détection de falsification en direct
Les laboratoires de recherche déploient des modèles d'apprentissage profond qui comparent les spectres de séries temporelles, signalant les anomalies impossibles à voir à travers des dosages à paramètre unique. Les études de validation précoces atteignent une précision de 95 %+ dans l'identification d'urine synthétique ou de pics d'oxydants. Le déploiement commercial est prêt à réduire les taux de faux négatifs et à alléger le fardeau d'interprétation sur les ORM, donnant aux fournisseurs de réactifs de spectrométrie de masse compatibles un avantage concurrentiel [2]Yi-Ching Lin, PS2MS: un Deep Learning-Based Prediction System for Identifying New Psychoactive Substances Using Mass Spectrometry,
ACS Publications, pubs.acs.org.
Analyse d'impact des contraintes
| Contrainte | (~) % Impact sur les prévisions TCAC | Pertinence géographique | Chronologie d'impact |
|---|---|---|---|
| Sensibilisation limitée parmi les petites et moyennes cliniques | -0.8% | Mondial, plus aiguë en Asie-Pacifique et MEA | Court terme (≤ 2 ans) |
| Passage vers des matrices non urinaires | -0.6% | Amérique du Nord et UE | Moyen terme (2-4 ans) |
| Contraintes de confidentialité des données sur les plateformes biométriques | -0.4% | UE et Amérique du Nord | Long terme (≥ 4 ans) |
| Pénuries sporadiques de réactifs et pics de matières premières | -0.3% | Mondial | Court terme (≤ 2 ans) |
| Source: Mordor Intelligence | |||
Sensibilisation limitée parmi les petites et moyennes cliniques
Les petits fournisseurs de soins de santé sous-estiment souvent la responsabilité liée aux échantillons invalides. Les enquêtes soulignent que 59 % des obstacles à la mise en œuvre du point de service sont liés à la formation et à l'assurance qualité, laissant de nombreuses cliniques sans vérification de température ou contrôles de gravité spécifique. Les politiques de remboursement refusent maintenant les demandes manquant de documentation de validité, mais les lacunes de connaissances persistent, ralentissant l'adoption [3]Blue Cross Blue Shield of Michigan, Drug Testing in Douleur Gestion and Substance Use Disorder Treatment,
bcbsm.com.
Passage vers des matrices non urinaires réduisant la demande SVT
L'autorisation fédérale des tests de fluide oral pour les employés gouvernementaux un incité les entreprises privées à adopter la salive comme matrice principale, ce qui réduit le risque de falsification et donc le besoin de Panneaux de validité urinaire multi-paramètres. Les prévisions suggèrent que 30 % des tests fédéralement réglementés pourraient migrer vers le fluide oral dans les quatre ans, réduisant le potentiel de croissance pour les consommables axés sur l'urine.
Analyse par segment
Par produit et service : les produits conservent l'échelle, les services accélèrent
Les produits ont ancré 66,67 % des revenus 2024, soutenus par la nature consommable des kits de dosage, réactifs oxydants, standards de créatinine, et coupelles de collecte à usage unique. Les bandes indicatrices de température seules ont généré un cycle de remplacement à haute vélocité, en particulier dans les grandes entreprises de logistique et d'énergie. Les services, cependant, affichent un TCAC de 7,21 % jusqu'en 2030 alors que les employeurs externalisent l'interprétation des résultats et les audits de conformité aux consultants ORM et laboratoires spécialisés. Les environnements médico-légaux favorisent les offres groupées qui fusionnent la gestion de la chaîne de possession avec les analyses d'apprentissage automatique. La taille du marché des tests de validité d'échantillons pour les services devrait atteindre 1,24 milliard USD d'ici 2030, maintenant l'élan malgré la domination des consommables.
La vague de services profite également de la médecine de collecte à distance. Les plateformes de télésanté contractent des laboratoires tiers pour vérifier la température et les niveaux d'oxydants des échantillons à l'arrivée, payant des frais premium pour l'adjudication le jour même. La demande bondit pour les examens ORM virtuels dans les programmes d'emploi transfrontaliers, élargissant les revenus adressables et solidifiant le marché des tests de validité d'échantillons comme une solution holistique plutôt qu'un seul vertical de produit.
Par type : tests de laboratoire dominants, POC gagne en vitesse
Les flux de travail de laboratoire ont détenu 59,65 % de part en 2024. Les laboratoires centralisés manient des systèmes de chromatographie liquide-spectrométrie de masse en tandem (LC-MS/MS) qui analysent la température, la gravité spécifique, la créatinine, le pH, et les oxydants avec une précision réglementaire. Cette infrastructure soutient le leadership de part de marché des tests de validité d'échantillons des grands laboratoires de référence. Pourtant les formats POC avancent de 7,29 % TCAC, propulsés par des photomètres portables et des coupelles immunochromatographiques qui vérifient trois paramètres de validité ou plus en minutes. La taille du marché des tests de validité d'échantillons liée aux plateformes POC devrait grimper à 1,38 milliard USD d'ici 2030 alors que la précision des dispositifs approche les standards de laboratoire.
Les secteurs à haut risque comme la construction déploient maintenant des analyseurs POC durcis sur les chantiers pour les tests post-incident, réduisant les temps d'arrêt. Pendant ce temps, les modèles hybrides voient les échantillons d'abord dépistés par des dispositifs POC et seuls les positifs-avec toute anomalie de validité signalée-envoyés aux laboratoires, optimisant la distribution de charge de travail.
Par utilisateur final : les lieux de travail mènent, les laboratoires accélèrent
Les programmes d'entreprise ont représenté 46,98 % des revenus 2024, cimentant leur rôle de consommateur principal de consommables de validité. Les employeurs des transports, pétrole et gaz, et secteur public maintiennent des tests obligatoires pré-emploi et aléatoires, assurant un volume stable. Les laboratoires de dépistage de drogues augmentent le plus rapidement à 7,33 % TCAC, reflétant la consolidation qui tire les volumes de petites cliniques vers des centres à haut débit.
Les cliniques de gestion de la douleur, sous surveillance des payeurs, externalisent de plus en plus vers des installations spécialisées capables de fournir des métriques de validité complètes. Les agences de justice pénale, une autre niche critique, exigent la traçabilité de la chaîne de possession et ont commencé à demander des journaux de température lisibles par machine, approfondissant le rôle des plateformes de validité avancées.
Note: Parts de segments de tous les segments individuels disponibles à l'achat du rapport
Analyse géographique
L'Amérique du Nord un conservé 41,34 % des revenus en 2024 et demeure le précurseur réglementaire pour le marché des tests de validité d'échantillons. Le Département de la Santé et des Services sociaux exige que chaque échantillon d'urine réglementé documente la température (32-38 °C), le pH (4,5-8,0), la gravité spécifique (≥1,003), et la créatinine (≥20 mg/dL) immédiatement après la collecte SAMHSA. La révision du panel de janvier 2025, qui un ajouté le fentanyl et le norfentanyl, un encore accentué le besoin des laboratoires pour une confirmation de validité précise pour éviter les faux négatifs sous les nouveaux seuils d'analytes Federal Register. Les mandats parallèles du Département des Transports s'appliquent à environ 10 millions de travailleurs sensibles à la sécurité, garantissant des volumes de test élevés. Le cadre orienté vie privée du Canada réduit les tests aléatoires mais met l'accent sur les programmes de fluide oral qui s'appuient encore sur la température et la documentation de chaîne de possession pour la défendabilité.
L'Asie-Pacifique affiche le TCAC le plus rapide de 7,41 % jusqu'en 2030, propulsé par les usines multinationales en Chine et en Inde qui intègrent les meilleures pratiques de l'Administration de la Sécurité et Santé au Travail (OSHA) américaine dans les opérations locales. Les géants du diagnostic mondial ont ouvert des centres régionaux pour fournir des kits de dosage et offrir des services ORM dans les langues natives. La conformité du commerce transfrontalier pousse les entreprises à adopter des systèmes de chaîne de possession de style américain, donnant au marché des tests de validité d'échantillons une nouvelle échelle. Les gouvernements régionaux étudient les statuts de tests de drogues obligatoires, particulièrement dans les transports et l'exploitation minière, ce qui intégrerait davantage les vérifications d'intégrité d'échantillons.
L'Europe offre une réglementation fragmentée. Les opérateurs ferroviaires allemands appliquent des règles de validité d'échantillons strictes modelées sur les directives fédérales américaines, alors que la France limite les tests aux rôles sensibles à la sécurité et impose des filtres de confidentialité plus stricts. Le Règlement sur les Dispositifs de Diagnostic In Vitro (RDIV) de l'UE impose des obligations de performance et de surveillance post-marché sur les dispositifs de validité entrant dans le bloc, élevant les barrières d'entrée tout en standardisant la qualité. Les employeurs pan-européens s'appuient ainsi sur des systèmes de collecte marqués CE qui intègrent des sceaux d'intégrité à code-barres et des journaux de garde cloud.
Le Moyen-Orient et l'Afrique suivent les standards internationaux de contractation pétrolière et gazière. Les régulateurs de l'aviation du CCG exigent des vérifications de validité supervisées par ORM, avec des protocoles de chaîne de possession reflétant les directives SAMHSA américaines. Les maisons minières d'Afrique du Sud s'associent avec des laboratoires mondiaux pour répondre aux attentes des acheteurs pour des métriques de test à haute intégrité. L'Amérique du Sud est menée par le Brésil, où la Loi 13.103/15 oblige les conducteurs professionnels à subir des évaluations toxicologiques périodiques qui incluent la documentation de validité d'échantillons ; la popularité des tests capillaires néanmoins exige des protocoles de validation croisée pour confirmer l'authenticité. Le secteur automobile en expansion de l'Argentine importe les directives DOT américaines pour satisfaire les partenaires de chaîne d'approvisionnement.
Paysage concurrentiel
Le marché des tests de validité d'échantillons présente une fragmentation modérée. Abbott, Thermo Fisher Scientific, Laboratory Corporation of America, Quest Diagnostics, et Siemens Healthineers représentent collectivement une portion décente du chiffre d'affaires mondial. Les avantages d'échelle découlent de portefeuilles intégrés dosage-à-analyses et de réseaux logistiques étendus. La plateforme iCUP d'Abbott intègre maintenant la surveillance de température en temps réel et des bandes oxydantes, regroupant la validité avec les dépistages de drogues rapides Abbott. Quest Diagnostics un élargi son empreinte internationale à 80+ nations, offrant des tableaux de bord de chaîne de possession basés sur le cloud qui rationalisent la conformité multinationale Quest Diagnostics.
La différenciation technologique anime la concurrence actuelle. Les partenariats entre laboratoires de référence et fournisseurs IA livrent des classificateurs de falsification d'apprentissage automatique, élevant l'adhésion des services. Siemens Healthineers pilote des flux de travail de spectrométrie de masse liés au cloud qui signalent les ratios créatinine-gravité spécifique atypiques en quasi-temps réel, réduisant les charges de rapport sur les ORM. Pendant ce temps, les fournisseurs spécialisés comme Labcon mettent l'accent sur les coupelles de collecte de qualité médicale conformes IATA, adressant les préoccupations de stérilité de chaîne d'approvisionnement Labcon.
Les start-ups se concentrent sur les innovations de salive et micro-échantillonnage-domaines prêts à éroder les volumes d'urine mais nécessitant encore une preuve d'identité du donneur et d'intégrité d'échantillon. Les acteurs établis couvrent en acquérant ou licenciant ces technologies, maintenant les revenus indépendamment des changements de matrice. Les fournisseurs régionaux en Asie-Pacifique courtisent les contrats multinationaux en offrant un support ORM bilingue et un suivi cloud clé en main, défiant la dominance nord-américaine.
Leaders de l'industrie des tests de validité d'échantillons
Abbott
Thermo Fisher Scientific
LabCorp
Healgen Scientific LLC
Premier Biotech, Inc.
- *Avis de non-responsabilité : les principaux acteurs sont triés sans ordre particulier
Développements récents de l'industrie
- Janvier 2025 : Le Département américain de la Santé et des Services sociaux un mis à jour les Directives Obligatoires, ajoutant le fentanyl et le norfentanyl tout en supprimant la MDMA et la MDA, obligeant les laboratoires à ajuster les flux de travail de validité Federal Register.
- Décembre 2024 : BD et Babson Diagnostics ont introduit la technologie de micro-échantillonnage de sang capillaire, étendant les concepts de tests de validité dans la collecte de sang à petit volume BD.
- Août 2024 : La FDA un autorisé le premier dépistage d'urine de fentanyl POC sur l'analyseur RYAN, catalysant la vérification de validité sur site FDA.
- Février 2024 : SAMHSA un publié un Manuel de Collecte d'Échantillons d'Urine révisé détaillant les seuils de validité mis à jour et les étapes de détection de falsification SAMHSA.
Portée du rapport mondial sur le marché des tests de validité d'échantillons
Selon la portée du rapport, les tests de validité d'échantillons (SVT) sont les tests de dépistage pour les échantillons d'urine pour détecter toute falsification, dilution, ou substitution. Les SVT fournissent des informations critiques concernant la fiabilité et la précision des résultats de tests de drogues aux cliniciens, et ils valident également que l'échantillon d'urine testé est un échantillon d'urine humaine valide. Le marché des tests de validité d'échantillons est segmenté par type de drogue (médicaments antibactériens, médicaments antifongiques, médicaments antiviraux, et autres médicaments), indication (infections du flux sanguin, infections du tractus urinaire, infections du site chirurgical, pneumonie, et autres indications), et géographie (Amérique du Nord, Europe, Asie-Pacifique, Moyen-Orient et Afrique, et Amérique du Sud). Le rapport de marché couvre également les tailles de marché estimées et les tendances pour 17 pays différents à travers les principales régions mondiales. Le rapport offre la valeur (en USD) pour les segments ci-dessus.
| Produits | Kits de dosage |
| Réactifs et calibrateurs | |
| Jetables | |
| Services |
| Tests de laboratoire |
| Tests rapides et POC |
| Lieux de travail |
| Systèmes d'application de la loi et de justice pénale |
| Laboratoires de dépistage de drogues |
| Centres de gestion de la douleur |
| Autres |
| Amérique du Nord | États-Unis |
| Canada | |
| Mexique | |
| Europe | Allemagne |
| Royaume-Uni | |
| France | |
| Italie | |
| Espagne | |
| Reste de l'Europe | |
| Asie-Pacifique | Chine |
| Japon | |
| Inde | |
| Australie | |
| Corée du Sud | |
| Reste de l'Asie-Pacifique | |
| Moyen-Orient et Afrique | CCG |
| Afrique du Sud | |
| Reste du Moyen-Orient et Afrique | |
| Amérique du Sud | Brésil |
| Argentine | |
| Reste de l'Amérique du Sud |
| Par produit et service | Produits | Kits de dosage |
| Réactifs et calibrateurs | ||
| Jetables | ||
| Services | ||
| Par type | Tests de laboratoire | |
| Tests rapides et POC | ||
| Par utilisateur final | Lieux de travail | |
| Systèmes d'application de la loi et de justice pénale | ||
| Laboratoires de dépistage de drogues | ||
| Centres de gestion de la douleur | ||
| Autres | ||
| Par géographie | Amérique du Nord | États-Unis |
| Canada | ||
| Mexique | ||
| Europe | Allemagne | |
| Royaume-Uni | ||
| France | ||
| Italie | ||
| Espagne | ||
| Reste de l'Europe | ||
| Asie-Pacifique | Chine | |
| Japon | ||
| Inde | ||
| Australie | ||
| Corée du Sud | ||
| Reste de l'Asie-Pacifique | ||
| Moyen-Orient et Afrique | CCG | |
| Afrique du Sud | ||
| Reste du Moyen-Orient et Afrique | ||
| Amérique du Sud | Brésil | |
| Argentine | ||
| Reste de l'Amérique du Sud | ||
Questions clés auxquelles répond le rapport
Quelle est la taille actuelle du marché des tests de validité d'échantillons ?
La taille du marché des tests de validité d'échantillons s'élève à 2,34 milliards USD en 2025 et devrait atteindre 3,21 milliards USD d'ici 2030.
Quelle région domine le marché des tests de validité d'échantillons ?
L'Amérique du Nord mène avec 41,34 % de part de revenus en 2024 en raison des exigences fédérales strictes en milieu de travail.
Pourquoi les services croissent-ils plus rapidement que les produits ?
La complexité croissante des protocoles, les tests à distance, et le besoin d'interprétation experte d'Officier de Révision Médicale stimulent un TCAC de 7,21 % pour les services.
Comment l'IA influence-t-elle les tests de validité d'échantillons ?
Les modèles d'apprentissage automatique détectent maintenant les modèles de falsification sophistiqués avec une précision de 95 %+, améliorant la fiabilité de laboratoire et la différenciation concurrentielle.
Quel impact ont les matrices non urinaires sur la croissance du marché ?
Le passage vers les fluides oraux et les tests capillaires réduit la demande pour les consommables de validité d'urine traditionnels mais ouvre des opportunités pour de nouveaux outils de vérification d'intégrité adaptés aux matrices alternatives.
Quel segment d'utilisateur final s'étend le plus rapidement ?
Les laboratoires de dépistage de drogues, soutenus par les tendances de consolidation et d'externalisation, devraient croître à un TCAC de 7,33 % jusqu'en 2030.
Dernière mise à jour de la page le:



