Taille et part du marché de la technologie d'amplification isotherme d'acides nucléiques
Analyse du marché de la technologie d'amplification isotherme d'acides nucléiques par Mordor Intelligence
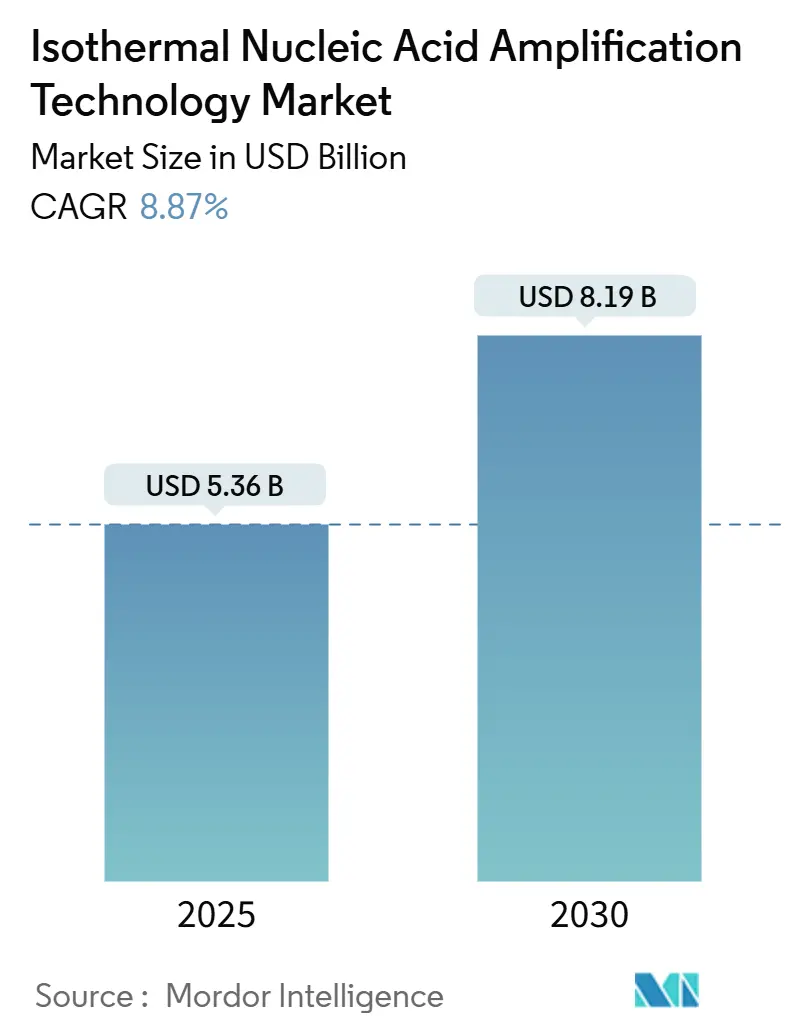
La taille du marché de la technologie d'amplification isotherme d'acides nucléiques est estimée à 5,36 milliards USD en 2025, et devrait atteindre 8,19 milliards USD d'ici 2030, à un TCAC de 8,87 % durant la période de prévision (2025-2030).
La croissance est alimentée par l'amplification à température constante, qui élimine le besoin de thermocycleurs encombrants et prend en charge les tests rapides au point de soins. Les hôpitaux déploient des plateformes INAAT dans les unités d'urgence pour réduire le délai d'obtention des résultats de plusieurs heures à quelques minutes, tandis que les fournisseurs de réactifs bénéficient de ventes de consommables régulières à forte marge. Les fabricants intègrent la microfluidique, les réactifs lyophilisés et la détection colorimétrique qui réduisent les coûts par test et élargissent l'utilisation dans des environnements non-laboratoires. L'adoption en Asie-Pacifique s'accélère grâce aux approbations d'appareils simplifiées qui raccourcissent le délai de mise sur le marché, tandis que l'Amérique du Nord mène en termes de revenus grâce aux cadres de remboursement établis.
Points clés du rapport
- Par technologie, l'amplification isotherme médiée par boucle (LAMP) a mené avec 44,34 % de part de revenus en 2024 et devrait enregistrer un TCAC de 13,36 % jusqu'en 2030.
- Par produit, les réactifs et consommables ont représenté 63,56 % des revenus de 2024, tandis que les instruments devraient croître à un TCAC de 11,24 % jusqu'en 2030.
- Par application, les tests de maladies infectieuses ont détenu 53,56 % de la part du marché de la technologie d'amplification isotherme d'acides nucléiques en 2024 ; l'oncologie et la biopsie liquide devraient croître à un TCAC de 16,11 %.
- Par utilisateur final, les hôpitaux et laboratoires de référence ont détenu une part de 56,78 % en 2024 ; les sites de soins au point de service devraient croître à un TCAC de 11,64 %.
- Par région, l'Amérique du Nord a capturé 35,67 % des revenus en 2024, tandis que l'Asie-Pacifique devrait enregistrer un TCAC de 15,64 % jusqu'en 2030.
Tendances et aperçus du marché mondial de la technologie d'amplification isotherme d'acides nucléiques
Analyse de l'impact des moteurs
| Moteur | (~) % Impact sur les prévisions de TCAC | Pertinence géographique | Échéancier d'impact |
|---|---|---|---|
| Adoption des maladies infectieuses au point de soins | +2.1% | Mondial, avec gains précoces en Amérique du Nord et UE | Moyen terme (2-4 ans) |
| Population vieillissante et fardeau des maladies chroniques | +1.8% | Mondial, concentré dans les marchés développés | Long terme (≥ 4 ans) |
| Changement de flux de travail de PCR vers INAAT | +1.5% | Noyau APAC, débordement vers MEA | Moyen terme (2-4 ans) |
| Économies de coût par test plus faibles | +1.3% | Mondial, accéléré dans les marchés émergents | Court terme (≤ 2 ans) |
| Cartouches microfluidiques alimentées par batterie | +0.9% | Amérique du Nord et UE, expansion vers APAC | Long terme (≥ 4 ans) |
| Spécificité des tests améliorée par CRISPR | +0.7% | Mondial, mené par les institutions de recherche | Long terme (≥ 4 ans) |
| Source: Mordor Intelligence | |||
Adoption des maladies infectieuses au point de soins
Les services d'urgence s'appuient désormais sur des panneaux respiratoires INAAT qui fournissent des réponses de qualité laboratoire en quelques minutes, améliorant le débit des patients et la gestion des antibiotiques. L'autorisation FDA du Xpert HCV de Cepheid en juin 2024 permet un diagnostic de l'hépatite C lors de la même visite à partir d'un échantillon de sang du bout du doigt, une étape importante qui élimine la perte de suivi sur plusieurs visites.[1]U.S. Food and Drug Administration, "FDA Authorizes First Point-of-Care Hepatitis C Test," fda.gov La précision des résultats reste équivalente à la PCR tandis que les réactions à température constante conviennent aux appareils portables alimentés par batterie, utiles dans des environnements aux ressources limitées.
Population vieillissante et fardeau des maladies chroniques
Les populations de plus de 65 ans nécessitent des contrôles réguliers de biomarqueurs pour les infections et la récidive du cancer. Les systèmes de biopsie liquide basés sur INAAT peuvent détecter une maladie résiduelle minimale avec une sensibilité de 94,1 %, permettant une surveillance à domicile ou en clinique communautaire.[2]Nature Communications, "Portable Dragonfly Platform Enables Field Molecular Diagnostics," nature.com L'intégration avec les plateformes de télémédecine rationalise l'examen des résultats, réduisant les visites hospitalières inutiles et diminuant les coûts du système.
Changement de flux de travail de PCR vers INAAT
Les laboratoires cliniques qui passent à LAMP rapportent 60 % moins de temps pratique car les étapes d'extraction sont simplifiées et les réactions fonctionnent à un réglage unique de 60-65 °C.[3]Frontiers in Cellular and Infection Microbiology, "Automation-Compatible LAMP Workflows Reduce Hands-On Time," frontiersin.org Les coupelles de réactifs lyophilisés expédient à température ambiante et s'insèrent dans les lignes d'automatisation existantes, maintenant un débit élevé tout en réduisant les besoins de maintenance typiques des thermocycleurs.
Économies de coût par test plus faibles
Les coûts d'investissement des instruments chutent d'environ 40 % lorsque les chauffages à température constante remplacent les cycleurs multi-zones. Les lectures colorimétriques éliminent l'optique coûteuse, poussant les coûts par test à haut volume en dessous de 5 USD pour les cibles respiratoires. La stabilité des réactifs à température ambiante réduit de 20-30 % les dépenses de chaîne du froid dans les économies émergentes, accélérant le déploiement.
Analyse de l'impact des contraintes
| Contrainte | (~) % Impact sur les prévisions de TCAC | Pertinence géographique | Échéancier d'impact |
|---|---|---|---|
| Concurrence des plateformes PCR et DCR | -1.9% | Mondial, plus fort dans les marchés établis | Moyen terme (2-4 ans) |
| Lacunes de sensibilisation et de remboursement | -1.4% | Amérique du Nord et UE principalement | Court terme (≤ 2 ans) |
| Volatilité de l'approvisionnement en enzymes pour réactifs Bst | -0.8% | Mondial, aigu dans les régions à approvisionnement contraint | Court terme (≤ 2 ans) |
| Obstacles stricts de preuves CLIA-Waiver / IVDR | -1.1% | Amérique du Nord et domaines réglementaires UE | Long terme (≥ 4 ans) |
| Source: Mordor Intelligence | |||
Concurrence des plateformes PCR et DCR
L'infrastructure PCR établie représente des coûts de changement significatifs pour les laboratoires qui ont investi dans des plateformes de cyclage thermique, des systèmes automatisés de manipulation d'échantillons et des programmes de formation de techniciens optimisés pour les flux de travail d'amplification traditionnels. Les plateformes PCR numériques intensifient encore la concurrence en offrant des capacités de quantification absolue que INAAT ne peut actuellement égaler, particulièrement dans les applications nécessitant une surveillance précise de la charge virale ou une analyse de variation du nombre de copies. Les directeurs de laboratoire citent les préoccupations de perturbation du flux de travail lors de l'évaluation de l'adoption d'INAAT, car les procédures de contrôle qualité existantes, les validations réglementaires et les compétences du personnel s'alignent sur les méthodologies PCR.
Lacunes de sensibilisation et de remboursement
La reconnaissance par les payeurs de soins de santé de l'utilité clinique d'INAAT est en retard par rapport aux capacités technologiques, créant des incertitudes de remboursement qui limitent l'adoption dans des environnements de soins de santé sensibles aux coûts. Le programme MolDX de Medicare exige des preuves cliniques étendues démontrant la précision diagnostique et les améliorations des résultats des patients avant d'établir des politiques de couverture pour les nouvelles technologies de diagnostic moléculaire. Le processus de génération de preuves nécessite généralement 18-24 mois de collecte de données cliniques, pendant lesquels les développeurs d'INAAT doivent financer des études sans résultats de remboursement garantis. La sensibilisation des médecins aux capacités d'INAAT reste limitée en dehors des spécialités de maladies infectieuses, de nombreux cliniciens revenant par défaut aux tests basés sur PCR familiers malgré les avantages potentiels en temps de retour et déploiement au point de soins.
Analyse des segments
Par technologie : La dominance LAMP stimule l'innovation
LAMP a capturé 44,34 % du marché de la technologie d'amplification isotherme d'acides nucléiques en 2024 et devrait croître à un TCAC de 13,36 % jusqu'en 2030. La méthodologie cible six régions géniques, conférant une haute spécificité sans cyclage thermique. Les approches complémentaires comme HDA et NEAR traitent les cas d'usage à basse température, tandis que TMA conserve sa valeur dans le dépistage sanguin où la détection d'ARN importe.
L'innovation de détection remodèle le marché de la technologie d'amplification isotherme d'acides nucléiques alors que les développeurs associent LAMP avec les systèmes CRISPR-Cas pour atteindre une sensibilité attomolaire en 30 minutes. Les bandelettes de flux latéral colorimétriques s'intègrent directement dans les cartouches, élargissant l'adoption dans les cliniques manquant de lecteurs de fluorescence.
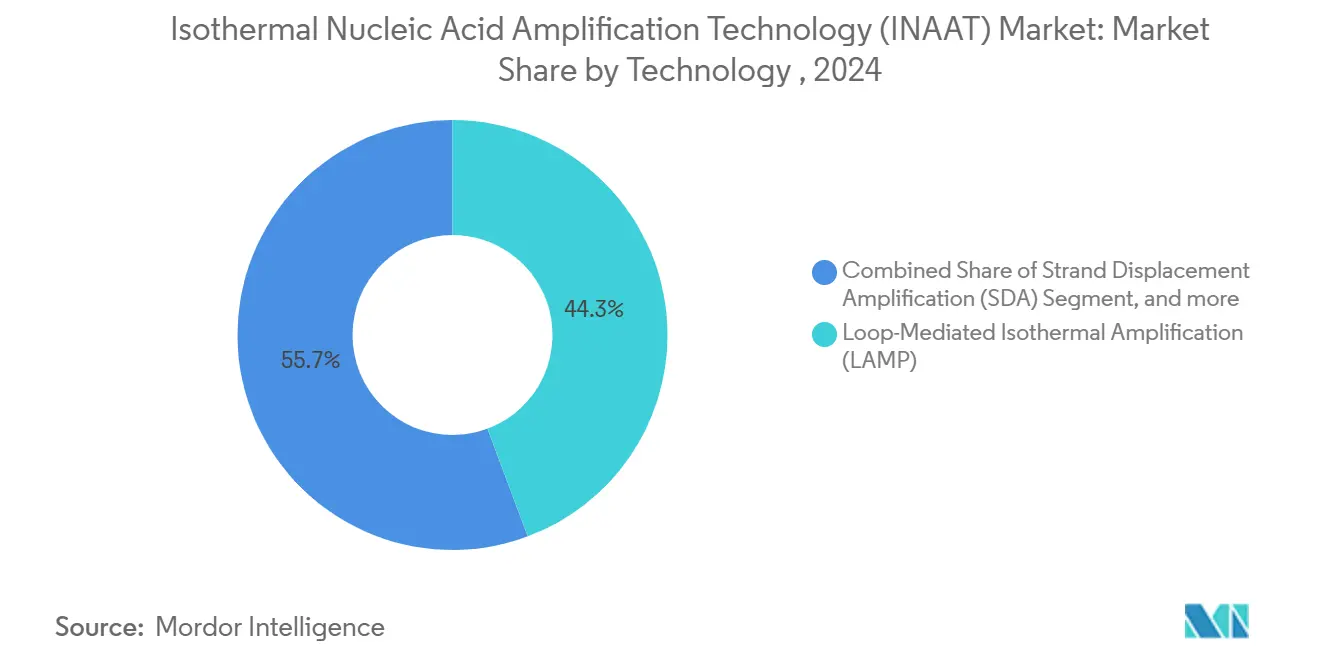
Note: Parts de segments de tous les segments individuels disponibles à l'achat du rapport
Par produit : Les revenus des réactifs financent l'innovation des instruments
Les réactifs et consommables ont généré 63,56 % des revenus de 2024, fournissant un flux de trésorerie récurrent qui subventionne la R&D. La résilience de l'approvisionnement en polymérase Bst reste critique car elle sous-tend la plupart des kits INAAT. Les instruments devraient croître de 11,24 % annuellement alors que les fournisseurs intègrent la microfluidique et l'extraction en une étape, comme en témoigne la cartouche de 30 minutes d'iPonatic réalisant une automatisation complète du flux de travail.
L'innovation des instruments se concentre sur l'intégration et la miniaturisation, avec des fabricants développant des plateformes portables qui combinent la préparation d'échantillons, l'amplification et la détection dans des formats de cartouche à usage unique. Le système iPonatic exemplifie cette tendance, livrant des tests complets d'acides nucléiques en 30 minutes utilisant l'extraction à température ambiante et des capacités de détection intégrées. L'intégration microfluidique permet une manipulation précise des fluides et un contrôle thermique tout en réduisant la consommation de réactifs et les risques de contamination, bien que la complexité de fabrication et les considérations de coût limitent l'adoption aux applications à haute valeur.
Par application : L'émergence de l'oncologie défie la dominance des maladies infectieuses
Les tests de maladies infectieuses ont conservé 53,56 % des revenus en 2024 mais perdront des parts relatives alors que l'oncologie gagne un TCAC de 16,11 %. L'autorisation FDA de 2024 du test ColoSense ARN de selles de Geneoscopy confirme le rôle d'INAAT dans le dépistage non invasif du cancer. Les centres de sang s'appuient également sur TMA pour raccourcir les périodes de fenêtre virale, soulignant l'accent large sur les pathogènes.
La traction oncologique exemplifie la capacité du marché de la technologie d'amplification isotherme d'acides nucléiques à traiter la surveillance continue, détectant l'ADN tumoral circulant avant que les modalités d'imagerie puissent confirmer la rechute. Les segments de sécurité alimentaire et vétérinaire ajoutent de la diversité en exploitant la tolérance d'INAAT pour les matrices complexes, soutenant les diagnostics de terrain où les laboratoires de culture sont rares.
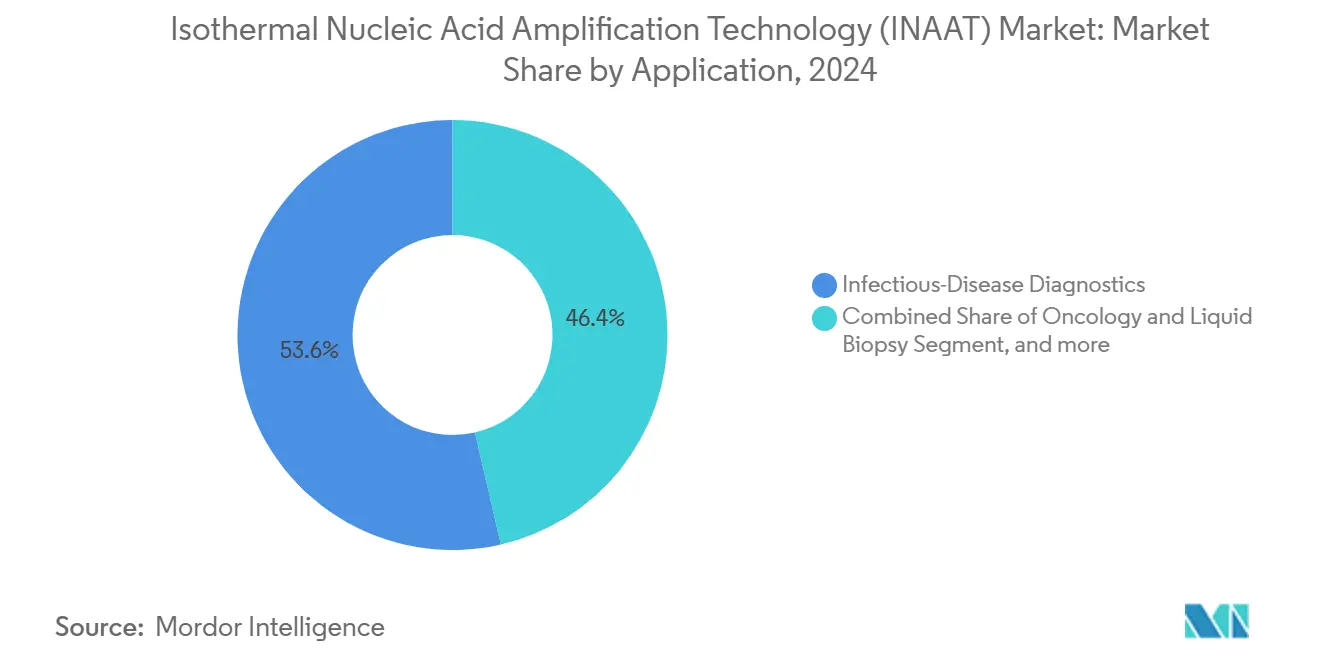
Note: Parts de segments de tous les segments individuels disponibles à l'achat du rapport
Par utilisateur final : L'adoption au point de soins s'accélère
Les hôpitaux et laboratoires de référence ensemble ont détenu 56,78 % des revenus en 2024, tirant parti de l'infrastructure moléculaire existante. Les unités d'urgence utilisent des panneaux respiratoires de trente minutes pour trier rapidement les patients, améliorant la gestion des lits. Les laboratoires de référence ajoutent INAAT pour les tests STAT pour se différencier des concurrents PCR de routine.
Les cliniques décentralisées et les chaînes de soins urgents devraient croître à un TCAC de 11,64 %, aidées par des analyseurs basés sur cartouche qui nécessitent une formation minimale. La station portable Dragonfly a démontré une réponse fiable aux épidémies dans des régions isolées sans alimentation secteur. Les centres académiques continuent de semer des percées que les partenaires commerciaux mettent à l'échelle, renforçant le cycle d'innovation à travers le marché de la technologie d'amplification isotherme d'acides nucléiques.
Analyse géographique
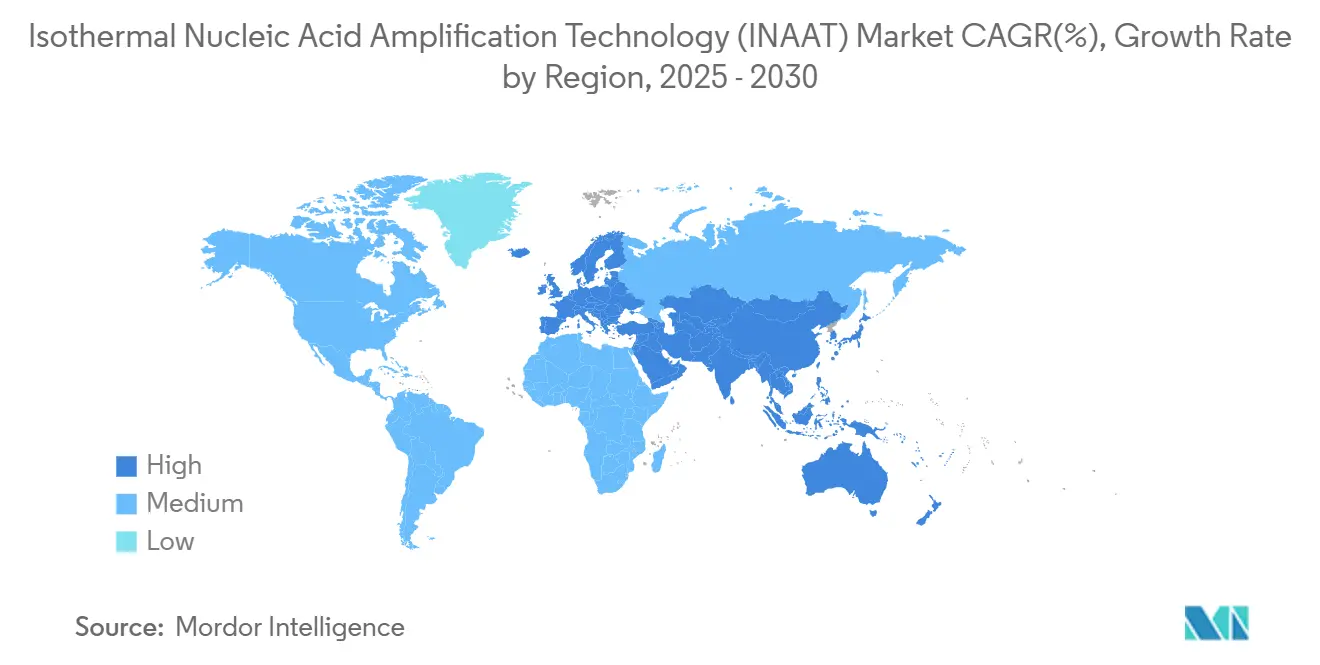
L'Amérique du Nord mène avec 35,67 % des revenus en 2024, soutenue par les voies FDA telles que les règles de dérogation CLIA qui amènent des panneaux respiratoires de quinze minutes dans les cliniques fda.gov. Une couverture d'assurance étendue permet aux hôpitaux d'adopter INAAT sans perturbation budgétaire. Le financement de la recherche et le capital-risque robuste accélèrent les lancements d'appareils domestiques.
L'Asie-Pacifique est le moteur de croissance, prévu à un TCAC de 15,64 %. La NMPA de Chine a raccourci les délais d'examen de 24 à 12 mois, attirant les multinationales à localiser la production nmpa.gov.cn. La population senior du Japon stimule les diagnostics à domicile, tandis que les programmes de santé publique de l'Inde s'approvisionnent en kits INAAT abordables pour la surveillance de la tuberculose et de la dengue. La fabrication locale atténue le risque de change et sécurise l'approvisionnement lors de perturbations mondiales.
L'Europe croît régulièrement alors que l'IVDR harmonise les normes, bien que les innovateurs plus petits fassent face à des obstacles de preuve plus élevés pour le marquage CE. L'Allemagne et le Royaume-Uni ancrent la demande grâce à de solides réseaux hospitaliers et une production de recherche translationnelle. Les politiques de maîtrise des coûts favorisent les systèmes à température constante qui économisent l'énergie et la main-d'œuvre par rapport à la PCR.
Paysage concurrentiel
Le marché reste modérément fragmenté. Abbott, Roche et Qiagen exploitent les réseaux de clients installés pour vendre croisé des cartouches INAAT, tandis que les spécialistes purs comme Meridian Bioscience et Molbio Diagnostics se concentrent sur l'étendue des tests. La participation de 105 millions USD de Bio-Rad dans Geneoscopy illustre la tendance des grandes firmes à s'associer pour accélérer le déploiement des tests d'oncologie.
Les acquisitions étendent les capacités de soins au point de service : bioMérieux a acheté SpinChip Diagnostics en janvier 2025 pour 111 millions EUR, ajoutant une plateforme de marqueurs cardiaques de 10 minutes qui complète sa suite de tests respiratoires. L'avantage concurrentiel dépend de la maîtrise réglementaire car les payeurs exigent des dossiers d'utilité clinique robustes avant que les remboursements n'arrivent.
Les opportunités d'espace blanc persistent dans les diagnostics de terrain ultra-rapides et dans les régions à faible infrastructure où les tests à température constante surpassent la PCR. Les fournisseurs associant INAAT avec CRISPR ou l'interprétation de résultats assistée par IA pourraient sécuriser des niches premium avant que les acteurs en place ne réingénierent leurs portefeuilles.
Leaders de l'industrie de la technologie d'amplification isotherme d'acides nucléiques
-
Becton Dickinson and Company
-
BioMerieux SA
-
Quidel Corporation
-
Qiagen N.V.
-
Tecan Genomics Inc.
- *Avis de non-responsabilité : les principaux acteurs sont triés sans ordre particulier

Développements récents de l'industrie
- Janvier 2025 : bioMérieux a finalisé l'acquisition de SpinChip Diagnostics pour 111 millions EUR (116 millions USD), accédant à une plateforme de diagnostics d'immunoessais innovante conçue pour les tests au point de soins avec livraison de résultats en 10 minutes à partir d'échantillons de sang total. L'acquisition renforce le portefeuille de soins au point de service de bioMérieux avec une technologie ciblant les marqueurs cardiaques pour le diagnostic d'infarctus du myocarde, avec un premier lancement de produit attendu en 2026 suite au marquage CE sous IVDR.
- Janvier 2025 : Geneoscopy a clôturé un tour de financement de série C de 105 millions USD mené par Bio-Rad Laboratories pour soutenir la commercialisation du test de dépistage du cancer colorectal ColoSense et faire avancer le pipeline de diagnostics des maladies inflammatoires de l'intestin. L'investissement exploite la technologie PCR numérique en gouttelettes de Bio-Rad pour améliorer la sensibilité et la spécificité des tests tout en élargissant l'accès au marché grâce aux canaux de distribution établis.
- Juin 2024 : La FDA a accordé l'autorisation de mise sur le marché à Cepheid pour le test Xpert HCV et le système GeneXpert Xpress, établissant le premier test ARN de l'hépatite C au point de soins capable de détecter l'ARN HCV à partir d'échantillons de sang du bout du doigt avec environ 60 minutes de délai d'exécution. L'autorisation permet des approches de test et traitement qui traitent les obstacles de test à plusieurs étapes résultant en infections non traitées.
- Mai 2024 : La FDA a approuvé l'appareil ColoSense de Geneoscopy pour la détection qualitative des marqueurs ARN associés aux néoplasies colorectales et de l'hémoglobine occulte dans les échantillons de selles, marquant le premier test de selles basé sur l'ARN pour les adultes âgés de 45 ans et plus à risque moyen de cancer colorectal. L'approbation inclut des exigences d'étude post-marché avec inscription de 12 500 sujets sur 36 mois pour confirmer l'efficacité clinique.
Portée du rapport sur le marché mondial de la technologie d'amplification isotherme d'acides nucléiques
Selon la portée du rapport, les technologies d'amplification d'acides nucléiques sont utilisées dans le domaine de la biologie moléculaire et des technologies d'ADN recombinant. Ces techniques sont utilisées comme méthodes principales pour détecter et analyser un petit nombre d'acides nucléiques. Les protocoles de technologie d'amplification isotherme d'acides nucléiques sont variés et ont de nombreux avantages, car ils sont extrêmement rapides et ne nécessitent pas de thermocycleurs. Le marché de la technologie d'amplification isotherme d'acides nucléiques (INAAT) est segmenté par technologie (amplification dépendante de l'hélicase (HDA), réaction d'amplification d'enzyme de coupure (NEAR), amplification isotherme médiée par boucle (LAMP), amplification par déplacement de brin (SDA), amplification basée sur la séquence d'acide nucléique (NASBA), amplification médiée par transcription (TMA), amplification isotherme à amorce unique (SPIA), autres technologies), par produit (instruments et réactifs), par utilisateur final (hôpital, laboratoires de recherche, autres utilisateurs finaux), et géographie (Amérique du Nord, Europe, Asie-Pacifique, Moyen-Orient et Afrique, et Amérique du Sud). Le rapport de marché couvre également les tailles de marché estimées et les tendances pour 17 pays différents à travers les principales régions, mondialement. Le rapport offre la valeur (en millions USD) pour les segments ci-dessus.
| Amplification dépendante de l'hélicase (HDA) |
| Réaction d'amplification d'enzyme de coupure (NEAR) |
| Amplification isotherme médiée par boucle (LAMP) |
| Amplification par déplacement de brin (SDA) |
| Amplification basée sur la séquence d'acide nucléique (NASBA) |
| Amplification médiée par transcription (TMA) |
| Amplification isotherme à amorce unique (SPIA) |
| Autres technologies |
| Instruments |
| Réactifs et consommables |
| Diagnostics de maladies infectieuses |
| Oncologie et biopsie liquide |
| Dépistage sanguin et sécurité transfusionnelle |
| Tests de sécurité alimentaire et hydrique |
| Diagnostics vétérinaires et agricoles |
| Hôpitaux et laboratoires de référence |
| Cliniques au point de soins / décentralisées |
| Instituts académiques et de recherche |
| Amérique du Nord | États-Unis |
| Canada | |
| Mexique | |
| Europe | Allemagne |
| Royaume-Uni | |
| France | |
| Italie | |
| Espagne | |
| Reste de l'Europe | |
| Asie-Pacifique | Chine |
| Japon | |
| Inde | |
| Australie | |
| Corée du Sud | |
| Reste de l'Asie-Pacifique | |
| Moyen-Orient et Afrique | CCG |
| Afrique du Sud | |
| Reste du Moyen-Orient et Afrique | |
| Amérique du Sud | Brésil |
| Argentine | |
| Reste de l'Amérique du Sud |
| Par technologie | Amplification dépendante de l'hélicase (HDA) | |
| Réaction d'amplification d'enzyme de coupure (NEAR) | ||
| Amplification isotherme médiée par boucle (LAMP) | ||
| Amplification par déplacement de brin (SDA) | ||
| Amplification basée sur la séquence d'acide nucléique (NASBA) | ||
| Amplification médiée par transcription (TMA) | ||
| Amplification isotherme à amorce unique (SPIA) | ||
| Autres technologies | ||
| Par produit | Instruments | |
| Réactifs et consommables | ||
| Par application | Diagnostics de maladies infectieuses | |
| Oncologie et biopsie liquide | ||
| Dépistage sanguin et sécurité transfusionnelle | ||
| Tests de sécurité alimentaire et hydrique | ||
| Diagnostics vétérinaires et agricoles | ||
| Par utilisateur final | Hôpitaux et laboratoires de référence | |
| Cliniques au point de soins / décentralisées | ||
| Instituts académiques et de recherche | ||
| Par géographie | Amérique du Nord | États-Unis |
| Canada | ||
| Mexique | ||
| Europe | Allemagne | |
| Royaume-Uni | ||
| France | ||
| Italie | ||
| Espagne | ||
| Reste de l'Europe | ||
| Asie-Pacifique | Chine | |
| Japon | ||
| Inde | ||
| Australie | ||
| Corée du Sud | ||
| Reste de l'Asie-Pacifique | ||
| Moyen-Orient et Afrique | CCG | |
| Afrique du Sud | ||
| Reste du Moyen-Orient et Afrique | ||
| Amérique du Sud | Brésil | |
| Argentine | ||
| Reste de l'Amérique du Sud | ||
Questions clés répondues dans le rapport
Qu'est-ce qui stimule la croissance récente du marché de la technologie d'amplification isotherme d'acides nucléiques ?
L'adoption rapide au point de soins, les coûts d'instruments plus bas et le soutien réglementaire continu en Amérique du Nord et en Asie-Pacifique propulsent un TCAC de 8,87 % jusqu'en 2030.
Quel segment technologique mène le marché ?
L'amplification isotherme médiée par boucle détient 44,34 % des revenus et est également le segment à croissance la plus rapide à un TCAC de 13,36 %.
Quelles régions se développent le plus rapidement ?
L'Asie-Pacifique devrait croître à un TCAC de 15,64 % en raison des approbations rationalisées et de l'investissement en infrastructure.
Quelles applications offrent la plus haute croissance future ?
Les tests d'oncologie et de biopsie liquide devraient croître à un TCAC de 16,11 % alors que le dépistage non invasif du cancer gagne l'acceptation médicale et des payeurs.
Quels sont les principaux obstacles à une adoption plus large d'INAAT ?
L'infrastructure PCR existante, les lacunes de remboursement et la volatilité de l'approvisionnement en enzymes restent les principales contraintes affectant l'adoption au cours des deux à quatre prochaines années.
Dernière mise à jour de la page le:



