Tamaño y Participación del Mercado de Controles de Calidad Moleculares
Análisis del Mercado de Controles de Calidad Moleculares por Mordor Intelligence
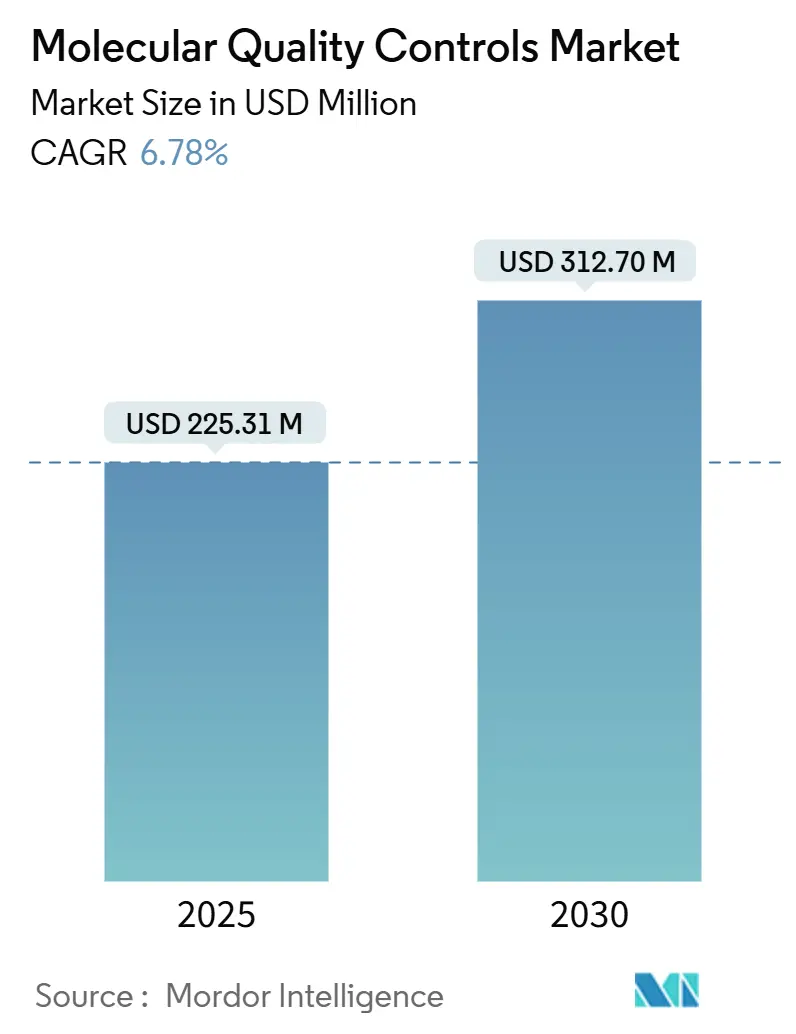
El tamaño del Mercado de Controles de Calidad Moleculares se estima en 225,31 millones de USD en 2025, y se espera que alcance los 312,70 millones de USD en 2030, con una TCAC del 6,78% durante el período de pronóstico (2025-2030). El crecimiento robusto se basa en tres fuerzas: la Regla Final de Pruebas Desarrolladas en Laboratorio (LDT) de la Administración de Alimentos y Medicamentos de Estados Unidos (FDA), el impulso global hacia la acreditación ISO 15189:2022, y el cambio rápido de los laboratorios desde pruebas de un solo analito hacia multiplexado y secuenciación de próxima generación (NGS). Los controles independientes de terceros siguen siendo la herramienta predeterminada para demostrar precisión analítica, mientras que los controles específicos del instrumento ganan impulso a medida que los laboratorios integran automatización y middleware.[1]Fuente: U.S. Food and Drug Administration, "FDA Takes Action Aimed at Helping to Ensure the Safety and Effectiveness of Laboratory Developed Tests," fda.gov La demanda se ve reforzada por la necesidad creciente de oncología para perfiles genómicos integrales, el aumento de mandatos de evaluación externa de calidad (EQA), y el movimiento clínico hacia plataformas moleculares en el punto de atención que aún deben cumplir estándares de calidad centralizados. Por el contrario, los altos costos de control por ejecución, cuellos de botella de suministro para materiales de referencia de patógenos raros, y vías regulatorias superpuestas moderan el gasto a corto plazo.
Conclusiones Clave del Informe
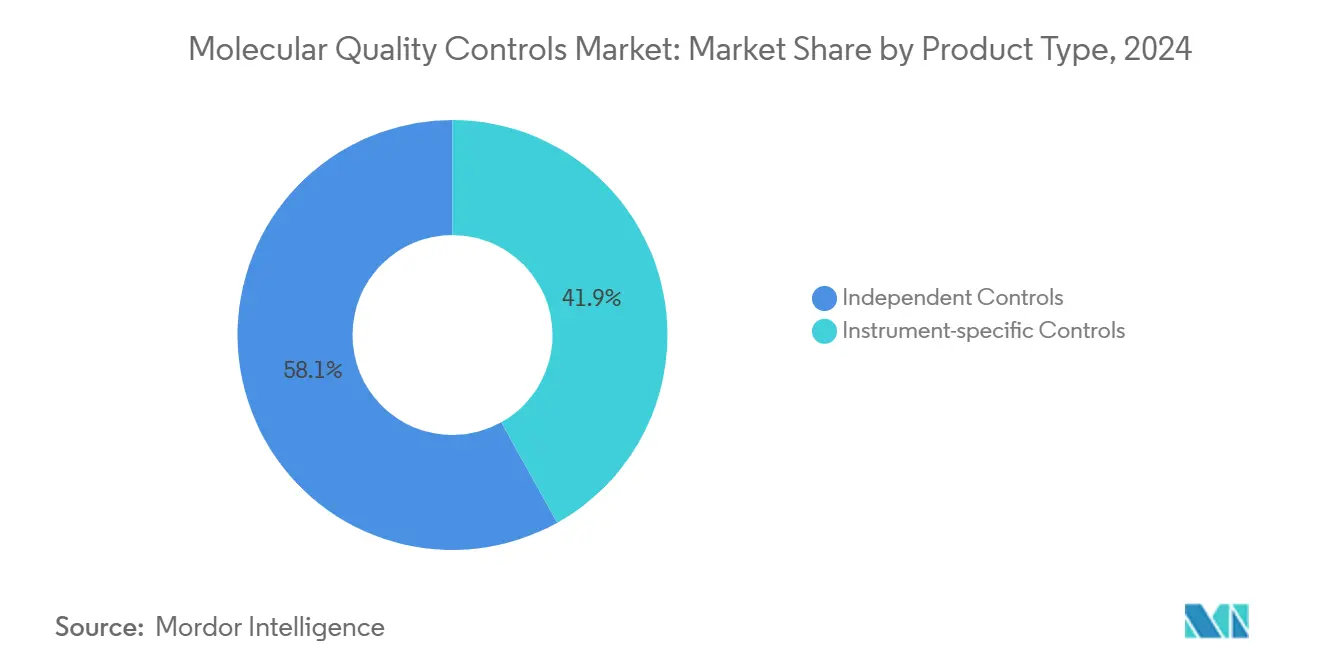
- Por tipo de producto, los controles independientes lideraron con el 58,11% de la participación del mercado de controles de calidad moleculares en 2024; se proyecta que los controles específicos del instrumento registren la TCAC más rápida del 7,55% hasta 2030.
- Por tecnología, los controles basados en PCR mantuvieron el 69,52% de la participación de ingresos en 2024, mientras que los controles basados en NGS se expanden a una TCAC del 7,23% hasta 2030.
- Por aplicación, las enfermedades infecciosas representaron el 55,32% del tamaño del mercado de controles de calidad moleculares en 2024; las pruebas oncológicas avanzan a una TCAC del 8,13% hasta 2030.
- Por usuario final, los laboratorios clínicos mantuvieron el 46,32% de la demanda en 2024; los fabricantes de DIV y CROs registran la TCAC más alta del 7,88% hasta 2030.
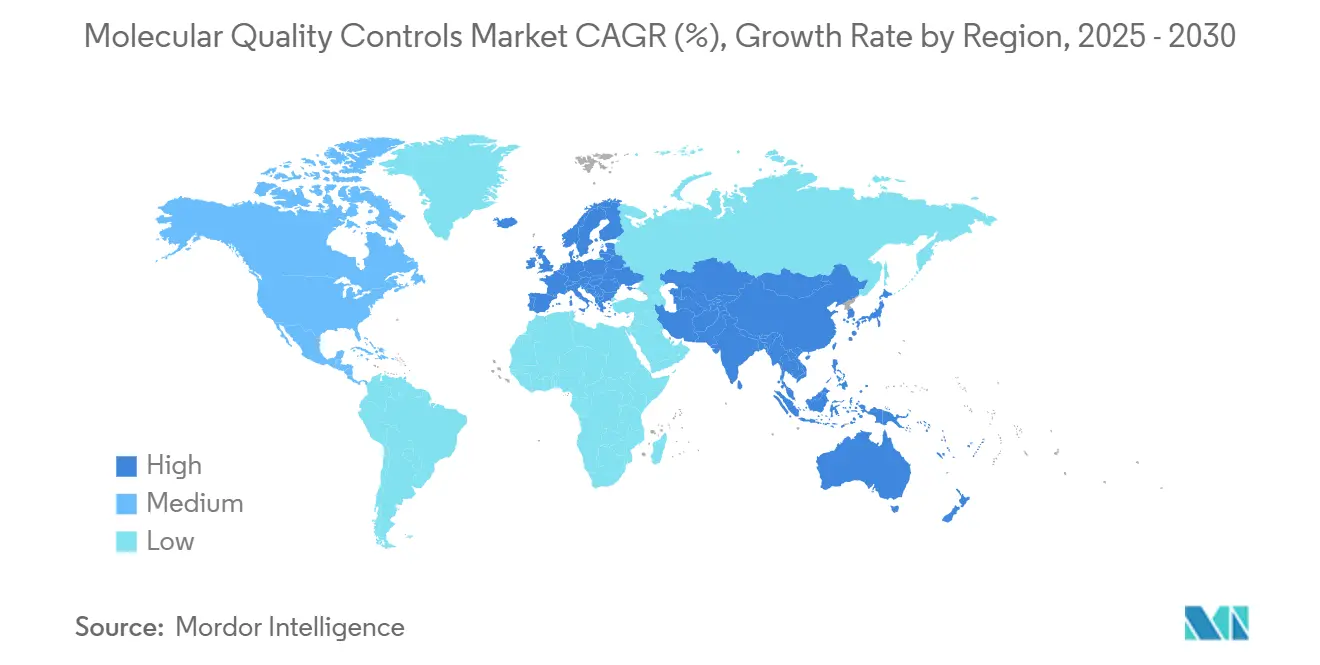
- Por geografía, América del Norte capturó el 38,14% de los ingresos en 2024; Asia-Pacífico es la región de crecimiento más rápido con una TCAC del 8,33% hasta 2030.
Tendencias e Insights del Mercado Global de Controles de Calidad Moleculares
Análisis del Impacto de los Impulsores
| Impulsor | (~) % Impacto en el Pronóstico de TCAC | Relevancia Geográfica | Cronología del Impacto |
|---|---|---|---|
| Aumento del Volumen de Pruebas en Diagnósticos Moleculares | +1.8% | Global, con concentración en América del Norte y Europa | Plazo medio (2-4 años) |
| Adopción Creciente de QC de Terceros Para Acreditación ISO 15189 | +1.5% | Global, particularmente mercados emergentes en APAC | Largo plazo (≥ 4 años) |
| Incidencia Creciente de Cáncer y Trastornos Genéticos | +1.2% | Global, con mayor impacto en regiones desarrolladas | Largo plazo (≥ 4 años) |
| Mandatos Más Estrictos de Evaluación Externa de Calidad (EQA) | +1.0% | América del Norte y UE, expandiéndose a APAC | Corto plazo (≤ 2 años) |
| Cambio a Paneles QC Multiplex Digitales | +0.8% | América del Norte y Europa, adopción temprana en APAC | Plazo medio (2-4 años) |
| Consolidación de Laboratorios Impulsando Integración de Datos QC Empresariales | +0.5% | América del Norte y Europa | Plazo medio (2-4 años) |
| Fuente: Mordor Intelligence | |||
Aumento del Volumen de Pruebas en Diagnósticos Moleculares
Los laboratorios de diagnóstico procesaron volúmenes sin precedentes durante la emergencia de salud pública de COVID-19, con la FDA autorizando 291 ensayos moleculares, demostrando la escalabilidad de plataformas de alto rendimiento.[2]Fuente: U.S. Department of Health and Human Services, "Testing & Diagnostics," hhs.gov Después de la pandemia, el volumen permanece elevado a medida que los laboratorios extienden las pruebas moleculares a farmacogenómica, vigilancia de resistencia antimicrobiana y paneles de cáncer hereditario. Cada objetivo multiplex añade capas de validación, obligando a los laboratorios a depender de controles robustos de terceros para evitar deriva analítica. Los paneles de control de calidad digitales integrados con sistemas de información de laboratorio han reducido los pasos de verificación manual en un 62,5%, subrayando el papel de la tecnología en el manejo de cargas de trabajo crecientes.
Adopción Creciente de QC de Terceros para Acreditación ISO 15189
ISO 15189:2022 eleva el estándar para la gestión de riesgos y para la integración en el punto de atención, empujando a los laboratorios hacia controles de origen externo que demuestran trazabilidad e independencia. La primera acreditación estadounidense bajo la nueva versión señaló un punto de inflexión temprano hacia el impulso de cumplimiento global. Los laboratorios tienen tres años para hacer la transición, anclando una demanda sostenida para productos del mercado de controles de calidad moleculares.
Incidencia Creciente de Cáncer y Trastornos Genéticos
Las tasas de incidencia de cáncer continúan aumentando globalmente, con las pruebas moleculares volviéndose esenciales para decisiones de tratamiento de oncología de precisión. Los paneles de NGS oncológicos interrogan cientos de genes, eventos de número de copias y fusiones, cada uno demandando controles estrictos para la precisión de detección de variantes. Los ensayos de biopsia líquida amplifican la complejidad al requerir detección de variantes de frecuencia ultra-baja, escalando la necesidad de controles sintéticos de alta sensibilidad. De manera similar, los paneles de enfermedades hereditarias que cubren más de 100 genes accionables requieren controles específicos de variantes para apoyar informes clínicos correctos.
Mandatos Más Estrictos de Evaluación Externa de Calidad
La actualización CLIA de 2024 introdujo 23 nuevas pruebas de competencia molecular y redujo los márgenes de error permitidos en un 33,3%, obligando a los laboratorios estadounidenses a actualizar los procedimientos de QC. El análisis longitudinal de 20 años de esquemas EQA para detección bacteriana basada en PCR/NAAT revela uso decreciente de ensayos internos y adopción aumentada de controles de calidad comerciales. Los esquemas paralelos en Europa bajo IVDR e ISO 15189 requieren participación regular en competencia, cimentando un canal de gasto impulsado por cumplimiento dentro del mercado de controles de calidad moleculares.
Análisis del Impacto de las Restricciones
| Restricción | (~) % Impacto en el Pronóstico de TCAC | Relevancia Geográfica | Cronología del Impacto |
|---|---|---|---|
| Alto Costo por Ejecución de Materiales QC Moleculares | -1.2% | Global, particularmente mercados emergentes sensibles al costo | Corto plazo (≤ 2 años) |
| Vía Regulatoria Compleja Multi-Agencia | -0.8% | América del Norte y Europa, expandiéndose globalmente | Plazo medio (2-4 años) |
| Reembolso Desfavorable para Pruebas Moleculares Confirmatorias | -0.6% | América del Norte y Europa | Largo plazo (≥ 4 años) |
| Fragilidad de la Cadena de Suministro para Materiales de Referencia de Patógenos Raros | -0.4% | Global, con impacto agudo durante brotes | Corto plazo (≤ 2 años) |
| Fuente: Mordor Intelligence | |||
Alto Costo por Ejecución de Materiales QC Moleculares
La economía de los controles de calidad moleculares presenta desafíos significativos para laboratorios que operan bajo presupuestos limitados, particularmente a medida que aumenta la complejidad de las pruebas. Los ensayos NGS reducen el costo general de atención al paciente comparado con PCR secuencial, pero aún demandan controles multi-analito costosos que pueden representar el 4-7% del costo por muestra, un margen no trivial para laboratorios pequeños. Los costos fijos de control escalan mal cuando los volúmenes de prueba son modestos, llevando a los laboratorios a extender intervalos de reemplazo y potencialmente comprometer la robustez analítica.
Vía Regulatoria Compleja Multi-Agencia
El panorama regulatorio para controles de calidad moleculares involucra múltiples agencias con jurisdicciones superpuestas, creando complejidad de cumplimiento que extiende cronogramas de desarrollo de productos y aumenta costos. La implementación de cuatro años de la Regla Final LDT de la FDA requiere sistemas de calidad tipo dispositivo, reportes de dispositivos médicos, y en muchos casos revisión previa al mercado.[3]Fuente: U.S. Food and Drug Administration, "Medical Devices; Laboratory Developed Tests," fda.gov Las evaluaciones de conformidad IVDR paralelas en Europa obligan a los fabricantes a abordar múltiples organismos de auditoría, alargando lanzamientos de productos y elevando costos de cumplimiento, especialmente para proveedores pequeños.
Análisis de Segmentos
Por Tipo de Producto: Los Controles Independientes Impulsan el Liderazgo del Mercado
Los controles independientes dominaron con una participación del 58,11% en el mercado de controles de calidad moleculares en 2024, reflejando la preferencia de los laboratorios por herramientas de verificación neutrales al proveedor que satisfacen los requisitos de documentación ISO 15189 y mitigan el sesgo de plataforma. La red Unity Data Management de Bio-Rad, activa en 38.000 laboratorios, ilustra cómo los controles de terceros agregan comparaciones entre pares para detectar desviaciones sistémicas rápidamente. Los productos independientes abarcan desde paneles multi-analito para patógenos respiratorios hasta variantes oncológicas personalizadas, permitiendo a los laboratorios estandarizar across diversos instrumentos.
Los controles específicos del instrumento, aunque más pequeños, se proyecta que registren una TCAC del 7,55% hasta 2030 a medida que se expanden la automatización y las plataformas integradas de muestra a respuesta. La estabilidad ajustada por el fabricante y la consistencia lote a lote ahorran tiempo de validación, una ventaja decisiva en entornos de alto rendimiento. Sin embargo, los temores de bloqueo del proveedor persisten, manteniendo los controles independientes como la opción de referencia para esquemas de competencia. El mercado de controles de calidad moleculares por lo tanto gravita hacia un modelo de doble abastecimiento en el que los laboratorios implementan controles independientes para acreditación mientras dependen de materiales específicos del instrumento para continuidad del flujo de trabajo diario.
Por Tecnología: El Dominio de PCR Enfrenta Disrupción de NGS
Los productos basados en PCR mantuvieron el 69,52% de los ingresos en 2024, anclados por pruebas de enfermedades infecciosas de alto volumen donde el tiempo de respuesta y el costo superan la amplitud. Estos controles típicamente contienen ácidos nucleicos virales o bacterianos estabilizados encapsulados en partículas no infecciosas para bioseguridad.
Los controles basados en NGS, sin embargo, avanzan a una TCAC del 7,23%, reflejando el cambio de oncología hacia paneles multi-gen y el uso creciente de perfiles genómicos integrales en trastornos hereditarios. Los kits QC de preparación de muestras evalúan complejidad de biblioteca, tamaño de fragmento y eficiencia de ligación de adaptador antes de la secuenciación, reduciendo costosas repeticiones. El tamaño del mercado de controles de calidad moleculares para paneles NGS está preparado para expandirse a medida que mejora el reembolso y continúan declinando los costos de secuenciación. Los controles de amplificación isotérmica ocupan casos de uso nicho como pruebas STI en el punto de atención, donde respuestas cualitativas rápidas son suficientes.
Por Aplicación: Liderazgo de Enfermedades Infecciosas Bajo Presión Oncológica
Las pruebas de enfermedades infecciosas mantuvieron el 55,32% del tamaño del mercado de controles de calidad moleculares en 2024, apoyadas por vigilancia continua de virus respiratorios y participación mandatoria en EQA para patógenos notificables. Los paneles multi-objetivo que cubren influenza, RSV y SARS-CoV-2 siguen siendo requisitos básicos para laboratorios clínicos.
Oncología, pronosticada para crecer a una TCAC del 8,13%, está reduciendo la brecha. La innovación en biopsia líquida y ensayos adaptativos de cáncer necesitan controles cuantitativos capaces de detectar variantes en frecuencias alélicas por debajo del 0,5%. Los laboratorios también incluyen datos QC en paquetes de envío electrónicos para aprobaciones de diagnósticos compañeros de la FDA estadounidense, una realidad procesal que eleva volúmenes de control por ensayo. Las pruebas genéticas y de enfermedades hereditarias ganan impulso a través de pantallas de portadores expandidas y orientación farmacogenómica, impulsando adopción más amplia de controles multiplex con distribuciones de variantes calibradas.
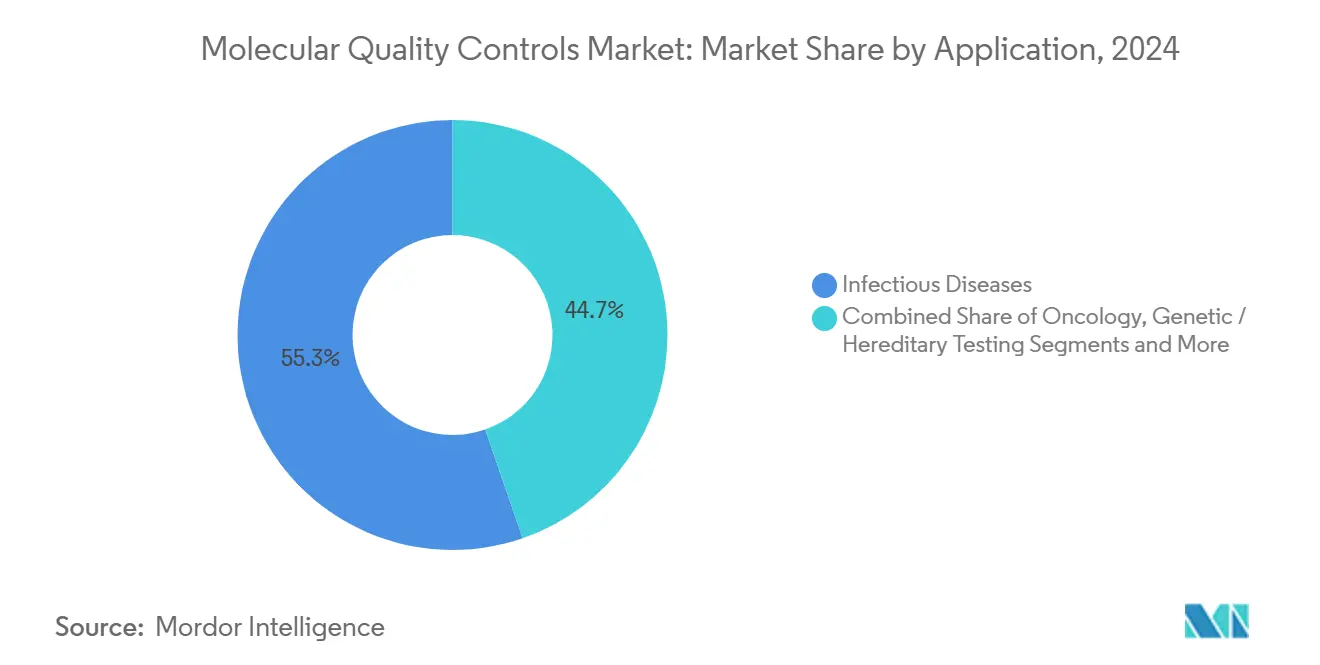
Nota: Participaciones de segmentos de todos los segmentos individuales disponibles con la compra del informe
Por Usuario Final: Los Fabricantes de DIV Aceleran la Integración Empresarial
Los laboratorios clínicos comandaron el 46,32% de los ingresos en 2024, pero las dinámicas de compra se desplazan cada vez más aguas arriba. Los fabricantes de DIV y CROs, creciendo al 7,88% de TCAC, incluyen controles en tuberías de desarrollo de ensayos para agilizar expedientes de marcado FDA o CE. El consumo de control se dispara durante la validación, conectando estudios de sensibilidad analítica, especificidad y límite de detección.
La consolidación empresarial también mueve la selección QC a equipos corporativos centrales, priorizando plataformas que ofrecen APIs de integración de datos y seguimiento automatizado de lotes. Para redes hospitalarias, el middleware que vincula métricas QC con datos de inventario reduce el desperdicio, dando a los proveedores que proporcionan paneles de control en la nube una ventaja competitiva. Los centros médicos académicos siguen siendo adoptantes importantes, particularmente donde la investigación traslacional crea diseños de ensayos novedosos que demandan materiales QC personalizados.
Análisis Geográfico
América del Norte lideró con el 38,14% de los ingresos en 2024, impulsada por reembolso sólido, alto volumen de pruebas, y el marco de la FDA que eleva los controles de terceros de mejor práctica a necesidad regulatoria. Los umbrales de rendimiento más estrictos de CLIA agravan la demanda a medida que los laboratorios amplían la frecuencia QC para mantener la acreditación. La modernización de Canadá de las regulaciones de dispositivos médicos apoya vías aceleradas para controles de calidad innovadores, sosteniendo crecimiento regional estable.
Asia-Pacífico es la geografía de crecimiento más rápido con una TCAC del 8,33%, impulsada por programas genómicos gubernamentales y cadenas de diagnóstico privadas en expansión. El reembolso de Japón de paneles oncológicos NGS y la inversión de Corea del Sur en fabricación de terapia celular y génica se traducen ambos en mayor consumo QC para flujos de trabajo NGS. Los fabricantes de instrumentos domésticos de China integran cada vez más software de seguimiento de lotes QC, amplificando la demanda local. A pesar de regulaciones fragmentadas, el mercado de controles de calidad moleculares se beneficia del impulso de APAC para armonizar estándares de calidad con principios ISO 15189 e IVDR, fomentando adopción de productos transfronterizos.
Europa exhibe crecimiento consistente de dígito medio único a medida que la implementación IVDR obliga a laboratorios y fabricantes a actualizar documentación de calidad. El Servicio Nacional de Salud del Reino Unido otorga contratos de laboratorio central que requieren cumplimiento ISO 15189:2022, incrustando uso QC en plantillas de adquisición. Oriente Medio y África y Sudamérica permanecen incipientes pero muestran ganancias incrementales de doble dígito donde se abren nuevos laboratorios de referencia. En estas regiones, proyectos de vigilancia de enfermedades infecciosas financiados por agencias multilaterales a menudo estipulan controles de terceros, dando a los proveedores un punto de apoyo temprano.
Panorama Competitivo
El mercado de controles de calidad moleculares está moderadamente concentrado. Bio-Rad, Roche y Thermo Fisher anclan el primer nivel, aprovechando carteras amplias de ensayos y capas informáticas para crear altos costos de cambio. La compra pendiente de Bio-Rad de Stilla Technologies combinará experiencia en PCR digital con su catálogo de controles independientes, expandiendo opciones cuantitativas para ensayos de vectores de terapia génica. Roche incorpora métricas de calidad de muestra en sus kits de preparación de muestras NGS, alineando materiales de control con automatización de flujo de trabajo.
Especialistas de tamaño medio como ZeptoMetrix y Microbiologics se enfocan en líneas de patógenos nicho, a menudo lanzando materiales de referencia dentro de semanas de amenazas emergentes, una capacidad valorada durante brotes. Las barreras de entrada radican principalmente en competencia regulatoria y escala de biofabricación; los recién llegados típicamente se asocian con fabricantes por contrato para cerrar brechas. La diferenciación competitiva es cada vez más centrada en datos: plataformas que transmiten resultados QC a paneles de control en la nube ofrecen análisis de rendimiento casi en tiempo real, una característica que los laboratorios usan para acortar ventanas de resolución de problemas de días a horas.
Las oportunidades abundan en pruebas en el punto de atención y descentralizadas, donde sistemas de flujo lateral y microfluídicos aún carecen de controles robustos de terceros. Los proveedores capaces de miniaturizar controles para formatos de cartucho están preparados para capturar volumen incremental. De manera similar, el auge de software de gestión de calidad impulsado por IA genera demanda inducida para proveedores de control que ofrecen certificados legibles por máquina e integración de códigos de barras, reforzando el bloqueo del ecosistema más allá de meras ventas de reactivos.
Líderes de la Industria de Controles de Calidad Moleculares
-
Bio-Rad Laboratories Inc
-
F. Hoffmann-La Roche AG
-
ZeptoMetrix Corporation
-
bioMérieux SA
-
Thermo Fisher Scientific Inc.
- *Nota aclaratoria: los principales jugadores no se ordenaron de un modo en especial
Desarrollos Recientes de la Industria
- Junio 2025: ZeptoMetrix lanzó NATtrol Influenza A H5N1 Quantitative Stock para fortalecer los flujos de trabajo de validación de ensayos de influenza aviar.
- Noviembre 2024: Microbiologics adquirió SensID, expandiendo su cartera de controles de oncología y medicina de precisión.
Alcance del Informe Global del Mercado de Controles de Calidad Moleculares
Los controles de calidad moleculares se utilizan para evaluar el rendimiento de pruebas moleculares como procedimientos de pruebas de ácidos nucleicos in vitro para ensayos de carga viral, detección de patógenos, unidades de plaquetas de aféresis con leucocitos reducidos (LRAP), infecciones asociadas con la atención sanitaria (HAIs) como neumonía, infecciones del tracto urinario y más. Estos productos se enfocan principalmente en la detección de defectos, control de calidad, y paneles de validación para apoyar en la implementación y monitoreo del rendimiento de lotes de kits de ensayo para laboratorios clínicos y de investigación, centros de diagnóstico de sangre, y fabricantes de DIV.
| Controles Independientes |
| Controles Específicos del Instrumento |
| Basada en PCR |
| Basada en NGS |
| Isotérmica/Otros NAAT |
| Enfermedades Infecciosas |
| Oncología |
| Pruebas Genéticas/Hereditarias |
| Salud Reproductiva y Prenatal |
| Otros |
| Laboratorios Clínicos |
| Hospitales y Centros Médicos Académicos |
| Fabricantes de DIV y CROs |
| Otros |
| América del Norte | Estados Unidos |
| Canadá | |
| México | |
| Europa | Alemania |
| Reino Unido | |
| Francia | |
| Italia | |
| España | |
| Resto de Europa | |
| Asia-Pacífico | China |
| Japón | |
| India | |
| Australia | |
| Corea del Sur | |
| Resto de Asia-Pacífico | |
| Oriente Medio y África | CCG |
| Sudáfrica | |
| Resto de Oriente Medio y África | |
| Sudamérica | Brasil |
| Argentina | |
| Resto de Sudamérica | |
| Sudáfrica |
| Por Tipo de Producto | Controles Independientes | |
| Controles Específicos del Instrumento | ||
| Por Tecnología | Basada en PCR | |
| Basada en NGS | ||
| Isotérmica/Otros NAAT | ||
| Por Aplicación | Enfermedades Infecciosas | |
| Oncología | ||
| Pruebas Genéticas/Hereditarias | ||
| Salud Reproductiva y Prenatal | ||
| Otros | ||
| Por Usuario Final | Laboratorios Clínicos | |
| Hospitales y Centros Médicos Académicos | ||
| Fabricantes de DIV y CROs | ||
| Otros | ||
| Por Geografía | América del Norte | Estados Unidos |
| Canadá | ||
| México | ||
| Europa | Alemania | |
| Reino Unido | ||
| Francia | ||
| Italia | ||
| España | ||
| Resto de Europa | ||
| Asia-Pacífico | China | |
| Japón | ||
| India | ||
| Australia | ||
| Corea del Sur | ||
| Resto de Asia-Pacífico | ||
| Oriente Medio y África | CCG | |
| Sudáfrica | ||
| Resto de Oriente Medio y África | ||
| Sudamérica | Brasil | |
| Argentina | ||
| Resto de Sudamérica | ||
| Sudáfrica | ||
Preguntas Clave Respondidas en el Informe
¿Por qué el mercado de controles de calidad moleculares está creciendo más rápido después de 2025?
La demanda se acelera a medida que la Regla Final LDT de la FDA endurece los requisitos del sistema de calidad, obligando a laboratorios mundiales a adoptar controles de terceros e impulsando una TCAC del 6,78% hasta 2030.
¿Qué categoría de producto tiene la mayor participación del mercado de controles de calidad moleculares hoy?
Los controles independientes, neutrales al proveedor, dominan con el 58,11% de participación porque satisfacen la documentación ISO 15189 y las necesidades de comparabilidad multiplataforma.
¿Qué tan rápido se están expandiendo los controles de calidad basados en NGS?
Se proyecta que los controles basados en NGS aumenten a una TCAC del 7,23%, reflejando el cambio de oncología hacia perfiles genómicos integrales y paneles hereditarios multi-gen.
¿Qué región contribuirá con los mayores ingresos incrementales para 2030?
Asia-Pacífico, preparada para una TCAC del 8,33%, añadirá los mayores ingresos nuevos debido a iniciativas de medicina genómica y crecientes inversiones en infraestructura de laboratorio.
¿Cuáles son las principales presiones de costos que enfrentan los laboratorios?
Los altos costos de materiales QC por ejecución y restricciones de suministro para referencias de patógenos raros pueden elevar gastos operativos hasta el 7% del costo del ensayo, especialmente en entornos de bajo volumen.
Última actualización de la página el:



