Marktgröße und Marktanteil der Regenerativen Medizin
Marktanalyse für Regenerativ Medizin von Mordor Intelligenz
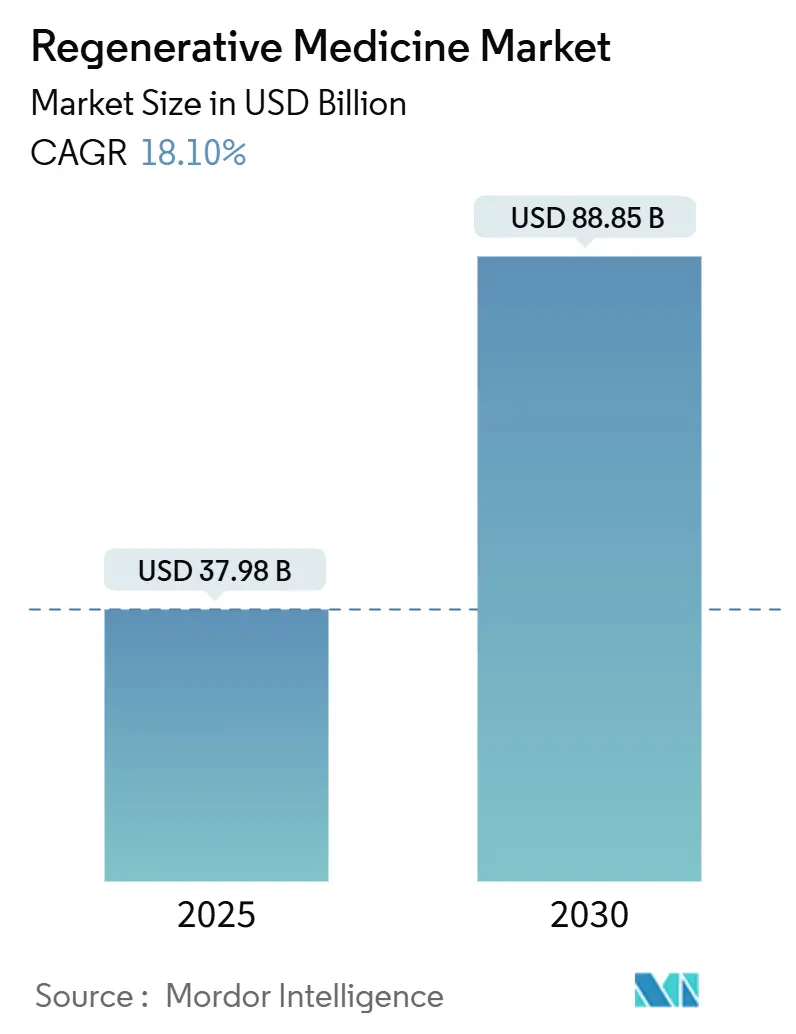
Die Marktgröße für Regenerativ Medizin wird auf 37,98 Milliarden USD In 2025 geschätzt und soll 88,85 Milliarden USD bis 2030 erreichen, mit einer CAGR von 18,10% während des Prognosezeitraums (2025-2030).
Nachhaltige Finanzierung für fortgeschrittene Zell- und Gentherapien, der Erfolg beschleunigter Zulassungsverfahren und starke Investitionen In die Fertigungsinfrastruktur steigern die Nachfrage In nahezu jedem Therapiebereich. Gen-Bearbeitung-Durchbrüche wie Crisper Therapeutika' Casgevy beschleunigen die kommerzielle Akzeptanz, während das allogene Modell historische Skalierungsbarrieren lindert, die autologe Ansätze limitierten. Asien-Pazifiks gestraffte Regulierungen und steigende klinische Studienaktivität positionieren die Region als zentralen Innovationshub. Gleichzeitig verursachen Erstattungshürden für kostenintensive autologe Produkte eine ungleichmäßige Akzeptanzkurve, die Kostenträger mit tieferen Ressourcen bevorzugt und Entwickler dazu veranlasst, ergebnisbasierte Vereinbarungen und andere Flexibel Zahlungsmodelle zu erkunden.
Wichtige Berichtserkenntnisse
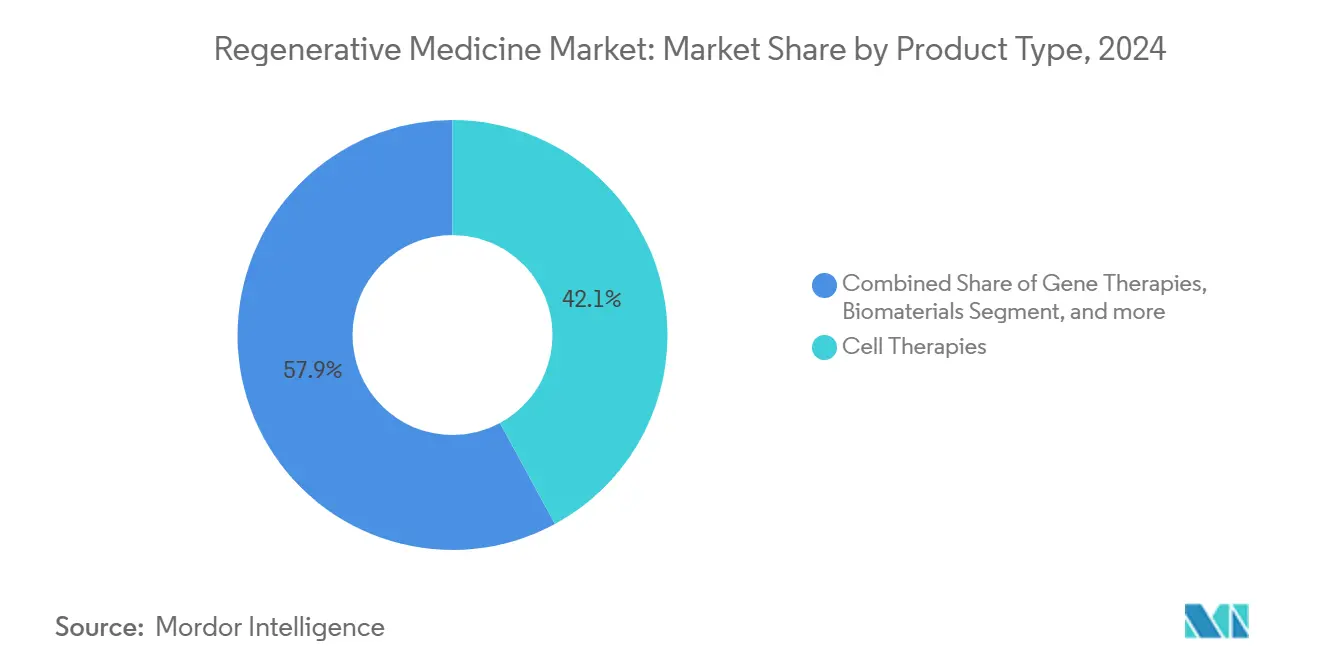
- Nach Produkttyp führten Zelltherapien mit 42,12% Umsatzanteil In 2024; Gentherapien werden voraussichtlich mit 25,39% CAGR bis 2030 expandieren.
- Nach Zellherkunft hielten allogene Therapien 55,14% des Marktanteils für Regenerativ Medizin In 2024, während autologe Therapien voraussichtlich mit 21,47% CAGR bis 2030 wachsen werden.
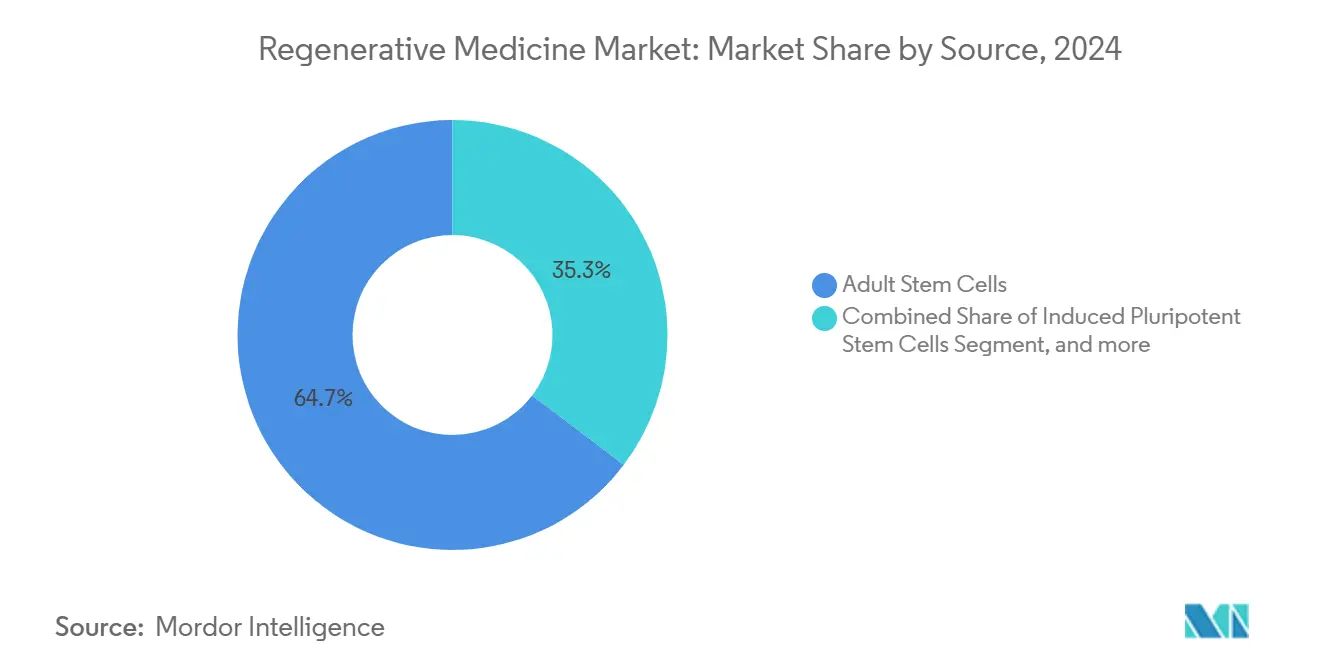
- Nach Stammzellquelle machten adulte Stammzellen 64,68% Anteil des Marktes für Regenerativ Medizin In 2024 aus; induzierte pluripotente Stammzellen (iPSCs) entwickeln sich mit 26,73% CAGR bis 2030.
- Nach Anwendung beherrschten Orthopädie und muskuloskelettale Erkrankungen 34,64% des Marktanteils für Regenerativ Medizin In 2024, wohingegen Onkologie voraussichtlich mit 24,59% CAGR bis 2030 steigen wird.
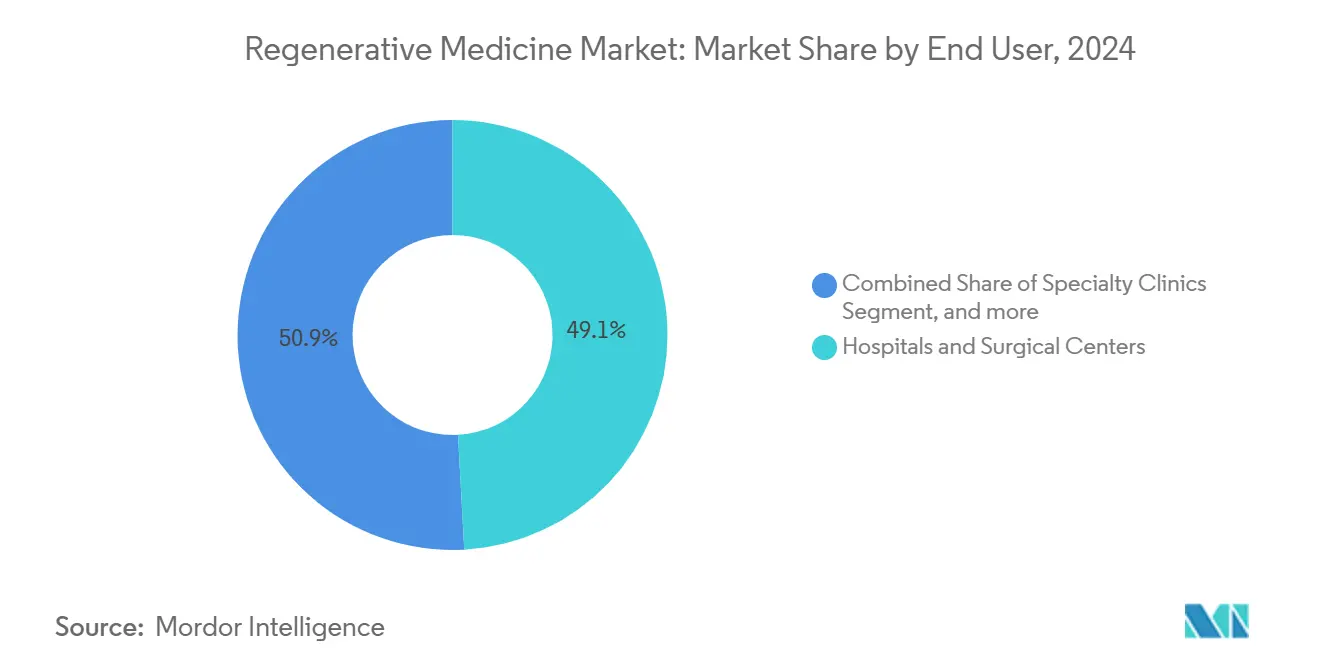
- Nach Endbenutzer dominierten KrankenhäBenutzer und chirurgische Zentren mit 49,13% Umsatzanteil In 2024; Biobanken und Zellbanken werden voraussichtlich mit 20,12% CAGR über den Prognosezeitraum wachsen.
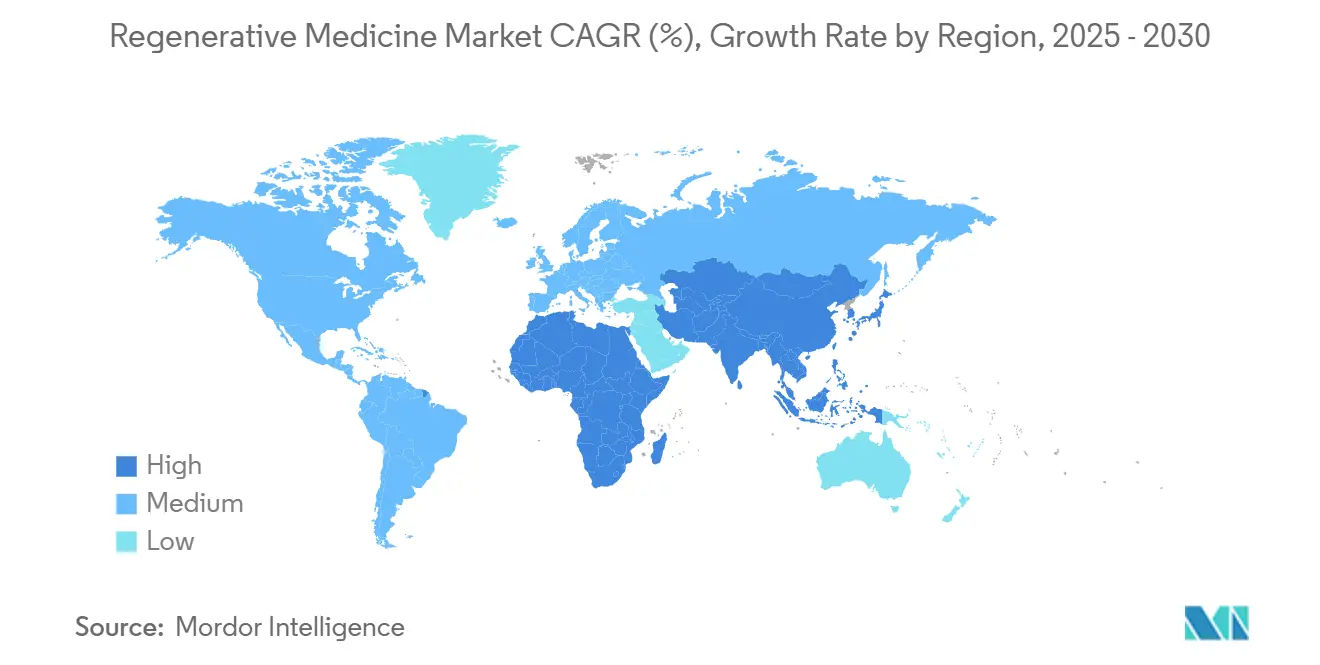
- Nach Geografie hielt Nordamerika 39,95% der Marktgröße für Regenerativ Medizin In 2024, während Asien-Pazifik bereit ist, mit 16,22% CAGR bis 2030 zu expandieren.
Globale Markttrends und Einblicke für Regenerativ Medizin
Treiber-Auswirkungsanalyse
| Treiber | (~) % Auswirkung auf CAGR-Prognose | Geografische Relevanz | Auswirkungszeithorizont |
|---|---|---|---|
| Schnelle allogene aus-Die-Regal-Therapien | +2.5% | Global, angeführt von Nordamerika | Mittelfristig (2-4 Jahre) |
| Altersbedingte muskuloskelettale Belastung | +2.0% | Asien-Pazifik, Europa | Langfristig (≥ 4 Jahre) |
| RMAT-Bezeichnungen verkürzen Zulassungen | +2.2% | Vereinigte Staaten | Kurzfristig (≤ 2 Jahre) |
| Steigende Akzeptanz der iPSC-Technologie | +1.8% | Nordamerika, Japan | Langfristig (≥ 4 Jahre) |
| Staatlich finanzierte nationale Zellfertigungshubs skalieren GMP-Kapazität | +1.7% | Vereinigte Staaten, Asien-Pazifik | Langfristig (≥4 Jahre) |
| Integration von 3D-Bioprinting mit Biomaterial-Gerüsten treibt personalisierte Hautersatzstoffe | +1.6% | Nordamerika, Europa | Mittelfristig (2-4 Jahre) |
| Quelle: Mordor Intelligence | |||
Schnelle klinische Umsetzung allogener Off-the-Shelf-Zelltherapien
Allogene Plattformen definieren Skalierbarkeit neu, indem sie patientenspezifische Herstellung durch standardisierte Chargen ersetzen, die kryokonserviert und nach Bedarf versandt werden können. Diese aus-Die-Regal-Konstrukte gewinnen an Dynamik, da Entwickler RMAT-Status sichern, der regulatorische Prüfungszyklen verkürzt. Im Dezember 2024 gewährte die FDA RMAT-Bezeichnung für Affimeds Acimtamig plus AlloNK-Regime nach einer frühen 83,3% Gesamtansprechrate und validierte damit das Modell für hämatologische Onkologie.[1]u.S. Lebensmittel Und Medikament Administration, "Regenerativ Medizin Fortgeschritten Therapie (RMAT) Designations," fda.gov Niedrigere Produktionskosten, gekoppelt mit expandierender GMP-Kapazität, ermöglichen es kleineren Unternehmen, Nischindikationen anzugehen, die früher wirtschaftlich nicht realisierbar waren. Da mehrere-Donor-iPSC-Plattformen reifen, werden die Kostenvorteile der allogenen Produktion voraussichtlich die Therapiepreise weiter komprimieren und den Patientenzugang erweitern.
Anstieg der muskuloskelettalen Erkrankungsbelastung in alternden Bevölkerungen befeuert Tissue-Engineering-Implantate
Die steigende Lebenserwartung verstärkt die Prävalenz von Osteoarthritis, degenerativer Bandscheibenerkrankung und verwandten Zuständen und spornt einen 34,64% Umsatzanteil für Orthopädie innerhalb des Marktes für Regenerativ Medizin an. Gewebe-Maschinenbau-Implantate bieten Langlebigkeit und biologische Integration, die traditionellen Prothesen überlegen sind, dennoch bestehen Kommerzialisierungshürden wie Biobürden-Kontrolle und Kälteketten-Logistik. Unternehmen, einschließlich Evonik, mildern diese Barrieren durch medizinische Polymere (RESOMER) und rekombinantes Kollagen (VECOLLAN), die Bioprinting-Genauigkeit und Lagerstabilität verbessern. Die Konvergenz fortgeschrittener Biomaterialien und 3D-Drucks ermöglicht anatomische Anpassung für komplexe Gelenkrekonstruktionen. Nationale Gesundheitssystem-Pilotprojekte In Japan und Deutschland demonstrieren bereits postoperative Lebensqualitätsgewinne, die eine breitere Erstattung von Gewebe-Maschinenbau-Implantaten unterstützen könnten und die Markttrends für Regenerativ Medizin weiter prägen.
Regenerative Medicine Advanced Therapy (RMAT) Bezeichnungen beschleunigen Zulassungen
Etabliert unter dem 21st Century Cures Act bietet der RMAT-Status intensiv FDA-Beratung und die Aussicht auf beschleunigte Zulassung basierend auf Surrogatendpunkten. Mehr als 35% zusätzliche allogene Kandidaten sicherten sich RMAT In 2024 gegenüber 2023 und unterstreichen seinen wachsenden Einfluss. Das auf Nabelschnurblut basierende REGENECYTE, das Long-COVID-Syndrom adressiert, trat kürzlich der Liste bei und gewann prioritäre Interaktionen, die Anlaufzeiten für zentrale Studien verkürzen. Entwickler passen nun klinische Designs an, um RMAT-Kriterien früh zu erfüllen, was wiederum Risikokapital In mittlere Programme zieht, die einst um Folge-Finanzierung kämpften. Schnellere regulatorische Feedback-Schleifen reduzieren Programmabbrüche und helfen neuartigen Modalitäten wie gen-editierten NK-Zellen, Patienten früher zu erreichen.
Zunehmende Akzeptanz der Stammzelltechnologie im Markt für Regenerative Medizin
Induzierte pluripotente Stammzellen (iPSCs) befinden sich auf einem 26,73% CAGR-Pfad, angetrieben von vielseitiger Differenzierungskapazität und Freiheit von embryonaler Gewebeethik. Der hiPSCore-Algorithmus, 2024 veröffentlicht, identifiziert 172 prädiktive Gen und gibt Herstellern ein robustes Qualitätstor, das das Risiko von Chargenfehlern bei der Hochskalierung senkt. Gleichzeitig haben Forschungsteams demonstriert, dass die anfängliche iPSC-Aussaatdichte quadratisch mit der Differenzierungsausbeute korreliert, eine Erkenntnis, die voraussichtlich Medienkosten In Großen Bioreaktoren senken wird. iPSC-abgeleitete Auto-T-Pipelines versprechen eine unerschöpfliche T-Zell-Versorgung, die langwierige autologe Erntezyklen umgeht und die Bedrohung durch T-Zell-Erschöpfung mildert. Regulatorische Grünlichter für erste iPSC-Studien am Menschen bei Parkinson-Krankheit erweitern das klinische Playbook über die Onkologie hinaus.
Hemmnis-Auswirkungsanalyse
| Hemmnis | (~) % Auswirkung auf CAGR-Prognose | Geografische Relevanz | Auswirkungszeithorizont |
|---|---|---|---|
| Begrenzte Erstattung für autologe Therapien | -3.0% | Global, ausgeprägt In Schwellenmärkten | Kurzfristig (≤ 2 Jahre) |
| Japan PMDA-Sicherheitsüberwachung für gen-editierte Konstrukte | -1.5% | Japan | Mittelfristig (2-4 Jahre) |
| Chargen-zu-Chargen-Variabilität In stammzellabgeleiteten Produkten behindert kommerzielle Hochskalierung | -2.1% | Global | Mittelfristig (2-4 Jahre) |
| Geringe Arztakzeptanz aufgrund von Handhabungskomplexität kryokonservierter Zelltherapien In Schwellenökonomien | -1.8% | Schwellenmärkte | Kurz-mittelfristig (≤3 Jahre) |
| Quelle: Mordor Intelligence | |||
Begrenzte Erstattungsverfahren für kostenintensive autologe Therapien
Preisschilder, die 1 Million USD pro geduldig überschreiten können, kollidieren mit budgetbegrenzten Kostenträgersystemen und bremsen die Geschwindigkeit, mit der autologe Behandlungen In die Routineversorgung eindringen. Wohlhabendere Gesundheitsnetzwerke In den Vereinigten Staaten und Westeuropa haben ergebnisbasierte Verträge pilotiert, dennoch bleibt die breite Akzeptanz sporadisch. Risikokapitalflüsse In Gewebe-Maschinenbau-Medizinprodukte haben sich gemäßigt, da Investoren Erstattungsrisiken gegen lange Entwicklungszeiten abwägen. Während Ratenzahlungs- und Rentenmodelle politische Traktion gewinnen, begrenzt die administrative Komplexität der Verfolgung realer Ergebnisse weiterhin die Skalierbarkeit. Diese Finanzierungsunsicherheit verstärkt das Interesse an kostengünstigeren allogenen und Gen-Bearbeitung-Lösungen und könnte die Trajektorie des Marktes für Regenerativ Medizin umgestalten.
Strenge Japan PMDA-Sicherheitsüberwachung erhöht Time-to-Market für gen-editierte Konstrukte
Japans PMDA, obwohl für progressive Regenerativ Medizin-Gesetzgebung gelobt, hat verstärkte Post-Marketing-Überwachung und aus-Ziel-Screening-Anforderungen für Gen-Bearbeitung-Technologien eingeführt. Unternehmen wie Rege Nephro haben klinische Sequenzierung gestaffelt, um Japan-spezifische Sicherheitsdatensätze zu generieren, bevor sie Studien zu uns-Standorten migrieren, was Zeitpläne verlängert und Kosten erhöht. Die erhöhte Prüfung intensiviert die Nachfrage nach sensibleren Tests, die niedrigfrequente Editierungen erkennen, und stimuliert die Zusammenarbeit zwischen Biotechnologie und akademischen Bildgebung-Labors. Obwohl die Maßnahmen Markteinführungen verzögern können, werden sie voraussichtlich das öffentliche Vertrauen In Gen-Bearbeitung-Therapeutika stärken und letztendlich breitere Akzeptanz In ganz Asien erleichtern und damit den Markt für Regenerativ Medizin antreiben.
Segmentanalyse
Nach Produkttyp: Gentherapien definieren Behandlungsparadigmen neu
Gentherapien sammeln sich auf einer 25,39% CAGR, die das Segment In Richtung Parität mit Zelltherapien drückt, die 42,12% des Marktanteils für Regenerativ Medizin In 2024 hielten. Die Zulassung von Casgevy und der ersten pränatalen Spinalmuskelatrophie-Intervention unterstreichen die expandierende klinische Reichweite des Gen-Editings. Entwickler verfeinern Lipid-Nanopartikel und virale Vektor-Lieferung, um Gewebetargeting und Dosispräzision zu verbessern, während Kostenträger langfristige Kostenversätze von potenziellen Heilungen bewerten. Regulatorische Leitlinien, die Potenz-Tests und Vektor-Shedding-Studien klären, glätten klinischen Fortschritt In Hämatologie, Neurologie und seltenen Stoffwechselzuständen. Lieferketten-Investitionen wie modulare virale Vektor-Suiten sind bereit, Engpässe zu reduzieren, da späte Pipelines anschwellen.
Dynamik im Gen-Bearbeitung stimuliert nachgelagerte Nachfrage nach Hilfsdienstleistungen, einschließlich
Notiz: Segmentanteile aller einzelnen Segmente bei Berichtserwerb verfügbar
Nach Zellherkunft: Allogene Lösungen treiben Skalierbarkeit
Allogene Produkte führten mit 55,14% Umsatzanteil des Marktes für Regenerativ Medizin In 2024 und kapitalisieren auf Chargenproduktion, die Qualität homogenisiert und pro-Dosis-Kosten senkt. Der Skalenunterschied übersetzt sich direkt In kürzere Vorlaufzeiten für akute Indikationen wie rezidiviertes Lymphom, wo Verzögerungen In der autologen Herstellung tödlich sein können. Multifunktionale iPSC-abgeleitete T-Zellen, die bereits robuste Anti-Myelom-Aktivität zeigen, sind positioniert, diese Trajektorie zu verstärken, sobald Phase-1-biologische Daten reifen.
Autologe Ansätze behalten jedoch einen Vorteil In personalisierter Tumorantigen-Erkennung und verbuchen derzeit solide 21,47% CAGR. Hybridmodelle - wo Patienten eine autologe Starterdosis gefolgt von allogener Konsolidierung erhalten - sind unter früher Untersuchung und könnten bestehende Grenzen verwischen. Lieferketten-Resilienz, einschließlich redundanter Spenderpools und automatisierter Zellauftau-Einheiten, bleibt zentral für die Gewährleistung von Produktkonsistenz während schneller globaler Bereitstellung.
Nach Quelle: iPSCs revolutionieren Entwicklungsparadigmen
Adulte Stammzellen hielten 64,68% der Marktgröße für Regenerativ Medizin In 2024, gestützt von Jahrzehnten klinischer Vertrautheit. Dennoch skalieren iPSCs mit 26,73% CAGR auf der Basis permissiver Patentlandschaften und der Fähigkeit, patientenspezifische oder vollständig universelle Linien abzuleiten. Das hiPSCore-Tool gibt Regulatoren standardisierte Metriken für Pluripotenz-Bewertung und reduziert die Notwendigkeit für erschöpfende nachgelagerte Teratom-Tests.
In der Produktion ermöglicht die dokumentierte quadratische Verbindung zwischen anfänglicher iPSC-Dichte und Differenzierungsausbeute prädiktive Chargenplanung und glättet Tech-überweisen zu kommerziellen Reaktoren. Erfolg In frühen Parkinson-Krankheit-Transplantaten erweitert Investoreninteresse über Onkologie hinaus, mit kardiovaskulären und ophthalmologischen Studien, die sich anstellen. Die Konvergenz von Crisper "Basis-Bearbeitung" mit iPSC-Plattformen könnte bald gleichzeitige Korrektur multipler monogener Defekte ermöglichen.
Notiz: Segmentanteile aller einzelnen Segmente bei Berichtserwerb verfügbar
Nach Anwendung: Onkologie treibt Innovation und Wachstum
Orthopädie verankert weiterhin 34,64% des Marktanteils für Regenerativ Medizin, aber Onkologie zeichnet eine 24,59% CAGR, die sie vor 2030 In die Spitze-Umsatzposition katapultieren könnte. RMAT-gestützte Assets wie Novartis' Kymriah-Erweiterungen im follikulären Lymphom heben die Bereitschaft des Kostenträgers hervor, kurative Absichtstherapien zu finanzieren. Präklinische Daten deuten darauf hin, dass iPSC-abgeleitete Auto-T-Konstrukte kryokonserviert werden können, ohne zytotoxische Potenz zu verlieren, wodurch Logistikkosten gesenkt und Studienrealisierbarkeit verbessert wird.
Über hämatologische Malignome hinaus profitieren solide Tumoranwendungen von Tandem-Gen-Bearbeitung-Techniken, die Checkpoint-Blockade-Modul In zelluläre Payloads einbetten und Persistenz In feindlichen Mikroumgebungen erhöhen. Diese Durchbrüche filtern In Neuro-Onkologie und seltene pädiatrische Krebsarten und erweitern die therapeutische Reichweite des Marktes für Regenerativ Medizin.
Nach Endbenutzer: Biobanken entstehen als kritische Infrastruktur
KrankenhäBenutzer und chirurgische Zentren repräsentierten 49,13% des Marktes für Regenerativ Medizin In 2024 Endbenutzer-Umsatz und spiegeln ihre Gatekeeper-Rolle In akuter Verabreichung wider.
Regulatoren entwerfen Rahmen, die Zustimmungs-, Eigentums- und Datenaustauschregeln klären, was wiederum Partnerschaften zwischen Biobanken und Therapieherstellern entsperrt. Wertschöpfungsketten-Integration von Sammlung bis Bettseite-Infusion wird voraussichtlich Bearbeitungszeiten komprimieren und Rückverfolgbarkeit verbessern. Diese Trends positionieren Biobanken als strategische Knoten, die verteilte Just-In-Zeit-Fertigungsmodelle ermöglichen.
Notiz: Segmentanteile aller einzelnen Segmente bei Berichtserwerb verfügbar
Geografieanalyse
Nordamerika kontrollierte 39,95% des Marktes für Regenerativ Medizin In 2024 und nutzte eine FDA-Struktur, die Durchbruchinnovation belohnt. Der RMAT-Pfad hat bereits mehrere erste Kandidaten ihrer Klasse grünes Licht gegeben, das wahrgenommene Entwicklungsrisiko gesenkt und substanzielle Kapitalzuflüsse ausgelöst. Novartis' 23 Milliarden USD Verpflichtung zur Fertigungserweiterung In den Vereinigten Staaten, mit sieben neuen Werken, die online kommen, veranschaulicht, wie Groß Pharma Lieferketten-Souveränität zementiert.[2]Novartis, "USD 23 Billion u.S. Herstellung Expansion Plan," novartis.com Frühe akademische Kooperationen, wie Mayo Clinics pädiatrisches Herz-Stammzell-Programm, speisen weiterhin die klinische Pipeline mit wirkungsstarken Indikationen. Persistente Erstattungsunterschiede schaffen jedoch Taschen begrenzten Zugangs selbst innerhalb einer allgemein Günstigen Umgebung.
Asien-Pazifik schreitet mit 16,22% CAGR voran, angetrieben von Japans adaptiven Lizenzregeln und Chinas 42% Anteil globaler industriegesponserte Studien In 2023. Harmonisierungsiniiativen bei Chinas NMPA reduzieren redundante Einreichungen und ermöglichen grenzüberschreitende Datennutzung. Staatlich unterstützte GMP-Hubs, typifiziert durch Wake Forest Institute für Regenerativ Medikamente mehrere-Orgel-Programm, skalieren Fertigungs-Know-how, das kleineren Unternehmen zugutekommt.[3]Wake Forest Institute für Regenerativ Medizin, "Translational Regenerativ Medizin Programs," wfirm.org Dennoch hemmen infrastrukturelle Lücken In Kälteketten-Logistik und Qualitätskontroll-Analytik noch die Geschwindigkeit, mit der Therapien über Tier-1-Städte hinaus expandieren.
Europa behält einen Wettbewerbsstandpunkt trotz regulatorischer Fragmentierung. Deutschland beherbergt die höchste Konzentration von Regenerativ-Medizin-Unternehmen, unterstützt durch eine kollaborative Forschungskultur und öffentlich-Privat Finanzierungsprogramme. Die Europäische Kommission hat begonnen, einheitliche Fortgeschritten-Therapie-Leitlinien zu entwerfen, mit dem Ziel, Fall-für-Fall-Bewertungen zu reduzieren, die derzeit Produktmarkteinführungen verlangsamen ec.europa.eu. Innovative Zahlungspilotprojekte, einschließlich meilensteinbasierter Erstattung In Italien für Gentherapie-Infusionen, helfen, klinischen Wert mit steuerlicher Umsicht zu versöhnen. Transatlantische Allianzen nehmen zu, mit EU-Unternehmen, die proprietäre Biomaterialien an uns-Entwickler lizenzieren, die spätphasige Studienexpertise bereitstellen.
Wettbewerbslandschaft
Die Wettbewerbslandschaft des Marktes für Regenerativ Medizin umfasst spezialisierte Biotechs, die frühe Entdeckung steuern, und Große Pharmaunternehmen, die spätphasige Assets skalieren. Novartis vertiefte sein Portfolio, indem es dazu überging, 91,04% der Anteile von MorphoSys AG In 2024 zu erwerben, ein Schritt, der onkologie-fokussierte Antikörper-Expertise In die Zell- und Gen-Plattform des Unternehmens integriert. Mittlere Unternehmen paaren sich mit Auftragsfertigungsorganisationen, um virale Vektor-Engpässe zu überwinden, während akademische Spin-offs hochwertige Entdeckungspipelines liefern.
Weiß-Raum-Opportunitäten bestehen In skalierbarer Fertigung und Nicht-Onkologie-Indikationen wie chronischer Nierenerkrankung und Autoimmunerkrankungen. Evoniks Markteinführung medizinisch-gradigen rekombinanten Kollagens zeigt, wie Materialwissenschaftsunternehmen Anteil erfassen, indem sie strukturelle Hürden im
Konsolidierung wird voraussichtlich beschleunigen, da vermarktete Gentherapien kommerzielle Modelle validieren. Etablierte Akteure suchen Plattformbreite, die allogene, Gen-Bearbeitung- und iPSC-Modalitäten umfasst, um Risiko zu diversifizieren und globale Kostenträger anzusprechen. Fertigungs-Exzellenzzentren entstehen als strategische Akquisitionsziele, weil sie sofortige Kapazität und regulatorisches Goodwill liefern. Diese graduelle Agglomeration wird voraussichtlich Gesamtservicestandards heben, dennoch weiterhin Raum für Nischeninnovatoren lassen.
Führende Unternehmen der Regenerativ Medizin Industrie
-
Smith+Nephew plc
-
Organogenesis Holdings Inc.
-
Baxter International Inc.
-
Medtronic
-
Integra LifeSciences Holdings Corporation
- *Haftungsausschluss: Hauptakteure in keiner bestimmten Reihenfolge sortiert
Jüngste Industrieentwicklungen
- Mai 2025: Malaysias Medizinisch Gerät Authority eröffnete Konsultation zu Nur-Export-Geräteregeln, im Einklang mit einer breiteren Ausnahmeverordnung. Der Entwurf, wenn implementiert, sollte grenzüberschreitende Sendungen vereinfachen und könnte indirekt Liefervorlaufzeiten für Zelltherapie-Hilfsgeräte verkürzen.
- April 2025: Rege Nephro erwarb Tamibarotene-Assets von Syros Arzneimittel zur Stärkung seines Autosomal Dominant polyzystisch Niere Krankheit-Programms, laut Unternehmensmitteilungen. Die Transaktion übertrug auch Fertigungsverträge und deutet an, dass Lieferketten-Eigentum schnell zu einem strategischen Vermögenswert In Bewertungsdiskussionen wird.
- Dezember 2024: Affimed erhielt FDA RMAT-Bezeichnung für seine Kombinationstherapie aus Acimtamig und Artiva Biotherapeutics' AlloNK zur Behandlung von rezidiviertem/refraktärem Hodgkin-Lymphom, basierend auf frühen Wirksamkeitsdaten, die eine 83,3% Gesamtansprechrate zeigten.
- September 2024: Poseida Therapeutika, Inc. sicherte sich die Regenerativ Medizin Fortgeschritten Therapie (RMAT)-Bezeichnung von der Vereint Staaten Lebensmittel Und Medikament Administration (FDA) für P-BCMA-ALLO1. Diese investigative Therapie, basierend auf Stammzell-Erinnerung-T-Zellen (TSCM), ist eine allogene Auto-T-Zellbehandlung In Phase-1/1b-klinischen Studien, die Patienten mit rezidiviertem oder refraktärem multiplem Myelom anvisiert.
Globaler Berichtsumfang für Regenerativ Medizin
Gemäß dem Umfang des Industrieberichts werden Regenerativ Medikamente verwendet, um Gewebe und Organe zu reparieren, ersetzen und regenerieren, die durch Verletzung, Krankheit oder den natürlichen Alterungsprozess betroffen sind. Diese Medikamente stellen die Funktionalität von Zellen und Geweben wieder her und werden In verschiedenen degenerativen Erkrankungen verwendet, wie Dermatologie, neurodegenerative Erkrankungen, kardiovaskuläre und orthopädische.
Der Markt für Regenerativ Medizin ist segmentiert nach Produkttyp, Zellherkunft, Quelle (Stammzelltyp), Anwendung, Endbenutzer und Geografie. Nach Produkttyp ist der Markt segmentiert In Zelltherapien, Gentherapien, Gewebe-Maschinenbau-Produkte, Biomaterialien und azelluläre Regenerativ Produkte (PRP, ECM). Nach Zellherkunft ist der Markt segmentiert In autolog, allogen und xenogen. Nach Quelle (Stammzelltyp) ist der Markt segmentiert In adulte Stammzellen, induzierte pluripotente Stammzellen, embryonale Stammzellen und hämatopoetische Stammzellen. Nach Anwendung ist der Markt segmentiert In Orthopädie & Muskuloskeletal, Dermatologie & Wundversorgung, Kardiovaskulär, Neurologie, Onkologie, Ophthalmologie und andere. Die anderen Anwendungen umfassen endokrine, renale, etc. Nach Endbenutzer ist der Markt segmentiert In KrankenhäBenutzer & chirurgische Zentren, Spezialkliniken, akademische & Forschungsinstitute und Biobanken & Zellbanken. Nach Geografie ist der Markt segmentiert In Nordamerika, Europa, Asien-Pazifik, Naher Osten und Afrika und Südamerika. Der Marktbericht deckt auch die geschätzten Marktgrößen und Trends für 17 verschiedene Länder über wichtige Regionen global ab. Der Marktbericht bietet den Wert (In Milliarden USD) für die oben genannten Segmente.
| Zelltherapien |
| Gentherapien |
| Tissue-Engineering-Produkte |
| Biomaterialien |
| Azelluläre regenerative Produkte |
| Autolog |
| Allogen |
| Xenogen |
| Adulte Stammzellen |
| Induzierte pluripotente Stammzellen |
| Embryonale Stammzellen |
| Hämatopoetische Stammzellen |
| Orthopädie & Muskuloskeletal |
| Dermatologie & Wundversorgung |
| Kardiovaskulär |
| Neurologie |
| Onkologie |
| Ophthalmologie |
| Andere |
| Krankenhäuser & chirurgische Zentren |
| Spezialkliniken |
| Akademische & Forschungsinstitute |
| Biobanken & Zellbanken |
| Nordamerika | Vereinigte Staaten |
| Kanada | |
| Mexiko | |
| Europa | Deutschland |
| Vereinigtes Königreich | |
| Frankreich | |
| Italien | |
| Spanien | |
| Restliches Europa | |
| Asien-Pazifik | China |
| Japan | |
| Indien | |
| Australien | |
| Südkorea | |
| Restliches Asien-Pazifik | |
| Naher Osten & Afrika | GCC |
| Südafrika | |
| Restlicher Naher Osten & Afrika | |
| Südamerika | Brasilien |
| Argentinien | |
| Restliches Südamerika |
| Nach Produkttyp | Zelltherapien | |
| Gentherapien | ||
| Tissue-Engineering-Produkte | ||
| Biomaterialien | ||
| Azelluläre regenerative Produkte | ||
| Nach Zellherkunft | Autolog | |
| Allogen | ||
| Xenogen | ||
| Nach Quelle | Adulte Stammzellen | |
| Induzierte pluripotente Stammzellen | ||
| Embryonale Stammzellen | ||
| Hämatopoetische Stammzellen | ||
| Nach Anwendung | Orthopädie & Muskuloskeletal | |
| Dermatologie & Wundversorgung | ||
| Kardiovaskulär | ||
| Neurologie | ||
| Onkologie | ||
| Ophthalmologie | ||
| Andere | ||
| Nach Endbenutzer | Krankenhäuser & chirurgische Zentren | |
| Spezialkliniken | ||
| Akademische & Forschungsinstitute | ||
| Biobanken & Zellbanken | ||
| Nach Geografie | Nordamerika | Vereinigte Staaten |
| Kanada | ||
| Mexiko | ||
| Europa | Deutschland | |
| Vereinigtes Königreich | ||
| Frankreich | ||
| Italien | ||
| Spanien | ||
| Restliches Europa | ||
| Asien-Pazifik | China | |
| Japan | ||
| Indien | ||
| Australien | ||
| Südkorea | ||
| Restliches Asien-Pazifik | ||
| Naher Osten & Afrika | GCC | |
| Südafrika | ||
| Restlicher Naher Osten & Afrika | ||
| Südamerika | Brasilien | |
| Argentinien | ||
| Restliches Südamerika | ||
Wichtige im Bericht beantwortete Fragen
Wie Groß ist die prognostizierte Marktgröße für Regenerativ Medizin bis 2030?
Der Sektor wird voraussichtlich etwa 88,85 Milliarden USD bis 2030 erreichen und spiegelt nachhaltiges zweistelliges Wachstum angetrieben von Gen- und Zelltherapien wider.
Welches Segment zeigt die schnellste CAGR zwischen 2025 und 2030?
Gentherapien werden voraussichtlich etwa 25,39% CAGR verbuchen und Zelltherapie- und Gewebe-Maschinenbau-Segmente übertreffen.
Wie Groß ist der Marktanteil allogener Zelltherapie In 2024?
Allogene Produkte halten etwa 55,14% Marktanteil und profitieren von standardisierten aus-Die-Regal-Fertigungseffizienzen.
Welche Region expandiert am schnellsten?
Asien-Pazifik führt mit geschätzten 16,22% CAGR, angetrieben von Japans progressiven Regulierungen und Chinas klinischen Studienaktivitäten.
Seite zuletzt aktualisiert am:



