药物警戒市场规模及份额
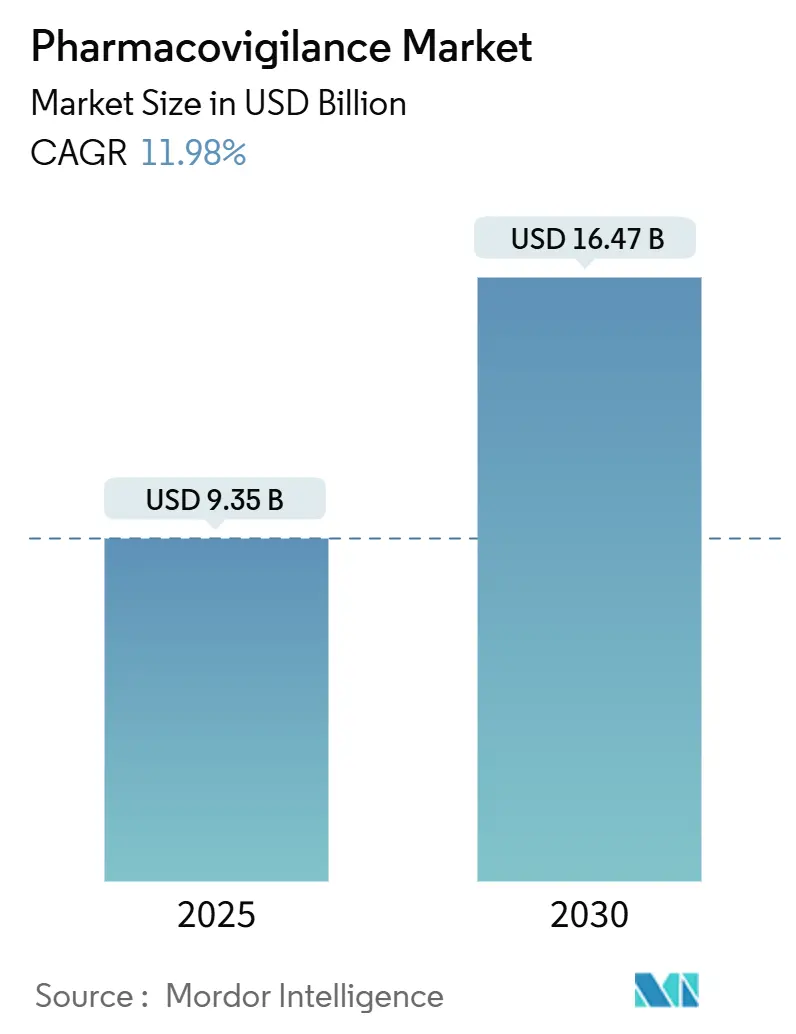
药物警戒市场分析 by 睿智信息
药物警戒市场2025年估值93.5亿美元,预计到2030年将达到164.7亿美元,以11.98%的复合年增长率增长。不断扩大的药物管线、更严格的上市后监督规则以及人工智能(AI)在安全监测工作流程中的快速采用维持了这一增长势头。[1]European Medicines Agency, "Guidance on the Application of the Amended Variations Regulation," ema.europa.eu 随着生物制剂、基因治疗和其他复杂疗法进入商业使用,制药公司正将资源重新投向主动安全管理。配备基于云的AI平台的合同研究组织(CRO)提供成本效益的合规性,加速了外包转移。上市后监督义务扩大了数据量,使电子健康记录(EHR)挖掘成为增长最快的报告方法。北美由于成熟的监管科学保持领导地位,但亚太地区(APAC)的协调倡议推动该地区实现双位数增长。[2]Food and Drug Administration, "International Regulatory Harmonization," fda.gov
关键报告要点
- 按服务提供商,合同外包在2024年以55.46%的收入份额领先;该细分市场正以13.73%的复合年增长率扩张至2030年。
- 按临床试验阶段,IV期上市后研究在2024年占药物警戒市场份额的32.18%,而临床前活动在2030年前呈现最高的13.13%复合年增长率。
- 按报告类型,自发性报告在2024年占药物警戒市场规模的43.45%;EHR挖掘预计在2025-2030年间以14.36%的复合年增长率增长。
- 按终端用户,制药公司在2024年占药物警戒市场规模的59.53%份额,医院在2030年前以14.45%的复合年增长率推进。
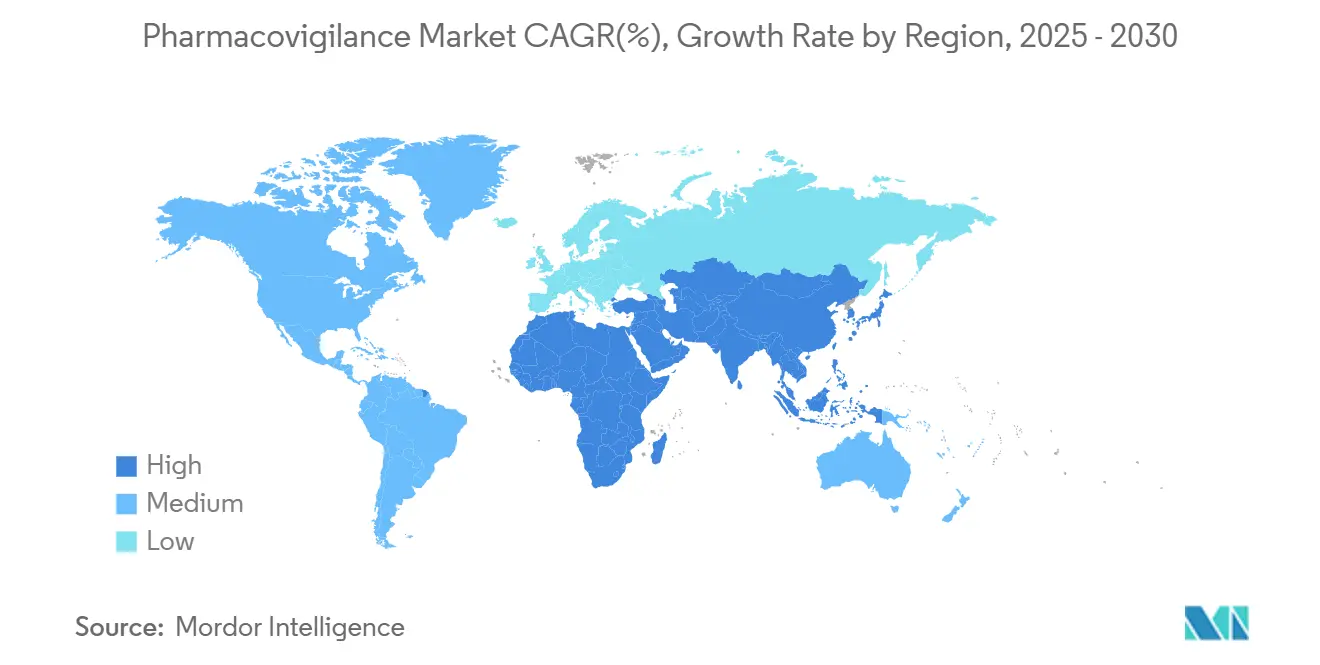
- 按地理位置,北美在2024年占药物警戒市场份额的44.18%,而亚太地区录得最快的13.64%复合年增长率至2030年。
全球药物警戒市场趋势及洞察
驱动因素影响分析
| 驱动因素 | (~) % 对复合年增长率预测的影响 | 地理相关性 | 影响时间线 |
|---|---|---|---|
| 不断上升的药物消费及开发管线 | +2.1% | 全球 | 长期 (≥ 4年) |
| 药物不良反应(ADR)发生率增加 | +1.8% | 全球,老龄化人口 | 中期 (2-4年) |
| PV服务外包给CRO/BPO供应商 | +2.3% | 北美及欧盟,亚太地区上升 | 短期 (≤ 2年) |
| AI驱动的信号检测及预测分析 | +1.9% | 北美及欧盟核心,向亚太地区扩散 | 中期 (2-4年) |
| 真实世界证据(RWE)平台的扩展 | +1.7% | 美国及欧盟领先,全球传播 | 长期 (≥ 4年) |
| 主动上市后安全的严格监管要求 | +2.0% | 全球 | 长期 (≥ 4年) |
| 来源: Mordor Intelligence | |||
不断增长的药物消费及开发管线
FDA在2024年批准了50个新分子实体,突显了突破性批准如何扩大每个申办者的上市后安全职责。[3]Food and Drug Administration, "Drug and Biologic Approvals," fda.gov基因治疗、CAR-T治疗和联合产品呈现独特的风险特征,需要在产品整个生命周期中进行警觉监测。有条件批准进一步提高了真实世界证据(RWE)预期,将预算重新导向持续监督基础设施。这些动态将药物警戒团队锁定在超越临床开发的长期扩张周期中,持续工作量增长。
药物不良反应(ADR)发生率增加
欧洲药品管理局(EMA)药物警戒风险评估委员会(PRAC)最近在观察到潜在的继发恶性肿瘤后,强调了对CAR-T受者的终身监测。[4]European Medicines Agency, "PRAC Meeting Highlights," ema.europa.eu老年人群中的多重用药增加了药物-药物相互作用,推高了ADR病例数量。疫情期间的疫苗推广验证了大规模信号检测网络的重要性,该网络能够在数周内处理数百万份安全报告。
PV服务外包给CRO/BPO供应商
申办者越来越多地将完整的药物警戒操作转移给维护全球合规中心和专用AI引擎的CRO。这些提供商无缝跨司法管辖区扩展,使中型生物技术公司能够满足复杂规则而不承担沉重的固定成本。印度和东欧的劳动套利模式也具有吸引力,但差异化现在取决于自动化摄入和预测性信号检测,而不是纯粹的成本节约。
AI驱动的信号检测及预测分析
IQVIA通过将大语言模型(LLM)副驾驶整合到日常工作流程中,目标是将常规病例处理费用减少50%。与此同时,Oracle在其安全平台中嵌入了先进的机器学习功能,以分流文献警报和自动化叙述写作。监管机构已通过草案指导做出回应,为AI在安全管理中的使用设定验证期望。
限制因素影响分析
| 限制因素 | (~) % 对复合年增长率预测的影响 | 地理相关性 | 影响时间线 |
|---|---|---|---|
| 网络安全及数据隐私风险 | -1.4% | 全球,欧盟及美国较高 | 短期 (≤ 2年) |
| 缺乏全球监管协调及数据标准 | -1.2% | 全球,新兴市场受影响最严重 | 长期 (≥ 4年) |
| 专业PV人才短缺及高离职率 | -1.6% | 北美及欧盟严重 | 中期 (2-4年) |
| 联合及ATMP治疗的复杂性 | -1.1% | 北美及欧盟,正在扩大 | 长期 (≥ 4年) |
| 来源: Mordor Intelligence | |||
网络安全及数据隐私风险
敏感患者数据的云部署使安全系统面临勒索软件和国家级入侵的风险。最近的医疗保健违规事件迫使数个申办者暂停EHR集成,同时进行审计以确保没有发生安全信号操控。《通用数据保护条例》(GDPR)和类似法律要求数据最小化和本地化策略,这些有时与全球分析目标冲突。
专业PV人才短缺及高员工离职率
行业调查预测,到2030年,随着AI技能、监管知识和治疗专业化融合成单一档案,合格的药物警戒专业人员将短缺35%。组织通过学徒计划和内部学院做出回应,但培养时间可能超过两年,造成近期瓶颈。
细分市场分析
按临床试验阶段:上市后监督推动增长
IV期研究在2024年占药物警戒市场份额的32.18%,反映了监管机构对创新疗法终身监测的需求。与临床前安全评估相关的药物警戒市场规模预计将以13.13%的复合年增长率扩张,这得益于基于风险的早期分析。适应性试验设计缩短了II期和III期,但提高了产品到达广泛人群后高保真度信号检测的重要性。更新的ICH E6(R3)指南迫使申办者在所有阶段嵌入质量设计指标,确保从首次人体给药开始可追踪的安全数据采集。
药物警戒市场通过将分散试验与直接对患者采样和可穿戴传感器相整合做出回应。AI模型在首次患者给药前模拟脱靶效应,为公司在风险管理规划方面提供先机。随着有条件批准的增加,授权后安全研究(PASS)预算超过传统III期支出,将IV期主导地位锁定在长期前景中。
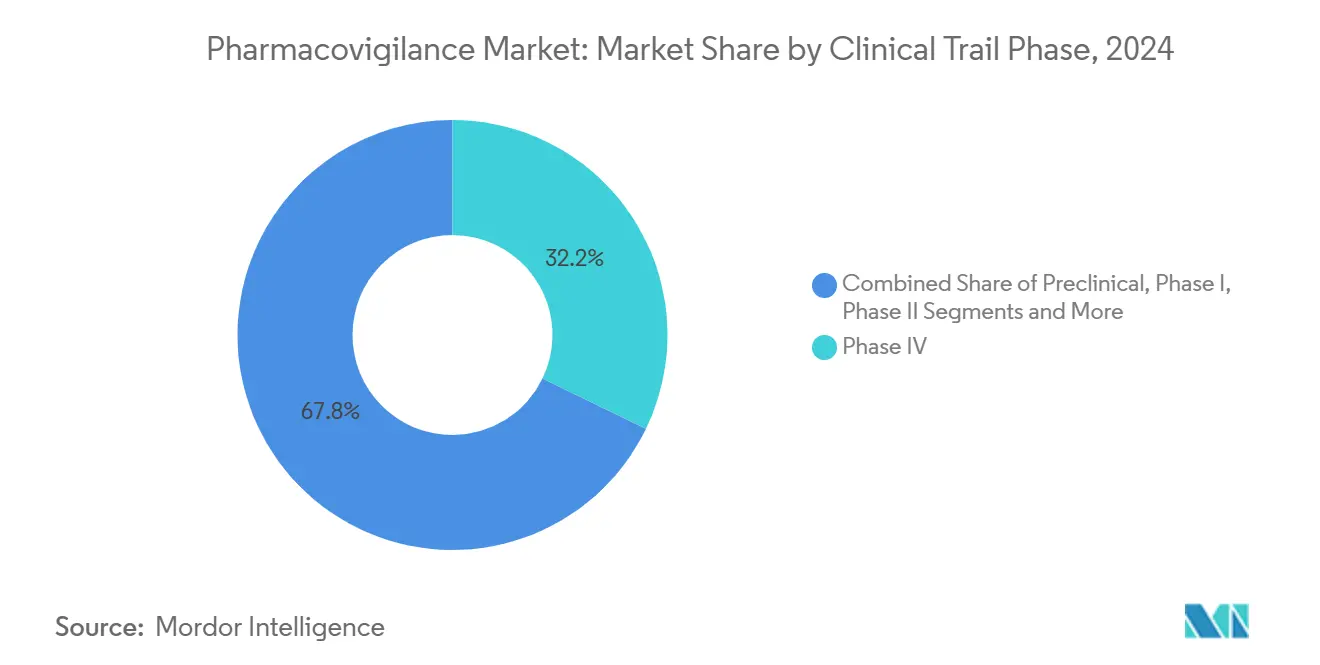
备注: 购买报告后可获得所有单个细分市场的细分份额
按服务提供商:外包通过技术整合加速
合同外包在2024年控制了55.46%的总收入,预计到2030年将以13.73%的速度增长,维持药物警戒市场的最大份额。内部单位保留关键决策制定,但越来越依赖CRO平台处理常规任务的混合模式。Parexel与Palantir的多年AI协议等战略联盟例证了技术增强型CRO如何培养竞争优势。
药物警戒行业现在重视可扩展的数据湖、用于科学文献的自然语言处理(NLP)和摄入中的机器人流程自动化。因此,即使是大型制药公司也将工作负载迁移到印度、爱尔兰和东欧的外部中心,将分散的供应商名单整合为保证AI投资路线图的主服务协议。
按报告类型:EHR挖掘成为技术颠覆者
自发性报告在2024年仍然是支柱,占43.45%,但与EHR挖掘相关的药物警戒市场规模预计将呈现最快的14.36%复合年增长率。FDA关于RWE的最终指导为自动提取结构化和非结构化临床数据以增强传统病例提交打开了大门。
AI算法解析医师笔记、实验室结果和影像资料库,比自发报告提前数周揭示隐藏的安全趋势。如赛诺菲的ARTEMIS项目等使用NLP引擎每年处理超过700,000个病例,释放人类专家进行根本原因分析。标准化障碍仍然存在,特别是在数据来源方面,但向自动化RWE摄入的轨迹是明确的。
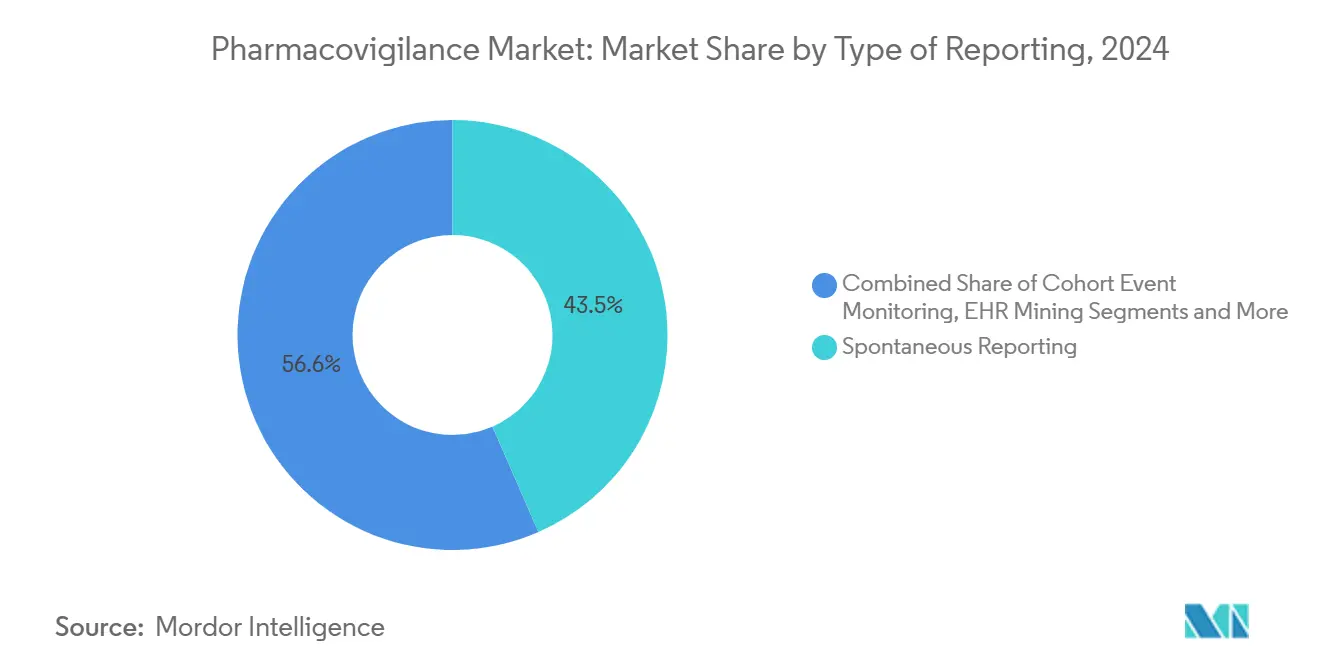
备注: 购买报告后可获得所有单个细分市场的细分份额
按终端用户:医院整合转变安全监测
制药公司占2024年支出的59.53%,但医院系统录得最高的14.45%复合年增长率,因为分散和实用试验将安全责任置于更接近护理点。与综合递送网络相关的药物警戒市场规模上升,因为医院部署RWE平台,向申办者提供近实时安全数据。
BARDA与Allucent的五年协议说明了政府资金如何加速医院参与对策试验。然而,互操作性差距和隐私法规仍然减缓跨境数据交换,延长过渡期。
地理分析
北美由于高研发强度、先进的EHR渗透率和明确的监管期望,在2024年占药物警戒市场的44.18%。随着FDA发布分步验证框架,AI试点获得快速接受,使该地区成为数字药物警戒的全球参考。
欧洲紧随其后,成熟的立法支撑EudraVigilance网络和新的AI反思文件,鼓励创新的同时要求算法透明度。对先进治疗药物的关注带来了专业监测需求,维持到2030年的投资。欧盟基础PASS的药物警戒市场规模随着孤儿药批准而增长。
亚太地区预计录得13.64%的复合年增长率,为全球最快,因为中国的监管改革和印度扩大的临床试验格局汇合。东盟国家统一标签和电子提交标准,简化多国安全活动。对国内生物技术制造的投资刺激了对本地化病例处理中心的需求。中东及非洲和南美洲随着药物警戒基础设施与药品进口量和新兴制造集群的规模化增加增量增长。
竞争格局
药物警戒市场呈现中等分化。IQVIA、ICON和Parexel保持相当规模的全球足迹,但以软件为先的提供商如ArisGlobal和Oracle正通过以AI为中心的产品缩小差距。ArisGlobal用LLM驱动的分流升级了其LifeSphere套件,在2024年看到了创纪录的新客户浪潮。
战略交易定义了竞争叙述。ICON对PRA Health Sciences的收购将两个全服务CRO整合在一个AI平台下,增加了上市后和真实世界研究的规模。赛诺菲与OpenAI和Formation Bio的合作标志着大型制药公司对垂直整合AI软件开发的兴趣。
在先进细胞和基因治疗监督、儿科药物安全以及日语和汉语源文档的NLP解决方案中,白色空间利基持续存在。提供即插即用安全云或基于令牌的数据交换模式的新进入者可能从缓慢现代化遗留平台的在位者手中夺取份额。
药物警戒行业领导者
-
高知特
-
凯捷
-
埃森哲
-
威普罗有限公司
-
IBM
- *免责声明:主要玩家排序不分先后
近期行业发展
- 2025年1月:ArisGlobal报告了其LifeSphere平台的显著客户增长和产品增强。
- 2024年9月:IQVIA推出其AI助手,通过综合庞大的医疗数据集加速信号检测。
- 2024年9月:勃林格殷格翰将LifeSphere MultiVigilance平台扩展到日本,加强亚太能力。
- 2024年5月:赛诺菲、Formation Bio和OpenAI公布了AI合作伙伴关系,以缩短药物开发和安全时间线。
全球药物警戒市场报告范围
药物警戒是与检测、评估、理解和预防不良反应或任何其他药物相关问题相关的科学和活动组。药物警戒专注于ADR(药物不良反应)和药物毒性。药物警戒市场包括在医院、药房和其他医疗保健部门进行临床试验期间进行的所有类型的不良事件报告。药物警戒市场按临床试验阶段(临床前、I期、II期、III期和IV期)、服务提供商(内部和合同外包)、报告类型(自发性报告、强化ADR报告、目标自发性报告、队列事件监测和EHR挖掘)、终端用户(医院、制药公司和其他终端用户)和地理位置(北美、欧洲、亚太、中东和非洲以及南美洲)进行细分。市场报告还涵盖全球主要地区17个不同国家的估计市场规模和趋势。报告为上述细分市场提供价值(以十亿美元计)。
| 临床前 |
| I期 |
| II期 |
| III期 |
| IV期 |
| 内部 |
| 合同外包 |
| 自发性报告 |
| 强化ADR报告 |
| 目标自发性报告 |
| 队列事件监测 |
| EHR挖掘 |
| 医院 |
| 制药公司 |
| CRO及其他终端用户 |
| 北美 | 美国 |
| 加拿大 | |
| 墨西哥 | |
| 欧洲 | 德国 |
| 英国 | |
| 法国 | |
| 意大利 | |
| 西班牙 | |
| 欧洲其他地区 | |
| 亚太地区 | 中国 |
| 日本 | |
| 印度 | |
| 澳大利亚 | |
| 韩国 | |
| 亚太其他地区 | |
| 中东和非洲 | 海湾合作委员会 |
| 南非 | |
| 中东和非洲其他地区 | |
| 南美洲 | 巴西 |
| 阿根廷 | |
| 南美洲其他地区 |
| 按临床试验阶段 | 临床前 | |
| I期 | ||
| II期 | ||
| III期 | ||
| IV期 | ||
| 按服务提供商 | 内部 | |
| 合同外包 | ||
| 按报告类型 | 自发性报告 | |
| 强化ADR报告 | ||
| 目标自发性报告 | ||
| 队列事件监测 | ||
| EHR挖掘 | ||
| 按终端用户 | 医院 | |
| 制药公司 | ||
| CRO及其他终端用户 | ||
| 按地理位置 | 北美 | 美国 |
| 加拿大 | ||
| 墨西哥 | ||
| 欧洲 | 德国 | |
| 英国 | ||
| 法国 | ||
| 意大利 | ||
| 西班牙 | ||
| 欧洲其他地区 | ||
| 亚太地区 | 中国 | |
| 日本 | ||
| 印度 | ||
| 澳大利亚 | ||
| 韩国 | ||
| 亚太其他地区 | ||
| 中东和非洲 | 海湾合作委员会 | |
| 南非 | ||
| 中东和非洲其他地区 | ||
| 南美洲 | 巴西 | |
| 阿根廷 | ||
| 南美洲其他地区 | ||
报告中回答的关键问题
药物警戒市场的当前价值是多少?
药物警戒市场2025年估值93.5亿美元。
药物警戒市场到2030年增长有多快?
预计将以11.98%的复合年增长率扩张,到2030年达到164.7亿美元。
哪种服务模式占最大的药物警戒市场份额?
合同外包以2024年55.46%的收入领先。
为什么亚太地区是增长最快的地区?
中国、印度和东盟国家的监管协调加上大型制造投资推动亚太地区13.64%的复合年增长率。
页面最后更新于: