人胚胎干细胞市场规模及份额
Mordor Intelligence人胚胎干细胞市场分析
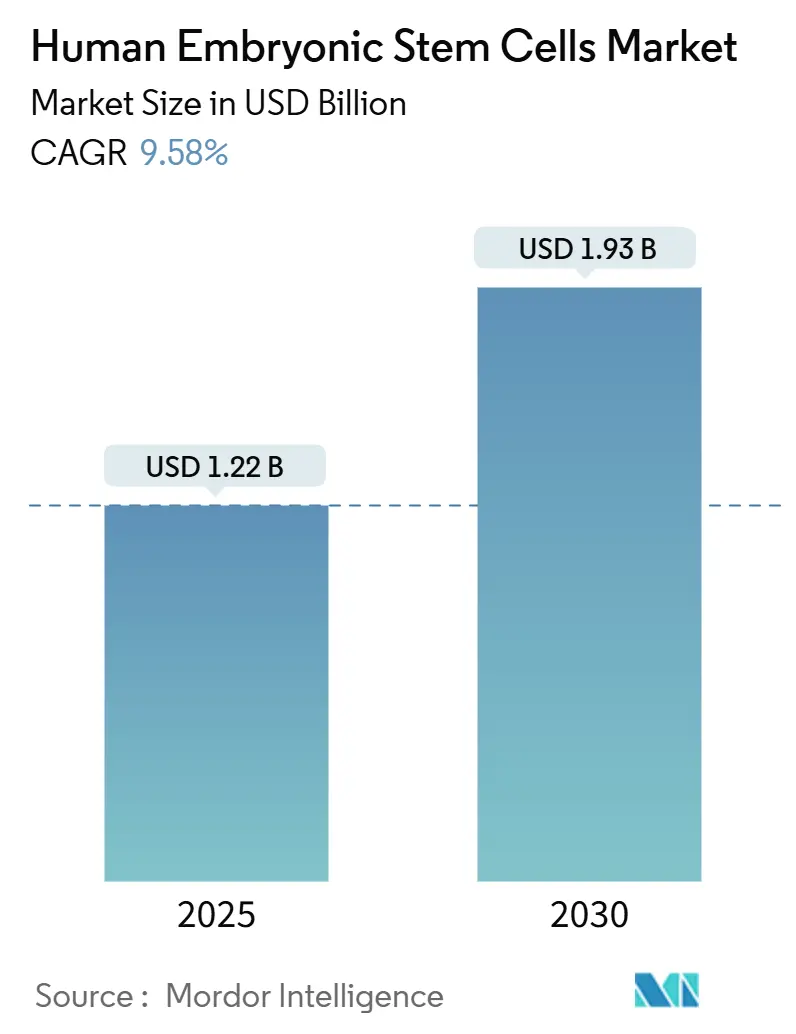
人胚胎干细胞市场规模估计2025年为12.2亿美元,预计到2030年达到19.3亿美元,预测期间(2025-2030)复合年增长率为9.58%。
CRISPR启动的细胞株工程技术进步、来源符合伦理的剩余IVF胚胎池稳步增长,以及无异种GMP培养系统的商业化应用,共同扩展了心脏、视网膜和内分泌疾病的治疗前景。随着自动化、封闭式生物工艺技术降低污染风险并将批次产量提升一倍,工业采用率上升,为人胚胎干细胞市场的早期参与者锐化竞争优势。[1]来源:Rebecca Ihilchik & Stacey Johnson,《AI赋能生物制造创新提升细胞与基因疗法的可及性和可负担性》,ISCT Global,isctglobal.org以FDA的RMAT通道和日本快速审批为例的监管支持,加速了从临床到市场的时间线,并吸引了数十亿美元的资金承诺。与此同时,基因编辑先驱与制造专家之间的跨学科合作压缩了开发周期,并扩大了人胚胎干细胞市场的知识产权防御性。加剧的伦理激进主义和不断上升的成本压力仍是值得关注的要点,但技术驱动的生产力提升有望抵消近期逆风。
关键报告要点
- 按应用划分,再生医学在2024年占据人胚胎干细胞市场58.57%的份额,而干细胞生物学研究在2030年前以10.86%的复合年增长率推进。
- 按产品类型划分,hESC细胞株在2024年占据人胚胎干细胞市场规模53.12%的份额;培养基与试剂预计在2025年至2030年间以11.69%的复合年增长率扩张。
- 按地理位置划分,北美在2024年以42.16%的收入份额领先,而亚太地区预计将以11.41%的复合年增长率实现2030年前最快增长。
全球人胚胎干细胞市场趋势与洞察
驱动因素影响分析
| 驱动因素 | (~) % 对复合年增长率预测的影响 | 地理相关性 | 影响时间线 |
|---|---|---|---|
| 心脏和恶性疾病高发病率 | +1.8% | 全球,集中在北美和欧洲 | 中期(2-4年) |
| 再生医学需求增长 | +2.1% | 全球,亚太增长市场领先 | 长期(≥ 4年) |
| 政府和私人资助项目增长 | +1.5% | 北美、欧洲、日本 | 短期(≤ 2年) |
| CRISPR启动的hESC细胞株工程 | +1.2% | 全球,美国、英国、日本的研发中心 | 中期(2-4年) |
| 无异种GMP培养系统降低污染风险 | +0.9% | 全球制造中心 | 短期(≤ 2年) |
| 剩余IVF胚胎扩大符合伦理的hESC供应 | +0.7% | 具有成熟IVF基础设施的地区 | 长期(≥ 4年) |
| 来源: Mordor Intelligence | |||
心脏和恶性疾病高发病率
心血管疾病和癌症合计占全球死亡率的大部分,为多谱系修复解决方案创造了持续的临床需求。人胚胎干细胞衍生的心脏球体在猪心梗模型中恢复收缩性,目前正进入首次人体缺血性心肌病试验。hESC衍生的胰岛细胞(VX-880)在12名1型糖尿病患者中的10名实现了胰岛素独立,突显了应用潜力的广度。随着人群水平心脏护理支出超过3500亿美元,商业兴趣加剧,将心脏代谢项目定位为人胚胎干细胞市场内的头条价值驱动因素。增材制造突破,如植入hESCs的3D打印心肌支架,进一步缩短转化路径。[2]来源:Sena Quinn,《用人干细胞3D打印心脏组织》,救生艇基金会,lifeboat.com这些数据总体验证了疾病修正潜力,并加强了到2030年的溢价定价机会。
再生医学需求增长
美国超过1200项活跃的细胞与基因治疗试验展示了再生医学如何从边缘走向前线护理。依赖人胚胎干细胞的异体平台实现了现成给药,解决了自体程序的历史规模限制。日本60多项iPS细胞研究说明了凝聚性政策、报销明确性和制造激励如何促进加速采用。FDA对间充质基质细胞疗法的里程碑式批准标志着监管机构准备清除临床验证产品,间接惠及hESC开发者。使用hESC衍生角膜上皮的视力恢复成功(≥90%疗效)提升了公众信任,为患者招募和投资者流入创造了正反馈循环。
政府和私人资助项目增长
CIRM的50亿美元捐赠基金将美国锚定为转化研究的资本丰富环境。公共拨款降低了早期研究风险,吸引风险投资和人胚胎干细胞市场的战略制药合作伙伴。日本的有条件批准框架补充了国家支持的基础设施支出,促使全球公司在东京附近建立GMP设施以更快进入市场。在私人方面,多年机构合同--如BARDA的干细胞衍生血小板项目--说明了扩展国防和应急响应用例,这些用例使收入来源多样化。这些并行资助渠道放大了发现速度并压缩了商业化风险。
CRISPR启动的hESC细胞株工程
CRISPR引物编辑在多能细胞中实现了36-73%的靶向效率,实现了同源疾病模型和低免疫原性治疗细胞株的快速构建。Cas12a多重系统现在允许同时插入多个编辑,加速候选物筛选周期。消除HLA-A、-B和-C抗原的概念验证工作显示了通用供体细胞的前景,尽管免疫活性小鼠的移植排斥强调了组合免疫逃避策略的需要。在Wellcome Sanger研究所生成的大规模变体库为靶点验证和毒性筛选提供了无与伦比的资源。总体而言,精密编辑降低了下游损耗并增强了人胚胎干细胞市场的产品组合可选性。
限制因素影响分析
| 限制因素 | (~) % 对复合年增长率预测的影响 | 地理相关性 | 影响时间线 |
|---|---|---|---|
| 高治疗和生产成本 | -1.4% | 全球,特别是成本敏感市场 | 中期(2-4年) |
| 严格且异质的全球法规 | -1.1% | 全球,地区强度不同 | 长期(≥ 4年) |
| 快速增长的iPSC替代品蚕食资金 | -0.8% | 全球研发中心 | 中期(2-4年) |
| 社交媒体驱动的伦理激进主义抑制采用 | -0.6% | 主要是西方市场 | 短期(≤ 2年) |
| 来源: Mordor Intelligence | |||
高治疗和生产成本
当前基于hESC的疗法通常超过每剂10万美元,这由手动洁净室操作和低工艺产率驱动。AI指导的机器人技术将劳动投入削减50%并提供批次间一致性,指向五年内低于5万美元的盈亏平衡制造。赛默飞世尔在新泽西州4.75亿美元的CDMO站点体现了针对成本压缩和法规合规的行业规模投资。模块化机器人集群可重复处理扩增、收获和最终灌装-完成,缩短活动时间并降低批次失败风险。来自东北大学的预测AI模型进一步优化营养供给和传代时机,将产量推向工业基准。这些收益必须保持势头以抵消付费者审查和价格敏感新兴市场需求。
严格且异质的全球法规
开发者需要应对拼凑式的批准要求,从欧盟2027年SoHO法规到FDA对无证诊所的分步执法。[3]来源:Sarah Rosenthaler,《欧盟人体来源物质新法规》,Schoenherr,schoenherr.eu日本的胚胎模型指导原则计划在2025年修订,说明前瞻性政策如何能够刺激投资,但也重塑合规工作负荷。国际细胞与基因治疗学会的亚太路线图旨在协调,但在采用之前,不同档案会增加管理成本。美国围绕联邦资助禁令的政治话语为长期资本规划增加了不确定性。
细分分析
按应用:再生医学推动临床转化
再生医学在2024年占据人胚胎干细胞市场58.57%的份额,受到临床读出的支撑,如OpRegen在地理性萎缩患者中+5.5字母视力提升。脊髓修复、胰岛细胞替代和心脏肌肉重建现在成为多中心试验的头条,加强了该细分市场在人胚胎干细胞市场内的主导收入轨迹。随着更多项目获得RMAT或Sakigake指定,付费者获得真实世界证据来证明报销合理性,推动良性采用周期。
干细胞生物学研究记录到2030年10.86%的复合年增长率,受益于自动化基因组编辑筛选和能够重现人体组织复杂性的类器官平台。CRISPR驱动的谱系追踪和高含量表型组学缩短了靶点识别时间线,而新颖的类器官共培养系统将疾病模型准确性提高了五倍。随着学术核心设施转向付费服务模式,研究支出回流到试剂和细胞株许可使用费,扩大了供应链参与者的经常性收入池。发现应用的人胚胎干细胞市场规模预计将随着多重筛选成为精准医学管线的组成部分而稳步攀升。

备注: 购买报告后可获得所有单独细分市场的细分份额
按产品类型:hESC细胞株主导,培养基和试剂增长强劲
商业化建立的hESC细胞株在2024年占据人胚胎干细胞市场规模53.12%的份额,受到可扩展主细胞库基础设施和成熟监管先例的支撑。通用供体编辑策略承诺更广泛的患者覆盖,无需定制制造,保持细胞株许可对寻求快速进入的大型制药公司的吸引力。来自Lonza的GMP培养基、试剂和辅助试剂盒形成高利润供应层;定制无异种配方通过工艺验证周期锁定经常性需求。
培养基和试剂以11.69%的复合年增长率扩张,搭乘个性化医学浪潮,特别是对于患者特异性矫正可最小化排斥风险的遗传性疾病。仪器和耗材供应商通过捆绑硬件-软件套件利用这一转变,例如Terumo-CiRA的自动化iPS细胞工作站实现90%的劳动节省。随着生产成本下降,自体管线可能获得利基孤儿疾病市场,补充大众市场异体产品。

备注: 购买报告后可获得所有单独细分市场的细分份额
地理分析
北美在2024年保持了全球收入42.16%的份额,这得益于强劲的NIH和CIRM资助、RMAT启动的快速通道审查以及广泛的CDMO产能。斯坦福领导的心脏试验、西北大学的脊髓倡议以及赛默飞世尔新的普林斯顿站点共同展示了该地区从实验室到市场的整合。围绕胚胎研究联邦资助的政治不确定性构成战略风险,但多样化的私人投资缓冲了潜在的公共预算波动。
亚太地区是增长最快的集群,凭借日本的有条件批准制度和中国国家支持的研究园区,到2030年以11.41%的复合年增长率推进。超过60项活跃的日本临床试验突出了监管敏捷性,而住友制药和尼康-Lonza制造联盟证明了来自跨国合作伙伴的资本流入。政府拨款涵盖设施建设和劳动力培训,在人胚胎干细胞市场内放大当地供应链成熟度。
欧洲的前景取决于2027年SoHO法规的有效推出。德国和英国维持着领先的学术集群;英国的合成胚胎实践规范标志着可能塑造大陆标准的政策创新。法国和意大利专注于眼科和软骨修复利基,而斯堪的纳维亚财团投资低温物流以扩大患者准入。西欧报销障碍持续存在,但跨境合作和欧盟范围内的HTA改革预计将简化认证产品的市场准入。

竞争格局
竞争是温和的,其特征是大型制药公司和追求同类首创适应症的利基生物技术公司的混合。Vertex Pharmaceuticals利用集中的研发支出提供VX-880数据,显示83%的治疗患者实现胰岛素独立,验证了单一资产深度的价值。Lineage Cell Therapeutics体现了管线广度,同时进行晚期眼科和早期脊髓项目以对冲开发风险。阿斯利康制药与安川的机器人联盟指向制造可扩展性作为关键战场,其中周期时间减少直接转化为竞争定价。
新兴技术进入者,包括尼康和OmniaBio,将AI启动的质量控制算法货币化,在每百万细胞成本指标上进行差异化。通用供体细胞工程是一个空白空间领域,学术-产业财团竞相完善能够逃避补体和NK细胞反应的多基因编辑平台。
随着第一代hESC细胞株的专利悬崖临近,品牌权益将越来越依赖制造能力和临床结果数据集,而不是基本知识产权保护。竞争的整体基调表明进一步整合,因为规模成为应对全球监管分歧不可缺少的要素。
人胚胎干细胞行业领导者
默克集团
STEMCELL Technologies Inc.
Vertex Pharmaceuticals
赛默飞世尔科技公司
Lineage Cell Therapeutics Inc.
- *免责声明:主要玩家排序不分先后

近期行业发展
- 2024年9月:艾伦研究所和NYSCF合作将结构细胞标签整合到种族多样化干细胞库中,以改善疾病模型包容性。
- 2024年9月:EPFL启动SCOL,一个共享类器官和iPSC设施,为所有校园研究组的转化干细胞项目提供服务。
全球人胚胎干细胞市场报告范围
人胚胎干细胞是从囊胚(早期植入前胚胎)的内细胞团中提取的多能干细胞。这些干细胞用于治疗各种疾病。
人胚胎干细胞市场按应用和地理位置进行细分。按应用划分,市场细分为再生医学、干细胞生物学研究、组织工程和毒理学测试。按地理位置划分,市场细分为北美、欧洲、亚太、中东与非洲以及南美。对于每个细分市场,市场规模以美元价值提供。
| 再生医学 |
| 干细胞生物学研究 |
| 组织工程 |
| 毒理学测试 |
| hESC细胞株 |
| 培养基与试剂 |
| 仪器与耗材 |
| 北美 | 美国 |
| 加拿大 | |
| 墨西哥 | |
| 南美 | 巴西 |
| 阿根廷 | |
| 南美其他地区 | |
| 欧洲 | 德国 |
| 英国 | |
| 法国 | |
| 意大利 | |
| 西班牙 | |
| 欧洲其他地区 | |
| 亚太 | 中国 |
| 日本 | |
| 印度 | |
| 澳大利亚 | |
| 韩国 | |
| 亚太其他地区 | |
| 中东与非洲 | 海湾合作委员会 |
| 南非 | |
| 中东与非洲其他地区 |
| 按应用 | 再生医学 | |
| 干细胞生物学研究 | ||
| 组织工程 | ||
| 毒理学测试 | ||
| 按产品类型 | hESC细胞株 | |
| 培养基与试剂 | ||
| 仪器与耗材 | ||
| 按地理位置 | 北美 | 美国 |
| 加拿大 | ||
| 墨西哥 | ||
| 南美 | 巴西 | |
| 阿根廷 | ||
| 南美其他地区 | ||
| 欧洲 | 德国 | |
| 英国 | ||
| 法国 | ||
| 意大利 | ||
| 西班牙 | ||
| 欧洲其他地区 | ||
| 亚太 | 中国 | |
| 日本 | ||
| 印度 | ||
| 澳大利亚 | ||
| 韩国 | ||
| 亚太其他地区 | ||
| 中东与非洲 | 海湾合作委员会 | |
| 南非 | ||
| 中东与非洲其他地区 | ||
报告中回答的关键问题
当前人胚胎干细胞市场规模是多少?
市场在2025年达到12.2亿美元,并有望稳步扩张。
预计到2030年的复合年增长率(CAGR)是多少?
预测复合年增长率为9.58%,将市场价值提升至2030年的19.3亿美元。
哪个应用领域目前占据最大收入份额?
再生医学以2024年58.57%的份额领先,得到不断推进的心脏、视网膜和内分泌项目支持。
哪个地区预计将实现最快增长?
亚太地区预计到2030年以11.41%的复合年增长率增长,受日本快速审批和中国不断扩张的研究基础设施推动。
更广泛采用的主要成本障碍是什么?
GMP制造成本使剂量价格保持在10万美元以上,尽管AI驱动的自动化正将生产费用削减多达50%。
CRISPR技术如何增强人胚胎干细胞产品?
CRISPR引物编辑提供36-73%的编辑效率,实现低免疫原性通用供体细胞株和高保真疾病模型,加速临床转化。
页面最后更新于:



