Tamanho e Participação do Mercado de Teste de Validade de Espécimes
Análise do Mercado de Teste de Validade de Espécimes pela Mordor Intelligence
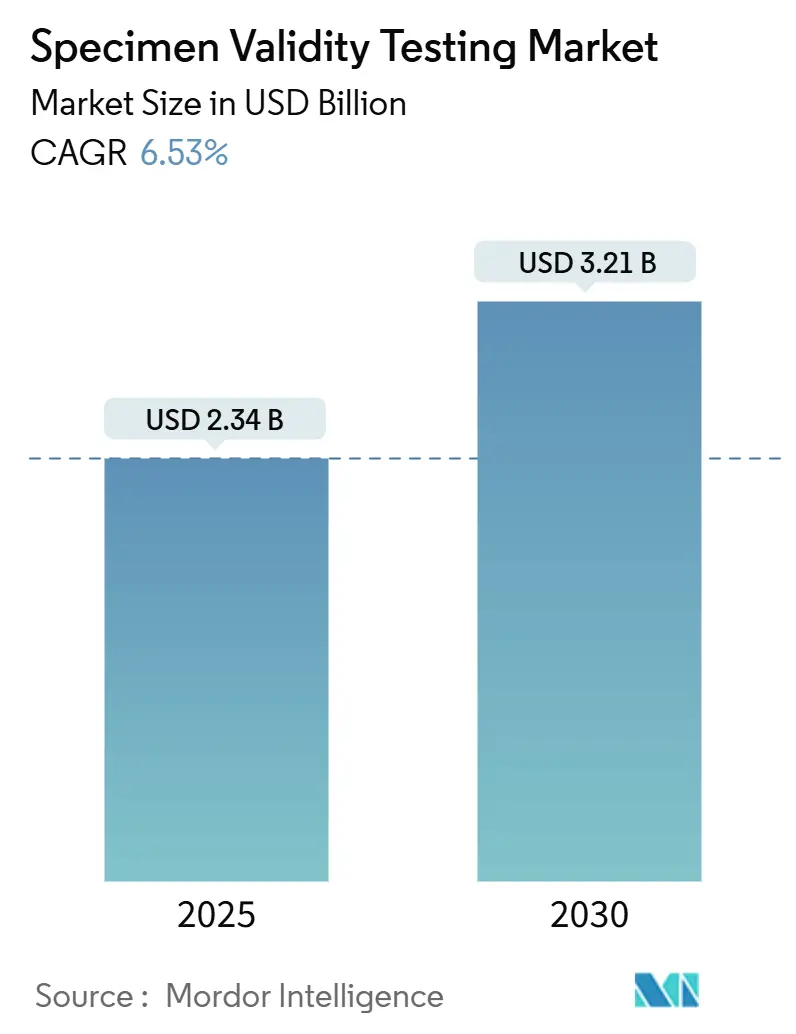
O tamanho do mercado de teste de validade de espécimes está avaliado em USD 2,34 bilhões em 2025 e está projetado para alcançar USD 3,21 bilhões até 2030, avançando a uma TCAC de 6,53%. A trajetória reflete o enrijecimento de mandatos de segurança no local de trabalho, adoção acelerada de plataformas de teste no ponto de atendimento (POC) e atualizações tecnológicas que detectam tentativas sofisticadas de adulteração. Empregadores nos setores de transporte, energia e saúde continuam a ampliar a cobertura de testes, enquanto atualizações governamentais-como a expansão do painel federal de janeiro de 2025 que agora inclui fentanil e norfentanil-elevam o padrão de integridade para todos os laboratórios. O aumento do uso de telessaúde também abriu um novo canal de coleta remota, impulsionando a demanda por dispositivos à prova de adulteração e análises orientadas por IA que verificam a integridade do espécime em tempo real. Embora matrizes não urinárias estejam ganhando favor, o mercado de teste de validade de espécimes permanece sustentado por programas de urina de alto volume que ainda dominam ambientes regulamentados.
Principais Conclusões do Relatório
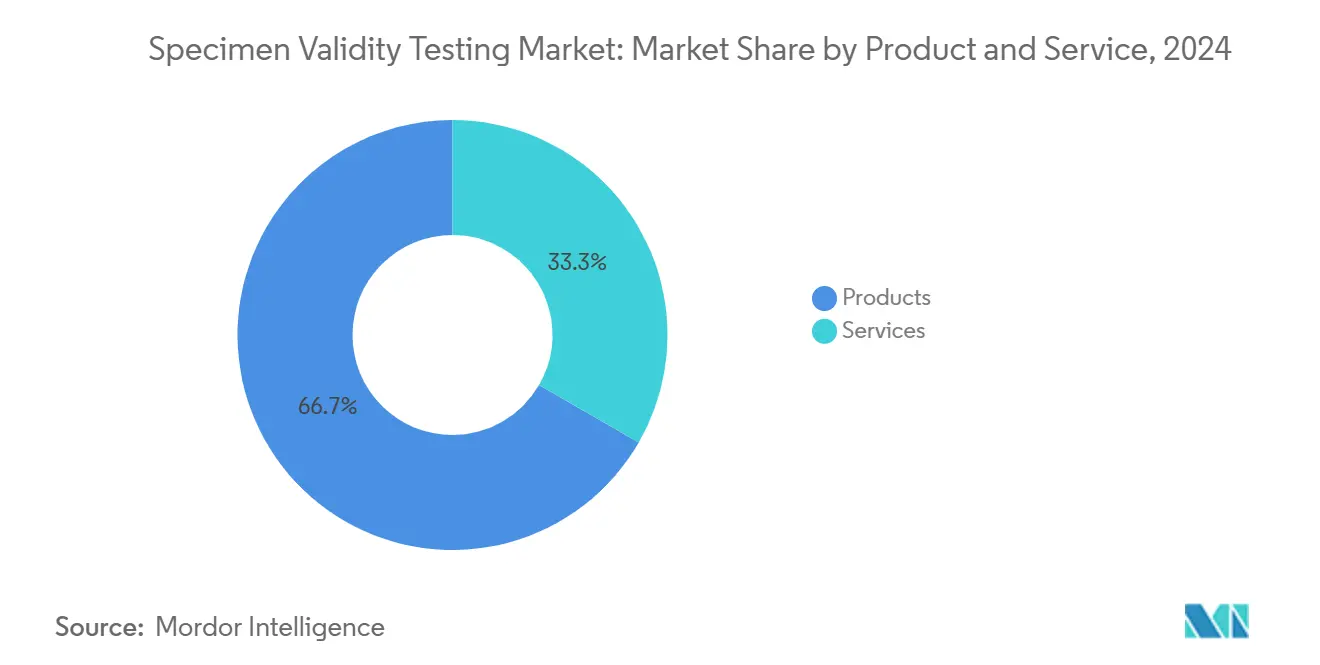
- Por produto e serviço, produtos consumíveis mantiveram 66,67% da participação de receita em 2024, enquanto os serviços estão previstos para registrar a TCAC mais rápida de 7,21% até 2030.
- Por tipo, teste laboratorial deteve 59,65% da participação do mercado de teste de validade de espécimes em 2024, enquanto plataformas POC estão programadas para expandir a uma TCAC de 7,29% até 2030.
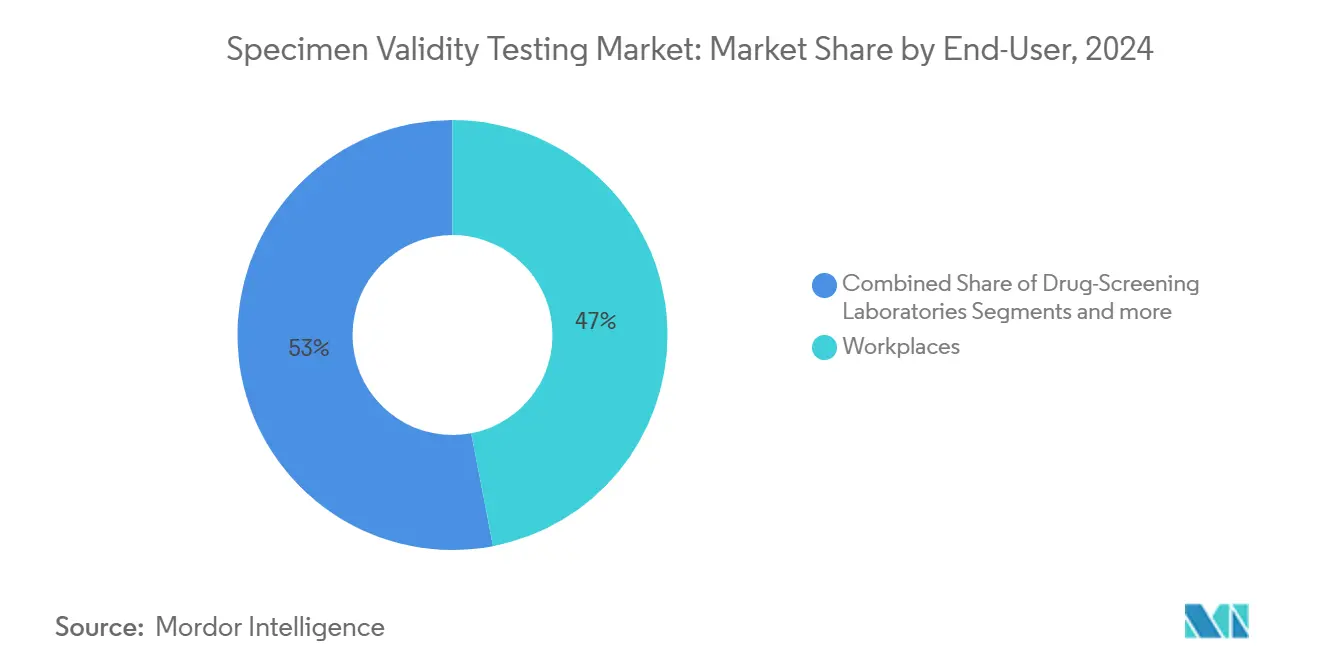
- Por usuário final, programas no local de trabalho lideraram com 46,98% da participação de receita em 2024; laboratórios de triagem de drogas registram a maior TCAC projetada de 7,33% até 2030.
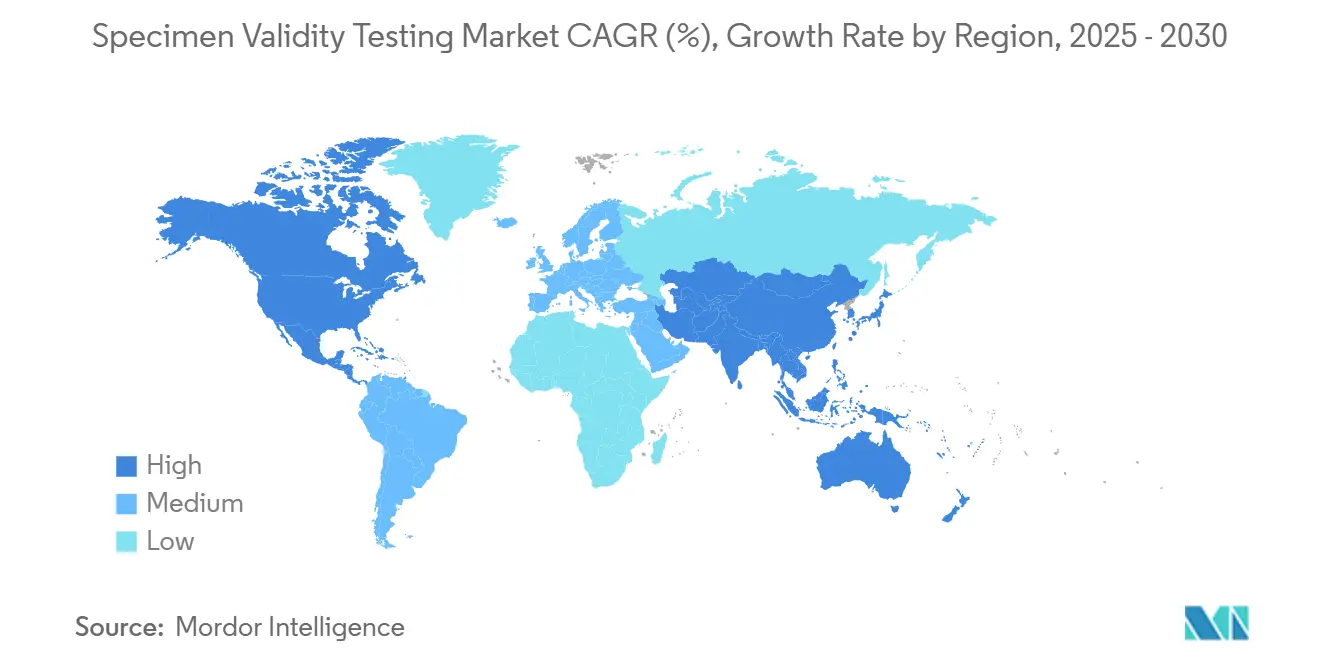
- Por geografia, a América do Norte comandou 41,34% da participação do tamanho do mercado de teste de validade de espécimes em 2024; a Ásia-Pacífico está definida para crescer a uma TCAC de 7,41% de 2025-2030.
Tendências e Insights do Mercado Global de Teste de Validade de Espécimes
Análise de Impacto dos Direcionadores
| Direcionador | (~) % Impacto na Previsão TCAC | Relevância Geográfica | Cronograma de Impacto |
|---|---|---|---|
| Crescimento de mandatos de teste de drogas no local de trabalho | +1.2% | Global, concentrado na América do Norte e UE | Médio prazo (2-4 anos) |
| Adoção rápida de dispositivos POC SVT | +0.9% | América do Norte e Ásia-Pacífico | Curto prazo (≤ 2 anos) |
| Expansão de telessaúde impulsionando kits domiciliares | +0.7% | América do Norte e UE | Médio prazo (2-4 anos) |
| Algoritmos de aprendizado de máquina para detecção de adulteração ao vivo | +0.6% | Global, liderado pela América do Norte | Longo prazo (≥ 4 anos) |
| Legalização da cannabis impulsionando painéis diferenciados | +0.5% | América do Norte, espalhando para UE | Curto prazo (≤ 2 anos) |
| Segurança da cadeia de suprimentos impulsionando controles estéreis | +0.4% | Global | Médio prazo (2-4 anos) |
| Fonte: Mordor Intelligence | |||
Crescimento de Mandatos de Teste de Drogas no Local de Trabalho
Reguladores em seis continentes estão fortalecendo regras de segurança corporativa, pressionando empregadores a verificar não apenas a presença de drogas, mas a autenticidade de cada amostra. Diretrizes alinhadas à OSHA nos Estados Unidos, Regulamentações de Transporte de Mercadorias Perigosas do Canadá, e a ordem obrigatória de teste de petróleo e gás do Ministério da Força de Trabalho de Omã destacam um movimento coletivo em direção a verificações mais rigorosas de validade de espécimes. Grandes conglomerados incorporam cada vez mais software de cadeia de custódia e supervisão de Oficial de Revisão Médica (MRO) em procedimentos operacionais padrão, mitigando risco de litígio após acidentes. O multiplicador de demanda resultante eleva vendas recorrentes de fitas de temperatura, ensaios de oxidantes e sistemas digitais de custódia [1]Autoridade Geral de Aviação Civil, MEIOS ACEITÁVEIS DE CONFORMIDADE,
gcaa.gov.ae.
Adoção Rápida de Dispositivos POC SVT
Analisadores portáteis recém-autorizados agora completam triagens de adulterantes em menos de seis minutos, atendendo ao padrão de "imediatez" exigido em investigações pós-incidentes. A autorização da Administração de Alimentos e Medicamentos dos EUA (FDA) para ensaios de fentanil no local estabeleceu um precedente para integrar verificações de validade em copos POC de etapa única. Empregadores valorizam o tempo de inatividade reduzido, enquanto laboratórios veem menos amostras rejeitadas, encurtando ciclos de faturamento. Fornecedores respondem com leitores modulares que imprimem relatórios prontos para conformidade, reforçando receitas recorrentes de consumíveis.
Expansão de Telessaúde Impulsionando Kits SVT Domiciliares
O gerenciamento remoto de pacientes com dependência de opioides e de controle da dor demanda kits de autocoleta que protegem contra substituição. Estudos acadêmicos mostram taxas de conclusão acima de 80% para submissões de urina remotas quando parâmetros de validade-temperatura, pH, creatinina-são incorporados aos dispositivos de coleta. Seguradoras de saúde agora exigem prova documental de validade antes de reembolsar códigos de alta complexidade, levando clínicas a adotar tubos de transporte à prova de adulteração e sensores de temperatura Bluetooth.
Algoritmos de Aprendizado de Máquina para Detecção de Adulteração ao Vivo
Laboratórios de pesquisa implantam modelos de aprendizado profundo que comparam espectros de séries temporais, sinalizando anomalias impossíveis de ver através de ensaios de parâmetro único. Estudos de validação inicial alcançam mais de 95% de precisão na identificação de urina sintética ou picos de oxidantes. O lançamento comercial está pronto para reduzir taxas de falsos negativos e aliviar o fardo de interpretação nos MROs, dando aos fornecedores de reagentes de espectrometria de massa compatíveis uma vantagem competitiva [2]Yi-Ching Lin, PS2MS: Um Sistema de Predição Baseado em Aprendizado Profundo para Identificar Novas Substâncias Psicoativas Usando Espectrometria de Massa,
ACS Publications, pubs.acs.org.
Análise de Impacto das Restrições
| Restrição | (~) % Impacto na Previsão TCAC | Relevância Geográfica | Cronograma de Impacto |
|---|---|---|---|
| Conhecimento limitado entre clínicas pequenas e médias | -0.8% | Global, mais agudo na Ásia-Pacífico e MEA | Curto prazo (≤ 2 anos) |
| Mudança para matrizes não urinárias | -0.6% | América do Norte e UE | Médio prazo (2-4 anos) |
| Restrições de privacidade de dados em plataformas biométricas | -0.4% | UE e América do Norte | Longo prazo (≥ 4 anos) |
| Escassez esporádica de reagentes e picos de matérias-primas | -0.3% | Global | Curto prazo (≤ 2 anos) |
| Fonte: Mordor Intelligence | |||
Conhecimento Limitado Entre Clínicas Pequenas e Médias
Provedores de saúde menores frequentemente subestimam a responsabilidade ligada a amostras inválidas. Pesquisas destacam que 59% das barreiras de implementação no ponto de atendimento se relacionam a treinamento e garantia de qualidade, deixando muitas clínicas sem verificação de temperatura ou verificações de gravidade específica. Políticas de reembolso agora negam reivindicações que carecem de documentação de validade, mas lacunas de conhecimento persistem, retardando a adoção [3]Blue Cross Blue Shield of Michigan, Teste de Drogas no Controle da Dor e Tratamento de Transtorno de Uso de Substâncias,
bcbsm.com.
Mudança para Matrizes Não Urinárias Reduzindo Demanda por SVT
A autorização federal de teste de fluido oral para funcionários governamentais levou empresas privadas a adotar saliva como matriz primária, o que reduz o risco de adulteração e, portanto, a necessidade de painéis de validade urinária multiparamétricos. Previsões sugerem que 30% dos testes regulamentados federalmente poderiam migrar para fluido oral dentro de quatro anos, reduzindo o potencial de crescimento para consumíveis focados em urina.
Análise de Segmentos
Por Produto e Serviço: Produtos Mantêm Escala, Serviços Aceleram
Produtos ancoraram 66,67% da receita de 2024, sustentados pela natureza consumível de kits de ensaio, reagentes oxidantes, padrões de creatinina e copos de coleta de uso único. Apenas fitas indicadoras de temperatura geraram um ciclo de substituição de alta velocidade, especialmente em grandes empresas de logística e energia. Serviços, no entanto, registram uma TCAC de 7,21% até 2030, à medida que empregadores terceirizam interpretação de resultados e auditorias de conformidade para consultores MRO e laboratórios especializados. Ambientes médico-legais favorecem ofertas agrupadas que mesclam gerenciamento de cadeia de custódia com análises de aprendizado de máquina. O tamanho do mercado de teste de validade de espécimes para serviços está previsto para alcançar USD 1,24 bilhão até 2030, mantendo impulso apesar do domínio dos consumíveis.
A onda de serviços também surfa na medicina de coleta remota. Plataformas de telessaúde contratam laboratórios terceirizados para verificar temperatura da amostra e níveis de oxidantes na chegada, pagando taxas premium por adjudicação no mesmo dia. A demanda dispara para revisões MRO virtuais em programas de emprego transfronteiriços, ampliando receita endereçável e solidificando o mercado de teste de validade de espécimes como uma solução holística em vez de apenas uma vertical de produtos.
Por Tipo: Teste Laboratorial Dominante, POC Ganha Velocidade
Fluxos de trabalho laboratoriais detiveram 59,65% da participação em 2024. Laboratórios centralizados manejam sistemas de cromatografia líquida espectrometria de massa tandem (LC-MS/MS) que analisam temperatura, gravidade específica, creatinina, pH e oxidantes com precisão regulatória. Essa infraestrutura sustenta a liderança da participação do mercado de teste de validade de espécimes de grandes laboratórios de referência. No entanto, formatos POC avançam 7,29% TCAC, impulsionados por fotômetros portáteis e copos imunocromatográficos que verificam cruzadamente três ou mais parâmetros de validade em minutos. O tamanho do mercado de teste de validade de espécimes vinculado a plataformas POC está esperado para subir para USD 1,38 bilhão até 2030, à medida que a precisão dos dispositivos se aproxima dos padrões laboratoriais.
Setores de alto risco como construção agora implantam analisadores POC robustos em locais de trabalho para testes pós-incidentes, reduzindo tempo de inatividade. Enquanto isso, modelos híbridos veem espécimes primeiro triados por dispositivos POC e apenas positivos-junto com quaisquer anomalias de validade sinalizadas-enviados para laboratórios, otimizando distribuição de carga de trabalho.
Por Usuário Final: Locais de Trabalho Lideram, Laboratórios Aceleram
Programas corporativos representaram 46,98% da receita de 2024, cimentando seu papel como principal consumidor de consumíveis de validade. Empregadores de transporte, petróleo e gás, e setor público mantêm testes obrigatórios pré-emprego e aleatórios, garantindo volume constante. Laboratórios de triagem de drogas sobem mais rapidamente a 7,33% TCAC, espelhando consolidação que puxa volumes de clínicas menores para centros de alto rendimento.
Clínicas de controle da dor, sob escrutínio de pagadores, cada vez mais terceirizam para instalações especializadas capazes de fornecer métricas de validade abrangentes. Agências de justiça criminal, outro nicho crítico, demandam rastreabilidade de cadeia de custódia e começaram a solicitar registros de temperatura legíveis por máquina, aprofundando o papel de plataformas avançadas de validade.
Nota: Participações de segmento de todos os segmentos individuais disponíveis na compra do relatório
Análise Geográfica
A América do Norte reteve 41,34% da receita em 2024 e permanece como definidora regulatória para o mercado de teste de validade de espécimes. O Departamento de Saúde e Serviços Humanos exige que cada espécime urinário regulamentado documente temperatura (32-38 °C), pH (4,5-8,0), gravidade específica (≥1,003), e creatinina (≥20 mg/dL) imediatamente após a coleta SAMHSA. A revisão do painel de janeiro de 2025, que adicionou fentanil e norfentanil, elevou ainda mais a necessidade dos laboratórios de confirmação precisa de validade para evitar falsos negativos sob novos limites de analitos Registro Federal. Mandatos paralelos do Departamento de Transporte aplicam-se a aproximadamente 10 milhões de trabalhadores sensíveis à segurança, garantindo altos volumes de teste. A estrutura orientada à privacidade do Canadá reduz testes aleatórios mas enfatiza programas de fluido oral que ainda dependem de documentação de temperatura e cadeia de custódia para defensibilidade.
A Ásia-Pacífico registra a TCAC mais rápida de 7,41% até 2030, impulsionada por fábricas multinacionais na China e Índia que incorporam melhores práticas da Administração de Segurança e Saúde Ocupacional dos EUA (OSHA) em operações locais. Gigantes diagnósticos globais abriram centros regionais para fornecer kits de ensaio e serviços MRO em idiomas nativos. A conformidade de comércio transfronteiriço impulsiona empresas a adotar sistemas de cadeia de custódia ao estilo americano, dando ao mercado de teste de validade de espécimes nova escala. Governos regionais estão estudando estatutos de teste obrigatório de drogas, particularmente em transporte e mineração, o que incorporaria ainda mais verificações de integridade de espécimes.
A Europa oferece regulamentação fragmentada. Operadoras ferroviárias alemãs aplicam regras rigorosas de validade de espécimes modeladas nas diretrizes federais americanas, enquanto a França limita testes a funções sensíveis à segurança e impõe filtros de privacidade mais rigorosos. O Regulamento de Diagnóstico In Vitro (IVDR) da UE impõe obrigações de desempenho e vigilância pós-mercado em dispositivos de validade que entram no bloco, elevando barreiras de entrada, mas padronizando qualidade. Empregadores pan-europeus assim se inclinam para sistemas de coleta com marca CE que integram selos de integridade com código de barras e registros de custódia em nuvem.
O Oriente Médio e África seguem padrões internacionais de contratação de petróleo e gás. Reguladores de aviação do CCG exigem verificações de validade supervisionadas por MRO, com protocolos de cadeia de custódia espelhando diretrizes americanas SAMHSA. Casas de mineração da África do Sul fazem parceria com laboratórios globais para atender expectativas de compradores por métricas de teste de alta integridade. A América do Sul é liderada pelo Brasil, onde a Lei 13.103/15 compele motoristas profissionais a passar por avaliações toxicológicas periódicas que incluem documentação de validade de espécimes; a popularidade do teste de cabelo, no entanto, demanda protocolos de validação cruzada para confirmar autenticidade. O setor automotivo em expansão da Argentina importa diretrizes do DOT americano para satisfazer parceiros da cadeia de suprimentos.
Cenário Competitivo
O mercado de teste de validade de espécimes apresenta fragmentação moderada. Abbott, Thermo Fisher Scientific, Laboratory Corporation of America, Quest Diagnostics e Siemens Healthineers coletivamente representam uma parcela decente da receita global. Vantagens de escala derivam de portfólios integrados de ensaio para análises e redes logísticas extensas. A plataforma iCUP da Abbott agora incorpora monitoramento de temperatura em tempo real e fitas de oxidantes, agrupando validade com triagens rápidas de drogas Abbott. A Quest Diagnostics expandiu sua presença internacional para mais de 80 nações, oferecendo painéis de cadeia de custódia baseados em nuvem que simplificam conformidade multinacional Quest Diagnostics.
A diferenciação tecnológica impulsiona a competição atual. Parcerias entre laboratórios de referência e fornecedores de IA entregam classificadores de adulteração de aprendizado de máquina, elevando aderência de serviços. A Siemens Healthineers testa fluxos de trabalho de espectrometria de massa ligados à nuvem que sinalizam razões atípicas de creatinina para gravidade específica em quase tempo real, reduzindo fardos de relatórios nos MROs. Enquanto isso, fornecedores especializados como Labcon enfatizam copos de coleta de grau médico, compatíveis com IATA, abordando preocupações de esterilidade da cadeia de suprimentos Labcon.
Startups focam em inovações de saliva e microamostragem-áreas prontas para erodir volumes de urina, mas ainda exigem prova de identidade do doador e integridade da amostra. Incumbentes se protegem adquirindo ou licenciando essas tecnologias, mantendo receita independentemente de mudanças de matriz. Provedores regionais na Ásia-Pacífico cortejam contratos multinacionais oferecendo suporte MRO bilíngue e rastreamento em nuvem completo, desafiando o domínio norte-americano.
Líderes da Indústria de Teste de Validade de Espécimes
Abbott
Thermo Fisher Scientific
LabCorp
Healgen Scientific LLC
Premier Biotech, Inc.
- *Isenção de responsabilidade: Principais participantes classificados em nenhuma ordem específica
Desenvolvimentos Recentes da Indústria
- Janeiro de 2025: O Departamento de Saúde e Serviços Humanos dos EUA atualizou Diretrizes Obrigatórias, adicionando fentanil e norfentanil enquanto removeu MDMA e MDA, compelindo laboratórios a ajustar fluxos de trabalho de validade Registro Federal.
- Dezembro de 2024: BD e Babson Diagnostics introduziram tecnologia de microamostragem de sangue capilar, expandindo conceitos de teste de validade para coleta de sangue de pequeno volume BD.
- Agosto de 2024: FDA autorizou a primeira triagem de fentanil em urina POC no analisador RYAN, catalisando verificação de validade no local FDA.
- Fevereiro de 2024: SAMHSA lançou um Manual de Coleta de Espécimes de Urina revisado detalhando limites de validade atualizados e passos de detecção de adulteração SAMHSA.
Escopo do Relatório Global do Mercado de Teste de Validade de Espécimes
Conforme o escopo do relatório, teste de validade de espécimes (SVT) é o teste de triagem para amostras de urina para detectar qualquer adulteração, diluição ou substituição. SVT fornece informações críticas sobre a confiabilidade e precisão dos resultados de testes de drogas para clínicos, e também valida que a amostra de urina testada é um espécime de urina humana válido. O mercado de teste de validade de espécimes é segmentado por tipo de droga (medicamentos antibacterianos, medicamentos antifúngicos, medicamentos antivirais e outros medicamentos), indicação (infecções da corrente sanguínea, infecções do trato urinário, infecções do local cirúrgico, pneumonia e outras indicações), e geografia (América do Norte, Europa, Ásia-Pacífico, Oriente Médio e África, e América do Sul). O relatório de mercado também cobre os tamanhos de mercado estimados e tendências para 17 países diferentes nas principais regiões globalmente. O relatório oferece o valor (em USD) para os segmentos acima.
| Produtos | Kits de Ensaio |
| Reagentes e Calibradores | |
| Descartáveis | |
| Serviços |
| Teste Laboratorial |
| Teste Rápido e POC |
| Locais de Trabalho |
| Sistemas de Aplicação da Lei e Justiça Criminal |
| Laboratórios de Triagem de Drogas |
| Centros de Controle da Dor |
| Outros |
| América do Norte | Estados Unidos |
| Canadá | |
| México | |
| Europa | Alemanha |
| Reino Unido | |
| França | |
| Itália | |
| Espanha | |
| Resto da Europa | |
| Ásia-Pacífico | China |
| Japão | |
| Índia | |
| Austrália | |
| Coreia do Sul | |
| Resto da Ásia-Pacífico | |
| Oriente Médio e África | CCG |
| África do Sul | |
| Resto do Oriente Médio e África | |
| América do Sul | Brasil |
| Argentina | |
| Resto da América do Sul |
| Por Produto e Serviço | Produtos | Kits de Ensaio |
| Reagentes e Calibradores | ||
| Descartáveis | ||
| Serviços | ||
| Por Tipo | Teste Laboratorial | |
| Teste Rápido e POC | ||
| Por Usuário Final | Locais de Trabalho | |
| Sistemas de Aplicação da Lei e Justiça Criminal | ||
| Laboratórios de Triagem de Drogas | ||
| Centros de Controle da Dor | ||
| Outros | ||
| Por Geografia | América do Norte | Estados Unidos |
| Canadá | ||
| México | ||
| Europa | Alemanha | |
| Reino Unido | ||
| França | ||
| Itália | ||
| Espanha | ||
| Resto da Europa | ||
| Ásia-Pacífico | China | |
| Japão | ||
| Índia | ||
| Austrália | ||
| Coreia do Sul | ||
| Resto da Ásia-Pacífico | ||
| Oriente Médio e África | CCG | |
| África do Sul | ||
| Resto do Oriente Médio e África | ||
| América do Sul | Brasil | |
| Argentina | ||
| Resto da América do Sul | ||
Principais Questões Respondidas no Relatório
Qual é o tamanho atual do mercado de teste de validade de espécimes?
O tamanho do mercado de teste de validade de espécimes está em USD 2,34 bilhões em 2025 e está projetado para alcançar USD 3,21 bilhões até 2030.
Qual região domina o mercado de teste de validade de espécimes?
A América do Norte lidera com 41,34% da participação de receita em 2024 devido aos requisitos federais rigorosos no local de trabalho.
Por que os serviços estão crescendo mais rápido que os produtos?
A crescente complexidade de protocolos, teste remoto e a necessidade de interpretação especializada de Oficial de Revisão Médica estão impulsionando uma TCAC de 7,21% para serviços.
Como a IA está influenciando o teste de validade de espécimes?
Modelos de aprendizado de máquina agora detectam padrões sofisticados de adulteração com mais de 95% de precisão, melhorando a confiabilidade laboratorial e diferenciação competitiva.
Qual impacto as matrizes não urinárias têm no crescimento do mercado?
A mudança para teste de fluido oral e cabelo reduz a demanda por consumíveis tradicionais de validade urinária, mas abre oportunidades para novas ferramentas de verificação de integridade adaptadas a matrizes alternativas.
Qual segmento de usuário final está se expandindo mais rapidamente?
Laboratórios de triagem de drogas, sustentados por tendências de consolidação e terceirização, estão definidos para crescer a uma TCAC de 7,33% até 2030.
Página atualizada pela última vez em:



