Taille et part du marché de la fabrication de vecteurs viraux
Analyse du marché de la fabrication de vecteurs viraux par Mordor Intelligence
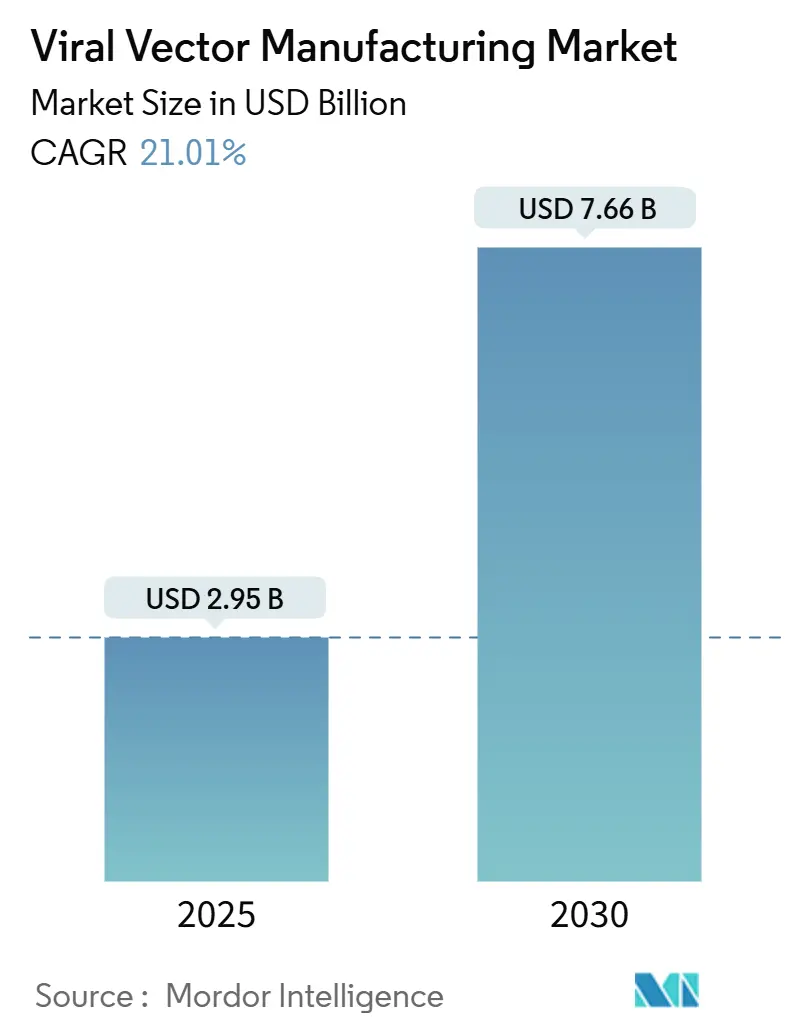
La taille du marché de la fabrication de vecteurs viraux s'élevait à 2,95 milliards USD en 2025 et devrait atteindre 7,66 milliards USD d'ici 2030, impliquant un TCAC de 21,01 %. Cette trajectoire reflète la transformation de la thérapie génique d'un créneau expérimental en une classe thérapeutique réglementée alors que le nombre de produits approuvés par la FDA est monté à 14 en 2024. Les autorisations révolutionnaires telles que Casgevy pour la drépanocytose et de nouvelles indications pour Elevidys dans la dystrophie musculaire de Duchenne ont validé la demande commerciale et accéléré le financement pour l'infrastructure de production. Plus de 8 milliards USD en projets de terrains vierges et d'extension ont été annoncés par les principales CDMO pendant 2024-2025, menés par Fujifilm Diosynth et Lonza, pourtant de nombreuses suites fonctionnent encore en dessous de 50 % d'utilisation car elles ont été conçues pour des travaux de phase précoce plutôt que pour une production commerciale soutenue. La consolidation s'intensifie alors que les acquéreurs recherchent des capacités de bout en bout, des analyses avancées et un savoir-faire réglementaire qui raccourcissent le délai de mise sur le marché.
Points clés du rapport
- Par type de vecteur, les plateformes virales adéno-associées ont représenté 72,45 % des revenus de 2024 tandis que les vecteurs adénoviraux sont projetés pour croître avec un TCAC de 23,56 % jusqu'en 2030.
- Par maladie, les troubles génétiques ont représenté 48,45 % de la part du marché de la fabrication de vecteurs viraux en 2024 ; les troubles neurologiques devraient s'étendre avec un TCAC de 24,67 % jusqu'en 2030.
- Par application, les thérapies in-vivo ont détenu 64,35 % de la taille du marché de la fabrication de vecteurs viraux en 2024 et les thérapies cellulaires ex-vivo progressent avec un TCAC de 23,55 % jusqu'en 2030.
- Par mode de fabrication, la production interne un capturé 62,45 % des revenus de 2024, tandis que la fabrication sous contrat devrait afficher un TCAC de 24,56 % jusqu'en 2030.
- Par géographie, l'Amérique du Nord un commandé 47,34 % des revenus de 2024 et l'Asie-Pacifique est projetée pour croître avec un TCAC de 22,56 % entre 2025 et 2030.
Tendances et perspectives du marché mondial de la fabrication de vecteurs viraux
Analyse de l'impact des moteurs
| Moteur | % d'impact sur les prévisions de TCAC | Pertinence géographique | Délai d'impact |
|---|---|---|---|
| Pipeline croissant de thérapies géniques et succès cliniques | +4.2% | Amérique du Nord, UE, Asie-Pacifique | Moyen terme (2-4 ans) |
| Externalisation croissante vers les CDMO et expansions de capacité | +3.8% | Amérique du Nord, Asie-Pacifique | Court terme (≤ 2 ans) |
| Fort financement en capital-risque et gouvernemental | +3.1% | Amérique du Nord, UE, Chine, Singapour | Moyen terme (2-4 ans) |
| Transition vers les plateformes de culture cellulaire en suspension | +2.9% | Centres mondiaux | Long terme (≥ 4 ans) |
| Adoption de bioréacteurs à usage unique | +2.7% | Mondial | Court terme (≤ 2 ans) |
| Ingénierie de capsides guidée par l'IA émergente | +2.4% | Amérique du Nord, UE, APAC sélectionnée | Long terme (≥ 4 ans) |
| Source: Mordor Intelligence | |||
Pipeline croissant de thérapies géniques et succès cliniques
Plus de 2 000 thérapies géniques étaient en développement en 2024, soulignant l'ampleur des indications progressant vers la commercialisation[1]Food and Drug Administration, ' Novel Gene Therapy Approvals and Guidance Documents ', fda.gov. L'approbation de Kebilidi pour le déficit en décarboxylase des acides aminés aromatiques L un marqué la première option thérapeutique pour ce trouble neurologique rare et un établi un précédent réglementaire pour la livraison AAV intraparenchymateuse. L'essai BENEGENE-2 un rapporté une chute de 71 % des épisodes hémorragiques pour l'hémophilie B, confirmant l'expression durable du facteur IX. De tels jalons cliniques renforcent la confiance des payeurs et stimulent des études de cohortes de patients plus importantes, ce qui à son tour élargit les exigences de volume de lots dans le marché de la fabrication de vecteurs viraux. À mesure que le savoir-faire des processus s'améliore, les coûts moyens de dose AAV ont chuté dans les dizaines de milliers de dollars, permettant l'exploration de maladies communes sans sacrifier la viabilité économique.
Externalisation croissante vers les CDMO et expansions de capacité
Les CDMO et fabricants hybrides devraient détenir 54 % de la capacité biologique mondiale d'ici 2028 - en hausse par rapport à 43 % en 2024 - reflétant un mouvement décisif vers des modèles à actifs légers parmi les développeurs de thérapies. Le partenariat de Charles River avec l'Institut Gates pour les services lentiviraux et le déploiement par Takara Bio de réacteurs à usage unique de 5 000 L illustrent l'échelle spécialisée que les sponsors louent maintenant au lieu de construire. UniQure un vendu son usine de Lexington et externalisé la fabrication d'Hemgenix à Genezen, démontrant le calcul économique qui favorise la production externe pour les vecteurs de haute complexité. Resilience un investi 225 millions USD pour augmenter la production au-delà de 200 millions d'unités d'ici 2025, montrant à quelle vitesse la demande augmente dans le marché de la fabrication de vecteurs viraux.
Fort financement en capital-risque et gouvernemental dans les thérapies cellulaires et géniques
Malgré un refroidissement plus large du financement biotech, les investisseurs ont versé du capital dans des plateformes manufacturables. VectorBuilder un sécurisé 76 millions USD pour une installation de 30 suites à Guangzhou, tandis que la Chine un réservé 4,17 milliards USD pour des projets de biofabrication à partir de 2025. La stratégie nationale de l'Allemagne un soutenu le centre de thérapie génique de 90 millions EUR de Roche à Penzberg. Le financement en capital-risque pour les entreprises d'édition génique un chuté à 280 millions USD en 2024, mais les tours de début 2025 pointent vers une confiance renouvelée alors que les programmes atteignent des essais pivots. L'allocation de capital favorise maintenant les entreprises qui démontrent des voies de production évolutives et assurées qualité dans le marché de la fabrication de vecteurs viraux.
Stratégies émergentes d'ingénierie de capsides guidée par l'IA
Les cadres d'apprentissage automatique tels que CAP-PLM prédisent la fitness des capsides AAV avec une haute précision, permettant aux développeurs de réduire les bibliothèques expérimentales et de couper le cycle de découverte[2]Phys.org Editors, ' Machine Learning Elevates AAV Capsid Design ', phys.org. Des capsides mieux conçues peuvent diviser par deux les exigences de dose de vecteur, atténuant les pressions de coût et libérant l'espace de fermenteur. Les premiers adopteurs aux États-Unis et en Europe ont intégré des plateformes IA dans le développement de processus, signalant des gains d'efficacité à long terme pour le marché de la fabrication de vecteurs viraux.
Analyse de l'impact des contraintes
| Analyse de l'impact des contraintes | (~) % d'impact sur les prévisions de TCAC | Pertinence géographique | Délai d'impact |
|---|---|---|---|
| Coût élevé des biens et préoccupations de tarification des thérapies | -2,8 % | Mondial, avec accent sur les marchés sensibles au prix | Moyen terme (2-4 ans) |
| Complexité réglementaire et retards de libération de lots | -2,1 % | Mondial, variant selon la juridiction réglementaire | Court terme (≤ 2 ans) |
| Contraintes de chaîne d'approvisionnement pour plasmides de grade GMP | -1,9 % | Centres de fabrication Amérique du Nord, Europe, Asie-Pacifique | Court terme (≤ 2 ans) |
| Concurrence des technologies de livraison non virales | -1,7 % | Mondial, notamment dans les clusters d'innovation de thérapies avancées | Long terme (≥ 4 ans) |
| Source: Mordor Intelligence | |||
Coût élevé des biens et préoccupations de tarification des thérapies
La production AAV s'étend encore sur environ trois semaines et coûte environ 50 000 USD par construction, avec des capsides vides gonflant les volumes et compliquant les calculs de titre[3]Form Bio Product Team, ' AI-Enabled Vector Design Platform ', formbio.com. Les prix commerciaux restent élevés - Casgevy liste à 2,2 millions USD et Hemgenix à 3,5 millions USD par patient - soulevant des préoccupations de payeurs concernant l'accessibilité financière. Les débats éthiques sur l'accès équitable limitent la pénétration du marché dans les régions à faible revenu. La fabrication de plateforme, les densités cellulaires plus élevées et l'analytique en ligne réduisent le gaspillage, pourtant des économies majeures n'apparaîtront qu'à mesure que les portefeuilles de phase tardive mûrissent et que les volumes augmentent dans le marché de la fabrication de vecteurs viraux.
Complexité réglementaire et retards de libération de lots
La révision Q5A(R2) de la FDA un approfondi les exigences de sécurité virale et allongé les packages de validation. Distinguer les capsides pleines des vides exige une ultracentrifugation analytique ou une photométrie de masse que de nombreuses usines n'ont pas. Les pénuries de main-d'œuvre pour ces compétences de niche ajoutent des retards supplémentaires. L'EMA harmonise les directives, pourtant les calendriers nationaux échelonnés forcent les fabricants à naviguer des voies parallèles. Ces obstacles ralentissent les lancements de produits et amortissent les perspectives de croissance pour le marché de la fabrication de vecteurs viraux.
Analyse des segments
Par type de vecteur : la dominance AAV stimule l'expansion du marché
Les vecteurs AAV ont livré 72,45 % des revenus de 2024 alors que la sécurité favorable, le tropisme tissulaire et six thérapies approuvées par la FDA ont ancré la demande. La taille du marché de la fabrication de vecteurs viraux pour les produits AAV devrait augmenter fortement alors que les traitements d'hémophilie et de dystrophie musculaire mettent à l'échelle les volumes commerciaux. Plus de 225 essais actifs s'appuient sur des squelettes AAV, cimentant des besoins de capacité pluriannuels. Les CDMO commandent des suites dédiées AAV qui exploitent les bioréacteurs en suspension pour augmenter la productivité.
Les vecteurs adénoviraux détiennent les perspectives de croissance les plus rapides à 23,56 % de TCAC jusqu'en 2030. L'ingénierie de sérotype novel atténue l'immunité préexistante, ouvrant des applications de vaccins à doses répétées et oncolytiques. Les vecteurs lentiviraux restent essentiels pour les flux de travail CAR-T autologues ; le contrôle de pH amélioré et l'inhibition compétitive freinent maintenant la perte de particules fonctionnelles de 62,1 % autrefois commune en fabrication. Les plateformes rétrovirales et oncolytiques servent des utilisations d'oncologie de niche, souvent en combinaison avec des inhibiteurs de point de contrôle, et bénéficient de partenariats de lignées cellulaires propriétaires qui améliorent le rendement.
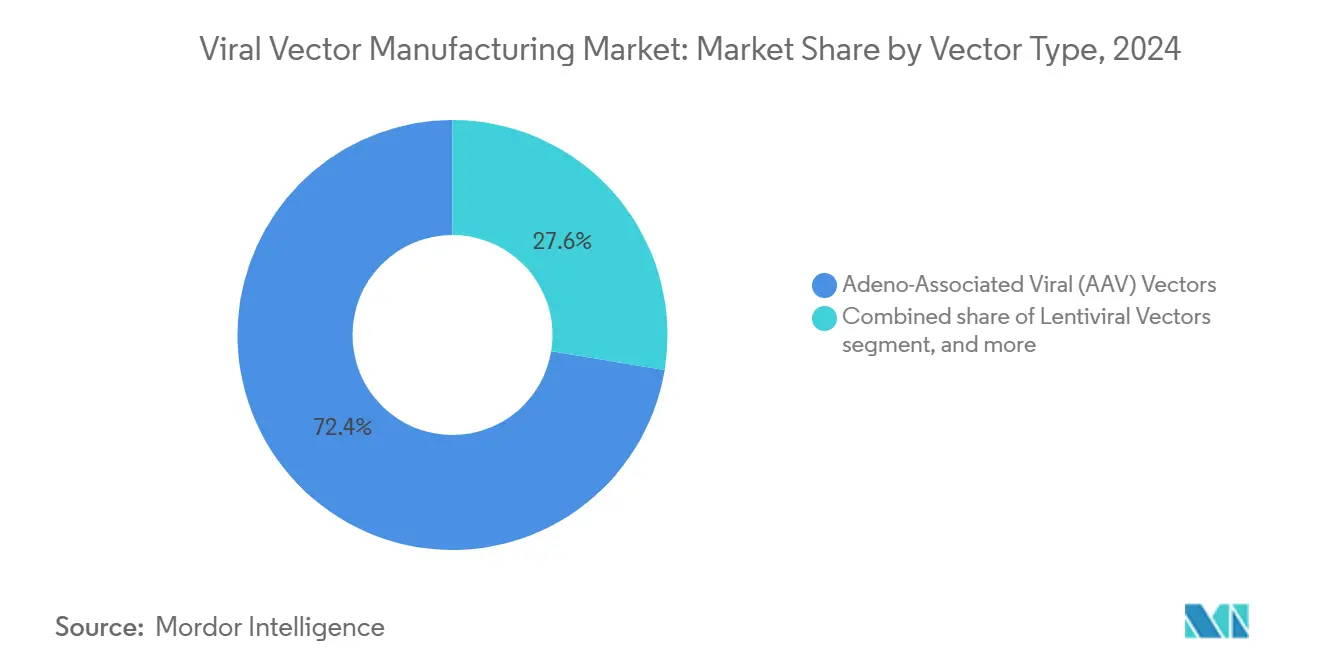
Note: Parts de segment de tous les segments individuels disponibles à l'achat du rapport
Par maladie : les troubles génétiques mènent les applications thérapeutiques
Les troubles génétiques ont représenté 48,45 % des revenus de 2024 parmi toutes les indications alors que les résultats curatifs justifiaient les structures de tarification premium. Les données à long terme dans l'hémophilie un, l'hémophilie B et la drépanocytose ont incité les payeurs à adopter des schémas de paiement basés sur les résultats. La taille du marché de la fabrication de vecteurs viraux pour ces conditions rares reste importante en raison de la demande refoulée, des programmes de dépistage néonatal et de l'utilisation élargie d'étiquettes.
Les troubles neurologiques devraient enregistrer un TCAC de 24,67 % jusqu'en 2030. Les méthodes de livraison intrathécale et intraparenchymateuse ont surmonté les barrières antérieures posées par la barrière hémato-encéphalique. Les lectures positives de sécurité et d'efficacité dans l'atrophie musculaire spinale et les maladies rétiniennes héréditaires stimulent de nouveaux candidats de Parkinson et SLA. L'oncologie conserve une part stable via les thérapies CAR-T qui dépendent de squelettes lentiviraux, tandis que les projets de maladies infectieuses pivotent vers les vecteurs adénoviraux pendant les scénarios d'épidémie.
Par application : les thérapies in-vivo stimulent la croissance du marché
Les thérapies in-vivo ont capturé 64,35 % des revenus de 2024 car elles ne nécessitent que la fabrication de vecteurs au lieu de manipulation cellulaire individualisée. Les innovations récentes de capside ont augmenté l'efficacité de transduction, permettant des doses plus faibles et raccourcissant les temps de perfusion. Deux candidats AAV intramusculaires ont déposé en 2025, soulignant le substrat élargissant pour l'administration directe.
Les programmes de thérapie cellulaire ex-vivo détiennent le taux de croissance le plus élevé à 23,55 % de TCAC, propulsés par des éditions pour la drépanocytose et la bêta-thalassémie qui ont validé l'économie de fabrication. Les lignées productrices modifiées telles que NuPro-2S réduisent les impuretés d'ADN de 89 %, améliorant la cohérence. La vaccinologie préventive exploite les vecteurs adénoviraux pour la préparation pandémique mais fait face à la pression concurrentielle des plateformes ARNm rapidement adaptables.
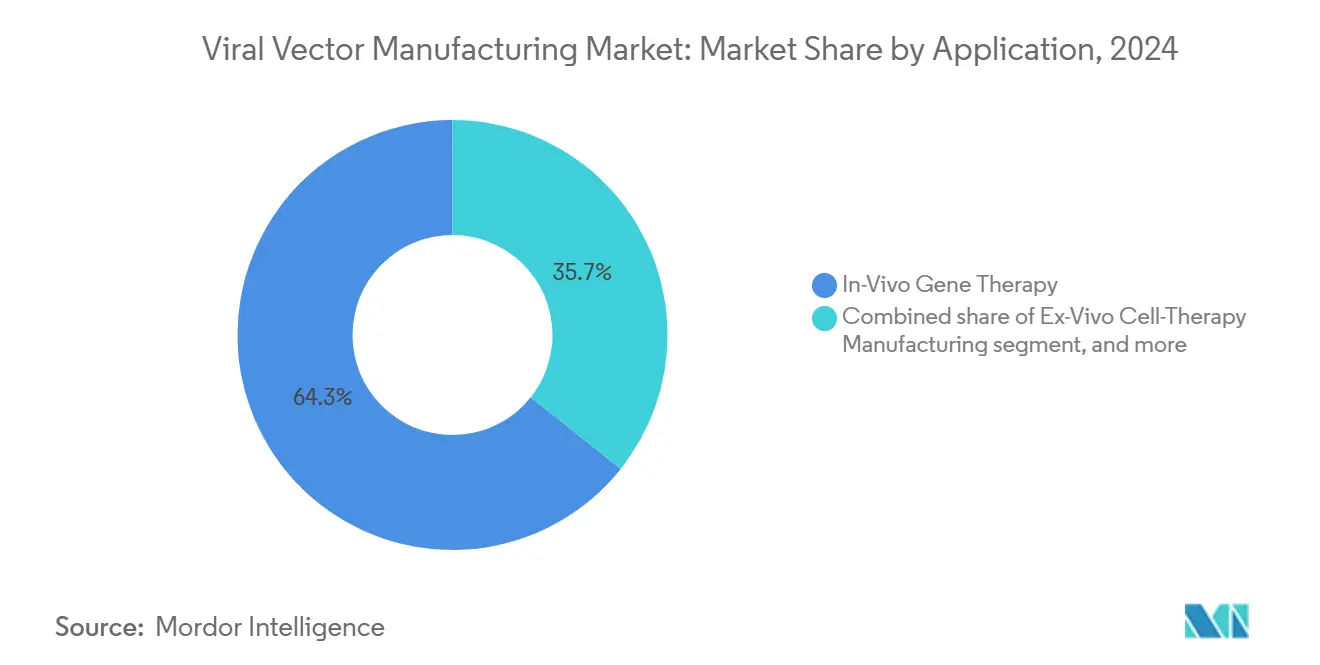
Note: Parts de segment de tous les segments individuels disponibles à l'achat du rapport
Par mode de fabrication : la fabrication sous contrat s'accélère
Les suites internes ont encore généré 62,45 % des revenus de 2024 alors que les entreprises sauvegardaient la connaissance des processus. Cependant, les limites de capacité et l'escalade des CapEx ont mené de nombreux sponsors à se déplacer vers des partenaires externes. Le marché de la fabrication de vecteurs viraux penche donc vers les CDMO qui fournissent une analytique clé en main, une validation de processus et un support réglementaire.
Les services contractuels devraient croître à 24,56 % de TCAC jusqu'en 2030. L'acquisition de Vacaville de 1,2 milliard USD de Lonza et l'expansion de Caroline du Nord de 1,2 milliard USD de Fujifilm Diosynth ont chacune ajouté plus de 300 000 L de volume de bioréacteur. Les stratégies hybrides gagnent en faveur alors que les développeurs gardent la R&D à petite échelle interne tout en externalisant les lots commerciaux, donnant la flexibilité sans renoncer au contrôle de propriété intellectuelle centrale.
Analyse géographique
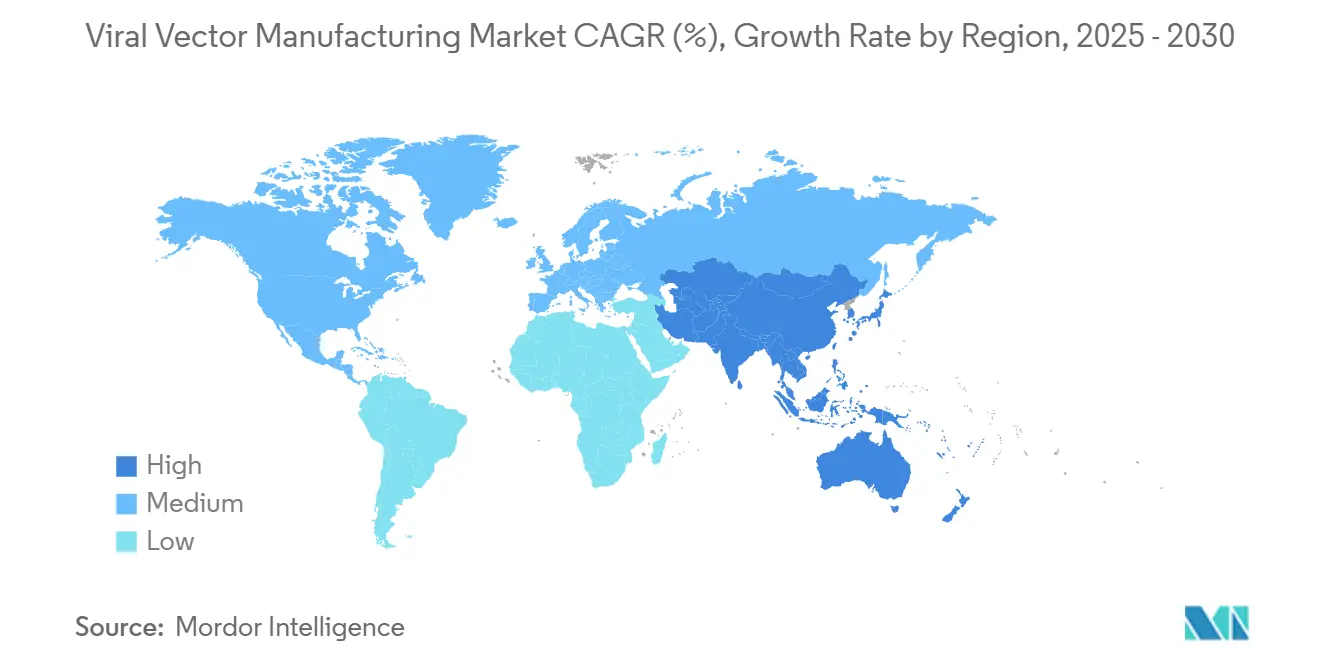
L'Amérique du Nord un détenu 47,34 % des revenus de 2024, stimulée par la feuille de route réglementaire claire de la FDA et les clusters biotechnologiques denses à Boston, Research Triangle Park et la région de la baie de San Francisco. La construction de capacité de 225 millions USD de Resilience dans l'Ohio et le site de 128 000 pi² de GenScript ProBio au New Jersey soulignent la foi des investisseurs dans l'infrastructure domestique. La région bénéficie également du bassin de main-d'œuvre le plus profond de spécialistes qualifiés en vecteurs.
L'Europe s'est classée deuxième et un reçu un coup de pouce du centre de Penzberg de 90 millions EUR de l'Allemagne et de l'installation entièrement robotisée de 43 millions USD de Novartis en Slovénie. Les directives EMA harmonisées rationalisent les dépôts, bien que le Brexit impose encore des examens de qualité double site pour les produits traversant la Manche. Les réglementations environnementales dans l'UE encouragent les systèmes à usage unique qui réduisent l'utilisation d'eau et les empreintes carbone, influençant les politiques d'approvisionnement à travers le marché de la fabrication de vecteurs viraux.
L'Asie-Pacifique devrait enregistrer un TCAC de 22,56 % jusqu'en 2030. La Chine un réservé 4,17 milliards USD pour les lignes de biofabrication commençant en 2025, tandis que le Japon, l'Inde et la Corée du Sud améliorent les cadres réglementaires pour attirer les essais multinationaux. WuXi Biologics un rapporté une croissance des revenus de 2024 qui finance des lignes de vecteurs supplémentaires à Wuxi et Suzhou. Les grandes populations de patients naïfs de traitement et les coûts opérationnels compétitifs font de la région une rampe de lancement préférée pour l'externalisation de phase tardive.
Paysage concurrentiel
Le marché de la fabrication de vecteurs viraux montre une concentration modérée alors que les CDMO leaders acquièrent des entreprises spécialisées pour intégrer le développement de lignées cellulaires, les dosages analytiques et la finition de remplissage sous un même toit. L'achat de 292,5 millions USD de Vigene Biosciences par Charles River, l'acquisition de 600 millions USD de Mirus Bio par Merck KGaA et le rachat de 1,2 milliard USD de l'usine Vacaville de Genentech par Lonza illustrent les primes payées pour l'évolutivité prouvée.
La différenciation technologique est maintenant essentielle. Le moteur IA de Form Bio prédit les capsides AAV optimales, réduisant les boucles d'essai-erreur et rasant des mois des calendriers de développement. Les lignées cellulaires modifiées qui coupent l'ADN résiduel sous les seuils réglementaires et les jumeaux numériques pilotés par IA qui prévoient les rendements de lots fournissent des gains de performance mesurables. Les opérateurs sans de tels ensembles d'outils risquent de concurrencer sur le prix plutôt que sur la science à valeur ajoutée.
Les perspectives d'espace blanc se trouvent dans les marchés émergents et les vecteurs de niche. VIVEbiotech un levé du capital frais pour élargir les services lentiviraux pour les programmes de neuro-oncologie. ViroCell Biologics un complété un financement sursouscrit pour accélérer la production en phase clinique au Royaume-Uni. Les nouveaux entrants peuvent encore gagner en traction en se spécialisant dans les sérotypes rares, la finition de remplissage régionale, ou l'analytique de prochaine génération.
Leaders de l'industrie de la fabrication de vecteurs viraux
Lonza
Thermo Fisher Scientific, Inc.
Charles River Laboratories
Fujifilm Diosynth Biotechnologies
Catalent
- *Avis de non-responsabilité : les principaux acteurs sont triés sans ordre particulier
Développements récents de l'industrie
- Mars 2025 : WuXi Biologics un rapporté des résultats solides pour 2024 et prévu une croissance accélérée pour 2025, citant une nouvelle capacité de vecteurs en Asie-Pacifique.
- Février 2025 : Takara Bio un lancé des bioréacteurs à usage unique de 50 L-5 000 L pour la production de vecteurs à grande échelle.
- Février 2025 : Novartis un ouvert une usine de vecteurs viraux automatisée de 40 millions EUR en Slovénie.
- Janvier 2025 : Fujifilm Diosynth un dit que 2025 sera son année d'expansion la plus importante, triplant le volume de bioréacteurs de Holly Springs.
- Décembre 2024 : VIVEbiotech un sécurisé un investissement de croissance d'Ampersand Capital Partners.
Portée du rapport du marché mondial de la fabrication de vecteurs viraux
Selon la portée de ce rapport, les vecteurs viraux représentent l'un des outils primaires pour délivrer le matériel génétique dans les cellules. Le marché de la fabrication de vecteurs viraux est segmenté par type, maladie, et application. Par type, le marché est segmenté en vecteurs adénoviraux, vecteurs viraux adéno-associés, vecteurs lentiviraux, vecteurs rétroviraux, et autres types. Par maladie, le marché est segmenté en cancer, troubles génétiques, maladies infectieuses, et autres maladies. Par application, le marché est segmenté en thérapie génique et vaccinologie. Par géographie, le marché mondial est segmenté en Amérique du Nord (États-Unis, Canada, Mexique), Europe (Allemagne, Royaume-Uni, France, Italie, Espagne, reste de l'Europe), Asie-Pacifique (Chine, Japon, Inde, Australie, Corée du Sud, reste de l'Asie-Pacifique), Moyen-Orient et Afrique (CCG, Afrique du Sud, reste du Moyen-Orient et Afrique), et Amérique du Sud (Brésil, Argentine, reste de l'Amérique du Sud).
Le rapport de marché couvre également la taille estimée du marché de la fabrication de vecteurs viraux et les tendances pour 17 pays à travers les principales régions mondiales. Le rapport offre la valeur (en milliards USD) pour les segments ci-dessus.
| Vecteurs viraux adéno-associés (AAV) |
| Vecteurs lentiviraux |
| Vecteurs adénoviraux |
| Vecteurs rétroviraux et γ-rétroviraux |
| Virus oncolytiques et autres virus modifiés |
| Cancer |
| Troubles génétiques |
| Maladies infectieuses |
| Troubles neurologiques |
| Autres domaines thérapeutiques |
| Thérapie génique in-vivo |
| Fabrication de thérapie cellulaire ex-vivo (CAR-T, TCR-T, etc.) |
| Vaccinologie préventive et thérapeutique |
| Fabrication interne |
| Fabrication sous contrat (CDMO) |
| Amérique du Nord | États-Unis |
| Canada | |
| Mexique | |
| Europe | Allemagne |
| Royaume-Uni | |
| France | |
| Italie | |
| Espagne | |
| Reste de l'Europe | |
| Asie-Pacifique | Chine |
| Japon | |
| Inde | |
| Australie | |
| Corée du Sud | |
| Reste de l'Asie-Pacifique | |
| Moyen-Orient et Afrique | CCG |
| Afrique du Sud | |
| Reste du Moyen-Orient et Afrique | |
| Amérique du Sud | Brésil |
| Argentine | |
| Reste de l'Amérique du Sud |
| Par type de vecteur | Vecteurs viraux adéno-associés (AAV) | |
| Vecteurs lentiviraux | ||
| Vecteurs adénoviraux | ||
| Vecteurs rétroviraux et γ-rétroviraux | ||
| Virus oncolytiques et autres virus modifiés | ||
| Par maladie | Cancer | |
| Troubles génétiques | ||
| Maladies infectieuses | ||
| Troubles neurologiques | ||
| Autres domaines thérapeutiques | ||
| Par application | Thérapie génique in-vivo | |
| Fabrication de thérapie cellulaire ex-vivo (CAR-T, TCR-T, etc.) | ||
| Vaccinologie préventive et thérapeutique | ||
| Par mode de fabrication | Fabrication interne | |
| Fabrication sous contrat (CDMO) | ||
| Géographie | Amérique du Nord | États-Unis |
| Canada | ||
| Mexique | ||
| Europe | Allemagne | |
| Royaume-Uni | ||
| France | ||
| Italie | ||
| Espagne | ||
| Reste de l'Europe | ||
| Asie-Pacifique | Chine | |
| Japon | ||
| Inde | ||
| Australie | ||
| Corée du Sud | ||
| Reste de l'Asie-Pacifique | ||
| Moyen-Orient et Afrique | CCG | |
| Afrique du Sud | ||
| Reste du Moyen-Orient et Afrique | ||
| Amérique du Sud | Brésil | |
| Argentine | ||
| Reste de l'Amérique du Sud | ||
Questions clés répondues dans le rapport
Quelle est la taille actuelle du marché de la fabrication de vecteurs viraux ?
Le marché est évalué à 2,95 milliards USD en 2025 et est projeté pour atteindre 7,66 milliards USD d'ici 2030 avec un TCAC de 21,01 %.
Quel type de vecteur domine le marché de la fabrication de vecteurs viraux ?
Les plateformes virales adéno-associées mènent avec une part de revenus de 72,45 % grâce aux profils de sécurité favorables et aux multiples thérapies approuvées par la FDA.
Pourquoi les CDMO gagnent-elles en importance dans l'industrie de la fabrication de vecteurs viraux ?
Les développeurs préfèrent les CDMO spécialisées pour leurs processus validés, leurs analyses avancées et leur capacité prête, évitant les CapEx élevés de construction d'usines propriétaires.
Quelle région croît le plus rapidement dans le marché de la fabrication de vecteurs viraux ?
L'Asie-Pacifique devrait croître avec un TCAC de 22,56 % jusqu'en 2030, soutenue par les initiatives de biofabrication multi-milliardaires de la Chine et les capacités régionales en expansion.
Quelle est la principale barrière de coût pour une adoption plus large des thérapies géniques ?
Les dépenses de production élevées maintiennent les prix des thérapies dans la fourchette de 2 millions USD - 3,5 millions USD, mais l'optimisation des processus réduit lentement le coût par dose.
À quel point la concurrence est-elle concentrée dans le marché de la fabrication de vecteurs viraux ?
Les cinq principaux fournisseurs contrôlent environ 60 % de la capacité commerciale mondiale, indiquant une concentration modérée qui permet encore aux nouveaux entrants de gagner des parts.
Dernière mise à jour de la page le:



