Tamaño y Participación del Mercado de Pruebas de Validez de Muestras
Análisis del Mercado de Pruebas de Validez de Muestras por Mordor Intelligence
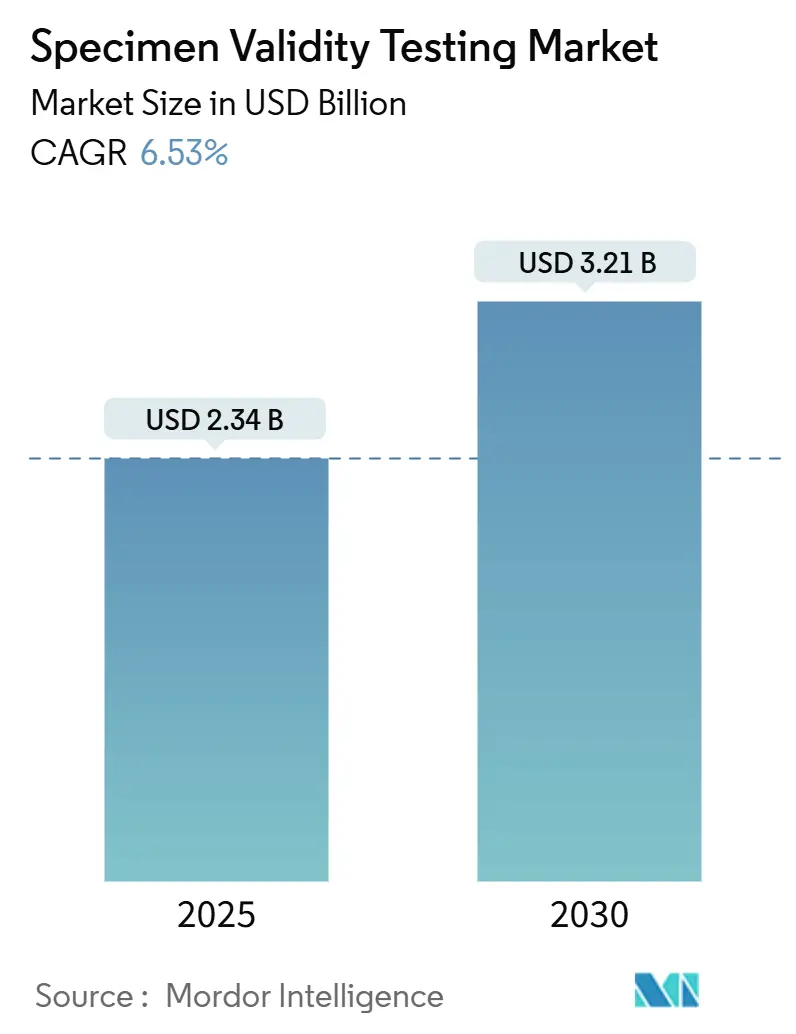
El tamaño del mercado de pruebas de validez de muestras está valorado en USD 2.34 mil millones en 2025 y se proyecta que alcance USD 3.21 mil millones para 2030, avanzando a una TCAC del 6.53%. La trayectoria refleja el endurecimiento de los mandatos de seguridad laboral, la adopción acelerada de plataformas de pruebas en el punto de atención (POC), y las actualizaciones tecnológicas que detectan intentos sofisticados de adulteración. Los empleadores en transporte, energía y atención médica continúan ampliando la cobertura de pruebas, mientras que las actualizaciones gubernamentales-como la expansión del panel federal de enero de 2025 que ahora incluye fentanilo y norfentanilo-elevan el estándar de integridad para todos los laboratorios. El aumento del uso de telemedicina también ha abierto un nuevo canal de recolección remota, impulsando la demanda de dispositivos a prueba de manipulación y análisis impulsados por IA que verifican la integridad de las muestras en tiempo real. Aunque las matrices no urinarias están ganando favor, el mercado de pruebas de validez de muestras se mantiene respaldado por programas de orina de alto volumen que aún dominan los entornos regulados.
Conclusiones Clave del Informe
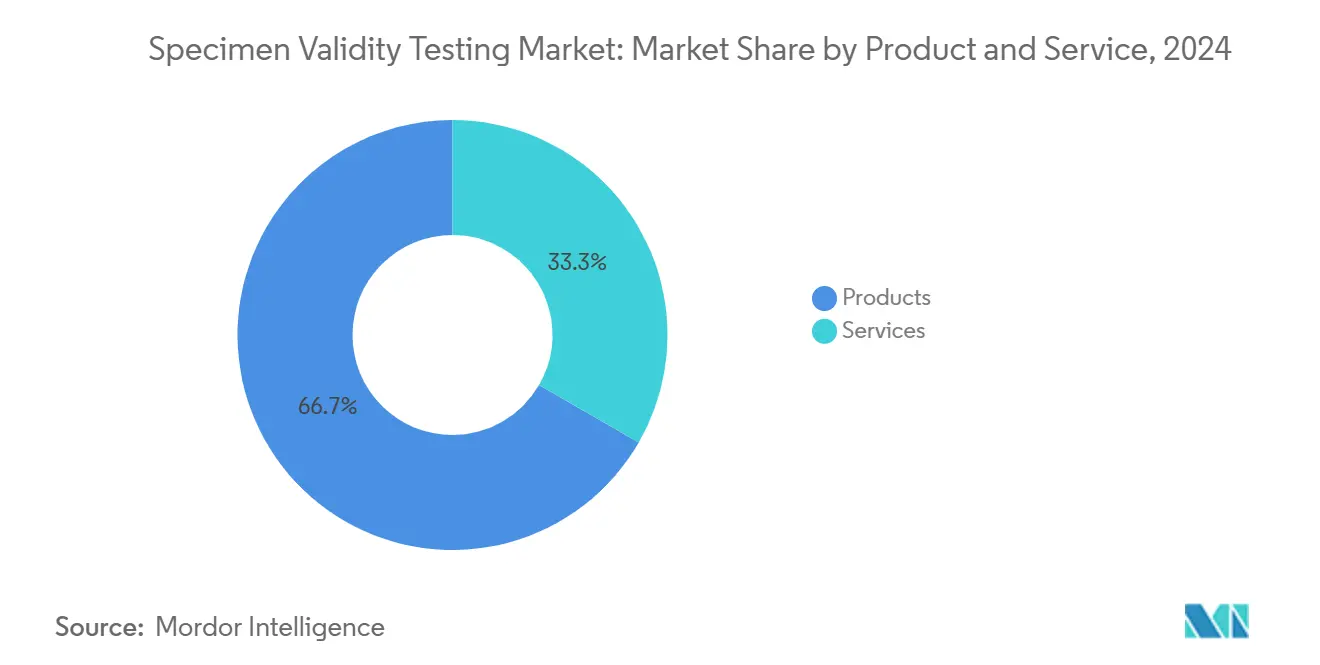
- Por producto y servicio, los productos consumibles mantuvieron el 66.67% de participación de ingresos en 2024, mientras que los servicios están pronosticados a registrar la TCAC más rápida del 7.21% hasta 2030.
- Por tipo, las pruebas de laboratorio mantuvieron el 59.65% de la participación del mercado de pruebas de validez de muestras en 2024, mientras que las plataformas POC están programadas para expandirse a una TCAC del 7.29% hasta 2030.
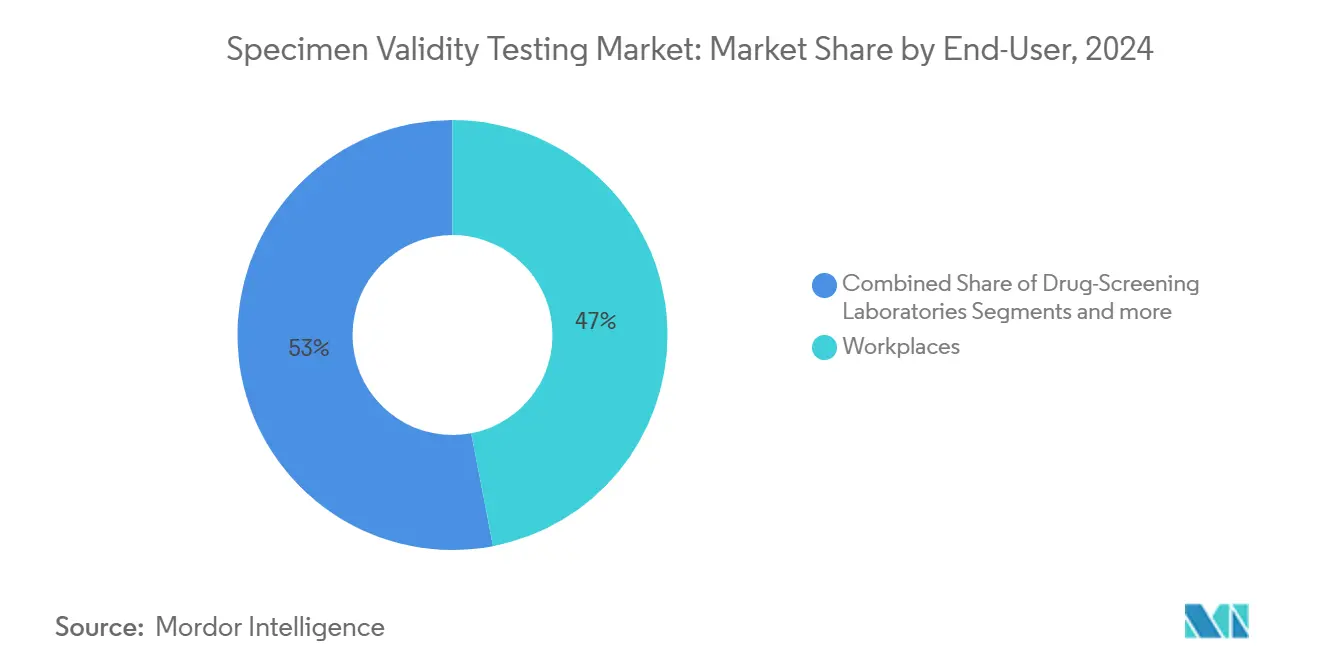
- Por usuario final, los programas laborales lideraron con el 46.98% de participación de ingresos en 2024; los laboratorios de detección de drogas registran la TCAC proyectada más alta del 7.33% hasta 2030.
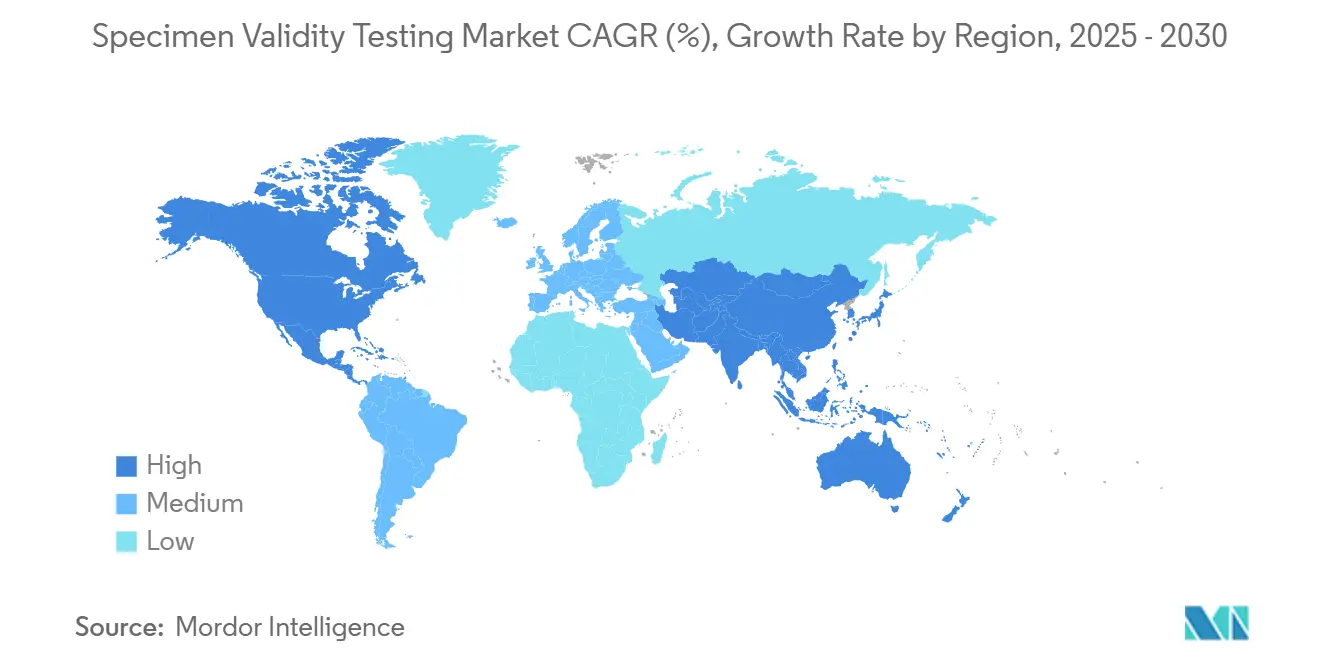
- Por geografía, América del Norte comandó el 41.34% de participación del tamaño del mercado de pruebas de validez de muestras en 2024; Asia-Pacífico está establecido para crecer a una TCAC del 7.41% de 2025-2030.
Tendencias e Información del Mercado Global de Pruebas de Validez de Muestras
Análisis de Impacto de Impulsores
| Impulsor | ( ~ ) % Impacto en Pronóstico TCAC | Relevancia Geográfica | Cronograma de Impacto |
|---|---|---|---|
| Crecientes mandatos de pruebas de drogas laborales | +1.2% | Global, concentrado en América del Norte y UE | Mediano plazo (2-4 años) |
| Adopción rápida de dispositivos SVT POC | +0.9% | América del Norte y Asia-Pacífico | Corto plazo (≤ 2 años) |
| Expansión de telemedicina impulsando kits domésticos | +0.7% | América del Norte y UE | Mediano plazo (2-4 años) |
| Algoritmos de aprendizaje automático para detección de adulteración en vivo | +0.6% | Global, liderado por América del Norte | Largo plazo (≥ 4 años) |
| Legalización del cannabis impulsando paneles diferenciados | +0.5% | América del Norte, expandiéndose a UE | Corto plazo (≤ 2 años) |
| Seguridad de cadena de suministro impulsando controles estériles | +0.4% | Global | Mediano plazo (2-4 años) |
| Fuente: Mordor Intelligence | |||
Crecientes Mandatos de Pruebas de Drogas Laborales
Los reguladores en seis continentes están fortaleciendo las reglas de seguridad corporativa, empujando a los empleadores a verificar no solo la presencia de drogas sino la autenticidad de cada muestra. Las directivas alineadas con OSHA en Estados Unidos, las Regulaciones de Transporte de Mercancías Peligrosas de Canadá, y la orden obligatoria de pruebas de petróleo y gas del Ministerio de Mano de Obra de Omán subrayan un movimiento colectivo hacia verificaciones de validez de muestras más estrictas. Las grandes corporaciones incorporan cada vez más software de cadena de custodia y supervisión de Oficial de Revisión Médica (MRO) en los procedimientos operativos estándar, mitigando el riesgo de litigio después de accidentes. El multiplicador de demanda resultante eleva las ventas recurrentes de tiras de temperatura, ensayos de oxidantes, y sistemas de custodia digital [1]Autoridad General de Aviación Civil, MEDIOS ACEPTABLES DE CUMPLIMIENTO,
gcaa.gov.ae.
Adopción Rápida de Dispositivos SVT POC
Los analizadores portátiles recientemente aprobados ahora completan las detecciones de adulterantes en menos de seis minutos, cumpliendo con el estándar de "inmediatez" requerido en investigaciones post-incidente. La autorización de la Administración de Alimentos y Medicamentos de EE.UU. (FDA) para ensayos de fentanilo en el sitio ha establecido un precedente para integrar verificaciones de validez en copas POC de un solo paso. Los empleadores valoran el tiempo de inactividad reducido, mientras que los laboratorios ven menos muestras rechazadas, acortando los ciclos de facturación. Los proveedores responden con lectores modulares que imprimen informes listos para cumplimiento, reforzando los ingresos recurrentes de consumibles.
Expansión de Telemedicina Impulsando Kits SVT Domésticos
El manejo remoto de pacientes con dependencia de opioides y manejo del dolor demanda kits de autorecolección que protejan contra la sustitución. Los ensayos académicos muestran tasas de finalización superiores al 80% para envíos de orina remotos cuando los parámetros de validez-temperatura, pH, creatinina-están integrados en los dispositivos de recolección. Las aseguradoras de salud ahora requieren prueba documental de validez antes de reembolsar códigos de alta complejidad, impulsando a las clínicas a adoptar tubos de transporte a prueba de manipulación y sensores de temperatura Bluetooth.
Algoritmos de Aprendizaje Automático para Detección de Adulteración en Vivo
Los laboratorios de investigación despliegan modelos de aprendizaje profundo que comparan espectros de series temporales, marcando anomalías imposibles de ver a través de ensayos de parámetro único. Los estudios de validación temprana logran una precisión del 95%+ en la identificación de orina sintética o picos de oxidantes. El lanzamiento comercial está listo para reducir las tasas de falsos negativos y aliviar la carga de interpretación en los MROs, dando a los proveedores de reactivos de espectrometría de masas compatibles una ventaja competitiva [2]Yi-Ching Lin, PS2MS: Un Sistema de Predicción Basado en Aprendizaje Profundo para Identificar Nuevas Sustancias Psicoactivas Usando Espectrometría de Masas,
ACS Publications, pubs.acs.org.
Análisis de Impacto de Limitaciones
| Limitación | ( ~ ) % Impacto en Pronóstico TCAC | Relevancia Geográfica | Cronograma de Impacto |
|---|---|---|---|
| Conciencia limitada entre clínicas pequeñas y medianas | -0.8% | Global, más agudo en Asia-Pacífico y MEA | Corto plazo (≤ 2 años) |
| Cambio hacia matrices no urinarias | -0.6% | América del Norte y UE | Mediano plazo (2-4 años) |
| Limitaciones de privacidad de datos en plataformas biométricas | -0.4% | UE y América del Norte | Largo plazo (≥ 4 años) |
| Escaseces esporádicas de reactivos y picos de materias primas | -0.3% | Global | Corto plazo (≤ 2 años) |
| Fuente: Mordor Intelligence | |||
Conciencia Limitada Entre Clínicas Pequeñas y Medianas
Los proveedores de atención médica más pequeños a menudo subestiman la responsabilidad vinculada a muestras inválidas. Las encuestas destacan que el 59% de las barreras de implementación en el punto de atención se relacionan con capacitación y aseguramiento de calidad, dejando a muchas clínicas sin verificación de temperatura o verificaciones de gravedad específica. Las políticas de reembolso ahora niegan reclamos que carecen de documentación de validez, pero persisten brechas de conocimiento, ralentizando la adopción [3]Blue Cross Blue Shield de Michigan, Pruebas de Drogas en Manejo del Dolor y Tratamiento de Trastorno por Uso de Sustancias,
bcbsm.com.
Cambio Hacia Matrices No Urinarias Reduciendo la Demanda SVT
La autorización federal de pruebas de fluido oral para empleados gubernamentales ha impulsado a las empresas privadas a adoptar la saliva como matriz principal, lo que reduce el riesgo de adulteración y por tanto la necesidad de paneles de validez de orina multi-parámetro. Los pronósticos sugieren que el 30% de las pruebas reguladas federalmente podrían migrar al fluido oral dentro de cuatro años, recortando el potencial de crecimiento para consumibles enfocados en orina.
Análisis de Segmentos
Por Producto y Servicio: Los Productos Mantienen Escala, los Servicios se Aceleran
Los productos anclaron el 66.67% de los ingresos de 2024, sostenidos por la naturaleza consumible de los kits de ensayo, reactivos oxidantes, estándares de creatinina, y copas de recolección de un solo uso. Las tiras indicadoras de temperatura solas generaron un ciclo de reemplazo de alta velocidad, especialmente en grandes empresas de logística y energía. Los servicios, sin embargo, registran una TCAC del 7.21% hasta 2030 ya que los empleadores subcontratan la interpretación de resultados y auditorías de cumplimiento a consultores MRO y laboratorios especializados. Los entornos médico-legales favorecen ofertas empaquetadas que fusionan la gestión de cadena de custodia con análisis de aprendizaje automático. El tamaño del mercado de pruebas de validez de muestras para servicios está pronosticado a alcanzar USD 1.24 mil millones para 2030, manteniendo el impulso a pesar del dominio de los consumibles.
La ola de servicios también se apoya en la medicina de recolección remota. Las plataformas de telemedicina contratan laboratorios de terceros para verificar la temperatura de la muestra y los niveles de oxidantes al llegar, pagando tarifas premium por adjudicación el mismo día. La demanda aumenta para revisiones MRO virtuales en programas de empleo transfronterizo, ampliando los ingresos direccionables y solidificando el mercado de pruebas de validez de muestras como una solución holística en lugar de solo una vertical de productos.
Por Tipo: Pruebas de Laboratorio Dominantes, POC Gana Velocidad
Los flujos de trabajo de laboratorio mantuvieron el 59.65% de participación en 2024. Los laboratorios centralizados manejan sistemas de cromatografía líquida-espectrometría de masas en tándem (LC-MS/MS) que analizan temperatura, gravedad específica, creatinina, pH, y oxidantes con precisión regulatoria. Esa infraestructura sustenta el liderazgo de participación del mercado de pruebas de validez de muestras de grandes laboratorios de referencia. Sin embargo, los formatos POC avanzan TCAC del 7.29%, impulsados por fotómetros portátiles y copas inmunocromatográficas que verifican cruzadamente tres o más parámetros de validez en minutos. El tamaño del mercado de pruebas de validez de muestras vinculado a plataformas POC se espera que ascienda a USD 1.38 mil millones para 2030 ya que la precisión del dispositivo se aproxima a los estándares de laboratorio.
Los sectores de alto riesgo como la construcción ahora despliegan analizadores POC ruguerizados en sitios de trabajo para pruebas post-incidente, reduciendo el tiempo de inactividad. Mientras tanto, los modelos híbridos ven las muestras primero detectadas por dispositivos POC y solo los positivos-junto con cualquier anomalía de validez marcada-enviados a laboratorios, optimizando la distribución de carga de trabajo.
Por Usuario Final: Los Centros de Trabajo Lideran, los Laboratorios se Aceleran
Los programas corporativos representaron el 46.98% de los ingresos de 2024, cementando su rol como el consumidor principal de consumibles de validez. Los empleadores de transporte, petróleo y gas, y sector público mantienen pruebas obligatorias de pre-empleo y aleatorias, asegurando volumen constante. Los laboratorios de detección de drogas aumentan más rápido a TCAC del 7.33%, reflejando la consolidación que atrae volúmenes de clínicas más pequeñas hacia centros de alto rendimiento.
Las clínicas de manejo del dolor, bajo escrutinio del pagador, subcontratan cada vez más a instalaciones especializadas capaces de proporcionar métricas de validez integrales. Las agencias de justicia criminal, otro nicho crítico, demandan trazabilidad de cadena de custodia y han comenzado a solicitar registros de temperatura legibles por máquina, profundizando el papel de las plataformas de validez avanzadas.
Nota: Participaciones de segmento de todos los segmentos individuales disponibles con la compra del informe
Análisis Geográfico
América del Norte retuvo el 41.34% de ingresos en 2024 y permanece como el marcador regulatorio para el mercado de pruebas de validez de muestras. El Departamento de Salud y Servicios Humanos requiere que cada muestra de orina regulada documente temperatura (32-38 °C), pH (4.5-8.0), gravedad específica (≥1.003), y creatinina (≥20 mg/dL) inmediatamente después de la recolección SAMHSA. La revisión del panel de enero de 2025, que agregó fentanilo y norfentanilo, aumentó aún más la necesidad de los laboratorios de confirmación de validez precisa para evitar falsos negativos bajo nuevos límites de analito Federal Register. Los mandatos paralelos del Departamento de Transporte se aplican a aproximadamente 10 millones de trabajadores sensibles a la seguridad, garantizando altos volúmenes de pruebas. El marco orientado a la privacidad de Canadá reduce las pruebas aleatorias pero enfatiza los programas de fluido oral que aún dependen de la temperatura y documentación de cadena de custodia para la defendibilidad.
Asia-Pacífico registra la TCAC más rápida del 7.41% hasta 2030, impulsada por fábricas multinacionales en China e India que incorporan las mejores prácticas de la Administración de Seguridad y Salud Ocupacional de EE.UU. (OSHA) en operaciones locales. Los gigantes de diagnóstico global han abierto centros regionales para suministrar kits de ensayo y proporcionar servicios MRO en idiomas nativos. El cumplimiento de comercio transfronterizo impulsa a las empresas a adoptar sistemas de cadena de custodia estilo estadounidense, dando al mercado de pruebas de validez de muestras nueva escala. Los gobiernos regionales están estudiando estatutos obligatorios de pruebas de drogas, particularmente en transporte y minería, lo que incorporaría aún más las verificaciones de integridad de muestras.
Europa ofrece regulación fragmentada. Los operadores ferroviarios alemanes aplican reglas estrictas de validez de muestras modeladas en las directrices federales estadounidenses, mientras que Francia limita las pruebas a roles sensibles a la seguridad e impone filtros de privacidad más estrictos. El Reglamento de Diagnóstico In Vitro (IVDR) de la UE impone obligaciones de rendimiento y vigilancia post-mercado en dispositivos de validez que ingresan al bloque, elevando las barreras de entrada pero estandarizando la calidad. Los empleadores paneuropeos por tanto se inclinan hacia sistemas de recolección marcados CE que integran sellos de integridad con código de barras y registros de custodia en la nube.
El Medio Oriente y África siguen estándares internacionales de contratación de petróleo y gas. Los reguladores de aviación del GCC requieren verificaciones de validez supervisadas por MRO, con protocolos de cadena de custodia que reflejan las directrices SAMHSA de EE.UU. Las casas mineras de Sudáfrica se asocian con laboratorios globales para cumplir con las expectativas del comprador para métricas de pruebas de alta integridad. América del Sur está liderada por Brasil, donde la Ley 13.103/15 obliga a los conductores profesionales a someterse a evaluaciones toxicológicas periódicas que incluyen documentación de validez de muestras; la popularidad de las pruebas de cabello sin embargo demanda protocolos de validación cruzada para confirmar autenticidad. El sector automotriz en expansión de Argentina importa directrices DOT de EE.UU. para satisfacer a los socios de la cadena de suministro.
Panorama Competitivo
El mercado de pruebas de validez de muestras presenta fragmentación moderada. Abbott, Thermo Fisher Scientific, Laboratory Corporation of America, Quest Diagnostics, y Siemens Healthineers colectivamente representan una porción decente de los ingresos globales. Las ventajas de escala provienen de carteras integradas de ensayo-a-análisis y redes logísticas extensas. La plataforma iCUP de Abbott ahora incorpora monitoreo de temperatura en tiempo real y tiras oxidantes, empaquetando validez con detecciones rápidas de drogas Abbott. Quest Diagnostics ha expandido su huella internacional a más de 80 naciones, ofreciendo paneles de cadena de custodia basados en la nube que simplifican el cumplimiento multinacional Quest Diagnostics.
La diferenciación tecnológica impulsa la competencia actual. Las asociaciones entre laboratorios de referencia y proveedores de IA entregan clasificadores de adulteración de aprendizaje automático, aumentando la adherencia del servicio. Siemens Healthineers pilotea flujos de trabajo de espectrometría de masas vinculados a la nube que marcan relaciones atípicas de creatinina-a-gravedad específica en tiempo casi real, reduciendo las cargas de informes en MROs. Mientras tanto, los proveedores especializados como Labcon enfatizan copas de recolección de grado médico, compatibles con IATA, abordando preocupaciones de esterilidad de la cadena de suministro Labcon.
Las start-ups se enfocan en innovaciones de saliva y micromuestreo-áreas listas para erosionar volúmenes de orina pero que aún requieren prueba de identidad del donante e integridad de la muestra. Las empresas establecidas se protegen adquiriendo o licenciando estas tecnologías, manteniendo ingresos independientemente de los cambios de matriz. Los proveedores regionales en Asia-Pacífico cortejan contratos multinacionales ofreciendo soporte MRO bilingüe y rastreo en la nube llave en mano, desafiando el dominio norteamericano.
Líderes de la Industria de Pruebas de Validez de Muestras
Abbott
Thermo Fisher Scientific
LabCorp
Healgen Scientific LLC
Premier Biotech, Inc.
- *Nota aclaratoria: los principales jugadores no se ordenaron de un modo en especial
Desarrollos Recientes de la Industria
- Enero 2025: El Departamento de Salud y Servicios Humanos de EE.UU. actualizó las Directrices Obligatorias, agregando fentanilo y norfentanilo mientras removía MDMA y MDA, obligando a los laboratorios a ajustar los flujos de trabajo de validez Federal Register.
- Diciembre 2024: BD y Babson Diagnostics introdujeron tecnología de micromuestreo de sangre capilar, expandiendo los conceptos de pruebas de validez a la recolección de sangre de pequeño volumen BD.
- Agosto 2024: FDA autorizó la primera detección de fentanilo urinario POC en el analizador RYAN, catalizando la verificación de validez en el sitio FDA.
- Febrero 2024: SAMHSA lanzó un Manual de Recolección de Muestras de Orina revisado detallando umbrales de validez actualizados y pasos de detección de adulteración SAMHSA.
Alcance del Informe Global del Mercado de Pruebas de Validez de Muestras
Según el alcance del informe, las pruebas de validez de muestras (SVT) son las pruebas de detección para muestras de orina para detectar cualquier adulteración, dilución, o sustitución. SVT proporciona información crítica sobre la confiabilidad y precisión de los resultados de las pruebas de drogas a los clínicos, y también valida que la muestra de orina probada es una muestra válida de orina humana. El mercado de pruebas de validez de muestras está segmentado por tipo de droga (medicamentos antibacterianos, medicamentos antifúngicos, medicamentos antivirales, y otros medicamentos), indicación (infecciones del torrente sanguíneo, infecciones del tracto urinario, infecciones del sitio quirúrgico, neumonía, y otras indicaciones), y geografía (América del Norte, Europa, Asia-Pacífico, Medio Oriente y África, y América del Sur). El informe de mercado también cubre los tamaños de mercado estimados y tendencias para 17 países diferentes a través de las principales regiones globalmente. El informe ofrece el valor (en USD) para los segmentos anteriores.
| Productos | Kits de Ensayo |
| Reactivos y Calibradores | |
| Desechables | |
| Servicios |
| Pruebas de Laboratorio |
| Pruebas Rápidas y POC |
| Centros de Trabajo |
| Sistemas de Aplicación de la Ley y Justicia Criminal |
| Laboratorios de Detección de Drogas |
| Centros de Manejo del Dolor |
| Otros |
| América del Norte | Estados Unidos |
| Canadá | |
| México | |
| Europa | Alemania |
| Reino Unido | |
| Francia | |
| Italia | |
| España | |
| Resto de Europa | |
| Asia-Pacífico | China |
| Japón | |
| India | |
| Australia | |
| Corea del Sur | |
| Resto de Asia-Pacífico | |
| Medio Oriente y África | GCC |
| Sudáfrica | |
| Resto de Medio Oriente y África | |
| América del Sur | Brasil |
| Argentina | |
| Resto de América del Sur |
| Por Producto y Servicio | Productos | Kits de Ensayo |
| Reactivos y Calibradores | ||
| Desechables | ||
| Servicios | ||
| Por Tipo | Pruebas de Laboratorio | |
| Pruebas Rápidas y POC | ||
| Por Usuario Final | Centros de Trabajo | |
| Sistemas de Aplicación de la Ley y Justicia Criminal | ||
| Laboratorios de Detección de Drogas | ||
| Centros de Manejo del Dolor | ||
| Otros | ||
| Por Geografía | América del Norte | Estados Unidos |
| Canadá | ||
| México | ||
| Europa | Alemania | |
| Reino Unido | ||
| Francia | ||
| Italia | ||
| España | ||
| Resto de Europa | ||
| Asia-Pacífico | China | |
| Japón | ||
| India | ||
| Australia | ||
| Corea del Sur | ||
| Resto de Asia-Pacífico | ||
| Medio Oriente y África | GCC | |
| Sudáfrica | ||
| Resto de Medio Oriente y África | ||
| América del Sur | Brasil | |
| Argentina | ||
| Resto de América del Sur | ||
Preguntas Clave Respondidas en el Informe
¿Cuál es el tamaño actual del mercado de pruebas de validez de muestras?
El tamaño del mercado de pruebas de validez de muestras se sitúa en USD 2.34 mil millones en 2025 y se proyecta que alcance USD 3.21 mil millones para 2030.
¿Qué región domina el mercado de pruebas de validez de muestras?
América del Norte lidera con el 41.34% de participación de ingresos en 2024 debido a requisitos federales laborales estrictos.
¿Por qué los servicios están creciendo más rápido que los productos?
La creciente complejidad del protocolo, las pruebas remotas, y la necesidad de interpretación experta del Oficial de Revisión Médica están impulsando una TCAC del 7.21% para servicios.
¿Cómo está influyendo la IA en las pruebas de validez de muestras?
Los modelos de aprendizaje automático ahora detectan patrones sofisticados de adulteración con precisión del 95%+, mejorando la confiabilidad del laboratorio y la diferenciación competitiva.
¿Qué impacto tienen las matrices no urinarias en el crecimiento del mercado?
El cambio hacia pruebas de fluido oral y cabello reduce la demanda de consumibles de validez de orina tradicionales pero abre oportunidades para nuevas herramientas de verificación de integridad adaptadas a matrices alternativas.
¿Qué segmento de usuario final se está expandiendo más rápidamente?
Los laboratorios de detección de drogas, respaldados por tendencias de consolidación y subcontratación, están establecidos para crecer a una TCAC del 7.33% hasta 2030.
Última actualización de la página el:



