Globale Virale Inaktivierung Marktgröße und -anteil
Globale Virale Inaktivierung Marktanalyse von Mordor Intelligence
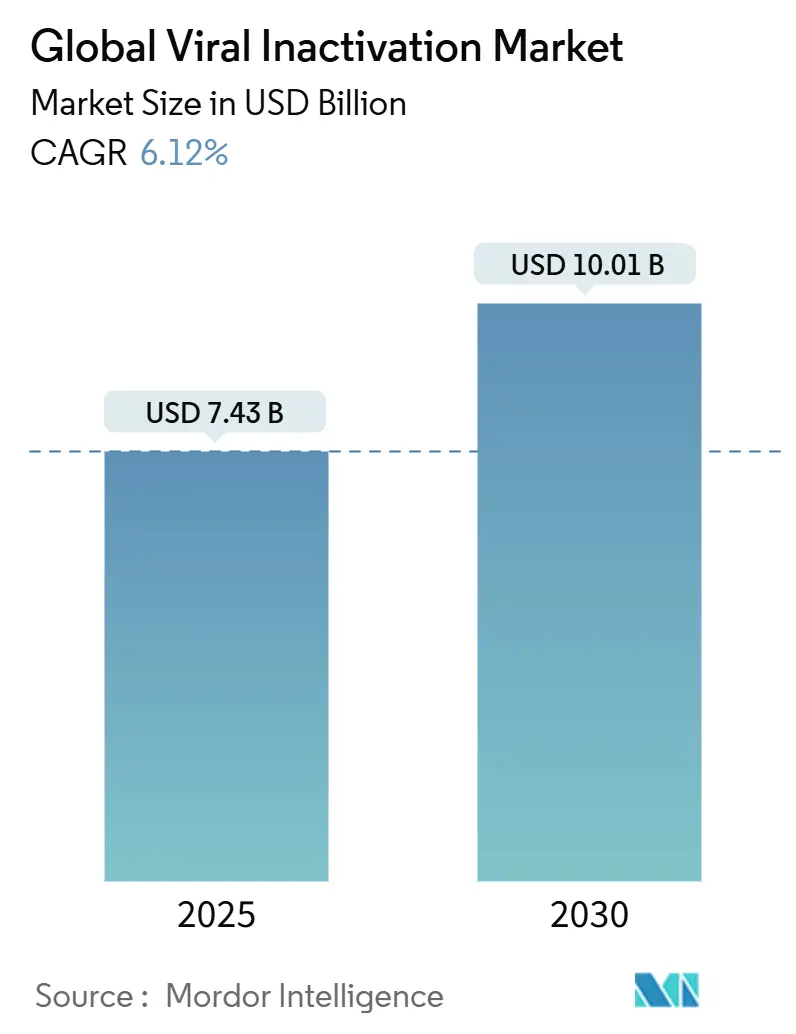
Der virale Inaktivierung Markt belief sich 2025 auf 7,43 Milliarden USD und wird voraussichtlich mit einer CAGR von 6,12% voranschreiten und bis 2030 10,01 Milliarden USD erreichen. Erhöhte Biologika-Produktion, steigende Zell- und Gentherapie (CGT) Volumina sowie strengere globale Sicherheitserwartungen verleihen dem Markt seine gegenwärtige Dynamik. Die Nachfrage beschleunigt sich, da Regulierungsbehörden veraltete Detergenzien wie Triton X-100 auslaufen lassen und Hersteller zu umweltverträglichen Chemikalien und wärmebasierten Ansätzen lenken. Die Auslagerung von viralen Clearance-Arbeiten an spezialisierte Labore steigt parallel zur raschen CDMO-Expansion, insbesondere in Asien-Pazifik, wo großangelegte virale Vektorkapazitäten aufgebaut werden, um westliche Biopharma-Projekte anzuziehen. Die Wettbewerbsintensität steigt weiterhin, da führende Filtrations-, Reagenz- und Serviceanbieter ihre Portfolios durch gezielte Akquisitionen erweitern, die auf die schnell wachsende CGT-Gelegenheit abzielen. Die kombinierte Wirkung dieser Faktoren festigt den virale Inaktivierung Markt als wesentlichen Ermöglicher der biopharmazeutischen Produktivität und Patientensicherheit.
Wichtige Berichtsergebnisse
- Nach Methode führte die Lösungsmittel-Detergenz-Technologie mit 46,43% Umsatzanteil im Jahr 2024; Pasteurisierung und Wärmebehandlung soll mit einer CAGR von 8,65% bis 2030 expandieren.
- Nach Produkt beherrschten Kits und Reagenzien 41,45% des virale Inaktivierung Marktanteils im Jahr 2024, während Validierungs- und Testdienste voraussichtlich jährlich um 8,93% bis 2030 wachsen werden.
- Nach Anwendung entfielen Impfstoffe und Therapeutika auf 49,54% der virale Inaktivierung Marktgröße im Jahr 2024; Zell- und Gentherapieprodukte schreiten mit einer CAGR von 8,88% bis 2030 voran.
- Nach Endverbraucher hielten Biopharma- und Biotechnologie-Unternehmen 53,45% der Nachfrage im Jahr 2024; CDMOs verzeichnen die höchste prognostizierte CAGR von 9,76% bis 2030.
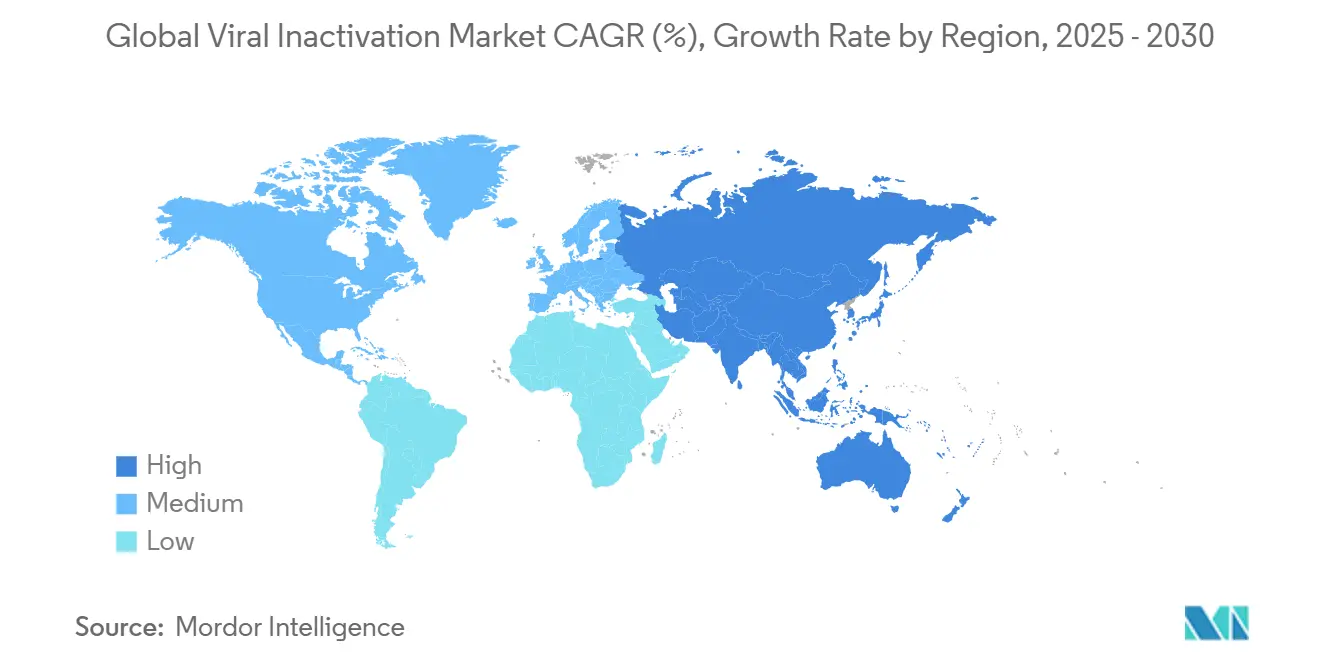
- Regional behielt Nordamerika 42,12% Anteil im Jahr 2024, während Asien-Pazifik auf Kurs für eine CAGR von 7,45% bis 2030 ist.
Globale Virale Inaktivierung Markttrends und Einblicke
Treiber-Auswirkungsanalyse
| Treiber | % Auswirkung auf CAGR-Prognose | Geografische Relevanz | Auswirkungszeitrahmen |
|---|---|---|---|
| Expansion von Biologika- und Gentherapie-Pipelines | +1.8% | Global (Nordamerika & Europa führend) | Mittelfristig (2-4 Jahre) |
| Steigende Häufigkeit viraler Kontaminationsrückrufe | +1.2% | Global (regulierte Märkte) | Kurzfristig (≤ 2 Jahre) |
| Strenge globale regulatorische Mandate für virale Sicherheit | +1.5% | Global (FDA, EMA, expandierendes APAC) | Langfristig (≥ 4 Jahre) |
| Wechsel zu Einweg-Bioprozessierungsplattformen | +0.9% | Nordamerika & Europa, Ausbreitung nach APAC | Mittelfristig (2-4 Jahre) |
| Auslaufen von Triton X-100 treibt alternative Lösungen | +0.6% | EU-getrieben, weltweite Übernahme | Kurzfristig (≤ 2 Jahre) |
| Risikokapitalfinanzierung für virale Vektor-CDMOs & Start-ups | +0.8% | Nordamerika (Übertragung nach APAC) | Mittelfristig (2-4 Jahre) |
| Quelle: Mordor Intelligence | |||
Expansion von Biologika- und Gentherapie-Pipelines
Pipeline-Wachstum bleibt der wichtigste Katalysator für den virale Inaktivierung Markt. Mehr als 1.200 aktive US-CGT-Klinische Studien wurden 2024 registriert, was eine beispiellose therapeutische Breite unterstreicht. CGT-Zulassungen, die nun insgesamt 37 in den Vereinigten Staaten betragen, vervielfachen virale Clearance-Arbeitslasten, da jede Vektorplattform orthogonale Inaktivierungstests erfüllen muss. Der Schwenk von der Behandlung seltener Störungen hin zu häufigen Krankheiten wie Herzinsuffizienz erfordert höhere Chargenvolumen und zwingt Hersteller dazu, skalierbare Sicherheitslösungen früh in der Entwicklung zu implementieren. Adeno-assoziierte Virusprogramme veranschaulichen die Komplexität und erfordern oft Kombinationen aus niedrigem pH-Wert, Lösungsmittel-Detergenz und Wärmehaltung, um Regulierungsbehörden zufriedenzustellen. Während sich CGT-Anlagen weltweit vermehren, speist jeder zusätzliche klinische Kandidat stetige Serviceeinnahmen für virale Inaktivierung Experten.
Steigende Häufigkeit viraler Kontaminationsrückrufe
Produktionsfehler lösen weiterhin kostspielige Medikamentenrückrufe aus, wobei zwischen 2018 und 2023 weltweit 2.900 sterile Produktrücknahmen verzeichnet wurden[1]U.S. Food & Drug Administration, "Drug Recall Enforcement Reports," fda.gov. Warnschreiben an multinationale Hersteller in 2024 und 2025 zeigen, dass unzureichende Clearance-Protokolle auch in ausgereiften Anlagen ein Problem bleiben. Ein einziges Kontaminationsereignis kann die Produktion an mehreren Standorten stoppen und Korrekturkosten von 100 Millionen USD oder mehr verursachen, was Redundanz zu einer besseren wirtschaftlichen Wahl als Sanierung macht. Unternehmen implementieren nun kontinuierliche Inline-Virusfilter, automatisierte Probenahme und Umweltüberwachung, um die Ereigniswahrscheinlichkeit zu reduzieren. Versicherungsträger haben begonnen, Policenprämien an validierte virale Sicherheitsinfrastrukturen zu koppeln und fügen finanzielle Motivation hinzu, Prozesse schnell zu verbessern.
Strenge globale regulatorische Mandate für virale Sicherheit
Revision Q5A(R2) erzwingt eine tiefere risikobasierte virale Bewertung für Biotechnologieprodukte und erhöht Datenerwartungen in Lizenzanträgen. Gleichzeitig verbietet das REACH-Programm der Europäischen Chemikalienagentur die Verwendung von Triton X-100 in der Produktion aus Umweltgründen und verpflichtet Unternehmen dazu, Detergenz-Schritte mit umweltfreundlicheren Optionen erneut zu validieren. Chinas Nationale Behörde für Medizinprodukte spiegelt westliche Anforderungen wider und zwingt inländische CDMOs dazu, virale Clearance-Labore zu überholen, um global wettbewerbsfähig zu bleiben. Harmonisierungsbemühungen in ICH-Regionen sind langfristig vorteilhaft, erhöhen jedoch vorübergehend die Entwicklungskomplexität und verlängern die Vorbereitungszeiten für Dossiers. Anbieter, die bewährte Inaktivierungspakete liefern können, die über Jurisdiktionen hinweg konform sind, erlangen einen entscheidenden Vorteil.
Wechsel zu Einweg-Bioprozessierungsplattformen
Einweg-Baugruppen haben die frühe Adoption weit überschritten und verankern nun die meisten neuen Säugetieranlagen, was virale Sicherheitsstrategien direkt verändert. Einweg-Reaktoren und nachgelagerte Module verringern das Kontaminationsrisiko, da sie vorsterilisiert ankommen und die Geräteumrüstung eliminieren. Virale Inaktivierungstanks, die auf Einweg-Chargen dimensioniert sind, verkürzen Haltezeiten und beschleunigen Umstellungen, wodurch die Anlagenauslastung gesteigert wird. Kleinere Biotech-Unternehmen profitieren am meisten und vermeiden Investitionen von 50 Millionen USD in Edelstahl bei gleichzeitiger Einhaltung regulatorischer Vorschriften. Der Trend befeuert auch die Nachfrage nach gebrauchsfertigen Inaktivierungspuffern, geschlossenen Heizsystemen und gammastabilen Kunststoffschläuchen und eröffnet neue Einnahmequellen für Komponentenhersteller.
Hemmnisse-Auswirkungsanalyse
| Hemmnisse-Auswirkungsanalyse | (~) % Auswirkung auf CAGR-Prognose | Geografische Relevanz | Auswirkungszeitrahmen |
|---|---|---|---|
| Hohe Investitionsausgaben für fortgeschrittene Inaktivierungsinfrastruktur | -0.8% | Global (kleine & mittelgroße Hersteller am meisten betroffen) | Langfristig (≥ 4 Jahre) |
| Komplexe und langwierige Validierungs- & regulatorische Genehmigungszyklen | -1.1% | Global (jurisdiktionelle Variation) | Mittelfristig (2-4 Jahre) |
| Lieferketten-Volatilität von GMP-gerechten Detergenzien und Filtern | -0.7% | Global (verstärkt in EU & Asien) | Kurzfristig (≤ 2 Jahre) |
| Technische Herausforderungen bei kontinuierlicher Inline-virale Inaktivierung-Einrichtung | -0.9% | Nordamerika & Europa Early Adopters | Mittelfristig (2-4 Jahre) |
| Quelle: Mordor Intelligence | |||
Hohe Investitionsausgaben für fortgeschrittene Inaktivierungsinfrastruktur
Vollständige virale Sicherheitssuiten mit BSL-2-Laboren, Wärmehaltungstanks, Nanofiltrations-Skids und orthogonalen Testinstrumenten können 50 Millionen USD überschreiten, was die Bau-oder-Kauf-Entscheidung für kleine Unternehmen unter intensive Prüfung stellt. Kapitalschwache Sponsoren schieben Investitionen oft auf, aber späte Nachrüstungen riskieren Markteinführungsverzögerungen, wenn Clearance-Studien die regulatorischen Akzeptanzkriterien nicht erfüllen. Selbst nach dem Gerätekauf bleiben laufende Kalibrierung, Biosicherheitszertifizierung und Kosten für qualifiziertes Personal hoch. Die Belastung verbreitert die Fähigkeitslücke zwischen großen integrierten Biopharma-Gruppen und aufkommenden Unternehmen und beschleunigt Outsourcing und Marktkonsolidierung.
Komplexe und langwierige Validierungs- und regulatorische Genehmigungszyklen
Eine einzige virale Clearance-Studie kann 18 Monate dauern und erfordert mehrere Modellviren, Worst-Case-Prozessparameter und erschöpfenden statistischen Beweis, dass die kumulative Reduktion Clearance-Ziele erfüllt. Zusätzlich zu analytischen Testvorlaufzeiten, Dossier-Überprüfung und möglichen Behördenfragen kann der Zeitplan die kommerzielle Markteinführung weit über ursprüngliche Projektionen hinaus verzögern. Begrenzte globale Vertragskapazität für Kategorie-C-Viren bedeutet, dass Sponsoren oft für Laborplätze anstehen und Zeitpläne weiter verlängern. Diese Verzögerungen tragen greifbare Nettobarwert-Strafen für Vermögenswerte-Eigentümer und können Investitionen in marginale therapeutische Kandidaten abschrecken.
Segment-Analyse
Nach Methode: Wärmebehandlung gewinnt an Dynamik trotz Lösungsmittel-Detergenz-Dominanz
Lösungsmittel-Detergenz-Verfahren sicherten sich 46,43% des Umsatzes im Jahr 2024 und bestätigten ihre Rolle als Standard-Ansatz für lipid-umhüllte virale Clearance in plasmaabgeleiteten und rekombinanten Proteinprodukten[2]Canadian Blood Services, "Solvent-Detergent Inactivation in Plasma Processing," blood.ca. Ihr validiertes Leistungsprofil erhält die Adoption aufrecht, insbesondere wo Legacy-Prozesse minimalen Änderungen gegenüberstehen. Pasteurisierung und verwandte Wärmemodalitäten schreiten jedoch mit einer CAGR von 8,65% voran, da Nachhaltigkeitsimperative die Prozessauswahl umgestalten. Dieses Wachstum hebt die virale Inaktivierung Marktgröße für wärmebasierte Geräteanbieter an, unterstützt durch verbesserte Formulierungen, die labile Proteine während 60°C-Haltungen schützen. Paralleles Interesse an niedrig-pH- und Caprylat-Methoden bleibt für monoklonale Antikörper bestehen, wo sanfte Bedingungen die Fc-Funktionalität schützen.
Das europäische Verbot von Triton X-100 beschleunigt die Aufnahme von Alternativen wie Virodex™-Detergenzien und Deviron®-Reagenzien, dennoch bleibt Wärme der regulationsagnostischste Weg. Hersteller wenden hybride Strategien an, die einen Detergenz-Schritt mit terminaler Pasteurisierung kombinieren, um orthogonale Log-Reduktionskredite zu sichern. Forschungsbemühungen zur Erkundung von Hochdruckbehandlung für virale Impfstoffe deuten auf längerfristige Methodendiversifizierungsmöglichkeiten hin, die den virale Inaktivierung Markt erweitern könnten, vorausgesetzt Skalierbarkeits-Hindernisse werden angegangen[3]Nature Research, "High Hydrostatic Pressure as a Viral Inactivation Tool," nature.com.
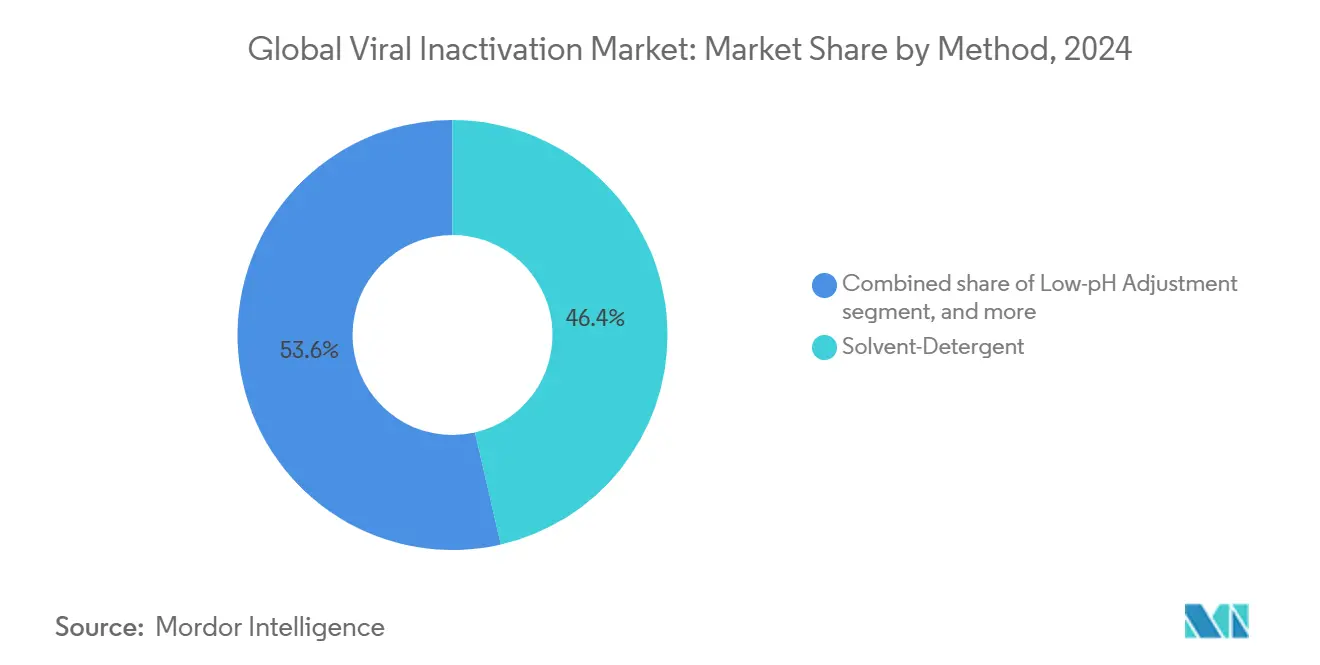
Notiz: Segmentanteile aller einzelnen Segmente verfügbar bei Berichtkauf
Nach Produkt: Servicesegment beschleunigt sich, da Validierungskomplexität zunimmt
Kits und Reagenzien lieferten 41,45% Umsatz im Jahr 2024, was die Grundnachfrage nach Verbrauchsmaterialien in jedem lizenzierten Bioprozess widerspiegelt. Konzentrierte Formulierungen und Einweg-Konditionierungsbeutel erhalten das Volumen trotz Detergenz-Neuformulierungsmandaten aufrecht. Validierungs- und Testdienste hingegen sollen jährlich um 8,93% wachsen und die virale Inaktivierung Marktgröße für externe Labore anheben, die End-to-End-Clearance-Pakete anbieten. Ihre Attraktivität steigt, da regulatorische Leitlinien Datenerwartungen intensivieren und da interne BSL-2-Kapazität knapp bleibt.
Führende Anbieter liefern modulare Studiendesigns, prädiktive virale Reduktionsmodellierung und GMP-konforme Berichtsvorlagen und eliminieren Monate aus Projektzeitleisten. Die Nachfrage nach virus Inaktivierungssystemen - geschlossene Heizgeräte, Nanofilter und skid-montierte Niedrig-pH-Reaktoren - expandiert auch im Einklang mit der Einweg-Bewegung, aber Services erfassen überproportionales Wachstum, da sie technische Expertise einbetten, die schwer in silico oder vor Ort zu replizieren ist.
Nach Anwendung: Zell- und Gentherapie treibt Nachfrage der nächsten Generation
Impfstoffe und Therapeutika umfassten 49,54% des Verbrauchs 2024 nach Wert und profitierten von hochvolumigen Influenza- und COVID-19-Kampagnen, die integrierte Lösungsmittel-Detergenz- oder Niedrig-pH-Haltungen in standardmäßigen Produktionsskripten einsetzen. Diese ausgereiften Produkte stützen weiterhin den virale Inaktivierung Markt, doch ihre CAGR bleibt hinter CGT zurück, da sie auf optimierten Linien mit wenig Raum für Margenerweiterung stehen. Zell- und Gentherapie-Modalitäten werden voraussichtlich mit einer CAGR von 8,88% skalieren und machen sie zum einzelnen am schnellsten wachsenden Nachfragetreiber innerhalb der virale Inaktivierung Industrie.
Vektorreiche Ernten fordern Betreiber heraus, Replikationskompetenz unter Detektionsgrenzen zu halten, während therapeutische Potenz geschützt wird. Lösungen kombinieren oft Tiefenfiltration, DNAse-Behandlung und gezielte Niedrig-pH-Inkubation neben Größenausschluss-Nanofiltration. Serviceunternehmen, die maßgeschneiderte CGT-Clearance-Protokolle anbieten, erfassen daher Premium-Verträge, während Gerätehersteller Hochdurchsatz-Systeme entwickeln, die kleine, Multiprodukt-CGT-Chargen effizient verarbeiten können.
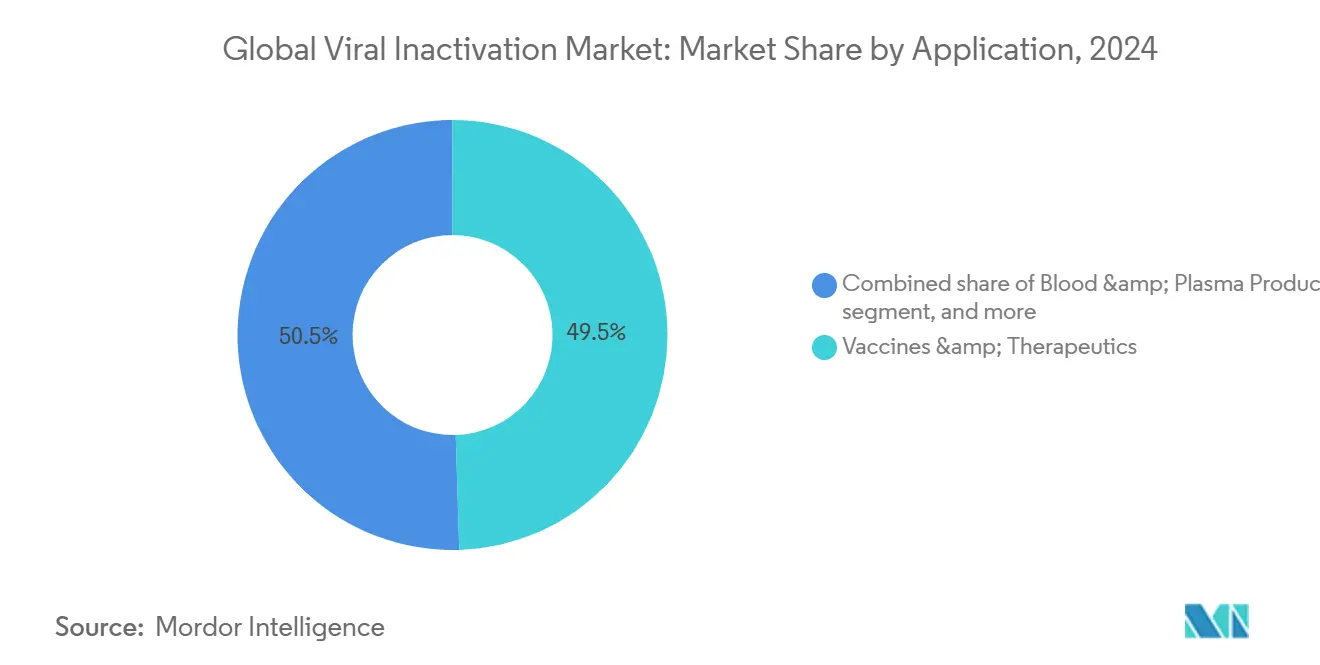
Notiz: Segmentanteile aller einzelnen Segmente verfügbar bei Berichtkauf
Nach Endverbraucher: CDMOs profitieren von Outsourcing-Trends
Biopharma- und Biotech-Unternehmen blieben 2024 die vorherrschende Kundschaft und absorbierten 53,45% der Gesamtausgaben, da sie die ultimative regulatorische Verantwortung für Produktsicherheit behalten. Ihr interner Kapazitätsfokus ruht auf Flaggschiff-Assets und lässt Raum für Drittanbieter-Kooperatoren, Überlauf und spezialisierte Assays zu verwalten. CDMOs zeigen eine prognostizierte CAGR von 9,76%, die höchste unter Endverbrauchern, angeheizt durch westliche Sponsoren, die Operationen zu indischen und singapurischen Anlagen verlagern, um geopolitische Risiken im Zusammenhang mit China-zentrischen Lieferketten zu mildern.
Napier-große CGT-CDMOs werben um Risikokapitalfinanzierung, um zweckgebaute Suiten zu errichten, die integrierte Vektorproduktion, Inaktivierung und Clearance-Tests in einem Campus beherbergen. Ihre Expansion erhöht Barrieren für kleine, eigenständige Testlabore, während sie Marktmacht bei Multi-Service-Vertragspartnern konsolidiert. CROs erhalten eine stabile Nische zur Unterstützung präklinischer Proof-of-Concept-Chargen, obwohl sie zunehmend mit CDMOs kooperieren, um einheitliche Angebote für Kunden zu präsentieren.
Geographie-Analyse
Nordamerika bewahrte 42,12% Umsatzanteil im Jahr 2024 und verankert weiterhin den virale Inaktivierung Markt durch fortgeschrittene CGT-Cluster in Massachusetts, North Carolina und Kalifornien. FDA-Durchsetzung, exemplarisch durch Q5A(R2), treibt die rasche Adoption orthogonaler Inaktivierung und Inline-Nanofiltration an und erhält Premium-Nachfrage nach hochspezifizierten Verbrauchsmaterialien aufrecht. Strategische Kapitalprojekte wie Novo Nordisks 4,1 Milliarden USD Füll-Finish-Expansion in Clayton, North Carolina, betten großangelegte virale Sicherheitssuiten ein, die mehrjährige Verbrauchsmaterial-Ausgaben sichern. Thermo Fisher Scientifics 4,1 Milliarden USD Kauf von Solventums Purification & Filtration-Portfolio im Februar 2025 konzentriert Fähigkeiten in der Region weiter und erweitert integrierte Clearance-Lösungen.
Asien-Pazifik verzeichnet die steilste Trajektorie mit einer CAGR von 7,45% bis 2030, unterstützt durch lokale politische Anreize, die Biologika-Selbstversorgung beschleunigen. Indiens CDMO-Markt, bewertet mit 15,63 Milliarden USD im Jahr 2023 und auf dem Weg zu 26,73 Milliarden USD bis 2028, befeuert einen raschen Anstieg in BSL-2-Laborbau und integrierten viralen Clearance-Services. Unterdessen erschwert Chinas Anti-Spionage-Gesetz, wirksam seit Juli 2023, ausländische GMP-Inspektionen und drängt westliche Käufer zur Diversifizierung der Lieferketten, doch die inländische Nachfrage nach viralen Clearance-Technologien bleibt robust inmitten des Fünfjahres-Biotech-Plans des Landes. Japanische Regulierungsbehördens frühe Befürwortung von Triton-X-Alternativen beschleunigt wärmebasierte Prozessvalidierung in lokalen Plasmaanlagen und hebt vielfältige regionale Technologiepräferenzen hervor.
Europa liefert bescheidene aber stetige Expansion, da die REACH-Richtlinie Detergenz-Neuformulierungsprojekte anregt, die sich direkt in virale Inaktivierung Marktnachfrage für Validierungsstudien übersetzen. Unternehmen wie Croda und Asahi Kasei führen die Antwort mit der Einführung konformer Tenside und ultraschneller Planova FG1-Filter an, die für hochvolumige monoklonale Antikörper-Anlagen entwickelt wurden. Staatlich geförderte Innovationszuschüsse in Deutschland und Frankreich ermutigen lokale KMUs zur Erprobung kontinuierlicher viraler Inaktivierungsreaktoren, obwohl Kapitalintensität das Skalierungs-Tempo relativ zu nordamerikanischen Initiativen begrenzt.
Wettbewerbslandschaft
Der virale Inaktivierung Markt ist mäßig konzentriert, wobei geschätzt wird, dass die fünf größten Anbieter 55-60% kombinierten Umsatz halten. Danahers Integration von Cytiva und Pall im Jahr 2024 schuf eine 7,5 Milliarden USD Bioprozessierungs-Division, die Filtration, Chromatographie und Einweg-Baugruppen anbietet, die gemeinsam jeden viralen Clearance-Checkpoint adressieren. Thermo Fishers jüngste Filtrations-Akquisition vergrößert seinen Katalog wärmestabiler Beutel, Tiefenfilter und Detergenz-Mischungen und positioniert es als Ein-Stopp-virale Sicherheitspartner für aufkommende CGT-Hersteller. Sartorius ergänzt Upstream-Bioreaktoren mit Downstream-Nanofiltrations-Modulen und statistischer Clearance-Software und unterstreicht den Trend zu Plattform-Ökosystemen.
Serviceanbieter zielen auf höhermargige Nischen ab. Charles River Laboratories stärkte seinen viralen Vektor-Footprint durch den 292,5 Millionen USD Kauf von Vigene Biosciences im Jahr 2024 und ermöglichte integrierte GMP-Produktion, Inaktivierung und Potenztests unter einem Qualitätssystem. Merck KGaAs 600 Millionen USD Akquisition von Mirus Bio im selben Jahr lieferte patentierte Transfektions-Reagenzien, die Vektortiter steigern und indirekt nachfolgende Inaktivierungsarbeitslasten erhöhen. Lonza setzt organische Ausbauten fort, verweist auf mehr als 70 virale Vektor-Entwicklungsprojekte seit 2023 und investiert in schnellzyklische Niedrig-pH-Skids, um sich durch Clearance-Durchsatz zu differenzieren.
Technologischer Wettbewerb konzentriert sich auf Nachhaltigkeit und Prozessökonomie. Crodas Virodex-Detergenzien und Asahi Kaseis Planova FG1-Filter unterstreichen die Wende zu umweltfreundlicheren, schnelleren Alternativen, die Pufferverbrauch und Zykluszeiten reduzieren. Aufkommende Akteure verfolgen Hochdruckbehandlungs-, photochemische und enzymatische Lösungen für fragile CGT-Ladungen, doch breite Adoption wartet auf Kostennachweise im kommerziellen Maßstab. Organisationen, die Geräte, Reagenzien, Software und Services in einem einzigen Vertrag bündeln können, sichern sich zunehmend bevorzugten Anbieterstatus während Anlagendesign-Reviews und verschärfen Barrieren für Nischen-Newcomer.
Globale Virale Inaktivierung Industrieführer
-
Merck KGaA
-
Sartorius AG
-
Texcell SA
-
Cytiva (Danaher Corporation)
-
Parker Hannifin Corp
- *Haftungsausschluss: Hauptakteure in keiner bestimmten Reihenfolge sortiert
Jüngste Branchenentwicklungen
- Februar 2025: Thermo Fisher Scientific erwarb Solventums Purification & Filtration-Geschäft für rund 4,1 Milliarden USD und erweiterte seine Bioproduktions- und virale Clearance-Fähigkeiten.
- Januar 2025: Croda führte die Virodex™-Reihe ein und bot Triton X-100-freie Tenside, die EU-REACH-Konformität für virale Inaktivierung Workflows erfüllen.
- August 2024: ViroCell Biologics schloss eine überzeichnete Wandelanleihe ab, um GMP-virale Vektorproduktion nach UK MHRA-Lizenzierung zu skalieren.
- Juli 2024: Avantor veröffentlichte J.T.Baker® Cell Lysis Solution und Endonuclease zur Verbesserung der AAV-Ernteffizienz mit geringerer Umweltauswirkung.
- Mai 2024: Merck KGaA schloss seine 600 Millionen USD Akquisition von Mirus Bio ab und stärkte virale Vektor-Herstellungstechnologien.
Globaler Virale Inaktivierung Marktbericht-Umfang
Gemäß dem Umfang des Berichts ist virale Inaktivierung eine Methode der viralen Verarbeitung, bei der das Endprodukt die Viren in inaktiver Form enthalten kann. Der Virus-Inaktivierungsprozess ist ein kritischer Schritt in der Prozessentwicklung für Biologika wie Gewebe- und Gewebeprodukte, Stammzellprodukte sowie Impfstoffe und Therapeutika. Der virale Inaktivierung Markt ist segmentiert nach Methode (Lösungsmittel-Detergenz-Methode, pH-Anpassungsmethode, Pasteurisierung und andere), Produkt (virale Inaktivierungssysteme und Zubehör, Kits und Reagenzien und andere), Anwendung (Impfstoffe und Therapeutika, Blut & Blutprodukte, Zell- & Gentherapieprodukte und andere), Endverbraucher (Pharma- und Biotechnologie-Unternehmen, Auftragsforschungsorganisationen und andere) und Geographie (Nordamerika, Europa, Asien-Pazifik, Naher Osten und Afrika sowie Südamerika). Der Marktbericht deckt auch die geschätzten Marktgrößen und Trends für 17 verschiedene Länder in den wichtigsten Regionen weltweit ab. Der Bericht bietet die Werte (USD Millionen) für die oben genannten Segmente.
| Lösungsmittel-Detergenz |
| Niedrig-pH-Anpassung |
| Pasteurisierung / Wärme |
| Andere Methoden |
| Virale Inaktivierungssysteme und Zubehör |
| Kits & Reagenzien |
| Validierungs- & Testdienste |
| Andere Produkte |
| Impfstoffe & Therapeutika |
| Blut- & Plasma-Produkte |
| Zell- & Gen-Therapieprodukte |
| Andere Anwendungen |
| Biopharma & Biotechnologie-Unternehmen |
| Auftragsforschungs- & Herstellungsorganisationen (CDMOs) |
| Auftragsforschungsorganisationen (CROs) |
| Andere Endverbraucher |
| Nordamerika | Vereinigte Staaten |
| Kanada | |
| Mexiko | |
| Europa | Deutschland |
| Vereinigtes Königreich | |
| Frankreich | |
| Italien | |
| Spanien | |
| Rest von Europa | |
| Asien-Pazifik | China |
| Japan | |
| Indien | |
| Australien | |
| Südkorea | |
| Rest von Asien-Pazifik | |
| Naher Osten & Afrika | GCC |
| Südafrika | |
| Rest von Naher Osten & Afrika | |
| Südamerika | Brasilien |
| Argentinien | |
| Rest von Südamerika |
| Nach Methode | Lösungsmittel-Detergenz | |
| Niedrig-pH-Anpassung | ||
| Pasteurisierung / Wärme | ||
| Andere Methoden | ||
| Nach Produkt | Virale Inaktivierungssysteme und Zubehör | |
| Kits & Reagenzien | ||
| Validierungs- & Testdienste | ||
| Andere Produkte | ||
| Nach Anwendung | Impfstoffe & Therapeutika | |
| Blut- & Plasma-Produkte | ||
| Zell- & Gen-Therapieprodukte | ||
| Andere Anwendungen | ||
| Nach Endverbraucher | Biopharma & Biotechnologie-Unternehmen | |
| Auftragsforschungs- & Herstellungsorganisationen (CDMOs) | ||
| Auftragsforschungsorganisationen (CROs) | ||
| Andere Endverbraucher | ||
| Geographie | Nordamerika | Vereinigte Staaten |
| Kanada | ||
| Mexiko | ||
| Europa | Deutschland | |
| Vereinigtes Königreich | ||
| Frankreich | ||
| Italien | ||
| Spanien | ||
| Rest von Europa | ||
| Asien-Pazifik | China | |
| Japan | ||
| Indien | ||
| Australien | ||
| Südkorea | ||
| Rest von Asien-Pazifik | ||
| Naher Osten & Afrika | GCC | |
| Südafrika | ||
| Rest von Naher Osten & Afrika | ||
| Südamerika | Brasilien | |
| Argentinien | ||
| Rest von Südamerika | ||
Schlüsselfragen beantwortet im Bericht
Was ist der prognostizierte Wert des virale Inaktivierung Marktes bis 2030?
Der Markt wird voraussichtlich bis 2030 10 Milliarden USD erreichen und mit einer CAGR von 6,12% expandieren.
Welche virale Inaktivierung Methode wächst am schnellsten?
Pasteurisierung und andere wärmebasierte Ansätze zeigen das höchste Wachstum mit einer erwarteten CAGR von 8,65% bis 2030.
Warum ist Asien-Pazifik die am schnellsten wachsende Region?
Expandierende CDMO-Infrastruktur, unterstützende Regierungspolitiken und Lieferketten-Diversifizierung von China nach Indien treiben eine regionale CAGR von 7,45%.
Wie beeinflusst das Auslaufen von Triton X-100 die Hersteller?
Unternehmen müssen Prozesse mit neuen Detergenzien wie Virodex™ neu validieren oder zu Wärmemethoden wechseln, was die Nachfrage nach Validierungsdiensten erhöht.
Welches Endverbraucher-Segment wird am schnellsten wachsen?
CDMOs führen mit einer CAGR von 9,76%, da Biopharma-Sponsoren komplexe virale Clearance-Arbeiten an spezialisierte Anbieter auslagern.
Welcher Score beschreibt die Marktkonzentration und warum?
Ein Score von 6 spiegelt mäßige Konzentration wider; die fünf größten Unternehmen halten nahezu 60% Umsatz, während zahlreiche Spezial- und regionale Unternehmen wettbewerbsfähig bleiben.
Seite zuletzt aktualisiert am:



