Marktgröße und Marktanteil für Mycoplasma-Tests
Mycoplasma-Tests Marktanalyse von Mordor Intelligence
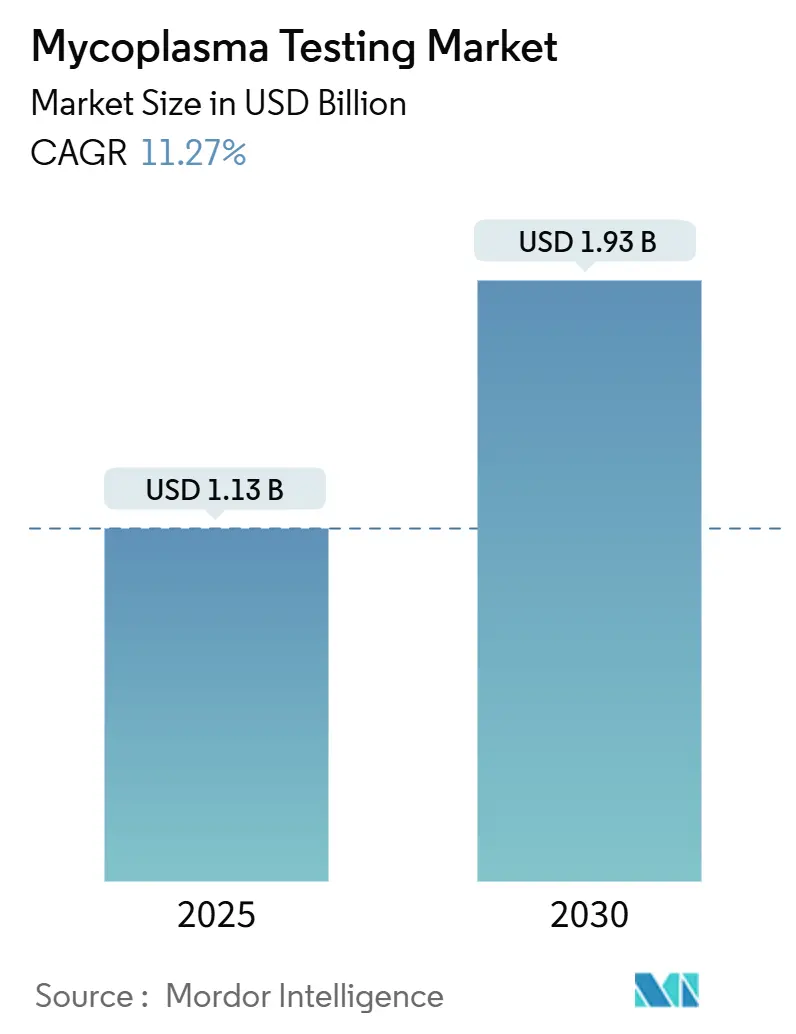
Die Marktgröße für Mycoplasma-Tests wird auf USD 1,13 Milliarden im Jahr 2025 geschätzt und soll USD 1,93 Milliarden bis 2030 erreichen, bei einer CAGR von 11,27% während des Prognosezeitraums (2025-2030).
Verschärfte regulatorische Kontrolle der Biologika-Herstellung, expandierende Zell- und Gentherapie-Produktion sowie wachsende Präferenz für schnelle Nukleinsäure-Methoden untermauern diese Entwicklung. Aufsichtsbehörden, angeführt von der FDA und EMA, verlangen validierte Mycoplasma-Erkennung an mehreren Punkten im Produktlebenszyklus und machen Compliance zu einer nicht-diskretionären Ausgabe für Biohersteller fda.gov. Digitale PCR und automatisierte Sample-to-Answer-Plattformen beschleunigen Chargenfreigabe-Zeitpläne, während der Outsourcing-Trend Testarbeitslasten auf Auftragsorganisationen überträgt, die Kapazitäten schnell skalieren können. Regionale Fertigungserweiterungen in China, Indien und Singapur kombiniert mit Steueranreizen fördern Laborausbau, jedoch dämpfen Mangel an qualifiziertem molekularem QA-Personal und hohe Automatisierungskosten die Adoptionsraten in kleineren Einrichtungen. Wettbewerbsdynamiken begünstigen Anbieter, die Instrumente, Kits und Dienstleistungen bündeln können, was Cross-Selling-Potenzial steigert und Kundenbeziehungen konsolidiert.
Wichtige Berichtsergebnisse
- Nach Produkt und Dienstleistung hielten Kits und Reagenzien einen Umsatzanteil von 46,17% im Jahr 2024, während Dienstleistungen voraussichtlich mit einer CAGR von 14,68% bis 2030 expandieren werden.
- Nach Technologie führte qPCR mit 64,39% des Mycoplasma-Tests Marktanteils im Jahr 2024, während digitale PCR voraussichtlich mit 16,26% bis 2030 wachsen wird.
- Nach Anwendung machte Zelllinie-Qualitätskontrolle 41,62% der Mycoplasma-Tests Marktgröße im Jahr 2024 aus; Gen- und Zelltherapie-Herstellung wird zwischen 2025 und 2030 mit einer CAGR von 17,82% steigen.
- Nach Endnutzer machten Biopharma- und Biotechnologieunternehmen 65,29% der Mycoplasma-Tests Marktgröße im Jahr 2024 aus; Auftragsherstellungsorganisationen verzeichneten das schnellste Wachstum und entwickelten sich mit einer CAGR von 15,45% bis 2030.
- Nach Geographie kommandierte Nordamerika 40,81% Anteil des Mycoplasma-Tests Marktes im Jahr 2024, jedoch entwickelt sich Asien-Pazifik mit einer CAGR von 18,62% bis 2030.
Globale Mycoplasma-Tests Markttrends und Erkenntnisse
Treiber-Impact-Analyse
| Treiber | (~) % Impact auf CAGR Prognose | Geografische Relevanz | Impact Zeitrahmen |
|---|---|---|---|
| Expansion von Biopharma- und Zell- & Gentherapie-Einrichtungen | +2.8% | Global, konzentriert in Nordamerika & EU | Mittelfristig (2-4 Jahre) |
| Regulatorische Mandate erfordern Mycoplasma-Freigabetests | +2.1% | Global, angeführt von FDA/EMA-Jurisdiktionen | Kurzfristig (≤ 2 Jahre) |
| Zunehmende Vorfälle von Zellkultur-Kontamination | +1.9% | Global, Hochvolumen-Fertigungszentren | Kurzfristig (≤ 2 Jahre) |
| Steigende Nachfrage nach schnellen, hochsensitiven PCR-Assays | +1.7% | Nordamerika & EU, Expansion nach APAC | Mittelfristig (2-4 Jahre) |
| Dezentrale QC-Labore in aufstrebenden Biotech-Zentren | +1.2% | APAC-Kern, Spillover nach MEA | Langfristig (≥ 4 Jahre) |
| VC-unterstütztes Wachstum von Synthetic Biology Start-ups | +0.9% | Nordamerika & EU, aufkommend in APAC | Langfristig (≥ 4 Jahre) |
| Quelle: Mordor Intelligence | |||
Expansion von Biopharma- und Zell- & Gentherapie-Herstellungseinrichtungen
Kapazitätssteigerungen in autologen und allogenen Therapieanlagen haben Probenvolumina vervielfacht, die 100% Chargenprüfung erfordern. Kontaminationsprävalenz in Zellkulturen liegt zwischen 15% und 35%, und FDA-Leitlinien schreiben nun Mycoplasma-Tests nach dem Pooling und vor dem Waschen vor, wodurch die Probenahmefrequenz erhöht wird.[1]American Type Culture Collection, "Cell Culture Contamination Studies," atcc.org Kontinuierliche Perfusions-Bioreaktoren erhöhen Echtzeit-Überwachungsanforderungen und treiben die Nachfrage nach automatisierten Analysegeräten voran, die höhere Durchsätze mit minimaler menschlicher Intervention bewältigen. Einrichtungsausbauten in Schwellenmärkten müssen Qualifikationsstudien abschließen, wodurch Greenfield-Nachfrage für Drittanbieter-Testdienste entsteht. Zusammen fügen diese Trends 2,8 Prozentpunkte zur Prognose-CAGR hinzu.
Regulatorische Mandate erfordern Mycoplasma-Freigabetests für Biologika
Die FDA-Regel für laborentwickelte Tests und EMA-Leitlinien für fortgeschrittene Therapie-Medizinprodukte erfordern validierte Assays von einer Master-Zellbank bis zu einem fertigen Medikament.[2]Federal Register Editorial Team, "Laboratory Developed Tests; Final Rule," federalregister.gov Die Leitlinien der Europäischen Arzneimittel-Agentur für Arzneimittel für neuartige Therapien schreiben umfassende Mycoplasma-Tests während des gesamten Herstellungsprozesses vor, von Master-Zellbanken bis zur endgültigen Produktfreigabe. Diese regulatorischen Änderungen schaffen nicht-diskretionäre Nachfrage nach Testdienstleistungen, da Hersteller keine Produkte freigeben können, ohne Mycoplasma-Abwesenheit durch validierte Methoden zu demonstrieren. Compliance-Ausgaben beschleunigen sich bis 2027, da stufenweise LDT-Aufsicht in Kraft tritt. Die stufenweise Implementierung neuer LDT-Regulierungen über vier Jahre schafft vorhersagbares Nachfragewachstum, da Labore ihre Testkapazitäten upgraden, um Compliance aufrechtzuerhalten.
Zunehmende Vorfälle von Zellkultur-Kontamination
Branchenfallstudien dokumentieren Filtrations-Bypass, DNA-Persistenz und Ladungsvarianten-Verschiebungen in monoklonalen Antikörpern nach unentdeckter Kontamination.[3]Wiley Editors, "Charge Variants in Contaminated mAbs," onlinelibrary.wiley.com Wirtschaftliche Folgen umfassen Chargenvernichtung, Anlagenstilllegungen und regulatorische Inspektionen, was proaktive Screening-Richtlinien veranlasst. Hochdichte Kulturen und längere Verweilzeiten in intensivierten Prozessen erhöhen das Risiko weiter und führen zu häufigeren Zwischentests.
Steigende Nachfrage nach schnellen, hochsensitiven PCR-basierten Assays
Digitale PCR erkennt ≤10 CFU/mL ohne Referenzkurven und bietet absolute Quantifizierung, die Freigabetest-Präzisionsanforderungen erfüllt. Plattformen wie das BIOFIRE Mycoplasma-System berichten Ergebnisse in 60 Minuten und verkürzen Chargenfreigabezyklen. KI-gesteuerte Analytik rationalisiert die Interpretation und reduziert Falschpositive. Regulatorische Zustimmungen, z.B. Health Canadas Freigabe von Roche MycoTOOL, validieren diese Technologien für kommerzielle Adoption.
Einschränkungen Impact-Analyse
| Einschränkung | (~) % Impact auf CAGR Prognose | Geografische Relevanz | Impact Zeitrahmen |
|---|---|---|---|
| Hohe Kapitalausgaben für automatisierte Systeme | -1.8% | Global, kleinere Labore betroffen | Kurzfristig (≤ 2 Jahre) |
| Falsch-positive/-negative Nachtest-Verzögerungen | -1.4% | Global, Hochvolumen-Standorte | Mittelfristig (2-4 Jahre) |
| Mangel an qualifizierten molekularen QA-Arbeitskräften | -1.1% | Nordamerika & EU, steigend in APAC | Langfristig (≥ 4 Jahre) |
| Regulatorische Verzögerung bei mikrofluidischen und Next-Gen-Assays | -0.8% | Global, jurisdiktionsspezifisch | Mittelfristig (2-4 Jahre) |
| Quelle: Mordor Intelligence | |||
Hohe Kapitalausgaben für die Implementierung automatisierter Erkennungssysteme
Einstiegs-automatisierte Analysegeräte kosten USD 100.000-500.000, mit jährlichen Serviceverträgen von über USD 50.000. Kleinere CTLs und akademische Labore haben Schwierigkeiten, solche Ausgaben zu rechtfertigen, was die Abhängigkeit von manuellen Kulturmethoden verlängert. FDA LDT-Compliance fügt Validierungskosten hinzu und belastet Kapitalbudgets, wodurch die kurzfristige Aufnahme gebremst wird. Kleinere Auftrags-Testlabore stehen vor besonderen Herausforderungen bei der Rechtfertigung von Automatisierungsinvestitionen angesichts ihrer begrenzten Probenvolumina und vielfältigen Testanforderungen. Die Komplexität der Validierung automatisierter Systeme für regulatorische Compliance fügt erhebliche Zeit- und Kostenbelastungen hinzu, wobei Validierungsstudien typischerweise 6-12 Monate und spezialisierte Expertise erfordern.
Falsch-Positive/-Negative Nachtest-Verzögerungen
DNA-Verschleppung und Kreuzkontamination lösen Bestätigungs-Workflows aus, die den Geschwindigkeitsvorteil der PCR untergraben, während falsch-negative Ergebnisse die Patientensicherheit bedrohen und regulatorische Kontrolle einladen. Diskordante Ergebnisse zwischen Kultur- und molekularen Assays verlängern Freigabezeitpläne um Wochen, besonders wenn Untersuchungsprotokolle keine Standardisierung aufweisen. Anforderungen von Aufsichtsbehörden für die Untersuchung atypischer Ergebnisse können Produktfreigaben um Wochen oder Monate verzögern, besonders wenn mehrere Testmethoden widersprüchliche Ergebnisse liefern. Der Übergang der Branche von kulturbasierten zu molekularen Methoden führt neue Variabilitätsquellen ein, die umfangreiche Methodenvalidierung und Vergleichsstudien erfordern, um Vertrauen in die Ergebnisse zu etablieren.
Segmentanalyse
Nach Produkt & Service: Ausgelagerte Dienstleistungen gewinnen an Schwung
Kits und Reagenzien behielten einen Anteil von 46,17% im Jahr 2024 und unterstreichen ihre Verbrauchsnatur innerhalb des Mycoplasma-Tests Marktes. Das Services-Segment wird mit 14,68% CAGR expandieren, da Biohersteller Methodenvalidierung und Routine-Screening an akkreditierte Labore delegieren. Hohe regulatorische Hürden und sich entwickelnde Assay-Formate ermutigen Unternehmen, Expertenkapazität zu kaufen, anstatt sie aufzubauen. Eurofins' Netzwerk von 45+ globalen Standorten illustriert, wie Skalierung Kosteneffizienz produziert, die einzelne Firmen nicht replizieren können.
Automatisierungsbereite Instrumente zeigen stetiges aber langsameres Wachstum, da Käufer sie oft an langfristige Reagenzienverträge binden. Die BIOFIRE-Plattform und Rapid Micro Biosystems' Fläschchen-Reader sprechen an, indem sie Geschwindigkeit mit Pharmakopöe-Compliance verbinden. Während Dienstleistungen wachsen, richten sich Kit-Anbieter an Drittanbieter-Labore unter Reagenzien-Mietmodellen aus, die Versorgungserlöse sichern. Diese Synergie konsolidiert Käufer-Lieferanten-Abhängigkeiten und treibt Volumen in beiden Kategorien.
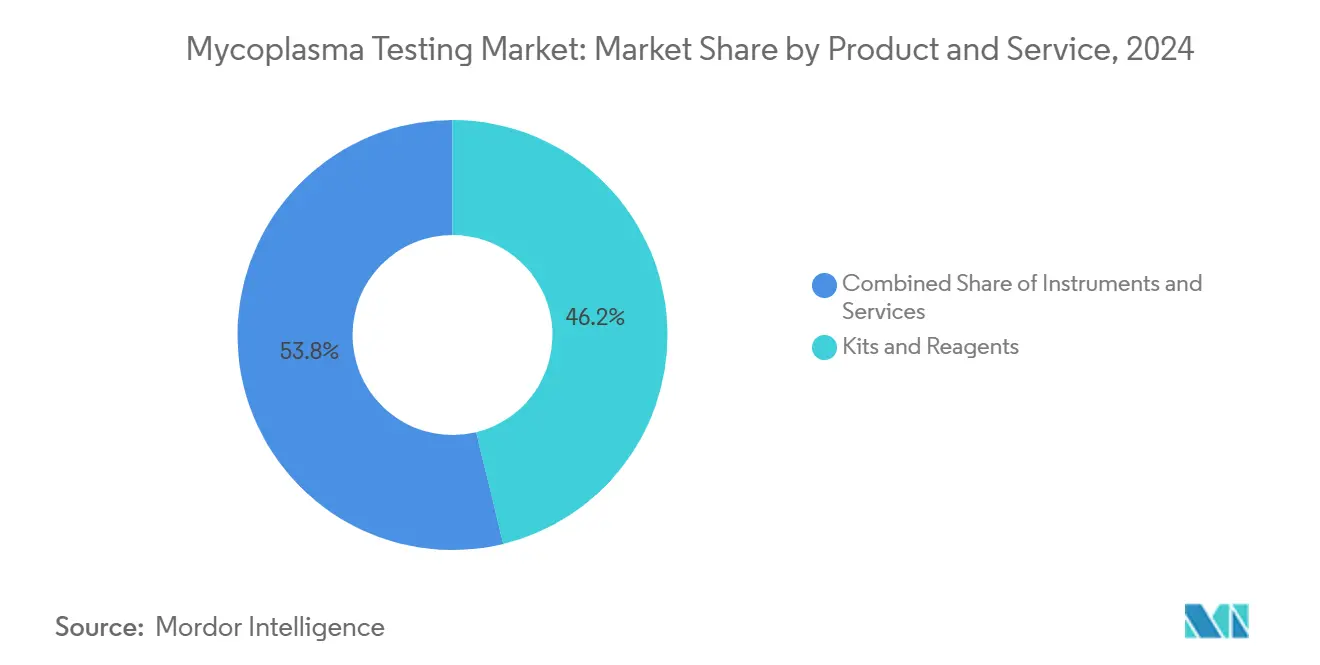
Notiz: Segmentanteile aller einzelnen Segmente verfügbar beim Berichtskauf
Nach Technologie: Digitale PCR stört etablierte Workflows
qPCR hält 64,39% des Mycoplasma-Tests Marktanteils 2024 dank etablierter Protokolle und breiter Instrumentenverfügbarkeit. Digitale PCR, mit einer Wachstumsrate von 16,26%, mildert Standardkurven-Fehler und erkennt seltene Ereignisse, die für Gentherapie-Chargen vital sind. Sensitivitätsgewinne resonieren mit regulatorischen Prüfern, die robuste Quantifizierung suchen. Konventionelle PCR bleibt eine Budget-Wahl für Legacy-Einrichtungen, während ELISA und DNA-Färbung in Nischen-akademischen Anwendungen relevant bleiben. Next-Generation-Sequenzierung verspricht Multiplex-Pathogen-Screens, wartet aber auf regulatorischen Konsens.
Aufsichtsbehörden akzeptieren nun Nukleinsäure-Methoden als äquivalent zur Kultur für Freigabetests, was digitale PCR-Aufnahme katalysiert. Instrumentenhersteller investieren in mikrofluidische Chip-Formate, die Reaktionsmischungen in tausende Partitionen schneiden und Erkennungsschwellen senken. KI-Augmentation senkt weiter Betreiber-Kompetenzbarrieren und erschließt breitere Labor-Adoption.
Nach Anwendung: Gentherapie treibt höchstes Aufwärtspotenzial
Zelllinie-Qualitätskontrolle dominierte den Mycoplasma-Tests Markt im Jahr 2024 mit einem Anteil von 41,62%. Doch Gen- und Zelltherapie-Herstellung wird alle anderen Anwendungen mit einer CAGR von 17,82% übertreffen. Verlängerte Kulturdauern, autologe Workflows und mehrstufige Manipulationen verstärken das Kontaminationsrisiko und zwingen zu häufigen In-Prozess-Kontrollen. Regulatorische Leitlinien behandeln jeden Herstellungsschritt als potenzielle Kontaminationsfenster und schwellen Probenzahlen an.
Bioproduktions-Chargenfreigabetests bleiben ein Grundpfeiler, während Rohmaterial- und Medientests Anteile gewinnen, da Firmen Upstream-Vektoren wie tierische Komponenten erkennen. Impfstoff- und Virushersteller erweitern Überwachung parallel zu steigenden viralen Vektor-Therapeutika-Pipelines. Akademische Entdeckungsarbeit liegt außerhalb strenger Freigaberegeln, verlangt aber dennoch periodisches Screening zum Schutz der Forschungsintegrität.
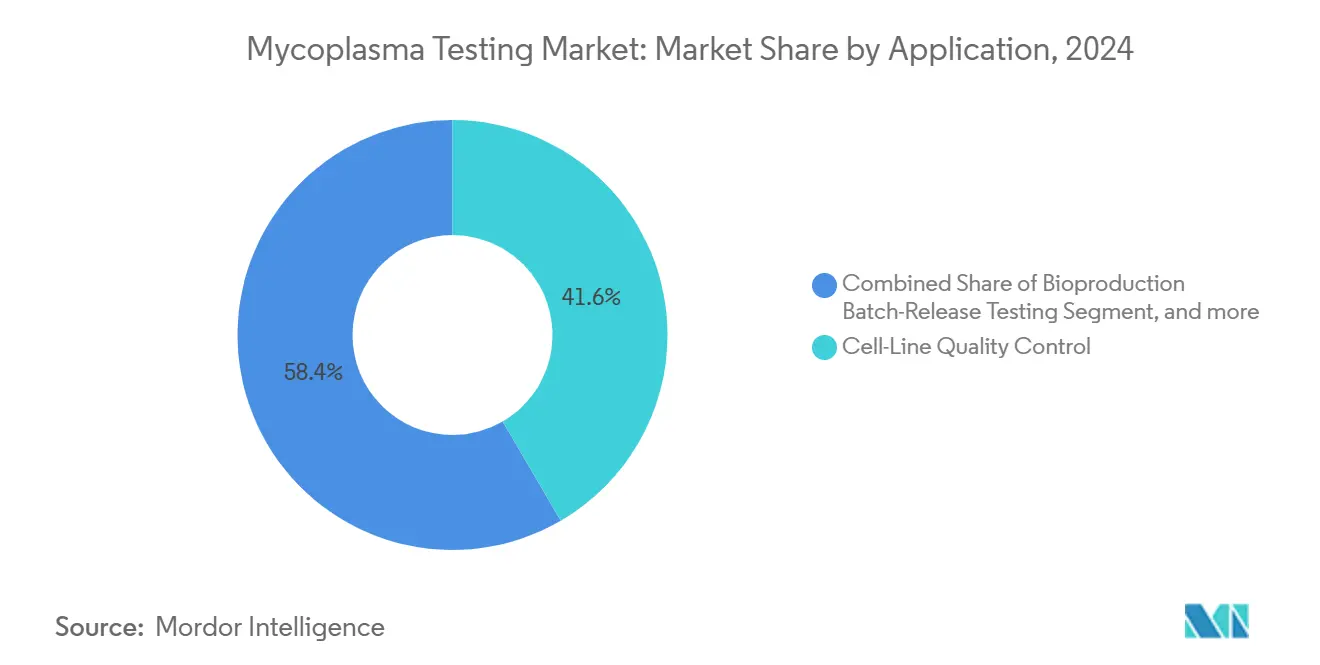
Notiz: Segmentanteile aller einzelnen Segmente verfügbar beim Berichtskauf
Nach Endnutzer: CMOs erfassen Outsourcing-Welle
Biopharma- und Biotechnologieunternehmen machten 65,29% des Endnutzer-Segments im Jahr 2024 aus, doch CMOs werden am schnellsten mit 15,45% CAGR wachsen, da virtuelle Biotech-Firmen auf Drittanbieter von Plasmid-Präparation bis Fill-Finish setzen. Die Mycoplasma-Tests Marktgröße für Auftragslabore erweitert sich, wenn Projekte von präklinisch zu kommerziellen Läufen skalieren.
Diagnostik- und Referenzlabore diversifizieren in Biologika-Support und jagen höher-margige Industriearbeit. Zellbanken schützen gegen Linien-Kreuzkontamination, da eine einzige verseuchte Master-Zellbank Jahre von Einreichungen invalidieren kann. Arbeitskräftemangel drängt sogar große Pharma dazu, Surge-Tests während Tech-Transfer oder Anlagenstillstandsperioden auszulagern, was die CMO-Wachstumskurve verstärkt.
Geografieanalyse
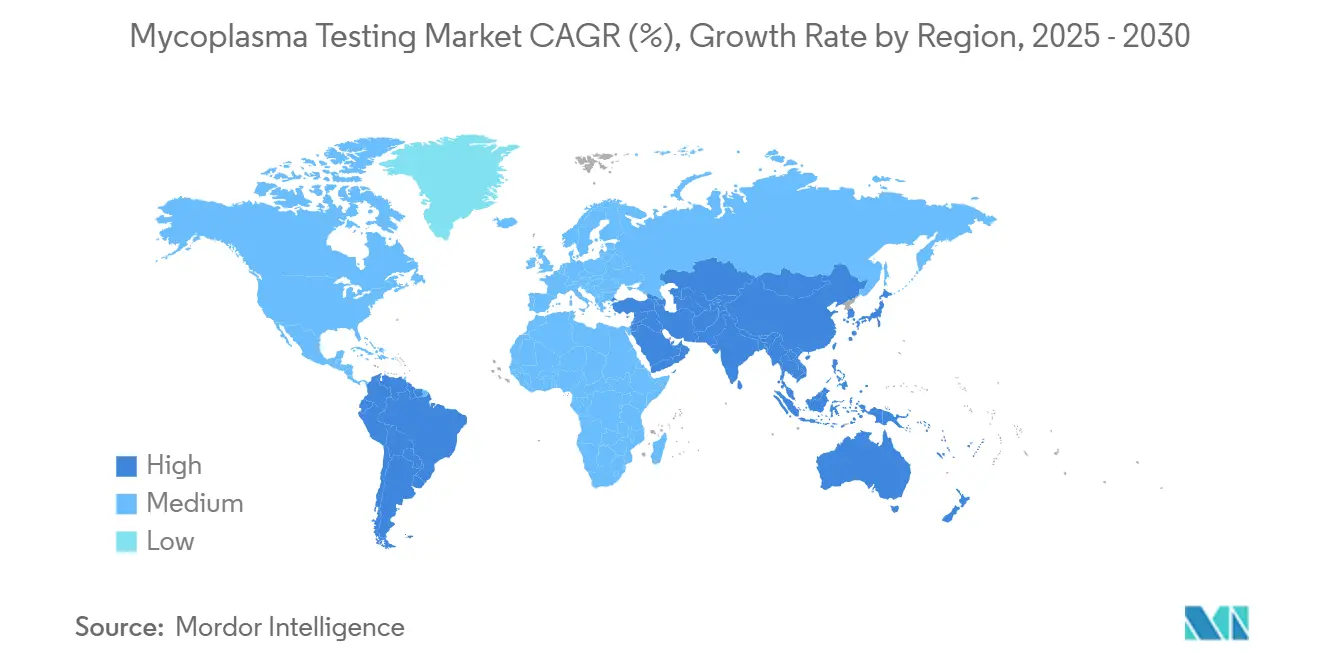
Nordamerika führte mit 40,81% des Umsatzes 2024, da FDA-Aufsicht, reife Bioprozessierungsinfrastruktur und frühe Technologieadoption stabile Nachfrage untermauern. Die Biocluster-Dichte und Kapitalverfügbarkeit der Region ermutigen schnellen Ersatz von Kulturmethoden durch automatisierte PCR-Systeme. Serviceanbieter nutzen Nähe zu Innovatoren und ermöglichen Just-in-Time-Probenlogistik und Compliance-Audits.
Europa folgt mit einem kohäsiven regulatorischen Rahmen von der EMA und harmonisierten Pharmakopöen, die multi-nationale Chargenfreigabe erleichtern. Die Mycoplasma-Tests Marktgröße gebunden an EU-Gentherapie-Studien steigt, da Deutschland, Spanien und das Vereinigte Königreich GMP-Einrichtungen beherbergen. Anbieter bedienen mehrsprachige Dokumentations- und Serialisierungsanforderungen und fördern informatikgestützte Assay-Plattformen.
Asien-Pazifik repräsentiert die am schnellsten wachsende Arena und expandiert mit 18,62% CAGR. Chinas Zelltherapie-Sektor profitiert von Regierungspriorätslisten, während Indiens produktionsgebundene Anreizprogramme Impfstoffexporteure anziehen. Singapurs dezentrale QC-Labore verkürzen Umlaufzeiten für regionale Biologika-Anlagen. Fragmentierte Regulierungen erfordern lokale Validierung und begünstigen globale Unternehmen, die Service-Hubs co-lokalisieren.
Südamerika und Naher Osten & Afrika hinken beim absoluten Umsatz hinterher, bieten aber unerschlossenes Aufwärtspotenzial, da heimische Impfstoffprogramme und Biosimilar-Anlagen proliferieren. Logistikhürden und begrenzte Kühlketten-Infrastruktur verlangsamen die Penetration schneller PCR-Geräte, doch öffentliche Gesundheitsinvestitionen könnten zukünftige Aufträge erschließen, sobald Trainings- und Servicenetzwerke reifen.
Wettbewerbslandschaft
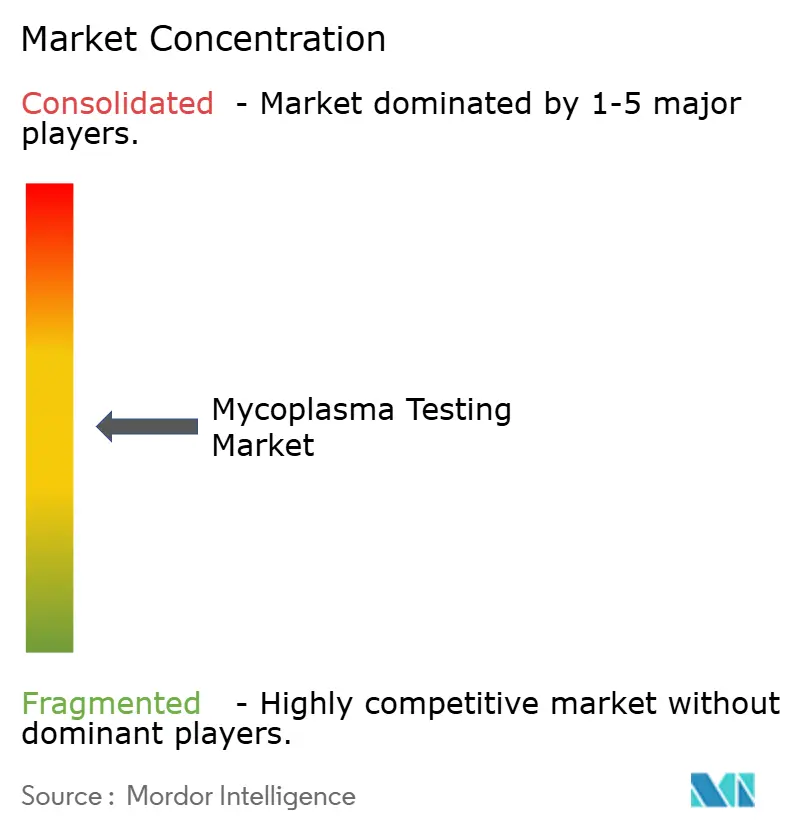
Der Mycoplasma-Tests Markt ist mäßig fragmentiert. Thermo Fisher Scientific, Charles River Laboratories und Merck KGaA kombinieren breite Reagenzien-Portfolios mit globalen technischen Service-Teams und verankern sie an der Spitze von Instrument- und Kit-Verkäufen. Danahers Fusion 2024 von Cytiva und Pall schuf ein USD 7,5 Milliarden Bioprozess-Kraftpaket, das Filtration, Kulturmedien und Tests unter einem Dach vereint.
Spezialisierte Labore wie Eurofins Scientific und SGS skalieren durch Multi-Site-GMP-Akkreditierungen und erfassen ausgelagerte Arbeitslasten, die geografische Nähe zu Abfülllinien erfordern. Ihr Wettbewerbsvorteil liegt in schlüsselfertigen Validierungspaketen, die Kunden-Zeitpläne komprimieren. Kleinere Innovatoren wie Minerva Biolabs fokussieren auf Reagenzien-nur-Nischen, während Rapid Micro Biosystems auf High-Throughput-QC-Labore mit automatisierten Reader-Systemen zielt.
Akquisitionsaktivität intensiviert sich, da Firmen End-to-End-Plattformbreite jagen. bioMérieux's Aufkauf 2025 von SpinChip Diagnostics fügt ultra-schnelle Immunoassay-Fähigkeit hinzu, um seine BIOFIRE-Molekularsuite zu ergänzen und das Unternehmen für Sample-to-Answer-Dominanz zu positionieren. KI-Partnerschaften zielen darauf ab, Interpretationsfehler zu reduzieren und Nachtest-Frequenz zu senken und bieten einen weiteren Hebel für Differenzierung.
Mycoplasma-Tests Branchenführer
-
Bionique Testing Laboratories Inc.
-
Thermo Fisher Scientific Inc.
-
Eurofins Scientific
-
Merck KGaA
-
ATCC
- *Haftungsausschluss: Hauptakteure in keiner bestimmten Reihenfolge sortiert
Jüngste Branchenentwicklungen
- Januar 2025: bioMérieux schloss die Akquisition von SpinChip Diagnostics ASA für EUR 111 (USD 127,3) Millionen ab und verbesserte seine Point-of-Care-Diagnostik-Fähigkeiten mit schneller Immunoassay-Technologie, die Ergebnisse aus Vollblutproben in 10 Minuten liefert. Die Akquisition stärkt bioMérieux's Position im Mycoplasma-Tests Markt durch Erweiterung seines Diagnostik-Plattform-Portfolios und Beschleunigung der Entwicklung schneller Testlösungen für biopharmazeutische Anwendungen.
- Juli 2024: SGS North America erweiterte seine Biologika-Testfähigkeiten im Lincolnshire Center of Excellence und verbesserte Instrumentierung und Expertise zur Unterstützung der wachsenden biopharmazeutischen Marktnachfrage. Die Erweiterung umfasst fortgeschrittene Mycoplasma-Testfähigkeiten und positioniert SGS, um erhöhte Nachfrage sowohl von kleinen als auch großen Molekül-Testanwendungen zu erfassen.
- Februar 2024: Standard BioTools Inc. ging eine Partnerschaft mit Next Gen Diagnostics ein, um Pathogen-Vollgenom-Sequenzierung zu automatisieren und bakterielle Sequenzierungskosten auf unter USD 10 pro Probe zu reduzieren. Die Partnerschaft adressiert Engpässe in Probenvorbereitung und Bioinformatik, die Mycoplasma-Test-Effizienz und -Skalierbarkeit beeinträchtigen.
- März 2024: US BioTek Laboratories akquirierte RealTime Laboratories, einen Pionier im Mykotoxin-Test, und erweiterte sein diagnostisches Testportfolio und geografische Reichweite. Die Akquisition verbessert US BioTek's Fähigkeiten in Kontaminationstests und bietet Zugang zu fortgeschrittenen Testtechnologien, die für Mycoplasma-Erkennungsanwendungen relevant sind.
Globaler Mycoplasma-Tests Marktbericht Umfang
Der Begriff 'Mycoplasma' bezieht sich auf eine Klasse von Bakterien, die häufig in Zellkultur vorhanden sind. Korrekter als Mollicutes bekannt, fehlt diesen Bakterien eine Zellwand, was sie gegen häufig verwendete Antibiotika wie Penicillin resistent macht. Mycoplasma verbreitet sich leicht durch Tröpfchen während der Zellkultur und kann in getrockneter Form monatelang überleben. Mycoplasma-Kontamination ist schwer mit einem Mikroskop zu sehen und erfordert spezifische Tests zur Erkennung. Kontamination kann tiefgreifende Auswirkungen auf experimentelle Arbeit haben. Der Mycoplasma-Tests Markt ist segmentiert nach Technologie (PCR, ELISA, enzymatische Methoden, DNA-Färbung und andere Technologien), Produkt (Instrumente, Kits und Reagenzien), Anwendung (Zelllinie-Tests, Bioproduktions-Tests und andere Anwendungen) und Geographie (Nordamerika, Europa, Asien-Pazifik, Naher Osten und Afrika und Südamerika). Der Marktbericht deckt auch die geschätzten Marktgrößen und Trends für 17 Länder in wichtigen Regionen weltweit ab. Der Bericht bietet den Wert (in USD Millionen) für die oben genannten Segmente.
| Instrumente | Real-time PCR Systeme |
| Schnelle mikrofluidische Analysegeräte | |
| Automatisierte Erkennungsplattformen | |
| Andere Instrumente | |
| Kits & Reagenzien | PCR-Assay-Kits |
| ELISA-Kits | |
| Enzymatische Assay-Kits | |
| Fluoreszenz-Färbe-Reagenzien | |
| Andere | |
| Dienstleistungen |
| Konventionelle PCR |
| qPCR |
| Digitale PCR |
| ELISA |
| Enzymatische Methoden |
| DNA-Färbung |
| Next-Generation-Sequenzierung |
| Andere NAATs |
| Zelllinie-Qualitätskontrolle |
| Bioproduktions-Chargenfreigabetest |
| Rohmaterial- & Medientests |
| Gen- & Zelltherapie-Herstellung |
| Impfstoff- & Virustests |
| Andere Anwendungen |
| Biopharma- & Biotechnologieunternehmen |
| Auftragsherstellungsorganisationen (CMOs) |
| Akademische & Forschungsinstitute |
| Zellbanken & Repositories |
| Diagnostik- & Referenzlabore |
| Nordamerika | Vereinigte Staaten |
| Kanada | |
| Mexiko | |
| Europa | Deutschland |
| Vereinigtes Königreich | |
| Frankreich | |
| Italien | |
| Spanien | |
| Rest von Europa | |
| Asien-Pazifik | China |
| Japan | |
| Indien | |
| Australien | |
| Südkorea | |
| Rest von Asien-Pazifik | |
| Naher Osten & Afrika | GCC |
| Südafrika | |
| Rest von Naher Osten & Afrika | |
| Südamerika | Brasilien |
| Argentinien | |
| Rest von Südamerika |
| Nach Produkt & Service | Instrumente | Real-time PCR Systeme |
| Schnelle mikrofluidische Analysegeräte | ||
| Automatisierte Erkennungsplattformen | ||
| Andere Instrumente | ||
| Kits & Reagenzien | PCR-Assay-Kits | |
| ELISA-Kits | ||
| Enzymatische Assay-Kits | ||
| Fluoreszenz-Färbe-Reagenzien | ||
| Andere | ||
| Dienstleistungen | ||
| Nach Technologie | Konventionelle PCR | |
| qPCR | ||
| Digitale PCR | ||
| ELISA | ||
| Enzymatische Methoden | ||
| DNA-Färbung | ||
| Next-Generation-Sequenzierung | ||
| Andere NAATs | ||
| Nach Anwendung | Zelllinie-Qualitätskontrolle | |
| Bioproduktions-Chargenfreigabetest | ||
| Rohmaterial- & Medientests | ||
| Gen- & Zelltherapie-Herstellung | ||
| Impfstoff- & Virustests | ||
| Andere Anwendungen | ||
| Nach Endnutzer | Biopharma- & Biotechnologieunternehmen | |
| Auftragsherstellungsorganisationen (CMOs) | ||
| Akademische & Forschungsinstitute | ||
| Zellbanken & Repositories | ||
| Diagnostik- & Referenzlabore | ||
| Nach Geographie | Nordamerika | Vereinigte Staaten |
| Kanada | ||
| Mexiko | ||
| Europa | Deutschland | |
| Vereinigtes Königreich | ||
| Frankreich | ||
| Italien | ||
| Spanien | ||
| Rest von Europa | ||
| Asien-Pazifik | China | |
| Japan | ||
| Indien | ||
| Australien | ||
| Südkorea | ||
| Rest von Asien-Pazifik | ||
| Naher Osten & Afrika | GCC | |
| Südafrika | ||
| Rest von Naher Osten & Afrika | ||
| Südamerika | Brasilien | |
| Argentinien | ||
| Rest von Südamerika | ||
Wichtige im Bericht beantwortete Fragen
Wie groß ist der aktuelle Mycoplasma-Tests Markt?
Der Markt wird auf USD 1,13 Milliarden im Jahr 2025 bewertet und soll bis 2030 USD 1,93 Milliarden erreichen.
Welches Segment wächst am schnellsten?
Gen- & Zelltherapie-Herstellung wird voraussichtlich mit 17,82% CAGR wachsen aufgrund strenger Kontaminationskontroll-Anforderungen.
Warum gewinnen CMOs Anteile bei Mycoplasma-Tests?
Biotech-Firmen lagern Herstellung und Qualitätskontrolle an CMOs aus, um Zugang zu validierten Laboren ohne große Kapitalausgaben zu erhalten, was CMO-Nachfrage um 15,45% CAGR antreibt.
Wie beeinflussen regulatorische Mandate das Marktwachstum?
FDA- und EMA-Regeln machen Mycoplasma-Tests vor Produktfreigabe obligatorisch und schaffen nicht-diskretionäre Ausgaben, die die Gesamt-Markt-CAGR erhöhen.
Welche Technologie stört traditionelle Methoden?
Digitale PCR bietet absolute Quantifizierung mit Erkennungsgrenzen um 10 CFU/mL und expandiert mit 16,26% CAGR, da Labore kulturbasierte Assays ersetzen.
Was schränkt schnelle Adoption automatisierter Plattformen ein?
Hohe Vorabkosten von USD 100.000-500.000 und Mangel an ausgebildetem molekularem QA-Personal verzögern Automatisierung, besonders in kleineren Laboren.
Seite zuletzt aktualisiert am:



