Bioburden-Testen-Marktgröße und -anteil
Bioburden-Testen-Marktanalyse von Mordor Intelligenz
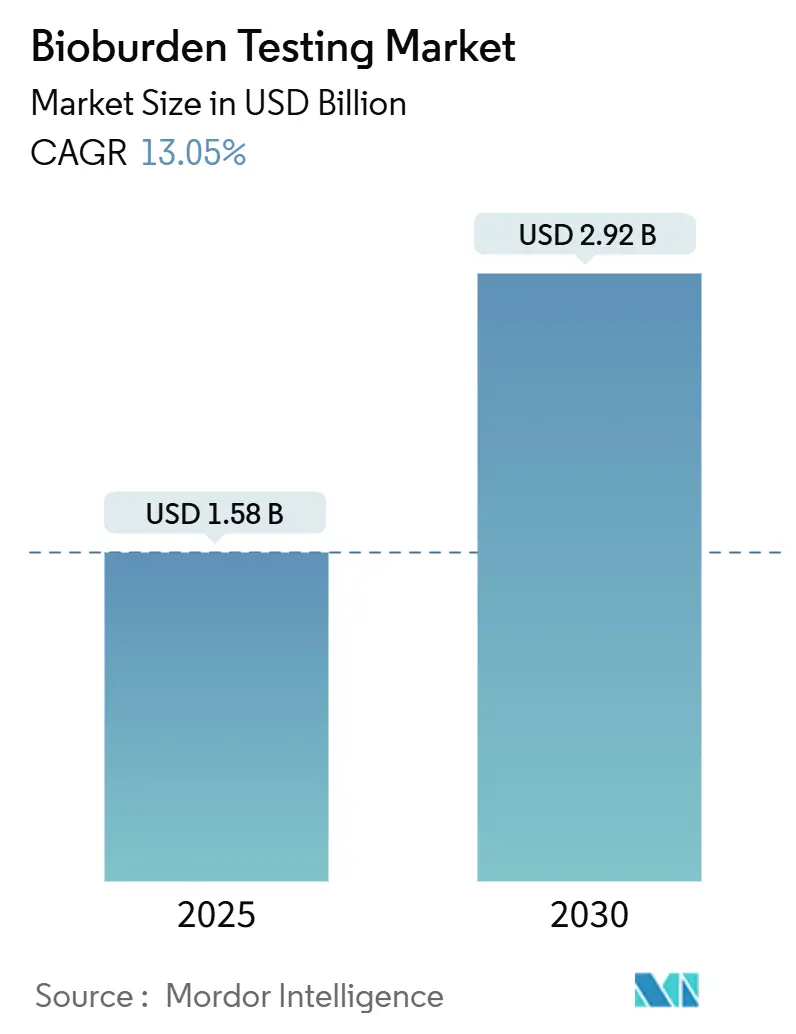
Der Bioburden-Testen-Markt erreichte USD 1,58 Milliarden im Jahr 2025 und wird voraussichtlich auf USD 2,92 Milliarden bis 2030 steigen, mit einem Wachstum von 13,05% CAGR. Die Nachfrage beschleunigt sich, da sich die Zell- und Gentherapie-Pipelines erweitern, Einweg-Bioprozess-Systeme proliferieren und Regulierungsbehörden die Echtzeit-Sterilitätsüberwachung intensivieren. Hersteller bevorzugen nun automatisierte, PCR-fähige Instrumente, die Erkennungsfenster verkürzen, während sie diese mit Einweg-Verbrauchsmaterialien koppeln, die chargenübergreifende Risiken eindämmen. Schnelle Enumerationstechnologien stärken den Bioburden-Testen-Markt weiter, indem sie Probe-zu-Ergebnis-Zeitlinien komprimieren, eine Notwendigkeit für kontinuierliche Fertigungslinien. Vertrag Entwicklung Und Herstellung Organizations (CDMOs) vertiefen die Adoption, da das Outsourcing wächst, während anhaltende Engpässe bei ausgebildeten Mikrobiologen das Interesse an KI-unterstützter Kolonienzählung anregen.
Wichtige Berichtserkenntnisse
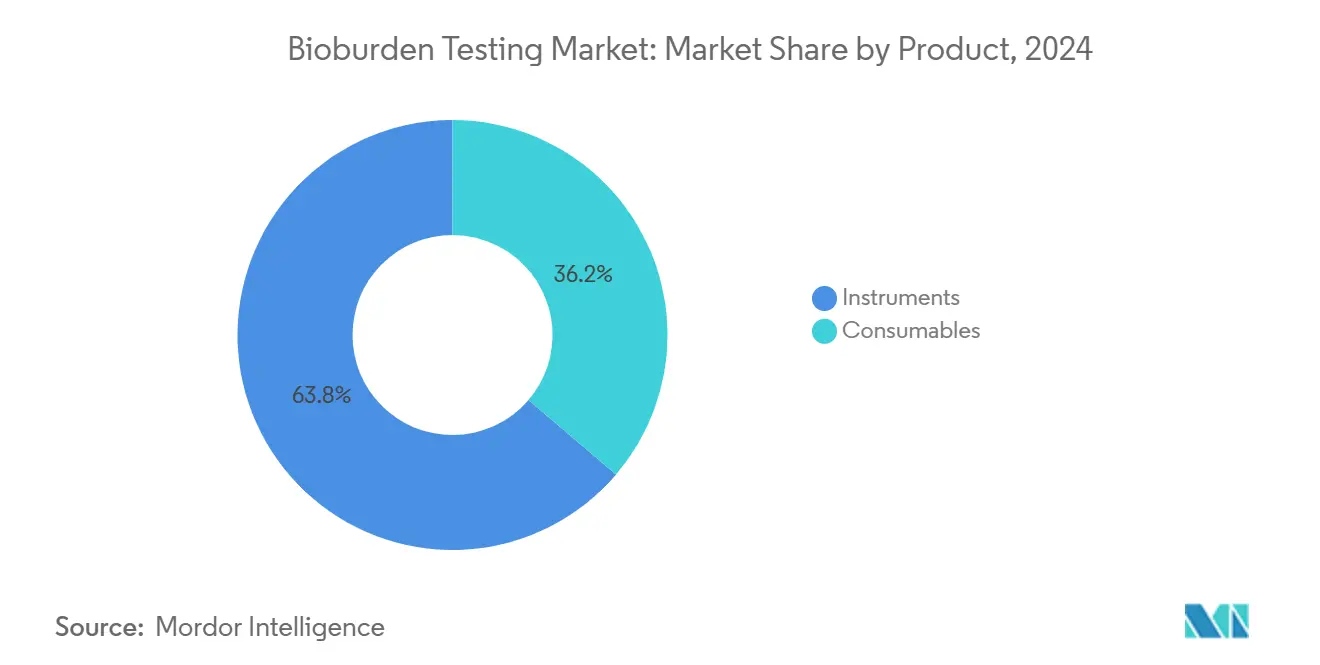
- Nach Produkttyp führten Instrumente mit einem Umsatzanteil von 63,76% am Bioburden-Testen-Markt im Jahr 2024; Verbrauchsmaterialien werden voraussichtlich mit einer CAGR von 16,24% bis 2030 steigen.
- Nach Enumerationsmethode hielten Plattenzähltechniken 39,45% des Bioburden-Testen-Marktanteils im Jahr 2024, während schnelle und Alternativ Methoden mit einer CAGR von 14,23% bis 2030 expandieren werden.
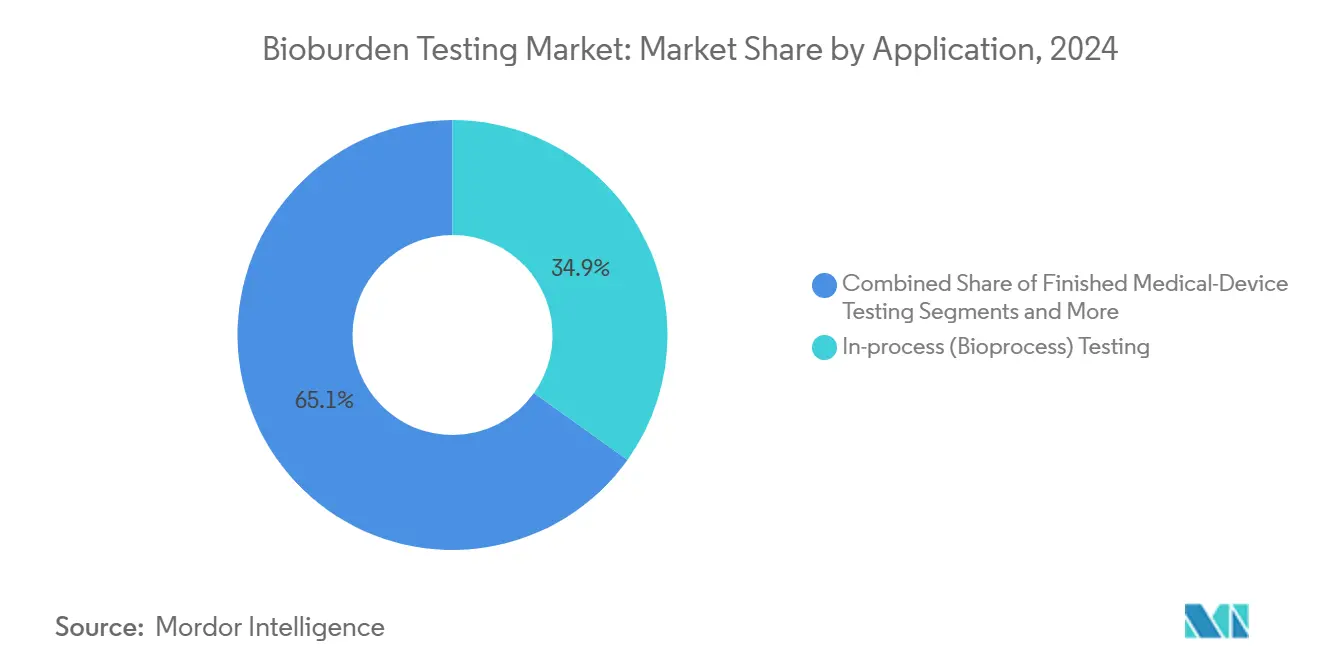
- Nach Anwendung machte In-Prozess-Bioprozess-Testen 34,87% der Bioburden-Testen-Marktgröße im Jahr 2024 aus, dennoch wird Umweltmonitoring voraussichtlich mit einer CAGR von 14,56% beschleunigen.
- Nach Endnutzer beherrschten Pharmazeutik- und Biopharmazeutik-Hersteller 49,71% der Nachfrage im Jahr 2024; CROs und CMOS sind bereit, mit 15,82% CAGR zu wachsen.
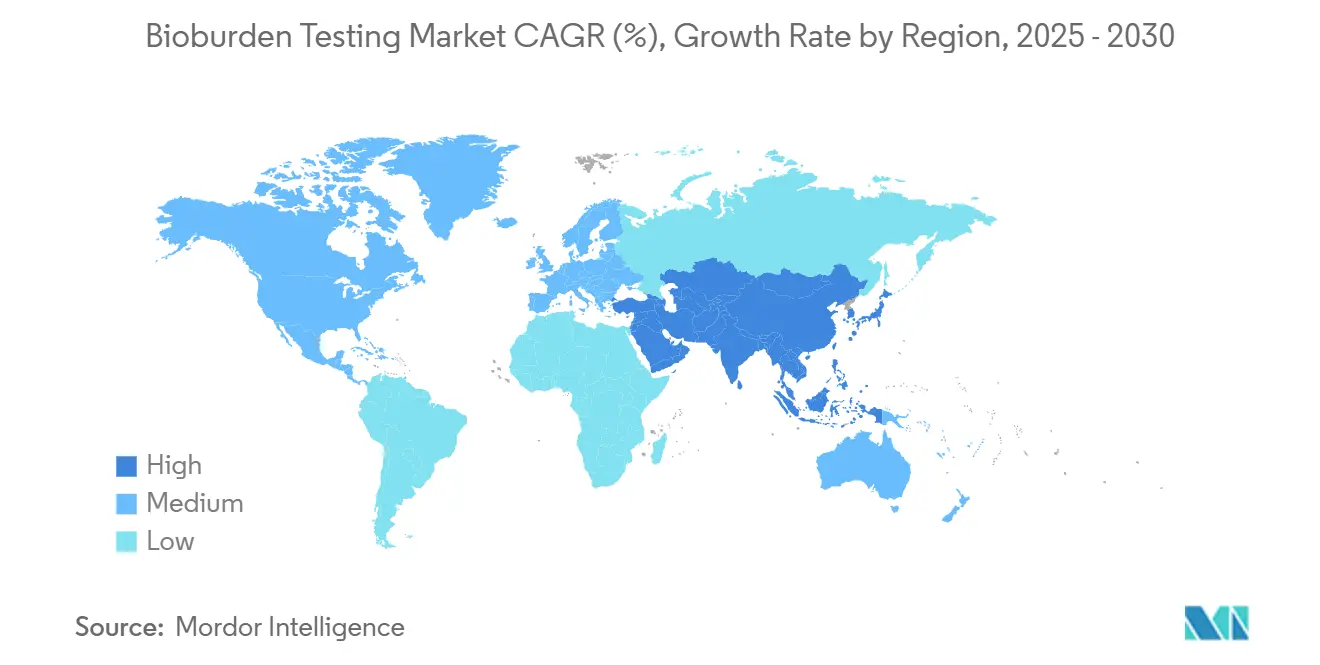
- Nach Geographie dominierte Nordamerika mit einem Umsatzanteil von 38,56% im Jahr 2024, während Asien-Pazifik voraussichtlich eine CAGR von 14,79% bis 2030 verzeichnen wird.
Globale Bioburden-Testen-Markttrends und Einblicke
Treiber-Auswirkungsanalyse
| Treiber | (~) % Auswirkung auf CAGR-Prognose | Geografische Relevanz | Auswirkungszeitrahmen |
|---|---|---|---|
| Hohe Häufigkeit von Produktrückrufen In schnellen Lieferketten | +2.1% | Nordamerika, EU | Kurzer Term (≤ 2 Jahre) |
| Strenge cGMP- und ISO 13485-Audits für Sterilitäts-Einhaltung | +1.8% | APAC, global | Mittlerer Term (2-4 Jahre) |
| Verschiebung hin zu Einweg- Bioprozessausrüstung | +1.6% | Nordamerika, EU, APAC | Mittlerer Term (2-4 Jahre) |
| Steigende Bioreaktor-Kontaminationsereignisse In Zell- & Gentherapie-Anlagen | +1.4% | Nordamerika, EU | Kurzer Term (≤ 2 Jahre) |
| Mikrobiom-basierte Therapeutika, die ultra-niedrige Erkennungsschwellen erfordern | +1.2% | Nordamerika, EU | Langer Term (≥ 4 Jahre) |
| Adoption kontinuierlicher Fertigung | +1.0% | Global | Langer Term (≥ 4 Jahre) |
| Quelle: Mordor Intelligence | |||
Hohe Häufigkeit von Produktrückrufen durch schnelle Lieferketten
Wiederkehrende Rückrufe unterstreichen, wie geschwindigkeitsorientierte Logistik Kontaminanten durch Routinekontrollen schlüpfen lassen kann. FDA-Mitteilungen 2024 für Sulfamethoxazol/Trimethoprim-Tabletten und Atovaquon-Suspensionen illustrierten die kostspieligen Folgen mikrobieller Versäumnisse.[1]u.S. Lebensmittel Und Medikament Administration, "Bionpharma Inc. Voluntary Recall von Atovaquone Oral- Suspension," fda.govHersteller betrachten präventive Tests nun als Günstiger als monatelange Stilllegungen und Markenschäden. Generikahersteller mit engen Margen spüren diesen Druck am stärksten, was routinemäßige Probenvolumen anhebt und den Bioburden-Testen-Markt als essentielles Qualitätstor positioniert.
Strenge cGMP- & ISO 13485-Audits für Sterilitäts-Compliance
Die uns-Qualitätsmanagementsystem-Verordnung von 2024 glich inländische Regeln an ISO 13485 an und erhöhte die Standards für Dokumentation und Echtzeitüberwachung.[2]u.S. Lebensmittel Und Medikament Administration, "Qualität Management System Regulation: Final Rule Amending Die Qualität System Regulation - Frequently Asked Questions," fda.gov PIC/S Annex 1-Revisionen erfordern kontinuierliche Überwachung statt periodischer Kontrollen. Als Sanofis Massachusetts-Werk 20% verworfene Läufe verzeichnete, hoben Regulierungsbehörden historische Kontaminationsraten hervor, was Mitbewerber zur Adoption automatisierter Warnungen und audit-bereiter Datenspuren veranlasste. Solche Mandate erweitern Instrumentenverkäufe und Software-Abonnements im gesamten Bioburden-Testen-Markt.
Verschiebung zu Einweg-Bioprozessausrüstung steigert Testvolumen
Einweg-Bioreaktoren, Filter und Anschlüsse vermeiden die für Edelstahlsysteme erforderlichen Reinigungsvalidierungen, zwingen jedoch zum Sterilitätsnachweis für jede Charge. Thermo Fisher und Sartorius berichteten von steigenden Bestellungen für Einweg-Assemblies, die mit schnellen Erkennungskits gebündelt sind. Jede Kampagne löst daher zusätzliche Chargenfreigabetests aus und schwellt die Verbrauchsmaterialnachfrage im Bioburden-Testen-Markt an.
Steigende Bioreaktor-Kontaminationsereignisse in Zell- & Gentherapie-Anlagen
Zelltherapie-Chargen im Millionenwert können durch eine einzige mikrobielle Intrusion verloren gehen, die Standardkultur-Tests möglicherweise nicht kennzeichnen. Aktualisierte FDA-Richtlinien zur Viralsicherheit betonen In-Prozess-Kontrollen und Rohmaterial-Screening. Anlagen installieren nun kontinuierliche Sensoren, die lebensfähige aber nicht kultivierbare Organismen erkennen und Käufe von Nächste-Generation-PCR- und Impedanz-Plattformen vorantreiben.
Beschränkungen-Auswirkungsanalyse
| Beschränkung | (~) % Auswirkung auf CAGR-Prognose | Geografische Relevanz | Auswirkungszeitrahmen |
|---|---|---|---|
| Hohe Anschaffungskosten automatisierter Enumerationsplattformen | -1.5% | Aufstrebende APAC, MEA | Kurzer Term (≤ 2 Jahre) |
| Mangel an ausgebildeten Mikrobiologen | -1.2% | APAC, MEA | Mittlerer Term (2-4 Jahre) |
| Falsch-negativ-Risiko bei schnellen Sterilitäts-Tests | -0.9% | Nordamerika, EU | Mittlerer Term (2-4 Jahre) |
| Versorgungsengpässe für hochreine Agar & Reagenzien | -0.7% | Global | Kurzer Term (≤ 2 Jahre) |
| Quelle: Mordor Intelligence | |||
Hohe Anschaffungskosten automatisierter Enumerationsplattformen
Systeme wie Schnell Mikro Biosystems' Wachstum Direct übersteigen USD 500.000, exklusive Validierungsausgaben. Kleine Generika-Anlagen kämpfen mit der Amortisation dieser Ausgaben, was die Instrumentenaufnahme trotz klarer Effizienzgewinne verlangsamt. Finanzierungshürden sind In Indien, Indonesien und Teilen Afrikas am akutesten, wo Kapitalbudgets eng bleiben.
Versorgungsengpässe für hochreine Agar & Reagenzien
Engpässe bei BD BACTEC-Flaschen und fetalem Kälberserum zwangen Labore 2024 zur Rationierung von Verbrauchsmaterialien.[3]amerikanisch Society für Mikrobiologie, "Managing Blut Kultur Bottle Shortages," asm.org Mit wenigen globalen Agar-Lieferanten hallt jede Störung weltweit nach und verlängert Lieferzeiten und erhöht Kosten.
Segmentanalyse
Nach Produkt: Automatisierung treibt Verbrauchsmaterialwachstum
Verbrauchsmaterialien verzeichneten die schnellste Umsatzexpansion mit 16,24% CAGR, obwohl Instrumente 2024 noch 63,76% des Bioburden-Testen-Marktes eroberten. Wachstum In der Einwegfertigung schiebt frische Kulturmedien, Filter und Schnelltestkits In jeden Produktionszyklus und hebt Volumennachfrage an. Automatisierte Identifikationsinstrumente profitieren von hochvolumigen Zell- und Gentherapie-Pipelines, die schnelle, präzise Messwerte erfordern.
Einwegartikel verankern nun Kontaminationspräventionsstrategien, da sie chargenübergreifende Rückstände eliminieren. Hersteller intensivieren Lieferantenaudits, um ununterbrochenen Verbrauchsmaterialfluss zu sichern und Reagenzienengpässe auszugleichen. Unterdessen bleiben KI-fähige Bildgebungsmikroskope und PCR-Modul Kapitalprioritäten für Große Anlagen, die Analysten-Berührungszeit reduzieren und Datenintegrität im Bioburden-Testen-Markt steigern wollen.
Nach Enumerationsmethode: Schnelle Technologien fordern traditionelle Ansätze heraus
Plattenzähl-Tests behielten 39,45% des Bioburden-Testen-Marktanteils 2024, dennoch steigen schnelle Techniken mit 14,23% CAGR aufgrund von Echtzeitfertigungsbedürfnissen. Durchflusszytometrie und ATP-Biolumineszenz liefern Antworten In Stunden, nicht Tagen, und unterstützen Anlagen, die kontinuierliche Linien adoptiert haben.
Hybride Testregime verschmelzen nun Legacy-Kulturplatten für regulatorische Vertrautheit mit fluoreszenzbasierten Zählungen für Geschwindigkeit. KI-Kolonienzähler reduzieren Ablesezeit auf 30 Sekunden bei 95% Genauigkeit. Diese Effizienzsteigerungen beseitigen Analytiker-Engpässe und verstärken die Bioburden-Testen-Marktgrößenaussichten bis 2030.
Nach Anwendung: Umweltmonitoring gewinnt regulatorische Betonung
In-Prozess-Testen war 2024 der größte Anteil der Bioburden-Testen-Marktgröße mit 34,87%. Dennoch ist Umweltmonitoring auf Kurs für die schnellsten Gewinne mit 14,56% CAGR nach den EU-Annex 1-Revisionen.
Hersteller erweitern Luft- und Oberflächenprobenahme über Reinräume hinaus In Ankleidungs-, Lager- und Personalzonen. Die bioMérieux 3P Unternehmen-Plattform integriert automatisierte Probenerfassung mit Wolke-Analytik und bietet audit-bereite Dashboards. Solche End-Zu-End-Sichtbarkeit stärkt Kontaminationskontrolle und untermauert langfristige Expansion für den Bioburden-Testen-Markt.
Notiz: Segmentanteile aller individuellen Segmente verfügbar beim Berichtskauf
Nach Endnutzer: CROs und CMOs treiben Outsourcing-Trend
Pharma- und Biotechnologie-Unternehmen generierten 49,71% der 2024-Nachfrage, dennoch positioniert Outsourcing-Momentum CROs und CMOS für 15,82% CAGR-Wachstum bis 2030. Zelltherapie-Sponsoren lehnen sich besonders an CDMOs an, um dedizierte Suiten zu liefern, die ultra-niedrige Bioburden-Schwellen ohne direkte Kapitalausgaben erreichen.
Akademische Labore unterstützen bei frühstufiger Test-Innovation, während Medizinproduktehersteller maßgeschneiderte Protokolle für Implantate anfordern, die keine terminale Sterilisation durchlaufen können. Erhöhte Spezialisierung vergrößert Dienstleistung-Rückstände und befeuert anhaltende Gewinne für den breiteren Bioburden-Testen-Markt.
Geografieanalyse
Nordamerika führte 2024 mit 38,56% der globalen Umsätze, da FDA-Regelharmonisierung und ein dichtes Netzwerk hochwertiger Biologika-Anlagen fortgeschrittene Erkennungsinvestitionen begünstigten. Kanada und Mexiko stärken regionale Summen durch Upgrade von Anlagen auf uns-Einhaltung-Niveau und erweitern Kundenstämme für schnelle Enumerationslieferanten.
Asien-Pazifik wird mit 14,79% CAGR wachsen, angetrieben von China, Indien, Südkorea und Singapur. Steigende GMP-Einhaltung und größere Biologika-Kapazität lösen Großbestellungen für automatisierte Inkubatoren, PCR-Bausätze und Einweg-Medienpacks aus. Öffentlich-Privat Ausbildungsinitiativen zielen darauf ab, Mikrobiologen-Lücken zu schließen, dennoch übersteigt die Nachfrage das Talentangebot In weiten Teilen Südostasiens und vergrößert Aussichten für KI-unterstützte Testmodule im Bioburden-Testen-Markt.
Europa hält Expansion durch strenge Annex 1-Durchsetzung aufrecht, die kontinuierliche Anlagenüberwachung erzwingt. Deutschland, das Vereinigte Königreich und Frankreich genehmigen beträchtliche Kapitalbudgets für Inline-Sensoren und Wolke-Datenmanagement-Suiten. Unterdessen registrieren Naher Osten, Afrika und Südamerika schrittweise Gewinne, da generika-getriebene Fertigungszentren In grundlegende Plattenzählkapazität investieren und allmählich zu schnelleren molekularen Tests übergehen.
Wettbewerbslandschaft
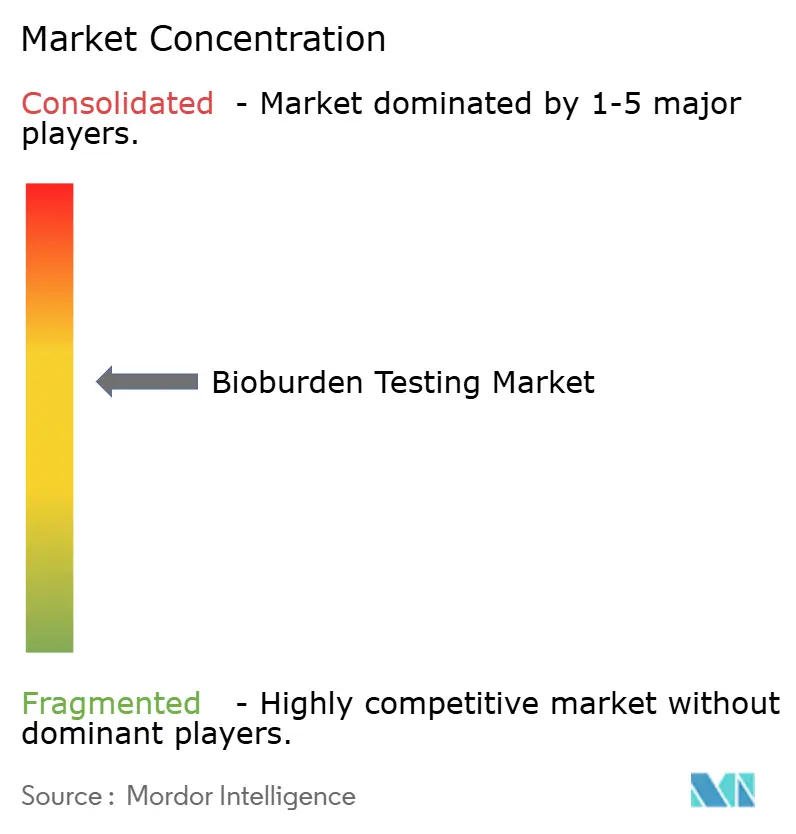
Der Sektor bleibt moderat fragmentiert. Becton Dickinson, Sartorius, Thermo Fisher Scientific und bioMérieux bieten integrierte Ökosysteme, die Instrumente, Medien und Analytik bündeln und etwa 42% des weltweiten Umsatzes erobern. Schnell Mikro Biosystems revolutioniert das Feld mit vollautomatisierter Kulturerkennung, die Freigabezeiten halbiert, ohne kompendiale Methoden zu ändern.
Strategische Züge betonen KI und maschinelles Lernen. BDs Plan, sein Biosciences Und Diagnostisch Lösungen-Geschäft In eine USD 3,4 Milliarden Pure-Play-Einheit auszugliedern, unterstreicht den Fokus auf Wachstumsnischen. Sartorius startete das Octet R8e-System im Mai 2025 und erhöhte Sensitivitätsbenchmarks für Echtzeit-biomolekulare Interaktionsanalyse.
Weiß-Raum-Chancen clustern um live-Biotherapeutika-Produkt-Tests, kontinuierliche Fertigungsintegrationen und unterversorgte Schwellenmärkte. Lieferanten, die sowohl Hardware als auch Validierungsberatung liefern können, haben einen Wettbewerbsvorteil, da Endnutzer zunehmend schlüsselfertige Kontaminationskontrollprogramme statt Einzelwerkzeuge suchen. Marktkonsolidierung wird erwartet, da Mid-Tier-Spieler Nischen-Softwareunternehmen akquirieren, um Datenintegritätsangebote zu stärken.
Bioburden-Testen-Industrie-Marktführer
-
Becton, Dickinson Und Company
-
Charles River Laboratories Inc.
-
Merck KGaA
-
Thermo Fisher Scientific
-
bioMérieux SA
- *Haftungsausschluss: Hauptakteure in keiner bestimmten Reihenfolge sortiert
Aktuelle Branchenentwicklungen
- Mai 2025: Sartorius führte das Octet R8e Biolayer-Interferometrie-System ein, das hochsensitive Echtzeit-Interaktionsanalyse für Zell- und Gentherapie-QC bietet.
- Februar 2025: BD kündigte Pläne an, sein Biosciences Und Diagnostisch Lösungen-Geschäft In ein unabhängiges Leben-Wissenschaften-Unternehmen mit USD 3,4 Milliarden Umsatz zu trennen.
- November 2024: bioMérieux veröffentlichte die 3P Unternehmen Umweltüberwachungs-Suite, die automatisierte Probenahme mit Wolke-basiertem Inkubationsmanagement verschmilzt.
- Oktober 2024: Mérieux NutriSciences erwarb die Lebensmitteltest-Division von Bureau Veritas für EUR 360 Millionen, verdoppelte seine Präsenz In Kanada und Asien-Pazifik und stärkte mikrobiologische Dienstleistung-Tiefe.
Globaler Bioburden-Testen-Marktbericht Umfang
Gemäß dem Berichtsumfang ist Bioburden-Testen ein integraler Bestandteil der Validierung und Revalidierung von Sterilisationsprozessen, Bewertung der Effizienz von Reinigungsprozessen, routinemäßige Überwachung von Herstellungsprozessen, Überwachung von Rohmaterialien, Komponenten oder Verpackungen und allgemeine Umweltüberwachungsprogramme. Der Bioburden-Testen-Markt ist segmentiert nach Produkt (Verbrauchsmaterialien und Instrumente), Enumerationsmethode (Membranfiltration, Plattenzählverfahren, Most Probable Number (MPN) und andere Enumerationsmethoden), Anwendung (Rohmaterialtests, Medizinproduktentests, In-Prozess-Tests, Gerätereinigungs-Validierung und andere Anwendungen) und Geographie (Nordamerika, Europa, Asien-Pazifik, Naher Osten und Afrika, und Südamerika). Der Marktbericht deckt auch die geschätzten Marktgrößen und Trends für 17 verschiedene Länder In wichtigen Regionen weltweit ab. Der Bericht bietet den Wert (In USD Millionen) für die oben genannten Segmente.
| Instrumente | Automatisierte Mikrobielle Identifikationssysteme |
| Polymerase-Kettenreaktion (PCR) Systeme | |
| Mikroskope | |
| Andere Instrumente | |
| Verbrauchsmaterialien | Kulturmedien & Reagenzien |
| Andere Verbrauchsmaterialien |
| Membranfiltration |
| Plattenzählverfahren |
| Most Probable Number (MPN) |
| Schnelle/Alternative Methoden (Durchflusszytometrie, ATP) |
| Rohmaterial-Testing |
| In-Prozess (Bioprozess) Testing |
| Fertiges Medizinprodukt-Testing |
| Gerätereinigungs-Validierung |
| Umweltmonitoring Tupfer & RODAC-Platten |
| Pharmazeutik- & Biopharmazeutik-Hersteller |
| Medizinproduktehersteller |
| Contract Research & Manufacturing Organizations (CROs/CMOs) |
| Akademische & Forschungslabore |
| Nordamerika | Vereinigte Staaten |
| Kanada | |
| Mexiko | |
| Europa | Deutschland |
| Vereinigtes Königreich | |
| Frankreich | |
| Italien | |
| Spanien | |
| Restliches Europa | |
| Asien-Pazifik | China |
| Japan | |
| Indien | |
| Australien | |
| Südkorea | |
| Restlicher Asien-Pazifik-Raum | |
| Naher Osten und Afrika | GCC |
| Südafrika | |
| Restlicher Naher Osten und Afrika | |
| Südamerika | Brasilien |
| Argentinien | |
| Restliches Südamerika |
| Nach Produkt | Instrumente | Automatisierte Mikrobielle Identifikationssysteme |
| Polymerase-Kettenreaktion (PCR) Systeme | ||
| Mikroskope | ||
| Andere Instrumente | ||
| Verbrauchsmaterialien | Kulturmedien & Reagenzien | |
| Andere Verbrauchsmaterialien | ||
| Nach Enumerationsmethode | Membranfiltration | |
| Plattenzählverfahren | ||
| Most Probable Number (MPN) | ||
| Schnelle/Alternative Methoden (Durchflusszytometrie, ATP) | ||
| Nach Anwendung | Rohmaterial-Testing | |
| In-Prozess (Bioprozess) Testing | ||
| Fertiges Medizinprodukt-Testing | ||
| Gerätereinigungs-Validierung | ||
| Umweltmonitoring Tupfer & RODAC-Platten | ||
| Nach Endnutzer | Pharmazeutik- & Biopharmazeutik-Hersteller | |
| Medizinproduktehersteller | ||
| Contract Research & Manufacturing Organizations (CROs/CMOs) | ||
| Akademische & Forschungslabore | ||
| Nach Geographie | Nordamerika | Vereinigte Staaten |
| Kanada | ||
| Mexiko | ||
| Europa | Deutschland | |
| Vereinigtes Königreich | ||
| Frankreich | ||
| Italien | ||
| Spanien | ||
| Restliches Europa | ||
| Asien-Pazifik | China | |
| Japan | ||
| Indien | ||
| Australien | ||
| Südkorea | ||
| Restlicher Asien-Pazifik-Raum | ||
| Naher Osten und Afrika | GCC | |
| Südafrika | ||
| Restlicher Naher Osten und Afrika | ||
| Südamerika | Brasilien | |
| Argentinien | ||
| Restliches Südamerika | ||
Schlüsselfragen im Bericht beantwortet
1. Wie hoch ist der aktuelle Wert des Bioburden-Testen-Marktes?
Der Markt generierte USD 1,58 Milliarden im Jahr 2025 und wird voraussichtlich USD 2,92 Milliarden bis 2030 erreichen.
2. Welches Segment trägt heute am meisten zur Bioburden-Testen-Marktgröße bei?
Instrumente machen 63,76% des 2024-Umsatzes aus, was anhaltende Investitionen In automatisierte Identifikations- und PCR-Plattformen widerspiegelt.
3. Warum gewinnen schnelle Enumerationsmethoden an Popularität?
Sie verkürzen Ergebniszeiten von Tagen auf Stunden, ein kritisches Bettürfnis für kontinuierliche Fertigungslinien, die sich keine langen Halteperioden leisten können.
4. Welche Region expandiert am schnellsten im Bioburden-Testen-Markt?
Asien-Pazifik wird voraussichtlich mit einer CAGR von 14,79% bis 2030 wachsen aufgrund erhöhter GMP-Einhaltung und Biologika-Kapazität.
Seite zuletzt aktualisiert am:



