Marktgröße und -anteil für aseptische Probenahme
Marktanalyse für aseptische Probenahme von Mordor Intelligence
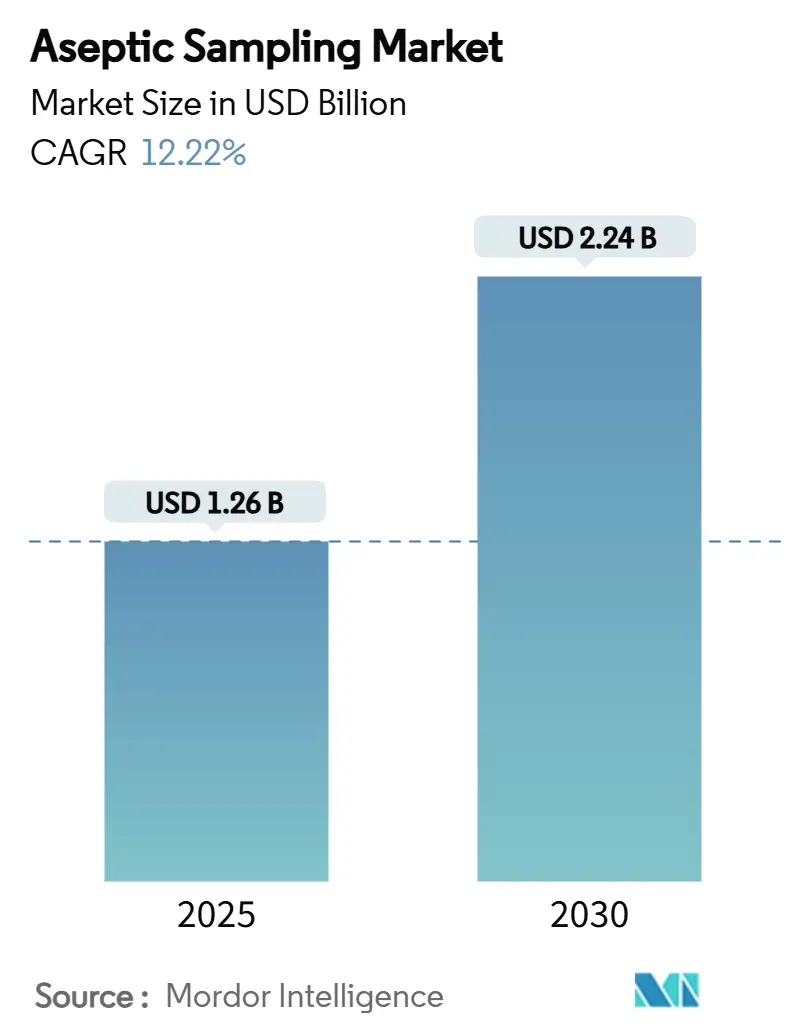
Der Markt für aseptische Probenahme steht bei 1,26 Milliarden USD im Jahr 2025 und ist auf dem Weg, bis 2030 2,24 Milliarden USD zu erreichen, mit einem Wachstum von 12,22% CAGR. Schnelle Investitionen in kontaminationsfreie Bioprozessierung, strengere Sterilitätsvorschriften und breitere Akzeptanz von Einwegsystemen unterstützen diese Expansion. Pharmahersteller sehen automatisierte Geräte als zuverlässige Absicherung gegen menschliche Fehler, während wachsende Zell- und Gentherapie-Pipelines Sterilitätskontrollen früher in der Entwicklung erzwingen. Digitale Prozessanalytik-Technologie (PAT) paart sich nun mit Probenahmehardware, um Echtzeit-Qualitätsdaten zu liefern, die Biologika-Chargen im Wert von mehreren Millionen Dollar schützen. Regional verteidigen nordamerikanische Hersteller die Führungsposition durch reife Infrastruktur und FDA-Aufsicht, doch asiatisch-pazifische Einrichtungen bauen Kapazitäten schneller aus, unterstützt durch staatliche Anreize und niedrigere Betriebskosten. Der Wettbewerb intensiviert sich, da integrierte Lösungsanbieter Hardware, Analytik und Datenmanagement zu einheitlichen Plattformen koppeln, die Validierungszeiträume verkürzen.
Zentrale Erkenntnisse des Berichts
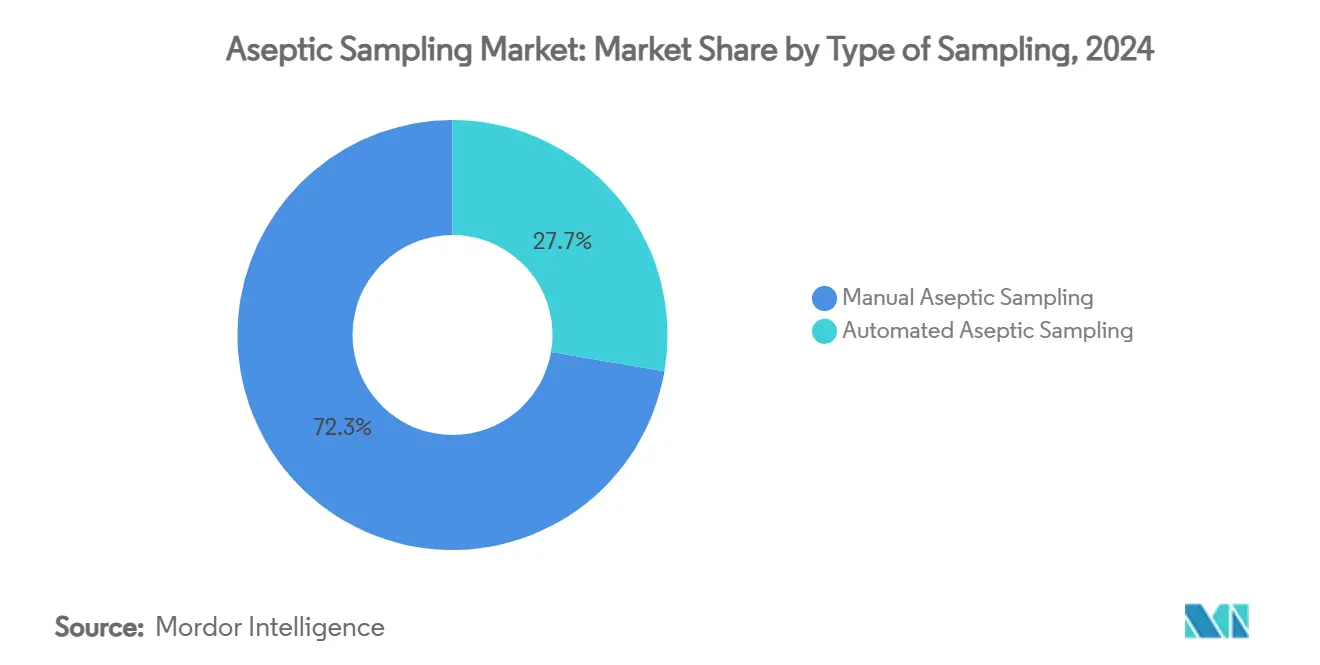
- Nach Art der Probenahme hielten manuelle Systeme 72,35% des Marktanteils für aseptische Probenahme im Jahr 2024, während automatisierte Systeme die höchste CAGR von 18,25% bis 2030 verzeichnen.
- Nach Probenahmeverfahren führten Online-Methoden mit 46,53% Umsatzanteil im Jahr 2024; At-line soll mit einer CAGR von 13,85% bis 2030 expandieren.
- Nach Anwendung entfielen 61,62% der Marktgröße für aseptische Probenahme im Jahr 2024 auf Upstream-Prozesse und wachsen mit einer CAGR von 12,2% bis 2030.
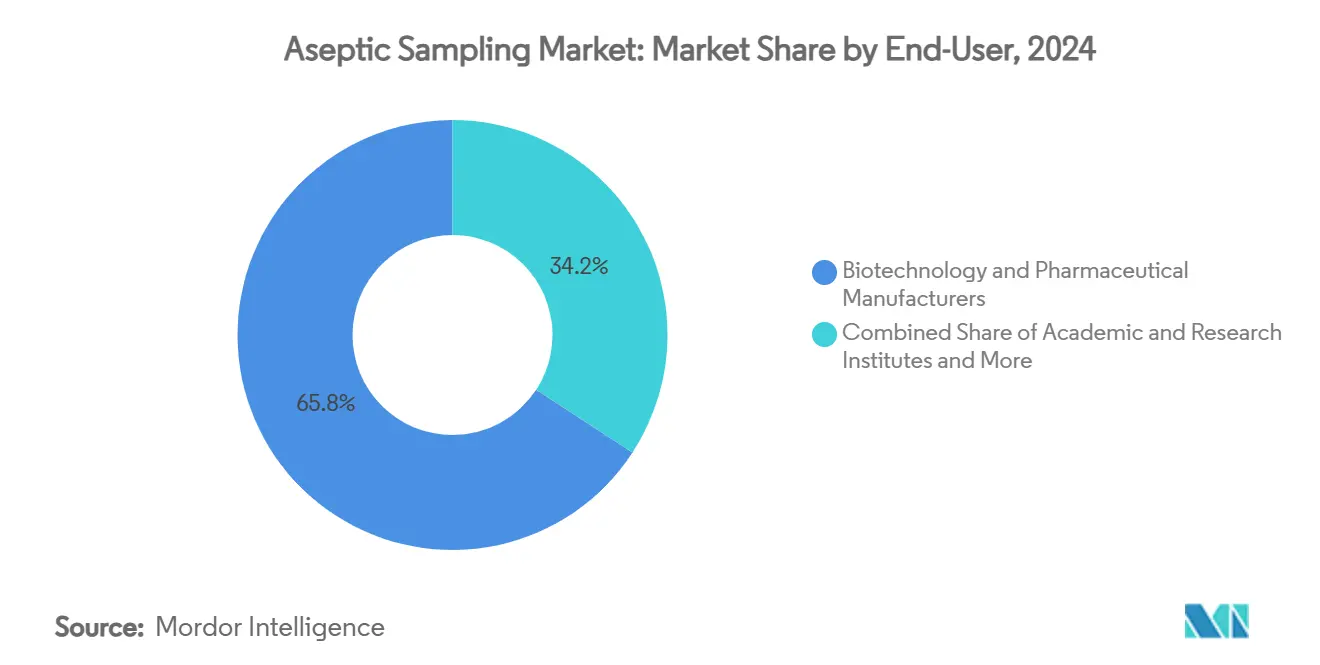
- Nach Endverbrauchern beherrschten Biotechnologie- und Pharmahersteller 65,82% der Marktgröße für aseptische Probenahme im Jahr 2024, während CDMOs mit einer CAGR von 14,61% steigen.
- Nach Komponentenmaterial eroberten Einwegsysteme 64,82% Umsatzanteil im Jahr 2024; wiederverwendbare Edelstahlsysteme verzeichnen eine CAGR von 13,61% bis 2030.
- Nach Geografie führte Nordamerika mit 41,82% Umsatzanteil im Jahr 2024; Asien-Pazifik zeigt die schnellste CAGR von 13,61% bis 2030.
Globale Trends und Einblicke zum Markt für aseptische Probenahme
Auswirkungsanalyse der Treiber
| Treiber | (~) % Auswirkung auf CAGR-Prognose | Geografische Relevanz | Auswirkungszeitraum |
|---|---|---|---|
| Strenge staatliche Vorschriften für Sterilitätssicherung | +1.8% | Nordamerika & Europa | Mittelfristig (2-4 Jahre) |
| Schnelle Skalierung von Zell- & Gentherapie-Pipelines | +2.2% | Nordamerika & Europa, Expansion nach Asien-Pazifik | Langfristig (≥ 4 Jahre) |
| Wechsel zu geschlossenen, einmalig verwendbaren Bioprozessen | +2.0% | Global, angeführt von Nordamerika | Mittelfristig (2-4 Jahre) |
| Einführung von In-line- und At-line-PAT zur Verbesserung der Chargenausbeuten | +1.5% | Nordamerika & Europa, selektiv Asien-Pazifik | Mittelfristig (2-4 Jahre) |
| KI-gesteuerte Kontaminationsvorhersageplattformen | +1.0% | Nordamerika & Europa als frühe Anwender | Langfristig (≥ 4 Jahre) |
| Quelle: Mordor Intelligence | |||
Strenge staatliche Vorschriften für Sterilitätssicherung
Globale Regulierungsbehörden verlangen nun strengere Probenahmehäufigkeit und Rückverfolgbarkeit in der aseptischen Produktion. Die überarbeitete FDA-Richtlinie erstreckt sich auf fortgeschrittene Therapiearzneimittel und schreibt routinemäßige Umgebungsüberwachung mit dokumentierter Validierung vor. Entsprechende EU-GMP-Anhang-1-Überarbeitungen gleichen Erwartungen zwischen Regionen ab und veranlassen Hersteller, Papierdokumentation durch elektronische Prüfpfade und automatisierte Geräte zu ersetzen, die jeden Eingriff aufzeichnen. Dieser Druck beschleunigt Upgrades in älteren Anlagen und schreibt geschlossene, einmalig verwendbare Wege in neuen Standorten vor, um Kontaminationsrisiken zu minimieren[1]U.S. Food and Drug Administration, "PAT - A Framework for Innovative Pharmaceutical Development, Manufacturing, and Quality Assurance," fda.gov.
Schnelle Skalierung von Zell- & Gentherapie-Pipelines
Die Kommerzialisierung von autologen und allogenen Therapien legt Sterilitätsschwachstellen offen, da jede Patientencharge null Toleranz für Kreuzkontamination hat. Hersteller spezifizieren daher automatisierte, geschlossene Probenahme, die Dokumentation der Überwachungskette sichert und diverse Virusvektoren und Zelltypen unterstützt. Da Zulassungen bis 2030 3.000 Therapien erreichen, erfordern Kapazitätserweiterungen modulare Skids, die ohne langwierige Validierungszyklen in Mehrprodukt-Suiten eingesetzt werden können[2]Cytiva, "Cytiva Opens New Korea Manufacturing Facility," cytiva.com.
Wechsel zu geschlossenen, einmalig verwendbaren Bioprozessen
Einweg-Bioreaktoren, Filter und Schläuche dominieren neue Anlagenbauten, da sie Reinigungsvalidierung eliminieren und Umrüstzeiten verkürzen. Ihre Verbreitung erzwingt kompatible Probenahmeschnittstellen, die Beutelintegrität bewahren und niedrige Extraktionswerte beibehalten. Auftragshersteller bevorzugen diese Plattformen, um schnell zwischen Kundenprogrammen zu wechseln, müssen aber dennoch Polymercharakterisierung unter sich entwickelnden Leachables-Richtlinien erfüllen.
Einführung von In-line- und At-line-PAT zur Verbesserung der Chargenausbeuten
Echtzeit-Analytik verlagert Qualitätskontrolle von Endpunkttests zu kontinuierlichen Einblicken. At-line-Sonden liefern nun alle paar Minuten Daten ohne Prozessexposition und ermöglichen Operateuren, Nährstoffe oder pH-Werte anzupassen, bevor Abweichungen sich ausbreiten. FDA-Ermutigung durch PAT-Rahmenwerke reduziert regulatorischen Widerstand und positioniert automatisierte Probenahme plus Spektroskopie als Grundpfeiler moderner Biologika-Herstellung.
Auswirkungsanalyse der Beschränkungen
| Beschränkung | (~) % Auswirkung auf CAGR-Prognose | Geografische Relevanz | Auswirkungszeitraum |
|---|---|---|---|
| Leachables & Extractables-Risiko bei Polymersystemen | -0.7% | Nordamerika & Europa | Kurzfristig (≤ 2 Jahre) |
| Hohe CAPEX für automatisierte aseptische Probenahme-Skids | -1.0% | Global, stärker in Schwellenmärkten | Mittelfristig (2-4 Jahre) |
| Komplexe Validierung für Mehrfachverbinder | -0.5% | Nordamerika & Europa | Kurzfristig (≤ 2 Jahre) |
| Quelle: Mordor Intelligence | |||
Leachables & Extractables-Risiko bei Polymersystemen
Einweg-Verteiler können organische Säuren, Weichmacher oder Spurenmetalle freisetzen, die empfindliche Biologika destabilisieren und erschöpfende chemische Profilierung erfordern. Unternehmen führen oft mehrwöchige Extraktionsstudien bei verschiedenen Temperaturen und Lösungsmitteln durch, was Kosten erhöht und Produkteinführungspläne verzögert. Das Fehlen harmonisierter globaler Teststandards vervielfacht auch analytische Arbeitslasten.
Hohe CAPEX für automatisierte aseptische Probenahme-Skids
Schlüsselfertige Skids kosten zwischen 500.000 und 2 Millionen USD und erfordern spezialisierte Wartungsteams, was ROI für kleine Biotechs mit niedrigen jährlichen Chargenzahlen unklar macht. Schwellenmärkte verschieben Käufe oft zugunsten validierter manueller Kits, besonders wenn Kreditfinanzierung knapp ist. Anbieter reagieren mit Leasingmodellen und modularen Upgrades, die schrittweise Automatisierung ermöglichen[3]Danaher Corporation, "Danaher Invests USD 1.5 Billion in Manufacturing Capacity," danaher.com.
Segmentanalyse
Nach Art der Probenahme: Automatisierung gewinnt an Boden
Manuelle Systeme beherrschten 72,35% des Marktanteils für aseptische Probenahme im Jahr 2024. Ihre niedrigen Kapitalausgaben und bewährten Compliance-Aufzeichnungen erhalten weit verbreitete Nutzung, besonders in älteren Anlagen, wo Infrastrukturänderungen Ausfallzeiten einladen. Automatisierte Module zeigen jedoch die schnellste CAGR von 18,25%, da Hersteller geringere Bedienerexposition und stärkere Datenintegrität anstreben. Automatisierte Skids integrieren mit Produktionsausführungssystemen, um jede Entnahme zu protokollieren und Ergebnisse sofort für Audit-Reviews zu archivieren. Diese Fähigkeit lindert Dokumentationsermüdung und erhöht Vertrauen bei FDA-Inspektionen. Steigende Chargenwerte in Zelltherapien schärfen Nachfrage nach Lösungen, die menschliche Eingriffe vollständig eliminieren und verstärken die langfristige Neigung zur Automatisierung im Markt für aseptische Probenahme.
Manuelle Kits besetzen noch Nischen wie frühe F&E oder geringe Biologika-Volumina, wo Budget wichtiger ist als Durchsatz. Anbieter positionieren nun Hybridplattformen, die manuelle Auslöser akzeptieren, aber Sterilisation zwischen Verwendungen automatisieren. Diese Brückenstrategie hilft preissensitiven Käufern, schrittweise zu migrieren ohne bestehende Protokolle zu verwerfen. Über den Prognosezeitraum wird breitere Harmonisierung elektronischer Aufzeichnungsstandards eine entscheidende Wendung zu automatisierten Geräten als Standard für kommerzielle Produktionslinien im Markt für aseptische Probenahme katalysieren.
Nach Probenahmeverfahren: At-line steigt stark
Online-Instrumente repräsentierten 46,53% des globalen Umsatzes im Jahr 2024 aufgrund ihrer Echtzeit-Rückmeldung. Sie ziehen kontinuierlich Mikro-Aliquots unter geschlossenen Bedingungen und ermöglichen sofortige pH- oder Nährstoffanpassungen. At-line-Geräte, mit der lebhaften CAGR von 13,85%, ziehen Operateure an, die häufige Analytik ohne die technische Komplexität vollständig integrierter Online-Schleifen wollen. At-line-Sonden stehen neben dem Behälter, halten Schlauchlängen kurz und ermöglichen schnelle Sensorwechsel. Dies reduziert Verstopfungsrisiko und vereinfacht Kalibrierungen.
Offline-Entnahmen bestehen für fortgeschrittene Analytik wie Virus-Clearance-Assays, die nicht miniaturisiert werden können. Doch jeder Offline-Transfer beinhaltet offene Handhabung, verlängert Bearbeitungszeit und riskiert Abweichungen. Da PAT-Richtlinien und Echtzeit-Freigabetests reifen, werden At-line-Einheiten wahrscheinlich schrittweise Anteil von Offline-Workflows abziehen. Standardisierte mechanische Schnittstellen und Einweg-Fließwege machen nun Nachrüstungen einfacher und fördern Adoption in mittelständischen Anlagen im Markt für aseptische Probenahme.
Nach Anwendung: Upstream dominiert, Downstream beschleunigt
Upstream-Prozesse absorbierten 61,62% Umsatz im Jahr 2024. Zellkulturstufen können wochenlang dauern, währenddessen mikrobieller Einbruch ganze Bioreaktor-Volumina im Wert von 10 Millionen USD gefährdet. Folglich planen Operateure mehrere sterile Entnahmen täglich für Stoffwechselprofilierung. Das Verfolgen von gelöstem Sauerstoff, Glukose und lebensfähigen Zellzahlen ermöglicht frühe Korrekturmaßnahmen und schützt Titer und Glykosylierungsmuster. Downstream-Reinigung registriert die höchste CAGR von 15,52%, da Chromatographieschritte für komplexe Modalitäten sich vervielfachen. Virusfiltration schreibt nun chargenweise Integritätsprüfungen vor, die aseptische Probenahme unmittelbar vor und nach der Filterkette erfordern. Der kumulative Bedarf für Sterilitätsbestätigung an jedem Haltepunkt setzt Probenahmehäufigkeit nach oben.
Formulierung und Fill-Finish intensivieren auch Kontrollen für hochwertige personalisierte Dosen, gemessen in Millilitern. Geschlossene Fläschchen-Probenahmeadapter ermöglichen Qualitätsteams, Potenz nach Füllung aber vor Lyophilisierung zu testen, ohne Behälter zu durchbrechen. Diese Aktivität zeigt, wie Downstream-Stufen zunehmend Upstream-Wachsamkeit spiegeln und ganzheitliche Adoption im Markt für aseptische Probenahme vorantreiben.
Nach Endverbrauchern: Hersteller halten Löwenanteil
Integrierte Biotechnologie- und Pharmaunternehmen behielten 65,82% Anteil im Jahr 2024, da sie Entdeckung bis Fill-Finish unter einem Qualitätssystem verwalten. Sie setzen Probenahmestrategien früh ein und skalieren sie über mehrere Anlagen, um Audits zu standardisieren. CDMOs, mit 14,61% CAGR voranschreitend, profitieren von Sponsor-Outsourcing. Ihr Wettbewerbsvorteil hängt von schnellem Tech-Transfer und Mehrproduktflexibilität ab, beide abhängig von modularen, einmalig verwendbaren Probenehmern, die Umrüstausfallzeiten minimieren.
Akademische Institute wenden kompakte, manuelle Kits für Explorationsarbeiten an, wo Budgets eng bleiben. Obwohl dieses Segment kleiner ist, bedeutet seine Rolle in Proof-of-Concept-Studien frühe Markenexposition für Anbieter, die später kommerzielle Ausrüstung verkaufen. Patientenvertretungsgruppen, die Gentherapie-Studien finanzieren, arbeiten auch mit CDMOs zusammen und verstärken weitere Verträge für umfassende Probenahme-Suiten im Markt für aseptische Probenahme.
Notiz: Segmentanteile aller einzelnen Segmente verfügbar beim Berichtskauf
Nach Komponentenmaterial: Einwegsysteme überwiegen
Einweg-Hardware repräsentierte 64,82% des globalen Umsatzes im Jahr 2024 und spiegelt universelle Industriemigration weg von festen Edelstahlnetzwerken wider. Plastikverteiler kommen vorsterilisiert an, reduzieren Reinigungschemikalien und Wasserverbrauch und unterstützen schnellere Linienwechsel. Angesichts steigender Umweltkontrolle wiegen Hersteller Plastikmüll gegen Wasser- und Dampfverbrauch ab. Dennoch bevorzugt die Gesamtbetriebskosten oft Einwegprodukte, wenn Einsparungen bei Arbeit, Validierung und Ausfallzeit bilanziert werden. Wiederverwendbare Edelstahlsets verzeichnen jedoch eine bemerkenswerte CAGR von 13,61%, wo kontinuierliche Verarbeitung oder sehr große Chargenvolumina langlebige Assets mit minimalen Verbrauchsmaterialkosten belohnen.
Jüngste Lieferanteninnovation führte gammastabile Fluorpolymerauskleidungen und recycelbare Beutelmaterialien ein, die Nachhaltigkeitsdebatten zu mildern versprechen. Parallele Investition in Integritätsprüfsensoren, die Beutelleistung vor jedem Lauf verifizieren, verstärkt Vertrauen. In den nächsten fünf Jahren erwartet der Markt für aseptische Probenahme Koexistenz beider Materialklassen, segmentiert nach Anlagengröße, Nachhaltigkeitszielen und regulatorischen Präferenzen.
Geografische Analyse
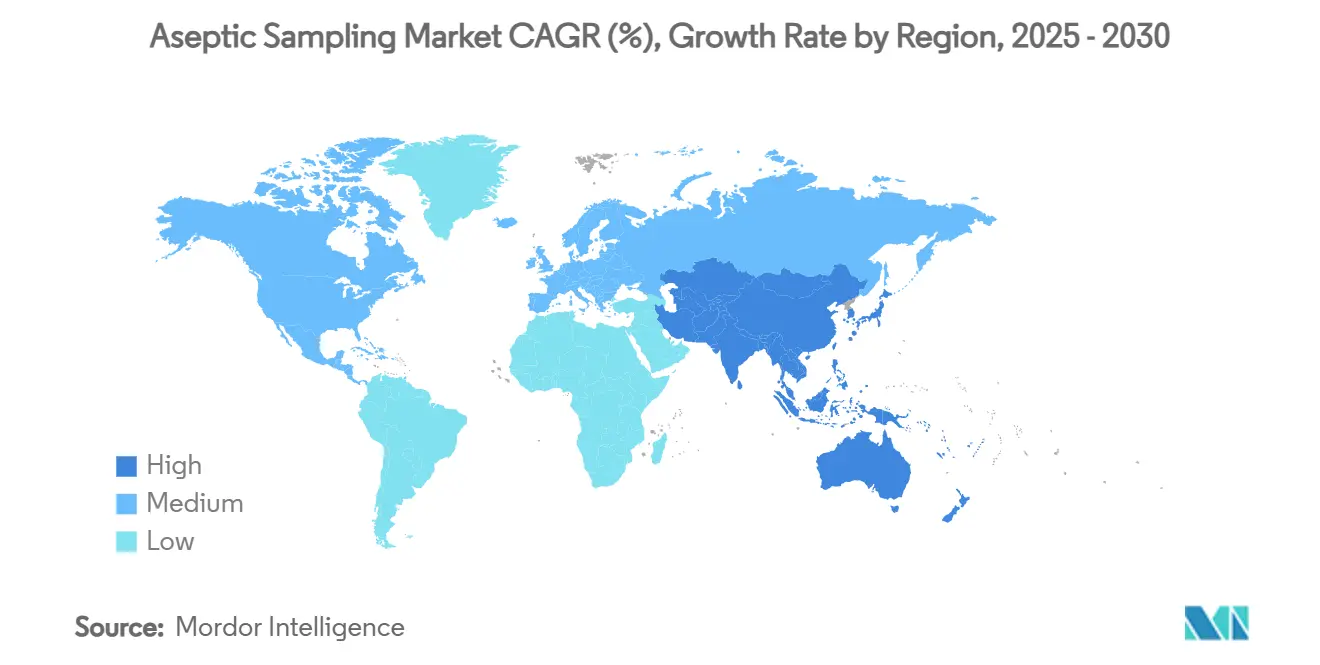
Nordamerika eroberte 41,82% Umsatz im Jahr 2024 und verteidigt seine Führung durch tiefe Biopharma-Pipelines, Benchmarking der FDA-Richtlinien und eine Dichte von CDMOs. Die Vereinigten Staaten beherbergen die meisten kommerziellen Zelltherapie-Einrichtungen und investieren stark in PAT. Kanada baut Biosimilar-Kapazität unter gezielten Bundeszuschüssen auf, während Mexikos kostengünstige Arbeitskraft generische Arzneimittelproduktion antreibt. Nachfrage steigt weiter durch Venture-Capital-Unterstützung erstklassiger Biologika, die erhöhte Sterilität erfordern.
Asien-Pazifik verzeichnet die stärkste CAGR von 13,61%, da Regierungen Kapazität subventionieren und Qualitätssteigerung durchsetzen. Südkoreas SK Pharmteco investierte 260 Millionen USD in Peptidsyntheseanlagen mit geschlossenen Probenehmern. Chinas Lokalisierungsrichtlinien verlangen heimische Versorgungssicherheit und befeuern neue Biologikaparks, die Einweg-Probenahme von Anfang an standardisieren. Indien bleibt Kraftwerk für pharmazeutische Wirkstoffe, wo kostensensitive Anlagen manuelle und Einweg-Kits mischen. Kollektiv treiben diese Programme den Markt für aseptische Probenahme tiefer in die Region und etablieren lokale Fertigungsbasen für globale Anbieter.
Europa bleibt stabil, verankert durch Deutschlands Ingenieursclusters und Frankreichs Biologika-Expansionen. Post-Brexit-Einrichtungen des Vereinigten Königreichs richten sich nach aktualisiertem Anhang 1 aus und treiben Nachrüstungen automatisierter Probenahme-Logger voran. Nachhaltigkeitsvorschriften drängen Hersteller, hybride Metall-Plastik-Verteiler zu erforschen und Lebenszyklusauswirkungen zu dokumentieren. Italienische und spanische Impfstoffhersteller rüsten ähnlich Ausrüstung auf, um Pandemie-Bereitschaftszuschüsse zu sichern. Diese Investitionen liefern stetiges, wenn weniger dramatisches Wachstum, das die Region als Innovationshub für den Markt für aseptische Probenahme hält.
Wettbewerbslandschaft
Der Markt für aseptische Probenahme zeigt moderate Fragmentierung, wobei die fünf größten Lieferanten einen erheblichen Anteil halten. Merck KGaA, Sartorius und Thermo Fisher Scientific nutzen breite Portfolios, die Probenahme-Sonden mit Bioreaktoren, Sensoren und Datensoftware paaren. Mercks 300-Millionen-Euro-Biologika-Expansion in Korea bettet seine Mobius-Einweg-Probenehmer ein, um Referenzinstallationen zu sichern. Sartorius skaliert sein TakeOne-Portfolio für Gentherapie-Bedürfnisse, indem es Mikro-Volumen-Ports hinzufügt, die zu kleinen, hochwertigen Chargen passen. Thermo Fisher integriert Probenahmeventile in seine HyPerforma-Bioreaktoren und bietet schlüsselfertige Qualifikation, die Anlagenkommissionierung verkürzt.
Mittelständische Spezialisten wie Saint-Gobain Life Sciences fokussieren auf Polymerinnovation und rollen mehrschichtige Filme mit niedrigeren Additivprofilen aus. Asahi Kasei zielt auf Virusfiltrationslinien mit Probenahme-Adaptern ab, die zu seinen Planova-Filtern passen. Start-ups liefern KI-Analytik, die Ausrüstungsdaten auf Kontaminationsrisiko-Dashboards überlagert. Akquisitionsaktivität bleibt lebhaft, da Vollsortiment-Lieferanten versuchen, Nischentechnologien in End-to-End-Suiten zu integrieren. Danahers Aldevron-Kauf erweitert sein Biologika-Ökosystem und verkauft Probenahme-Skids über bestehende Genommedizin-Kunden.
Preiskonkurrenz intensiviert sich hauptsächlich bei Verbrauchsmaterialien, während Kapitalausrüstungsdifferenzierung auf Validierungsdokumentation, Sensorintegration und lokaler Unterstützung beruht. Anbieter, die Extraktionsdossiers straffen und cloud-ready Datenausgaben bieten, gewinnen Vorteile unter verschärften regulatorischen Erwartungen. Über den Prognosehorizont wird kollaborative Entwicklung zwischen Lieferanten und CDMOs voraussichtlich standardisierte Verbindungsformate hervorbringen, die Interoperabilität im Markt für aseptische Probenahme vorantreiben.
Branchenführer für aseptische Probenahme
-
GEA Group
-
Merck KGaA
-
Keofitt A/S
-
Saint-Gobain Life Sciences
-
Sartorius AG
- *Haftungsausschluss: Hauptakteure in keiner bestimmten Reihenfolge sortiert
Jüngste Branchenentwicklungen
- April 2025: QIAGEN umriss drei neue Probenvorbereitung-Instrumente, einschließlich des QIAsymphony Connect für 2025-Launch, um Laborautomatisierungseffizienz zu erhöhen.
- Juni 2024: Beckman Coulter Life Sciences debütierte das Biomek Echo One System, das genomische Probenvorbereitungszeit dramatisch verkürzt.
Globaler Berichtsumfang zum Markt für aseptische Probenahme
Entsprechend dem Berichtsumfang ist aseptische Probenahme eine sterile Methode zur Probensammlung, die während biopharmazeutischer Prozesse implementiert wird, um wahrscheinliche Kontaminationen oder Veränderungen bei der Probennahme des Arzneimittels für Forschung und Analyse zu vermeiden. Der Markt für aseptische Probenahme ist segmentiert nach Art der Probenahme (Manuelle aseptische Probenahme (Beutel, Flaschen und andere) und Automatisierte aseptische Probenahme), Anwendung (Upstream-Prozess und Downstream-Prozess), Endverbrauchern (Biotechnologie- und Pharmahersteller, Auftragsforschungs- und Herstellungsorganisationen und andere) und Geografie (Nordamerika, Europa, Asien-Pazifik, Naher Osten und Afrika und Südamerika). Der Marktbericht deckt auch die geschätzten Marktgrößen und Trends für 17 verschiedene Länder in wichtigen Regionen weltweit ab. Der Bericht bietet den Wert (in Millionen USD) für die oben genannten Segmente.
| Manuelle aseptische Probenahme | Beutel |
| Flaschen | |
| Andere Behälter | |
| Automatisierte aseptische Probenahme |
| Online-Probenahme |
| At-line-Probenahme |
| Offline-Probenahme |
| Upstream-Prozess |
| Downstream-Prozess |
| Biotechnologie- & Pharmahersteller |
| Auftragsforschungs- & Herstellungsorganisationen |
| Akademische & Forschungsinstitute |
| Einwegsysteme |
| Wiederverwendbare (Edelstahl-basierte) Systeme |
| Nordamerika | Vereinigte Staaten |
| Kanada | |
| Mexiko | |
| Europa | Deutschland |
| Vereinigtes Königreich | |
| Frankreich | |
| Italien | |
| Spanien | |
| Übriges Europa | |
| Asien-Pazifik | China |
| Japan | |
| Indien | |
| Südkorea | |
| Australien | |
| Übriges Asien-Pazifik | |
| Naher Osten und Afrika | GCC |
| Südafrika | |
| Übriger Naher Osten und Afrika | |
| Südamerika | Brasilien |
| Argentinien | |
| Übriges Südamerika |
| Nach Art der Probenahme | Manuelle aseptische Probenahme | Beutel |
| Flaschen | ||
| Andere Behälter | ||
| Automatisierte aseptische Probenahme | ||
| Nach Probenahmeverfahren | Online-Probenahme | |
| At-line-Probenahme | ||
| Offline-Probenahme | ||
| Nach Anwendung | Upstream-Prozess | |
| Downstream-Prozess | ||
| Nach Endverbrauchern | Biotechnologie- & Pharmahersteller | |
| Auftragsforschungs- & Herstellungsorganisationen | ||
| Akademische & Forschungsinstitute | ||
| Nach Komponentenmaterial | Einwegsysteme | |
| Wiederverwendbare (Edelstahl-basierte) Systeme | ||
| Geografie | Nordamerika | Vereinigte Staaten |
| Kanada | ||
| Mexiko | ||
| Europa | Deutschland | |
| Vereinigtes Königreich | ||
| Frankreich | ||
| Italien | ||
| Spanien | ||
| Übriges Europa | ||
| Asien-Pazifik | China | |
| Japan | ||
| Indien | ||
| Südkorea | ||
| Australien | ||
| Übriges Asien-Pazifik | ||
| Naher Osten und Afrika | GCC | |
| Südafrika | ||
| Übriger Naher Osten und Afrika | ||
| Südamerika | Brasilien | |
| Argentinien | ||
| Übriges Südamerika | ||
Hauptfragen, die im Bericht beantwortet werden
Wie groß ist der aktuelle Markt für aseptische Probenahme?
Der Markt für aseptische Probenahme wird auf 1,26 Milliarden USD im Jahr 2025 geschätzt und soll bis 2030 2,24 Milliarden USD erreichen.
Welches Segment wächst am schnellsten im Markt für aseptische Probenahme?
Automatisierte aseptische Probenahme-Systeme expandieren mit einer CAGR von 18,25% bis 2030 und übertreffen manuelle Alternativen.
Warum sind Einwegsysteme für aseptische Probenahme beliebt?
Sie eliminieren Reinigungsvalidierung, verkürzen Wechselzeiten und minimieren Kontaminationsrisiko, wodurch sie 64,82% Umsatzanteil im Jahr 2024 erhalten.
Welche Region führt bei der Einführung aseptischer Probenahme?
Nordamerika hält 41,82% globalen Umsatz aufgrund reifer Bioprozessierungs-Infrastruktur und strenger FDA-Aufsicht.
Wie beeinflussen regulatorische Änderungen die Nachfrage nach aseptischer Probenahme?
Aktualisierte FDA- und EU-GMP-Anhang-1-Richtlinien erhöhen Probenahmehäufigkeit und Dokumentationsanforderungen und treiben Investitionen in automatisierte, geschlossene Systeme voran.
Was ist die Hauptbeschränkung für breitere Automatisierung?
Hohe Kapitalausgaben von 500.000 bis 2 Millionen USD pro Skid schrecken kleinere Unternehmen ab, besonders in Schwellenmärkten.
Seite zuletzt aktualisiert am:



